在使用同步荧光法测叶绿素a时,该如何设置日立F-7000型荧光分光光度计相关参数?
我自己开发了一款海水水下叶绿素分析仪器,不知道如何对仪器进行定标,配置叶绿素标准曲线是采用丙酮为基体的叶绿素溶液呢还是培养活体藻类进行稀释测定?如果采用丙酮基体的溶液定标是不是会与实际值差距较大?
分析叶绿素a的高速离心机有什么具体参数要求?叶绿素荧光仪能否直接测叶绿素a ?国家环保局认可吗?
叶绿素a存在于一切独立营养植物中,是一种能将光合作用的光能传递给化学反应系统的惟一色素。因此,叶绿素a就成为水中有机物的源泉。通过测定叶绿素a,可以了解海洋、湖泊和河流中植物性浮游生物的现存量和基础生产量,可掌握水体中藻类现存量。因此,叶绿素a指标是评价水体富营养化程度最直接有效的方法,也是目前科学地预测其发展趋势的有效方法。根据实测资料分析,当叶绿素a含量从常量上升至10 mg/m3以上,并有迅速增加的趋势,就可预测水体即将发生富营养化。(一)叶绿素a的分光光度法测定在一定量的水样中添加1%碳酸镁悬浮液1 mL,充分搅匀,用玻璃纤维滤纸或微孔滤膜过滤。若不能立即提取,将带样品的滤膜放人冰箱保存(1~2 d)。将载有藻类的滤膜放人研钵中,加入90%丙酮6~7 mL,研磨至呈糊状,再用90%丙酮溶液洗入具塞刻度离心管中,密封,放置暗处静置萃取6~20 h。以3500~4000r/min转速离心lO~15 min,取上清液转入1 cm比色皿中,以90%丙酮溶液为参此,于波长665 nm和750 nm处测吸光度,然后加入几滴l mol/L盐酸酸化,于波长665 nm和750 nm处再测吸光值。叶绿素a浓度计算公式为:Chla=27.3×665一E750)一(A665一A750)]×V丙酮/V水样式中:Chla——叶绿素a含量(μg/L);E665,E750——丙酮萃取液分别于波长665 nm和750 nm的吸光度;A665,A750——丙酮萃取液酸化后分别于波K 665 nm和750 nm的吸光度;V丙酮——丙酮萃取液的体积,mL;V水样——水样过滤的体积,L。(二)叶绿素a的荧光法测定适合于藻类较少的贫营养湖泊或外海洋中的叶绿素a的测定。基本原理是,当丙酮提取液经紫外线照射时,叶绿素a显现其固有的红色荧光特征,其浓度与荧光强度存在一定的规律性,因此可定量测定叶绿素a的含量。由于所用的光源强度高,故荧光法的灵敏度比分光光度法约高两个数量级。[/td][/tr][/table]

地表水体的富营养化引起藻类及其它浮游生物迅速繁殖,导致溶解氧下降,水质恶化,鱼类和其它生物大量死亡,甚至引发供水危机。色素是藻类光合作用时吸收、转化和传递光能的主要物质,叶绿素以多种形式存在于藻类植物中,大约占有机物干重的1-2%,是估算其生物量的重要指标,快速准确测定水体中叶绿素a浓度对于评价水体营养状态和水质管理具有重要意义。 叶绿素测定方法有很多,大致分为萃取测定、荧光活体测定及水华遥感监测。萃取分析利用有机溶剂萃取植物细胞叶绿素进行光谱光度测定,根据分析技术的不同分为分光光度法、荧光法和高效液相色谱法。萃取分析只要操作准确,提取完全,可以得到准确和重复性好的结果,但是过程繁琐,不方便用于连续监测。 AOA在线藻类分析仪利用叶绿素荧光特性进行分类定量分析,活体测量,无需样品预处理,仪器操作简单,可以快速地获得大量叶绿素数据,广泛运用在在线监测。为保证在线分析仪的有效运行,需要用标准样品来校准、性能考核和日常数据质量控制,但国内还未开发叶绿素的标准样品和质控样品,已知叶绿素含量(用萃取方法测定)的浮游植物悬浮液被认为是最好的标样替代品。当水体发生水华,生物多样性下降,往往是一种藻类成为绝对优势,可作为纯种藻类标准样品,本文将几个代表性的比对实验整理分析,探讨误差原因。[b]1.比对方法[/b]1.1清洗AOA在线藻类分析仪蠕动泵、测量室及其底盖,检查纯水透光率值。1.2水样不经任何处理,测量叶绿素浓度值。1.3剩余水样酌量加入1%碳酸镁悬浊液(按1升水量加入1ml),防止酸化。1.4带回实验室,尽快分析,实验室分析方法依据《无水乙醇热浴超声法测定淡水中的叶绿素a》[sup][/sup]。[b]2实验2.1微囊藻水样2.1.1样品来源[/b] 2014年8-10月某水库出现铜绿微囊藻水华,采集水华“浓密”处水样作为标准储备液,分别取0、2、5、10、15、20、25、50、100ml,用纯水稀释成500ml,检查两种方法叶绿素a和藻密度线性。取水库水华严重区、进水口、湖心和出水口四个水样,做实际水样比对分析。[img=,690,690]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011537059882_3331_3247383_3.jpg!w690x690.jpg[/img][b]2.1.2实验结果[img=,690,361]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011538312332_220_3247383_3.png!w690x361.jpg[/img][/b]表1微囊藻稀释水样比对结果[b][img=,622,352]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011539397062_938_3247383_3.png!w622x352.jpg[/img][/b]图2微囊藻水样线性比对[img=,690,215]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011611492722_7678_3247383_3.png!w690x215.jpg[/img]表2含微囊藻实际水样比对表1、表2和图2表明,两种测量方法的结果与藻类数量之间存在非常显著的相关性,但AOA在线分析仪测量结果低于分光光度法,浓度越高,差异性越大。[b]2.1.3结果分析[/b]2.1.3.1分光光度法误差分析 萃取后叶绿素,对光照和氧气很敏感,极易造成不可逆的分解,因此,节时高效是分光光度法的质量保证,而温度是质控措施的关键。在超声波萃取过程,提高温度加快叶绿素溶出速度,同时,叶绿素降解的速度也是加快的,最佳超声波萃取条件:60℃萃取25分钟,2小时内完成测定。另外,实验室遮光也是必要。[img=,690,690]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011541253150_3659_3247383_3.jpg!w690x690.jpg[/img]2.1.3.2AOA荧光法误差来源 AOA在线藻类分析仪原理:叶绿素具有荧光特性,一定的激励光,任何一种藻产生的荧光强度与其所含叶绿素a成正比,几种不同藻混合体产生的荧光强度等于各自荧光的总和。采用325纳米、450纳米、525纳米、570纳米、590纳米和610纳米作为激励光,其中325纳米是用来补偿黄色物质(有机物),测定685nm的光强,计算总叶绿素a值和不同藻的浓度。(1)水样原始性状发生变化暗室环境下,激励光照到藻上,能量分成三部分:光合作用、叶绿素自发荧光和热能辐射。如果藻的活性强,光合作用消耗的能量就越多,产生荧光的强度越小,反之,如果藻的活性弱,荧光强度就强。荧光能量和光合作用的能量是相互竞争的,叶绿素荧光常常被认为光合作用无效指标的依据。比对实验的样品,从采样经实验室样品处理,到水质自动监测站仪器分析,剩余样品送回实验室做分光光度法比对,再紧凑也需要3-4天完成,运输、保存过程,叶绿素在活体内也和其它物质处于不断更新变化中,可能衰老、也可能分解破坏,比对实验要求的同步水平也不可能实现,这是比对误差不可忽视的部分。(2)微囊藻特殊的细胞结构使水样分布不均匀微囊藻群体有胶鞘和伪空泡,可以自由漂浮在水中,水样在实验室静置一天后,出现明显的分层,测量过程难以保证均匀分布。[img=,690,690]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011542423667_4598_3247383_3.jpg!w690x690.jpg[/img](3)工作温度与校准温度不一致参考各类荧光法仪器说明书,浮游生物悬浊液的荧光反应受温度的影响很大,有些仪器的温度补偿2%⁄ ℃,但这种经验补偿不能保证准确的现场测量,因为每一种浮游植物的荧光强度随温度变化程度不同。这台AOA藻类分析仪安装测试在冬季,这次比对实验在9月份进行,温差亦有影响。(4)浊度的影响 实验室分光光度法经过0.8um滤纸过滤,比色扣除750nm吸光度值,只要操作正确,浊度的影响很小。水中的悬浮颗粒物对激励光和产生的荧光有反射、散射和阻挡的作用,造成激励光和荧光产量的下降,YSI3026传感器检测结果:1NTU的 浊度影响大约是0.03ug/L叶绿素。 除色素以外的细胞结构(细胞壁、胶被、储藏物质)以溶解有机碳为主要成分,对紫外光和蓝光具有强烈的吸收,也可视为影响测定的悬浮物,AOA在线藻类分析仪称之为黄色物质,用325纳米补偿。铜绿微囊藻细胞壁分为两层,内层是纤维素,外有胶鞘,有相当的厚度,互相溶合形成多细胞群体。图5显示黄色物质与叶绿素含量相关,AOA的测量结果反映了铜绿微囊藻细胞群体特征。分光光度法和AOA扣除浊度方法各有不同,是否有可比性,有待进一步了解。[img=,586,305]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011543564741_5446_3247383_3.png!w586x305.jpg[/img]图5(5)水样镜检微囊藻绝对优势,视野内不见其它藻类,AOA分析结果有少量绿藻、硅藻,其它的比对实验也出现藻类识别错误。[b]2.2薄甲藻水样[img=,690,920]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011545089042_4958_3247383_3.jpg!w690x920.jpg[/img][/b]图6[b]2.2.1实验结果[/b][img=,690,289]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011547036798_1735_3247383_3.png!w690x289.jpg[/img]表3薄甲藻水样比对结果2.2.2结果分析2.2.2.1镜检视野内为单一薄甲藻,与AOA定性结果相差较大。从图7可知,绿藻和硅甲藻的光谱图很相似,从光谱图识别绿藻和硅甲藻是困难的,AOA的藻类分类和藻密度估量值仅能作为参考,要将监测数据做水体生态评估的依据,必须结合实验室镜检和萃取分析方法。[img=,690,496]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011547417547_4700_3247383_3.png!w690x496.jpg[/img]图72.2.2.2薄甲藻AOA测量值约为光度法的1/3,薄甲藻有鞭毛,可以自由游动,离开有利的生活条件则很快失去活性,沉入水底不再活动,且细胞内容物溶出。不能保证水样原始性状,是叶绿素a比对测定误差的主要来源。[img=,690,690]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011548482013_3683_3247383_3.jpg!w690x690.jpg[/img][color=#423B3B]2.2.2[/color][color=#423B3B].3[/color][color=#423B3B]薄甲藻细胞内容物溶出后,显微镜照片清楚看到细胞壁很薄,AOA测量结果印证黄色物质影响极小。[/color][b]2.3小球藻[img=,690,920]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011550015246_3694_3247383_3.jpg!w690x920.jpg[/img]图9 小球藻[/b]垃圾渗滤液水样,实验室放置几周,变绿,镜检结果:小球藻绝对优势,少量硅藻。[b]2.3.1实验结果[/b][img=,690,367]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011551332128_4472_3247383_3.png!w690x367.jpg[/img]表4小球藻水样比对[b]2.3.2结果分析[img=,537,303]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011552368052_2948_3247383_3.png!w537x303.jpg[/img][/b]图10小球藻水样线性分析2.3.2.1藻类分类与实验室镜检结果基本吻合;2.3.2.2低浓度出现少量蓝藻,因为仪器刚做完微囊藻样品,检测室可能有少量残留,比对实验之前彻底清洗检测室很有必要;2.3.2.3分光光度法相关系数小于AOA,并非方法不可行,而是叶绿素萃取太依赖分析人员的操作,稍有疏忽就会造成萃取损失,相比之下仪器要稳定可靠些。2.3.2.4小球藻叶绿素a测量结果AOA/分光光度法比值0.7-1.5,高于铜绿微囊藻和薄甲藻。两种方法测量结果比较接近的原因是因为小球藻不会运动,活体样品保持比较稳定的悬浮液状态,而AOA测量结果高于分光光度法的误差,一方面来自叶绿素和藻密度系数的确定,一方面来自萃取的损失。[img=,601,407]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011554177672_7731_3247383_3.png!w601x407.jpg[/img]图11AOA仪器校正界面 荧光测定仪校准即确定叶绿素和藻密度相关系数,可以给活体叶绿素传感器提供的最好标准物是浮游植物悬浮液,此悬浮液亦有部分用萃取方法测定叶绿素含量,并且应该从监测地点获得,这样的标准物质产生的荧光可以尽可能接近现场的生物体。荧光测定同时受浊度、温度、细胞活性、不同藻的种类、大小、形状、和叶绿素种类的影响,这些都大大限制活体测量的准确度。2.4不同水体样品分析[img=,690,267]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011555277271_2806_3247383_3.png!w690x267.jpg[/img]表5不同水体样品分析2.4.1与单一藻类样品结果一致,绿藻含量高的水样AOA测量值偏高,微囊藻水样上浮分层、甲藻和裸藻活性降低下沉造成水样不均匀分布,是比对结果偏低的一个因素。而在线监测时,水样中的藻类足够鲜活,吻合度会好些。2.4.2按照AOA提供的分类方法(图12),绿藻和蓝藻分类结果与镜检匹配,单一种类薄甲藻检测结果显示为绿藻、隐藻、蓝藻、极少量甲藻,镜检中数量可观的硅藻、裸藻在AOA测量结果中未见。[img=,600,350]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011602453540_1118_3247383_3.jpg!w600x350.jpg[/img]图122.4.3水库水质良好,杂质少,其它水体有机杂质含量相对高,AOA黄色物质测量结果与水体洁净程度吻合。[b]小结[/b]:萃取分析耗时长,不方便用于连续监测,需要有经验、高效率的分析人员才能得到准确、重复性好的结果。活体荧光法简便易操作,但准确度受更多因素的限制。两种方法不可互相替代,而应该取长补短,互为参照。参考文献 王丽娟,章岳蓬,郭步平等. 无水乙醇热浴超声法测定淡水中的叶绿素a.当代环保,2010,2(4):14-17.
原先用普通的可见分光光度法测了一系列的叶绿素含量。可老板不满意,叫用F-4500荧光仪测量。新手的我查了半天也没找到相关的标准方法,他又急着要,哭啊!不知道哪位大侠有这方面的资料,可否指点一下小弟。弟弟先在这儿谢谢您了!
各位大神,地表水同一个水样中叶绿素a含量,采用国标分析方法(分光光度法)的实验室检测结果,和市售自动检测仪器(传感器荧光法)的检测结果差好几个数量级,请问采用什么方法能够让国标方法的检测结果作为实验室真值,和自动检测仪器检测结果比对得上,或者说采用某种函数或算法,让两种方法的结果能够进行线性拟合,用来检验自动检测仪器的准确性?
荧光分光光度法测海水叶绿素a,脱镁叶绿素a为负值怎么回事
[font=宋体, SimSun][size=18px]根据《安徽省环境保护产业协会团体标准管理办法》相关要求,经专家组立项评审,现对2024年第一批团体标准(见附件)进行立项公示。[/size][/font][font=宋体, SimSun][size=18px]请申报单位按照有关要求,广泛听取意见,严格把控标准质量,按时完成团体标准制定任务。[/size][/font][font=宋体, SimSun][size=18px]为使各立项标准的制定更具广泛性、适用性,欢迎有意参与立项编制的有关企业、科研机构、高等院校等相关单位和个人与我会秘书处联系。[/size][/font][font=宋体, SimSun][size=18px]公示期间,任何单位和个人如对标准项目存在异议,请在公示期起7日内将意见反馈至我会秘书处。[/size][/font][font=宋体, SimSun][size=18px]联系电话:0551-62822367[/size][/font][font=宋体, SimSun][size=18px]附件:2024年第一批团体标准立项项目表[/size][/font][table][tr][td][font=宋体, SimSun][size=18px]序号[/size][/font][/td][td][font=宋体, SimSun][size=18px]项目名称[/size][/font][/td][td][font=宋体, SimSun][size=18px]主要起草单位[/size][/font][/td][/tr][tr][td][font=宋体, SimSun][size=18px]1[/size][/font][/td][td][font=宋体, SimSun][size=18px]《叶绿素荧光法水体初级生产力在线监测仪技术规范》[/size][/font][/td][td][font=宋体, SimSun][size=18px]中国科学院合肥物质科学研究院[/size][/font][/td][/tr][tr][td][font=宋体, SimSun][size=18px]2[/size][/font][/td][td][font=宋体, SimSun][size=18px]《藻类光合抑制法水质生物毒性在线监测仪技术规范》[/size][/font][/td][td][font=宋体, SimSun][size=18px]中国科学院合肥物质科学研究院[/size][/font][/td][/tr][tr][td][font=宋体, SimSun][size=18px]3[/size][/font][/td][td][font=宋体, SimSun][size=18px]《工业污染地块土壤和地下水修复工程全流程管理指南》[/size][/font][/td][td][font=宋体, SimSun][size=18px]合肥东部新中心建设投资有限公司[/size][/font][/td][/tr][tr][td][font=宋体, SimSun][size=18px]4[/size][/font][/td][td][font=宋体, SimSun][size=18px]《建设用地土壤污染风险管控和修复工程环境监理技术指南》[/size][/font][/td][td][font=宋体, SimSun][size=18px]合肥东新建邦环境修复有限公司[/size][/font][/td][/tr][tr][td][font=宋体, SimSun][size=18px]5[/size][/font][/td][td][font=宋体, SimSun][size=18px]《施工单位野外施工生态环境保护技术规程》[/size][/font][/td][td][font=宋体, SimSun][size=18px]安徽省公路桥梁工程有限公司[/size][/font][/td][/tr][/table][font=宋体, SimSun][size=18px][/size][/font][img]https://www.ttbz.org.cn/ueditor/dialogs/attachment/fileTypeImages/icon_pdf.gif[/img][url=https://www.ttbz.org.cn/upload/file/20240603/6385300438275050114134069.pdf]关于2024年第一批团体标准立项的公示.pdf[/url]
请问哪里有内置式烟气在线分析系统(采用紫外荧光法)的测量原理以及仪器说明?它的采样系统是怎样的结构?
标准里说的说的标准叶绿素 已买,但是就是不明白,为什么做出来酸化前的荧光值不稳定,变化还是挺大的,酸化后也是变化很多,里面的酸化因子是不是固定的,校准的那个标准浓度值是不是可以随意配制 ,小白求教了。还有就是做过这个方法的大神,可否告知一下,你标准叶绿素的浓度,以及做出来R,或者Ra Rb F 的值大概是多少?万分感激
我是分子荧光的新手,现在单位买了一台日立F-4500,不知道?还需要?资料和辅助才能做叶绿素叶绿素a(Sigma公司)的标准那里有卖啊?
内置式烟气在线分析系统,采用紫外荧光法,请问哪里有相关的文章或者仪器资料介绍?
如题[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=24112]叶绿素荧光原理[/url]
如何在水中提取叶绿素?利用某个波长检测叶绿素产生荧光,如何在水样中萃取叶绿素。
[align=center][size=16px][/size][/align][size=16px] 光合作用是地球上最重要的化学反应,植物、藻类及光合细菌等吸收光能、将[/size][size=16px]CO[/size][font='calibri'][sub][size=16px]2[/size][/sub][/font][size=16px]和水转化为有机物并释放[/size][size=16px]O[/size][font='calibri'][sub][size=16px]2[/size][/sub][/font][size=16px]。获得光能的叶绿素分子从基态跃迁到激发态,激发态的叶绿素分子可通过三种途径释放能量回到基态:推动光化学反应、以热的形式耗散、释放光子产生荧光。这三种途径的总和是一定的,因此叶绿素荧光的变化反映了光化学效率和热耗散能力的变化。叶绿素荧光成像是[/size][size=16px]广泛应用[/size][size=16px]的[/size][size=16px]光合生理研究的重要探针[/size][size=16px],[/size][size=16px]叶绿素荧光显微成像又将研究尺度进一步拓展到细胞、亚细胞水平。叶绿素荧光技术发展出了很多不同的测量程序,以慢诱导荧光动力学曲线为例,通过测量光([/size][size=16px]ML[/size][size=16px])、作用光([/size][size=16px]AL[/size][size=16px])、饱和脉冲光([/size][size=16px]SP[/size][size=16px])激发样品,记录动力学曲线并计算叶绿素荧光参数[/size][size=16px],[/size][size=16px]可以用于反映植物光合作用机理和光合生理状况([/size][size=16px]朱新广[/size][size=16px],[/size][size=16px]2021[/size][size=16px])。[/size][size=16px][/size][size=16px] 叶绿素荧光成像技术能记录整个叶片、植株等样品不同区域的荧光动力学分布变化,实现从宏观到微观的光合机理研究。叶绿素荧光成像由于其无损、高通量的技术特征,在光合作用相关突变体筛选领域成为了广泛应用的重要技术,为光合作用机理及抗[/size][size=16px]逆研究[/size][size=16px]提供了强大的技术支持。叶绿素荧光显微成像技术最早出现于[/size][size=16px]2000[/size][size=16px]年,[/size][size=16px]K[/size][size=16px]ü[/size][size=16px]pper[/size][size=16px]等人将叶绿素荧光脉冲调制式激发光源与显微镜结合,首次获得了显微尺度的叶绿素荧光图像([/size][size=16px]K[/size][size=16px]ü[/size][size=16px]pper[/size][size=16px] [/size][size=16px]et al.[/size][size=16px], 2000[/size][size=16px])。叶绿素荧光显微成像技术在国外已经展开多方面研究应用,[/size][size=16px]目前国内的叶绿素荧光成像显微研究尚处于起步阶段,多个课题组都[/size][size=16px]正[/size][size=16px]在[/size][size=16px]探索[/size][size=16px]这项技术[/size][size=16px]在[/size][size=16px]不同研究领域中[/size][size=16px]的[/size][size=16px]应用。[/size][size=16px][/size][size=16px] 叶绿素荧光技术[/size][size=16px]适用研究样品微观结构上光[/size][size=16px]合功能[/size][size=16px]的空间差异,例如叶片横截面栅栏组织与海绵组织的差异,[/size][size=16px]C[/size][size=16px]4[/size][size=16px]植物花环结构[/size][size=16px]中维管束鞘细胞与叶肉细胞的差异[/size][size=16px],藻类中有差异的单个细胞、异形胞[/size][size=16px]等。我们多年来与[/size][size=16px]吉林师范大学、四川省农业科学研究院[/size][size=16px]等[/size][size=16px]单位[/size][size=16px]合作[/size][size=16px],[/size][size=16px]目前已合作发表的[/size][size=16px]3[/size][size=16px]篇相关论文是国内该领域[/size][size=16px]开创性[/size][size=16px]的应用成果,[/size][size=16px]以叶绿素荧光显微成像的特色优势技术[/size][size=16px]为光合作用的微观[/size][size=16px]探究提供有力支撑[/size][size=16px]。[/size][size=16px][/size][size=16px] Yu[/size][size=16px]等[/size][size=16px]发现[/size][size=16px]狗枣猕猴桃[/size][size=16px]([/size][size=16px]A[/size][size=16px]ctinidia [/size][size=16px]kolomikta[/size][size=16px])[/size][size=16px]的白化[/size][size=16px]叶片[/size][size=16px]通过调整叶片结构及基因表达调控,仍然保持了相对较高的光合能力[/size][size=16px]。[/size][size=16px]应用[/size][size=16px]叶绿素荧光显微成像技术[/size][size=16px]比较了[/size][size=16px]白化和绿色叶片栅栏组织、海绵组织的叶绿素荧光参数,[/size][size=16px]揭示了白化叶片海绵组织光[/size][size=16px]合能力[/size][size=16px]增强的机理[/size][size=16px]。[/size][size=16px]绿叶中栅栏组织[/size][size=16px]F[/size][font='calibri'][size=14px][sub][size=16px]v[/size][/sub][/size][/font][size=16px]/[/size][size=16px]F[/size][font='calibri'][size=14px][sub][size=16px]m[/size][/sub][/size][/font][size=16px](最大光化学效率)[/size][size=16px]更高,而白叶中海绵组织[/size][size=16px]显著增厚,[/size][size=16px]F[/size][font='calibri'][size=14px][sub][size=16px]v[/size][/sub][/size][/font][size=16px]/[/size][size=16px]F[/size][font='calibri'][size=14px][sub][size=16px]m[/size][/sub][/size][/font][size=16px]更高[/size][size=16px],[/size][size=16px]光[/size][size=16px]合能力[/size][size=16px]增强,补偿[/size][size=16px]了[/size][size=16px]白化的影响,成为叶片光合作用主力组织[/size][size=16px]([/size][size=16px]Yu [/size][size=16px]et al.[/size][size=16px], 2022[/size][size=16px])[/size][size=16px]。[/size][size=16px]接下来[/size][size=16px]Chen[/size][size=16px]等又比较了两种猕猴桃白化叶片的光保护策略差异[/size][size=16px],狗枣猕猴桃的白叶[/size][size=16px]主要通过反射实现光保护,强光下花青素[/size][size=16px]积累,叶片[/size][size=16px]转变为粉色[/size][size=16px],更有效地保护叶片[/size][size=16px];[/size][size=16px]而[/size][size=16px]葛[/size][size=16px]枣猕猴桃([/size][size=16px]A[/size][size=16px]ctinidia[/size][size=16px] [/size][size=16px]polygama[/size][size=16px])[/size][size=16px]强光下[/size][size=16px]仍为白色[/size][size=16px],[/size][size=16px]具[/size][size=16px]有更[/size][size=16px]强[/size][size=16px]的叶绿[/size][size=16px]素荧光参数,说明[/size][size=16px]它[/size][size=16px]具有更高的强光适应能力[/size][size=16px]([/size][size=16px]Chen[/size][size=16px] [/size][size=16px]et al.[/size][size=16px], 202[/size][size=16px]3[/size][size=16px])。[/size][size=16px]Liu[/size][size=16px]等比较了干旱处理下的玉米叶肉细胞和维管束鞘细胞,发现这两种细胞具有不同的不同光保护策略[/size][size=16px]。对玉米[/size][size=16px]完整叶片的分析显示,[/size][size=16px]随着干旱处理程度增强,[/size][size=16px] [/size][size=16px]F[/size][font='calibri'][size=14px][sub][size=16px]v[/size][/sub][/size][/font][size=16px]/[/size][size=16px]F[/size][font='calibri'][size=14px][sub][size=16px]m[/size][/sub][/size][/font][size=16px]、[/size][size=16px]Φ[/size][font='calibri'][size=14px][sub][size=16px]PSII[/size][/sub][/size][/font][size=16px](实际光化学效率)[/size][size=16px]降低,[/size][size=16px]NPQ[/size][size=16px](非光化学猝灭[/size][size=16px]系数[/size][size=16px])[/size][size=16px]显著升高[/size][size=16px]。进一步应用[/size][size=16px]叶绿素荧光显微成像[/size][size=16px]的分析结果[/size][size=16px]与完整叶片[/size][size=16px]相符合,并且发现[/size][size=16px]与叶肉细胞相比,维管束鞘细胞[/size][size=16px] [/size][size=16px]F[/size][font='calibri'][size=14px][sub][size=16px]v[/size][/sub][/size][/font][size=16px]/[/size][size=16px]F[/size][font='calibri'][size=14px][sub][size=16px]m[/size][/sub][/size][/font][size=16px]、[/size][size=16px]Φ[/size][font='calibri'][size=14px][sub][size=16px]PSII[/size][/sub][/size][/font][size=16px]更低,干旱胁迫后[/size][size=16px]NPQ[/size][size=16px]升高更显著[/size][size=16px],[/size][size=16px]不同细胞的变化趋势[/size][size=16px]差异[/size][size=16px]表明它们[/size][size=16px]具有不同的光保护策略[/size][size=16px],[/size][size=16px]维管束鞘细胞中可能具有更强的热耗散能力[/size][size=16px]([/size][size=16px]Liu [/size][size=16px]et al.[/size][size=16px], 2022[/size][size=16px])。[/size][size=16px][/size][size=16px] 叶绿[/size][size=16px]素[/size][size=16px]荧光显微成像技术在光合作用的微观研究领域具有独特的技术优势,在[/size][size=16px]光合作用机理研究、环境及毒理胁迫与抗性筛选、优良品系选育等领域[/size][size=16px]具[/size][size=16px]有广阔的应用前景。目前多家单位的科研人员[/size][size=16px]都[/size][size=16px]在[/size][size=16px]探索该技术[/size][size=14px][size=16px]的新应用,我们也正在[/size][size=16px]将该技术拓展到[/size][size=16px]多个新的领域,例如对[/size][size=16px]原生质体[/size][size=16px]以及[/size][size=16px]种子、茎秆等非叶片器官的[/size][size=16px]研究[/size][size=16px]。[/size][/size][font='黑体']参考文献:[/font][font='calibri'][size=13px][1] [/size][/font][font='calibri'][size=13px]朱新广[/size][/font][font='calibri'][size=13px], [/size][/font][font='calibri'][size=13px]许大全主编[/size][/font][font='calibri'][size=13px]. [/size][/font][font='calibri'][size=13px]光合作用研究技术[/size][/font][font='calibri'][size=13px], [/size][/font][font='calibri'][size=13px]上海科学技术出版社[/size][/font][font='calibri'][size=13px], 2021[/size][/font][font='calibri'][size=13px][2] [/size][/font][font='calibri'][size=13px]H[/size][/font][font='calibri'][size=13px]. [/size][/font][font='calibri'][size=13px]Küpper[/size][/font][font='calibri'][size=13px],[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]I[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]?etlík[/size][/font][font='calibri'][size=13px], [/size][/font][font='calibri'][size=13px]M[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]Trtílek[/size][/font][font='calibri'][size=13px],[/size][/font][font='calibri'][size=13px] et al. [/size][/font][font='calibri'][size=13px]Photosynthetica[/size][/font][font='calibri'][size=13px], 2000, 38, s553-570 [/size][/font][font='calibri'][size=13px][3] [/size][/font][font='calibri'][size=13px]M[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]Yu, [/size][/font][font='calibri'][size=13px]L[/size][/font][font='calibri'][size=13px]. [/size][/font][font='calibri'][size=13px]Chen, [/size][/font][font='calibri'][size=13px]D[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] H[/size][/font][font='calibri'][size=13px]. [/size][/font][font='calibri'][size=13px]Liu[/size][/font][font='calibri'][size=13px],[/size][/font][font='calibri'][size=13px] et al. [/size][/font][font='calibri'][size=13px]Front. Plant Sci.[/size][/font][font='calibri'][size=13px], 2022, 13: 856732 [/size][/font][font='calibri'][size=13px][4] [/size][/font][font='calibri'][size=13px]L[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] Chen[/size][/font][font='calibri'][size=13px],[/size][/font][font='calibri'][size=13px] D[/size][/font][font='calibri'][size=13px]. [/size][/font][font='calibri'][size=13px]Q[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] Wen[/size][/font][font='calibri'][size=13px],[/size][/font][font='calibri'][size=13px] G[/size][/font][font='calibri'][size=13px]. [/size][/font][font='calibri'][size=13px]L[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] Shi[/size][/font][font='calibri'][size=13px],[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]et al.[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]Physiol. Plant.[/size][/font][font='calibri'][size=13px], 2023, [/size][/font][font='calibri'][size=13px]175:[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]e13880[/size][/font][font='calibri'][size=13px][5] [/size][/font][font='calibri'][size=13px]W[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] J[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]Liu, [/size][/font][font='calibri'][size=13px]H[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]Liu, [/size][/font][font='calibri'][size=13px]Y[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] E[/size][/font][font='calibri'][size=13px].[/size][/font][font='calibri'][size=13px] [/size][/font][font='calibri'][size=13px]Chen[/size][/font][font='calibri'][size=13px],[/size][/font][font='calibri'][size=13px] et al. [/size][/font][font='calibri'][size=13px]Front. Plant Sci.[/size][/font][font='calibri'][size=13px], 2022, 13: 885781[/size][/font]
[align=center]水中油在线监测法--紫外荧光法与红外法的对比介绍[/align] 水中的油分属于有机污染物的一种,其降解会导致水中溶解氧含量的下降,导致水质恶化,因此,在污水排放口以及地表水监测领域,水中油是重要的监测指标。在线水中油是近年来水质监测的新热点,可以覆盖到工业冷却水、循环水、锅炉用水、中水回用、污水排放等应用领域,尤其是在石化、炼油等行业的循环水处理领域。同时水中油也是地表水监测的一项重要指标。 国家环境保护总局 2002-12-25发布的自2003-01-01开始实施的中华人民共和国环境保护行业标准(HJ/T 92—2002)《水污染物排放总量监测技术规范》指出水污染物排放总量监测项目和监测方法中石油类、动植物油监测方法的自动在线监测法为(红外法、荧光法)。[align=left](1)红外法[/align][align=left]1)测定原理:采用有机溶液(四氯化碳、四氯乙烯等)萃取水样后,用三波长红[/align][align=left]外光度法或非分散红外法测定。[/align][align=left]2) 性能指示:[/align][align=left](1) 测定范围:0-20mg/L至0-100mg/L[/align][align=left](2) 重线性:±10%以内[/align][align=left](3) 测定周期:10min[/align][align=left](4) 输出信号: DC0-5V 4-20mA DC[/align][align=left](2)荧光法[/align][align=left] 紫外荧光作为最快速且具有良好选择性的方法,它可以检测到非常低浓度的水中油,是一种可靠性强维护量低的稳定测量系统,它适用于江河,湖泊和水库;设备冷却水;废水(炼油厂和化工厂排出的污水)[/align][align=left] 测定原理:水中石油类的测定也可以采用荧光法,主要测定水中含苯环的化合物,该方法采用直接测定水样的方法。多环芳烃具有很强的荧光特性,他们可以吸收紫外荧光,同时,受到紫外光激发会产生可见光波段的荧光,在波长254nm的荧光照射下,油类物质特征比230nm时要强。经过大量实验,我们确定用254nm的紫外光激发,水中油中的多数成分具有最强烈的荧光特性。不需要试剂,降低运行成本。采用与手工油类测定方法的比对实验,可间接得到水中的石油类浓度。 采用荧光法制成的仪器对水中油有非常良好的选择性,分析技术可应用于实验室也可应用于现场在线监测,荧光法测水中油很容易解决水中悬浮物等的影响,一般来说不需要对化合物和样品的背景干扰进行修正,荧光法检出限低(最低可达0.001mg/L),动态检测范围宽(0.005mg/L-1000mg/L),干扰因素少,即时测量分析速度快,可有效测量溶于水的油(光折射、散射法只能测量少的油滴)。[/align][align=left][b][color=black]两种监测方法对比:[/color][/b][/align][align=left][color=black] [/color][/align][table=625][tr][td][align=center][color=black] [/color][/align][align=center][color=black]方法[/color][/align][/td][td][align=center][color=black]紫外荧光法[/color][/align][align=center][color=black]Uvpcx[/color][color=black](HX1000)[/color][/align][/td][td][align=center][color=black]萃取+红外[/color][/align][align=center][color=black]吸收法[/color][/align][/td][td][align=center][color=black]吹脱+离子火焰[/color][/align][align=center][color=black]检测器(FID)[/color][/align][/td][td][align=center][color=black]紫外荧光法[/color][/align][align=center][color=black]开放式流通池流通池+汞灯[/color][/align][/td][/tr][tr][td][align=center][color=black]测量时间[/color][/align][/td][td][align=center][color=black]5[/color][color=black]分钟[/color][/align][/td][td][align=center][color=black]5[/color][color=black]分钟[/color][/align][/td][td][align=center][color=black]30Kg[/color][/align][/td][td][align=center][color=black]30Kg[/color][/align][/td][td][align=center][color=black]30Kg[/color][/align][/td][/tr][tr][td][align=center][color=black]用车或客机随身运输[/color][/align][/td][td][align=center][color=black]可以[/color][/align][/td][td][align=center][color=black]不可以[/color][/align][/td][td][align=center][color=black]不可以[/color][/align][/td][td][align=center][color=black]不可以[/color][/align][/td][/tr][tr][td][align=center][color=black]安装时间[/color][/align][/td][td][align=center][color=black]一小时[/color][/align][/td][td][align=center][color=black]几天[/color][/align][/td][td][align=center][color=black]几天[/color][/align][/td][td][align=center][color=black]几小时[/color][/align][/td][/tr][/table][align=left] [/align][align=left] 目前紫外荧光法已在美国、加拿大、瑞士、俄罗斯等发达地区和国家广泛应用并被列为标准。我国国家标准《海洋监测规范》GB17378.5-1998 也采用荧光法测量海水中的油,国家环境保护总局颁布的 HU/T 92-2002 《水污染物排放总量监测技术规范》中也明确规定水中油自动在线测量法为荧光法,我国水利部门也考虑采用荧光法测量地表水中的油污染。在地表水及水源水监测领域,水中油日益成为一个重要的监测参数。[/align][align=left] 油田采出水基本监测物质为水中油、悬浮物、温度等值,通过监测这几项指标的数值可以对采油过程进行指导,及时修改水处理过程中的参数,降低损失。[/align][align=left] 将采出水处理后回注于油层,不仅可以回收水中的原油、实现水的循环利用、改善环境污染情况,而且提供了充足的注水水源、节约大量的淡水资源,取得了显著的经济效益和社会效益。如果把含油废水处理后,重新回注地层,以补充地层的压力,不仅可以避免环境污染,而且节约大量的水资源。[/align][align=left] [/align]
用XRF荧光法分析炉渣中的S含量,准吗?和碳硫分析仪相比如何?欢迎各位积极讨论!
X荧光硫元素分析仪是为了适应油品中硫含量检测需要而开发制造的X荧光分析仪。它采用能量色散原理,机电一体微机化设计,分析快速、准确。其重复性、再现性都符合国家标准GB/T 17040和GB 11140的相关要求,也符合美国国家标准D 4294-03的要求,它为原油或石油化工生产过程中硫含量的检测,提供了帮助。[font=&]得利特(北京)科技有限公司20多年专注于油品分析仪器的研发和销售活动,我公司产品有:油液污染度检测仪、酸值测定仪、微量水分测定仪、凝点倾点测定仪、体积电阻率测定仪、介电强度测定仪、介质损耗测定仪、水溶性酸测定仪、界面张力测定仪、析气性测定仪、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析仪、多功能振荡仪、腐蚀性硫测定仪、闭口闪点测定仪等多种绝缘油分析仪器、燃料油分析仪器、润滑油分析仪器,水质分析检测仪器、气体检测仪器,型号多,质量保证,可定制。最近新出了:动力粘度测定仪、智能粘度测量仪、相对粘度测定仪、PVC比浓粘度测定仪、特性粘度测定仪、粘均分子量测定仪、聚酯粘度仪、自动乌氏粘度仪、自动粘度仪、自动尼龙粘度仪。[/font]

[size=16px] 叶绿素测定仪如何检测植物氮含量 叶绿素测定仪通常用于测定叶片中的叶绿素含量,而不是植物的氮含量。要测定植物的氮含量,通常需要使用其他类型的仪器和方法,如Kjeldahl法、Dumas法或氮元素分析仪。 以下是如何使用Kjeldahl法来测定植物的氮含量的基本步骤: 样品准备: 收集你要测定的植物样品,并将其剪碎成小块,以便更容易处理。 将样品干燥,以去除多余的水分。 氮的提取: 将干燥的植物样品加入Kjeldahl消解管中。 向样品中加入硫酸(H2SO4)和催化剂,通常是硒或汞的化合物。这些化学品将有机氮转化为无机氮。 使用Kjeldahl消解仪将样品消解,通常是在高温下进行。 蒸发和冷却: 将消解后的样品加热以蒸发水分,直到样品中只剩下无机氮。 将消解管中的液体冷却,使其凝结成液体。 中和和滴定: 向冷却的液体中加入氢氧化钠(NaOH)以中和其中的酸性。 使用酸碱指示剂,如酚酞或溴甲酚绿,来监测酸性的中和点。 然后,使用已知浓度的硫酸(H2SO4)溶液进行滴定,直到液体再次变酸,指示剂的颜色发生改变。滴定的体积可以用于计算氮的含量。 计算氮含量: 使用已知的滴定体积和硫酸浓度,计算出样品中的氮含量,通常以百分比或毫克/克的形式表示。 需要注意的是,Kjeldahl法是一种相对复杂的化学分析方法,需要严格的实验室条件和设备,以确保准确性和安全性。测定氮含量的其他方法可能也可行,具体选择取决于你的实验室资源和样品类型。如果你没有化学分析的经验,云唐建议最好寻求专业的实验室支持或咨询专业化学家。[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2023/09/202309181126073212_7562_6098850_3.jpg!w690x690.jpg[/img][/size]
任何用荧光分光光度计测绿叶中叶绿素的含量?
[align=center][b][/b][/align][align=center][b]原子荧光法测汞的试剂影响分析[/b][/align][align=center][/align][b]摘 要[/b]:硼氢化钾浓度和盐酸浓度对原子荧光法测汞产生重要影响,分别从化学反应原理和数理统计角度对此进行定性和定量分析。结果表明,校准曲线的灵敏度随着硼氢化钾浓度升高而下降;当硼氢化钾浓度为0.5 g/L时,曲线斜率平均值为1262,标准偏差和离散系数分别为8.4 %和0.007,表明曲线的灵敏度和稳定性较高;当盐酸浓度为5 %时,空白荧光值最低。在该优化实验条件下测量0.25 μg/L和0.50 μg/L标准样品,标准偏差分别为1.1 %和0.7 %,精密度和准确度较高。[b]关键词[/b]:原子荧光;汞;硼氢化钾;盐酸[align=center][/align][align=center][b]The Effect of the Reagent on the Mercury by Aomic Fluorescence Spectrometry[/b][/align][align=left][b][b]Abstract:[/b][/b]The concentrations of potassium borohydride and hydrochloric acid have important impact on the determination of mercury by atomic fluorescence spectrometry. In terms of perspective of chemical reaction and mathematical statistics,the impact was analyzed with qualitative and quantitative analysis method. The results show that when the concentration of potassium borohydride is 0.5 g/L,the average value of the curve slopes is 1262,and the standard deviation and dispersion coefficient is 8.4 % and 0.007,respectively. The measurement sensitivity and reliability are higher. When the concentration of hydrochloric acid is 5 %,the blank value is the lowest. Under the optimized experimental condition,0.25 μg/L and 0.50 μg/L standard samples were measured with a standard deviation of 1.1 % and 0.7 %,respectively,and the precision and accuracy are higher.[/align][align=left][b]Key words:[/b]atomic fluorescence spectrometry;mercury;potassium borohydride;hydrochloric acid[/align][align=left][/align][align=left] 汞及其化合物属于毒性物质,过量的汞被人体摄入后,会损害肾脏、心脏、甲状腺等器官,甚至造成神经系统紊乱和慢性汞中毒[sup][/sup]。同时,汞污染具有远距离迁移性、持久性及高生物富集性等特性,通过排放废水、废气、废渣等方式进入自然环境,对水体、空气、土壤、动植物等造成危害。因此,汞被联合国环境规划署列为全球性优先控制污染物,成为全世界广泛关注的环境污染物之一[sup][/sup]。在我国,水体汞污染主要是由工业废水排放引起的,有研究指出,吉林松花江流域、贵州万山地区等都曾受过严重汞污染,已出现人群汞中毒病例报告[sup][[/sup][sup]3[/sup][sup]][/sup]。鉴于此,《污水综合排放标准(GB 8978-1996)》规定汞排放浓度不得超过0.05 mg/L[sup][/sup]。此外,新型人工合成化学物质的投入使用,导致地下水中含汞化学组分发生了变化。2017年新颁布的《地下水质量标准(GB/T 14848-2017)》对汞的指标限值进行了相应的修订,例如,Ⅰ类水标准由0.05 μg/L修订为0.1 μg/L,Ⅱ类水标准由0.5 μg/L修订为0.1 μg/L[sup][/sup]。因此,不断提高测量技术,准确测定水中汞含量,对人体健康和环境安全具有重要的意义。[/align][align=left] 目前,我国研究人员对汞的测量方法进行了大量的研究,包括分光光度法、冷[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法、冷原子荧光法、阳极溶出伏安法、[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]电感耦合等离子体质谱[/color][/url]法以及生化检测方法等[sup][/sup]。其中,原子荧光法具有检出限和测定下限低、灵敏度高、干扰因素少、操作简便等优点,是国内环境监测领域普遍采用的测汞方法。然而不同实验室的环境参数、仪器类型、测量条件等存在差异,因此需要不断优化测量条件,提高分析灵敏度和精密度。在测量过程中会受到一些因素的影响,其中,硼氢化钾和盐酸浓度的影响较为关键。本研究通过量化分析试剂的影响,确定最佳浓度,以满足测量天然水体中痕量汞的测定要求。[/align][align=left][b]1. 实验方法[/b][/align][align=left][b]1.1 原理[/b][/align][align=left] 在酸性介质中,二价汞离子被硼氢化钾还原成汞原子,由载气(氩气)带入原子化器,氢气与氩气在点火装置作用下形成氩氢火焰。在汞空心阴极灯照射下,基态汞原子受激发并跃迁至高能态,然后由去激发由高能态跃迁至基态时,产生具有特征波长(253.7 nm)的原子荧光。根据朗伯-比尔定律,在一定范围内汞浓度与荧光强度成正比,由此可测量汞浓度。[/align][align=left][b]1.2 仪器与试剂[/b][/align][align=left][b]1.2.1 仪器参数[/b][/align][align=center][b][b]表1 仪器参数设置[/b][/b][/align][align=center][img=,690,225]http://ng1.17img.cn/bbsfiles/images/2018/08/201808011650384665_8402_2116599_3.png!w690x225.jpg[/img][/align][align=left][b] [/b] (注:为避免广告嫌疑,仪器型号已略去)[/align][align=left]1.2.2 试剂[/align][align=left]1) 实验用水:电导率为18 mΩcm的去离子水;2) 盐酸、硝酸、硼氢化钾、氢氧化钾均为优级纯;3) 汞标准溶液:100 mg/L,由环境保护部标准样品研究所提供;4) 汞固定液:0.5 g重铬酸钾溶于950 mL水,加入50 mL硝酸,充分混匀;5) 汞标准储备液:量取10.0 mL汞标准溶液至500 mL容量瓶中,用汞固定液稀释至标线,充分混匀,该溶液的汞浓度为2.0 mg/L;6) 汞标准中间液:量取2.5 mL汞标准储备液至250 mL容量瓶中,用汞固定液稀释至标线,充分混匀,该溶液的汞浓度为20.0 μg/L;7) 汞标准使用液:量取5.0 mL汞标准中间液至100 mL容量瓶中,加入体积分数5%盐酸定容至标线,充分混匀,该溶液的汞浓度为1.0 μg/L;8) 本实验所用仪器可自动配制标准溶液系列,汞浓度分别为0.1 μg/L、0.2 μg/L、0.4 μg/L、0.8 μg/L、1.0 μg/L;9) 汞标准质量控制样品(编号202036):量取10.0 mL该溶液至250 mL容量瓶中,加入3 %硝酸定容至标线,充分混匀,该样品浓度范围为6.68±0.73 μg/L,由XX样品研究所提供。(注:标准样品名称已略去)[/align][align=left][b]1.2.3实验步骤[/b][/align][align=left] 按照表1内容设置仪器参数,根据仪器操作规程进行测量。[/align][align=left][b]2. 结果与讨论[/b][/align][align=left][b]2.1 硼氢化钾浓度对荧光强度的影响[/b][/align][align=left] 在酸性条件下,样品溶液中的汞(Hg)与硼氢化钾(KBH[sub]4[/sub])反应生成汞蒸气。化学反应方程式如下:[/align][align=center][img=,284,54]http://ng1.17img.cn/bbsfiles/images/2018/08/201808011701366440_1452_2116599_3.png!w284x54.jpg[/img][/align][align=left] 硼氢化钾的分解在pH 3.8-14之间为二级反应,反应速率常数为1.22 × 10[sup]8 [/sup]mol/min(30 ℃),该反应可在极短时间内完成,表明硼氢化钾的稳定性较差。在酸性条件下,硼氢化钾易分解产生氢气,所以需要先配制碱液再加入硼氢化钾,以抑制反应向右进行,防止溶液中硼氢化钾分解损失。在碱性条件下,硼氢化钾可将离子态汞还原成原子态汞。由朗伯-比尔定律可知,汞浓度与荧光强度成正比,当汞浓度变化时,荧光强度也随之变化,因此硼氢化钾浓度也会对荧光强度产生影响。硼氢化钾浓度过低,汞难以被充分还原,导致荧光强度偏低;浓度过高,产生大量的氢气会稀释汞浓度,同样导致荧光强度降低。硼氢化钾浓度的确定,应满足两个要求,一是硼氢化钾浓度应是稍过量的,使样品溶液中的汞被充分还原;二是硼氢化钾溶液为临用现配,在测量结束后往往会有剩余,在充分还原汞的前提下,应减少试剂消耗量,降低对环境的污染。不同研究者对硼氢化钾最佳浓度进行了研究,研究结果见表2。[/align][align=center][b]表2 不同试剂浓度及仪器参数比较[/b][/align][align=center][img=,690,231]http://ng1.17img.cn/bbsfiles/images/2018/08/201808011704005598_2631_2116599_3.png!w690x231.jpg[/img][/align][align=left] 注:“—”表示作者未该数据;“*”表示硝酸浓度。(仪器型号已略去)[/align] 研究表明,除硼氢化钾浓度外,实验室温度、盐酸浓度、负高压、灯电流、原子化器高度等因素也对测量结果造成影响[sup] [/sup]。胡刚等[sup][/sup]研究表明,负高压增大、灯电流减小,以及原子化器高度降低,都会导致仪器信号噪声增大,灵敏度降低。纪久成等[sup][/sup]研究表明,环境温度、湿度,以及光漂移也对测量值造成影响。在不同实验条件下,各研究者分析了硼氢化钾的最佳浓度,其变化范围为0.1~20 g/L。尽管差异较大,但曲线的相关系数都大于0.999,符合《水质 汞、砷、硒、铋和锑的测定 原子荧光法(HJ 694-2014)》中大于或等于0.995的规定[sup][/sup]。在环境监测领域中,一般用曲线相关系数作为精密度的指标,用曲线斜率作为灵敏度的指标。部分研究者以曲线相关系数和斜率为指标来确定硼氢化钾最佳浓度。然而,仅以该指标作为评价方法,笔者认为缺乏严谨性。例如,原子荧光光谱仪中的汞灯存在光漂移现象,荧光强度随着测量次数增加而升高,即使相关系数符合规定要求,但变化了的荧光强度会影响样品测量结果,导致误差增大。为更准确评价硼氢化钾浓度的影响,本研究运用数理统计方法中的标准偏差和离散系数,结合相关系数和斜率进行综合判断。按照表1内容设定仪器参数,并配制不同浓度的硼氢化钾溶液,按照臧慕文[sup][/sup]推荐的测量次数,每种浓度分别测量4次,得出各点浓度及校准曲线,以此分析硼氢化钾浓度对荧光值的影响。实验结果见表3。[align=center][b]表3 硼氢化钾浓度测量结果[/b][/align][align=center][img=,690,537]http://ng1.17img.cn/bbsfiles/images/2018/08/201808011706225918_4392_2116599_3.png!w690x537.jpg[/img][/align][align=center] 由表3可知,硼氢化钾浓度从0.1 g/L到15.0 g/L变化时,斜率变化范围为841~1340,相关系数变化范围为0.9996~1.0000,说明各浓度硼氢化钾线性拟合度较好。在统计学中,用斜率表征测量方法的灵敏度,灵敏度越高,单位浓度待测物质变化引起的测量信号响应量越大,反之越小。对硼氢化钾各浓度对应的曲线斜率求平均值,计算结果见表3。当硼氢化钾浓度为0.1 g/L时,灵敏度最高,其值为1321;浓度为15.0 g/L时,灵敏度最低,其值为854。可见,随着硼氢化钾浓度升高,平均斜率呈下降趋势。根据式(1)和式(2)反应原理,硼氢化钾浓度升高时,稀释了原子态汞的浓度,从而降低了汞的荧光强度,灵敏度降低。朱茂森等[sup][[/sup][sup]8[/sup][sup]][/sup]研究结果表明,当硼氢化钾浓度从0.3 g/L升高到20.0 g/L时,曲线的斜率逐渐降低,与本研究结果一致。从灵敏度角度分析,测量溶液中的汞应尽量使用低浓度硼氢化钾,以提高测量精确度。[/align] 然而,灵敏度越高不代表测量效果越好。当灵敏度高时,若曲线波动较大,会导致误差增大,稳定性和可靠性降低。引用数理统计中标准偏差和离散系数进行分析,可量化评价测量结果的稳定性和可靠性。标准偏差用来表征该组数据的离散性,计算方法见式(3);当不同组数据的平均水平相差较大时,可用离散系数来评价其离散性,计算方法见式(4)。[align=center][img=,172,138]http://ng1.17img.cn/bbsfiles/images/2018/08/201808011708030848_7428_2116599_3.png!w172x138.jpg[/img][/align] 式中,S为标准偏差,y为斜率值,[img=,15,26]file:///C:\Users\ADMINI~1\AppData\Local\Temp\ksohtml\wps5122.tmp.png[/img] 为斜率平均值,n为测量次数,σ为离散系数。 根据式(3)和(4)计算斜率的标准偏差和离散系数,计算结果见表3。结果表明,当硼氢化钾浓度从0.1 g/L到15.0 g/L变化时,斜率的标准偏差变化范围为8.4~15.0 %,离散系数变化范围为0.007~0.017。当硼氢化钾浓度为0.5 g/L时,标准偏差和离散系数最低,分别为8.4 %和0.007,表明曲线斜率在该浓度点变化较稳定,可靠性较高。当硼氢化钾浓度为0.1 g/L和15.0 g/L时,标准偏差和离散系数均最高,表明硼氢化钾浓度对曲线斜率有重要影响。浓度过低,虽然斜率最高,但波动较大;浓度过高,硼氢化钾已稀释了汞蒸气浓度,降低了斜率,可靠性较低。因此,当曲线相关系数满足规定要求、灵敏度较高,且标准偏差和离散系数较低时,在测量河流、地下水等天然水体中痕量汞时,可适当降低硼氢化钾浓度。本实验确定硼氢化钾最佳浓度为0.5 g/L,与《水质 汞、砷、硒、铋和锑的测定 原子荧光法(HJ 694-2014)》中10.0 g/L的规定浓度相比,消耗量降低了95 %。潘腊青等[sup][/sup]研究的最佳浓度为0.1 g/L~0.7 g/L,朱茂森等[sup][/sup]研究的最佳浓度范围为0.3 g/L,均与本研究结果相差不大。[b]2.2 硼氢化钾浓度和盐酸浓度对空白值的影响 [/b] 在分析过程中,原子荧光空白值对结果有重要的影响。影响空白值的因素包括试剂(实验用水、酸、还原剂等)、测量条件(负高压、原子化器高度、灯电流等)以及外界环境条件(温度和湿度)等。胡刚等[sup][[/sup][sup]14[/sup][sup]][/sup]研究结果表明,盐酸浓度过高,导致空白荧光值难以达到空白判定值要求,测量结果不确定度增大,可靠性降低。尚立成等[sup][[/sup][sup]18[/sup][sup]][/sup]研究表明,硼氢化钾浓度越高,空白值越高。本实验分别配制0.1 g/L、0.5 g/L、1.0 g/L、5.0 g/L、10.0 g/L五种浓度的硼氢化钾(氢氧化钾浓度为0.5 %),并分别配制3 %、5 %、7 %、9 %四种浓度的盐酸,通过测量汞空白值来分析其变化趋势。分析结果见图1。[align=center][img=,482,334]http://ng1.17img.cn/bbsfiles/images/2018/08/201808011709247728_290_2116599_3.png!w482x334.jpg[/img][/align][align=center][b]图1 盐酸浓度与硼氢化钾浓度对空白值的影响[/b][/align][align=center] 由图1可知,当硼氢化钾浓度不变时,随着盐酸浓度升高,空白荧光值呈先下降后上升的趋势,盐酸浓度为5 %时空白荧光值最低。盐酸作为载流,有两方面作用,一是使硼氢化钾在酸性条件下维持稳定的分解速率,二是使汞元素保持一定的价态。在5 %盐酸浓度下,硼氢化钾可维持较高的分解速率,且汞在反应过程中保持稳定的价态,这些因素有利于降低空白荧光值,浓度过低或过高都会导致空白荧光值升高。因此,5 %盐酸浓度可作为载流的最佳浓度。此外,由图1可知,盐酸浓度一定时,随着硼氢化钾浓度升高,空白荧光值也随之升高。这也可以解释本文上节中硼氢化钾浓度升高则汞荧光值降低的现象,由于汞荧光强度是扣除空白值后得到的结果,当空白值升高时,汞荧光强度相对降低,灵敏度也相应降低。[/align][align=left][b]2.3 标准溶液和质量控制样品的测定[/b][/align] 本研究中,当硼氢化钾浓度为0.5 g/L、盐酸浓度为5 %时,仪器的灵敏度和稳定性较高。在不改变仪器参数条件下,分别测量0.25 μg/L、0.50 μg/L浓度的标准溶液及质量控制样品(编号202036)。测量结果见图2及表4。[align=center][img=,397,305]http://ng1.17img.cn/bbsfiles/images/2018/08/201808011711063338_5818_2116599_3.png!w397x305.jpg[/img][/align][align=center][b]图2 汞标准曲线[/b][/align][align=center][b]表4 标准溶液及质量控制样品测量结果[/b][/align][align=center][img=,588,314]http://ng1.17img.cn/bbsfiles/images/2018/08/201808011711559360_6271_2116599_3.png!w588x314.jpg[/img][/align][align=center][b] [/b]由图2可知,汞标准曲线拟合方程为y = 1250.38x - 16.4376,相关系数为0.9997,曲线的精密度较好。由表5可知,在实验确定条件下测量标准溶液和质量控制样品,数据标准偏差较小,具有较高的精密度。只有根据仪器参数条件确定最佳硼氢化钾浓度和盐酸浓度,并在测量过程中强化质量控制,才能充分发挥该方法的快速、准确的优点,提高分析的准确性和可靠性。[/align][b]3 结论[/b]1) 从化学反应原理分析,硼氢化钾存在最佳反应浓度,过低或过高都会导致荧光强度降低,在保证汞被充分还原的前提下,应使硼氢化钾稍过量。2) 当硼氢化钾浓度为0.5 g/L时,曲线标准偏差和离散系数最低,分别为8.4 %和0.007,表明斜率在该浓度点变化较稳定,可靠性较高。该实验条件可使硼氢化钾消耗量减少95 %。3) 硼氢化钾浓度越低,空白荧光值越低;当盐酸浓度为5 %时,空白荧光值最低,灵敏度最高。4) 采用优化的测量条件测定标准溶液和质量控制样品,数据标准偏差较小,具有较高的精密度,对于准确测量水中汞元素浓度具有重要的意义。[align=center][b]参考文献[/b][/align] 魏艳红,郭建强,陈志明,等. 环境汞污染对人体健康的影响及预防措施. 大众科技,2014,3:59-61. 胡月红. 国内外汞污染分布状况研究综述. 环境保护科学,2008,34(1):38-41. 许研,陈永青,等. 我国环境汞污染现状及其对健康的危害. 职业与健康,2012,28(7):879-881. GB8978-1996,污水综合排放标准[s]. GB/T 14848-2017,地下水质量标准[s]. 于莉,陈纯,李贝,等. 总汞环境样品的前处理技术及分析方法研究进展. 中国环境监测,2014,30(1):129-137. 潘腊青,章维维,池怡,等. 原子荧光光度法测定地表水中的痕量汞. 分析仪器,2013,5:11-14. 朱茂森,冯吉平,李非. 氢化物发生—原子荧光光谱法测定水中痕量汞的实验研究. 东北水利水电,2015,3(3):1-3,64,71. 翟丽. 浅析原子荧光法测定水中汞. 2013,3:9-10,13. 张芳芝,嵇红军,常忠阳. AFS断续流动氢化物原子荧光光度计测定饮用水中汞. 北方环境,2013,29(2):134-137. 袁小燕,董雄伟,张勇. 原子荧光光度计测定水中汞的方法研究. 中国化工贸易,2013,(7):303-303. 刘景龙,罗守娟. 不同工作温度下原子荧光法测定水质中汞含量. 广州化学,2018,43(2):76-79. 兰岚. 原子荧光法测定地表水中汞的分析方法. 江西化工,2015,5:110-111. 胡刚,童诚,马文,等. 原子荧光使用中影响空白值的因素分析. 计测技术,2015,(z1). 纪久成,王德友. 原子荧光法测汞空白影响因素及解决办法. 东北水利水电,2013,31(8):59-60. HJ694-2014,水质 汞、砷、硒、铋和锑的测定 原子荧光法[s]. 臧慕文. 应重视数理统计方法在成分分析中的应用. 化学试剂,2012,34(7):577-580,584. 尚立成,李玲,张转赟,等. 浅析降低原子荧光空白值的方法. 甘肃科技,2012,28(17):56-57.[/s][/s][/s]
实验室检测水质叶绿素a的分析方法SL 88-1994,分光光度法。标准里没有说明叶绿素a的检出限,敢问此分析方法,叶绿素a的检出限。http://simg.instrument.com.cn/bbs/images/default/em09511.gif
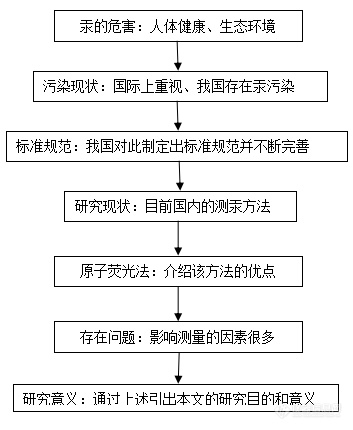
[align=center][b][/b][/align][align=center][b]以《原子荧光法测汞的试剂影响因素分析》为例,谈谈我的原创写作过程的经历[/b][/align][align=center][b][/b][/align][align=left][b]一、 背景概述:[/b][/align] 我国的原子荧光分析技术在老一辈科学家集体攻关下,经过四十多年的发展,目前在国际上处于领先地位,在环境监测、食品检验、农产品检验等领域应用很广。对于检测者来说,除了了解仪器类型、工作原理、构造组成外,更多关注操作步骤、参数优化、保养维护、问题解决等方面。原子荧光的操作步骤很简单,按照说明书操作就可以了;参数设置一般是厂家工程师在安装仪器时预先设定好的;保养维护方面,只要保养得好,仪器寿命就得到延长。在检测过程中,总会出现大大小小的问题。这些问题的解决,有时候相当费时费力,对检测者来说,简直是一种折磨。不过,“多年媳妇熬成婆”,干那么几年,遇到的问题基本都解决了,无论是仪器操作还是查找问题都会得心应手。要使仪器能准确测量水、气、土等样品,就需要关注下影响因素,调整仪器使之达到最佳状态。[b]二、影响因素:[/b] 影响原子荧光法测量的因素很多,总的来说,基本分成四大类:1. 环境条件:实验室温度、湿度、光照;2. 仪器参数:预热时间、负高压、灯电流、原子化器高度等;3. 试剂因素:包括实验用水、试剂纯度、硼氢化钾浓度、盐酸浓度等;4. 其他因素:包括仪器管路污染、器皿污染等等。 在做实验过程中,我遇到过各种问题,除了仪器硬件故障外,其他的问题都是细节方面的,比如仪器的记忆效应,反复清洗后才恢复原先水平;器皿受到污染,清洗效果不好,只能更换一批器皿;空白偏高,后来发现是盐酸问题,更换厂家的盐酸后空白才降低,等等。环境行业标准中,一般按照《水质 汞、砷、硒、铋和锑的测定 原子荧光法(HJ694-2014)》来测量天然水和污废水。标准中对硼氢化钾做出了规定,汞是10g/L,砷硒铋锑是20g/L,并要求是用的时候配,不用的时候不配,时效性很强。每次做完样品后,总会有剩余的硼氢化钾溶液,这就不可避免造成浪费,甚至额外的污染。在国内对硼氢化钾,还有盐酸浓度的研究论文很多。借着参加原创大赛的机会,我读了一些论文,并对测汞方面的试剂(硼氢化钾浓度和盐酸浓度)影响因素做了一些研究分析。 如果仅仅按照其他人的研究内容来设计实验,很容易落入窠臼,没有创新可言。每篇论文或多或少有局限性,比如对某一内容未开展讨论或者挖掘不够深入,数据统计分析不能有效支撑结论等。如果多数研究都没有对这个论述开展讨论,那么这个很可能是个创新点。[b]三、写作过程:[/b]1. 搜索文献。在知网、万方、百度等网站通过关键词搜索文献;2. 浏览文献。先大致浏览文献,有个整体框架,然后找出其中几篇最有用的论文细读;3. 设计实验。按照实验方案做实验,得出数据。4. 处理数据。可以用Excel、SPSS、Origin等数据处理软件对数据进行统计分析。5. 写作。围绕统计结果由点到面分析阐述。6. 修改。修改过程不比写论文轻松,毕竟是初稿,有些想法没有在文章里充分体现出来,这就需要反复修改,不断完善。注重文章的逻辑性。[b]四、内容概要:1. 前言[/b][align=center][b][img=,353,430]http://ng1.17img.cn/bbsfiles/images/2018/08/201808011738454408_5769_2116599_3.png!w353x430.jpg[/img][/b][/align][align=left][b]2. 实验方法[/b][/align][align=left] 内容包括仪器的工作原理、仪器参数设置、试剂以及实验步骤。为避免打广告嫌疑,我隐去文章中厂家的仪器类型信息。[/align][align=left][b]3. 结果与讨论[/b][/align][align=left]1)硼氢化钾浓度对曲线斜率的影响。这部分文章很多,但没有给出反应公式,也没有对反应过程进行深入论述,我参考了仪器厂家说明书和化学方面的资料,确定了反应式。围绕反应式,从原理方面讨论硼氢化钾过低或过高都会有影响。再应用数理统计方法,分析硼氢化钾的浓度对曲线斜率的影响。从标准偏差和离散系数确定最佳浓度。[/align][align=left]2)硼氢化钾和盐酸浓度对空白的影响。其他研究者都是把硼氢化钾和盐酸的浓度分开讨论的,本实验把这两种试剂结合起来,分析对空白的共同影响。[/align][align=left]3)在优化的实验条件下,对标准溶液和质控样品进行了测试,结果很满意。[/align][align=left][b]五、不足之处[/b][/align][align=left] 这篇文章写完后,也有一些不足之处。国标方法(HJ694-2014)中规定了地表水、地下水、生活污水和工业废水的检测方法。本文仅针对地表水、地下水的天然痕量汞进行了分析,没有对生活污水和工业废水等可能存在高浓度汞进行分析。含高浓度汞的水样应使用多大浓度的硼氢化钾和盐酸,本论文没有进行分析。如果以后有时间和精力,也对这方面开展分析研究。此外,也有一些方向可供研究:[/align][align=left]一是对其他元素,包括砷、硒等元素的硼氢化钾浓度和盐酸浓度展开分析。[/align][align=left]二是对盐酸和硝酸的比较,对于盐酸和硝酸,有人认为硝酸存在强氧化性,会把硼氢化钾氧化,降低了硼氢化钾的还原性,影响了测量效果。这方面也可以进行分析。三是干扰分析。原子荧光存在一些干扰,包括光谱干扰、重金属干扰和物理干扰。这些有什么样的干扰,程度有多大,也可以研究。[/align][align=left] 文章的内容详见另一篇帖子,欢迎各位版友进行批评指正。[/align][align=left][b]最后,感谢仪器信息网版主李经理、大耳朵的耐心解答和热情帮助。也希望与各位版友互相交流、共同提高。[/b][/align][b][/b]
不好意思了,没找到分子荧光区只好来这里求问了,用分子荧光光度计测叶绿素a,那个比色皿用蒸馏水洗洗不干净,壁面有白白的一层附在上面,想请教下这种比色皿测完样品后怎么清洗?如果需要浸泡什么的话,是用?%的盐酸、?%的酒精还是什么?不胜感激,谢谢
各位老师,我想寻找一种检测叶绿素a、叶绿素b和叶绿素铜钠的含量,目前使用紫外-可见光分光光度计,采用的是标准曲线法,但是非常麻烦;希望能够找到更简便快捷的测量方法或者仪器,精确度要求99.99%。请各位老师指点!!
[size=16px] 叶绿素测定仪是一种用于测量植物叶片中叶绿素含量的设备。叶绿素是植物中进行光合作用的关键色素,它们吸收光能并将其转化为化学能以支持植物的生长和发展。以下是一般情况下使用叶绿素测定仪测量植物叶绿素相对含量的步骤: 样本准备: 从要测量的植物中选取代表性的叶片样本。这些叶片应该是健康的、没有损伤的,并且尽可能避免太老或太嫩的叶片。 叶片处理: 如果需要,将叶片处理成较小的块状或碎片,以确保测量时样本的均匀性。同时,避免过度损伤叶片,因为这可能会影响叶绿素的测量结果。 提取叶绿素: 使用适当的提取液(比如乙醇、乙醚等)将叶片中的叶绿素提取出来。提取的过程通常需要在低温下进行,以防止叶绿素的降解。 测量光吸收: 将提取液中的叶绿素溶液置于叶绿素测定仪中。这种仪器通过照射样本并测量样本对不同波长光的吸收来确定叶绿素的含量。最常见的方法是使用分光光度计,它可以测量不同波长下样本吸收的光强度。 建立标准曲线: 使用已知浓度的叶绿素标准溶液,进行一系列测量以建立标准曲线。标准曲线可以用来将样本吸收的光强度值转换为叶绿素浓度值。 测量样本: 使用同样的方法测量你的样本,获取其吸收的光强度值。 计算叶绿素含量: 根据标准曲线,将样本的光吸收值转化为叶绿素浓度。如果你感兴趣的是叶绿素的相对含量,可以将不同样本的叶绿素浓度与标准样本进行比较。 请注意,使用叶绿素测定仪需要一定的实验操作技能和基本的化学常识。在操作之前,云唐建议仔细阅读仪器的操作手册,并根据实际情况调整实验步骤。另外,确保在实验过程中遵循安全操作规范,使用适当的防护措施。[/size]
[size=16px] 叶绿素测定仪通常用于测量植物叶片中的叶绿素含量,而不是直接测量氮含量。然而,叶绿素含量与植物的氮素含量之间存在一定的关联,因为氮是叶绿素分子中的一个重要组成部分。叶绿素测定可以作为一种间接方法来估计植物的氮含量。 要测量植物的氮含量,通常可以使用以下方法之一: Kjeldahl法:这是一种传统的分析方法,可以测量有机物中的氮含量。样品首先被消化,然后氮被转化为氨,并通过滴定酸来测量氨的含量,从而计算样品中的氮含量。 Dumas法:这是一种更现代的方法,类似于Kjeldahl法,但使用燃烧而不是消化来将样品中的有机氮转化为氨。然后通过化学反应测量氨的含量,从而计算氮含量。 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法:这是一种通过[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]来分析样品中的氮化合物的方法。样品在高温条件下分解产生氮气,然后氮气被送入[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]进行分析。 光谱法:虽然叶绿素测定仪主要用于叶绿素含量测量,但某些光谱数据也可以用于估计氮含量。光谱数据中的某些特征可以与氮含量之间存在的关联进行校准,从而进行估算。 请注意,这些方法可能需要特定的实验室设备和技术,并且样品的处理和分析可能会有一定的复杂性。云唐建议选择合适的方法取决于你的实验目的、设备可用性以及实验室的专业知识。如果你不熟悉这些分析方法,最好是在有经验的人的指导下进行实验。[/size]
[size=16px] 叶绿素测定仪是一种用于测量植物叶片中叶绿素含量的设备。它在植物生理学、生态学和农业研究中非常有用。然而,是否认为叶绿素测定仪好用取决于具体的使用情境和需求。 以下是一些使用叶绿素测定仪的优点和考虑因素: 优点: 快速准确: 叶绿素测定仪能够快速测量叶片中的叶绿素含量,提供准确的结果,节省时间和人力成本。 非破坏性: 使用叶绿素测定仪通常不需要摘取植物叶片,因此不会对植物造成破坏,可以进行长期监测。 数据量大: 叶绿素测定仪能够高通量地收集数据,适用于大规模实验和研究。 定量分析: 通过叶绿素测定仪,您可以获取叶绿素含量的定量数据,有助于更深入地理解植物生长和环境因素之间的关系。 考虑因素: 成本: 叶绿素测定仪可能需要较高的投资成本,包括设备购买和维护费用。 操作复杂性: 操作叶绿素测定仪可能需要一定的技术培训,特别是对于没有相关经验的人员。 适用范围: 叶绿素测定仪主要用于叶绿素含量的测量,如果您需要其他植物参数的数据,可能需要其他类型的设备或方法。 样本处理: 样本的准备和处理可能会影响测量结果的准确性,需要注意标准化的操作步骤。 综合考虑以上因素,如果您在植物研究、农业实验或环境监测等领域需要准确测量叶绿素含量,叶绿素测定仪可能会非常有用。然而,在购买之前,云唐建议您仔细评估您的研究需求、预算以及操作和维护的可行性。[/size]

今天有个兄弟问了一下一台仪表是不是能测量总硫的事情,反正今天不是很忙,就把关于硫分析的仪表给整理了一下,不过大多数东西大家可能都知道。我说的东西基本都是用我的理解和我的语言来说明的,鉴于我的表达能力比较低,所以可能出现不少错误,大家也多多指正,见谅....硫分析仪是一个总称,对于我们搞在线的常见的有三种 1.硫化氢分析仪 2.比值分析仪(硫化氢/二氧化硫) 3.总硫分析仪一个一个说:1.硫化氢分析仪:分析方法我见过的有 1.醋酸铅纸带法 2.紫外吸收法 3.色谱法 4.电化学法醋酸铅纸带法 大概原理说下,硫化氢跟醋酸铅反应变成硫化铅,这玩意会在纸带上产生个褐色的斑点,然后用光来测这个斑点形成的反应速率,因为样品的流量是一定的,所以就能靠反应速率知道硫化氢浓度了。 不过这玩意得换纸带和醋酸铅,并且醋酸铅还有毒,这表测量微量的硫化氢很不错,常量的就不行了,记得好像得用什么东西稀释样品。紫外吸收法:硫化氢对紫外光谱的某一波段吸收很大,特定浓度的硫化氢在特定波段的吸收量是一定的,然后根据不同波段的全程光谱来计算硫化氢含量,这是我的理解,至少我接触的AAI的OMA300是这样的。色谱法:常量用TCD (热导检测器)微量用FPD(火焰光度检测器),有些色谱厂商说TCD 测硫化氢能到50ppm以下,不知道是否可行。电化学法:这玩意好像只用在硫化氢气体检测器上,一些炼油厂化工厂到处都是,尤其是硫磺装置。在线仪表好像没有,便宜,精度不高,时间长了失效,在高浓度环境下也很快就失效了。2.比值分析仪,就是硫化氢和二氧化硫的比,我见到的都用在硫磺回收上,即克劳斯硫磺回收技术。 我就见过 紫外吸收法和色谱法两种。 紫外法:原理跟上面的那个是一样的,因为二氧化硫对紫外光也有吸收。详细的就不说了,再说就涉及的多了,羟基硫硫蒸气都出来, 实在是懒得打字,以后有机会再说。 色谱法:跟上面硫化氢的差不多,只不过多了个SO2罢了,但是硫磺回收的工况实在是太恶劣了,用色谱的话对 取样和预处理系统的要求太苛刻了,经常出问题,不是这堵就是那堵的,今天阀堵了 明天进样管堵了,太折腾人了。3.总硫分析仪:测液体或者气体中无机硫和有机硫的总量得。我见过醋酸铅纸带法,紫外荧光法 、X射线法。 醋酸铅纸带法跟硫化氢的一样,只不过多了个反应炉,把乱七八糟的都整成硫化氢,然后测量。紫外荧光法,这个是荧光,上面的吸收,都是紫外,但不一样的。 这个稍微有点乱,样品进入一个富氧环境下裂解生成SO2、CO2、H2O 啥的一堆东西,然后把不要的统统搞掉,就剩SO2了。然后SO2被紫外光照射变成了激发态的SO2,这玩意不稳定,一会就衰变了,就在这衰变的过程中释放了点特定波长的荧光,好了,测这荧光就OK了。 X射线我只是见过仪表,原理大概看了下,不过这玩意好像欧盟已经不用了?因为有辐射?反正我是不准备搞这个表了,原理涉及到中子啥的,太复杂了,懒得打字了。 乱七八糟掰乎了一大堆,有错误请大家指正,共同进步....谢谢。。-----------------------------------------------------------------------------------------------------------------------------------------------------------------------------------http://ng1.17img.cn/bbsfiles/images/2011/03/201103012126_280209_2159354_3.jpg这个是加拿大的 Galvanic的总硫 下面圆柱是反应炉,如果光测硫化氢的话就没这个圆桶桶子,中间是表,上面黑色的是装醋酸铅溶液,纸带啥的。一顿翻 就找到这么一张例图,其它的找不到了,不知道哪去了,找到了再给大家看。睡觉,明天出差....