三乙胺在液相色谱流动相中有什么作用?
三乙胺在液相色谱中流动相中有什么作用?
三乙胺在液相色谱流动相中有什么作用?
三乙胺在液相色谱流动相中有什么作用?
三乙胺在液相色谱流动相中有什么作用?
三乙胺在液相色谱流动相中有什么作用?
昨天做样,峰拖尾狠严重。同事建议加点三乙胺改善一下峰型。于是在水相中添加了少许三乙胺(分析纯),重新过滤、超声,然后准备做样。可是基线一直呈锯齿状上下波动,柱压也较未加三乙胺前有所升高。冲了好长时间柱子,仪器状态一直未改善。这是因为什么原因引起的啊?我们用的流动相是:90%甲醇和10%水。大家平时加三乙胺做扫尾剂时都是怎么处理的啊?是否必须用色谱纯的三乙胺?欢迎大家帮忙解答和集体讨论~~~[em09512]
[color=#444444]最近做一个中间体的分离,但液相色谱峰宽,是碱性物质,除了加三乙胺还有什么方法?[/color]
在液相分析中,有时会用到三乙胺的,看到资料说三乙胺对色谱柱的影响是不可逆的,但有些说是好好冲洗对柱子影响不是很大的,到底怎么样呢?大家用的话,一般的加入量是多少呢,用完后又是怎么冲洗的呢?
各位前辈,小弟想问一下乙二醇甲醚和三乙胺能用液相色谱分析吗,如果能流动相是什么啊?条件呢?我们的液相是带紫外的检测器。谢谢
通常液相色谱分析中,在流动相中加乙酸和三乙胺,大家来谈谈,在什么情况下需要加乙酸,什么情况下加三乙胺,加多少是怎么控制的?
在用液相色谱分析某些酸性药品时,有的时候会在流动相中加入三氟乙酸,加入三氟乙酸的目的是什么啊?有时候还会在流动相中加入二乙胺,目的是什么啊?仅仅是要调节pH值么?还有就是,二乙胺可以用三乙胺代替么?哪位高手给解答一下啊,具体点的。
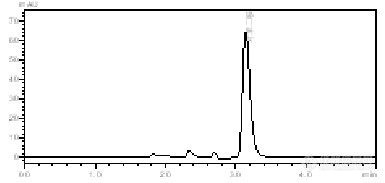
染发剂中对苯二胺等染料的HPLC测定方法采用《化妆品卫生规范》所规定的液相色谱标准检测方法,对氧化型染发剂中包括对苯二胺和邻苯二胺在内的八种染料进行检测。[size=4][b]分析方法[/b]色谱柱:Shimadzu Shim-pack VP-ODS 4.6×150mm 5μm检测波长:280nm 流动相:乙腈:(水:三乙醇胺=98:1)=5:95 流速:1mL/min 柱温:室温进样量:10μL洗脱方式:等度洗脱。[/size][size=4]流动相中使用了三乙醇胺,比较少见,它在分析苯胺类化合物有什么突出的优点吗?可否用三乙胺替代?[/size][img]http://ng1.17img.cn/bbsfiles/images/2010/05/201005082043_217200_1638724_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2010/05/201005090755_217230_1638724_3.jpg[/img]
对苯二胺硫酸盐、间苯二胺硫酸盐、邻苯二胺硫酸盐,用液相色谱C18柱能用吗?应配怎样的流动相? 它们的稀水溶液PH值在2-3左右。我用硫酸调流动相PH到2左右出两个峰。 又用三乙胺调PH到7多点还是两个
SN/T 3538-2013 出口食品中六种合成甜味剂的检测方法 液相色谱-质谱/质谱法本标准规定了出口食品中甜蜜素、糖精钠、安塞蜜、阿斯巴甜、阿力甜、纽甜6种人工合成甜味剂检测的液相色谱-质谱/质谱测定和确证方法。本标准适用于奶粉、液态奶、酸奶、奶油、奶酪、冰激凌、红酒、果汁、糕点、蜜饯、甜酸藠头中甜蜜素、糖精钠、安赛蜜、阿斯巴甜、阿力甜、纽甜的测定。[size=16px][color=#ff6666][b]问题:我想用来检测酸奶中的甜味剂,不明白 提取液为什么是甲酸-三乙胺(PH4.5)溶液,加入蛋白沉淀剂后,再加入5ml三氯甲烷的作用是什么?[/b][/color][/size][size=16px][color=#ff6666][b]HLB净化,用的是它的哪个基团或者哪方面的效应?[/b][/color][/size]
我现在测生物碱(吗啡)的含量,分离度可以了但老是拖尾,三乙胺的量都加到0.1%了,还能不能再增加了?再增加有效果吗?三乙胺肯定能消除拖尾现象吗?各位有做过生物碱的吗?传授一下经验咯。我实在是着急呀,各位大侠帮帮忙呀,盼望中…………
请问一下,有没有办法用液相法来检三乙胺和异丙胺,或者在哪里看到过这方面的资料,谢谢。
请问如何用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定三乙胺的含量。
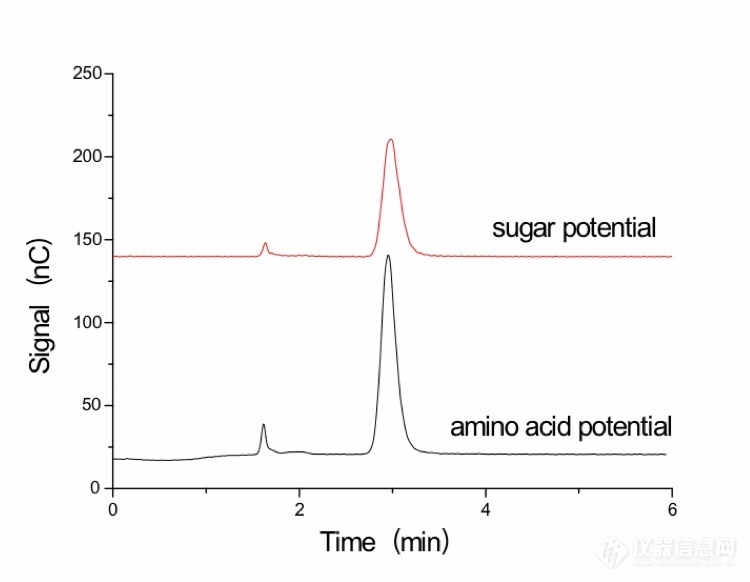
[align=center][b][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱后补液-积分脉冲安培法检测阿立哌唑中残留三乙胺[/b][/align][b]摘要[/b]目的:建立测定阿立哌唑原料药中三乙胺残留量的新方法。方法:采用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱后补液-积分脉冲安培法。采用阳离子交换柱,以30 mmol/L甲烷磺酸为淋洗液,流速1.0 mL/min;柱后补液为500 mmol/L NaOH溶液,流速0.2 mL/min;波形为氨基酸电位。结果:三乙胺在0.1322-1.322 mg/L范围内线性关系良好(R[sup]2[/sup]=0.9994),加标回收率在101.7%~105.9%之间,RSD为1.85%(n=6)。结论:建立的方法准确、可靠、灵敏度高,适用于测定阿立哌唑原料药中三乙胺的残留量分析。[b]关键词[/b][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url];积分脉冲安培;阿立哌唑;三乙胺阿立哌唑(aripiprazole),化学名为7-{4--丁氧基}-3,4-二氢-2(1H)喹啉酮,是日本Otsuka公司开发的新型非典型抗精神病药,临床主治各种急、慢性精神分裂症和情感障碍[sup][/sup]。阿立哌唑的合成路线较多[sup][/sup],在合成过程中曾用到三乙胺,因此产品中有可能会残留微量的基因毒性杂质三乙胺,由于三乙胺具有助溶和轻度的防腐作用,因此对三乙胺残留量的监测是阿立哌唑药物质量控制过程中必不可少的一部分。目前三乙胺已收载于人用药品注册技术要求国际协调会(ICH),Q3C(R6)中[sup][/sup],规定其限度为500mg/Kg,欧洲药品质量管理局(EDQM)也规定其残留限度为320mg/Kg。通常,三乙胺采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[sup][/sup]和溴酚蓝分光光度法[sup][/sup]进行测定。有不少人采用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]检测乙醇胺、二甲胺等胺类[sup][/sup],但用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]测定三乙胺很少见。李向春[sup][/sup]等采用Dionex IonPac CS17色谱柱,MSA 6mM等度淋洗,采用CSR循环再生电抑制模式测定了草甘膦合成工艺中的三乙胺。上述方法中检出限最低的为[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法,可达约48 mg/kg。但阿立哌唑中残留的三乙胺含量很低,采用上述方法灵敏度不够,且阿立哌唑中主体干扰较大,无法满足要求。潘思[sup][/sup]等采用柱后衍生[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]-脉冲安培法来测定盐酸羟胺,采用Dionex IonPac CS16 (4×250 mm)色谱柱,流动相是30 mmol/L甲磺酸溶液,流速为1.0 ml/min;衍生剂为500 mmol/L氢氧化钠,流速为0.3 ml/min,该方法检测限为0.012 mgL[sup]-1[/sup],定量限为0.037 mgL[sup]-1[/sup]。因此本文借鉴该方法来测定三乙胺的含量,并对淋洗液浓度及流速、柱后补液的浓度及流速、电位波形进行优化,通过考察其线性关系、精密度、稳定性来验证方法的可行性。[b]1实验部分1.1 仪器与试剂[/b]Thermo ICS5000+ 型[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url],包括单元四元梯度泵,AS-AP自动进样器,DC模块含安培检测器,Chromeleon 6.80色谱工作站;色谱柱为Dionex IonPac CS17 (4×250 mm),保护柱为Dionex IonPac CG17(4×50 mm); Mettler Toledo AL204型电子分析天平;Millipore-Q Advantage A10型超纯水机。三乙胺(99.5%),盘锦研峰科技有限公司;甲烷磺酸(99.5%),阿拉丁试剂有限公司;50% NaOH(w/w),分析纯,德国Merck公司; OnGuard[sup]TM [/sup]RP柱(1 cc),美国Thermo公司;阿立哌唑供试品(1[sup]#[/sup],2[sup]#[/sup],3[sup]#[/sup]),某药厂提供。[b]1.2 溶液的配制[/b]1.2.1 三乙胺标准溶液的配制精确称取66.1 mg三乙胺标准品于50 mL容量瓶中,用30 mmol/L MSA淋洗液溶解定容,配制得到132 2 mg/L标准储备液,稀释得到26.44 mg/L的标准溶液。再逐级用淋洗液稀释得到浓度分别为1.322 mg/L、0.661 0 mg/L、0.440 7 mg/L、0.264 4 mg/L、0.132 2 mg/L的三乙胺系列储备液。1.2.2 甲烷磺酸淋洗液溶液的配制称取19.28 g 甲烷磺酸于2.0 L PP淋洗液瓶中,加超纯水到2000 mL,摇匀,所得溶液的浓度约为100 mmol/L。1.2.3 NaOH溶液的配制称取81.09 g 50%NaOH(w/w)于2.0 L PP淋洗液瓶中,加超纯水到2000 mL,摇匀,所得溶液的浓度约为500 mmol/L。1.2.4 实际样品溶液的配制称取50.1 mg 阿立哌唑供试品于25 mL容量瓶中,准确加入10 mL乙腈,置于50℃水浴中溶解,摇匀,随后准确加入10 mL超纯水,置于冰箱中冷藏60分钟后取出,阿立哌唑会以沉淀形式析出。静置后离心,取上清液用经活化的RP柱(活化方式:先用5 mL甲醇对RP柱进行冲洗,放置30 min后,用10 mL超纯水进行冲洗,备用)进行过滤,先丢弃最初的3 mL,取滤液即得浓度约为2500 mg/L的供试品溶液。[b]1.3 色谱条件[/b]淋洗液:A 超纯水(70%),B 100 mmol/L甲烷磺酸(30%),流速为1.0 mL/min,等度淋洗;柱后补液:500 mmol/L NaOH溶液,流速为0.2 mL/min;波形:氨基酸电位;进样量:25 μL;柱后衍生管:375μL。[b]2 结果与讨论2.1 色谱条件的确定[/b]2.1.1 淋洗液浓度的选择实验选取20 mmol/L、25 mmol/L、30 mmol/L的甲烷磺酸溶液作为淋洗液分别测定1.322 mg/L的三乙胺标样,检测结果显示其保留时间分别为3.567min、3.189min、2.953min,峰高分别为47.31 nC、103.7 nC、119.8 nC。表明30 mmol/L的淋洗液灵敏度最高,且保留时间适宜。若使用更高浓度的甲烷磺酸溶液作为淋洗液,则三乙胺的保留时间会更短,但可能存在与其他快出峰杂质分离度变差,影响定量。因此选取30 mmol/L的甲烷磺酸溶液作为实验的淋洗液。2.1.2 检测电位的选择伯胺的有机化合物,在碱性条件下,用金电极采用糖电位和氨基酸电位都有较高的响应。糖电位为脉冲安培检测,氨基酸电位为积分安培检测,脉冲安培检测在一个脉冲周期中对电流积分所施加的电位是单一的,它存在一个短暂的间歇以使充电电流衰减,而积分安培对工作电极施加的是一种对应时间波形的循环电位,即电极先被氧化然后再被还原为其原始状态。因此,在CS17柱分离后,用NaOH补液调节pH到碱性。选取糖电位和氨基酸电位这两种波形分别测定1.322 mg/L的三乙胺标样,结果如图1。从图1可以看出,二者的噪音差别不大,且氨基酸电位波形的响应值高,因此选取氨基酸电位波形作为实验的波形。[align=center][img=,690,535]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312150078580_1354_3426139_3.jpg!w690x535.jpg[/img][/align][align=center][b]图1 电位波形的影响[/b][/align][align=center]Fig.1 Effect of potential waveform[/align]2.1.3 柱后补液流速的选择实验选取氨基酸电位波形的柱后补碱NaOH溶液的0.2 mL/min、0.3 mL/min流速分别测定1.322 mg/L的三乙胺标样,结果如图2。从图2可以看出,氨基酸电位波形时,0.2 mL/min柱后补碱NaOH溶液的响应值高于0.3 mL/min柱后补碱NaOH溶液。若柱后补液流速到0.1ml/min,由于淋洗液为酸,补液为强碱,过低的补液流速和淋洗液的混合效果不好,且流量精度会降低,导致噪音变大。因此实验选择柱后补碱NaOH溶液流速为0.2 mL/min。[align=center][img=,690,531]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312150354680_6766_3426139_3.jpg!w690x531.jpg[/img][/align][align=center][b]图2 柱后补液流速的影响[/b][/align][align=center]Fig.2 Effect of post-column rehydration flow rate[/align][b]2.2 方法学验证[/b]2.2.1 线性关系、检出限和定量限本实验考察0.132 2-1.322 mg/L 范围内三乙胺的线性关系。待仪器稳定后,将配制的标准系列溶液由低浓度到高浓度顺序依次进样,平行测定三次,计算峰面积并取平均值。结果表明,三乙胺的线性关系良好,回归方程为y=1.076x+0.344 5,R2为0.999 4。三乙胺检测方法的检出限浓度为0.045 mg/L,相当于样品检出限含量为18.2 mg/kg,定量限浓度为0.15 mg/L,相当于样品的定量限含量为60.7 mg/kg。2.2.2 标准溶液进样重复性取三乙胺测定线性关系中浓度为0.661 0 mg/L的标准溶液作为进样重复性溶液,连续测定6次,记录峰面积。结果显示测得三乙胺峰面积的RSD为1.9 %(n=6),说明该分析方法较稳定,具有较好的进样重复性。2.2.3 实际样品分析取三批供试品,配制好实际样品溶液(约2500 mg/L),按上述色谱条件,对实际阿立哌唑样品进行检测,色谱图见图3。从图3中可以看出,阿立哌唑供试品中未检测到三乙胺毒性杂质,小于18.2 mg/kg。[align=center][img=,690,478]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312150529972_3514_3426139_3.jpg!w690x478.jpg[/img][/align][align=center][b]图3 实际样品色谱图[/b][/align][align=center]Fig.3 Chromatogram of the actual sample[/align]2.2.4 加标回收实验对供试品1[sup]#[/sup]中成分三乙胺进行回收率实验。精密量取2.5 mL浓度为2500 mg/L的实际样品溶液分别置于5 mL容量瓶中,分别精密加入2.5 mL浓度为1.322 mg/L、0.661 0 mg/L、0.440 7 mg/L的对照品储备液,混合均匀。在上述色谱条件下进样测定,每个浓度平行测定三次,回收率结果见表1。从表1中可以看出,样品不同水平加标回收率在101.7%~105.9%之间,说明该检测方法可信度较高。[align=center][b]表1 样品加标回收率[/b][/align][align=center]Table 1 Results ofrecovery tests for sample[/align] [table=657][tr][td] [align=center]化合物[/align] [align=center](compound)[/align] [/td][td] [align=center]样品含量[/align] [align=center](sample amount)/( mg/L)[/align] [/td][td] [align=center]加标量[/align] [align=center](addition)/( mg/L)[/align] [/td][td] [align=center]检测量[/align] [align=center](measured amount)/( mg/L)[/align] [/td][td] [align=center]回收率[/align] [align=center](recovery)/%[/align] [/td][/tr][tr][td=1,3] [align=center]三乙胺(Triethylamine)[/align] [/td][td] [align=center]-[/align] [/td][td] [align=center]0.066 1[/align] [/td][td] [align=center]0.070 0[/align] [/td][td] [align=center]105.9[/align] [/td][/tr][tr][td] [align=center]-[/align] [/td][td] [align=center]0.132 2[/align] [/td][td] [align=center]0.134 4[/align] [/td][td] [align=center]101.7[/align] [/td][/tr][tr][td] [align=center]-[/align] [/td][td] [align=center]0.220 4[/align] [/td][td] [align=center]0.232 4[/align] [/td][td] [align=center]105.4[/align] [/td][/tr][/table][align=center][/align][b]3 结论[/b]上述实验结果表明,采用[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱后补液-安培法,在30 mmol/L的甲烷磺酸溶液淋洗液,流速为1 mL/min,柱后补碱为500 mmol/L的NaOH溶液,流速为0.2 mL/min,氨基酸电位波形的色谱条件下,能准确地分析阿立哌唑中基因毒性杂质三乙胺的残留量,最低检出限为18.2 mg/kg,灵敏度高,满足药典的要求,该方法准确度、精密度和稳定性较好。在阿立哌唑的质量控制中,该方法对三乙胺残留量的控制有重大意义。[b]参考文献:[/b] Zhang P, Li Z D, Jiao Z. Second generation atypical antipsychoticdrug aripiprazole. Chin Pharm J, 2005, 40(3): 238-240.张璞,李中东,焦正.第二代非典型抗精神病药一阿立哌唑. 中国新药杂志,2005,40(3):238-240. Wu C Y, Zhu Y C. Synthesis ofaripiprazole. Chin J Mod Drug Appl, 2010, 4(1): 11-12.吴春艳,朱永超. 阿立哌唑的合成 . 中国现代药物应用,2010,4(1):11-12. Li M D, Cai J, JiM. Synthesis of atypical antipsychotic new drug aripiprazole. Prog PharmSci, 2004, 28(6): 274-276.李铭东,蔡进,吉明. 非典型抗精神病新药阿立哌唑的合成.药学进展,2004,28(6):274-276. Liu X J, Wang T T,Zhong Y L, et al. Synthesis of antipsychotic aripiprazole. JShengyang Pharm Univ, 2013, 30(4): 253-255.刘秀杰,王媞媞,钟永亮,等. 抗精神病新药阿立哌唑的合成. 沈阳药科大学学报,2013,30(4):253-255. Xu J M, Wu Q Y,Zhang J, et al. Research on preparation of aripiprazole. J PharmPractice徐建明,吴秋业,张俊,等. 阿立哌唑的制备工艺研究. 药物实践杂志,2005,23(5):269-270. Ge H X, Wang L C,Ni S L. Improved Synthesis of Antipsychotic DrugAripiprazole. Chin JMAP, 2007, 24(4): 294-295.葛海霞,王礼琛,倪生良. 抗精神病药阿立哌唑的合成工艺改进. 中国现代应用药学,2007,24(4):294-295. Chen G Y, Chen X B,Liu G M, et al. Improved Synthesis of Aripiprazole. Shandong Chem Ind,2009, 38(9): 3-5.陈光勇,陈旭冰,刘光明,等. 阿立哌唑的合成工艺改进. 山东化工,2009,38(9):3-5. ICH guideline Q3C (R6 on impurities: guideline for residual solvents. (2016-12). Ma Z Q, Lu G H, YinJ J, et al. Determination of Residual Triethylamine in Rupatadine Fumarate byGas Chromatography. Guangdong Chem, 2018, 45(14): 213-214.马振千,鹿贵花,印嘉佳,等. [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定富马酸卢帕他定中三乙胺的含量. 广东化工,2018,45(14):213-214. Guo J T, Yu F.Determination of Triethylamine Residue in Tetraethyl Ammonium Bromide AqueousSolution by Capillary Gas Chromatography. Guangdong Chem, 2018, 45(14):213-214.郭建亭,于飞. 毛细管[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定四乙基溴化铵水溶液中三乙胺的残留. 化学世界,2017,12:727-729. Wu W P, Ming D.Determination of Triethylamine Residues in Raw Material of Mirtazapine by GasChromatography. Yunnan Chem Tech, 2018, 45(8): 130-131.伍蔚萍,明丹. [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定米氮平原料药中三乙胺残留量. 云南化工,2018,45(8):130-131. Jin Z Q.Discussion on problems of water Triethylamine determination. Tech Wind,2014, 23: 108.金梓谦. 分光光度法测定水中三乙胺有关问题探讨. 科技风,2014,23:108. Chen Z, Wang D,Zhang J N, et al. Optimization of Detection Technology for TriethylamineHydrochloride in Industrial Effluent. Salt Sci and Chem Ind J, 2019, 48(3):29-32.陈峥,王丹,张金娜,等. 工业废水中三乙胺盐酸盐检测技术的优化. 盐科学与化工,2019,48(3):29-32. Chen M S, Liang Z,Tang H Y, et al. Simultaneous determination of the migration of five alcoholamines in plastics food contact materials and articles by non-suppressed ion chromatography.AL, 2018, 37(10): 1183-1188.陈旻实,梁震,唐寰宇,等. 非抑制[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定塑料食品接触材料中五种醇胺迁移量. 分析试验室,2018,37(10):1183-1188. Fang L M, Hu M,Chen A L, et al. Determination of the residual dimethylamine in arbidolhydrochloride by ion chromatography. Chin J Pharm Anal, 2016,36(10):1852-1856.方琳美,胡咪,陈爱连,等. [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定盐酸阿比朵尔中残留的二甲胺含量. 药物分析杂志,2016,36(10):1852-1856. Li X C, Ding M M,Cai Q, et al. Determination of Triethylamine in Glyphosate Synthesis by IonChromatography. Qingdao: Proceedings of the 13th Ion Chromatography AcademicConference. 2010.李向春,丁敏敏,蔡琪,等. [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定草甘膦合成工艺中的三乙胺. 青岛:第13届[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]学术报告会论文集. 2010. Pan S, Shi C O,Liu Y M, et al. Determination of hydroxylamine hydrochloride in micafunginsodium by ion chromatography with pules amperometric detection. Anal Instru,2018(2): 58-61.潘思,施超欧,刘玉梅,等. [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱后补液-积分脉冲安培法检测米卡芬净钠中残留盐酸羟胺. 分析仪器,2018(2):58-61.
利用顶空-[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法测试三乙胺含量,感觉前后两针互相干扰,进完一针样品后,再进空白,会有三乙胺的峰,然后再进一次空白三乙胺的峰面积会减小,应该是三乙胺残留了,请问有什么办法让三乙胺不残留。
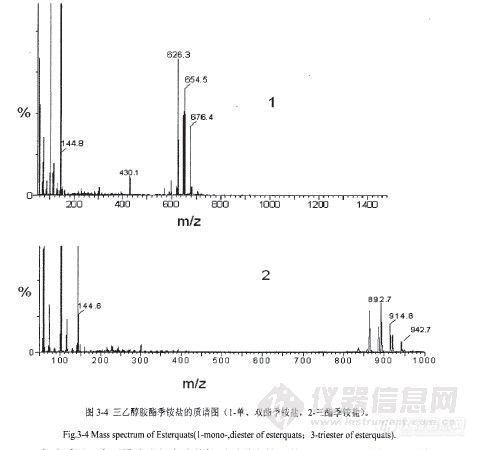
宫志鹏:建立了反相高效液相色谱法测定三乙醇胺酯中单、双、三酯含量的方法。采用Diamonsil C18色谱柱(250X4.6mm,5I,tm),柱温30。C,溶剂为氯仿,流动相为甲醇和氯仿,检测器为电雾式检测器。通过讨论k’值和兄与流动相极性、流速和柱温的关系,确定了梯度洗脱程序,30rain内三乙醇胺单、双、三酯得到了较好的分离。三乙醇胺单、双、三酯在20.500mg·L.1范围内线性关系良好,线性相关系数分别是0.9980、o.9991和0.9913,最低检出质量浓度分别(3s/N)是1.0mg·L~、1.5mg·L-1和1.5mg·L-1,相对标准偏差(n=6)分别是2.45%、1.81% 和1.98%。优化了反相高效液相色谱测定三乙醇胺酯季铵盐中单、双酯混合季铵盐与三酯季铵盐含量的方法。样品经过乙醚萃取处理,采用Inertsil CN.3色谱柱(250× 4.6ram,5Irtm),柱温50。C,溶剂为正丙醇,流动相为正丙醇和水,梯度洗脱, 检测器为电雾式检测器,并采用液相色谱.质谱法确证,15min内三乙醇胺单、双酯混合季铵盐与三酯季铵盐得到了较好的分离。单、双酯混合季铵盐与三酯季铵盐在25.750mg·L。1范围内线性关系良好,线性相关系数分别是O.9966和O.9913,检出F艮(3s/y)是0.8mg·LJ和10.0mg·L一,相对标准偏差(n=6)分别是0.5 l%和12.38%。:三乙醇胺酯,三乙醇胺酯季铵盐,梯度洗脱,高效液相色谱,电雾式检测器Abstract :An analytical method of reversed phase hi曲performance liquid chromatography(RP-HPLC)was developed for determination of triethanolamine mono-,di—and triesters.Established a gradient elution programme by analyzing the relationship of k’,R and elution rate,elution polarity,temperature. Triethanolamine mono-,di-and triesters were detected and separated successfully by Diamonsil Cls column(250x4.6mm,59m)and column temperature of 30"C,with chloroform as solvent and methanol-chloroform as the mobile phase in gradient elution and with a Charged aerosol deteror.The linear ranges of triethanolamine mono一,di-and triesters were 20-500 mg‘L。(r=O.9980),20-500 mg·L。1(r=0.9991)and 20—500mg‘L_(r=0.9913)respectively.The measurable lowest limits were 1.0rag‘L一, 1.5mg’L—and 1.5mg‘L—and the RSDs were 2.45%.1.8 1%and 1.98%respectively. An analytical method of reversed phase hi曲performance liquid chromatography(RP—HPLC)was optimized for determination of triesterquats in 1 5min.Mono-,diesterquats mixture and triesterquats were detected and separated ccessfully by Inertsil CN一3 column(250x4.6mm,5pm)and column temperature of 30。C.with n—propanol as solvent and n—propanol—water as the mobile phase in gradient elution and with a charged aerosol deteror.The linear ranges of mono一, diesterquats mixture and triesterquats were 25-750mg·L-1(FO.9966) and 25-750mg’L叫(r=0.9913)respectively.The measurable lowest limits were 0.8mg‘L。1 and 10.0mg。L-1 and theRSDs were 0.51%and 12.38%respectively. Key words:triethanolamine esters,esterquats,gradient elution,high performance liquid chromatograph,charged alesol detectionhttp://ng1.17img.cn/bbsfiles/images/2012/08/201208131731_383588_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208131732_383589_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208131732_383590_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208131732_383591_2352694_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208131732_383592_2352694_3.jpg
最近需要检测酯类物质,其中含有1-4PPm的三乙胺,每次检测,都是同一个样品三乙胺含量忽高忽低,有时能达到几十PPm,我的仪器条件是福立9790二型,柱温起始80,保持2分钟,然后20度/min至200,检测器250,进样口230,样品4各组分,乙醇,苯,三乙胺,酯类,色谱柱是DB-5,想请大侠帮帮忙,有什么好办法没有?是三乙胺这种物质在色谱中残留呢,还是气化不好?
各位大神,峰拖尾,领导说加入三乙胺,她也不说怎么加,我甲醇:水=40:60的流动相应该加入多少三乙胺?
你好,我们新购C18柱,在做苦参素液相条件时用的流动相为:乙腈:水:三乙胺:磷酸=8:92:0.25:0.25严重拖尾.用上述条件洗脱时,色谱柱柱效明显下降.我想问问:用什么方法能够恢复原状.
做肉中环丙沙星残留量的测定,国标方法中,流动相是这样配制的:0.05mol/L磷酸-三乙胺溶液:取浓磷酸3.4mL,用水稀释至1000mL。用三乙胺调pH至2.4。本人用的是85%磷酸(色谱纯),取了3.4mL,稀释至1000mL。搅匀后,测pH是3.6。这是不可能再往里面加三乙胺了,三乙胺是碱性的,越加pH只会越大。但这时我往溶液中起码再加入了十几毫升的磷酸,pH也才是3.0左右。我应该继续往溶液中加磷酸,直到pH=2.4吗? 这样流动相中磷酸是不是过多了?国标中这个溶液的配制方法是不是有问题呢?磷酸是中强酸,才取3.4mL配成1000mL,pH怎么可能低于2.4?这时如果还往里面加三乙胺,pH只会越来越大,永远也不可能调至2.4了。望大家帮我分析下,到底哪里出错了?感激不尽!
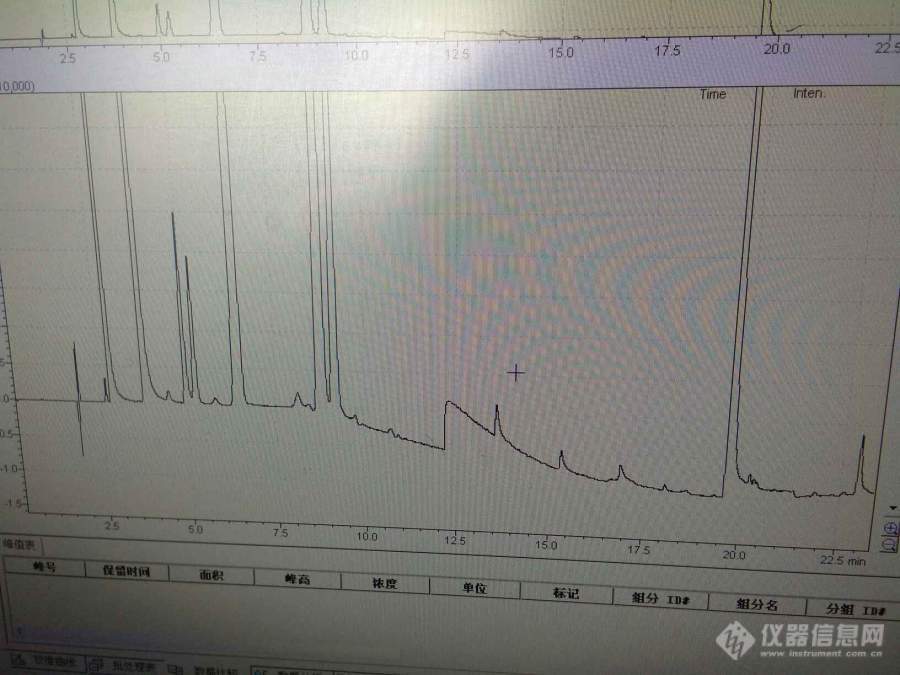
[color=#444444]我想请问一下,[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]中,顶空进样,溶剂为N-甲基吡咯烷酮,柱子DB-624,溶液里面成分有甲醇,乙醇,乙腈,二氯甲烷,正己烷,乙酸乙酯,四氢呋喃,三乙胺,吡啶,DMF,目前三乙胺峰判断不出来,也不确定到底有没有出来峰,图谱已传上,请教一下[/color][color=#444444][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2019/06/201906141009051727_9546_1752329_3.jpg!w690x517.jpg[/img][/color]

在RP液相色谱中,为了得到较好的峰形和分离度,会在流动相中加入适量的酸,碱和盐,由此也会引发各种各样的问题,再加上中药化药的分析方式的不同,现将个人实验经历及实际感触简要介绍如下(1)压力 当在流动相中加入分析纯的缓冲盐(如磷酸二氢钾)或其他酸(甲酸、磷酸)碱(三乙胺)后需要用滤膜过滤是众所周知的事情,而在使用缓冲盐的时候会有析出,在管路中析出表现为压力升高,在单向阀处则会出现压力大幅度波动,出现这类情况的主要原因还是缓冲盐遇到难溶有机溶剂所致。在反向色谱中,甲醇和乙腈为最常用的有机相,相比之下缓冲液在乙腈中更容易析出(如图,将20 ml ACN加入到30 mL 30 mmol的磷酸二氢钾中,侧面与顶端)。http://ng1.17img.cn/bbsfiles/images/2014/11/201411292249_525214_2421690_3.pnghttp://ng1.17img.cn/bbsfiles/images/2014/11/201411292250_525216_2421690_3.jpg 最近因为用40%的乙腈-60% KH2PO4废掉一个保护住,清洗两次仪器。 当方法中乙腈称为比用有机相时,为避免色谱柱中存在的大量有机相遇盐析出可先用适量比例的有机相-纯水饱和色谱柱,此外,若为梯度洗脱,则应该将有机相的初始比例尽量调低。(2)色谱柱的维护当流动相中含有缓冲液时,对于色谱柱的损害变强,为增加色谱柱的使用寿命,我们会选择使用保护住和预柱(附注:保护住和预柱的安装位置不同作用也不同,大家可以在液相版面去搜索,也可查阅附件),二者各有分工,保护住确实可以有效地解决绝大部分进入色谱柱前的杂质,甚至饱和流动相(本为保护住的功能),若是将保护柱作为预柱使用,则会加速保护住柱芯的更换频率。http://ng1.17img.cn/bbsfiles/images/2014/11/201411292251_525217_2421690_3.png 左图为全新柱芯,中间为用了三个月的缓冲盐(主要为磷酸盐、三氟乙酸类偏酸性),右图为半个多月的三乙胺pH 11-ACN(45:55)。可以明显发现三乙胺-乙腈对C-18的保护住具有明显的的溶解作用,随后使得系统压力超过4000 psi而停止运行。在缓冲液,尤其是碱性缓冲液使用频率较高的实验室中,预柱的使用则显得十分必要。此外,若是将预柱作为保护住接在进样器后,色谱柱之前,很可能会影响色谱峰的峰形,甚至影响分离,而基线波动也会明显变大,在示差检测器(RI)中可以有3倍的差距,在化药做杂质方法时,噪音的大小可能成为分析结果的关键因素。(3)基线的波动在梯度洗脱过程中,加入缓冲盐的流动相可能会引起基线漂移,当检测波长较低时(〈220 nm),这种变化会更加明显。这种漂移的主要原因是流动相及缓冲盐的末端吸收,及分析过程中流动相的比例发生变化所致,因此要想解决这种漂移,可以从这两个方面入手。(1 选择末端吸收更低的流动相和缓冲盐,有机相乙腈比甲醇好;(2 减小有机相与水相中缓冲物质的差异,在部分化药分析中,会将水相和有机相中均加入相同量的缓冲物质,eg. A相 ACN-H2O-TFA(950:50:1); B相ACN-H2O-TFA(50:950:1)
要测一个原料药中三乙胺的残留。仪器是安捷伦的6890N,7694E,条件如下:色谱柱HP-1,柱温100,进样口250,分流比1:1,柱压7.7psiFID250顶空平衡30min,温度70/100/110三乙胺浓度16ug/ml(用水溶),取2ml至10ml顶空瓶我的问题是我进了三乙胺后跟了一针空白,三乙胺的位置有出峰,再跟一针空白就没有了,我试着做进样精密度,连续进了三针峰面积从29涨到了40,RSD非常差。而且换了DB-624的柱子,这个问题还是存在,哪位大侠指点一下!
[color=#444444]三乙胺-丙酮-盐的混合液,三乙胺的含量在5%以下,请问有什么好的方法可以测定三乙胺的含量,在实验室用氢火焰毛细柱打可以出峰,但是如果含量特别低时担心[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]打不出,导致微量三乙胺检测不出来。查文献有溴酚蓝分光光度法、红外色谱,[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]、电位返滴定法,以及混合液放入盐酸,用过量NaOH滴定未反应酸,溴酚蓝做指示剂等方法。请问这几种方法哪个比较准确,并且好操作,谢谢各位了![/color]
我求解,三乙胺残留量气相检测需要注意什么?三乙胺好检测吗?检测它难点在哪儿?色谱柱选择针对该应用有什么讲究吗?极性柱和非极性柱哪种好些?试过HP-innowax柱,水做溶剂,顶空进样(平衡105度,瓶加压30psi),峰形不好,拖尾。峰面积RSD有时超过15%。跟它一同进柱子的丙酮、乙酸乙酯等组分,都表现良好。FID检测器对它的响应好不好,够不够灵敏?顶空瓶中水溶液中浓度为9ppm,agilent 7697顶空,分流比5:1,峰面积15左右,正常不?有人说三乙胺溶液中应加少量氢氧化钠处理,再做效果好,可行不?