http://simg.instrument.com.cn/bbs/images/brow/em09511.gif大家有使用固相萃取和凝胶净化设备中,对各个步骤,及分离效果,回收率有问题的可以咨询我哦
GPC凝胶净化色谱/SPE固相萃取/定量浓缩联用仪,在实验室内的前处理效果不知道怎么样?瑞士布奇有一款多样品定量浓缩仪,不知道这款仪器的使用效果怎么样,是不是比GPC凝胶净化色谱/SPE固相萃取/定量浓缩联用仪的前处理效率更高呢?望老师们给予建议。谢谢!!!
最近单位在做农残的测量,请问下毛细柱和填充柱前处理的区别很大么,我们现在买了固相萃取柱,规格为1000mg/6ml,能否代替凝胶净化装置,样品如何处理。

搞晕了,方法上都是自己装填3-5g硅胶和无水硫酸钠的玻璃净化柱来净化的。我又听说网上有那种成品的固相萃取硅胶柱,大概几百毫克的样子。这两个有什么区别啊?求教
今天我们实验室想做油脂类的农残 所以启用凝胶净化 (我的前任留下的)但发现没法使用 在上样之后 色素完全扩散, 不知道这个柱子还能不能使用, 先问下大神们有没有啥好方法来解决这个问题 是否能够进行从新装填填料 流动相环己烷 乙酸乙酯 1:1
兽药残留引发的畜产品安全问题已成为公认的食品安全问题,引起社会的广泛关注。建立简便、快速、灵敏的兽药残留检测方法无疑成为检测和控制兽药残留的重要前提。兽药残留分析是复杂混合物中痕量组分的分析技术,最显著的特点是需要严格的样本前处理步骤。在兽药残留检测中60%~80%的工作量和操作成本花在样品前处理。样品前处理包括液液萃取、离心、沉淀、蒸馏等传统技术和固相萃取、凝胶净化、分子印迹等现代分离技术。传统方法由于自动化程度低、净化效率低、选择性差、成本高、劳动强度大、环境污染严重等缺点而逐渐不能满足兽药残留分析的发展要求。 固相萃取技术由于其溶剂使用量少、操作简单、选择性高、重现性好,已发展成为分离和浓缩各种样品中痕量分析物质的一种强有力的工具。1978 年商用固相萃取柱问世以后,固相萃取技术更被广泛应用于复杂基质的前处理,目前已成为兽药残留分析前处理的主流技术。 1 固相萃取技术基本原理 固相萃取(Solid Phase Extraction,SPE)技术基于液相色谱原理,可近似看作一个简单的色谱过程。原理是利用固体吸附剂将液体样品中的目标化合物吸附,与样品的基体和干扰化合物分离,然后再用洗脱液洗脱或加热解吸附,达到分离和富集目标化合物的目的。固相萃取可分为在线萃取和离线萃取。前者萃取与色谱分析同步完成,而后者萃取与色谱分析分步完成,两者在原理上是一致的。 2 基本操作过程 2.1 柱预处理(柱活化) 用适当的溶剂淋洗SPE 柱,以使吸附剂保持湿润,可以吸附目标化合物或干扰化合物。不同模式固相萃取小柱活化用的溶剂不同,其目的有2 个:一是除去填料中可能存在的杂质;二是使填料溶剂化,提高固相萃取的重现性。 2.2 上样 将液态或溶解后的固态样品倒入预处理后的SPE 柱,然后利用抽真空、加压或离心的方法使样品通过SPE 柱,在该步骤中,分析物被保留在吸附剂上。 2.3 淋洗和洗脱 样品进入SPE 柱、目标化合物被吸附后,视分离模式和样品性质而定,可采用适当的洗脱剂将目标化合物直接淋洗下来;也可先将干扰化合物淋洗掉,再用适当的洗脱剂将目标化合物洗脱,通常采用后一种方法更有利于样品的净化。淋洗和洗脱同上所述,可采用抽真空、加压或离心的方法使淋洗液或洗脱液流过吸附剂。 3 影响因素 3.1 吸附剂 目前常用的吸附剂有正、反相吸附剂、离子交换吸附剂和抗体键合吸附剂等,试验时尽量选择与目标化合物极性相似的吸附剂,其用量大小与目标物性质(极性、挥发性)及其在水样中的浓度直接相关。 3.2 洗脱溶剂 在SPE 中,洗脱溶剂的选择与目标物性质及使用的吸附剂有关,楼蔓藤等给出了常见有机溶剂的极性和洗脱强度,试验过程中可根剧被测物的物理、化学性质选用。洗脱剂体积应以淋洗完全为前提,体积最小的为最佳,可通过多次洗脱法(小体积),根据回收率的变化曲线找到最佳的洗脱液体积,显然,洗脱体积越小富集倍数越高。 3.3 保留体积在加样过程中,保留体积是SPE 技术的关键因素之一,它代表了进行痕量富集时能有效处理的水样体积。根据色谱分析仪的最小检出量和水样中有机物的浓度,可以估算出欲富集的最小水样体积。另外,样液的pH 值也影响样品的吸附效率。 3.4 流速 流速的控制对SPE 至关重要,流速过大将引起SPE 柱的穿漏,流速太小则处理速度太慢。柱预处理过程中流速适中,保证溶液充分湿润吸附剂即可,上样和洗脱过程则要求流速尽量慢些,以使分析物尽量保留在柱内或达到完全洗脱,否则会导致分析物流失,影响回收率的大小。尤其离子交换过程,进行比较缓慢,应采用较低的流速(0.5~2.0 mL/min)。 4 结语固相萃取技术以其既可用于复杂样品中微量或痕量目标化合物的提取,又可用于净化、浓缩或富集的优势,不仅在兽药残留分析领域中担任重要的角色,而且在农药残留中也成为主要的前处理工具。随着人们对食品安全问题的关注,固相萃取技术不断得到发展与完善,多样化、标准化、仪器化和自动化的SPE 样品处理技术越来越成熟,将会更加广泛地应用于复杂样品的前处理中,成为目前样品前处理的主流技术。
本实验室准备上凝胶净化系统,主要是进行样品前处理(蔬菜、水果、茶叶、大米)。各大侠有在用的,请指教一二:品牌型号、价位、感觉如何?谢谢
农残中会用到凝胶净化色谱,虽然不常见,但是必须得有。我们想买一套制备液相,是否可以代替凝胶净化色谱因为制备液相平时可以做科研用
油脂样品乙腈正己烷液液分配及固相萃取柱净化来测定塑化剂的除油酯效果的初步考察看到许多网友对于含油脂样品的处理方法的讨论和几家厂商的处理净化方案,也一直在想除油净化效果如何?所以就测定一下,供大家参考。对于含油脂样品,例如食用油、黄油等动物油样品的塑化剂的测定,因为里面含大量油脂,不能用一般的溶剂提取后进行GCMS分析,需对样品净化以除去油脂。一种办法是凝胶色谱法(GPC)来净化,但设备比较贵,溶剂使用量大,还需氮吹除去溶剂。另一种方法就是乙腈正己烷液液分配加固相萃取柱净化来除去油脂。可能还有其它方法,但我不知道。下面简单的考察一下第二种办法除油的效果。1试剂dSPE玻璃萃取管(纯油基质型):1.0g/12mL(上海某公司提供)正己烷色谱纯。乙腈色谱纯。17种邻苯二甲酸酯类化合物混合标准液正己烷饱和的乙腈乙腈饱和的正己烷2 仪器与装置美国安捷伦7890A/5975C气相色谱-质谱联用仪高温气相色谱仪(HTGC):HP5890 plus漩涡混合器氮吹仪固相萃取仪SPE10 mL具塞玻璃刻度试管10 mL3样品处理准确称取0.5g的油脂样品于10mL具塞玻璃刻度试管(加入适量内标物),加4mL正己烷饱和的乙腈,2mL乙腈饱和的正己烷,漩涡震荡1min,静止或离心分层,吸去上层正己烷相,下层乙腈相待净化。在dSPE玻璃萃取管,用7mL二氯甲烷、7mL乙腈活化柱子,然后取上述乙腈相2mL加到柱子上并用试管收集,待样品过柱后再用4mL乙腈洗脱并一起收集,进GCMS分析。(如果要提高检测限,洗脱液可用氮吹仪吹干,加正己烷定容样液至1.0mL,样液供GC-MS分析,外标法)。4 GC/MS条件色谱条件: 色谱柱:安捷伦HP-5MS (30m×0.25 mm (i.d.)×0.25μm)毛细管柱;升温程序:60℃保持1min,以20℃/min升至220℃,保持1min,再以5 ℃/min升至280℃,保持8 min。(实际分析时间可以缩短) 载气(He,纯度99.999%以上)流速1 mL/min;进样口温度250℃,不分流进样;进样量:1μl。质谱条件: 电子轰击(EI)离子源;电子能量70eV;传输线温度280℃;离子源温度[/
各位老师:想问下5009.19中测有机氯时前处理需要的凝胶净化柱要用什么类型的填料啊?在这里先谢谢了!
现在好多农残检测的国标、行标里都有凝胶净化的方式,不知道使用的多么?效果如何?成本高么?有用过的老师介绍一下啊~~
最近计划用凝胶净化系统对样品进行前处理,不知道用这个GPC带浓缩的净化样品,对于检测样品有机磷、有机氯、拟除虫菊脂类的效果怎么样?)再有没有合适的处理含水少的样品标准可以参照。我找到的是果蔬类中有用此法净化,但是称样量是25克很大,而且收集体积很大105-185毫升。望有用过凝胶净化样品上质谱的给说说。。。。。。。。。。。。
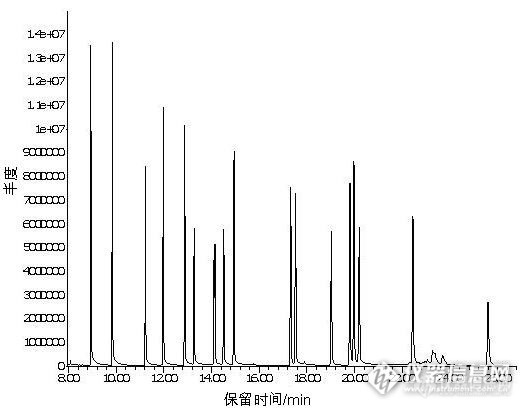
加压流体萃取-凝胶渗透净化-气质法测定土壤中64种SVOC前言:半挥发性有机物(Semi-volatile organic,简称SVOC)主要包括多环芳烃类、有机农药类、氯苯类、苯胺类、邻苯二甲酸酯类、苯酚类等化合物。土壤中半挥发性有机物的提取,传统的索式提取法耗时耗力,很难满足大量样品的检测需求;加压溶剂萃取提取技术具有提取时间短、效率高、消耗溶剂少的特点。现参考标准(HJ 834-2017土壤和沉积物 半挥发性有机污染物的测定 气相色谱-质谱法)来进行相关实验的分析。本实验使用了全自动高效快速溶剂萃取仪提取土壤中的64种SVOC,全自动凝胶净化系统进行净化,平行定量浓缩系统浓缩后用气质联用仪进行检测的一整套方法。该方法能够高效、稳定地达到实验的要求,可以提供领域范围内的良好应用。关键词:土壤 SVOC 1、实验部分1.1仪器和设备1.1.1 HPSE-E高效快速溶剂萃取系统;1.1.2 GPC 1000全自动凝胶净化系统:具可变波长紫外检测器,高效不锈钢凝胶净化柱;1.1.3 MultiVap-10平行定量浓缩系统;1.1.4 7890B气相色谱-5977B质谱联用仪1.2 试剂和样品1.2.1正己烷(色谱纯);1.2.2丙酮(色谱纯);1.2.3乙酸乙酯(色谱纯);1.2.4环己烷(色谱纯);1.2.5二氯甲烷(色谱纯);1.2.6快速溶剂萃取溶剂:用正己烷(1.2.1)和丙酮(1.2.2)按1:1体积比混合;1.2.7凝胶渗透色谱流动相:用乙酸乙酯(1.2.3)和环己烷(1.2.4)按1:1 体积比混合;1.2.8 SVOC标准使用液(200mg/L,溶剂为丙酮-二氯甲烷1:1);1.2.9内标使用液(400 mg/L,溶剂为丙酮-二氯甲烷1:1);1.2.10替代物标准使用液(200mg/L,溶剂为丙酮-二氯甲烷1:1);1.2.11硅藻土:置于马弗炉中400℃烘4h,冷却后置于玻璃瓶中于干燥器内保存。1.3土壤样品处理1.3.1 提取取研细过筛后的环境土壤样品20.0g,与7g硅藻土混合均匀,装填至34mL的萃取罐中。同样方法装填好两个萃取罐后,置于FLEX-HPSE样品架中(双通道运行,最多可连续萃取30个样品),萃取溶剂为丙酮正己烷混合溶剂(1.2.6),系统压力10Mpa,萃取温度100℃,加热平衡时间3min,静态萃取时间6min,冲洗体积60%,N2吹扫60s,循环运行两次,萃取液收集到50mL浓缩杯中。1.3.2 浓缩将收集管置于MultiVap-10中,浓缩温度30℃,开启定容功能。最后置换溶剂为乙酸乙酯环己烷混合溶剂(1.2.7),样品体积在5mL左右。1.3.3 净化净化过程采用凝胶渗透色谱净化的方式,具体方法如下:按照图1方法进行净化实验,收集时间为8min~32min,收集液用MultiVap-10浓缩,定容浓缩完成后再浓缩一定时间,溶液转移至2mL进样瓶中,加入适量内标后,定容至1mL,待测。https://ng1.17img.cn/bbsfiles/images/2022/10/202210081532527249_7872_3191395_3.png图1 凝胶净化方法1.4土壤加标回收率实验按1.3.1方法装填土壤样品,进行加标实验,20.0g样品加目标物(1.2.9)和替代物(1.2.13)各10μg,然后按照1.3.1~1.3.3方法进行实验,分别进行三组6个平行样品,用来测定加标回收率。1.5 分析步骤1.5.1 气质条件色谱柱:HP-5MS,30m*0.25mm*0.25μm;进样口温度:250℃;不分流进样;载气流速:1.0mL/min;恒流模式;进样量:1.0μL;柱温:35℃保持2min,以15℃/min升温至150℃,保持5min;再以3℃/min升温至290℃,保持2min。离子源:电子轰击源,70eV;四极杆温度:150℃;离子源温度:230℃;辅助加热温度:280℃;溶剂延迟时间:4.0min;扫描模式:全扫描Scan(化合物保留时间,定量和定性离子见表1)。表1定量和定性选择离子序号化合物名称RT/min定量离子定性离子1定性离子21N-亚硝基二甲胺5.1942744322-氟酚(SS)7.6264112923苯酚-D6(SS)9.119971---4苯酚9.139466405双(2-氯苯酚)醚9.2393636562-氯苯酚9.281281306471,3-二氯苯9.501461117581,4-二氯苯-D4(IS1)9.60150115---91,4-二氯苯9.63146148111101,2-二氯苯9.8514614811111二(2-氯异丙基)醚10.0312110777122-甲基苯酚10.051081077713N-亚硝基二正丙胺10.274370130144-甲基苯酚10.301071087715六氯乙烷10.3711710920116硝基苯-D5(SS)10.51821285417硝基苯10.54771235118异佛尔酮10.918213854192-硝基苯酚11.041396581202,4-二甲基苯酚11.121071227721二(2-氯乙氧基)甲烷11.279363123222,4-二氯苯酚11.4416216463231,2,4-三氯苯11.531477410924萘-d8(IS2)11.62136108---25萘11.66128129---264-氯苯胺11.791271296527六氯丁二烯11.82118260223284-氯-3-甲基苯酚12.72107142144292-甲基萘12.9611514114230六氯环戊二烯13.28130235239312,4,6-三氯苯酚13.70196198200322,4,5-三氯苯酚13.81196198200332-氟联苯(SS)13.91172171170342-氯萘14.25162127----352-硝基苯胺14.70138659236邻苯二甲酸二甲酯15.4016377---372,6-二硝基甲苯15.691656389383-硝基苯胺15.70659213839苊烯15.7315276---40苊-d10(IS3)16.3716416216041苊16.5215376---422,4-二硝基苯酚17.031846315443二苯并呋喃17.43168139---442,4-二硝基甲苯17.681658963454-硝基苯酚17.761391096546邻苯二甲酸二乙酯19.20149177---47芴19.3616616382484-氯苯基苯甲醚19.5820414177494-硝基苯胺19.9165138108504,6-二硝基-2-甲基苯酚20.021985110551偶氮苯20.547718251522,4,6-三溴苯酚(SS)20.9033262143534-溴二苯基醚21.632501417754六氯苯22.7228428628255五氯苯酚24.36266184---56菲-d10(IS4)25.4818880---57菲25.6517817617958蒽26.0117817617959咔唑27.6016716613960邻苯二甲酸二正丁酯31.121491507661荧蒽34.4320220020362芘36.03202200201634,4’-三联苯-D14(SS)38.1024424524364邻苯二甲酸丁基苄基酯42.601499120665苯并(α)蒽45.4622822622966?-d12(IS5)45.5024023624167屈45.7022822622968邻苯二甲酸二(2-二乙基己基)酯47.481491675769邻苯二甲酸二正辛酯52.34149279---70苯并(b)荧蒽53.1425212625071苯并(k)荧蒽53.3525212625072苯并(α)芘55.2225225025373苝-d12(IS6)55.6126426026374茚并(1,2,3-cd)芘61.9427613827475二苯并(ah)蒽62.2627813927676苯并(ghi)苝63.312761382742、实验结果2.1 76种半挥发性有机物色谱图分离情况(含内标和替代物)图2 76种半挥发性有机污染物总离子流谱图2.2 土壤样品加标色谱图图3 土壤样品加标色谱图2.3 加标样品回收率表2 加标样品回收率物质名称回收率(%)平均值(%)RSD(%)123456N-亚硝基二甲胺48.2 48.8 49.3 51.8 47.8 55.6 50.3 5.9 2-氟酚(SS)53.9 60.8 51.4 54.1 58.2 54.6 55.5 6.1 苯酚-D6(SS)52.8 54.0 54.2 51.0 56.5 50.4 53.2 4.2 苯酚54.5 59.0 64.6 62.8 59.2 65.8 61.0 6.9 双(2-氯苯酚)醚53.1 65.0 58.7 60.3 55.9 57.6 58.4 6.9 2-氯苯酚56.1 64.1 53.4 54.5 58.1 62.6 58.1 7.5 1,3-二氯苯54.0 53.4 57.5 60.8 53.9 55.1 55.8 5.1 1,4-二氯苯59.3 57.7 51.9 52.8 48.0 47.8 52.9 9.1 1,2-二氯苯50.9 49.2 44.4 51.6 51.7 45.3 48.9 6.6 二(2-氯异丙基)醚58.3 51.1 59.7 71.8 59.9 59.0 60.0 11.1 2-甲基苯酚54.9 63.2 55.9 71.9 58.2 68.8 62.2 11.3 N-亚硝基二正丙胺56.7 59.8 58.5 74.9 61.6 62.2 62.3 10.4 4-甲基苯酚54.0 53.6 55.8 57.7 56.8 60.8 56.5 4.7 六氯乙烷59.4 53.2 68.9 61.7 58.4 53.8 59.2 9.7 硝基苯-D5(SS)53.0 54.3 56.4 69.5 58.9 61.1 58.9 10.2 硝基苯51.9 47.2 54.9 63.8 59.7 60.2 56.3 10.9 异佛尔酮52.4 63.6 59.5 53.5 68.6 64.5 60.4 10.7 2-硝基苯酚60.3 57.5 55.1 56.9 59.0 53.6 57.1 4.3 2,4-二甲基苯酚57.3 53.1 45.0 47.6 57.7 55.6 52.7 10.0 二(2-氯乙氧基)甲烷63.8 61.9 56.9 74.9 63.4 73.8 65.8 10.8 2,4-二氯苯酚65.8 56.9 68.1 59.1 66.3 62.3 63.17.0 1,2,4-三氯苯52.3 56.9 51.6 54.4 60.1 50.5 54.3 6.7 萘53.5 50.7 58.4 50.2 58.9 53.6 54.26.8 4-氯苯胺51.2 48.0 50.1 42.8 46.4 49.1 47.9 6.3 六氯丁二烯51.4 49.0 43.9 50.0 40.1 46.0 46.7 9.1 4-氯-3-甲基苯酚68.5 60.3 68.6 73.1 74.3 70.5 69.2 7.2 2-甲基萘65.4 59.3 61.1 53.7 57.6 66.9 60.7 8.1 六氯环戊二烯60.7 62.7 66.7 58.6 59.8 64.1 62.14.8 2,4,6-三氯苯酚68.7 57.4 60.4 60.2 61.5 60.4 61.4 6.2 2,4,5-三氯苯酚62.5 67.1 66.8 61.2 62.1 70.9 65.1 5.82-氟联苯(SS)60.4 53.1 55.8 56.1 62.9 61.8 58.4 6.7 2-氯萘50.5 65.9 64.5 59.3 59.0 71.5 61.8 11.7 2-硝基苯胺62.5 62.6 78.6 74.4 68.6 73.5 70.0 9.4 邻苯二甲酸二甲酯72.0 63.1 71.8 70.8 73.4 79.6 71.8 7.4 2,6-二硝基甲苯58.7 62.5 75.6 67.4 75.3 75.2 69.1 10.7 苊烯59.0 53.3 59.5 54.2 57.3 65.8 58.2 7.7 3-硝基苯胺46.3 52.6 54.6 47.6 53.5 53.5 51.4 6.8苊56.5 61.5 58.7 66.0 76.5 67.2 64.4 11.2 2,4-二硝基苯酚43.138.343.042.145.845.142.9 6.2 二苯并呋喃63.4 62.6 64.3 74.6 68.1 79.5 68.8 10.0 2,4-二硝基甲苯54.7 55.0 63.8 65.3 59.9 71.3 61.7 10.4 4-硝基苯酚61.5 73.6 84.3 73.6 69.5 77.5 73.3 10.4 邻苯二甲酸二乙酯80.5 78.0 77.2 80.2 82.3 73.8 78.7 3.8 芴67.1 71.3 66.3 77.9 70.9 82.0 72.6 8.5 4-氯苯基苯甲醚66.0 70.4 66.3 78.8 71.2 68.9 70.3 6.7 4-硝基苯胺53.350.450.458.450.747.451.8 7.2 4,6-二硝基-2-甲基苯酚58.9 60.0 68.7 59.3 73.7 70.9 65.3 10.1 偶氮苯68.6 61.2 66.8 80.8 72.5 73.1 70.5 9.4 2,4,6-三溴苯酚(SS)70.6 77.9 77.5 74.2 71.0 64.0 72.5 7.2 4-溴二苯基醚80.3 79.0 77.9 83.7 78.2 71.3 78.4 5.2 五氯苯酚74.6 70.6 75.6 69.1 76.8 67.9 72.4 5.1六氯苯71.4 71.1 69.3 81.4 77.3 90.1 76.8 10.4 菲88.3 88.8 84.7 100.6 89.5 84.0 89.3 6.7 蒽74.1 77.5 68.7 82.2 78.2 92.8 78.9 10.4 咔唑85.4 95.5 80.1 99.2 92.7 75.6 88.1 10.5 邻苯二甲酸二正丁酯112.4 123.4 101.7 117.5 121.0 105.4 113.6 7.6 荧蒽95.0 87.8 91.8 81.1 80.0 92.1 88.0 7.0 芘74.2 86.0 72.8 83.9 87.3 85.0 81.5 7.8 4,4’-三联苯-D14(SS)78.7 78.7 73.7 70.7 81.4 79.1 77.1 5.2邻苯二甲酸丁基苄基酯80.5 95.6 76.4 79.9 92.4 96.2 86.8 10.2 苯并(α)蒽73.5 88.8 70.7 86.0 82.3 77.9 79.9 8.9 屈76.2 91.5 73.6 88.5 83.7 91.4 84.2 9.2 邻苯二甲酸二(2-二乙基己基)酯111.2 114.4 116.0 118.3 108.3 115.0 113.9 3.1 邻苯二甲酸二正辛酯107.6 111.8 115.0 104.4 115.7 108.7 110.5 4.0 苯并(b)荧蒽75.2 93.4 85.1 90.6 88.1 83.1 85.9 7.5 苯并(k)荧蒽71.2 93.8 70.5 88.9 87.2 79.5 81.9 11.8 苯并(α)芘77.6 94.7 74.5 70.6 88.5 84.4 81.7 11.1 茚并(1,2,3-cd)芘85.1 92.4 84.4 91.0 85.3 100.3 89.8 6.9 二苯并(ah)蒽81.2 84.2 80.8 94.1 84.1 95.5 86.7 7.5 苯并(ghi)苝87.6 85.8 80.3 85.6 73.6 78.5 81.9 6.6 3、结论由表2可知,加压流体萃取-凝胶净化-气质法测定土壤中的64种半挥发性有机污染物,土壤加标回收率为42.9%~113.9%,RSD为3.1~11.8%;替代物回收率为53.2%~77.1%,RSD为4.2~10.2%。参考标准:1、HJ 834-2017土壤和沉积物 半挥发性有机污染物的测定 气相色谱-质谱法
请教:全自动凝胶净化浓缩仪(GPC)可用于哪些方面,回收率如何,仪器稳定吗?
针对柑橘样品的净化,大家建议是什么固相萃取柱?有经验的人,多多建议啊。谢谢。我采用弗洛里硅固相萃取柱试过,效果不佳,定容后的样品是明显的淡黄色。进样后前面几分钟有明显的大面积基体杂质。
我们实验室想买一台GPC凝胶净化色谱仪用于食品检测的样品前处理,不知哪种型号比较理想,大概价位是多少,哪家的性价比更高?请各种高手相助!
实验室想买一台GPC凝胶净化色谱仪用于食品检测的样品前处理,请各位使用过该仪器的同志们帮忙推荐一下产品,及各产品的优缺点。谢谢啦!
国标5009.19中食品中有机氯农药多组分残留量的测定中,采用凝胶色谱层析纯化,用哪种固相萃取柱可替代?
我是菜鸟,问几个问题,请大家帮帮我,谢谢!GBT19426-2006 《蜂蜜、果汁和果酒中497种农药及相关化学品残留量的测定 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]-MS法》中,样品前处理过程为:先用二氯甲烷萃取,再用Envi-Carb 和Sep-park-NH2串联进行净化。请问:1、这两种固相萃取小柱的功能有什么不同,为什么要一起联用?2、选择SPE柱是根据什么原理,是样品极性吗?有没有参考表之类的东东?3、为什么联用的柱子越来越小?4、还有哪些常用的SPE柱?
以下是一次农残检测培训中的一些净化处理经验,与大家分享下农残分析中常用的净化方法有:液-液分配法、柱层析法、固相萃取法、吹扫蒸馏法、磺化法、凝结剂沉淀法和薄层色谱法等。1、柱子预处理(固定相活化)活化的目的是创造一个与样品溶剂相容的环境并去除柱内所有杂质。通常需要两种溶剂来完成上述任务,第一个溶剂(初溶剂)用于净化固定相,另一个溶剂(终溶剂)用于建立一个合适的固定相环境使样品分析物得到适当的保留。注意:终溶剂不应强于样品溶剂,若使用太强的溶剂,将降低回收率。另外,在活化的过程中和结束时,固定相都不能抽干,因为这将导致填料床出现裂缝,从而得到低的回收率和重现性,样品也没得到应有的净化。如果在活化步骤中出现干裂,所有活化步骤都得重复。 2、上样上样步骤指样品加入到固相萃取柱并迫使样品溶剂通过固定相的过程,这时分析物和一批样品干扰物保留在固定相上。为了保留分析物,溶解样品的溶剂必须较弱。如果溶剂太强,分析物将不被保留,结果回收率将会很低,这一现象叫穿漏。尽可能使用最弱的样品溶剂,可以使溶质得到最强的保留或者说最窄的谱带。3、淋洗分析物得到保留后,通常需要淋洗固定相以洗掉不需要的样品组分,淋洗溶剂的洗脱强度是略强于或等于上样溶剂。淋洗溶剂必须尽量地弱以洗调尽量多的干扰组分,但不能强到可以洗脱任何一个分析物的程度。注意:淋洗时不宜使用太强溶剂,否则会将强保留杂质洗下来。使用太弱溶剂,会使淋洗体积加大。可改为强、弱溶剂混用;但混用或前后使用的溶剂必须互溶。4、洗脱 淋洗过后,将分析物从固定相上洗脱。溶剂必须进行认真选择,溶剂太强,一些更强保留的不必要组分将被洗出来;溶剂太弱就需要更多的洗脱液来洗出分析物,这样固相萃取柱的浓缩功效就会削弱。一般菜样:如白菜、甘蓝、黄瓜、萝卜等,可根据需要选用 C18柱、 Florisil柱、NH2柱等净化。 深色样品:如菠菜、菜心、青椒和胡萝卜,含色素多,可用石墨碳黑柱去除色素。茶叶:含咖啡因多,用Si小柱净化可较好地去除。大豆、花生:含油脂多,净化时用SAX、PSA小柱去脂。 高糖高盐样品:如葡萄干、梅脯、腌黄瓜等可采用硅藻土柱助滤。由于不同样品存在一定的基质增强效应,因此用试剂配制标准溶液测定样品往往会造成检测结果偏高的现象,采用样品空白提取液配制标准溶液,可以有效弥补基质增强效应带来的定量偏差。
http://www.instrument.com.cn/show/Breviary.asp?FileName=C70556%2Ejpg&iwidth=200&iHeight=200 莱伯泰科有限公司 的 GPC Cleanup 800 全自动凝胶净化系统(GPC Cleanup 800)已参加“国产好仪器”活动并通过初审。自上市以来,这款产品已经被多家单位采用,如果您使用过此仪器设备或者对其有所了解,欢迎一起聊聊它各方面的情况。您还可以通过投票抽奖、参与调研等方式参与活动,并获得手机电子充值卡。【点击参与活动】 仪器简介: GPC Cleanup 800全自动凝胶净化系统,是一款将高度自动化与准确、快速完美结合的样品净化前处理系统。可以自动完成样品进样、分离净化、目标组分收集系列操作,GPC Cleanup 工作站执行数据采集、保存和管理功能。可以与Vortex定量浓缩系统在线联用,自动实现样品预浓缩-GPC凝胶净化-定量浓缩过程。 性能指标 GPC Cleanup 800全自动凝胶净化系统 ASF800自动液体处理器自动完成样品进样和组分收集过程。样品盘与收集盘可任意组合,进样位置和收集位置可任意设定,具有隔垫穿刺功能,全密闭系统 高精度双柱塞串联输液泵,最大工作压力42MPa,最大流量50.00mL/min 标配190-600nm可变波长UV-Vis检测器,最大限度满足应用需求 进样清洗平台可精确控制进样及在线清洗过程 具备溶剂回收功能,保护环境,节约溶剂 灵活多变的净化程序适合多种应用。六种收集模式六段收集程序可自由编辑,本机存储无限多个净化方法,便于实验室方法管理 GPC 2.0系统工作站软件版本功能强大,界面更加人性化。可以完成系统控制、数据采集以及数据的保存、管理等一系列操作 可在线控制和在线修改所有参数,满足突发情况下实验需求 高分辨不锈钢凝胶净化柱,效率更高,速度更快,节省时间和溶剂,也可选配其它类型的净化柱 也可选配254nm/280nm固定波长紫外检测器 【了解更多此仪器设备的信息】
要做多环芳烃样品净化,不知道选用什么固相萃取柱比较好呢,请大神指点
想了解做样品前处理的浓缩和凝胶净化两个模块的仪器是盘合的好 还是美国J2的好,求用过的大侠指点!!!最好能说下优点心得,谢谢http://simg.instrument.com.cn/bbs/images/default/em09502.gif
请问聚苯乙烯凝胶净化柱具体怎么填充?麻烦知道的师傅们说的详细点,把应该注意些什么细节都给说一下,还有使用的时候应该注意些什么事项,万一柱子干了怎么办?谢谢
凝胶净化系统(GPC)主要用在哪些方面?
需要一台净化油脂的凝胶净化系统,大家有没有什么好的牌子推荐?
使用固相萃取C18小柱萃取尿液中多环芳烃,使用了超纯水、甲醇活化,甲醇和超纯水的混合液平衡,加入5mL尿液,之后用正己烷洗脱,收集的液体进行氮吹,但是有好像凝胶一样的东西氮吹不掉。不知道什么原因,恳请各位前辈指点迷津!!!
实验室2010年买了一台LCTech的全自动凝胶净化色谱仪,但是一直没有用起来,现在想重新用起来,可是仪器的浓缩腔体也脏了,好多操作都不怎么会用,想请厂家过来培训和维护下,可是价钱又太贵,想请论坛里的大侠留个电话,咨询下。
每天做实验,每天都有疑点,所以每天都来论坛看一下各位高手的经验。问大家桔子高效液相测吡虫啉净化都是用什么固相萃取小柱?我用的标准GB/T 23379, 说用ENVI-18柱,可我的是ENVI-Carb柱,和C18柱不知道能用不?求高手指点
[em09] 我中心计划采购凝胶净化系统(GPC),用于农残分析的前处理.但不知现在有哪家的仪器好.请指教!我们考察了以下公司的产品,但是越考察越搞不明白:FMS 吉尔森 J2 LCTECH OI请指点!