
[b][font='Times New Roman'][font=宋体]解答:[/font][/font][/b][font=宋体][font=宋体]([/font]1[font=宋体])[/font][/font][font='Times New Roman'][font=宋体]分析型液相色谱是用来给一种或多种组分进行定量和定性,而制备型液相色谱则是用来对产品的单体进行提取和纯化。所以将制备型高效液相色谱仪定义为大容量色谱柱和高流速是不准确的。[/font][/font][font=宋体][font=宋体]([/font]2[font=宋体])[/font][/font][font='Times New Roman'][font=宋体]与传统的纯化方法(如蒸馏、萃取)比较,制备液相是一种更有效的分离方法,因此被广泛应用在样品和产品的提取和纯化上。随着合成、植化、生化和制药等领域对高纯度组份的需求不断增加,制备型液相色谱仪应用的领域也在迅速的扩大发展。[/font][/font][font=宋体][font=宋体]([/font]3[font=宋体])[/font][/font][font='Times New Roman'][font=宋体]半制备液相色谱通常也称为分析兼半制备液相色谱,理论上分析型液相色谱都是可以进行半制备的,只不过分析兼半制备液相色谱在流速和样品通量上有所提高。一般来说,按照流量划分,半制备一般为[/font]50mL/min[font=宋体],譬如[/font][font=Times New Roman]Thermo Fisher[/font][font=宋体]的[/font][font=Times New Roman]UltiMate? 3000 [/font][font=宋体]半制备系统[/font][/font][font=宋体];[/font][font='Times New Roman']100mL/min[font=宋体]以上的大流量为制备色谱。[/font][/font][font='Times New Roman'][font=宋体][img=,256,256]https://ng1.17img.cn/bbsfiles/images/2021/03/202103172149596942_4027_3389662_3.jpg!w256x256.jpg[/img][/font][/font]
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=41260]反相液相色谱对多肽的分离、纯化与制备[/url]
随着全球“回归自然”的热潮,对天然植物活性成分的研究开发也就成了当前医药、食品、化妆品等领域的热点,基于天然产物资源开发的产业已被认为是世界上最有前途、最具生机的行业之一。从天然植物资源中分离天然活性成分具有很多的困难和问题,因为大多数植物资源中所含有的活性成分含量低,且存在于复杂的介质中,色谱分离法一直是天然产物成分分离的常用的方法,例如有柱色谱法和制备型高效液相色谱法等,但是,物质在固态填充物的不可逆吸附和变性是固相色谱所遇到的共同问题。另外,从分析到制备规模的放大,所需费用也相当昂贵。逆流色谱是一种无需任何固定相支撑体的液-液分配色谱分离技术,不存在对样品组分的吸附、变性、失活、拖尾等不良影响,节省填充材料和溶剂消耗;它的操作简便,重现性好,分离量较大,粗提物样品可以直接进样分离。目前已有许多成功应用的实例作为参考,所以在操作时溶剂系统的变换更为方便、快捷。对天然产物的分离纯化,是高速逆流色谱非常适合的应用领域。我国是世界上最早将逆流色谱技术应用于天然植物和中草药成分分离纯化的国家。早在1980年,张天佑教授就自行研制出了国产的逆流色谱仪,并开创了在天然植物和中草药领域的应用研究工作 。此后的20多年中,越来越多的中国科技工作者利用我国的资源优势和技术优势,在这一技术领域和应用领域做出了成绩和贡献。 不同种类天然产物的分离虽然已有文献总结,但系统性和更新程度还有待完善。山东省科学院分析测试中心王晓研究员的研究团队以在天然产物分离方面取得的优异成绩为基础,对不同种类的天然产物分离正在进行全面的最新的总结。不日,最新的不同种类天然产物的分离总结及独有的相关见解将面世。
[color=red]【由于该附件或图片违规,已被版主删除】[/color][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=31325]制备高效液相色谱分离纯化荷叶碱[/url]
全自动层析分离纯化系统和制备液相是一样的吗?有什么区别?
高速逆流色谱法分离纯化丹参并尝试制订中药指纹图谱顾铭* 欧阳藩 苏志国(中国科学院过程工程研究所生化工程国家重点实验室,北京,100080)摘要 用国产高速逆流色谱(HSCCC)分离纯化中草药——丹参,选用正己烷-乙醇-水体系,固定相保留率达到78.8%。采用分步洗脱,3个产地丹参各分离得到12个洗脱组分,经高效液相色谱仪和紫外光谱仪检测证明3张HSCCC洗脱图谱中对应洗脱峰为同一组分。HSCCC洗脱图谱不包含非共有峰,并且对应洗脱峰保留时间的相对标准偏差RSD3%,符合国家标准关于制订指纹图谱方法学考察资料的技术参数。因此,HSCCC作为制订指纹图谱的方法之一具有可行性。关键词 高速逆流色谱(HSCCC),中药指纹图谱,丹参中图分类号 R917仪器TBE-300半制备型高速逆流色谱仪(深圳同田生化技术有限公司,中国)。聚四氟乙烯管缠绕在3个水平轴上形成螺旋管(管直径2.6mm,分离体积300mL),进样圈20mL。高速逆流色谱配备了柱塞式泵(S系列,北京圣益通技术开发有限责任公司,中国),紫外检测仪(8823A,北京新技术应用研究所,中国),记录仪(3057型,四川记录仪器厂,中国)。
[color=#444444]用液相跑某一个样品,发现杂质峰比较多,欲将主峰物质进一步分离纯化,收集相应峰馏分。用普通的分析检测型的HPLC可以做到吗?还是用制备型色谱?只要收集到一点点就可以,然后可以做定性分析...我查文献里说都是用制备型色谱分离,希望懂色谱的高手指导一下,多谢[/color]
高速逆流色谱法分离纯化丹参并尝试制订中药指纹图谱顾铭* 欧阳藩 苏志国(中国科学院过程工程研究所生化工程国家重点实验室,北京,100080)摘要 用国产高速逆流色谱(HSCCC)分离纯化中草药——丹参,选用正己烷-乙醇-水体系,固定相保留率达到78.8%。采用分步洗脱,3个产地丹参各分离得到12个洗脱组分,经高效液相色谱仪和紫外光谱仪检测证明3张HSCCC洗脱图谱中对应洗脱峰为同一组分。HSCCC洗脱图谱不包含非共有峰,并且对应洗脱峰保留时间的相对标准偏差RSD3%,符合国家标准关于制订指纹图谱方法学考察资料的技术参数。因此,HSCCC作为制订指纹图谱的方法之一具有可行性。关键词 高速逆流色谱(HSCCC),中药指纹图谱,丹参中图分类号 R917仪器TBE-300半制备型高速逆流色谱仪(深圳同田生化技术有限公司,中国)。聚四氟乙烯管缠绕在3个水平轴上形成螺旋管(管直径2.6mm,分离体积300mL),进样圈20mL。高速逆流色谱配备了柱塞式泵(S系列,北京圣益通技术开发有限责任公司,中国),紫外检测仪(8823A,北京新技术应用研究所,中国),记录仪(3057型,四川记录仪器厂,中国)。*通讯作者。Tel: 86-10-82627061;Fax: 86-10-62558174;E-mail: rainbow_gm@sina.com
[b][font=宋体]解答:[/font][/b][font=宋体]([/font]1[font=宋体])化学合成的肽产品是一个纯度不好的粗产品,其一是因为在合成肽过程中各种副反应、消旋化等造成的副反应肽;二是在脱保护过程中,由于保护基的残留,肽键的断裂、烷基化等造成的杂质。由于杂质与合成的肽在分子结构和化学性质上非常相似,给肽的分离纯化带来了困难,需要根据对目的肽的要求选择适当的方法进行纯化。[/font][font=宋体]([/font]2[font=宋体])目前用于分离纯化合成多肽的液相色谱模式主要有三种:一是凝胶过滤色谱,按照肽分子的大小进行分离;二是离子交换色谱,按肽分子所具有的带电基团的性质和数目进行分离;三是反相色谱,按照肽分子的疏水性强弱进行分离。[/font][font=宋体]([/font]3[font=宋体])通常采用制备或者半制备色谱对合成多肽化合物进行分离纯化。制备色谱的进样品量很大,因此要求进样系统能满足大体积进样要求,例如计量泵、定量环的体积会不同于普通分析型色谱。进样量的增加导致制备色谱柱子的分离负荷相应加大,也就必须加大色谱柱填料,增大制备色谱的直径和长度。如[/font]GB/T 20770-2008[font=宋体]《粮谷中[/font]486[font=宋体]种农药及相关化学品残留量的测定[/font][font=宋体]液相色谱[/font][font=宋体]-[/font][font=宋体]串联质谱法》中使用的色谱柱要求柱长[/font]400mm[font=宋体],内径[/font]25mm[font=宋体]。要将待分离组分从如此规格的色谱柱中洗脱下来,就需要使用相对多的流动相,因此制备色谱的管路也比分析色谱粗很大,同时泵的流速也较高,通常需要设置为[/font]5mL/min[font=宋体]。由于制备或者半制备色谱仅用于分离纯化,不用于定量或定性分析,对泵的精密度、检测器的灵敏度等要求较低。[/font][font='微软雅黑','sans-serif'][color=black][back=white]领取更多《实战宝典》请进:[url]http://instrument-vip.mikecrm.com/2bbmrpI[/url][/back][/color][/font][font='微软雅黑','sans-serif'][color=black][back=white] [/back][/color][/font]
[align=center][/align][font=宋体]一、原理[/font][font=宋体]1.[/font][font=宋体]多糖的分级与纯化[/font][font=宋体]多糖纯化的实质是将粗多糖中的杂质(包括蛋白质、色素、低聚糖、无机盐等非糖物质)除去而获得分子量和极性均一的多糖组分。比较常用的方法有:醇沉法、超滤法和柱层析法等。其中柱层析法应用比较普遍,多用于样品的精细分级,具有操作简单,重现性好的优点,但样品上样量小。用于多糖分离的柱层析主要有两类:一类是通过分子量大小进行分级的凝胶柱层析,如Sephadex G-100(200、50、25、10)、SepharoseCL-6B等系列;另一类是离子交换层析,是根据多糖所带电荷的性质不同选择相应的离子交换柱对多糖进行分级。如待分离的多糖带有负电荷,可选择阴离子型的DEAE-纤维素柱或DEAE-Sepharose柱进行分级,以获得均一的多糖组分。[/font][font=宋体]通过热水煮提方法提取的多糖,通常是混合物,且分子量不均一,其单糖组成、分子结构和聚合度往往不同,可通过柱层析的方法,对其进行分级以达纯化的目的。本实验中,采用[/font]DEAE-[font=宋体]纤维素柱层析的方法对中草药中水溶性粗多糖进行分级纯化,分离纯化出各级分多糖,[/font][font=宋体]为后续研究多糖的结构特征和生物活性奠定基础。[/font][font=宋体]2.[/font][font=宋体]苯酚—硫酸法[/font][font=宋体]游离的寡糖、多糖中的己糖或糖醛酸在浓硫酸的作用下,脱水生成糠醛,再与苯酚作用起显色反应,在一定范围内其颜色深浅与糖的含量成正比,吸收值与糖含量呈线性关系。且己糖在[/font]490 nm[font=宋体]处(戊糖及糖醛酸在[/font]480 nm[font=宋体])有最大吸收,故用比色法测定多糖含量。该法简单,快速,灵敏,且颜色持久,同一台设备同一光源仅需制作一条标准曲线。[/font][font=宋体] [/font][font=宋体]二、步骤[/font]1.[font=宋体]中草药水溶粗多糖的提取流程[/font][font=宋体]中草药粉末[/font][font=Symbol][/font][font=宋体]蒸馏水浸泡过夜[/font][font=Symbol][/font][font=宋体]超声[/font]/[font=宋体]微波[/font][font=Symbol][/font][font=宋体]水浴浸提[/font][font=Symbol][/font][font=宋体]过滤去除药渣[/font][font=Symbol][/font][font=宋体]定容[/font][font=Symbol][/font][font=宋体]多糖含量测定[/font][font=宋体]加等体积[/font]95%[font=宋体]乙醇[/font][font=Symbol][/font]4[font=宋体]℃冰箱过夜,醇沉多糖[/font][font=Symbol][/font]5000r/min[font=宋体]离心去上清液[/font][font=Symbol][/font][font=宋体]粗多糖[/font][font=Symbol][/font][font=宋体]脱蛋白[/font][font=Symbol][/font][font=宋体]脱色素[/font][font=Symbol][/font][font=宋体]透析[/font][font=Symbol][/font][font=宋体]浓缩[/font][font=Symbol][/font][font=宋体]冷冻干燥得水溶多糖[/font][font=Symbol][/font]DEAE-[font=宋体]纤维素色谱柱[/font][font=Symbol][/font][font=宋体]收集多糖组分[/font][font=Symbol][/font][font=宋体]测定每[/font]50s[font=宋体]洗脱液的[/font]OD[font=宋体]值[/font][font=Symbol][/font][font=宋体]绘制横坐标为管数与纵坐标为[/font]OD[font=宋体]值的洗脱曲线[/font][font=宋体]根据洗脱曲线收集多糖溶液[/font][font=Symbol][/font]4[font=宋体]℃无水乙醇醇沉过夜[/font][font=Symbol][/font][font=宋体]离心[/font][font=Symbol][/font][font=宋体]多糖沉淀[/font][font=Symbol][/font][font=宋体]常规干燥[/font][font=Symbol][/font][font=宋体]纯度鉴定[/font][font=Symbol][/font][font=宋体]纯多糖[/font]2.[font=宋体]脱蛋白[/font][font=宋体]由于粗多糖中含有一定量游离的和结合的蛋白,为保证多糖的纯度,必须将蛋白质脱去。常用的脱蛋白方法有[/font]Sevag[font=宋体]法、三氯乙酸法和蛋白酶法(如链蛋白酶、胰蛋白酶、木瓜蛋白酶)等。[/font][font=宋体]([/font]1[font=宋体])[/font]Sevag[font=宋体]法[/font][font=宋体]根据蛋白质在有机溶剂(如氯仿)中易发生变性析出的特点[/font][font=宋体],把多糖配制成[/font]5%[font=宋体]的糖液,然后按照[/font]1:3[font=宋体]的体积比加入[/font]Sevag[font=宋体]试剂(氯仿∶正丁醇[/font]=4[font=宋体]∶[/font]1[font=宋体]),混匀后剧烈振荡,静置分层后吸去水层与溶剂层交界处的变性蛋白质,重复操作多次,直到除尽蛋白质为止。[/font][font=宋体]([/font]2[font=宋体])三氯乙酸法[/font][font=宋体]将粗多糖配成[/font]5%[font=宋体]的糖液,加入[/font]30%[font=宋体]三氯乙酸溶液,使三氯乙酸终浓度为[/font]15%[font=宋体],在[/font]4℃[font=宋体]冰箱中放置过夜,离心弃去沉淀,得无蛋白的多糖溶液,再用[/font]1 mol/L NaOH[font=宋体]溶液中和至[/font]PH[font=宋体]为[/font]7[font=宋体]。[/font][font=宋体]([/font]3[font=宋体])蛋白酶法[/font][font=宋体]将粗多糖配成[/font]5%[font=宋体]的糖液,用酸碱调[/font]pH[font=宋体]至中性,加链蛋白酶[/font]0.5 L[font=宋体],放恒温箱中[/font]37℃[font=宋体]保温[/font]24 h[font=宋体]后,加热升温至[/font]80℃[font=宋体]使酶失活,离心,得无蛋白的多糖溶液。[/font]3.[font=宋体]脱色[/font][font=宋体]([/font]1[font=宋体])[/font] [font=宋体]活性炭法[/font][font=宋体]将脱蛋白后的多糖配成[/font]5%[font=宋体]的糖液,用[/font]NaOH[font=宋体]溶液调[/font]pH[font=宋体]为[/font]4.5[font=宋体],加入活性炭粉末,于[/font]80℃[font=宋体]保温[/font]2 h[font=宋体]后过滤。反复进行[/font]3[font=宋体]次,直到溶液颜色不再降低为止。[/font][font=宋体]([/font]2[font=宋体])过氧化氢法[/font][font=宋体]将脱蛋白后的多糖溶液,用浓氨水调至[/font]pH[font=宋体]为[/font]8.0[font=宋体],逐滴滴加[/font]20%H[sub]2[/sub]O[sub]2[/sub][font=宋体]至溶液为浅黄色,[/font]50℃[font=宋体]水浴,保温[/font]2 h[font=宋体]后过滤。[/font]4.[font=宋体]透析脱盐[/font][font=宋体]将脱蛋白、脱色后多糖配成[/font]5%[font=宋体]溶液,置于透析袋中,先用自来水逆向流水透析[/font]72 h[font=宋体]后,再用蒸馏水透析[/font]24 h[font=宋体],每[/font]4 h[font=宋体]换水一次。[/font]5.[font=宋体]干燥[/font][font=宋体]将脱蛋白、脱色、脱盐后的中草药多糖溶液,水浴[/font]80℃[font=宋体]浓缩至[/font]10 mL[font=宋体],加三倍体积的无水乙醇过夜,离心取沉淀,经无水乙醇、乙醚洗涤后,常规干燥得中草药去蛋白去色素的多糖。[/font]6.[font=宋体]多糖含量测定[/font][font=宋体]采用苯酚[/font]-[font=宋体]硫酸法测定样品中的多糖含量。绘制标准曲线,根据葡萄糖标准曲线和样品吸光值计算其糖含量。[/font][font=宋体]标准曲线的制作:准确称取[/font]105℃[font=宋体]干燥恒重的标准葡萄糖[/font]50 mg[font=宋体]定容于[/font]500 mL[font=宋体]容量瓶中,加水至刻度,用移液管分别吸取[/font]0[font=宋体]、[/font]0.1[font=宋体]、[/font]0.2[font=宋体]、[/font]0.3[font=宋体]、[/font]0.4[font=宋体]、[/font]0.5[font=宋体]、[/font]0.6[font=宋体]、[/font]0.7[font=宋体]、[/font]0.8[font=宋体]、[/font]0.9[font=宋体]、[/font]1.0 mL[font=宋体]转入试管中,各以蒸馏水补至[/font]1.0 mL[font=宋体],每个浓度重复四个平行。然后分别向每支试管中加入[/font]4%[font=宋体]苯酚试剂[/font]1mL[font=宋体]及浓硫酸[/font]2 mL[font=宋体],摇匀,沸水浴中煮沸[/font]10 min[font=宋体],冷却至室温,放置[/font]10 min[font=宋体]后在[/font]λ= 480 nm[font=宋体]处测定吸光值[/font]A[font=宋体]。以吸光值[/font]A[font=宋体]为纵坐标,糖含量[/font]C[font=宋体]为横坐标,得糖的标准曲线。[/font][font=宋体]样品溶液制备:精密称取水溶性粗多糖[/font]5 mg[font=宋体],先加[/font]10 mL[font=宋体]蒸馏水溶解,然后定容至[/font]50 mL[font=宋体]。[/font][font=宋体]样品含量测定:用移液管吸取样品液[/font]1.0 mL[font=宋体],加入[/font]4%[font=宋体]苯酚溶液[/font]1 mL[font=宋体]及浓硫酸[/font]2 mL[font=宋体],按上述方法进行操作,测其吸光值,以标准曲线计算样品糖含量[/font][font=宋体]按下式计算中草药多糖的质量浓度与得率。[/font] [img=,300,41]https://ng1.17img.cn/bbsfiles/images/2021/11/202111021041176368_5305_3528941_3.gif!w300x41.jpg[/img]7.[font=宋体]分级[/font][font=宋体]([/font]1[font=宋体])[/font] DEAE-[font=宋体]纤维素的预处理和装柱[/font][font=宋体]将[/font]DEAE-[font=宋体]纤维素用蒸馏水充分浸泡溶胀后,倾倒除去水分,再用[/font]0.5 M NaOH[font=宋体]溶液浸泡[/font]1 h[font=宋体],用蒸馏水反复洗涤至[/font]PH[font=宋体]等于[/font]7[font=宋体]。再用[/font]0.5 M[font=宋体]的[/font]HCl[font=宋体]溶液浸泡[/font]1 h[font=宋体],用蒸馏水洗至中性,真空清除气泡,备用。[/font][font=宋体]装柱时,先将[/font]DEAE-[font=宋体]纤维素沿着玻璃棒缓慢倒入,以防产生气泡。柱子装好后,依次用[/font]5[font=宋体]倍柱体积的蒸馏水、[/font]3[font=宋体]倍柱体积的[/font]1.0 M NaCl[font=宋体]和[/font]5[font=宋体]倍柱体积的蒸馏水进行平衡,流速设定为[/font]20 cm/ h[font=宋体]。[/font][font=宋体]([/font]2[font=宋体])水溶性粗多糖的离子交换柱层析的线性梯度洗脱[/font][font=宋体]称取[/font]50 mg[font=宋体]水溶性粗多糖,溶于[/font]5 mL[font=宋体]蒸馏水中,在已平衡好的[/font]DEAE-[font=宋体]纤维素离子交换柱([/font]1.5 × 14 cm[font=宋体],[/font]Cl[sup]-[/sup][font=宋体]型)上进行上样,先用[/font]100 mL[font=宋体]蒸馏水做流动相进行洗脱,再用[/font]0~1.0 M NaCl[font=宋体]溶液[/font]300 mL[font=宋体]进行线形梯度洗脱,流速[/font]1.0 mL/min[font=宋体],每个试管收集[/font]3 mL[font=宋体]洗脱液,苯酚—硫酸法测定洗脱液中相对的糖含量分布。[/font]8.[font=宋体]纯度鉴定[/font][font=宋体]([/font]1[font=宋体])高效液相色谱法[/font][font=宋体]采用高效液相色谱仪系统,[/font] 10A[font=宋体]检测器,[/font]CLASS-Vp[font=宋体]工作站,[/font]TSK-gel G-3000PWXL[font=宋体]不锈钢色谱柱([/font]7.8 × 300 mm)[font=宋体],柱温为[/font]40℃[font=宋体]。[/font][font=宋体]取各级多糖样品溶于[/font]0.7 M Na2SO4[font=宋体]溶液中,其多糖终浓度为[/font]2 mg/mL[font=宋体],上样[/font]20 μL[font=宋体],流动相为[/font]0.7 M Na2SO4[font=宋体]溶液,流速为[/font]0.5 mL/min[font=宋体]。[/font][font=宋体]([/font]2[font=宋体])紫外光谱分析[/font][font=宋体]将水溶性粗多糖各级分多糖样品配成[/font]0.1 mg/mL[font=宋体]的溶液,用[/font]752PC[font=宋体]型紫外可见分光光度计于[/font]200-400 nm[font=宋体]处扫描检测。[/font][font=宋体]([/font]3[font=宋体])旋光仪分析[/font][font=宋体]不同的多糖具有不同的比旋度,它们在不同浓度的乙醇中具有不同溶解度,所以,如同一多糖水溶液经不同浓度的乙醇沉淀所得的沉淀物,具有相同比旋度,则证明该多糖为均一组分。[/font][font=宋体]将评估多糖样品溶于水,成为近似半饱和溶液,置于磁力搅拌器上,在搅拌下加乙醇,使溶液中乙醇浓度达到[/font]20%[font=宋体],搅拌片刻,使沉淀完全,离心得沉淀。上清液中再继续滴加乙醇,使溶液中乙醇浓度达[/font]40%[font=宋体],所产生的沉淀再经离心。前后两次沉淀,分别干燥后在相同条件下测定其水溶液的比旋度。[/font][font=宋体]将[/font]10 mL5%[font=宋体]饱和糖液用国产[/font]WXG[font=Symbol]-[/font]6[font=宋体]型自动旋光仪,钠灯光源,以蒸馏水调零点,[/font]1dm[font=宋体]管室温下测定。[/font]
AKATA制备型液相色谱蛋白分析仪纯化蛋白步骤很简单的,比较适合初学者。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=113913]AKATA制备型液相色谱蛋白分析仪纯化蛋白步骤[/url]
制备色谱可以分离纯化地质样品中的金属离子吗
看书时遇到了个问题,想请教各位大侠:制备液相色谱与半制备液相色谱有何区别,他们各自的原理是什么?在用途方面有何差异?
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=31404]正相液相制备色谱分离纯化三七叶甙中人参皂甙单体Rb3[/url]
常用分离纯化技术研究开发 1) 高效液相色谱填料和色谱柱2) 手性色谱固定相的制备与应用3) 手性药物及其中间体的拆分与转化4) 生物磁分离技术和产品5) 高通量分离纯化技术与装置6) 蛋白质组分析技术与产品7) 高效毛细管电泳分离分析技术 1) 高效液相色谱填料和色谱柱高效液相色谱法(HPLC)是六十年代末发展起来的化学分离分析方法。在这一方法中,微米级的多孔颗粒被用作固定相,而有机溶剂或水溶液被用作流动相。 样品溶液在高压泵的驱动下,流过装填固定相的色谱柱。 在流动过程中,化合物在流动相与固定相之间多次分配,由于分配系数的差异,化合物在固定相中的滞留时间有所不同,因此可利用HPLC来实现对混合物的分离。色谱柱是HPLC的核心部件,由不锈钢空管和填充其中的固定相组成。为了分离不同类型的化合物,一台HPLC通常需要配备若干不同类型的色谱柱。色谱柱又是实验室消耗品,因为它的使用寿命是一定的。样品污染,流动相侵蚀和柱结构变化等问题可能造成色谱柱的损坏。 因此,需要根据使用情况定期更换色谱柱。HPLC中使用的色谱柱种类繁多。 根据色谱填料表面功能团的特性,色谱柱可分成正相柱,反相柱,手性柱,离子交换柱,亲和柱等。而根据色谱柱的几何尺寸,色谱柱又可分成毛细管柱,微型柱,分析柱,半制备柱,制备柱等。使用反相柱的HPLC是目前所有色谱方法中应用最广泛的一种,在食品分析,药物分析,环境分析,药品质量控制,临床医疗诊断,天然产物活性成分鉴定和环境毒物监测等方面都有着广泛的应用。而制备型HPLC更是当前分离纯化手性药物,抗癌药物如紫杉醇,合成核酸,合成多肽,重组蛋白等生物分子的不可或缺的工具。近年来,制药工业尤其是生物制药工业在我国迅速发展,国家对药品质量管理的要求不断提高,这些因素决定了未来几年我国的高效液相色谱产品市场将进入一个高速扩张期。我国的液相色谱分离纯化产品的市场容量当在亿元人民币以上,而目前这一市场主要为安捷伦等外国公司所垄断。我们开展了以球型多孔硅胶为基质的HPLC色谱填料的合成研究,开发了具有自主知识产权的硅胶生产工艺路线,并对硅胶的硅烷化反应进行了系统研究,建立起制备反相液相色谱固定相的优化条件,由我们开发的技术所生产的球型多孔硅胶具有粒径分布均匀,孔径分布范围窄,比表面积可控,表面官能团浓度高和机械强度高等特点,完全能满足现代液相色谱的要求。在此基础上,我们又研究了高效液相色谱柱制备技术,优化了高压装柱法中匀浆液、顶替液的组成,所生产的色谱柱达到或超过了国外同类产品的性价比。欢迎国内企业来人来电洽谈合作,与名校携手,共同打造色谱产品的中国品牌。file:///C:\Users\我是发~1\AppData\Local\Temp\ksohtml\wps_clip_image-11116.png峰号 样品拖尾因子塔板数/米1 丙酮1.26678722对氯硝基苯1.08698843甲苯1.02717284萘1.0068072 *TOP*2) 手性色谱固定相的制备与应用手性在近十年来成为现代制药工业的主要关注点,这主要归因于人们日益增强的认识:外消旋体药物中的一对手性体可能具有不同的药理活性、药代动力学和药效学效应。一个异构体也许能产生所希望的治疗活性,而另一个则可能是无效的,甚至是有害的。最
[求助] 我在分析型液相中已找到适合的分离条件,当放大转到制备液相中时重现性不好,请大家指教!!!
文件为caj格式的:[b]高效制备液相色谱柱技术的研究进展[/b]摘 要 本文概述了高效制备液相色谱柱的柱型结构、填料以及柱填充方法等研究的最新进展,讨论了制备柱与分析柱的不同特征,对目前普遍使用的压缩型制备柱的类型!结构及填充方法作了较为全面的评述,总结比较了工业化制备色谱填料不同于分析色谱填料的特点,探讨了高效制备液相色谱柱技术的应用和发展前景。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=26347]高效制备液相色谱柱技术的研究进展[/url]
具体的方法随各中草药的性质不同而异,以后将通过实例加以叙述,此处只作一般原则性的讨论。 (一)溶剂分离法:一般是将上述总提取物,选用三、四种不同极性的溶剂,由低极性到高极性分步进行提取分离。水浸膏或乙醇浸膏常常为胶伏物,难以均匀分散在低极性溶剂中,故不能提取完全,可拌人适量惰性填充剂,如硅藻土或纤维粉等,然后低温或自然干燥,粉碎后,再以选用溶剂依次提取,使总提取物中各组成成分,依其在不同极性溶剂中溶解度的差异而得到分离。例如粉防己乙醇浸膏,碱化后可利用乙醚溶出脂溶性生物碱,再以冷苯处理溶出粉防己碱,与其结构类似的防己诺林碱比前者少一甲基而有一酚羟基,不溶于冷苯而得以分离。利用中草药化学成分,在不同极性溶剂中的溶解度进行分离纯化,是最常用的方法。 广而言之,自中草药提取溶液中加入另一种溶剂,析出其中某种或某些成分,或析出其杂质,也是一种溶剂分离的方法。中草药的水提液中常含有树胶、粘液质、蛋白质、糊化淀粉等,可以加入一定量的乙醇,使这些不溶于乙醇的成分自溶液中沉淀析出,而达到与其它成分分离的目的。例如自中草药提取液中除去这些杂质,或自白及水提取液中获得白及胶,可采用加乙醇沉淀法;自新鲜括楼根汁中制取天花粉素,可滴人丙酮使分次沉淀析出。目前,提取多糖及多肽类化合物,多采用水溶解、浓缩、加乙醇或丙酮析出的办法。 此外,也可利用其某些成分能在酸或碱中溶解,又在加碱或加酸变更溶液的pH后,成不溶物而析出以达到分离。例如内酯类化合物不溶于水,但遇碱开环生成羧酸盐溶于水,再加酸酸化,又重新形成内酯环从溶液中析出,从而与其它杂质分离;生物碱一般不溶于水,遇酸生成生物碱盐而溶于水,再加碱碱化,又重新生成游离生物碱。这些化合物可以利用与水不相混溶的有机溶剂进行萃取分离。一般中草药总提取物用酸水、碱水先后处理,可以分为三部分:溶于酸水的为碱性成分(如生物碱),溶于碱水的为酸性成分(如有机酸),酸、碱均不溶的为中性成分(如甾醇)。还可利用不同酸、碱度进一步分离,如酸性化台物可以分为强酸性、弱酸性和酷热酚性三种,它们分别溶于碳酸氢钠、碳酸钠和氢氧化钠,借此可进行分离。有些总生物碱,如长春花生物碱、石蒜生物碱,可利用不同rH值进行分离。但有些特殊情况,如酚性生物碱紫董定碱(corydine)在氢氧化钠溶液中仍能为乙醚抽出,蝙蝠葛碱(dauricins)在乙醚溶液中能为氢氧化钠溶液抽出,而溶于氯仿溶液中则不能被氢氧化钠溶液抽出;有些生物碱的盐类,如四氢掌叶防己碱盐酸盐在水溶液中仍能为氯仿抽出。这些性质均有助于各化合物的分离纯化。 (二)两相溶剂萃取法: 1.萃取法:两相溶剂提取又简称萃取法,是利用混合物中各成分在两种互不相溶的溶剂中分配系数的不同而达到分离的方法。萃取时如果各成分在两相溶剂中分配系数相差越大,则分离效率越高、如果在水提取液中的有效成分是亲脂性的物质,一般多用亲脂性有机溶剂,如苯、氯仿或乙醚进行两相萃取,如果有效成分是偏于亲水性的物质,在亲脂性溶剂中难溶解,就需要改用弱亲脂性的溶剂,例如乙酸乙酯、丁醇等。还可以在氯仿、乙醚中加入适量乙醇或甲醇以增大其亲水性。提取黄酮类成分时,多用乙酸乙脂和水的两相萃取。提取亲水性强的皂甙则多选用正丁醇、异戊醇和水作两相萃取。不过,一般有机溶剂亲水性越大,与水作两相萃取的效果就越不好,因为能使较多的亲水性杂质伴随而出,对有效成分进一步精制影响很大。 两相溶剂萃取在操作中还要注意以下几点: 1)先用小试管猛烈振摇约1分钟,观察萃取后二液层分层现象。如果容易产生乳化,大量提取时要避免猛烈振摇,可延长萃取时间。如碰到乳化现象,可将乳化层分出,再用新溶剂萃取;或将乳化层抽滤,或将乳化层稍稍加热;或较长时间放置并不时旋转,令其自然分层。乳化现象较严重时,可以采用二相溶剂逆流连续萃取装置。 2) 水提取液的浓度最好在比重1.1~1.2之间,过稀则溶剂用量太大,影响操作。 3) 溶剂与水溶液应保持一定量的比例,第一次提取时,溶剂要多一些,一般为水提取液的1/3,以后的用量可以少一些,一般1/4-1/6。 4)一般萃取3~4次即可。但亲水性较大的成分不易转入有机溶剂层时,须增加萃取次数,或改变萃取溶剂。 萃取法所用设备,如为小量萃取,可在分液漏斗中进行;如系中量萃取,可在较大的适当的下口瓶中进行。在工业生产中大量萃取,多在密闭萃取罐内进行,用搅拌机搅拌一定时间,使二液充分混合,再放置令其分层;有时将两相溶液喷雾混含,以增大萃取接触,提高萃取效率,也可采用二相溶剂逆流连续萃取装置。 2.逆流连续萃取法:是一种连续的两相溶剂萃取法。其装置可具有一根、数根或更多的萃取管。管内用小瓷圈或小的不锈钢丝圈填充,以增加两相溶剂萃取时的接触面。例如用氯仿从川楝树皮的水浸液中萃取川楝素。将氯仿盛于萃取管内,而比重小于氯仿的水提取浓缩液贮于高位容器内,开启活塞,则水浸液在高位压力下流入萃取管,遇瓷圈撞击而分散成细粒,使与氯仿接触面增大,萃取就比较完全。如果一种中草药的水浸液需要用比水轻的苯、乙酸乙酯等进行萃取,则需将水提浓缩液装在萃取管内,而苯、乙酸乙酯贮于高位容器内。萃取是否完全,可取样品用薄层层析、纸层析及显色反应或沉淀反应进行检查。 3.逆流分配法(CounterCurrentDistribution,CCD):逆流分配法又称逆流分溶法、逆流分布法或反流分布法。逆流分配法与两相溶剂逆流萃取法原理一致,但加样量一定,并不断在一定容量的两相溶剂中,经多次移位萃取分配而达到混合物的分离。本法所采用的逆流分布仪是由若干乃至数百只管子组成。若无此仪器,小量萃取时可用分液漏斗代替。预先选择对混合物分离效果较好,即分配系数差异大的两种不相混溶的溶剂。并参考分配层析的行为分析推断和选用溶剂系统,通过试验测知要经多少次的萃取移位而达到真正的分离。逆流分配法对于分离具有非常相似性质的混合物,往往可以取得良好的效果。但操作时间长,萃取管易因机械振荡而损坏,消耗溶剂亦多,应用上常受到一定限制。 4.液滴逆流分配法:液滴逆流分配法又称液滴逆流层析法。为近年来在逆流分配法基础上改进的两相溶剂萃取法。。对溶剂系统的选择基本同逆流分配法,但要求能在短时间内分离成两相,并可生成有效的液滴。由于移动相形成液滴,在细的分配萃取管中与固定相有效地接触、摩擦不断形成新的表面,促进溶质在两相溶剂中的分配,故其分离效果往往比逆流分配法好。且不会产生乳化现象,用氮气压驱动移动相,被分离物质不会因遇大气中氧气而氧化。本法必须选用能生成液滴的溶剂系统,且对高分子化合物的分离效果较差,处理样品量小(1克以下),并要有一定设备。应用液滴逆流分配法曾有效地分离多种微量成分如柴胡皂甙原小檗碱型季铵碱等。液滴逆流分配法的装置,近年来虽不断在改进,但装置和操作较繁。目前,对适用于逆流分配法进行分离的成分,可采用两相溶剂逆流连续萃取装置或分配柱层析法进行。

[color=#333333]制备柱是高效液相色谱是一种分析方法,制备色谱是一种分离纯化手段。我们学习了太多的理论,但是对制备柱知之甚少,我从相关网站上找了两张Kromasil制备柱的图片。[/color][color=#333333]制备柱和分析柱的最大区别就是柱容量。普通液相色谱柱的直径约为0.5厘米,而制备色谱柱的直径多为1到10厘米。制备柱所需的填料是分析柱的数倍,甚至几百倍。[/color][color=#333333][img=,280,280]http://ng1.17img.cn/bbsfiles/images/2018/07/201807031307373153_9331_2428063_3.jpg!w280x280.jpg[/img][img=,254,241]http://ng1.17img.cn/bbsfiles/images/2018/07/201807031307482187_2703_2428063_3.png!w254x241.jpg[/img][/color]
用中压制备液相色谱是否可以有效地分离二甲苯和石油类烷烃。
一. 逆流色谱技术简介现代逆流色谱技术起源于上世纪50年代的逆流分溶法(Counter Current Distribution, CCD),它利用不同物质在所选择的两相溶剂中的分配系数不同而通过多次逆流分溶对物质进行分离。它采用数百个分离管进行操作,每一次操作后,上层液体被转移至盛有新的下层溶剂的分离管中,而往原分离管中加入新的上层溶剂,看起来好似两相的液体以相反的方向流动,故称为逆流分溶法。逆流分溶法存在许多缺点,如使用易破碎的玻璃仪器,分离时间长,需要连续稀释样品等。但与液相色谱相比,它无需固体作固定相,从而避免了因此而带来的一系列问题。因此,在CCD基础上发展起来的逆流色谱(Counter Current Chromatography, CCC)在采用了与液相色谱相似的连续洗脱、检测和分布收集技术后从上世纪70年代开始得到迅速的发展,并在天然和合成化合物的分离纯化中发挥了日益重要的作用。上世纪70年代出现的液滴逆流色谱(Droplet Counter Current Chromatography, DCCC)使流动相形成液滴,通过作为固定相的液柱而达到分离纯化的目的。其装置主要由输液部分、检测收集部分和玻璃管液柱部分(300-500根60cm X 1.8mm的玻璃管)组成。由于流动相形成液滴,在细的玻璃管中与液体固定相有效地接触,摩擦不断形成新的表面,促进溶质在两相溶剂中的分配,所以分离效果好,而且不产生乳化现象。对于易氧化的物质,还可用氮气驱动流动相。采用DCCC分离纯化了许多包括中草药和抗生素在内的天然产物如柴胡皂甙和短杆菌肽, 短杆菌酪素和四环素等。液滴逆流色谱解决了操作自动化的问题,但仍存在分离时间长,使用易破碎的玻璃管,分离度还不高等问题。逆流色谱技术的重大突破出现在上世纪80年代,根据被分离混合物的理化特性,选择二元或多元的两相溶剂体系,以上相或下相为固定相,将其注满色谱柱后使色谱柱作特定的高速旋转运动,并用由此产生的离心力场支撑柱内的液体固定相,然后以另相为流动相,携带溶解的混合物由输入泵推入色谱柱,穿过两个液相对流的管柱,各组分根据在两相中的分配系数不同而得到分离。根据离心力场的不同可将现代逆流色谱分为离心分配色谱(Centrifugal Partition Chromatography, CPC),也称盘管行星离心色谱(Coil Planet Centrifuge, CPC)和高速逆流色谱(High Speed Counter Current Chromatography, HSCCC),前者属流体静力平衡系统,色谱柱由一系列刻在圆盘或圆筒内的导管相联的柱体组成,通过单轴旋转产生恒定的重力场,两个旋转密封的接口分别连接流动相的进口和出口;后者属流体动力平衡系统,由聚四氟乙烯软管绕制成的色谱柱除绕离心轴旋转外,还围绕自轴旋转,产生变化的重力场,并采用无旋转密封的连接方式。分离时两相液体被剧烈振动的离心力场依其界面特征被甩成极细的微粒,样品各组分在两相微粒的表面上分配并在微粒振荡与对流的环境中有效传递,相当于把通常的溶剂萃取高效(13次/秒以上)、自动、连续地予以完成。泡沫逆流色谱(Foam Counter Current Chromatography, Foam CCC)技术是在HSCCC的基础上发展起来的。使用时,氮气和流动相同时从相反方向注入管柱中形成气体和流动相的逆流,然后从盘管中部注入的混合物根据形成泡沫的能力得到分离,易形成泡沫的的组分随[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]被洗脱收集在泡沫流出部分,而其它组分则随流动相流出。在盘管行星离心色谱基础上还发展了交叉轴盘管行星离心色谱(Cross-axis Coil Planet Centrifuge, X-axis CPC),这种仪器在使用中产生一种行星式运动,使得盘管支架在围绕离心中轴转动(公转)的同时还沿着自己的水平方向轴旋转(自转),使得部分的离心力矢量作用于盘管的半径方向,以防止因两相乳化而降低固定相保留率的现象出现。因此,X-axis CPC大大稳定了固定相的保留率,特别适用于大量制备性分离纯化。现代逆流色谱技术为化合物的分离纯化提供了一个新的手段,与HPLC等液-固色谱技术比较,由于分离原理不同,二者间存在很强的互补性。它无需固体作固定相,不存在固体对样品组分的吸附、玷污、变性、失活、拖尾等现象,能实现很高的回收率,节省昂贵的材料消耗和溶剂消耗(HPLC的1/10以下),运行使用的后续投入较低。逆流色谱在无需更换不同极性的色谱柱情况下,通过提高极性溶剂或非极性溶剂比例的方法,可以实现流动相从弱极性到强极性或相反的转化。由于色谱柱容积大,无填料,柱内空间全部是有效空间,因此,样品负载能力强,制备量大,重现性好。实验室规模的盘管总体积为100mL的逆流色谱仪一次可分离0.5-2克的粗品,而3000mL容量的制备型逆流色谱仪一次可分离15-60克的粗品。但是,与[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]和高效液相色谱等相比,逆流色谱的分离效率即理论塔板数还不高(一般在1000以下),一次分离所需时间还较长(以小时计),因此,还不宜用于组成复杂的混合物的全谱分离分析。逆流色谱技术在基本原理以及溶剂系统选择等方面还有待于进一步的普及、研究、开发与应用。目前,HSCCC等技术在生物化学、医药学、农业、环境、材料、化工、海洋生物以及无机离子等众多领域已得到成功应用,1996年美国出版的《High-Speed Countercurrent Chromatography》一书被选编为著名的分析化学丛书第132卷,2000年9月在英国Brunel大学召开了逆流色谱技术第一届国际学术会议,每年一度的国际分析化学与应用光谱学学术会议上,都设有CCC的专题组,“Journal of Chromatography” ,“Journal of Liquid Chromatography” 等重要学术刊物都有这一技术的论文发表。我国在CCC技术及其应用研究方面与国际发展同步,1980年研制出了我国第一台逆流色谱仪,并用于国产抗敌素成分的分离与分析检定,发表了一大批用HSCCC等分离制备中草药和茶叶等天然产物活性成分的论文,引起国际同行的瞩目,2002年在北京召开了逆流色谱技术的第二届国际学术会议。但是,在逆流色谱技术应用于抗生素的分离纯化方面,我国与国际上发展趋势相比还存在很大差距,相关论文甚少,因此,在我国开展高速逆流色谱技术分离纯化抗生素的工作有着广阔的应用和发展前景。二. 溶剂选择无论是用HPLC或CCC技术分离混合物,分离度(Rs)是一个很重要的参数,如下图所示,在HPLC中,提高分离度是通过使峰形变窄的方法达到的,而在CCC或CPC中,则是通过改进选择性来实现的,这种选择性主要取决于样品在两相溶剂中的分配系数。因此,溶剂系统的选择在CCC技术中尤为重要。 选择溶剂时要考虑到样品的极性、溶解度、电荷态和形成复合物的能力等,溶剂体系的沉降时间应小于30秒,以得到满意的固定相保留率。测定方法如下,各取2毫升平衡后的上相和下相液体移入一个5毫升的刻度玻璃管中,密封上下摇动5次后静置于水平面上并测定两相分层的时间即沉降时间。样品的分配系数K值(K=上相中样品浓度/下相中样品浓度,可由HPLC方法得出)最好在1左右,一般在0.2到2之间。以上相作固定相时为例,若K《《1,样品很快随流动相流出,达不到分离效果;若K》》1,样品出峰时间拉长,形成宽峰。由于CCC的理论塔板数在800左右,因此要得到高的分离度,样品各组分间的分离因子( , 各组分的K值之比)应大于1.5。此外,两相溶剂的体积应尽量相同以避免溶剂的浪费,溶剂最好挥发性强,这样完成操作后只要将洗脱液浓缩即可得到纯样品。 选择溶剂体系时,首先选出一个能使样品全部溶解的溶剂体系,然后调整各溶剂的比例使得被分离各组分满足K值和 值的要求,以提高分离度。可以采用相图来研究改变某一相的组成对另一相组成的影响,Sø rensen等人对近百种三元溶剂相图研究后,总结归纳出三类溶剂体系:乙酸乙酯—正丁醇—水(EtOAc—BuOH—H2O),适用于极性弱的样品;水—二甲亚砜—四氢呋喃(H2O—DMSO—THF),适用于极性强的难溶性样品如两性霉素B;氯仿—甲醇—水(CHCl3—MeOH—H2O),适用于大部分样品。此后又发展了其它通用的多元溶剂体系如正戊烷—乙酸乙酯—甲醇—水(Heptane—EtOAc—MeOH—H2O)体系和正戊烷—甲醇—甲基叔丁基醚—甘醇二甲醚—水(Heptane—MeOH—MtBE—Glyme—水)体系等。常用溶剂体系的选择可参考表1,首先根据样品的理化特性选出最佳溶剂,然后在左右两栏中再选择相应的数种溶剂,以组成选择性最好的多元溶剂体系。
仪器信息网最新消息 2009.09.02JAI(日本分析工业株式会社)最新推出全自动循环制备液相色谱LC-9110NEXT/LC-9130NEXT型全自动循环制备液相色谱独特的机身一体化设计,采用8.4英寸手触液晶交互界面,可以进行从输液到制备分离的全部设定。其革新的结构布局设计,将手动进样器至于设备之外,有效缩短了更换密封圈所需的时间。同时,输液泵和检测器等也可自前端取出,大大提升了仪器的可维护性。 LC-9110NEXT/LC-9130NEXT型全自动循环制备液相色谱除了具有JAI特色的循环功能外,还具有[color=#DC143C]自动重复操作、自动清洗、序列进样等功能,完美实现了操作自动化,同时也极大简化了日常清洗维护的工序[/color]。此外,LC-9110NEXT/LC-9130NEXT还具有已经获得专利的逆流防止功能,完全[color=#DC143C]解决了循环制备HPLC高背压对于检测器的损害问题以及溶剂峰的逆流问题[/color],保证样品不会在检测器和色谱柱等地方发生损失。
菌发酵液,过3K超滤膜,取3K以下的滤液过制备液相,目的是找出一种活性物质,但完全不知道这是一种什么物质,有可能是有机酸也有可能是小分子肽,过制备液相用的是甲醇-三氟乙酸,30min甲醇从10%-100%.。用的C18反相柱。出来的峰形很差,分不太开,但基本确定物质在前面4-7分钟左右出来的,极性比较大的物质。请问应该怎样改变条件,让峰形好一些,或者有没有其他的分离纯化思路?谢谢了!!!!
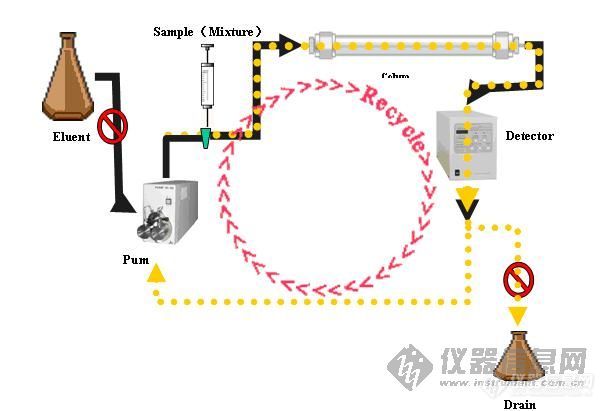
循环制备液相色谱就是较之平常的液相色谱多了个循环功能,对于一次过柱不能达到较好的分离效果的物质循环多次过柱,变相的提高了柱效,使样品达到较好的分离效果。其流程路如下:[img]http://ng1.17img.cn/bbsfiles/images/2009/08/200908140931_165538_1622597_3.jpg[/img] 由于采用了循环技术,其分离效果常规液相色谱有较大提高,对于手性物质及同分异构体也能达到很好的分离效果。对于一般样品省去了摸索最佳溶剂配比的过程,通过多次循环就能达到非常好的分离效果。利用循环功能对端基不同的样品进行分离样品为1-Benzyl-carboethoxy-4-piperidonehydrochloride (A)和1-Benzylcarbomethoxy-4-piperidonehydrochloride的混合物[img]http://ng1.17img.cn/bbsfiles/images/2009/08/200908140933_165539_1622597_3.jpg[/img]
[font=微软雅黑][size=16px]制备色谱是以分离出纯物质为目的的色谱系统,分析色谱是以分析出样品组分信息为目的的色谱系统,基于他们目的的不同,制备色谱相对于分析色谱有很多不同特征,不能简单等同。[/size][/font] [font=微软雅黑][size=16px]当我们在实验室中想得到纳克乃至毫克级的纯物质时,稍微改装下分析型色谱系统就能简单轻松的完成,不过,若所需制备的纯品量很大,此时,再用分析型色谱系统分离纯化,可以预见这将是一场“灾难”。[/size][/font] [size=16px][font=微软雅黑]制备色谱常用的色谱模式有低压,中压,高压三种,以应对不同类型和不同纯度要求的样品的分离,同时尽可能减少成本。[/font][/size] [size=16px][font=微软雅黑]低压:一般而言,低压适合易分离化合物,但分离时间长很容易造成敏感化合物分解。[/font][/size] [size=16px][font=微软雅黑]Flash:Flash是应对低压分离时间长而出现的替代方法,尽管其分辨率不及中压,仍常被用于简单的分离问题。[/font][/size] [size=16px][font=微软雅黑]中压:中压一般采用恒流泵提供恒定的流动相流速,填料颗粒更小,分辨率更高,耐受更高压力和更快流速,同时操作与低压和Flash基本一致,而苏州汇通研发的中压玻璃层析柱,可以完美转接到各类低压和Flash系统,进一步为您节约仪器成本。[/font][/size] [size=16px][font=微软雅黑]高压:高压通常在分离制备的最后阶段采用,应用于分离困难的样品,纯度甚至能达到99.9%。[/font][/size] [size=16px][font=微软雅黑]在开发制备色谱方法时,很多人都存在这样的错误认识,认为制备色谱的流动相纯度不需要优先考虑,分析用色谱纯,制备马马虎虎就行了,不过我们从另一方面思考下,制备过程中流动相的使用量一般都很大,其中的杂质积聚后,对产品的纯度影响将会十分可观,因此,对于杂质的流向需要与纯化过程关联起来,使用纯度较高的流动相是必要的。[/font][/size]
最近公司打算接一个甘草深加工开发项目, 打算从甘草中分离纯化制备甘草酸, 甘草多糖还有甘草酮类物质。 前期工作已经开始进行, 现在需要采购一台制备型[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url], 用来分离和纯化甘草黄酮中的异甘草素, 预算还可以, 求推荐型号。 谢谢大家了

高效液相色谱法对金黄色葡萄球菌肠毒素B的快速分离纯化与检测 以金黄色葡萄球菌肠毒素为代表的一类蛋白质可以导致人类及其他灵长类动物的呕吐和腹泻,本实验开发了一种两步高效液相色谱法快速纯化金黄色葡萄球菌肠毒素B(SEB)的方法,首先将无菌的滤液通过反相色谱柱进行吸附,通过一个梯度洗脱的溶剂系统获得SEB,首先采用含有醋酸铵的乙腈水溶液洗脱,然后再用三氟乙酸(TFA)水溶液洗脱,以除去其他杂质。随后用含有TFA的乙腈水溶液将吸附的SEB洗脱下来。样品再经过阳离子交换色谱柱进行纯化。本方法可以得到初始滤液中40%-50%的SEB,通过十二烷基硫酸钠聚丙烯酰胺凝胶电泳分离免疫印迹法分析表明,经HPLC纯化的SBE免疫性质和生化性质同标准的SEB相似。 金黄色葡萄球菌肠毒素为金黄色葡萄球菌的某些菌株产生的一类蛋白质,能引起人类及其他灵长类动物的食物中毒反应,症状以呕吐和腹泻为主。根据血清特异性抗体反应将他们分为几类:金黄色葡萄球菌肠毒素A(SEA),SEB,SEC,SED,SEE等9个型。除了能引起食物中毒,还有超抗原作用,能够提高内毒素休克的风险。SEA,SEB,SEC这三种毒素的理化性质(包括分子大小,碱基序列,基本结构)已经被广泛研究。金黄色葡萄球菌肠毒素具有相似的结构,具有单个多肽链和一个二硫键。 文献中金黄色葡萄球菌肠毒素的纯化一般是阳离子交换色谱与凝胶色谱交替使用的多步骤过程。这些步骤主要用于色谱或电泳中纯毒素单个蛋白质分析,对于金黄色葡萄球菌肠毒素分子模式的了解对于我们了解其在发病中的作用非常重要。这些结构与功能的研究也为我们更加简单和快速的纯化和分析毒素提供了参考。材料和方法:金黄色葡萄球菌株S6的培养粗滤液作为SEB的初始来源,菌株S6是SEB的高产菌株。菌株在1L的培养液(包含有1%的蛋白胨,0.5%的酵母提取物,0.5%的NaCI)中培养,并于37℃条件下摇床培养24小时。通过离心(6000转/min,30min)获得除菌后的培养液,然后经过0.45um滤膜过滤得到滤液。色谱条件:分析性高效液相:安捷伦液相1200,菲罗门液相色谱柱4.6﹡150﹡5u,流速:0.8ml/min,进样量1ml,http://ng1.17img.cn/bbsfiles/images/2014/09/201409301407_516501_2206222_3.png制备型高效液相:大连依利特,色谱柱SinoChrom ODS-AP ,10μm20*250mm;流速:20ml/min;制备型阳离子色谱柱为TSK-GELG3000SWXL5μm,7.8×300m流动相A:0.01 M醋酸铵pH值=5.5;;流动相B为乙腈;流动相C为0.1%三氟乙酸(TFA);流动相D为乙腈含有0.1%TFA。试剂均为色谱纯。http://ng1.17img.cn/bbsfiles/images/2014/09/201409301408_516502_2206222_3.png制备色谱图如下:http://ng1.17img.cn/bbsfiles/images/2014/09/201409301409_516503_2206222_3.jpg制备第二步:制备型阳离子色谱柱为TSK-GELG3000SWXL5μm,7.8×300mhttp://ng1.17img.cn/bbsfiles/images/2014/09/201409301410_516505_2206222_3.png制备色谱图如下:http://ng1.17img.cn/bbsfiles/images/2014/09/201409301409_516504_2206222_3.jpg纯化后的样品于12%聚丙烯酰胺-SDS凝胶中进行电泳,电泳后进行染色或蛋白质印迹分析结果与讨论:本试验探索出一条高效液相色谱法对金黄色葡萄球菌肠毒素B的分离纯化方法,效果明显。
目前,新药研发市场竞争如火如荼,大小药物研发公司都在奋力一搏,但是真正能成功的如凤毛麟角。本公司提供制备色谱分离纯化包括SFC手性、非手性服务,反相制备,杂质制备服务及技术咨询服务可以真正加快你得到你的目标化合物的速度。欢迎大家跟帖
制备液相色谱的上样量与什么有关
制备型高效液相色谱系统的应用领域制备型高效液相色谱系统主要应用在植化、合成、制药、生物及生化等领域的产品的提取及纯化工作中。在不同的工作领域中,组份的提取和纯化量的差异是很大的。在生物技术领域中,酶的分离是微克级;在植化和合成化学领域中,为了鉴别未知成份并进行结构测定,需要得到一至若干毫克的纯品;在药品和医药学测试中,需要克级的标准品和对照品;在当今的工业级提纯中,制药成份往往需要千克级的提取。制备型高效液相的应用领域可以归纳在下表中。 成份量:所在领域 微克: 生物技术领域的酶的分离、生物学和生化学测试 毫克: 结构描述和特征鉴定,包括:生产中的副产品、生物矩阵的新陈代谢产物、天然产物 克级: 对照品(分析标准)毒物学分析所需组份:高纯品中的主要成份、副产品的分离提取 千克级:工业规模生产,活性成份,药物 制备方法的发展和扩大规模的计算 在分析液相中色谱柱的典型进样量是微克级,甚至更低。样品量和固定相之比有的甚至小于1:100000。进样体积一般来说都大大小于色谱柱体积(小于1:100)。 在这种条件下,会达到很好的分离效果,峰形尖锐并且很对称。而在制备液相中,最大的区别就是超量进样。其结果,超量进样的方法和分析方法的放大将在下章内介绍。 吸附变化线 分析液相的目的是给一种组份定性、定量。重要的色谱参数有溶解度、峰宽和峰的对称性。如果进样量越来越多,峰高和峰面积会增加,但峰的对称性和容量因子保持不变。如下图。 在分析液相中,最佳的峰形应是一条高斯曲线。峰的标准背离 бV 描述了其对称性和与高斯曲线的相似性。容量因子是与一种不保留物质的保留时间t0相关的保留时间。 如果将超过一定量的样品注射进色谱柱,吸附变化线就会成非线性。这意味着峰形会变的不再对称,表现为严重的拖尾和容量因子的缩小。如下图。在制备液相中,这种效果称作浓缩超量进样。在一些情况中,根据进样量的增加,容量因子也相应变大,并造成很强的前峰。既然吸附变化线取决于组份的多少,那么液相色谱柱的载样能力就必须根据不同的制备液相实验来决定。 色谱柱载样和超量载样 大样品量的纯化有两种可行的方法:分析系统的放大或色谱柱超量载样。分析系统的放大意味着使用直径更大的制备柱、更高的流速和根据色谱柱的长度增加进样量并保持样品浓度不变。峰形仍会保持尖锐而对称。这种方法需要大型的色谱柱和大量的溶剂来分离较少的样品,因此这种方法是不经济的。 因此色谱柱超量载样,暨在相同的分析条件下超量进样通常是一种很好的选择。使用色谱柱超量载样的方法,在分析柱上甚至可以进行毫克级的分离。但更大 量的样品分离就需要整个系统的放大。色谱柱超量载样可以通过两钟方法进行— 浓缩法和体积超载法。 在浓缩法中,样品的浓度会提高,但进样体积保持不变。容量因子k’降低,同时峰形从高斯曲线变为矩形。如下图。浓缩法超量载样只有在样品组份在流动相中具有良好的溶解性的条件下才有可能采用。 如果样品组份的溶解性很差,浓缩法超量载样不能使用。同时更多的样品体积注射到色谱柱中,这种技术称作体积法超量载样。超过一定的进样体积,峰高不变,但峰变宽并且呈矩形。在制备液相中浓缩法超量载样比体积法超量载样更受欢迎,因为可被分离的样品量更高。既然组份的溶解性通常是一个限制因素,所以两钟超量载样技术通常被结合起来使用。两种技术的概览浓缩法超量载样 体积法超量载样 取决于组份在流动相中的溶解性 取决于进样体积 吸附变化线的制备部分 吸附变化线的分析部分 生产效率决定于选择性 生产效率决定于制备柱直径 受固定相粒度大小的影响不大 需要小颗粒填料 方法的放大 浓缩法超量载样和体积法超量载样都会导致组份溶解性的降低。既然组份的分离需要一定的溶解性,那么在放大分析方法的时候,优化溶解性、特别是选择性就是一项很重要的工作。 因为选择性和超量载样潜力是相互依靠的,选择性的提高会提高一次运行中所分离的样品量,因此从分析方法到制备方法的放大和方法的优化需要三个步骤。 1. 优化分析方法的选择性。2. 在分析柱上进行超量载样。3. 放大到制备柱 制备型高效液相色谱的目的 判断制备型高效液相色谱使用的结果有三个重要参数:产品的纯度、产量和生产效率。三个参数之间是相对独立的,因此很难同时使用这三个参数来优化制备型高效液相色谱方法。见图形6。 色谱图1显示在制备型高效液相色谱的使用中有很高的生产效率,但是两种组份的分离效果却是很差的。这种方法很可能得到两种组份的高纯品,但是产量和收率却是很低的。 在色谱图2中峰有很好的分离,因此这种方法可以得到两种组份的高纯品和高产量,但是生产效率却很低。 色谱图3中的情况是三个参数综合后得到的最优化的结果。峰在基线上被完全分开,这使得产品纯度、产量和生产效率都达到最高。 在实际应用中,每个参数的重要性都是不同的。如为了进行活性或药物测试,某种组份必须被完全单独提取,那么组份的纯度是最重要的参数,产量和生产效率是其次的。如果某种合成中间体必须被纯化,并且需要有足够的量为下一步合成作准备,那么纯度就不是最重要的了。而生产效率在这种情况下就是个首先需要解决的问题,因为其直接关系到完成整个合成工作的进程和速度。同时产量也是很重要的,因为高价值组份的损失需要控制在最少的范围内。