需要将石英玻璃片与盖玻片粘起来,并将样品密封中间,所以需要用双面胶。盖玻片是60mm*24mm的,在片状的双面胶带上凿出一个框来,用框将石英玻璃与盖玻片粘结在一块。希望双面胶的宽度大于24mm,厚度最好为0.1mm,最好不是那种一卷一卷的,因为在双面胶中间凿出一块比较费事;希望是双面贴纸的,这样凿就比较方便。哪位能给个主意?谢谢了
大家制样时用的什么盖玻片啊???我买的盖玻片 洗不干净, 直接看时就能看到 上面分布了 很多裂纹 和 颗粒(其实不是颗粒)状的 点点很麻烦
如题,样品中有大颗粒,介质超声不能把颗粒分散。滴到裁片后盖玻片盖不平,硬压一是损坏盖片,第二是颗粒会变形,有什么好办法。
有谁用显微镜测过0.17盖玻片的厚度,用OLYMPUS OLS3000激光共聚焦显微镜试试?
纺织品成分定性分析中,盖玻片是一次性的吗?还是要反复清洁使用?
JB/T 8230.3-1997显微镜用载玻片JB/T 8230.4-1997 显微镜用盖玻片
成分分析中大家定性用的盖玻片是一次性的,还是清洗后反复用?
固体样品,做共聚焦。普通镜头不加盖玻片。高倍油镜不知道能不能直接测
成分分析定性分析中用到的盖玻片是一次性的吗?
用0.1ml藻类计数框、0.1ml的[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液器[/color][/url][/color][/url]来测水中的藻类计数,用了各种方法加样(包括《水和废水检测方法》),只要盖玻片一盖,都会有水样因虹吸作用溢出一点在框上面和框外面,跟我想象中不一样,请问下有做过的老师,这是正常现象还是属于我操作问题,或者是计数框容积不达标呢?
薄膜样品分析需要glass slide,可以用显微镜的microscopy glass slide吗?还有,上面样品风干后, 怎么储存玻片?用生物课上的玻片夹子可以吗?XRD样品没有盖玻片啊。谢谢回复!
求助ISO8037-1 ISO8037-2 ISO8255-1 ISO8255-2
在做革兰氏染色前,载玻片该如何清洗才能玻片上保证玻片上无颗粒.
两块玻片 一块是空白的 一块涂有硅之类的膜层 可以直接测这两块玻片 然后通过光谱差减得到膜层的吸收率吗 因为膜层太薄 刮下来几乎没有 所以想直接测 请问有人试过吗 谢谢
纸浆疏解后,悬浮液滴于载玻片上,烘干后放在显微镜下观察。有的片子觉得有留样价值,不知如何封片,长期保留、储存。不褪色。并有什么盒子专放单个载玻片的吗?想贴上标签放起来。谢谢!
求助行业各位大佬,我用拉曼光谱测液体油,但是800/1200波段的峰被载玻片掩盖了,求问怎么才能去除玻璃对吸收峰的影响。得到样品油在这个波段下的吸收峰
光学显微镜的覆盖差可以计算吗?如果可以,怎么计算呢?因样品的特殊性质小弟需要隔一层玻璃(非盖玻片)观察样品现想知道玻璃造成的覆盖差有多大或者是显微镜能忍受的玻璃有多厚谢谢大家!
求助行业各位大佬,我用拉曼光谱测液体油,但是800/1200波段的峰被载玻片掩盖了,求问怎么才能去除玻璃对吸收峰的影响。得到样品油在这个波段下的吸收峰[img]https://ng1.17img.cn/bbsfiles/images/2021/01/202101221626582196_9721_5054953_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2021/01/202101221626580410_9205_5054953_3.png[/img]
请教各同行载玻片(副溶)如何制作,需要哪些器皿,具体操作是怎样的,谢谢~~
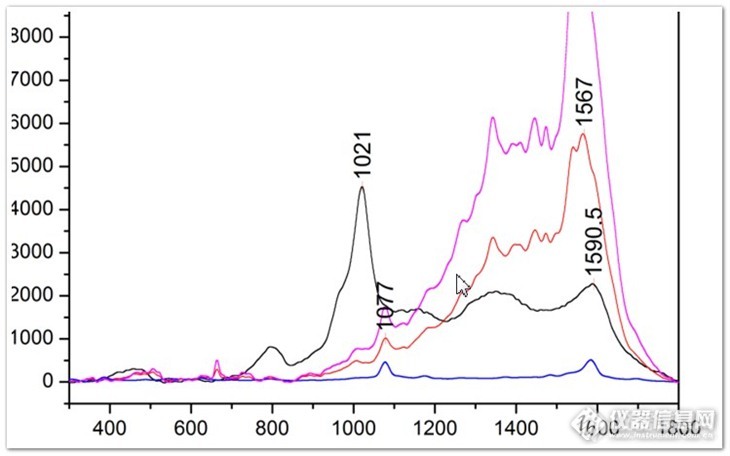
小的刚刚制备了一批表面增强的拉曼光谱。但是在测试的时候遇到了一个问题:同一个样品,放入毛细管中测量(液相)和滴在玻片上(烘干态)测量,峰位不一样。不知道是峰位发生了偏移还是有杂质峰? 滴在玻片上(烘干)后测量的峰位是符合预期的。我要的两个峰位是苯环的峰位950-1050和1500-1700。 欢迎大家讨论、指点我一下~~ 具体情况见下图。这幅是在毛细管中测量:峰位波数在883,1454;中间还有两个双峰。http://ng1.17img.cn/bbsfiles/images/2012/12/201212131130_412275_2651523_3.jpg这幅是在玻片上测量,峰位在1021和1567.符合预期。http://ng1.17img.cn/bbsfiles/images/2012/12/201212131131_412277_2651523_3.jpg我不知道这是为什么?求大家指点。也欢迎一起讨论啊。我的样品是基于银粒子的表面拉曼增强。溶剂是乙醇。
1.新玻璃器皿的洗涤方法 新购置的玻璃器皿含游离碱较多,应在酸溶液内先浸泡数小时。酸溶液一般用2%的盐酸或洗涤液(见本小节“3”)。浸泡后用自来水冲洗干净。 2.使用过的玻璃器皿的洗涤方法 (1)试管、培养皿、三角烧瓶、烧杯等可用瓶刷或海绵沾上肥皂或洗衣粉或去污粉等洗涤剂刷洗,然后用自来水充分冲洗干净。热的肥皂水去污能力更强,可有效地洗去器皿上的油污。洗衣粉和去污粉较难冲洗干净而常在器壁上附有一层微小粒子,故要用水多次甚至10次以上充分冲洗,或可用稀盐酸摇洗一次,再用水冲洗,然后倒置于铁丝框内或有空心格子的木架(图Ⅰ-10)上,在室内晾干。急用时可盛于框内或搪瓷盘上,放烘箱烘干。 玻璃器皿经洗涤后,若内壁的水是均匀分布成一薄层,表示油垢完全洗净,若挂有水珠,则还需用洗涤液浸泡数小时,然后再用自来水充分冲洗。 装有固体培养基的器皿应先将其刮去,然后洗涤。带菌的器皿在洗涤前先浸在2%煤酚皂溶液(来苏尔)或0.25%新洁尔灭消毒液内24小时或煮沸半小时,再用上法洗涤。带病原菌的培养物最好先行高压蒸汽灭菌,然后将培养物倒去,再进行洗涤。 盛放一般培养基用的器皿经上法洗涤后,即可使用,若需精确配制化学药品,或做科研用的精确实验,要求自来水冲洗干净后,再用蒸馏水淋洗三次,晾干或烘干后备用。 (2)玻璃吸管吸过血液、血清、糖溶液或染料溶液等的玻璃吸管(包括毛细吸管),使用后应立即投入盛有自来水的量筒或标本瓶内,免得干燥后难以冲洗干净。量筒或标本瓶底部应垫以脱脂棉花,否则吸管投入时容易破损。待实验完毕,再集中冲洗。若吸管顶部塞有棉花,则冲洗前先将吸管尖端与装在水龙头上的橡皮管连接,用水将棉花冲出,然后再装入吸管自动洗涤器内冲洗,没有吸管自动洗涤器的实验室可用冲出棉花的方法多冲洗片刻。必要时再用蒸馏水淋洗。洗净后,放搪瓷盘中晾干,若要加速干燥,可放烘箱内烘干。 吸过含有微生物培养物的吸管亦应立即投入盛有2%煤酚皂溶液或0.25%新洁尔灭消毒液的量筒或标本瓶内,24小时后方可取出冲洗。 吸管的内壁如果有油垢,同样应先在洗涤液内浸泡数小时,然后再行冲洗。 (3)载玻片与盖玻片用过的载玻片与盖玻片如滴有香柏油,要先用皱纹纸擦去或浸在二甲苯内摇晃几次,使油垢溶解,再在肥皂水中煮沸5—10分钟,用软布或脱脂棉花擦试,立即用自来水冲洗,然后在稀洗涤液中浸泡0.5—2小时,自来水冲去洗涤液,最后用蒸馏水换洗数次,待干后浸于95%酒精中保存备用。使用时在火焰上烧去酒精。用此法洗涤和保存的载玻片和盖玻片清洁透亮,没有水珠。 检查过活菌的载玻片或盖玻片应先在2%煤酚皂溶液或0.25%新洁尔灭溶液中浸泡24小时,然后按上法洗涤与保存。
有谁见过显微镜的自动载玻片,最好有图片
金相显微镜相关知识 一、应用领域 金相显微镜适用于工矿企业、院校及科研等机构作材料内部组织结构观察、电子企业、夹层电路观察、化工企业、对各种粉末进行质量监控等。 L2030A透反射(双色)正置金相显微镜配置透反射照明系统,长距平场消色差物镜(无盖玻片)、大视野目镜和内置偏光观察装置,光学系统成像清晰,视野广阔。 特点:带简易偏光,大视野,成像清晰,调试方便,拓展性强。可接工业相机,可配分析测量软件。 二、主要功能/参数 型号:正置上下光源金相显微镜 L2030A 目镜:大视野 WF10X(Φ18mm) 物镜:(20 40 60只能选2个) 长距平场消色差物镜(无盖玻片)PL 5X/0.12 长距平场消色差物镜(无盖玻片)PL L10X/0.25 长距平场消色差物镜(无盖玻片)PL L20X/0.40 长距平场消色差物镜(无盖玻片)PL L40X/0.60 长距平场消色差物镜(无盖玻片)PL L60X/0.75 (弹簧) 目镜筒:三目镜,倾斜30˚,(内置检偏振片,可进行切换) 落射照明系统:6V 20W卤素灯,亮度可调 落射照明器带视场光栏、孔径光栏、起偏振片,(黄,蓝,绿)滤色片和磨砂玻璃 调焦机构:粗微动同轴调焦, 微动格值:2μm,粗动松紧可调,带锁紧和限位装置 转换器 :四孔(内向式滚珠内定位) 五孔 ([fo
我做的是在石英玻璃片上沉积的薄膜,因为一次实验要做好多片。过程中需要有个托放石英片的托架,听说有放载玻片的盒(架),不知道能不能用。具体要求:每一个石英片都能跟其他的分开,并且能固定住,而且不能碰到有膜的那一面(因为检测时要到送别的单位去,路上怕弄坏已沉积好的膜),我的石英玻璃尺寸30mm×30mm
有个1微米厚的薄膜,在玻璃质的载玻片上,可以把它直接放到SEM的载物台上吗?一般都说要用硅片,我不知道直接放行不行?SEM的电压低于2KV谢谢啦。。。
玻璃器皿的清洗方法清洁的玻璃器皿是实验得到正确结果的先决条件,因此,玻璃器皿的清洗是实验前的一项重要准备工作。清洗方法根据实验目的、器皿的种类、所盛放的物品、洗涤剂的类别和沾污程度等的不同而有所不同。现分述如下: 1. 新玻璃器皿的洗涤方法新购置的玻璃器皿含游离碱较多,应在酸溶液内先浸泡数小时。酸溶液一般用2%的盐酸或洗涤液(见本小节“3”)。浸泡后用自来水冲洗干净。 2. 使用过的玻璃器皿的洗涤方法(1)试管、培养皿、三角烧瓶、烧杯等可用瓶刷或海绵沾上肥皂或洗衣粉或去污粉等洗涤剂刷洗,然后用自来水充分冲洗干净。热的肥皂水去污能力更强,可有效地洗去器皿上的油污。洗衣粉和去污粉较难冲洗干净而常在器壁上附有一层微小粒子,故要用水多次甚至10次以上充分冲洗,或可用稀盐酸摇洗一次,再用水冲洗,然后倒置于铁丝框内或有空心格子的木架上,在室内晾干。急用时可盛于框内或搪瓷盘上,放烘箱烘干。 玻璃器皿经洗涤后,若内壁的水是均匀分布成一薄层,表示油垢完全洗净,若挂有水珠,则还需用洗涤液浸泡数小时,然后再用自来水充分冲洗。 装有固体培养基的器皿应先将其刮去,然后洗涤。带菌的器皿在洗涤前先浸在2%煤酚皂溶液(来苏尔)或0.25%新洁尔灭消毒液内24小时或煮沸半小时,再用上法洗涤。带病原菌的培养物最好先行高压蒸汽灭菌,然后将培养物倒去,再进行洗涤。盛放一般培养基用的器皿经上法洗涤后,即可使用,若需精确配制化学药品,或做科研用的精确实验,要求自来水冲洗干净后,再用蒸馏水淋洗三次,晾干或烘干后备用。 (2)玻璃吸管吸过血液、血清、糖溶液或染料溶液等的玻璃吸管(包括毛细吸管),使用后应立即投入盛有自来水的量筒或标本瓶内,免得干燥后难以冲洗干净。量筒或标本瓶底部应垫以脱脂棉花,否则吸管投入时容易破损。待实验完毕,再集中冲洗。若吸管顶部塞有棉花,则冲洗前先将吸管尖端与装在水龙头上的橡皮管连接,用水将棉花冲出,然后再装入吸管自动洗涤器内冲洗,没有吸管自动洗涤器的实验室可用冲出棉花的方法多冲洗片刻。必要时再用蒸馏水淋洗。洗净后,放搪瓷盘中晾干,若要加速干燥,可放烘箱内烘干。 吸过含有微生物培养物的吸管亦应立即投入盛有2%煤酚皂溶液或0.25%新洁尔灭消毒液的量筒或标本瓶内,24小时后方可取出冲洗。 吸管的内壁如果有油垢,同样应先在洗涤液内浸泡数小时,然后再行冲洗。 (3)载玻片与盖玻片用过的载玻片与盖玻片如滴有香柏油,要先用皱纹纸擦去或浸在二甲苯内摇晃几次,使油垢溶解,再在肥皂水中煮沸5-10分钟,用软布或脱脂棉花擦试,立即用自来水冲洗,然后在稀洗涤液中浸泡0.5-2小时,自来水冲去洗涤液,最后用蒸馏水换洗数次,待干后浸于95%酒精中保存备用。使用时在火焰上烧去酒精。用此法洗涤和保存的载玻片和盖玻片清洁透亮,没有水珠。检查过活菌的载玻片或盖玻片应先在2[/
如题,现在我要做聚合物的红外光谱,要么是用溶液,要么就涂膜。用溶剂法麻烦,液体池清洗。现在问题是溶剂涂膜的话我有氟化钠的两块玻片(圆形,较厚)。溴化钾不能用?是因为溶剂中有水吗?每次用完之后得用氯仿之类的溶剂清洗,还不能擦拭?再就是以前看老师们做,就是直接把聚合物溶剂滴在一个类似载玻片一样的玻璃片上,红外灯烤烤干就可以做的?怎么现在要这么麻烦的处理。另外,我是透光的聚合物膜,不能直接放入样品池做红外吗?我用的是岛津的FTIR。很少自己动手用这个设备,一些问题较为初级,请各位前辈指教。
如题,我们公司想购买一款XRF,能将扫描样品做成玻片类,再进行扫描分析,大家有没有推荐的
我们实验课需要用到矿物晶相结构薄片(偏光显微镜或者金相显微镜上使用),但原来的已经使用太长时间了,想换一下,请问哪个地方有售?谢谢!
许多关于细胞利用的一些生物学应用,如微生物学、细胞培养、血液检查等要求我们在实验中确定细胞的浓度。细胞计数非常简单,需要有一个计数板,称为血细胞计数板,或血细胞计数器。19世纪法国解剖学家Louis-Charles Malassez发明了这种血细胞计数板。血细胞计数板是由一片较厚的特制玻片构成,中间有一个垂直线网格。网格的尺寸是给定的,因此每条线覆盖的区域是已知的,这样就可以对一定体积内的溶液中的细胞数量进行计数,为后期的血细胞检测奠定基础。最为常见的血细胞计数板类型的中部有一个“H”形结构,上面有两个像镜子一样抛光的网格表面,并可在上面加上外罩。加载血细胞计数板开始进行计数之前,用擦镜纸拭去灰尘颗粒,确保血细胞计数板及其盖玻片处于洁净状态。安装在血细胞计数板上的盖玻片是特制的,明显厚于传统的显微镜盖玻片,这是因为它必须能够克服液滴的表面张力。确保在加载细胞悬液之前,先将盖玻片放置在计数表面,然后将吸液头和样本放进其中的一个V型孔中,并小心地挤出样本。利用毛细管作用充填盖玻片下部的区域。必须放入足够的液体以便覆盖整个镜片的表面,通常需要大约10ul,但不要溢出表面。您可以在一台血细胞计数板中加载两个样本,每个样本进入两个网格。将加载完的血细胞计数板放置在显微镜台上,然后将计数格在低倍镜焦距中显示。将样本静置几分钟,不要移动盖玻片,以免产生气泡导致计数困难。在血细胞计数板上进行血细胞计数一个血细胞计数板的整个网格包括9个方格,每个方格的面积为1mm2。血细胞计数板的中心区域有25个较大的方格,每个大的方格中又包含16个小方格。当进行计数时,仅对那些位于大方格两侧的各行中的细胞进行计数,以避免重复计数。悬液必须稀释到足够的程度,这样,细胞或其它颗粒才能均匀分布,不会再网格中相互重叠。为了判断细胞的活性,通常采用一种特殊的染色剂(如用台盼蓝稀释样本)。这种染色方法,又称为染色