我就挺好奇的,酸性样品要用0.1%氨水溶液做流动相,那直接购买的25%HPLC氨水最少100ml起订,四五毫升就够配1L0.1%氨水了,那剩下的25%氨水该怎么储存?可别0.1%氨水还没用完25%氨水就发霉长菌了?实验室要现配氨水浓度和纯度都掌控不了,只能直接买现成氨水。
看到一个方法中用到3%的氨水(v/v.),而试剂项目中纯氨水是30%(以NH3计),就是想问一下因为是v/v.也就是体积比,就不用考虑纯氨水的浓度了,只要拿30%纯氨水3份配上97份的蒸馏水就行了,不知哪位高手能帮确认一下吗?
我想测定中控分析中工业氨水的浓度 但是只查到了化学试剂氨水的国标 请问能不能按照化学试剂氨水的国标来测定工业氨水的浓度?谢谢!!
稀氨水是指多少浓度的氨水啊(?%)?大侠请指教
[B]氨水[/B] 分子式:NH3.H2O 分子量:35.045 氨的水溶液叫氨水,分子式为NH3.H2O及NH4OH,含氮12%~16%,氮素形态为NH3、NH4,属于铵态氮肥。我国目前氨水的产量不到氮肥总产量的0.2%。氨水的生产是由合成氨导入水中稀释而成。氨水除由氮肥厂生产外,炼焦工厂、煤炭干馏和石油工业也可生产浓度不同的氨水作为副产品。还可利用氮肥厂氨加工过程中的含氨尾气,用水吸收后生产稀氨水,含氮量为1%~3%,价格低廉,适于就近施用。我国常用的氨水浓度为含氨15%、17%和20%三种,国外农用氨水的浓度稍高,一般含氨25%(含氮20%)的产品。 氨水为无色透明或微带黄色的液体,工业副产品的氨水因含有多种杂质而有不同的颜色。氨在水中溶解度很大,一体积水可溶解700体积氨,但由于氨在溶液中呈不稳定的结合状态,大都以氨分子状态存在水中,只有一部分以氨的水合物(NH3.H2O)和极少量NH4OH存在。所以氨水是一种弱碱(pH值10左右),但因氨分子极为活泼,使氨水在常温下容易挥发,对容器有腐蚀性,对人有刺激性。在贮运和施用时要用耐腐蚀并能密封的容器及机具。 氨水的挥发损失受浓度,气温及容器的密闭程度等因素的影响。氨水的浓度越高,放置时间越长,液面暴漏越多,则氨的挥发损失越多。为了尽可能减少贮运和施用过程氨挥发损失,目前生产厂常在氨水中通入一定量的二氧化碳将其碳化,使一部分氨与二氧化碳结合,形成含有NH4HCO3、(NH4)2CO3和NH4OH(NH3.H2O)的混合液,称“碳化氨水”。碳化氨水比普通氨水能明显减少氨挥发。 氨水的施用原则是“一不离土,二不离水”。不离土就是要深施覆土;不离水就是加水稀释以降低浓度、减少挥发,或结合灌溉施用。由于氨水比水轻,灌溉时要注意避免局部地区积累过多而灼伤植株。氨水可作基肥也可作追肥。 氨水是氨溶于水得到的水溶液。它是一种重要的化工原料,也是化学实验中常用的试剂. 也称"气肥".(附:氨水的溶质为NH3) 氨水(AQUA AMMONIAE) 为一无色透明的液体,具有特殊的强烈刺激性臭味,正因为它具有局部强烈兴奋的作 用,因此将特定浓度的氨水,直接接触皮肤会使皮肤变红,并有灼热感,因此小心. 氨气是化肥工业的中坚产品,易溶于水而生成氨水,呈碱性。由于氨水可以作为肥料直接施于农田,所以在农村使用很普遍。在氨水分装、运输和使用过程中,常有不慎溅入眼睛的事故发生。当眼部被氨水灼伤后,如不采取急救措施,可造成角膜溃疡、穿孔,并进一步引起眼内炎症,最终导致眼球萎缩而失明。 氨水在低温时可析出一水合氨晶体,它的熔点为-79℃,因此NH3H2O是氨存在于水溶液的主要成分。氨水中也有很小一部分一水合氨发生电离, 中存在下列平衡: 可见氨水中有H2O、NH3H2O、NH3三种分子,有少量OH-、 三、掌握性质 由于氨水中含有多种成分,而使其表现出多重性质。 1)刺激性:因水溶液中存在着游离的氨分子。 (2)挥发性:氨水中的氨易挥发。 (3)不稳定性:—水合氨不稳定,见光受热易分解而生成氨和水。 NH3H2O=NH3↑+H2O 实验室中,可用加热浓氨水制氨,或常温下用浓氨水与固体烧碱混合的方法制氨,其装置与操作简便,且所得到的氨气浓度较大,做“喷泉”实验效果更佳。由于氨水具有挥发性和不稳定性,故氨水应密封保存在棕色或深色试剂瓶中,放在冷暗处。 (4)弱碱性:氨水中一水合氨能电离出OH-,所以氨水显弱碱性,具有碱的通性: ①能使无色酚酞试液变红色,能使紫色石蕊试液变蓝色,能使湿润红色石蕊试纸变蓝。实验室中常见此法检验NH3的存在。 ②能与酸反应,生成铵盐。浓氨水与挥发性酸(如浓盐酸和浓硝酸)相遇会产生白烟。 NH3+HCl=NH4Cl (白烟) NH3+HNO3=NH4NO3 (白烟)而遇不挥发性酸(如硫酸、磷酸)无此现象。实验室中可用此法检验NH3或氨水的存在。 工业上,利用氨水的弱碱性来吸收硫酸工业尾气,防止污染环境。 SO2+2NH3H2O=(NH4)2SO3+H2O(NH4)2SO3+SO2+H2O=2NH4HSO3 (5)沉淀性:氨水是很好的沉淀剂,它能与多种金属离子反应,生成难溶性弱碱或两性氢氧化物。例如: 生成的Al(OH)3沉淀不溶于过量氨水。 生成的白色沉淀易被氧化生成红褐色沉淀 4Fe(OH)2+O2+2H2O=4Fe(OH)3 红褐色 利用此性质,实验中可制取Al(OH)3、Fe(OH)3等。 (6)络合性:氨水与Ag+、Cu2+、Zn2+三种离子能发生络合反应,当氨水少量时,产生不溶性弱碱或两性氢氧化物,当氨水过量时,不溶性物质又转化成络离子而溶解。 AgOH+2NH3H2O=[Ag(NH3)2]++OH-+2H2O 实验室中用此反应配制银氨溶液。 Zn(OH)2+4NH3H2O=[Zn(NH3)4]2++2OH-+4H2O 可用此反应来鉴别两性氢氧化物氢氧化铝和氢氧化锌。 Cu(OH)2+4NH3H2O=[Cu(NH3)4]2++2OH-+4H2O (深蓝色) 表现出弱的还原性,可被强氧化剂氧化。如氨水可与Cl2发生反应: 3Cl2+8NH3H2O=6NH4Cl+N2+8H2O 氨水中毒如何处理 氨水中毒在农村较为常见,因为它是广泛使用的化肥之一。 一旦氨水沾污皮肤,先用清水或2%的食醋液冲洗;若皮肤局部出现红肿、水泡,可用2%的食醋液冲洗;若皮肤局部出现红肿、水泡,可用2%的硼酸液湿敷。鼻粘膜受到强烈的刺激,可滴入1%的麻黄素溶液,重者应吸入糜蛋白酶。 氨水溅入眼内,应立即用生理盐水反复冲洗,再滴入氯霉素眼药水,仍感不适时须请医生急诊和治疗。 发现氨水吸入中毒者(出现呼吸道、眼、鼻、皮肤粘膜的严重刺激感,并伴随咳嗽、流涕、发痒、气促、紫绀、烦躁等症状),应让他迅速离开现场,并脱去被氨水污染的衣、裤;口服食醋50-100毫升,同时服用维生素c50毫克,每日3次;若出现咽喉梗塞,肺气肿等症状,应请医生急诊治疗,以免发生意外。 一份氨气溶于一份水中称为一合水氨 氨气物理性质 相对分子质量 17.031 氨气在标准状况下的密度为0.7081g/L 氨气极易溶于水,溶解度1:700 化学性质 跟水反应 氨溶于水时,氨分子跟水分子通过*氢键结合成一水合氨(NH3• H2O),一水合氨能小部分电离成铵离子和氢氧根离子,所以氨水显弱碱性,能使酚酞溶液变红色。氨在水中的反应可表示为: 一水合氨不稳定受热分解生成氨和水
各位前辈,大家好!小弟从事实验室电位滴定工作有3个年头了,最近滴定28%氨水浓度时发现第一天测试浓度NH3在28%,过了2天之后再测试就降低到27%了,并且浓度随时间有持续下降的趋势,氨水保存在白色不透光塑料瓶22℃保存,请教各位前辈有没有类似经历,出现浓度下降趋势的原因是因为氨水挥发并且从瓶口不断溢出造成的么?
大家说说都是怎样制备无氨水的,制出来的无氨水怎样验证是否合格?
近来我进一批氨水,做实验用的,厂家说是用液氨冲的,回来时我用移准管吸取1mL氨水用0.5mol/L的硫酸进行滴定,消耗体积3ml多,测出来氨水的的氨含量约为26g/L,但PH值只用9左右(用1-14的广泛试纸测的),可闻起不来氨味很淡且还有点硫化氢气体的味,怎么回事呀????????????、以前买时没出现过]]
我想买高纯氨水,试用过优级纯的,还不行。主要是要钾含量低一点,氨水含量低一点也不要紧,不知哪里有卖?价格高一点也不要紧。

[color=#DC143C]氨水[/color][img]http://ng1.17img.cn/bbsfiles/images/2009/11/200911112341_183908_1610969_3.jpg[/img]概述 名称:氨水 别称:氢氧化铵;阿摩尼亚水 英文名称:Ammonium Hydroxide Ammonia Water 分子式:NH3H2O 分子量:35.045 结构:水合氨分子是氨分子和水供给的氢以配位键相结合形成的。 CAS No.:1336-21-6 国标编码:82503 危险标记:20(碱性腐蚀品)[color=#DC143C]基本性质[/color] 性状:无色透明液体,有强烈的刺激性气味。 熔点:-77℃ 蒸汽压:1.59kPa(20℃) 相对密度:氨含量越多,密度越小。质量分数28%的氨水相对密度0.91,35%的0.88。 电离常数:K=1.8×10ˇ-5(25℃) 稳定性:受热或见光易分解 其它:极易挥发出氨气。浓氨水对呼吸道和皮肤有刺激作用,并能损伤中枢神经系统。具有弱碱性。[color=#00008B]主要性质[/color] 挥发性 氨水易挥发出氨气,随温度升高和放置时间延长而增加挥发率,且浓度的增大挥发量增加。 腐蚀性 氨水有一定的腐蚀作用,碳化氨水的腐蚀性更加严重。对铜的腐蚀比较强,钢铁比较差,对水泥腐蚀不大。对木材也有一定腐蚀作用。 弱碱性 氨水中存在以下化学平衡: NH3+H2O=(可逆)=NH3H2O NH3H2O=(可逆)=NH4+ +OH- 因此仅有一小部分氨分子与水反应而成铵离子NH4+和氢氧根离子OH-,故呈弱碱性。 氨水具有碱的通性: ①能使无色酚酞试液变红色,能使紫色石蕊试液变蓝色,能使湿润红色石蕊试纸变蓝。实验室中常用此法检验NH3的存在。 ②能与酸反应,生成铵盐。浓氨水与挥发性酸(如浓盐酸和浓硝酸)相遇会产生白烟。 NH3+HCl=NH4Cl (白烟) NH3+HNO3=NH4NO3 (白烟) 而遇不挥发性酸(如硫酸、磷酸)无此现象。实验室中可用此法检验NH3或氨水的存在。 工业上,利用氨水的弱碱性来吸收硫酸工业尾气,防止污染环境。 SO2+2NH3H2O=(NH4)2SO3+H2O (NH4)2SO3+SO2+H2O=2NH4HSO3氨极易溶于水的喷泉实验
1)蒸馏吸收法:将约3L二级氨水倾入5L硬质玻璃烧瓶中,加入少量10g/L高锰酸钾溶液至溶液呈微红紫色,烧瓶口接回流冷凝管,冷凝管的上端与三个洗气瓶连接(第一个洗气瓶盛10g/L EDTA溶液,其余两个均盛离子交换水)。第三洗气瓶与接收瓶连接,接收瓶为有机玻璃瓶置于混有食盐和冰块的水槽内,瓶内盛有1.5L离子交换水。用调压变压器控制温度,当温度升至40℃时,氮气通过洗气瓶后被接收瓶的水吸收。当大部分氨挥发后,最后升温至80℃使氨全部摔发。接收瓶中的氨水含量稍低于25%。 2)等温扩散法:将约2L二级氨水倾入洗净的大干燥器(液面勿触及瓷托板),瓷托板上放置3~4个分盛200mL离子交换水的聚乙烯或石英广口容器,从托板小孔,加入2~3g氢氧化钠,迅速盖上干燥器嚣,每天摇动一次,5~6天后氨水含量可达10~12%。
大家能不能跟我交流下关于无氨水制备的技巧啊,我的无氨水空白值大得离谱,比未蒸馏前高出好多倍!
浓氨水的浓度怎么测?
有一批氨水,有较大臭味,朋友说是从中石油复产出来的,像是硫化氢,有没有什么好办法可以去除氨水中臭味和硫,我可以寄样品,方法可行,必有重谢,联系电话:13131921003
流动相中0.1%氨水如何配置?这个0.1%是体积比吗?我看试剂瓶上写的≥25% in the water,它纯度不是100%,如果要配置1000ml的流动相,需要加多少的氨水啊?4ml吗?
最近做氨氮的曲线时发现空白值较之以往升高了许多,但是我们实验室目前没有制备无氨水的设备,想请教一下制备无氨水需要什么设备?
10%的氨水溶液市购的氨水含量为25%的是吧?我直接取10ml 25%的氨水,稀释到100ml还是把25%的氨水稀释2.5倍?
做氨氮的项目要使用无氨水,制备起来倒是不麻烦。但是经常使用,可能需要经常制备。你们检测氨氮制备无氨水吗?还是使用超纯水代替?
固体制剂中用到了氨水,这个残留怎么检测啊~
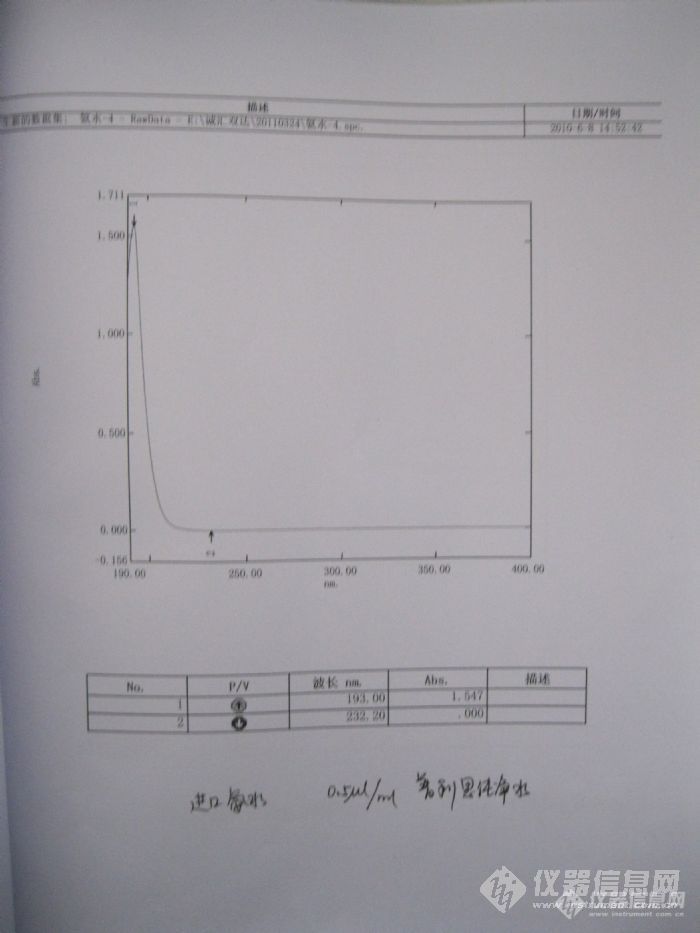
我们扫描的是MERCK的p.a.级别的氨水,UV扫描如如下:http://ng1.17img.cn/bbsfiles/images/2011/04/201104080911_287710_1790097_3.jpg是由25%氨水配制的。浓度在图上。水的末端吸收很小的,可以忽略,此处不上传了。上面的UV吸收是否正常?我想可能是氨水存在n轨道→δ*轨道电子跃迁造成的。
我公司因条件限制,无法加0.1毫升的硫酸去重蒸馏,也不制去离子水的仪器,请问还有没有其它的方法来制无氨水?
按食品5009做合成色素,遇到一个小疑问,乙醇+氨水+水比例是7:2:1,这里的氨水是浓氨水,还是标准前面提到的2mL浓氨水稀释到100mL的氨水?
无氨水的制取有什么讲究没有?另外这个无氨水是否符合使用要求,如何去判别呢?
购买的氨水为25%,其浓度为13,38M,如何将其浓度变为15M?
急求氨水浓度的标定方法,万分感谢。
各位老师,请问下,[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]流动相中加甲酸或者氨水时,甲酸和氨水还需要稀释吗
大家做氨时候的无氨水都是怎么弄的那?买的还是自己做的啊?要是自己买仪器做?大家有什么推荐的么?谢谢啦~
最近实验要用到固相萃取 我想问下各位老师,经过氨水淋洗溶液偏碱性,能直接进柱子吗
求救!氨水的提纯方法!!谢谢
实验室做低含量硅,要求氨水超纯,普通分析纯的氨水如何精制?饱和法?