之前使用的是AJL的300SB-C18柱子,0.8ml/min,甲醇:水=90:10 ,95:5,100:0,241nm,胆甾-4-烯-3酮标品总是出现M状的峰。现在新换了一个迪马的柱子,甲醇:水=91.5:8.5,60min才出现峰,出峰时间有点过长了,但总归是觉得迪马柱子算还是不错,各位版友认为呢?有个小问题是:16min有个峰,标品也是有个小峰,不知道哪个算是胆甾-4-烯-3酮的峰?
出现未知肽,是什么原因老师们好,我把酪蛋白用胰蛋白酶,酶切后,再通过载体分离的方法,分离出的多肽,有三条在库里边收不到,这是什么原因啊?
同一台气相,5A分子筛柱填充柱,2米加TCD检测器。当用氢气做载气时,进空气分析,氧含量20.9(面积归一法),没有问题。换成氩气做载气时(因为要同时分析氢,并排除空分气体中Ar气干扰,氧氩合峰),同样进空气,氧含量24(面积归一法)。 是不是氧氮在氩气做载气时响应值变化了(与H2做载气时相比),看文献说氩气做载气时,热导线性变差(相对于H2做载气),但没有提及氧氮响应值的变化。 各位高手,有没有知道的,忘告知! 谢谢!
高纯氮作载气测定氮中杂质,氢是出正峰,但氩出反峰,这正常吗?请各位赐教!
祝大家双蛋快乐!圣诞、元旦期间免分下载本版面资料(自12月25日起到1月2日):下载地址:http://www.instrument.com.cn/download/search.asp?searchType=admin%5Fname&keywords=wsy18&page=1下载后跟帖说明资料名称即可加分返还积分,每个ID最多可返还10积分。
中航工业计算所机载、弹载计算机航空科技重点实验室日前通过中航工业科技与信息化部的验收并揭牌。机载、弹载计算机航空科技重点实验室依托中航工业计算所,是中航工业建设和管理的重点实验室之一,其任务是围绕航空科技发展战略目标和武器装备发展的需求,开展探索性、创新性的公共计算资源基础研究、应用基础研究、应用研究以及重点型号研制中的关键技术攻关,是开展航空科技集团机载、弹载计算机自主创新研究,吸引与培养高水平研究人才,学术交流、合作与科学实验的重要基地。 实验室由并行处理研究、容错技术研究、工程化研究和软件技术研究等四个研究单元组成,主要研究方向为实时分布式计算机系统和并行信号处理系统、容错计算机系统、机载计算机抗恶劣环境、计算机系统软件和地面开发环境。试运行以来,实验室共承担了总装、空装、集团等的预先研究、基金类课题43项,突破关键技术若干项,获奖15项,申请专利及软件著作权16项。
红外三级鉴定法可以区别和鉴定栽培和野生丹参,红外三级鉴定包括普通红外光谱、二阶导数谱和二维红外相关光谱,并且表观分辨率逐渐提高。栽培与野生丹参一维谱图峰形相似度很高,只是吸收峰波数有一定的差异。二阶导数谱则可看到在1500~1180cm -1波段栽培丹参在1410cm-1处有单峰,而野生丹参则出现分叉峰,分别在1420cm-1、1406cm-1处。在1180~850cm-1波段,栽培丹参在993cm-1、872cm-1处有比较强的吸收峰,而野生丹参在1032cm-1处有比较强的吸收峰。二维红外相关光谱中差异更明显,在1170~860cm-1波段,野生丹参在950cm-1处有很强的自动峰,而栽培丹参在此没有吸收峰;1500~1170cm-1波段野生丹参的峰强度要较栽培丹参大,依据自动峰的不同可以很容易的分辨出栽培与野生丹参。红外三级鉴定方法是一种快速有效的鉴定中药材的方法。
矿难、洪水......每一条黑色的新闻,每一组黑色的数字,从开始的震惊到现在的淡漠甚至麻木。 是因为这些事情的频繁发生?屡见而不鲜吗?或是越来越关注自己内心,不再敏锐的感知周遭?还是对客观纷争无能为力而选择逃避? 触动这些想法的是东北那场洪水,那个小学校,那些鲜嫩生命的凋零。 有人说这是中国的别斯兰。别斯兰的悲剧是因恐怖分子而有,我们的愤怒还有明确的目标指向。那么,这场洪水呢?也许因为洪水是天灾,惋惜是最初的感受。惋惜之后,在看过记者出于寻找真相,表达真相的良知而做的记录:来自上游村庄打到镇政府的报警电话被忽视;在个别家长发出预警,带走自己孩子的情况下,老师的漠然等待,灾难降临时的束手无策; 教室很多地方,印满了小小的泥手印,最高处已经接近了天花板,水线在窗户上最高的一块玻璃的下面;洪水中这个小镇失去了超过三分之一的孩子;甚至回溯到学校选址、建设时的官僚与fb...... 我不知道在沙兰小镇发生的是否还能只算是一场天灾?谁该对这些的孩子负责。 机会总是光临有准备的人,还有一句话:有备无患。灾难来临的时候,因人为的懈怠会多加一份人祸,也能因人的智慧,果敢而挽救很多。 一个个糊满了泥浆冰冷的小身体,曾经有活的机会,最终只能接受死别的现实,失去孩子的家庭会伤心欲绝。这些家庭以外的人们呢,身在远方的我们呢?作为一个个体,无权责备发生过的事情中的任何人,责备也没有意义。只要求、提醒自己保持一些警醒与鲜活,无论是面对丽日阳光还是阴霾满天,让自己保持健康去爱的能力,爱自己,爱别人,爱世界,不要一路淡漠下去。 “昨天我不爱这个世界,而今天我能爱这个世界一刻,区别仅仅在于自己是否努力过。”
氨氮的新国标在哪里可以下载啊
[font=宋体]在分子生物学和生物工程领域,蛋白表达载体构建是至关重要的技术之一,它涉及到将目的基因插入到适当的表达载体中,以便在宿主细胞内进行蛋白表达。这一过程不仅有助于研究基因的功能和蛋白质的结构,还为药物开发、基因治疗等领域提供了有力支持。本文将详细介绍蛋白表达载体构建的整个流程,包括目的基因的选择、载体的选择与改造、基因插入、转化、筛选与鉴定等关键步骤。[/font][font=宋体] [/font][b][font=宋体]蛋白表达载体构建流程:[/font][/b][font=宋体] [/font][font=宋体][font=宋体]①[/font][font=Calibri]NCBI[/font][font=宋体]查找目的基因的[/font][font=Calibri]CDS[/font][font=宋体]序列[/font][/font][font=宋体][font=宋体]进入[/font][font=Calibri]NCBI[/font][font=宋体](美国国家生物技术信息中心)的网站。[/font][/font][font=宋体]在搜索框中输入目的基因的名称或关键词。[/font][font=宋体][font=宋体]在搜索结果中找到[/font][font=Calibri]CDS[/font][font=宋体]([/font][font=Calibri]Coding Sequence[/font][font=宋体])序列,通常会显示基因的[/font][font=Calibri]DNA[/font][font=宋体]序列。[/font][/font][font=宋体][font=宋体]记录或复制所需的[/font][font=Calibri]CDS[/font][font=宋体]序列信息。[/font][/font][font=宋体] [/font][font=宋体]②选择合适的表达载体[/font][font=宋体]根据目的基因的性质和所需的表达水平,选择适合的表达载体。[/font][font=宋体]考虑载体的克隆容量、复制子类型、筛选标记等。[/font][font=宋体] [/font][font=宋体]③确定双酶切位点[/font][font=宋体]根据目的基因和载体,选择合适的双酶切位点。[/font][font=宋体][font=宋体]确保酶切位点在[/font][font=Calibri]CDS[/font][font=宋体]序列和载体上都是独特的,避免切割其他部位。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]④[/font][font=Calibri]Primer 5[/font][font=宋体]预测目的序列酶切位点[/font][/font][font=宋体][font=宋体]使用[/font][font=Calibri]Primer 5[/font][font=宋体]或其他相关软件,根据已知的[/font][font=Calibri]CDS[/font][font=宋体]序列设计酶切位点的引物。[/font][/font][font=宋体]通过软件预测引物的特异性,确保它们仅与目的基因结合。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]⑤双酶切[/font][font=Calibri]buffer[/font][/font][font=宋体][font=宋体]根据选择的酶,准备相应的酶切[/font][font=Calibri]buffer[/font][font=宋体]。[/font][/font][font=宋体][font=宋体]注意[/font][font=Calibri]buffer[/font][font=宋体]的[/font][font=Calibri]pH[/font][font=宋体]值和离子浓度,确保酶的活性。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][font=宋体]⑥目的基因[/font][font=Calibri]CDS[/font][font=宋体]序列引物设计[/font][/font][font=宋体][font=宋体]根据[/font][font=Calibri]CDS[/font][font=宋体]序列,设计一对引物用于[/font][font=Calibri][url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]扩增目的基因。[/font][/font][font=宋体]确保引物的特异性,避免与其他基因序列发生非特异性结合。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]⑦转化[/font][font=宋体][font=宋体]制备感受态细胞,使其处于易于接受外源[/font][font=Calibri]DNA[/font][font=宋体]的状态。[/font][/font][font=宋体][font=宋体]将[/font][font=Calibri][url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]扩增得到的目的基因与载体混合,进行转化反应。[/font][/font][font=宋体]将转化后的细菌在选择培养基上培养,筛选含有重组载体的阳性克隆。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]⑧双酶切及鉴定[/font][font=宋体][font=宋体]提取阳性克隆的质粒[/font][font=Calibri]DNA[/font][font=宋体]。[/font][/font][font=宋体]使用设计的引物进行双酶切反应。[/font][font=宋体]对酶切产物进行电泳分析,观察是否获得预期的片段,并进行凝胶回收。[/font][font=宋体] [/font][font=宋体] [/font][font=宋体]⑨测序[/font][font=宋体]将回收的酶切产物进行序列测定。[/font][font=宋体][font=宋体]对比测序结果与目的基因的[/font][font=Calibri]CDS[/font][font=宋体]序列,确保没有突变或错误。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体]⑩阳性菌落扩大培养,用于后期蛋白纯化研究[/font][font=宋体] [/font][font=宋体]选择测序正确的阳性菌落进行扩大培养。[/font][font=宋体]在摇瓶或发酵罐中进行高密度培养,为后续的蛋白表达提供充足的原料。[/font][font=宋体]在确定目的基因在载体上正确表达后,可以进行蛋白纯化研究。[/font][font=宋体]通过适当的纯化技术,如亲和层析、离子交换等,分离和纯化目的蛋白。[/font][font=宋体]对纯化的蛋白进行质量分析和功能研究。[/font][font=宋体] [/font][font=宋体][font=宋体]综上所述,蛋白表达载体构建是一个系统性的过程,涉及到多个关键步骤和复杂的技术操作。通过遵循这一流程,研究人员能够成功地在宿主细胞内表达所需蛋白,并进一步对其进行分析和功能研究。随着生物技术的不断发展,蛋白表达载体构建的应用领域将越来越广泛,为人类对生命现象的深入理解和疾病的防治提供更多可能性。因此,不断优化和完善这一技术对于生命科学领域的发展至关重要。更多[url=https://cn.sinobiological.com/resource/protein-review/protein-production][b]蛋白表达生产[/b][/url]详情可以关注[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/protein-production[/font][/font]
为什么下载资料时就弹出一个二维码?无法下载资料?很不爽!
在GB/T 5750.12-2006微生物大肠杆菌测定中,先取10mL水样于10mL双料乳糖蛋白胨培养液中,取1mL水样接种到10mL单料乳糖蛋白胨培养液中,在取稀释10倍的水样于10mL单料乳糖蛋白胨培养液中,每一稀释度接种管5管。那请教下大家, 为什么要先双倍再单倍、单倍,这样培养的区别在哪里?可不可以都用单倍或都用双倍或三倍?浓度高的培养基中为什么移取的水样要多点呢?请大家多多指教。我是新手。谢谢!
[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]用高纯氮做载气可以吗,还是一定要用氦气的?
祝大家元旦快乐!节日期间(1-3日)认证会员可全部免分下载、普通会员每节1分下载如下资料:1、“现代色谱分析”视频教程(第1-16课);2、“波谱分析”视频教程(第1-32课)。下载地址:http://www.instrument.com.cn/download/search.asp?searchType=admin%5Fname&keywords=wsy18&page=3友情提示:非认证会员请尽快去论坛认证,以获得众多优惠。例如,通过认证即可获得50积分的奖励等等。详见:http://www.instrument.com.cn/bbs/shtml/20080812/1417975/

测定动物肌肉组织和鸡蛋中残留的11种甾体激素类药物甾体化合物具有一个四环的(A、B、C、D)母核,这个母核像“田”字,并且在C10和C13处各有一个角甲基,在C17处有一侧链,这样在母核上的三个侧链像“巛”字,“甾”字十分形象的表示了这类化合物。它们能促进畜禽生长,提高饲料转化率,有利于蛋白质的沉积,在畜牧业养殖中经常使用。但蛋白同化激素在动物食品中的残留可能会危及消费者的健康,具有潜在的致癌性。我国农业部于2002年发布的第235号文件中规定丙酸睾酮、苯丙酸诺龙、甲睾酮、群勃龙等在动物性食品中的最高残留限量为不得在动物性食品中检出”。因此,检测可食性动物源食品中蛋白同化类激素及其代谢产物残留量是一项重要的指标。本实验建立了同时检测猪、牛、羊及鸡的肌肉组织与鸡蛋中睾酮、甲基睾酮、群勃龙、勃地龙、诺龙、美雄酮、司坦唑醇、丙酸诺龙、丙酸睾酮及苯丙酸诺龙等10种蛋白同化激素类药物和孕激素黄体酮残留量的快速方法。1.1仪器与试剂ACQUITYlM超高压液相色谱仪和Micromass—Quattro Premier质谱仪(美国Waters公司)。睾酮(testosterone)、甲基睾酮(methyltestosterone)、黄体酮(progesterone)、群勃龙(trenbolone)、勃地龙(boldenone)、诺龙(nandrolone)、美雄酮(大力补,methandienone)、司坦唑醇(康力龙,stanozol01)、丙酸诺龙(nandrolone propionate)及丙酸睾酮(testosterone propionate)对照品购自德国Dr.Ehrenstoffer公司;苯丙酸诺龙(nadrolone phenylpropionate)对照品购自中国兽药监察所。叔丁基甲醚、乙腈、甲醇均为色谱纯(德国Merck公司);甲酸和碳酸钠均为分析纯(广州化学试剂厂);水为超纯水。1.2储备液的制备准确称取适量的睾酮、甲基睾酮、黄体酮、群勃龙、勃地龙、诺龙、美雄酮、司坦唑醇、丙酸诺龙、丙酸睾酮及苯丙酸诺龙,用甲醇分别配制成l g/L的单标准溶液及10 mg/L的混合标准溶液,冰箱中保存,备用。1.3色谱-质谱条件1.3.1色谱条件色谱柱:Ultimate XB-C18 4.60×250mm,5 um .Part Number 00201-31043 Serial Number 211302350.流动相:A相为0.1%甲酸水溶液,B相为0.1%甲酸乙腈溶液;梯度洗脱程序:0—5.0 min,50%B--,90%B;5.O一7.0 min,90%B;7.O一7.5 min,90%B一50%B;7.5—10.0 min,50%B;流速:0.3 mL/min。柱温:室温。进样体积:lo斗L。1.3.2质谱条件离子源:电喷雾离子源(ESI),电压3 200 V,温度300 oC。扫描方式:正离子模式。检测方式:多反应监测(MRM)。脱溶剂气、锥孔气均为高纯氮气,流速分别为600,20 L/h;碰撞气为高纯氩气,压力为0.36 Pa(3.6×lO—mbar)。锥孔电压、碰撞能量及定性离子对、定量离子对等参数见表1。http://ng1.17img.cn/bbsfiles/images/2015/07/201507021634_553131_2433088_3.png 1.4试样制备称取约500 g猪、牛、羊或鸡肌肉组织,切碎后匀浆备用;取10枚鲜鸡蛋,去壳,均质备用。1.5样品前处理称取5 g均质试样(精确至0.01 g),置于50mL离心管中,加入叔丁基甲醚25 mL。于10 000r/min均质30 S,振荡10 min;于4℃、6 000 r/min条件下离心10 min,上清液转移至100 mL梨形瓶中,残渣中再加入20 mL叔丁基甲醚振荡提取一次。合并离心后的上清液,并用旋转蒸发仪于45℃水浴中蒸发至干。加人流动相A与B(体积比为1:1)混合溶液2.0 mL,超声溶解残渣,予一20℃冰箱中放置30 min,取适量溶液于16 000 r/min下离心5 min,上清液过O.22斗m针头滤膜,滤液供测定。 1.6标准曲线的绘制空白试样按照“1.5”节方法处理,取适量空白上清液加入不同量的蛋白同化激素标准储备液,配制成1,2,4,10,20及100斗g/L的基质空白标准溶液,混匀后进样。以待测物色谱图的峰面积为纵坐标,相应待测物质量浓度为横坐标,进行回归运算,求得直线回归方程。1.7回收率试验添加质量浓度为50,100,500斗g/L的混合标准工作液0.1 mL,制得1,2,10斗g/kg添加水平的样品,按上述方法处理,测定回收率。1.8检出限与定量限的测定取适量混合标准工作液,制得0.2,0.3,0.4,0.5斗g/kg添加水平的样品,按“1.5”节所述方法处理,以最低检出浓度计算,3倍信噪比为检出限,10倍信噪比为定量限。 http://ng1.17img.cn/bbsfiles/images/2015/09/201509101132_565576_2433088_3.png 11种甾体激素类药物的RMR离子流图(10 ug/L)

为庆祝分坛12月的大礼包,特在圣诞再派大礼包…………要的速速来…………灌水越多,红包越多…………http://ng1.17img.cn/bbsfiles/images/2012/12/201212231928_414565_1607403_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/12/201212231928_414566_1607403_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/12/201212232112_414601_1607403_3.pnghttp://ng1.17img.cn/bbsfiles/images/2012/12/201212231933_414568_1607403_3.jpg
[color=#333333]植物甾醇能够抑制胆固醇的吸收,从而降低胆固醇。植物甾醇广泛存在于油脂和植物性食物中,例如米糠油、玉米油、芝麻油、蔬菜、水果、豆类、坚果及谷物。[/color]
一个水样铁含量很高,水混浊,测总氮是需要将水样怎么处理?过滤消解再测?
请高手指导:如果检测器堵塞,能否用载气再反向来吹出堵塞的担体?如能,做时应注意事项有哪些?
气相色谱用载气氮气,在不考虑成本的情况下,能否使用液氮?ECD FID FPD等检测器?

10,抽取5个版友);中奖名单m3071659(注册ID:m3071659)莫名其妙(注册ID:moyueqiu)zengzhengce163(注册ID:zengzhengce163)zgx3025(注册ID:v2844608)sixingxing(注册ID:v2889187)http://ng1.17img.cn/bbsfiles/images/2016/08/201608041537_603432_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/08/201608041537_603433_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================中性甾醇方法:GC基质:标准溶液应用编号:101211化合物:5-α- 胆甾烷; 粪甾醇; 胆固醇; 菜子甾醇; 粪甾酮; 菜油甾醇、菜子甾醇; 豆甾醇; β- 谷甾醇固定相:DM-225色谱柱/前处理小柱:DM-225 30m x 0.25mm x 0.25um色谱条件:柱温:260 ℃ 恒温 载气:He, 45cm/sec, 240 ℃ 进样方式:分流, 30:1, 260 ℃ 样品:中性甾醇和植物甾醇,1.5 μL, 200ng on-column 检测:FID, 8 x 10-11 AFS, 260 ℃ 文章出处:CFR00431关键字:甾醇,食品,GC,DM-225, 5-α- 胆甾烷; 粪甾醇; 胆固醇; 菜子甾醇; 粪甾酮; 菜油甾醇、菜子甾醇; 豆甾醇; β- 谷甾醇谱图:http://www.dikma.com.cn/Public/Uploads/images/CFR00431.png图例:1. 5-α- 胆甾烷;2. 粪甾醇;3. 胆固醇;4. 菜子甾醇;5. 粪甾酮;6. 菜油甾醇、菜子甾醇;7. 豆甾醇;8. β- 谷甾醇
“双蛋”期间,每天将有5课仪器分析(视频教程),对认证会员开放免分下载,普通会员每课1分下载。因为不是顺序开放,敬请各位版友关注!今天认证会员可免分下载第1-5课。下载地址:http://www.instrument.com.cn/download/search.asp?searchType=admin%5Fname&keywords=wsy18&page=3友情提示:非认证会员请尽快去论坛认证,以获得众多优惠。例如,通过认证即可获得50积分的奖励等等,详见:http://www.instrument.com.cn/bbs/shtml/20080812/1417975/
最近看到安捷伦帮助文件里编写宏的问题,不知道是否可以在Data Analysis的主菜单栏添加一个菜单加载运行自己写的macro?还望高手指教?

凯氏定氮法检测期间微生物负载情况研究1凯氏定氮法检测前后产品中微生物负载情况研究本部分主要是考察人血白蛋白原液蛋白质含量检测前后产品中微生物负载水平的变化情况。1.1 材料供试品:人血白蛋白原液蛋白质含量检测前后的制品;培养基:青岛日水生物技术有限公司生产的胰酪大豆胨营养琼脂培养基(成品),批号:20150825。30-35 ℃细菌培养箱;净化超净工作台;无菌试管等。1. 2方法(1)样品的采集采用无菌的塑料试管,对连续生产的201601批至201610批共10批人血白蛋白产品原液蛋白质含量检测前后的制品进行取样,共得到20个样品。(2)试验方法根据《中国药典》2015版三部1105通则“微生物计数法”要求,在超净工作台下,每个样品取样1 ml接种到无菌的胰酪大豆胨琼脂培养基(φ脂培培养基)上,轻轻摇动,待样品分布均匀涂布后,放置于30-35 ℃细菌培养箱中培养3天,进行细菌计数。每个样品至少接种2个平皿,同时做阴性对照。1.3实验结果经30-35 ℃培养3天后,观察平皿培养结果,发现阴性对照无细菌菌落生长,人血白蛋白原液201601批至201610批细菌含量较多,菌落数均在100 cfu/ml以上,且部分平皿无法进行细菌菌落的准确计数。结果表明,人血白蛋白产品原液蛋白质含量检测前后制品中微生物含量存在批间差异,但总体来看微生物含量较多,且检测前后明显增多。图1至8为部分批次产品凯氏定氮法检测前后微生物的负载情况,图1,3,5,7为检测前,图2,4,6,8为检测后。[align=center] [img=,250,163]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151544_01_1626619_3.png[/img][/align][align=center]图1人血白蛋白201601批 [/align][align=center][img=,236,164]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151545_01_1626619_3.png[/img][/align][align=center] 图2人血白蛋白201602批[/align][align=center][img=,251,175]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151545_02_1626619_3.png[/img][/align][align=center]图3人血白蛋白201603批[/align][align=center][img=,234,174]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151546_01_1626619_3.png[/img][/align][align=center] 图4人血白蛋白201605批[/align][align=center][img=,251,166]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151546_02_1626619_3.png[/img][/align][align=center]图5人血白蛋白201606批[/align][align=center][img=,234,165]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151546_03_1626619_3.png[/img][/align][align=center] 图6人血白蛋白201608批[/align][align=center][img=,256,156]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151546_04_1626619_3.png[/img][/align][align=center]图7 人血白蛋白201609批 [/align][align=center][img=,256,156]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151547_01_1626619_3.png[/img] [/align][align=center] 图8 人血白蛋白201610批[/align]2产品中微生物负载量变化情况研究本部分主要考察凯氏定氮法检测蛋白质含量期间,随时间的延长人血白蛋白原液中微生物负载量变化的情况。通过对比检测前后制品原液中微生物负载水平的变化情况,分析由于检测时间较长带来的微生物数量的变化情况。2.1材料2.1.1 试剂供试品:人血白蛋白原液蛋白质含量检测前的制品;培养基:青岛日水生物技术有限公司生产的胰酪大豆胨营养琼脂培养基(成品),批号:20150825。2.1.2 仪器和软件30-35 ℃细菌培养箱;净化超净工作台;无菌试管等。2.2方法2.2.1样品的采集采用无菌的塑料试管,对连续生产的201601批至201603批共3批人血白蛋白产品原液蛋白质含量检测前的制品进行取样,每批样品至少取样20 ml。2.2.2试验方法根据《中国药典》2015版三部1105通则“微生物计数法”要求,将每批样品分样到13个无菌无热源的试管中,1 ml/管。放置于10-20 ℃的条件下密封保存,在超净工作台下分别把0 min、1 min、2 min、3 min、5 min、10 min、15 min、30 min、1 h、2 h、3 h时的样品取0.1 ml接种到无菌的胰酪大豆胨琼脂培养基上,轻轻摇动,待样品分布均匀涂布后,放置于30-35 ℃细菌培养箱中培养3天,进行细菌计数。每个样品至少接种2个平皿,同时做阴性对照。2.3 实验结果经30-35 ℃培养3天后,观察平皿培养结果,发现阴性对照无细菌菌落生长,表1为人血白蛋白原液201601批至201603批样品不同时间段接种的平皿中菌落平均数,图9为201601批至201603批产品不同时间段微生物数量变化趋势。[align=center]表1 不同时间段接种的平皿中菌落平均数[/align][align=center][img=,583,142]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151550_01_1626619_3.png[/img][/align][align=center][/align][align=center][img=,606,282]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151551_01_1626619_3.png[/img][/align][align=center]图9 201601批至201603批产品不同时间段微生物数量变化趋势[/align]从培养结果看,人血白蛋白原液201601批至201603批样品0 min、1 min、2 min、3 min、5 min、10 min、15 min、30 min,样品中的菌落数几乎没有变化;1 h后样品中菌落数有增长趋势。本次试验结果表明,人血白蛋白产品原液在等待凯氏定氮法检测蛋白质含量期间,制品中微生物负载量有增长的趋势。根据试验结果推算,在2-3小时后每ml人血白蛋白原液中至少含100 CFU,那么批量1000L的制品中至少含有109 个微生物,如此数量的微生物肯定会对人血白蛋白的质量(如纯度、热源)有一定的影响。但具体使用凯氏定氮法检测人血白蛋白原液蛋白质含量前后产品质量指标(如纯度、热原质等)的变化情况还有待进一步研究。结合[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]检测技术快速检测(2-3分钟)的特点,如果在人血白蛋白实际生产中应用[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]快速检测技术,除了能够快速准确的为人血白蛋白生产提供非常有意义的指导外,还能有效控制产品中的微生物负载量,大大降低人血白蛋白产品的质量风险。参考文献刘文芳. 人血白蛋白分离工艺的历史沿革及发展 . 中国输血杂志, 2008, 21(4):323-326.倪道明.《血液制品》 . 北京:人民卫生出版社, 2003.03: 19.Quinlan GJ,Martin GS, Evans TW. Albumin: biochemical properties and therapeutic potential . Hepatology. 2005. 41(6):1211-9.杨阳, 刘玉红, 王凤山.《人血清白蛋白的制备与应用研究进展》 .《中国药学杂志》, 2011, 46(24):1857-1860.杨晓波, 王晓雷, 王峰.人血白蛋白提取工艺的对比分析与改进方案 . 生命科学仪器, 2010, 08(2):44-48.张建军, 高缘, 孙婉瑾. 白蛋白作为药物载体的研究 . 化学进展, 2011, 23(8): 1747-1754.郭宾,李川. 药物与血浆蛋白结合的药理学基础及其研究进展 . 中国临床药理学和治疗学, 2005, 10(3): 241-253.张敏. 人血浆白蛋白的生理功能及临床应用 . 四川生理科学杂志, 2011, 33(1):36-38.肖婷予, 王斌. 人血白蛋白临床应用调查与分析 . 药物与临床, 2010, 45(13)1036.
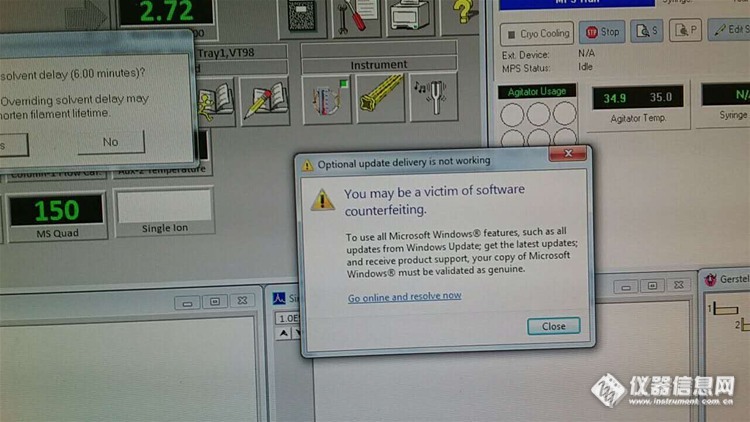
为何工作站界面老是弹出如下图这个对话窗口呢?http://simg.instrument.com.cn/bbs/images/default/emyc1010.gif弹出来,关闭了,一会它又弹出来!!!http://simg.instrument.com.cn/bbs/images/default/em09501.gifhttp://ng1.17img.cn/bbsfiles/images/2017/04/201704241436_01_2911392_3.jpg友友们,有遇到这个情况的吗?老是弹出来看起来好烦!http://simg.instrument.com.cn/bbs/images/default/em09504.gif如何才能不让这个窗口再弹出呢?http://simg.instrument.com.cn/bbs/images/default/emyc1010.gif
凯氏定氮法检测期间微生物负载情况研究1凯氏定氮法检测前后产品中微生物负载情况研究本部分主要是考察人血白蛋白原液蛋白质含量检测前后产品中微生物负载水平的变化情况。1.1 材料供试品:人血白蛋白原液蛋白质含量检测前后的制品;培养基:青岛日水生物技术有限公司生产的胰酪大豆胨营养琼脂培养基(成品),批号:20150825。30-35 ℃细菌培养箱;净化超净工作台;无菌试管等。1. 2方法(1)样品的采集采用无菌的塑料试管,对连续生产的201601批至201610批共10批人血白蛋白产品原液蛋白质含量检测前后的制品进行取样,共得到20个样品。(2)试验方法根据《中国药典》2015版三部1105通则“微生物计数法”要求,在超净工作台下,每个样品取样1 ml接种到无菌的胰酪大豆胨琼脂培养基(φ脂培培养基)上,轻轻摇动,待样品分布均匀涂布后,放置于30-35 ℃细菌培养箱中培养3天,进行细菌计数。每个样品至少接种2个平皿,同时做阴性对照。1.3实验结果经30-35 ℃培养3天后,观察平皿培养结果,发现阴性对照无细菌菌落生长,人血白蛋白原液201601批至201610批细菌含量较多,菌落数均在100 cfu/ml以上,且部分平皿无法进行细菌菌落的准确计数。结果表明,人血白蛋白产品原液蛋白质含量检测前后制品中微生物含量存在批间差异,但总体来看微生物含量较多,且检测前后明显增多。图1至8为部分批次产品凯氏定氮法检测前后微生物的负载情况,图1,3,5,7为检测前,图2,4,6,8为检测后。[align=center] [img=,250,163]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151544_01_1626619_3.png[/img][/align][align=center]图1人血白蛋白201601批 [/align][align=center][img=,236,164]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151545_01_1626619_3.png[/img][/align][align=center] 图2人血白蛋白201602批[/align][align=center][img=,251,175]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151545_02_1626619_3.png[/img][/align][align=center]图3人血白蛋白201603批[/align][align=center][img=,234,174]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151546_01_1626619_3.png[/img][/align][align=center] 图4人血白蛋白201605批[/align][align=center][img=,251,166]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151546_02_1626619_3.png[/img][/align][align=center]图5人血白蛋白201606批[/align][align=center][img=,234,165]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151546_03_1626619_3.png[/img][/align][align=center] 图6人血白蛋白201608批[/align][align=center][img=,256,156]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151546_04_1626619_3.png[/img][/align][align=center]图7 人血白蛋白201609批 [/align][align=center][img=,256,156]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151547_01_1626619_3.png[/img] [/align][align=center] 图8 人血白蛋白201610批[/align]2产品中微生物负载量变化情况研究本部分主要考察凯氏定氮法检测蛋白质含量期间,随时间的延长人血白蛋白原液中微生物负载量变化的情况。通过对比检测前后制品原液中微生物负载水平的变化情况,分析由于检测时间较长带来的微生物数量的变化情况。2.1材料2.1.1 试剂供试品:人血白蛋白原液蛋白质含量检测前的制品;培养基:青岛日水生物技术有限公司生产的胰酪大豆胨营养琼脂培养基(成品),批号:20150825。2.1.2 仪器和软件30-35 ℃细菌培养箱;净化超净工作台;无菌试管等。2.2方法2.2.1样品的采集采用无菌的塑料试管,对连续生产的201601批至201603批共3批人血白蛋白产品原液蛋白质含量检测前的制品进行取样,每批样品至少取样20 ml。2.2.2试验方法根据《中国药典》2015版三部1105通则“微生物计数法”要求,将每批样品分样到13个无菌无热源的试管中,1 ml/管。放置于10-20 ℃的条件下密封保存,在超净工作台下分别把0 min、1 min、2 min、3 min、5 min、10 min、15 min、30 min、1 h、2 h、3 h时的样品取0.1 ml接种到无菌的胰酪大豆胨琼脂培养基上,轻轻摇动,待样品分布均匀涂布后,放置于30-35 ℃细菌培养箱中培养3天,进行细菌计数。每个样品至少接种2个平皿,同时做阴性对照。2.3 实验结果经30-35 ℃培养3天后,观察平皿培养结果,发现阴性对照无细菌菌落生长,表1为人血白蛋白原液201601批至201603批样品不同时间段接种的平皿中菌落平均数,图9为201601批至201603批产品不同时间段微生物数量变化趋势。[align=center]表1 不同时间段接种的平皿中菌落平均数[/align][align=center][img=,583,142]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151550_01_1626619_3.png[/img][/align][align=center][/align][align=center][img=,606,282]http://ng1.17img.cn/bbsfiles/images/2017/09/201709151551_01_1626619_3.png[/img][/align][align=center]图9 201601批至201603批产品不同时间段微生物数量变化趋势[/align]从培养结果看,人血白蛋白原液201601批至201603批样品0 min、1 min、2 min、3 min、5 min、10 min、15 min、30 min,样品中的菌落数几乎没有变化;1 h后样品中菌落数有增长趋势。本次试验结果表明,人血白蛋白产品原液在等待凯氏定氮法检测蛋白质含量期间,制品中微生物负载量有增长的趋势。根据试验结果推算,在2-3小时后每ml人血白蛋白原液中至少含100 CFU,那么批量1000L的制品中至少含有109 个微生物,如此数量的微生物肯定会对人血白蛋白的质量(如纯度、热源)有一定的影响。但具体使用凯氏定氮法检测人血白蛋白原液蛋白质含量前后产品质量指标(如纯度、热原质等)的变化情况还有待进一步研究。结合[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]检测技术快速检测(2-3分钟)的特点,如果在人血白蛋白实际生产中应用[url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]近红外光谱[/color][/url]快速检测技术,除了能够快速准确的为人血白蛋白生产提供非常有意义的指导外,还能有效控制产品中的微生物负载量,大大降低人血白蛋白产品的质量风险。参考文献刘文芳. 人血白蛋白分离工艺的历史沿革及发展 . 中国输血杂志, 2008, 21(4):323-326.倪道明.《血液制品》 . 北京:人民卫生出版社, 2003.03: 19.Quinlan GJ,Martin GS, Evans TW. Albumin: biochemical properties and therapeutic potential . Hepatology. 2005. 41(6):1211-9.杨阳, 刘玉红, 王凤山.《人血清白蛋白的制备与应用研究进展》 .《中国药学杂志》, 2011, 46(24):1857-1860.杨晓波, 王晓雷, 王峰.人血白蛋白提取工艺的对比分析与改进方案 . 生命科学仪器, 2010, 08(2):44-48.张建军, 高缘, 孙婉瑾. 白蛋白作为药物载体的研究 . 化学进展, 2011, 23(8): 1747-1754.郭宾,李川. 药物与血浆蛋白结合的药理学基础及其研究进展 . 中国临床药理学和治疗学, 2005, 10(3): 241-253.张敏. 人血浆白蛋白的生理功能及临床应用 . 四川生理科学杂志, 2011, 33(1):36-38.肖婷予, 王斌. 人血白蛋白临床应用调查与分析 . 药物与临床, 2010, 45(13)1036.
下载的总氮标准,打印时被保护,需要权限密码,是最近有什么变化吗?以前没遇到过
祝大家圣诞快乐!今天认证会员可免分下载如下全套资料:1、“现代色谱分析”视频教程(第1-16课);2、“波谱分析”视频教程(第1-32课)。下载地址:http://www.instrument.com.cn/download/search.asp?searchType=admin%5Fname&keywords=wsy18&page=3友情提示:非认证会员请尽快去论坛认证,以获得众多优惠。例如,通过认证即可获得50积分的奖励等等。详见:http://www.instrument.com.cn/bbs/shtml/20080812/1417975/
再制蛋类产品省级监督抽查质量不合格产品及其企业名单序号企业名称产品名称规格商标生产日期主要不合格项目不合格 项目标准规定值产品明示值实测值1厦门凰华食品有限公司烤蛋/个/40353山梨酸g/kg不得检出/0.3
同时用热导检测器分析氢、氧、氮用氩气作载气好还是氦气好?灵敏度会是一样吗?