乙酸对叔丁基环己酯 和乙酸邻叔丁基环己酯如何区分?谢谢
求助硫酸特布他林雾化溶液原研在国内上市的说明书和进口标准!!!谢谢!!!!!!
用氨基酸自动分析仪测定氨基酸含量,配制不同pH的柠檬酸钠缓冲液的作用是什么?是淋洗不同的氨基酸?如果用732阳离子树脂吸附氨基酸,用氨水来淋洗,测定氨基酸总量,原理上可行吗?谢谢!
土壤样品使用HF,HCL,HNO3,HCLO4四酸消解,ICP-AES测试后的磷是全磷吗
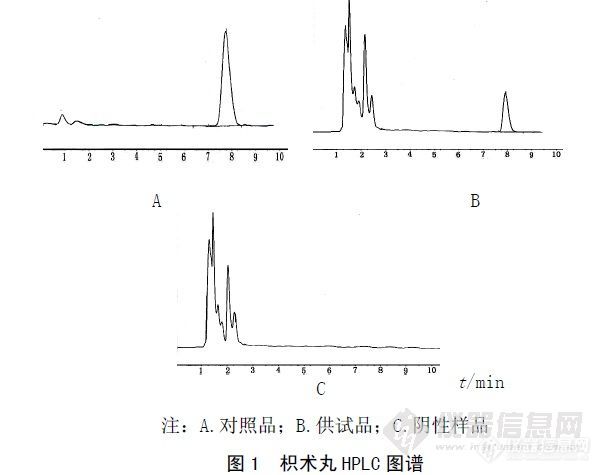
作者:蔡俊安;(河南百年康鑫药业有限公司;)摘要:目的建立枳术丸中辛弗林含量测定的方法。方法采用高效液相色谱法,Diamonsil ODS1 C18色谱柱,以甲醇-磷酸二氢钾水溶液(取磷酸二氢钾0.6 g、十二烷基磺酸钠1.0 g、冰醋酸1 mL,加水溶解并稀释至1 000 mL,50∶50)为流动相,流速为1.0 mL/min,λ=275 nm。结果辛弗林在0.065 6~0.656μg范围内呈良好线性,回归方程为:Y=478 526.3X+827.146,r=0.999 8,平均加样回收率为99%,RSD=0.99%(n=6)。结论本方法简便、准确,专属性强,测定结果重复性好,为枳术丸中辛弗林的定量分析提供了有效方法。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208131030_383386_1606903_3.jpg
请问大家遇到过女贞醛,乙酸邻叔丁基环己酯只是看到一个峰,第二个看不到的情况?含量较小时候。
各位色友:利用高效液相分析醇酸树脂中的醇和酸,关键如何进行前处理,请不吝赐教,谢谢!!!!
请问哪位版友有农产品中三氯异氰尿酸、三乙膦酸铝、氟苯脲、氟吡甲禾灵、氟酰胺、环酰菌胺的测定方法? 三氯异氰尿酸在棉花、水稻上的测定方法,三乙膦酸铝在蔬菜、水果中的测定方法,氟苯脲在蔬菜、水果中的测定方法,氟吡甲禾灵在水果、咖啡豆中的测定方法,氟酰胺在稻米中测定方法,环酰菌胺在蔬菜、水果及其干制品中的测定方法。最好是国标或行标。先致谢了。

NY/T1275-2007蔬菜水果中吡虫啉残留量的测定,这个试验有人做过吗?http://ng1.17img.cn/bbsfiles/images/2013/10/201310232111_472518_1645480_3.jpg第二行“上述浓缩试样用10mL石油醚+乙酸乙酯(8.5+1.5)分三次移入小柱,弃去淋洗液”既然浓缩试样用石油醚+乙酸乙酯分三次移入小柱,为何要弃去淋洗液,这时淋洗液里不是已经含有浓缩试样了吗?

10,抽取5个版友);中奖名单:dyd3183621(注册ID:dyd3183621)WUYUWUQIU(注册ID:wulin321)zgx3025(注册ID:v2844608)捌道巴拉巴巴巴(注册ID:v3082413)牛一牛(注册ID:v2700892)http://ng1.17img.cn/bbsfiles/images/2016/11/201611221514_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/11/201611221514_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================枸橼酸喷托维林片方法:HPLC基质:药品应用编号:101511化合物:枸橼酸喷托维林固定相:Diamonsil C18(2)色谱柱/前处理小柱:Diamonsil C18(2) 5u 150 x 4.6mm样品前处理:【有关物质】 取本品细粉适量(约相当于枸橼酸喷托维林50 mg),置50 ml量瓶中,加流动相适量,超声5 min,振摇使枸橼酸喷托维林溶解用流动相稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液;精密量取1 ml,置100 ml量瓶中,用流动相稀释至刻度,摇匀,作为对照溶液。 【含量测定】 取本品20片,精密称定,研细,精密称取适量(约相当于枸橼酸喷托维林25 mg),置100 ml量瓶中,加流动相适量,超声5 min,振摇使枸橼酸喷托维林溶解,用流动相稀释至刻度,摇匀,滤过,测定。色谱条件:检测波长:UV 215 nm 流动相:水(取三乙胺10 ml,用水稀释至1000 ml,用磷酸调节p H至3.0)-甲醇(45:55) 洗脱方式:等度 进样量:20 ul文章出处:P525关键字:枸橼酸喷托维林,2010版中国药典,HPLC,含量测定,钻石二代,Diamonsil C18(2),2010版中国药典,HPLC,含量测定,钻石二代,Diamonsil C18(2)谱图:http://www.dikma.com.cn/Public/Uploads/images/juyuansuanpentuoweilin-1.GIFhttp://www.dikma.com.cn/Public/Uploads/images/juyuansuanpentuoweilin-2.GIFhttp://www.dikma.com.cn/Public/Uploads/images/juyuansuanpentuoweilin-3.GIF
试问:硫酸铈能否氧化对叔丁基苯酚?可以直接电位滴定测对叔丁基苯酚的纯度吗?实验室电位滴定仪:梅特勒T50。若手动滴定,指示剂采用二苯胺磺酸钠还是邻二氮杂菲-亚铁?望指点
最近摸索一些有机磷[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]条件,发现用2mmol/L乙酸铵做流动相时,上述两种物质响应很差,峰型也不好看,换成纯水后响应也高了,峰型也好看了,很奇怪为啥乙酸铵对这其离子化有抑制作用呢?
磷用还原性酸的影响有多大?
林可霉素,盐酸克林霉素,大观霉素,3种药物的ASE和手动2种方式提取大观霉素回收率低,药物极性强,易溶于水,溶于甲醇。乙腈,甲醇,水,甲酸水都已试过,求各位大神指教。
求助高效液相色谱法测盐酸氯卡色林有关物质及含量的测定[b],[color=#444444]还有手性纯度的测定方法。[/color][/b]
方法GBT 18204.2-2014 公共场所卫生检验方法 第2部分 化学污染物尿素的测定中安替比林需要先用1+1硫酸溶解,然后用混酸定容,硫酸浓度不能大于1+1,想问一下混酸怎么配置?[img]https://ng1.17img.cn/bbsfiles/images/2019/01/201901110813319903_3040_3472894_3.png[/img]
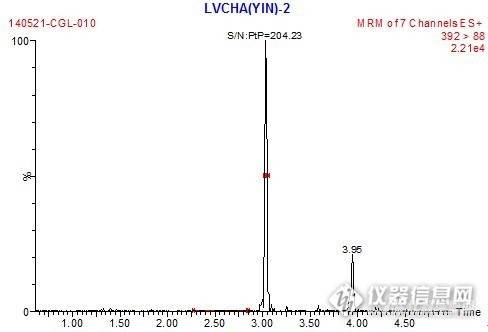
【生活中的仪器分析】样 品:蔬菜、水果、茶叶、茶粉等食品检测项目:草甘膦、草铵膦、氨甲基膦酸参考标准:SN/T 1923-2007检测仪器:a.WATERS液相色谱串联质谱仪:配有电喷雾(ESI)离子源(可用其他品牌作用等效的高效液相色谱质谱仪替代)b.Biotagevacmaster固相萃取仪c.IPRE Qclean PMG草甘膦专用固相萃取柱d.BiotageTurbovap LV 快速浓缩仪e.IKA MS3 涡旋混匀器g.TOMY-MX307离心机g.昆山超声波清洗器实验过程:1.提取及预处理称取2-5g(精确到0.001g)试样于50 mL聚丙烯离心管中,加入100μL内标液,加入20.0 mL水超声提取30min,于10000 r/min离心5min,取1.0 mL上清液于2mL子弹头离心管中,加入100μL酸度调节剂(注A),涡旋混匀,15000r/min离心5 min,待净化。注A:酸度调节剂配制方法:纯水+色谱纯甲醇+盐酸=160+40+13.4(V/V/V)2.固相萃取净化І将PMG-І柱(蓝柱)用2mL甲醇和2 mL 0.5%甲酸淋洗活化并自然滴干,将加入酸度调节剂处理的提取液(2)转移到小柱上,用5mL刻度试管收集流出液(1-2滴/秒),用1.0mL 0.5%甲酸洗柱并真空抽干,合并流出液,用移液枪吸取50%NaOH调pH7-9(用1-14pH试纸,根据样品不同约20-50μL),加水定容到3 mL刻度,混匀,待衍生。3.衍生步骤准确吸取600 μL净化液(3)于2mL子弹头离心管中,加入200 μL 5%硼砂溶液,边涡旋,边加入200 μL 25g/L FMOC-Cl乙腈溶液(注B),放置10min,加入50 μL甲酸,涡旋混匀,15000 r/min离心5min,吸取上清液准备过PMG-ІІ柱。注B:25 g/L FMOC-Cl乙腈溶液配制方法:称取0.25 gFMOC-Cl,溶解于10 mL色谱纯乙腈中。4.固相萃取净化ІІ 将PMG-ІІ柱(红柱)用2 mL甲醇和2 mL 0.5%甲酸淋洗并自然滴干,将上清液过PMG-ІІ柱,用3 mL水淋洗小柱,真空抽干5-10 min,再加入2 mL正己烷淋洗小柱,滴干后真空抽干5 min,最后用5 mL 5%氨水/甲醇洗脱小柱(1-2 mL/min)并用5 mL刻度试管收集流出液,45℃,氮气吹至近干,用20%乙腈定容1.0 mL,涡旋混匀,过0.2 μm PTFE膜后上机测试。5.测定5.1色谱条件a.色谱柱:Waters BEH-C18,1.7 μm,2.1 mm×100 mm;b.流动相:5mmol/L乙酸铵:乙腈梯度洗脱,梯度表见表1; 表1 流动相及梯度 时间(min)流速(mL/min)5mmol/L乙酸铵(%)乙腈(%)00.3901020.362384.40.362384.50.35956.50.35956.60.390109.00.39010c.检测器:串联四极杆质谱仪;d.柱温:35℃;e.进样量:10 μL。5.2质谱分析条件a)电离源:电喷雾正离子模式;b)毛细管电压:3.50KV;c)源温度:120℃;d)脱溶剂气温度:400℃;e)脱溶剂气流量:700L/h;f)碰撞室压力:2.7í10-3mbar;g)特征离子及参数见表2。 表 2 草甘膦和氨甲基膦酸的主要特征离子 化合物保留时间(min)母离子+(m/z)锥孔电压(V)子离子(m/z)碰撞能量(eV)草甘膦1.32392.215*88.02515214.01
做黄酒总糖检测,配备费林乙液要求用酒石酸钾钠试剂,单位买的是含四个结晶水的酒石酸钾钠,有同行说必须用无水的酒石酸钾钠才行。个人认为标准没指明用哪种,那么用含结晶水的也就可以了。想问问各位,用哪个才对?
求氨基酸邻啡咯啉铜配合物的相关文献,谢谢各位老师了
求助肠溶阿司匹林片中游离水杨酸的含量测定!谢谢大家了!
各位老师你们好,我们现在遇到一个难题,硫磷混合酸中硫酸的测定,请大家帮助,谢谢!
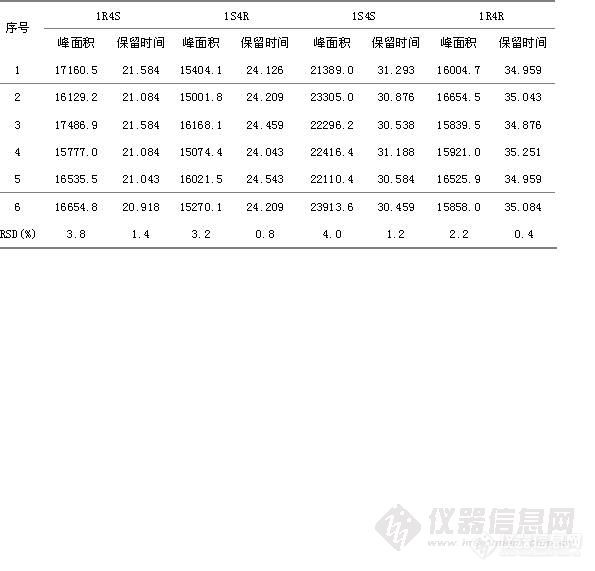
HPLC法测定盐酸舍曲林片的有关物质 摘要:目的:建立盐酸舍曲林片有关物质的测定方法,其外标法测定其四种光学异构体,自身对照法测定其它有关杂质。方法:采用依利特Hypersil ODS2色谱柱(4.6mm×150mm,5μm);流动相为磷酸二氢钠缓冲液 β-环糊精12.8g,HP-β-环糊精17.3g,加水至1000ml]-乙腈[font=Times New Roman]-[font=宋体]三乙胺([font=Times New Roman]800[font=宋体]:[font=Times New Roman]200[font=宋体]:[font=Times New Roman]10[font=宋体])[font=Times New Roman],[font=宋体]用磷酸调节[font=Times New Roman]p H [font=宋体]为[font=Times New Roman]2.5±0.5为流动相,流速为每分钟1ml/min,检测波长为214nm。结果:建立了β-环糊精、HP-β-环糊精手性流动相拆分盐酸舍曲林光学异构体,的方法,结论:该方法专属性好,无干扰,盐酸舍曲林异构体与主峰分离良好。可作为控制盐酸舍曲林片质量的方法。关键词:HPLC外标法;HPLC自身对照法;盐酸舍曲林片;光学异构体; β-环糊精; HP-β-环糊精。盐酸舍曲林是一种选择性抑制[font=Times New Roman]5-[font=宋体]羟色胺再摄取的抗抑郁药([font=Times New Roman]SSRI[font=宋体]),为新一代抗抑郁药的代表药物,目前已跃成为抗抑郁治疗的一线药和首选药。盐酸舍曲林由美国辉瑞公司开发,并于[font=]1990[font=宋体]年[font=]12[font=宋体]月最初在英国上市,目前为止已经在[font=]30[font=宋体]个国家陆续上市。盐酸舍曲林(商品名:郁尔复片剂)于[font=Times New Roman]1996[font=宋体]年[font=Times New Roman]12[font=宋体]月获得中国药品行政保护,并于当年在中国以片剂形式(不含原料药)上市,用于治疗精神抑郁症。现在国内各大医院、药店均有销售。盐酸舍曲林在中国无专利保护。[font=Times New Roman]2004[font=宋体]年[font=Times New Roman]6[font=宋体]月该行政保护终止。由于盐酸舍曲林存在4种光学异构体,在合成工艺过程中可能会引入中间杂质盐酸舍曲林顺式左旋异构体,盐酸舍曲林反式左旋异构体,反式右旋异构体,因其均为手性异构体,眼前其异构体检测方法为毛细管电泳法,且只对其异构体顺式左旋异构体进行检测,其它杂质检测采用反相HPLC,且其盐酸舍曲林主峰不能很好的与其相邻异构体分开,参照相关文献,并经方法学研究,建立了盐酸舍曲林有关物质的检测方法,采用HPLC外标法测定[
http://simg.instrument.com.cn/bbs/images/default/emyc1007.gif支持分坛团队和化学药分析版。我公司产品注射用帕米膦酸二钠执行标准为《中国药典》2010年版二部。含量测定项下的内容为:“【含量测定】照离子色谱法(附录 V J)测定色谱条件与系统适用性试验用阴离子交换色谱柱;以3mmol/L草酸溶液为流动相,流速为每分钟1.2ml;检测器为电导检测器。理论板数按帕米瞵酸二钠峰计算不低于2000。”我们在检测中发现,含量测定色谱柱的理论塔板数下降较快。经研究,将流动相由“3mmol/L草酸溶液”改变为“**溶液”,可使柱效明显稳定。方法学验证结果显示,变更后的方法准确、可靠。可用于我公司产品注射用帕米膦酸二钠含量测定。1仪器与试药1.1仪器岛津LC-20A高效液相色谱仪,配CDD-10A VP电导检测器。所用仪器和量具均经校准或检定。1.2试药对照品帕米膦酸二钠(经160℃干燥至恒重,按干燥品计含量100.2%,按100%计。)。辅料、水为超纯水。2方法与结果2.1色谱条件色谱柱Dionex IonPac AS22阴离子交换色谱柱(4 mm ×250 mm),配保护柱(4 mm ×50 mm);流动相**溶液;检测器为电导检测器;柱温35℃;流速1.2ml/min。进样量为20μl。理论塔板数按帕米膦酸二钠峰计算应不低于2000。2.2溶液的制备2.2.1空白辅料储备液:取辅料适量,按处方配成溶液备用。2.2.2空白辅料溶液:取空白辅料储备液5ml置于50ml容量瓶中,加水定容至刻度。2.2.3对照品溶液:精密称取帕米膦酸二钠对照品约30mg,置于50ml容量瓶中,用水溶解并定容。2.2.4供试品溶液:精密称取帕米膦酸二钠对照品适量(根据不同验证项目,称取不同量),置于50ml容量瓶中,加水溶解后,加入5ml空白辅料储备液并用水定容。2.3专属性试验空白溶剂:水。取空白溶剂、空白辅料溶液、对照品溶液、供试品溶液,照2.1色谱条件,依法测定,记录色谱图。(附图略)结果显示,对照品溶液和供试品溶液的色谱图中帕米膦酸二钠峰与其他峰之间分离度良好,分离度大于1.5;空白溶剂及空白辅料溶液色谱图中在帕米膦酸二钠峰处无干扰峰。本方法有良好的专属性。2.4 线性关系及范围精密称取帕米膦酸二钠对照品14.58、24.28、30.58、36.13、45.80 mg,分别置50ml量瓶中,用水适量溶解后,加入5ml空白辅料储备液并用水定容,摇匀,制成每1ml中含帕米膦酸二钠0.2916、0.4856、0.6116、[/fon
目的:通过观察盐酸林可霉素对小鼠肠道菌群,肠道组织病理学改变,血中淋巴细胞数的影响规律,以期为科学研究正确使用盐酸林可霉素造成菌群失调动物模型提供参考资料。方法:盐酸林可霉素连续灌胃3d停止给药,于停药后第1天,第4天,第7天,和第10天检测肠球菌数,双歧杆菌数,血中淋巴细胞数和肠道病理改变,评价盐酸林可霉素对小鼠肠道菌群的影响规律。结果:灌胃3d停止用药后第1天和第4天双歧杆菌减少,肠球菌增加,与正常组比较差异有统计学意义(P0.05),肠道黏膜皱褶变浅,上皮内杯状细胞减少。停药后第1天出现血中淋巴细胞数减少。结论:盐酸林可霉素短期大量给药,可造成小鼠菌群失调,肠道组织损伤,免疫功能受损,该损伤持续约1周。盐酸林可霉素是科学研究中用于造成菌群失调动物模型的常用抗生素,其抑制细菌生长,尤其抑制益生菌的作用非常明显,但各家用该药的方法、剂量有较大差别,由于动物的耐受性较强,菌群失调能持续的时间不清,本实验尝试在肠道菌群变化、肠组织损伤等方面来研究林可霉素造成菌群失调的规律。以期为该药在科学研究中的使用提供数据依据,现报告如下。
15%硫磷混酸该怎么配啊?谢谢。
用原子荧光做有机膦酸类阻垢缓蚀剂羟基亚乙基二膦酸(HEDP)中砷含量和用ICP做出的结果差别很大,不知道为何,请高手指点
在反应釜内,将盐酸在釜内喷淋。[em0912]
[font=&][color=#333333]一、固定和保存总磷[/color][/font] [font=&][color=#333333]加入硫酸可以固定和保存水样中的总磷,防止其在保存过程中发生化学变化或生物降解,从而确保测定结果的准确性。硫酸的强酸性可以抑制微生物的活性,减少其对水样中有机物的分解作用,同时也有助于保持水样中磷的化学形态稳定。[/color][/font] [font=&][color=#333333]二、调节pH值[/color][/font] [font=&][color=#333333]硫酸的加入还可以调节水样的pH值,使其达到适合总磷测定的范围。在总磷的测定过程中,通常需要将水样调节至酸性环境,以促进磷的释放和转化,使其更易于被测定。硫酸作为一种强酸,可以有效地降低水样的pH值,满足测定要求。[/color][/font] [font=&][color=#333333]三、促进磷的转化[/color][/font] [font=&][color=#333333]硫酸的加入还有助于促进水样中不同形态磷的转化。例如,在酸性条件下,磷酸盐的水解和分解速度会加快,从而使其转化成更易于分析的形式。这对于提高总磷测定的灵敏度和准确性具有重要意义。[/color][/font] [font=&][color=#333333]四、减少干扰[/color][/font] [font=&][color=#333333]在某些情况下,水样中可能含有其他干扰物质,如铁、铝等金属离子或悬浮物等。这些干扰物质可能会影响总磷的测定结果。硫酸的加入可以在一定程度上减少这些干扰物质的影响,提高测定的准确性。[/color][/font] [font=&][color=#333333]五、其他注意事项[/color][/font] [font=&][color=#333333]在加入硫酸时,需要注意以下几点:[/color][/font] [font=&][color=#333333]硫酸的加入量应根据水样的具体情况和测定方法进行确定,避免过量或不足。[/color][/font] [font=&][color=#333333]加入硫酸后应充分混匀水样,以确保其均匀分布。[/color][/font] [font=&][color=#333333]在测定前需要对水样进行适当的前处理,如过滤、稀释等,以去除悬浮物和干扰物质。[/color][/font]
[font=&][color=#333333]一、固定和保存总磷[/color][/font] [font=&][color=#333333]加入硫酸可以固定和保存水样中的总磷,防止其在保存过程中发生化学变化或生物降解,从而确保测定结果的准确性。硫酸的强酸性可以抑制微生物的活性,减少其对水样中有机物的分解作用,同时也有助于保持水样中磷的化学形态稳定。[/color][/font] [font=&][color=#333333]二、调节pH值[/color][/font] [font=&][color=#333333]硫酸的加入还可以调节水样的pH值,使其达到适合总磷测定的范围。在总磷的测定过程中,通常需要将水样调节至酸性环境,以促进磷的释放和转化,使其更易于被测定。硫酸作为一种强酸,可以有效地降低水样的pH值,满足测定要求。[/color][/font] [font=&][color=#333333]三、促进磷的转化[/color][/font] [font=&][color=#333333]硫酸的加入还有助于促进水样中不同形态磷的转化。例如,在酸性条件下,磷酸盐的水解和分解速度会加快,从而使其转化成更易于分析的形式。这对于提高总磷测定的灵敏度和准确性具有重要意义。[/color][/font] [font=&][color=#333333]四、减少干扰[/color][/font] [font=&][color=#333333]在某些情况下,水样中可能含有其他干扰物质,如铁、铝等金属离子或悬浮物等。这些干扰物质可能会影响总磷的测定结果。硫酸的加入可以在一定程度上减少这些干扰物质的影响,提高测定的准确性。[/color][/font] [font=&][color=#333333]五、其他注意事项[/color][/font] [font=&][color=#333333]在加入硫酸时,需要注意以下几点:[/color][/font] [font=&][color=#333333]硫酸的加入量应根据水样的具体情况和测定方法进行确定,避免过量或不足。[/color][/font] [font=&][color=#333333]加入硫酸后应充分混匀水样,以确保其均匀分布。[/color][/font] [font=&][color=#333333]在测定前需要对水样进行适当的前处理,如过滤、稀释等,以去除悬浮物和干扰物质。[/color][/font]
哪位大虾能否解释一下“临界酸浓度”的概念!xiexie[em11]