以下所述校正因子均为FID中物质相对正庚烷的相对校正因子! 查资料环己酮的FID校正因子为1.38,但是环己醇仅有TCD的校正因子,无FID的校正因子。 若按照有效碳数法计算,查资料羰基贡献为0,即环己酮校正因子按有效碳数法计算:7*98/(100*5)=1.37。请问下羟基的贡献是多少呢,环己醇FID校正因子是多少? 文献理论上看,羰基贡献为0,羟基贡献应大于零,也就是说环己醇的响应因子应比环己酮大,也就是环己醇的校正因子比环己酮小。 仪器实测环己酮校正因子1.20,环己醇1.11。 求帮助!
[color=#444444]环己烯水合制备环己醇的实验,反应结束后用乙酸乙酯萃取,最终得到含有环己烯、环己醇、乙酸乙酯的有机相(应该有一些副产物)。[/color][color=#444444] [url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析产物中环己烯和环己醇的质量,来确定环己烯的转化率和反应选择性。准备用内标法,没确定好用什么内标物,最好是毒性比较小的,望大神相助!谢谢![/color]
求助:工业级环己醇测定的相关国标
[color=#444444]双氧水做氧化剂,杂多酸做催化剂氧化环己醇,反应产物主要是环己酮([url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析)外,还有己二酸,除此之外还有什么产物?越具体越好,分别用用什么方法定性定量分析?[/color]
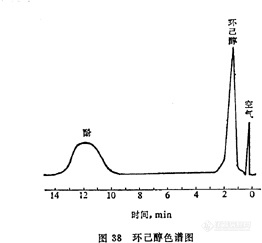
空气中环己醇的测定方法 1 原理空气中环己醇、酚经己二酸乙二醇聚酯柱分离后,用氢焰离子化检测器检测,以保留时间定性,峰高定量。2 仪器2.1 注射器,100ml,1ml。2.2 微量注射器,1微升。2.3 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],氢焰离子化检测器。5ng环己醇给出的信噪比不低于3∶1。色谱柱:柱长2m,内径4mm不锈钢柱。己二酸乙二醇聚酯:201担体=15∶100柱温:120℃汽化室温度:170℃检测室温度:140℃载气(氮气):48ml/min3 试剂3.1 环己醇,色谱纯。3.2 己二酸乙二醇聚酯,色谱固定液。3.3 201担体,40~60目。4 采样取100ml注射器,在采样点用现场空气抽洗3次,然后抽取100ml空气,将注射器套上橡皮帽,垂直放置,当天分析。5 分析步骤5.1 对照试验:将100ml注射器取下塑料帽,抽取100ml清洁空气,与样品同时分析,作为对照。5.2 样品处理:将样品与对照样品注射器垂直放置,记录实验室的温度和气压。5.3 标准曲线的绘制:用微量注射器准确抽取一定量的环己醇(于20℃时1微升环己醇质量为0.9624mg)注入100ml注射器中,配成一定浓度的标准气体。取一定量的上述标准气体用空气稀释成0.025、0.050、0.1、0.5微克/ml的标准气体。[img]http://ng1.17img.cn/bbsfiles/images/2007/05/200705201514_52393_1625938_3.jpg[/img]分别取1ml进样,测量保留时间及峰高,每个浓度重复3次,取峰高的平均值,以环己醇的含量对峰高作图,绘制标准曲线。保留时间为定性指标。5.4 测定:取1ml空气样品直接进样,用保留时间定性,峰高定量。6 计算X=C*1000/V0式中:X——空气中环己醇的浓度,mg/m3;C——由标准曲线上查出的环己醇含量,微克;V0——标准状况下的样品体积,ml。7 说明7.1 本法不能将环己醇与环己酮分离。7.2 本法检测限为5ng。
老师您好!关于环己烷氧化产物的分析我还有一个问题要请教:环己烷氧化的主要产物是环己醇、环己酮、己二酸以及己二酸二环己醇酯。我目前需要测定这些氧化产物的浓度,以确定氧化过程动力学方程。关于前两种产物,文献中已有现成的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析法;关于后两种产物酸、酯的分析,却依然在采用误差比较大、费时比较久的化学滴定法。我想放弃化学分析法,而采用可能误差会小一些而且又切实可行的某种仪器分析法比如高效液相色谱,但不知是否可行而且也不知道该如何去寻找合适的色谱条件和具体分析方法。请前辈多多指教!
我要分离苯 环己烷 环己醇 环己烯 采用GC1690 SE-54毛细管色谱柱 分离条件如何选择啊
要测定环己醇和环己酮的校正因子?该用什么做内标物比较好?对柱温等其他温度该怎样设定比较好?另外麻烦高手教一下怎样设置程序升温啊
分离苯 环己烷 环己醇 环己烯 采用GC1690 SE-54毛细管色谱柱 分离条件如何选择啊
我的原料是辛烯、产物为1,2-辛二醇。内标想用环己醇。[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]是北分的SP-3420A。我用什么色谱柱合适?
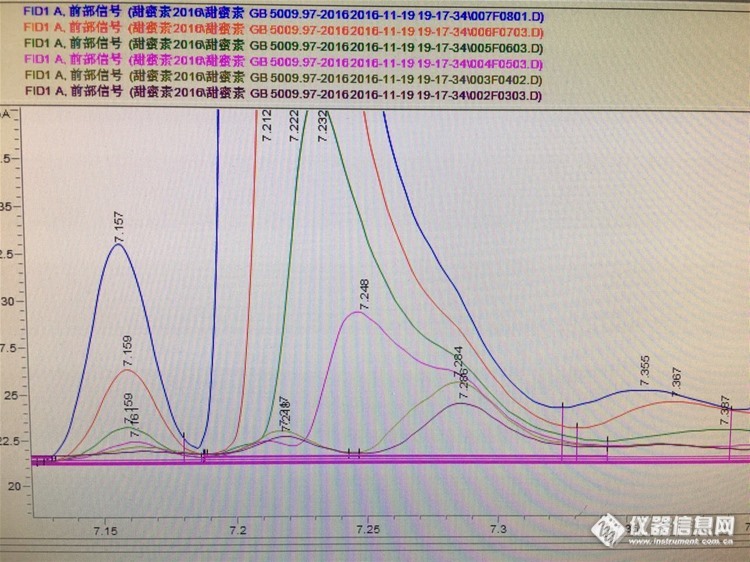
请问有人做GB 5009.97-2016的甜蜜时光素吗?为什么浓度低的环己醇的峰很奇怪……好友回复:进的标品的话,那就只能舍弃这个点了,这不关浓度的事,因为各物质都存在响应的高低,既然标品都成这样了,如果配置过程中没问题,那就是这个浓度不行了,你先再老化一下柱子吧,你重新割一下柱子,并且确保切口平整,柱子伸进进样口最好5mm这样,先从高浓度开始进样,试试看吧大家说说看~http://ng1.17img.cn/bbsfiles/images/2017/01/201701191701_669708_3150883_3.jpghttp://ng1.17img.cn/bbsfiles/images/2017/10/2016112217295387_01_3150883_3.jpg
各位专家,谁能赐教分析下列溶液组分中的苯胺和DAM含量可以采用什么分析方法?溶液组分:氯化钠、氢氧化钠、苯胺、DAM、环己胺、环己醇
在前面的问题中,混合溶液中的苯胺、DAM、含量在5ppm左右。环己胺、环己醇的含量在2ppm以下
我们有一个酯类API,合成过程中加入正己醇生成的酯,该API需要测定正己醇残留,正己醇沸点约157℃,因此采用150℃的顶空条件测定样品,发现样品中的正己醇残留色谱峰面积其大,可能是该API在顶空条件下降解生成了正己醇,那么这样我如何实验证明该正己醇是降解的,样品中的正己醇残留应该怎么测定呢?谁有过类似的经历,分享一下。
请问各位老师,有没有做过地毯胶黏剂检测?按照GB18587-2001,测试地毯胶黏剂中的2-乙基己醇,具体分析方法采用ISO16017-1:2000。请问是将胶黏剂涂抹在模拟板上后,按照小型环境试验舱进行采样,然后对样品分析吗?
化学位移试剂的原理是什么啊??怎么能将化学位移非常接近的H的信号给分开,能分开正己醇的所有的H吗??
求助。。请问各位大佬,我做了个催化反应,溶剂是水,产物中有甲醇,环己醇等等,进[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的时候我是用的乙酸乙酯萃取,其余产物可以萃取出来,但是甲醇萃取不出,不能定量;若用乙醇稀释下反应产物,很多物质又不会出峰;怎样才能在色谱中准确测出甲醇含量?(产物:甲醇,环己醇,苯酚,2-甲氧基环己醇,环己酮)
[color=#444444]本人所做的反应产物包括的最可能成分有:环己烷(或环己烯)、环己酮、环己醇、己二酸,可能还有少量丁二酸和戊二酸。现在想定量分析一下己二酸、环己酮和环己醇,当然能把产物都分析出来最好。文献有说先用还原法把己二酸还原,然后[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]或液相色谱(或色-质联用)分析。但不知道用的多大浓度的还原试剂,以及指示剂用的啥。不知道大家有没有做过类似产物分析的,望不吝赐教!!!在此先谢谢各位![/color]
[color=#444444]本人所做的反应产物包括的最可能成分有:环己烷(或环己烯)、环己酮、环己醇、己二酸,可能还有少量丁二酸和戊二酸。现在想定量分析一下己二酸、环己酮和环己醇,当然能把产物都分析出来最好。文献有说先用还原法把己二酸还原,然后[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]或液相色谱(或色-质联用)分析。但不知道用的多大浓度的还原试剂,以及指示剂用的啥。不知道大家有没有做过类似产物分析的,望不吝赐教!!!在此先谢谢各位![/color]
纯度 %(A/A) ≥99.90 环己胺 %(A/A) ≤0.0150 环己醇 %(A/A) ≤0.0150 甲基苯胺 %(A/A) ≤0.0100 高沸物 %(A/A) ≤0.0150 苯胺含量%≥ (m/m) 99.80 99.60 99.40干品凝固点℃ ≥ -6.2 -6.4 -6.6硝基苯含量%(m/m) ≤% 0.002 0.010 0.015水分%(m/m) ≤ 0.10 0.30 0.50低沸物含量%≤ (m/m) 0.005 0.007 0.010高沸物含量%≤ (m/m) A/A和m/m是什么意思?
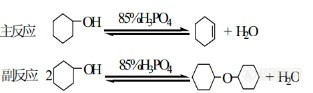
[align=center][b][b][font=黑体]分馏柱在环己烯制备实验中的使用及其作用[/font][/b][/b][/align][align=center][font='Times New Roman']Application and function of fractionation column in cyclohexene preparation experiment[/font][/align][align=center][font=宋体][font=宋体]北京化工大学[/font] 材料科学与工程学院 高元[/font][/align][font=宋体] [/font][font=黑体]摘要[/font][font=宋体]:[/font][font=宋体]目前大学化学实验教学中,大多采用环己醇制备[/font][font=宋体]环己烯[/font][font=宋体]。环己醇[/font][font=宋体]在加热以及[/font][font=宋体]酸[/font][font=宋体]催化的条件下发生[/font][font=宋体]消去反应,生成环己烯。本文简单介绍了分馏法用环己醇制备环己烯的实验原理和实验方法[/font][font=宋体],[/font][font=宋体]阐述了分馏柱在实验中的作用原理和优点;介绍了采用[/font][font=宋体]带分水器回流替代分馏的[/font][font=宋体]改进[/font][font=宋体]方法[/font][font=宋体],希望对现有的实验室环己烯制备实验方案提出一些建议和看法[/font][font=宋体][font=宋体]。[/font] [/font][font=黑体]关键词[/font][font=宋体]:环己烯;制备;[/font][font=宋体]分馏柱[/font][align=left][font=宋体][/font][font=黑体]前言[/font][font=宋体]环己烯又名四氢化苯,由环己醇脱水而制得[/font][font=宋体],[/font][font=宋体]是一种很重要的有机合成原料[/font][font=宋体],可以用于聚合物合成、催化剂溶剂、合成医药的中间体以及作[/font][font=宋体]为反应溶剂[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体]1][/font][/sup][font=宋体]。[/font][font=宋体]实验室[/font][font=宋体]制备[/font][font=宋体]环己烯[/font][font=宋体]的方法,[/font][font=宋体]是[/font][font=宋体]在[/font][font=宋体][font=宋体]环己醇在催化剂磷酸或硫酸的存在下[/font], 加热分馏[/font][font=宋体],[/font][font=宋体]得到粗产品[/font][font=宋体],[/font][font=宋体]再用氯化钠饱和溶液洗涤[/font][font=宋体]、[/font][font=宋体][font=宋体]用[/font]5%的碳酸钠溶液中和微量的酸[/font][font=宋体],[/font][font=宋体]经过洗涤、分液、干燥、蒸馏而得到精制[/font][font=宋体]环己烯[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=等线]2[/font][/sup][sup][font=宋体]][/font][/sup][font=宋体]。[/font][font=宋体]本文主要探讨分馏柱在环己烯制备实验中的作用,简要介绍采用[/font][font=宋体]带分水器回流替代分馏[/font][font=宋体]的方法,以此作为对现有教学实验的改进建议。[/font][img=,313,93]https://ng1.17img.cn/bbsfiles/images/2021/12/202112011029317337_7606_3237657_3.jpg!w313x93.jpg[/img][font=黑体]1[/font][font=黑体] [/font][font=黑体]实验原理[/font][font=宋体]主反应为可逆反应,本实验采用的措施是:[/font][font=宋体]一[/font][font=宋体]边反应[/font][font=宋体],一[/font][font=宋体][font=宋体]边蒸出反应生成的环己烯和水形成的二元共沸物(沸点[/font]70.8℃,含水10%)。但是[/font][font=宋体],[/font][font=宋体]原料环己醇[/font][font=宋体](分析纯)[/font][font=宋体]也[/font][font=宋体]可以跟[/font][font=宋体][font=宋体]水形成二元共沸物(沸点[/font]97.8℃,含水80%)。为了使产物以共沸物的形式蒸出反应体系,而又不[/font][font=宋体]附[/font][font=宋体]带原料环己醇,本实验采用分馏装置[/font][font=宋体],[/font][font=宋体][font=宋体]并控制柱顶温度不超过[/font]90℃[/font][sup][font=宋体][2][/font][/sup][font=宋体][font=宋体]。[/font] [/font][font=宋体][font=宋体]实验装置如图[/font]1所示。[/font][font=宋体][font=宋体]在该实验中,若使用硫酸作为催化剂,一般产率不高,且硫酸腐蚀性强,容易产生碳渣及[/font]SO[/font][sub][font=宋体][font=宋体]2 [/font][/font][/sub][font=宋体]等副产物,后处理麻烦,污染环境[/font][sup][font=宋体][3][/font][/sup][font=宋体][font=宋体]。因此,本实验选用了[/font]8[/font][font=宋体]5%[/font][font=宋体][font=宋体]的磷酸[/font](分析纯[/font][font=宋体])[/font][font=宋体]作为脱水剂。[/font][font=宋体] [/font][font=黑体]2[/font][font=黑体].[/font][font=黑体]分馏[/font][font=黑体]2[/font][font=黑体].1 [/font][font=黑体]分馏柱[/font][/align][align=center][img=,274,223]https://ng1.17img.cn/bbsfiles/images/2021/12/202112011030007833_8836_3237657_3.png!w274x223.jpg[/img][/align][align=left][font=宋体][color=#333333][font=宋体][/font][/color][/font][/align][align=center][font='等线 Light'][font=黑体]图[/font][/font][font='等线 Light']1[/font][font='等线 Light'] [font=黑体]环己烯[/font][/font][font=黑体]分馏装置[/font][sup][font=宋体][4][/font][/sup][/align][align=center][font='Times New Roman']Figure 1. Cyclohexene fractionation unit[/font][/align][align=left][font=宋体][color=#333333][font=宋体][/font][/color][/font][/align][align=left][font=宋体][color=#333333][font=宋体][/font][/color][/font][/align][align=left][font=宋体][color=#333333][font=宋体]本实验使用的是刺形分溜柱,分馏柱的刺形内壁用来[/font][/color][/font][font=宋体][color=#333333][font=宋体]填充[/font][/color][/font][font=宋体][color=#333333][font=宋体]分馏柱,[/font][/color][/font][font=宋体][color=#333333][font=宋体]增大[/font][/color][/font][font=宋体][color=#333333][font=宋体]了[/font][/color][/font][font=宋体][color=#333333][font=宋体]液相和[url=https://insevent.instrument.com.cn/t/Mp]气相[/url][/font][/color][/font][font=宋体][color=#333333][font=宋体]的接触面积,[/font][/color][/font][font=宋体][color=#333333][font=宋体]使其充分进行热交换,提高不同沸点的物质[/font][/color][/font][font=宋体][color=#333333][font=宋体]的[/font][/color][/font][font=宋体][color=#333333][font=宋体]分离效率。[/font][/color][/font][font=宋体][color=#333333] [/color][/font][font=黑体]2[/font][font=黑体].2 [/font][font=黑体]分馏[/font][img=,274,63,left]file:///C:\Users\yangcf\AppData\Local\Temp\ksohtml\wps3F10.tmp.png[/img][font=宋体][color=#333333]在沸腾温度下,两种挥发性液体混合物在反应容器中达到气[/color][/font][font=宋体][color=#333333]-液平衡状态,得到的蒸气中含有较多易挥发的气体组分,将此部分蒸气体经液化转化为液体;液相中含有较多难挥发的高沸点组分。这样就完成了一次蒸馏。[/color][/font][font=宋体][color=#333333][font=宋体]将上述由蒸气冷凝而成的液体重新蒸馏,再次产生的蒸气中,易挥发物质组分的比例会增大,进而液化得到易挥发物质更多的液体。利用这样一连串的系统的重复蒸馏,最后可以得到接近纯组分的两种液体。[/font][/color][/font][font=宋体]分馏就是[/font][font=宋体]将这一连串的重复蒸馏控制在分馏柱中,让[/font][font=宋体]上升的蒸汽和下降的冷凝液在分馏柱中进行多次热交换,从而使低沸点的物质不断上升、被蒸出[/font][font=宋体],[/font][font=宋体]高沸点的物质不断地被冷凝、下降[/font][font=宋体],[/font][font=宋体]流回[/font][font=宋体]到[/font][font=宋体]加热容器中[/font][font=宋体],最终[/font][font=宋体]将沸点不同的物质分离[/font][font=宋体]。简单地讲,就是[/font][font=宋体]在分馏柱中进行多次蒸馏。[/font][font=宋体] [/font][font=黑体]2.3[font=黑体]分馏柱[/font][/font][font=黑体]的[/font][font=黑体]优点[/font][font=宋体]反复多次的简单蒸馏,既浪费时间,在重复多次蒸馏操作中的损失[/font][font=宋体]又[/font][font=宋体]大[/font][font=宋体],且[/font][font=宋体]设备复杂,所以,通常是利用分馏柱进行多次气化和冷凝[/font][font=宋体],[/font][font=宋体]得到接近纯组分的两种液体[/font][font=宋体],[/font][font=宋体]这就是分馏。工业上的[/font][font=宋体]精馏塔[/font][font=宋体]就相当于分馏柱。[/font][font=宋体] [/font][font=黑体]3[/font][font=黑体]. 环己烯制备实验的改进[/font][font=宋体]目前各有机化学实验教材中,环己烯的制备方法都采用分馏的方法,该方法存在分离提纯困难、产物纯度不高和收率较低的缺陷。[/font][font=宋体][img=,85,271]https://ng1.17img.cn/bbsfiles/images/2021/12/202112011031386093_8635_3237657_3.jpg!w85x271.jpg[/img]在杜钦芝[/font][font=宋体]的[/font][font=宋体]改进方法中[/font][sup][font=宋体][5][/font][/sup][font=宋体],采用[/font][font=宋体]了[/font][font=宋体]带分水器回流的方法替代分馏的方法[/font][font=宋体],在[/font][font=宋体]烧瓶上安装分水器,分水器上接球形冷凝管[/font][font=宋体][font=宋体](见图[/font]2)[/font][font=宋体]。将烧瓶在石棉网上加热回[/font][img=,85,271,left]file:///C:\Users\yangcf\AppData\Local\Temp\ksohtml\wps3F11.tmp.jpg[/img][font=宋体]流。[/font][font=宋体]在[/font][font=宋体]分水器中预先加入适量饱和食盐水,以[/font][font=宋体]增大[/font][font=宋体]分水器中有机层的高度,使其能[/font][font=宋体]够[/font][font=宋体]及时流回[/font][font=宋体]到[/font][font=宋体]烧瓶[/font][font=宋体]中[/font][font=宋体],并降低环己醇在水中的溶解度[/font][font=宋体]。当[/font][font=宋体]水面达到分水器支管时,及时放出少量水。[/font][font=宋体]改进后的实验方法,不但实验操作更为简单,[/font][font=宋体]而且由于[/font][font=宋体]使用了分水器,[/font][font=宋体]反应[/font][font=宋体]平衡向产物方向移动,反应几乎可以进行完全,避免了因环己醇与环己烯[/font][font=宋体]、[/font][font=宋体]环[/font][font=宋体]己[/font][font=宋体]醇与水形成的共沸物馏出,所以分离提纯简单,产物的纯度高,[/font][font=宋体]回收[/font][font=宋体][font=宋体]率可提高到[/font]60%~70%,完全可以替代传统的分馏制备方法运用于实验教学中。[/font][font=宋体] [/font][font=黑体]总结与展望[/font][img=,212,67,left]file:///C:\Users\yangcf\AppData\Local\Temp\ksohtml\wps3F22.tmp.png[/img][font=宋体][font=宋体]本实验涉及多个基础有机化学实验基本操作[/font],[/font][font=宋体]是一个[/font][font=宋体]能够有效提高学生的综合实验技能的基础有机化学实验。[/font][font=宋体]分馏操作在整个实验中的作用十分重要,分馏的效果直接影响到最终产品的回收率和纯度,因此,有必要认识分馏柱的使用方法和作用,探究更加简单高效的分馏制备方法。[/font][font=宋体] [/font][font=黑体]参考文献[/font][font=宋体][[/font][font=宋体]1][/font][font=等线] [/font][font=宋体][font=宋体]李芬芳[/font],安道利,刘秀萍,王艳[/font][font=宋体].[/font][font=等线] [/font][font=宋体]环己烯制备实验的改进[/font][font=宋体][[/font][font=宋体]J].山西大同大学学报(自然科学版)[/font][font=宋体].[/font][font=宋体]2015,31(01):31-32[/font][font=宋体][[/font][font=宋体]2][/font][font=宋体] [font=宋体]张丽丹[/font],李顺来,张春婷[/font][font=宋体].新编[/font][font=宋体]大学化学实验[/font][font=宋体][M].[/font][font=宋体][font=宋体]北京[/font]:化学工业出版社[/font][font=宋体],2020(9):118-124[/font][font=宋体][3][/font][font=等线] [/font][font=等线][font=等线]张颖[/font],姜文清,卞国庆.[/font][b][font=微软雅黑][color=#333333] [/color][/font][/b][font=等线][font=等线]环己烯合成实验的绿色化改进[/font][[/font][font=等线]J].化学教育[/font][font=等线].[/font][font=等线]2012,33(03):65-68[/font][font=宋体][4][/font][font=等线] [/font][font=宋体]李福枝[/font][font=宋体],[/font][font=宋体]肖细梅[/font][font=宋体],[/font][font=宋体]龚慧芳[/font][font=宋体],[/font][font=宋体]傅欣[/font][font=宋体],[/font][font=宋体]周晓媛[/font][font=宋体].[/font][font=宋体]浅谈环己烯制备实验中的有关注意事项[/font][font=宋体][[/font][font=宋体]J].化学工程与装备[/font][font=宋体].[/font][font=宋体]2010(08):21-23[/font][font=宋体][5][/font][b][font=宋体][color=#333333] [/color][/font][/b][font=宋体]杜钦芝[/font][font=宋体].[/font][font=宋体][font=宋体]环己烯制备方法的改进[/font][[/font][font=宋体]J][/font][font=宋体].[/font][font=宋体]教育教学论坛[/font][font=宋体].[/font][font=宋体]2020(31):[/font][font=宋体]391-392[/font][/align]
根据5009.97测食品中的甜蜜素时,用Hp-5的柱子,出三个峰都是衍生物吗,有的说一个是环己醇亚硝酸酯,环己醇,两种物质,积分时要几个峰加和吗,还是只算环己醇亚硝酸酯?
用赛默飞[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]检测甜蜜素,甜蜜素有衍生物,建立曲线时要用环己醇亚硝酸酯与环己醇峰面积之和,如何把环己醇亚硝酸酯与环己醇峰面积加和到一个组分进行曲线建立。
假如有乙醇,丙醇,丁醇,戊醇,己醇,辛醇,还有酯在OV-17的出峰顺序是怎么样的

检测甘油,有对照乙二醇、二甘醇,内标正己醇,条件:DB-624(30m*0.53mm 3.um),进样量1ul,分流比10:1,进样口200°,FID250°,程序:起始100(维持4′),以50°/min升120°(维持10′),再以50°/min升220°(维持6′).后加设降温和平衡时间。样品处理:系统适用性性乙二醇、二甘醇,内标正己醇各100mg稀释至100ml(系统储备液),精取1ml+4g甘油样品至100容量瓶, 所 有 溶剂都是色谱甲醇。 对照液:乙二醇、二甘醇,内标正己醇各50mg至100ml(标储液),取5ml稀释至25ml。问题:6月份同样方法检测,一切正常(当时柱子新买来活化后检1批乙醇,) 这两天同一根柱子检测(中间检测了3批乙醇),结果系统适用性乙二醇出不来峰了。正己醇和二甘醇峰面积无论是储备液还是系统适用性都没什么差异。储备液中的乙二醇有峰面积,但与之前浓度相当情况下峰面积小1/3,系统适用性就出不来了,对照液要算校正因子f,之前差不多2-3左右,现在超过10了。乙二醇的安剖瓶色标5ml有之前开启后密封冷藏的,也有新开的,两种情况都差不多,批号都是081226。http://ng1.17img.cn/bbsfiles/images/2012/07/201207251613_379663_2481522_3.jpg6月份的对照液,峰依次是:乙二醇--正己醇--二甘醇。http://ng1.17img.cn/bbsfiles/images/2012/07/201207251616_379664_2481522_3.jpg6月的系统适用性,7.8′乙二醇峰还是不错的,但这次此峰消失了。后面的正己醇、二甘醇相当浓度峰面积也相当。请问问题可能在哪里呢?
7月2日将50ug/ml的环己基氨基磺酸钠标准溶液在[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]上机测试,得出色谱图。 然后将50ug/ml的环己基氨基磺酸钠标准溶液分为两部分,分别储存在冷冻和冷藏的条件下密封保存。 在7月10日的时候,分别取出在[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]上机测试,得出色谱图。 将三个环己基氨基磺酸钠的色谱图进行对比。 [img=,690,309]https://ng1.17img.cn/bbsfiles/images/2024/08/202408161522359457_3024_5979722_3.png!w690x309.jpg[/img] 环己基氨基磺酸钠的色谱图会出现两个色谱峰,分别是环己醇亚硝酸酯、环己醇。 我发现两个问题 1、7月10日的色谱图和7月2日的色谱图相比(期间其他条件都没有变化),环己醇亚硝酸酯、环己醇的出峰位置都提前了5-10秒,算是色谱峰漂移了。理论上应该是再跑一个当天衍生化的环己基氨基磺酸钠标准溶液上机进行对比,但是近期比较忙这一本就没有做。后期有机会做了,我再反馈这一个问题。 2、在冷藏和冷冻条件下的环己基氨基磺酸钠标准溶液的环己醇亚硝酸酯、环己醇的面积有一些差别。冷藏条件和冷冻条件相比,冷藏条件下的环己醇亚硝酸酯的面积变小了,环己醇的面积变大了。但是面积总和相比几乎一样,因此可以判定,环己醇亚硝酸酯在指定温度下,是可以继续转化为环己醇的。 [img=,690,511]https://ng1.17img.cn/bbsfiles/images/2024/08/202408161523569214_3530_5979722_3.png!w690x511.jpg[/img] [img=,690,513]https://ng1.17img.cn/bbsfiles/images/2024/08/202408161524065331_7755_5979722_3.png!w690x513.jpg[/img] [img=,690,535]https://ng1.17img.cn/bbsfiles/images/2024/08/202408161524102083_9380_5979722_3.png!w690x535.jpg[/img] 根据标准曲线查看7月10日分别上机的环己基氨基磺酸钠标准溶液的含量,分别是58.7689 ug/ml和58.5511 ug/ml,7月2日上机检测的含量是51.2462 ug/ml,我们可以看出来标准溶液保存8天后,检测的数值就有不少误差了,而且是数值变大了。这一点不知道是什么原因
最近去北京培训,老师说甜蜜素出两个峰,我回来做了一下,柱子是FFAP,分别是4min和9min,想问一下哪个峰是环己醇,哪个峰是环己醇亚硝酸酯,定量是把两个峰加和吗?通常标样是前一个峰大,后一个峰小。如果样品是前一个峰小,后一个峰大,该怎么定量呢
[color=#444444]想测环己烯环己醇乙酸环己酯相对苯的质量校正因子,求具体步骤。是称一定量的环己烯,环己醇,乙酸环己酯三者和苯的混合物,还是各自和苯的混合物打[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]。谁能帮忙写详细点。是不是还要配不同质量的求平均。[/color]

食品中甜蜜素测定心得食品中甜蜜素测定方法一般都是按照GB/T5009.97-2003进行的,方法的原理是在硫酸介质中环己基氨基磺酸钠与亚硝酸钠反应,生成环己醇亚硝酸酯,利用气相色谱法进行定量测定。而在实际工作中发现,环己醇亚硝酸酯主峰并不稳定,每次做标准曲线线性都不是很理想,于是考察了一下其稳定性。连续进同一个浓度的标准品,发现主峰的面积在不断减小,后面随之出现了一个小峰,并且在逐渐增大。通过用质谱进行定性发现,小峰是环己醇。通过资料查询得知,环己醇亚硝酸酯的确不稳定,会在衍生后逐渐转变成环己醇。这就是为什么同时出现两个峰,主峰不断减小,后面的小峰逐渐变大的缘故。当发现这个问题之后,似乎还是没有办法从根本上解决这个问题。因为在平时的工作中,一般都是批量处理样品和标准品。现在气相色谱都是自动序列进样,只要处理好样品之后放在样品盘上就可以依次自动进样测定了。这个就出现了一个问题。在这个过程中,不管是样品还是标准品中,都存在这一个潜移默化的变化,也就是环己醇亚硝酸酯在逐渐向环己醇转化,各个样品及标准品的转化程度又各不相同,因为每个样品和标准品不可能在同一时间进样,所以在处理完之后到进样前这段时间的长短不一,就造成了各个样品检测结果的误差。仔细研究了一下,标准中处理方法。衍生过程中是需要在冰浴中进行的,低温应该就是这个衍生反应的必备条件。但是在提取之后,提取液就离开了冰浴的环境,这个是否就是环己醇亚硝酸酯向环己醇转化的有力时机呢?为了解开这个疑问,我们又做了如下实验。我们在衍生之后,让其停留在比色管中,在进样之前一直停留在冰浴里面,这样的实验结果发现,转化的确是像被暂停了一般,因为不同时间进样的重复性非常好。实验结果让我们很兴奋,但是这种操作方法对我们自动进样器来说没有什么优势,不能完成序列进样,非常浪费时间。于是我们又进行了下一步试验。既然在比色管放在冰浴没有问题,是否可以把提取液转移到进样瓶中,再把进样瓶保存在冰浴里,看看是否变化呢?实验结果证明,我们的想法是正确的,只要控制低温环境就可以延缓这种转化。由此我们也总结出一个规律,这个转化其实是与温度高低有密切关系的。所以尽量降低环境温度也是一个不错的方法。这种转化似乎是无法彻底避免的,只能尽量去降低室温来延缓其转化速度,尤其是在夏天,空调温度设低一点。另外,我们也发现安捷伦气象色谱仪的百位盘有一个特殊的地方,我想应该就是可以接冷凝水或者别的降温措施,来提供低温环境的。http://ng1.17img.cn/bbsfiles/images/2014/12/201412292105_529965_2830723_3.jpg以上是我的一点拙见,希望对大家有所启示。进一步研究还需要大家继续进行,有不妥之处,欢迎大家拍砖。
有没有做食品添加剂的?现在大量需要食品级正辛醇,正己醇,正庚醇要求99.5%,每月需求10-20吨。有意联系15066514528