各位大侠,我现在在做将胰蛋白酶固定在毛细管内壁形成一个酶解微反应器,先是用NaOH将毛细管内壁活化,带上负电荷,然后让带正电荷的胰蛋白酶溶液(将酶配在Tris-HCl,同时含有20mM CaCl2 ,pH 8.0,低于酶的等电点)进入毛细管,通过静电吸引固定上酶,发现在做电泳时候酶的活性损失厉害,估计是酶慢慢的都掉下来了,于是我又在上述步骤后再加上进一定浓度的海藻酸钠,想形成海藻酸钙凝胶加固酶在毛细管内壁上的稳定性,但是发现酶的起始活性比不用海藻酸钠时候还要低很多,请问哪位大侠能帮忙给我建议一个好的方法,将酶稳定的固定在毛细管内壁上且活性能够损失比较少。谢谢了!
《中国药典》二部对镁盐的鉴别罗列了两种方法:其一:取供试品溶液,滴加氨试液即产生白色沉淀,加氯化铵试液,沉淀溶解,再加磷酸氢二钠试液1滴,振摇,即生成白色沉淀,沉淀不溶于氨试液。对于这个方法做含有次硝酸铋的碳酸镁鉴别时,专属性不好,在加入氯化铵试液时,沉底不溶解,据我了解应该是次硝酸铋的干扰原因,请问哪位高手知道在次鉴别的前处理上将铋盐掩蔽而不影响镁盐反应的方法?多谢了
在下做的固定化胰蛋白酶涂层柱:先硅烷化,再用戊二醛将胰蛋白酶与内壁上的—NH2结合,再用NaCNH4还原得到所要的柱子。遇到的主要问题就是发现固定上的酶很容易掉下来,而且内壁涂层很不均匀,是一段一段的,就是一段有酶一段没有固定上酶,电泳时因为酶会掉下来,所以运行个4次左右柱子就会堵,很郁闷。。。求大虾帮忙。。。
有做过溶酶体贮积症[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]检测酶活的老师吗?最近在做这个实验,通过酶活反应将底物转化为产物,通过产物的量与酶的体积、反应时间等计算酶活。排查了不少因素,也仿照大量文献报道的酶反应剂都应用到实验中,而得到的酶活却与文献、NCBI上的阈值有一定出入,如果自己买到第三方校准品,自己根据自己的实验结果定正常人水平的酶活阈值可以吗?有哪些需要注意的吗?谢谢!

维权声明:本文为gl19860312原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。 本实验室主要工作就是:微生物发酵与代谢调控 、蛋白的分离纯化 、生物材料的研发与生产( 化妆品 、面膜、人工血管 、人工骨................)http://ng1.17img.cn/bbsfiles/images/2010/12/201012061858_264950_2019107_3.jpg啤酒酵母细胞自溶技术破壁研究摘要:研究了PH、温度、食盐浓度三个因素对啤酒酵母细胞破壁的影响,确定出最佳的自溶法破壁条件 。进而为分离啤酒废酵母中的有效活性成分奠定了基础。关键词:啤酒酵母;破壁;自溶The Research of Autolysis on the Beer Yeast Cells wallAbstract:This paper researched the condition of autolysis on the waste yeast cells wall with three factors (pH 、Temperature 、Salt density) and determined the best condition based on autolysis. And build basis for separating the activity forms from beer waste yeasts.Key words: The beer yeast; Breaking Cells wall; Autolysis引言啤酒酵母(S.csrsviside)属于真菌门酵母属,多数为单细胞微生物,细胞呈圆形或卵圆形,革兰氏染色呈阳性G+。啤酒酵母细胞是由细胞壁、细胞膜、液泡、颗粒和线粒体等部分组成,细胞年幼的时候细胞壁很薄,所以不明显;细胞年老时,细胞壁较厚。啤酒酵母细胞内不但含有丰富的蛋白质、维生素、葡聚糖及甘露聚糖等营养及保健成分,可作为食用单细胞蛋白,此外还含有辅酶I、细胞色素,卵磷脂、RNA,,这些物质或其降解产物及衍生物如氨基酸制剂和核苷酸及核酸制剂等在生物化学、医药及保健食品中最有重要的作用。由于啤酒废酵母价格便宜,因此可利用啤酒废酵母来提取、制备这些物质。啤酒废酵母(waste brewer's yeast)是啤酒生产的副产物,是指啤酒酿造后沉降的酵母泥,主要是由大量的弱细胞和死细胞组成。在啤酒生产过程中,每生产 100吨啤酒大约有1-1.5吨废酵母 (以干重计)产生。传统的处理方法,是弃置不用或作为饲料处理,直接排放到河流湖泊中,将造成环境污染,同时也是对财富的浪费;因其具有坚韧的细胞壁和特有的酵母臭,适口性差,不易消化和吸收,故烘干作为饲料用的经济效益不高。充分利用啤酒废酵母可以有效地减轻污染,实现资源的二次转化,也可产生巨大的经济效益,如开发酵母抽提物。 为了增加酵母抽提物产量国内外同行做出不同努力,开展了有些研究。目前关于啤酒酵母破壁的研究很多,大体可归纳为:化学破壁(酸解、碱解)、物理破壁(液体剪 切、固体剪切等)、生物破壁(酶解、自溶)。其中,化学破壁不仅会造成一些营养成分的破坏,而且为有效成分的提取增加困难;物理破壁虽然方法简单、成本低,能完好保存营养成分,但其破壁效果较差;生物破壁中的酶解法会增加提取成本,故均不能大规模广泛的应用。而采用自溶法进行细胞破壁是一种简便易行的操作过程,通过确定啤酒酵母细胞最适合的自溶条件,可以建立一套利用酵母细胞生产酵母抽提物的工艺和方法,旨在为啤酒酵母的综合利用寻求一种新的方法,为工业化生产提供理论基础和实践指导。1.4实验方法 工艺流程 啤酒废酵母(保藏)—— 活化、两次斜面培养—— 接种、平板划线——摇瓶培养——取对数期的酵母细胞——做稀释梯度——做影响因素(温度、食盐浓度、pH并固定时间60分钟)的实验-——做正交试验——镜检(血球计数法)——计算啤酒酵母细胞的破碎率——得到自溶的最佳工艺参数1.5啤酒废酵母自溶条件的确定酵母自溶的实质是酵母细胞内的蛋白质在自身蛋白酶的作用下,降解为游离的氨基酸,那么,一切影响酶促反应的因素均影响酵母细胞的自溶,如自溶温度、食盐浓度、pH值、自溶时间等。自溶法是以存在酶活性的新鲜活酵母为原料,利用酵母细胞本身的酶系,在一定条件下,将酵母体内的糖类物质、蛋白质和核酸分解为还原糖、氨基酸、肤类、核昔酸等小分子物质并从酵母细胞内抽提出来的一种方法。利用自溶法生产的酵母抽提物,蛋白质分解率高,游离氨基酸含量高,风味好,成本较低,但呈味核昔酸含量低.目前,欧美及我国所生产的酵母抽提物绝大部分都是采用这种方法。[font=仿宋_GB2
各位大神们,本人小白一枚,最近在把重组的大肠杆菌破壁离心,取上清过柱子,纯化酶,但是酶活非常低甚至没有了,正在找问题,请各位大神指教啊,(1)用来破壁的液体,一般要用pbs缓冲液嘛,ph多少的,pbs里面要加氯化钠嘛,一般ph是多少?(2)我上的镍柱,结合液是20mmol/L的pbs.ph值为7.4的,里面还加了0.5mlo/L的氯化钠,5mmol/L的咪唑。洗脱液是20mmol/L的pbs.ph值为7.4的,里面加了0.5mlo/L的氯化钠,500mmol/L的咪唑,我这个有没有问题呀。(3)我当时透析用的水,透析了30小时吧,用的转子,里面加的冰,换了4次水,是不是应该也要用缓冲液透析呢,用pbs嘛,那这里面不需要加盐吧。(4)我们这个酶用来降解的物质会跟pbs还有盐酸反应,我也担心测酶活时会受缓冲液影响。请各位大神指教啊(5)这个破壁用的以及透析用的缓冲液需要灭菌或除菌嘛,一般都怎么操作
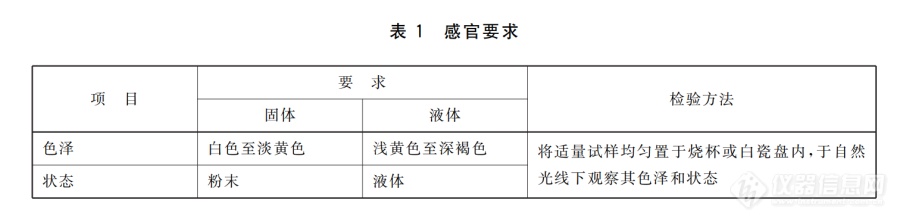
[align=center][font='宋体'][size=29px]溶菌酶[/size][/font][/align][size=24px]赵浩博[/size][size=12px]溶菌酶又称细胞壁质酶或[/size][size=12px] N- 乙酰胞壁质聚糖水解酶。1922 年英国细菌学家 A. Fleming 发现人的唾液、 眼泪中存[/size][size=12px]在有溶解细菌细胞壁的酶,[/size][size=12px] 因其具有溶菌作用, 故命名为溶[/size][size=12px]菌酶。[/size][size=12px] 此后在人和动物的多种组织、 分泌液, 及某些植物、[/size][size=12px]微生物中也发现了溶菌酶的存在。[/size][size=12px] 随着研究的不断深入, 发[/size][size=12px]现不仅有溶解细菌细胞壁的溶菌酶,[/size][size=12px] 还有作用于真菌细胞壁[/size][size=12px]的种类,[/size][size=12px] 同时对其作用机制也有了更进一步的了解。 近几[/size][size=12px]年,[/size][size=12px] 人们根据溶菌酶的溶菌特性, 将其应用于医疗、 食品、[/size][size=12px]畜牧及生物工程中。[/size][size=12px]溶菌酶来源不同,其分子大小不一样,其氨基酸排列顺序也有所不同,如:[/size][size=12px] T4 噬菌体溶菌酶由 164 个[/size][size=12px]氨基酸组成,分子量为[/size][size=12px] 19 ku;鸡蛋溶菌酶只有 129 个[/size][size=12px]氨基酸,其分子量约为[/size][size=12px] 14.3 ku;人溶菌酶由 130 个氨[/size][size=12px]基酸残基组成,分子量为[/size][size=12px] 14.6 ku;植物中分离出的溶[/size][size=12px]菌酶,其分子量较大,约为[/size][size=12px] 24 ku~29 ku。各种溶菌酶[/size][size=12px]的等电点在[/size][size=12px] 10.7~11.5 之间,化学性质十分稳定, pH 在1.2~11.3 范围内剧烈变化时,其结构几乎不变,活性不[/size][size=12px]受影响,此外,溶菌酶对热也极为稳定,在[/size][size=12px] pH3.0 条件[/size][size=12px]下,沸水浴中加热[/size][size=12px] 60 min 其活力仍保持 90 %以上。[/size][size=12px]目前鸡蛋清溶菌酶是研究最清楚的一种溶菌酶并已投入商业化生产。它是由[/size][size=12px] 18 种 129 个氨基酸残基[/size][size=12px]构成的单一肽链,有[/size][size=12px] 4 个 S-S 键的氨基酸 Cys,等电点[/size][size=12px]约为[/size][size=12px] 11.1,最适溶菌温度为 45 ℃~50 ℃, pH 为 6.0~7.0。在酸性环境中,溶菌酶对热的稳定性很强, pH4~7[/size][size=12px]范围内,[/size][size=12px] 100 ℃处理 1 min 仍有近 100 的活力, 210 ℃加[/size][size=12px]热[/size][size=12px] 1.5 h 仍具有活性;在中性水溶液中,溶菌酶可维持[/size][size=12px]数天而不失去活性;在碱性条件下,其稳定性较差[/size][size=12px]。[/size][font='宋体'][size=14px]1. [/size][/font][font='宋体'][size=12px]溶菌酶的理化性质[/size][/font][size=12px]溶菌酶纯品呈白色、微黄或黄色的结晶体或无定形粉末,无异味,微甜,易溶于水,不溶于丙酮、乙醚。溶菌酶遇碱易被破坏,但在酸性环境下,溶菌酶对热的稳定性很强,在[/size][size=12px]pH值为4-7时,100℃处理1min,仍能较好地保持活力:pH值为3时,能耐100℃加热处理45min。 [/size][size=12px]溶菌酶化学性质非常稳定,当[/size][size=12px]pH值在一定范围内剧烈变化时,其结构几乎不变。溶菌酶不可逆变性的临界点是77℃,随溶剂的变化,不可逆变性临界点也发生变化,当溶菌酶所处溶液pH值小于1时,不可逆变性临界点降低到43℃。[/size][size=12px]溶菌酶最适[/size][size=12px]pH为5.3~6.4,可用于低酸性食品防腐;溶菌酶作为防腐剂安全性高,可被冷冻或干燥处理,且活力稳定。 [/size][size=12px]溶菌酶对几种变性剂的敏感程度为[/size][size=12px]:二恶烷二甲基乙酰胺二甲基甲酰胺丙酮,并且随溶剂用量的增加而直线下降。[/size][font='宋体'][size=14px]2. [/size][/font][font='宋体'][size=12px]溶菌酶的制备[/size][/font][size=12px]目前溶菌酶可以以鸡蛋清和蛋壳膜为材料提取制得,常用的方法有亲和层析法、离子交换树脂法、直接结晶法和聚丙烯酸沉淀法等。[/size][size=12px]亲和层析法是利用蛋白质和酶的生物学特异性,即蛋白质或酶与其配体之间所具有的专一性亲和力而设计的色谱技术。酶一底物复合物形成之后,在一定的条件下分离复合物便得到纯净的酶。常常使用的吸附剂为几丁质及其衍生物,如:几丁质粉、羧甲基几丁质、几丁质包埋纤维素、脱氨几丁质粉、[/size][size=12px]N-酰化壳聚糖、脱氨再生几丁质凝胶。[/size][size=12px]离子交换法是利用离子交换剂与溶液中的离子之间所生的交换反应来进行分离的,分离的效果较好,广泛用于微量组分的富集。一般流程为:鲜蛋一预处理一搅拌吸附一上柱洗脱一等电点沉淀一透析一喷雾干燥一成品。[/size][size=12px]溶菌酶在等电点以下较广泛的[/size][size=12px]pH值范围内,分子带正电荷,可吸附于弱酸性阳离子交换树脂上,洗脱后盐析,可得溶菌酶沉淀,再进行精制可得成品。蛋清吸附724树脂,洗涤缓冲液洗脱,硫酸铵溶液盐析透析,用NaOH去碱性蛋白,冻干溶菌酶,冻干粉沉淀干燥得到溶菌酶。在5—10℃下,将新鲜蛋清540kg加入到已处理好的80kg 724树脂中,搅拌吸附6h,在0—5℃静置过夜。倾出上层蛋清,树脂离心甩干,用蒸馏水反复洗去黏附的卵蛋白,然后将树脂装入柱内,用0.15mol/L、pH=6.5磷酸缓冲溶液约150L洗涤树脂,再用约600L的10%硫酸铵溶液洗脱,收集洗脱液。洗脱液中加硫酸铵,使最终含硫酸铵量为40%,有白色沉淀生成,冷处放置过夜。虹吸上层清液,沉淀吸滤抽干,再用1倍蒸馏水溶解沉淀呈稀糊状,然后装入透析袋,在约5℃的条件下,对蒸馏水透析24h左右,中间换水2—3次。离心去除沉淀,沉淀再用少量水洗一次,洗液与离心液合并。再往透析清液中慢慢加入1mol/L氢氧化钠溶液,同时不断搅拌,使pH值上升到8.0—9.0,如有白色沉淀,即离心除去。然后用3mol/L盐酸调pH=5.0,冷冻干燥,即得白色片状溶菌酶。也可将离心液用3mol/L盐酸调pH=3.5,在搅拌下缓慢加入5%的固体氯化钠,在约5℃的温度下静置48h,离心,沉淀用0℃丙酮洗涤,干燥,即得溶菌酶。[/size][size=12px]在蛋清中加入一定量的碘化物或碳酸盐等盐类,并调[/size][size=12px]pH值至9.5—10.0,溶菌酶会以结晶形式慢慢析出,而大多数蛋白质仍然在溶液。在超滤浓缩脱盐后,为获得较纯产品,采用结晶纯化酶液经超滤处理后,用NaOH调整pH 9.5,离心去除。上清液在缓缓搅拌下,加NaCl至5%,静置一周,得粗结晶。结晶溶于pH 4.6醋酸水中,分去不溶物后,进行重结晶,结晶的最终得率为60%左右。即每公斤蛋清中可得重结晶品近1.3 g,活力测定为8000U/mg。 [/size][size=12px]聚丙烯酸沉淀法为将提取过滤后含酶洗脱液,首先经过吸附步骤,即将过滤后的澄清溶液用[/size][size=12px]20%的NaOH溶液调pH至6.0,在调pH值的过程中不停的搅拌。有少量的乳白色沉淀析出,然后加入15%聚丙烯酸,立即有白色沉淀析出,加至pH值为3.0为止,静置17个小时进行静析,得到粘附于底部的乳白色胶状物。第二步解离,将前步得到的溶菌酶聚丙烯酸凝聚物。加入少量蒸馏水并用0.5 mol/L的碳酸钠,将其溶解,转移后,将pH值调到9.5。加入5%CaCl2溶液将溶菌酶聚丙烯酸解离,至无沉淀析出,然后过滤,得到澄清溶液。第三步盐[/size][size=12px]析,将所得澄清溶液加入[/size][size=12px]5%的NaCI溶液搅拌均匀。放入冰箱调温度为0℃。待有晶体析出后,用无水乙醇洗涤数次,置恒温培养箱中40℃条件下干燥称重。[/size][font='宋体'][size=14px]3. [/size][/font][font='宋体'][size=12px]溶菌酶的应用[/size][/font][font='宋体'][size=12px]本文主要从溶菌酶在食品添加剂中的应用展开进行论述。[/size][/font][size=12px]3[/size][size=12px].1 用于水产、肉类的防腐[/size][size=12px]将溶菌酶应用于水产品、肉类的保鲜防腐,目前已做了大量的研究。如早在[/size][size=12px] 2001 年前陈舜胜等就研[/size][size=12px]究了溶菌酶复合保鲜剂在冷藏([/size][size=12px]5 ℃)与冰藏(0 ℃~1 ℃)[/size][size=12px]条件下对虾、带鱼段、扇贝柱和柔鱼的保鲜效果,结果表明,使用溶菌酶([/size][size=12px]0.05 %)复合保鲜液浸泡后冷藏或[/size][size=12px]用溶菌酶([/size][size=12px]0.05 %~0.08 %)复合保鲜液制备保鲜冰冰[/size][size=12px]藏,与常规保鲜方法相比,可将上述水产品的保鲜期延长约一倍的时间。[/size][size=12px]2012 年张观科又报道:采用溶[/size][size=12px]菌酶、[/size][size=12px]Nisin、甘氨酸、VC、山梨酸钾、NaCl 等不同的配比[/size][size=12px]的复合生物保鲜剂在不同温度对牡蛎进行保鲜贮藏研究。结果表明,采用[/size][size=12px] Nisin 和溶菌酶配合的生物保鲜[/size][size=12px]剂的保鲜效果最佳(在[/size][size=12px]-3 ℃微冻条件下,保藏 30 天后[/size][size=12px]感官性状仍然良好)[/size][size=12px] 。而钱曦利用海藻糖、蜂胶、茶多[/size][size=12px]酚、魔芋葡甘露聚糖、[/size][size=12px]Nisin、溶菌酶、壳聚糖和姜汁 8种[/size][size=12px]天然保鲜剂对鹿肉保鲜进行研究,结果表明:单独使用时,溶菌酶对鹿肉样品就有较明显的抑菌作用(最佳抑菌浓度为[/size][size=12px] 0.5 %);而采用复合天然保鲜剂(茶多[/size][size=12px]酚、溶菌酶、海藻糖、[/size][size=12px]Nisin 复合)效果更好,可以有效的[/size][size=12px]提高鹿肉的货架期至[/size][size=12px] 36 d。从以上研究结果来看,溶菌[/size][size=12px]酶尤其是它在与其他保鲜剂按一定比例复合使用时,对水产及肉类能起到较好的防腐保鲜效果。[/size][size=12px]3[/size][size=12px].2 在低度酒类、饮料中的应用[/size][size=12px]日本已成功的使用鸡蛋清溶菌酶代替水杨酸作防腐剂用于清酒的防腐[/size][size=12px]。在国内,倪瑛和钟立人研[/size][size=12px]究了溶菌酶在葡萄酒生产中的应用。因为在葡萄酒生产中乳酸菌会将苹果酸转变为乳酸,但如果在酒精发[/size][size=12px]酵的前期就完成了这种反应,会对葡萄酒的感官产生不良影响,而控制乳酸菌生长的传统方法是使用[/size][size=12px] SO2,[/size][size=12px]但[/size][size=12px] SO2 的使用不仅对人体产生毒性,同样影响葡萄酒[/size][size=12px]的品质。因此,倪瑛等尝试将溶菌酶替代或补充[/size][size=12px] SO2 调[/size][size=12px]控乳酸菌的生长,结果显示,在葡萄原汁中加入[/size][size=12px] 0.1 %~0.15 %的溶菌酶,乳酸菌生长被抑制;在白葡萄酒中溶[/size][size=12px]菌酶剂量加至[/size][size=12px] 0.5 %时,可完全抑制苹果酸向乳酸的转[/size][size=12px]变。此外,将溶菌酶用于饮料防腐也有报道,如常凯等将溶菌酶([/size][size=12px]0.05 %) 、甘氨酸和 NaCl 进行复配用于生[/size][size=12px]产脱脂山核桃乳,其抑菌效果较显著,降低了山核桃乳的杀菌强度,延长了产品货架期。从以上结果看,在葡萄酒的生产中溶菌酶可作为[/size][size=12px]SO2 天然的、安全的替代或补充品来抑制乳酸菌的生[/size][size=12px]长,在其他低度果酒中也可做类似的尝试;同样将溶菌酶用饮料的防腐也有较显著的效果。[/size][size=12px]3[/size][size=12px].3 在乳制品中的应用[/size][size=12px]由于溶菌酶对肠道中腐败性微生物有特殊的杀灭作用,同时可直接或间接地促进肠道中双歧杆菌的增殖[/size][size=12px]。因此,有大量有关溶菌酶应用于婴幼儿奶粉的[/size][size=12px]专题论述[/size][size=12px] 冯棋琴,等:溶菌酶在食品工业中的研究进展[/size][size=12px]35研究报道,如刘浩强等研究了鸡蛋溶菌酶对婴幼儿[/size][size=12px]配方奶粉的抑菌效果,结果表明,婴幼儿配方奶粉在喷雾干燥后添加[/size][size=12px] 10 mg/100 mL~50 mg/100 mL 的鸡蛋[/size][size=12px]溶菌酶效果最好。张明江[/size][size=12px]等关于婴幼儿配方奶粉中[/size][size=12px]溶菌酶的添加工艺的研究也得出了相似的结论,既奶粉喷雾干燥后添加[/size][size=12px] 500 mg/L 的溶菌酶抑菌效果最好。[/size][size=12px]3[/size][size=12px].4 在水果保鲜上的应用[/size][size=12px]水果经过溶菌酶处理,其表面的细菌被有效的抑制或杀灭,从而延长水果的保鲜期。胡晓亮等[/size][size=12px]采用溶[/size][size=12px]菌酶与溶菌酶复合保鲜剂对马陆葡萄进行涂膜保鲜,结果表明:溶菌酶单独使用有一定的保鲜效果,但将溶菌酶([/size][size=12px]0.1 %)和海藻酸钠(1 %)复合使用对抑制马陆[/size][size=12px]葡萄的感官品质下降效果更为显著,在([/size][size=12px]4±1) ℃条件下[/size][size=12px]贮藏[/size][size=12px] 25 d 后,仍保持果实的硬度和组织形态,质量损[/size][size=12px]失率仅为[/size][size=12px] 9.34 %。[/size][size=12px]溶菌酶本身作为一种天然蛋白质,能在胃肠内作为营养物质被消化和吸收,对机体无毒性,也不会在体内残留,安全性很高,加之有效的防腐特性,溶菌酶已受到了食品行业的青睐。但目前实际应用的且已商品化的是鸡蛋清溶菌酶,它的抗菌谱较窄,只对[/size][size=12px] G+细菌起作用,底物特异性[/size][size=12px]强,且投入[/size][size=12px]/效率低,这限制了它们的广泛使用。为了扩[/size][size=12px]大溶菌酶使用领域及防腐效果,可以将鸡蛋清溶菌酶与其他天然保鲜剂(如海藻糖、茶多酚、[/size][size=12px]Nisin、溶菌酶、[/size][size=12px]壳聚糖等)配合使用。[/size][size=12px]此外,随着科学技术的发展,人们还可以采用一些高科技手段(如采用微生物发酵法生产溶菌酶,采用酶修饰法合成溶菌酶复合物如溶菌酶[/size][size=12px]-环糊精、溶菌酶-半乳甘露聚糖等)生产并改良溶[/size][size=12px]菌酶。经过改良的溶菌酶不仅抗菌活性稳定,而且具有良好的乳化性能。当这些杀菌谱广、成本低、安全性高溶菌酶复合剂以及人工合成溶菌酶商品化时,溶菌酶的使用范围定会越来越广,将会在各行业发挥不可估量的作用。[/size][font='宋体'][size=14px]4. [/size][/font][font='宋体'][size=12px]溶菌酶的限量,检测与标准[/size][/font][size=12px]溶菌酶可水解细菌的细胞壁[/size][size=12px], 造成藤黄微球菌的溶解而引起溶液吸光度值的降低。[/size][size=12px]一个溶菌酶活力单位定义为[/size][size=12px]25 ℃ ,pH 6.2 条件下, 使用藤黄微球菌悬浊液在450 nm 处每分钟引[/size][size=12px]起吸光度变化为[/size][size=12px]0.001 所需溶菌酶的量。[/size][size=12px]试剂和材料[/size][size=12px]藤黄微球菌:ATCC4698 或 CICC10680。[/size][size=12px]0.1 mol/L 磷酸盐缓冲液:pH 6.2。[/size][size=12px]称取[/size][size=12px]11.70 g 磷酸二氢钠(NaH[/size][font='宋体'][size=12px]2[/size][/font][size=12px]PO[/size][font='宋体'][size=12px]4[/size][/font][size=12px] 2H[/size][font='宋体'][size=12px]2[/size][/font][size=12px]O) 、7.86 g 磷酸氢二钠(Na[/size][font='宋体'][size=12px]2[/size][/font][size=12px]HPO[/size][font='宋体'][size=12px]4[/size][/font][size=12px]12H[/size][font='宋体'][size=12px]2[/size][/font][size=12px]O) 及0.372 g[/size][size=12px]乙二[/size][size=12px]胺四乙酸二钠 (EDTA-[/size][font='宋体'][size=12px]2[/size][/font][size=12px]Na)于无菌水中并稀释定容至1000mL。调整缓溶液pH至6.2±0.1。[/size][size=12px]注[/size][size=12px]: 用小份缓冲溶液检查pH, 以避免缓冲溶液被污染。如果需要, 通过加入更多的磷酸二氢钠溶液或磷酸氢二钠[/size][size=12px]溶液调整[/size][size=12px]pH。[/size][size=12px]溶菌酶标准品: 蛋清溶菌酶。[/size][size=12px]底物溶液: 用磷酸盐缓冲液制备50 mL 藤黄微球菌悬浊液。 使用前, 底物于37 ℃ 培养30 min。[/size][size=12px]该底物溶液室温下可稳定[/size][size=12px]2 h。 以磷酸盐缓冲液调分光光度计零点, 然后测定底物溶液的吸光度,450 nm 下读数应为0.70±0.1。[/size][size=12px]仪器和设备[/size][size=12px]分光光度计: 精度±0.001。pH 计。[/size][size=12px]注[/size][size=12px]: 所用的器皿应保持无菌, 保证工作环境的清洁。[/size][size=12px]分析步骤[/size][size=12px]试样溶液的制备[/size][size=12px]准确称取[/size][size=12px]100 mg±0.1 mg 试样, 置于50 mL 容量瓶中, 用约25 mL 磷酸盐缓冲液搅拌溶解并稀释[/size][size=12px]定容[/size][size=12px], 充分混匀。 再转移3 mL 上述试样制备溶液至100 mL 容量瓶中, 用磷酸盐缓冲液搅拌溶解并稀[/size][size=12px]释定容。[/size][size=12px]标准溶液的制备[/size][size=12px]精确称取[/size][size=12px]50 mg 蛋清溶菌酶标准品于50 mL 容量瓶中, 用约25 mL 磷酸盐缓冲液搅拌溶解并稀释[/size][size=12px]定容[/size][size=12px], 充分混匀(如果需要, 冷冻该溶液以备后续测定)。转移3 mL 上述标准制备溶液至100 mL容量[/size][size=12px]瓶中[/size][size=12px], 用磷酸盐缓冲液搅拌溶解并稀释定容。测定[/size][size=12px]取[/size][size=12px]3 份标准溶液和3 份试样溶液进行测定。[/size][size=12px]25 ℃ 室温下, 将1 cm 比色皿放入分光光度计, 用磷酸盐缓冲液调整吸光度零点。 吸2.9 mL 底物[/size][size=12px]溶液于比色皿[/size][size=12px], 最初450 nm 处吸光度应为0.70±0.10,3 min 之内初始吸光度值变化应小于或等于0.003 时, 方可开始测定。 吸取0.1 mL 标准溶液加入底物溶液, 充分混合。 记录3 min 吸光度值的变[/size][size=12px]化[/size][size=12px], 每15s 记录一次吸光度值。 每分钟吸光度值变化应在0.03~0.08, 若不在要求范围需调整试样溶液[/size][size=12px]的浓度。[/size][size=12px] 重复操作测定试样溶液。[/size][size=12px]反应[/size][size=12px]1 min 后稳定, 计算时忽略最初1 min 的读数。[/size][size=12px]结果计算[/size][size=12px]酶活力[/size][size=12px] X , 按式计算:[/size][align=center][size=12px]X =(A[/size][font='宋体'][size=12px]1[/size][/font][size=12px] -A[/size][font='宋体'][size=12px]2[/size][/font][size=12px])[/size][size=12px]/([/size][size=12px]2 × m ×0.001[/size][size=12px])[/size][/align][size=12px]式中[/size][size=12px]:[/size][size=12px]A1 ———[/size][size=12px]试样在[/size][size=12px]450 nm [/size][size=12px]处反应[/size][size=12px]1 min [/size][size=12px]时的吸光度[/size][size=12px] [/size][size=12px]A2 ———[/size][size=12px]试样在[/size][size=12px]450 nm [/size][size=12px]处反应[/size][size=12px]3 min [/size][size=12px]时的吸光度[/size][size=12px] [/size][size=12px]m ———用于分析的试样制备溶液中的溶菌酶质量, 单位为毫克(mg) [/size][size=12px]2 ———获得1 min 和3 min 吸光度读数所用的时间, 单位为分钟(min) [/size][size=12px]0.001———由单位溶菌酶每分钟引起的吸光度降低的值。[/size][size=12px]试验结果以平行测定结果的算术平均值为准。[/size][size=12px] 在重复性条件下获得的两次独立测定结果的绝对差[/size][size=12px]值不大于算术平均值的[/size][size=12px]10%。[/size][size=12px]最终对于溶菌酶的检测要求罗列如下:[/size][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108081546089787_7027_1608728_3.png[/img][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108081546090379_7253_1608728_3.png[/img][/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/08/202108081546091326_4621_1608728_3.png[/img][/align][size=12px]注:本标准适用于以鸡蛋清为原料[/size][size=12px], 经提取、精制等工艺制得的食品添加剂溶菌酶。[/size][size=12px]溶菌酶作为一种天然球状蛋白质,[/size][size=12px] 能促进营养物质被人[/size][size=12px]体消化吸收,[/size][size=12px] 对人体无毒性, 也不会在体内残留, 是一种安[/size][size=12px]全性很高的食品保鲜剂、[/size][size=12px] 营养保健品和药品。 由于每一类型[/size][size=12px]的溶菌酶都有其最适的作用条件,[/size][size=12px] 而且底物特异性强, 因[/size][size=12px]此,[/size][size=12px] 在应用溶菌酶时, 必需注意以下几个事项: ①充分掌握[/size][size=12px]溶菌酶的酶学特性,[/size][size=12px] 掌握食品中的营养成分、 pH 值、 食盐[/size][size=12px]浓度等影响溶菌酶效果的因素以及造成某种食品腐败的主要微生物群体,[/size][size=12px] 采用适当的添加量和添加方法才能收到应有的[/size][size=12px]防腐效果。[/size][size=12px] ②为了有效的发挥溶菌酶作用效力, 可以考虑与[/size][size=12px]其它物质配伍使用。[/size][size=12px] 如将溶菌酶与甘氨酸混合使用, 其防腐[/size][size=12px]效果则远远高于单独使用溶菌酶。[/size][size=12px] 因为甘氨酸含量达到一定[/size][size=12px]程度时,[/size][size=12px] 能抑制微生物细胞壁的合成, 这种作用对革兰氏阳[/size][size=12px]性菌和阴性菌均有效,[/size][size=12px] 从而增了溶菌酶效力的发挥。 也可[/size][size=12px]以考虑与植酸、[/size][size=12px] 聚合磷酸盐等配伍使用, 以增强溶菌酶革兰[/size][size=12px]氏阴性细菌的抑菌作用。[/size][size=12px] 不管与哪种物质配伍使用, 使用之[/size][size=12px]前都要进行小试。[/size][size=12px]参考文献:[/size][font='宋体'][size=14px][1] [/size][/font][font='宋体'][size=12px]GB 1886.257-2016,食品安全国家标准 食品添加剂 溶菌酶[s].[/s][/size][/font][font='宋体'][size=14px][2] [/size][/font][font='宋体'][size=12px]范林林[/size][/font][font='宋体'][size=12px], 林楠, 冯叙桥,等. 溶菌酶及其在食品工业中的应用[J]. 食品与发酵工业, 2015, 41(003):248-253.[/size][/font][font='宋体'][size=14px][3] [/size][/font][font='宋体'][size=12px]冯棋琴[/size][/font][font='宋体'][size=12px], 周立梅, 高文功,等. 溶菌酶在食品工业中的研究进展[J]. 食品研究与开发, 2015, 000(005):134-136[/size][/font][font='宋体'][size=14px][4] [/size][/font][font='宋体'][size=12px]张新宝[/size][/font][font='宋体'][size=12px], 陈红兵. 溶菌酶的性质及其在食品防腐中的应用[J]. 江西食品工业, 2008(4):42-45[/size][/font]
取一份试样调节PH=10,以铬黑T作指示剂,用EDTA滴定锌和镁离子总含量。另取一份试样加氟化铵1g作掩蔽剂,来掩蔽钙,镁离子,加入3ml三乙醇胺掩蔽铝离子。盐酸羟胺溶液作还原剂,在PH=10的条件下用EDTA直接滴定锌离子。这样做是否合理,请大家讨论以下。
请问各位老师,α-淀粉酶溶解之后应该是个什么现象,悬浊液?还是还有固体颗粒状的东西呢,在做5009.82的时候遇到这个问题了,我们溶解出来是含有固体颗粒的沉淀的,结果做出来比标示值大了200%怎么做都降不下来,不知道是不是淀粉酶的原因,求各位老师指导一下??????
石煤提钒酸性废水闭路循环处理技术 摘要 石煤提钒是近几十年新产生的行业,其生产工艺尚未完全成熟,相应配套的环保技术设备不完整。本文首次提出酸性废水闭路循环处理技术及工艺,为提钒工艺研究院所以及钒厂技改提供借鉴参考资料。 关键词 石煤提钒 酸性废水 闭路循环处理 本世纪以前,钒制品产品处于缓慢上升趋势,截止上个世纪90年代中期,我国钒制品生产能力1.3-1.5万吨,主要集中在大型企业,环境污染问题不严重,90年代中期以后,随着国际钒价大幅上扬,本世纪初,我国五氧化二钒总产量约为2万吨,目前保守估计5万吨生产能力,尤其是21世纪以后,我国钒业发展更加迅猛。随着钒业发展,带来的环境问题日益严重,虽然国家制定了相应的产业政策,主要是责令关闭一些小型钒厂,提高了行业准入政策等。但在湖南、陕西等地还是陆续发生了一些钒业污染事故,严重破换了当地的生态环境。这些事故大都是石煤提钒型企业,石煤提钒生产工艺一直处于摸索阶段,是从小型生产方式转变而来,生产历史较短。大规模工业化生产工艺尚不完全成熟,但随着资源、环境的限制,石煤提钒设备投资少,生产成本低综合利用等优势,会有一定规模的发展。 1.石煤提钒酸性废水处理现状1.1吸附尾液成份石煤提钒浸岀液经过树脂提钒后的尾液或萃取提钒后的萃余液,都含有大量的残余酸及硫酸盐等。根据多家钒厂矿石成分的分析,可以间接了解尾液的化学成分。通过矿石成分可以看出原液中,第一类是SiO2,第二类是AL、Fe、Mg金属,第三类是S、P阴离子,第四类是H2SO4。焙烧及添加剂、硫酸浓度对原液中杂质含量影响很大,但成分大致相同。石煤矿石成份(﹪) 1.2尾液石灰中和处理 石灰中和处理是目前石煤提钒通常采用的方法,酸性尾液与石灰中和在碱性条件下,金属氧化物与氢氧化钙生成金属氧化物沉淀与水分离,硫、磷阴离子与钙生成新盐仍然溶解在尾液中,不能分离;硫酸与石灰生成硫酸钙溶在尾液里,二氧化硅也溶解在尾液中。所以采用石灰中和并没有把杂质从尾液中分离出来,只是起到调整PH值的作用。石灰中和法没有起到分离作用,同时浪费资源,是一种不可取的处理方法。化学沉淀法难以从硫酸体系中分离杂质,利用阻滞法从尾液中分离残余硫酸。 2.吸附尾液闭路循环处理工艺 2.1处理工艺流程 酸性浸岀液PH值0.5-1.0左右,含钒量1-5g/L左右,经过离子交换或萃取后,形成的酸性尾液,含有大量金属杂质和SiO2等杂质,这些杂质溶解在酸性尾液中,在酸性体系重金属离子不产生沉淀,不能分离,利用酸回收机分离尾液中的残余酸和相应的硫酸盐,回收的再生酸返回浸出工序补充部分新酸循环使用。中性废水进入污水站,絮凝、压滤分离出的泥饼作为资源回收使用,废水可从浸出渣冲洗水或与综合废水处理排放,也可经膜处理后作为酸回收机反洗水,整个系统闭路循环。2.2酸分离回收处理利用特种填料阻滞分离原理,酸性尾液进入酸分离回收设备,填料将硫酸阻滞在填料上,金属离子随溶液流出设备,尾液成为近中性金属废水,根据用户需求,进入下一步处理工序,然后用水溶解填料上的硫酸,流出溶液形成再生酸,返回酸浸工序循环使用。酸性原液分离数据酸性尾液分离曲线酸性尾液分离溶液 3.小结 尾液中残余硫酸是阻碍处理效果的主要原因,酸分离回收设备将残余酸从尾液中分离并回收重新返到生产工序中,不仅变废为宝,节约资源,同时为石煤提钒废水治理,实现吸附尾液闭路循环,解决关键性的技术和设备,为下一步资源回收,钒厂多元化生产奠定了基础。
做生物样品,加了固体酶,没有溶解,这样酶应该没起作用吧?还能用来做实验吗??请大家多多指导一下,本人对酶了解甚少,谢谢!!
做生物样品,加了固体酶,发现很难溶解,稀释到2600units/ml了(即2mg加2ml缓冲溶液),发现还有大部分酶没有溶解,有什么办法可解决这个问题?(保证酶的浓度大于2000units/ml的情况下)
加热蛋白溶菌酶能杀灭诺如病毒日本东京海洋大学的一个研究小组日前宣布,在实验中发现,加热处理鸡蛋蛋白含有的溶菌酶,能灭活诺如病毒。这是由于溶菌酶能破坏包裹诺如病毒基因的外壳。诺如病毒会引发急性肠胃炎和食物中毒。这种病毒具有强大的感染力,只要有10至100个病毒体进入人体,就会导致感染,目前还没有有效的抗病毒剂。研究小组利用实验鼠的诺如病毒替代人类诺如病毒进行了实验。他们将蛋白中含有的溶菌酶在100摄氏度下加热40分钟,使其变性。接下来,将含有1%加热处理过的溶菌酶的溶液与实验鼠诺如病毒混合在一起,并观察了1分钟之后的变化。溶菌酶是蛋白等含有的一种能水解致病菌中黏多糖的碱性酶。研究人员发现,诺如病毒基因量大幅减少,以致无法检出,并观察到病毒体出现膨胀。他们认为这是由于包裹病毒基因的外壳被破坏导致的。研究人员指出,实验鼠诺如病毒和人类诺如病毒从遗传学上来看非常类似,所以这种加热变性处理的蛋白溶菌酶对人类诺如病毒应该也有效果。他们希望将其制成消毒喷雾剂,在下一年度达到实用化。
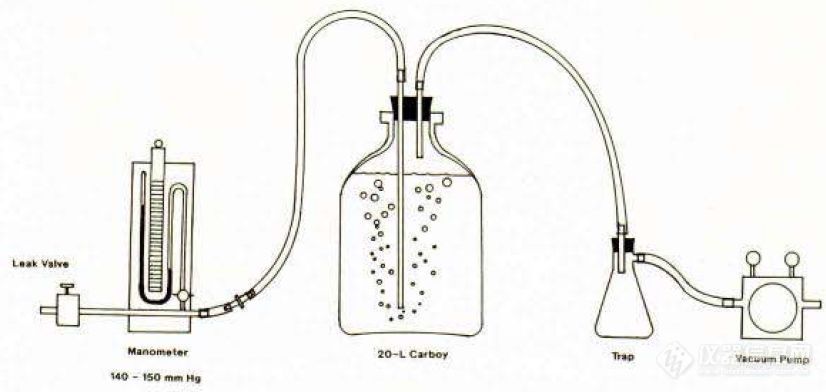
小编在此前文章中为小伙伴们带来了德国DosaTec DosaPrepX8全自动溶媒配制仪后,有不少伙伴来电咨询溶媒配制的法规要求到底有哪些,本文中小编整理了相关要求,以飨读者。各类法规对溶媒(溶出介质)的要求如下,且听小编慢慢道来。[b]USP[/b]药典各论中规定了药品需要采用的溶媒介质,如果采用的是缓冲液,则需要调整溶媒的pH在规定值的±0.05范围内。溶媒中溶解的气体如果使实验结果产生偏差,则需要在实验前进行脱气。脱气的方法可以是:在不断搅拌的状态下加热介质,到大约41℃,立即通过0.45μm或更小孔径的滤膜过滤,在真空状态下继续搅拌约5min。其它经过验证的脱气方法也可以被采用。[align=center][img=,600,284]https://ng1.17img.cn/bbsfiles/images/2019/09/201909101044411772_4638_932_3.jpg!w690x327.jpg[/img][/align][align=center][color=#333333]早期根据USP要求设计的脱气装置[/color][/align][b]USP 溶出方法的开发与验证[/b]在选择溶媒介质时,需要考虑缓冲液、pH值和表面活性剂对药物溶解度和稳定性的影响,当然剂型的主要参数,如硬度、脆度、增溶剂等助剂的加入也会影响药物溶出的释放机理(速释、缓释和控释)和崩解速率。建立溶出方法时,需要符合漏槽条件,即溶媒体积需要至少为药物饱和溶液体积的三倍,达到这个漏槽条件后,溶出结果才能反映为剂型的真正溶出特性。采用水和有机相的混合溶媒是不被提倡的,但如果经过适当的评估,这种类型的溶媒也可以被接受。溶媒的脱气是非常重要的,气泡存在于药剂表面或溶出篮表面,会使药物溶出受阻,导致检测结果偏差。气泡也会附着在转轴、桨和溶出杯内壁,存在于药剂表面的气泡会增加药剂浮力,增加溶出速率,同时减小了药剂与溶媒的接触面,而降低了溶出速率。[align=center][img=,600,795]https://ng1.17img.cn/bbsfiles/images/2019/09/201909101044460307_1108_932_3.png!w448x594.jpg[/img][/align][color=#333333][/color][align=center]篮法溶出实验中,未脱气的溶媒可能产生气泡聚集(A和B)[/align]含表面活性剂的溶媒,通常无需脱气处理,因为脱气反而会产生很多气泡。对于胶囊或者凝胶涂覆的药品,在溶出实验中可以增加酶类物质。[b]溶出机械验证与性能确认工具包USP Toolkit 2.0[/b]溶媒加热的时间需要尽量缩短,需要达到USP要求的脱气要求,真空度建议达到100mbar以下。溶媒体积需要控制在±1%允许范围内,体积需要在室温下测得,更精确的测量方法是采用重量法测量溶媒体积。溶出实验中,溶媒温度需要控制在±0.5℃范围内,每个溶出杯内的溶媒温度都要单独测量。[b]《口服固体制剂溶出度试验技术指导原则》对溶出介质的规定[/b]如有可能,溶出度试验应尽可能在生理条件下进行,这样可以参比制剂体内行为解释相关的溶出度。溶出介质的体积一般为500,900和1000mL,最好为漏槽条件,但不强制要求。应采用pH为1.2~6.8的水性介质,一般不超过pH8.0。某些制剂和组分对溶出介质中溶解的空气敏感,因此需要脱气。[align=center][img=,300,260]https://ng1.17img.cn/bbsfiles/images/2019/09/201909101044490080_5202_932_3.jpg!w272x236.jpg[/img] [img=,300,261]https://ng1.17img.cn/bbsfiles/images/2019/09/201909101044519813_2858_932_3.jpg!w271x236.jpg[/img][/align][color=#333333][/color][color=#333333][/color]下面我们梳理一下法规要求和Dosatec DosaPrepX8的符合性: [table=535][tr][td=1,1,249]法规具体要求项[/td][td=1,1,165]DosaPrepX8性能[/td][td=1,1,121]符合性[/td][/tr][tr][td=1,1,249]溶媒体积控制在±1%[/td][td=1,1,165]1%[/td][td=1,1,121]✔ [/td][/tr][tr][td=1,1,249]更精确的体积测量方法是重量法[/td][td=1,1,165]重量法[/td][td=1,1,121]✔ [/td][/tr][tr][td=1,1,249]溶出介质的体积为500,900和1000mL[/td][td=1,1,165]150~8000mL可选[/td][td=1,1,121]✔ [/td][/tr][tr][td=1,1,249]真空度建议达到100mbar[/td][td=1,1,165]一般<100mbar[/td][td=1,1,121]✔ [/td][/tr][tr][td=1,1,249]pH为1.2~6.8的水性介质[/td][td=1,1,165]完全符合[/td][td=1,1,121]✔ [/td][/tr][tr][td=1,1,249]pH要求值的±0.05内[/td][td=1,1,165]完全符合[/td][td=1,1,121]✔ [/td][/tr][tr][td=1,1,249]溶媒加热的时间需要尽量缩短[/td][td=1,1,165]整个配制过程仅15min,包含混合、加热和脱气。[/td][td=1,1,121]✔ [/td][/tr][/table]
外媒:欧洲多国收紧防疫措施应对奥密克戎扩散,荷兰再度实施封锁,要求关闭所有"非必需"公共场所.
有测壁纸中的可溶性元素的吗?用icp-oes测壁纸中的8种可溶性元素,在测加标回率时发现As,Sb,Cd的回收率偏低,不知问题出在那了? 是不是壁纸样品基体影响太大呢?各位指点一下.
苯并吡喃酮作为一个非常重要的结构内核单元,广泛地存在于很多天然产物中,并且是一些具有生物活性的化合物的特定前导化合物。此外该类化合物也因其具有一些光致变色效应和热致变色性质而受到广泛关注。 生物催化作为一种绿色高效的现代有机合成技术,在医药、能源、材料等领域显示出巨大的潜力。酶作为一种高效,环境友好的催化剂,已经成为传统有机金属和小分子催化剂的有效补充,尤其是酶的非专一性在有机合成方面的应用备受研究者的青睐。近些年,已有一系列关于水解酶催化非专一性的C-C键以及C-杂原子键的形成反应的报道,但是对于单酶催化的多步串联反应的报道较少。基于此,我们设计和发展基于水解酶催化非专一性的domino反应,发现枯草杆菌α-淀粉酶可以有效地催化水杨醛和丁烯酮发生oxa-Michael/aldol缩合反应合成2H-苯并吡喃酮类化合物。2H-苯并吡喃酮的生物合成在25 mL烧瓶中加入水杨醛(2 mmol),不饱和醛或酮(10 mmol),50 mg 枯草杆菌α-淀粉酶(BSA),再加入500μL去离子水和4.5 mL DMSO,将其置于50℃恒温摇床中震荡反应(200 rpm)。TLC跟踪检测反应(紫外灯下观测),反应完全后,加入20 mL蒸馏水停止反应,然后用乙酸乙酯萃取(3×10 mL),有机相用无水硫酸钠干燥后,经减压蒸馏除去溶剂,经柱层析分离得目标产物(硅胶:300-400目,流动相:石油醚[font='Times
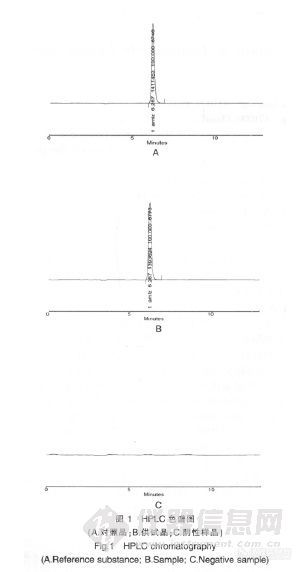
作者:孙蕊;刘世超; (河南省洛阳市中心医院药剂科;河南省洛阳市妇女儿童医疗保健中心药剂科;)摘要:目的:建立高效液相法测定奥美拉唑镁肠溶片含量的方法。方法:采用Diamonsil-C18(4.6 mm×150 mm,5μm)色谱柱;流动相:甲醇-水-磷酸-三乙胺(65∶35∶0.12∶0.3);检测波长:302 nm;流速:1.0 ml/min。结果:奥美拉唑镁在13.3182~31.0758μg范围内与峰面积呈良好的线性关系(r=0.999 0),平均回收率为101.14%,RSD=1.64%。结论:本法简便、准确、重现性好,可用于奥美拉唑镁肠溶片的质量控制。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208201413_384697_1606903_3.jpg
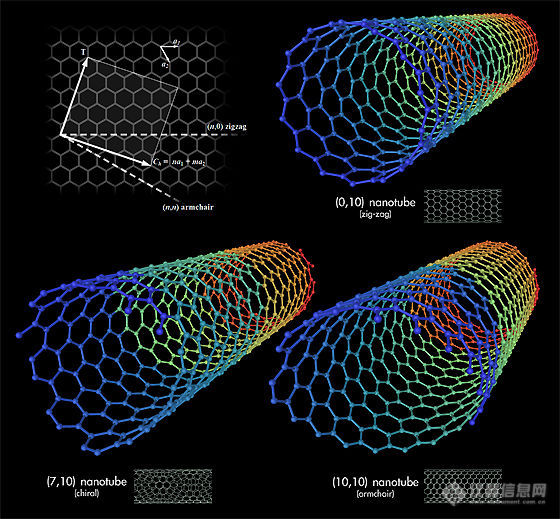
[align=center][color=#666666] [/color][/align][color=#666666]在回流操作或浓缩溶液时,经常会有结晶析出在液面上方的烧瓶内壁上,且附着牢固,不仅不能继续参加反应,有时还会因热稳定性差而逐渐分解变色。[/color][color=#666666]遇此情况,可轻轻振摇烧瓶,以内部溶液浸润结晶,使其溶解。[/color][color=#666666]如果装置活动受限,不能振摇烧瓶时,可用冷的湿布敷在烧瓶上部,使溶剂冷凝沿器壁流下时,溶解析出的结晶。[/color]
如何克服熔剂挂壁后黏附炸裂问题?
称取0.2000g吡虫啉,用100ml甲醇溶解,可是最后还是有很多吡虫啉没有溶解。为什么?怎样才可以使全部吡虫啉都能溶解呢? 此外,还有什么溶剂可以溶解吡虫啉比甲醇更好的吗?
1 前言 煤灰的熔融性是动力用煤高温特性的重要测定项目之一,是动力用煤的重要指标,它反映煤中矿物质在锅炉中的变化动态。测定煤灰熔融性温度在工业上特别是火电厂中具有重要意义。 第一,可以提供锅炉设计选择炉膛出口烟温和锅炉安全运行的依据。在设计锅炉时,炉膛出口烟温一般要求比煤灰的软化温度低50~100℃,在运行中也要控制在此温度范围内,否则,会引起锅炉出口过热器管束间灰渣的“搭桥”,严重时甚至发生堵塞,从而导致锅炉出口左右侧过热蒸汽温度不正常。 第二,可以预测燃煤的结渣。因为煤灰熔融性温度与炉膛结渣有密切关系。根据煤粉锅炉的运行经验,煤灰的软化温度小于1350℃就有可能造成炉膛结渣,妨碍锅炉的连续安全运行。 第三,可为不同锅炉燃烧方式选择燃煤。不同锅炉的燃烧方式和排渣方式对煤灰的熔融性温度有不同的要求。煤粉固态排渣锅炉要求煤灰熔融性温度高些,以防炉膛结渣;相反,对液态排渣锅炉,则要求煤灰熔融性温度低些,以避免排渣困难。因为煤灰熔融性温度低的煤在相同温度下有较低的粘度,易于排渣。 第四,可判断煤灰的渣型。根据软化区间温度(DT—ST)的大小,可粗略判断煤灰是属于长渣或短渣。一般认为当(ST—DT)=200~400℃为长渣;(ST—DT)=100~200℃为短渣。通常锅炉燃用长渣煤时运行较安全。燃用短渣煤时,由于炉温增高,固态排渣炉可能在很短的时间内就出现大面积的严重结渣情况;燃用长渣煤时,DT、ST之间的温差虽超过200℃,但固态排渣炉的结渣相对进行得较为缓慢,一旦产生问题,也常常是局部性的。 综上所述,是煤灰熔融性测定的重要性,必须掌握煤灰熔融性的准确测定方法,以达到确保锅炉安全经济燃烧的目的。2 测定煤灰熔融性设备的技术要求 按国家标准GB219—74规定要求,应用硅碳管高温炉应满足有足够大的恒温区,恒温区内温差应不大于5℃;能按照规定的温升速度升温至1500℃;炉内气氛能方便控制为弱还原性或氧化性;能在试验过程中随时观察试样的变化情况;电源要有足够容量,可连续调压。 铂铑—铂热电偶及高温计,测温范围为0~1600℃,最小分度为5K,经校正后(半年校正一次)使用,热电偶要用气密性刚玉管保护,防止热端材质变异。 灰锥模子,由对称的两半块构成的黄铜或不锈钢制品。 灰锥托板模,由模座、垫片和顶板三部分构成,用硬木或其他坚硬材料制做。 常量气体分析器,可测定一氧化碳、二氧化碳和氧气含量。3 气氛条件的控制 煤灰熔融性温度测定的气氛一般有两种,一种是氧化性气氛,另一种是弱还原性气氛。常用的气氛是弱还原性气氛。这是因为在工业锅炉的燃烧中,一般都形成由CO、H2、CH4、CO2和O2为主要成分的弱还原性气氛,所以煤灰熔融性温度测定一般也在与之相似的弱还原性气氛中进行。所谓弱还原性气氛,是指在1000~1300℃范围内,还原性气体(CO、H2、CH4)总含量在10%~70%之间,同时在1100℃以下时,它们和CO2的体积比不大于1:1,含氧量不大于0.5%。 对于弱还原性气氛的控制方法,一般有两种,一种是封碳法,它是将一定量的木碳、石墨、无烟煤等含碳物质封入炉中,这些物质在高温炉中燃烧时,产生还原气体(CO、H2、CH4),形成弱还原性气氛。封碳法简单易行,在国内普遍采用。另一种是通气法,在测定煤灰熔融性温度的炉内通入40%±5%的一氧化碳和60%±5%的二氧化碳混合气或50%±10%的二氧化碳和50%±10%的氢气混合气。通气法容易调节并能获得规定的气体组成。对于氧化性气氛的控制,是煤灰熔融性温度测定炉内不放置任何含碳物质,并使空气在炉内自由的流通,这一方法更为简单,也被许多电厂采用。4 测定步骤4.1 灰的制备 取粒度小于0.2mm的分析煤样,按照测定灰分的方法,将煤样置于瓷方皿内,放入箱形电炉中,使温度在30min内逐渐升到500℃,在此温度下保持30min,然后升至815±10℃,关闭炉门灼烧1h,使煤样全部灰化,之后取出方皿冷却至室温,再将煤灰样用玛瑙钵研细,使之粒度全部达到0.1mm以下。4.2 灰锥的制做 取1~2g煤灰样放在瓷板或玻璃板上,用数克糊精水溶液湿润并调成可塑状,然后用小尖刀铲入不锈钢灰锥模中挤压成高为20mm,底边长7mm的正三角形锥体,锥体的一个棱面垂直于底面。用小尖刀将模内灰锥小心地推至瓷板或玻璃板上,放在空气中干燥或放入60℃恒温箱内干燥后备用。4.3 在弱还原性气氛中测定 用10%糊精水溶液将少量氧化镁调成糊状,用它将灰锥固定在灰锥托板的三角坑内,并使灰锥的垂直棱面垂直于托板表面。将带灰锥的托板置于刚玉舟的凹槽内,如用封碳法来产生弱还原性气氛,预先在舟内放置足够量的碳物质。打开高温炉炉盖,将刚玉舟徐徐推入炉内,使灰锥位置恰好处于高温恒温区的中央,将热电偶插入炉内,使其顶端处于灰锥正上方5mm处,关上炉盖,开始加热并控制升温速度为:900℃以下时,(15~20℃/min),900℃以上时(5±1℃/min)。如用通气法产生弱还原性气氛,应通入1:1的氢气和二氧化碳混合气体,当炉内温度为600℃时开始通入二氧化碳,以排除炉内的空气,700℃时开始通入混合气体。气密性较好的炉膛,每分钟通入100ml,以不漏入空气为准。每20min记录一次电压、电流和温度。随时观察灰锥的形态变化(高温下观察时,需戴上墨镜),记录灰锥的四个熔融特征温度:变形温度DT,软化温度ST,半球温度HT,流动温度FT。待全部灰锥都达到流动温度或炉温升至1500℃时断电,结束试验,待炉子冷却后,取出刚玉舟,拿下托板,仔细检查其表面,如发现试样与托板作用,则需另换一种托板重新试验。5 测定结果的判断 在测定过程中,灰锥尖端开始变圆或弯曲时温度为变形温度DT,如有的灰锥在弯曲后又恢复原形,而温度继续上升,灰锥又一次弯曲变形,这时应以第二次变形的温度为真正的变形温度DT。 当灰锥弯曲至锥尖触及托板或锥体变成球形或高度不大于底长的半球形时的温度为软化温度ST。 当灰锥变形至近似半球形即高等于底长的一半时的温度为半球温度HT。 当灰锥熔化成液体或展开成高度在1.5mm以下的薄层或锥体逐渐缩小,最后接近消失时的温度为流动温度FT。某些灰锥可能达不到上述特征温度,如有的灰锥明显缩小或缩小而实际不熔,仍维持一定轮廓;有的灰锥由于表面挥发而锥体缩小,但却保持原来形状;某些煤灰中SiO2含量较高,灰锥易产生膨胀或鼓泡,而鼓泡一破即消失等,这些情况均应在测定结果中加以特殊说明。6 测定结果的表达 将记录灰锥的四个熔融特征温度(DT、ST、HT、FT)的重复测定值的平均值化整到10℃报出。当炉内的温度达到1500℃时,灰锥尚未达到变形温度,则该灰样的测定结果以DT、ST、HT、FT均高于1500℃报出。由于煤灰熔融性是在一定气氛条件下测定的,测定结果应标明其测定时的气氛性质及控制方法。标明托板材料及试验后的表面状况,及试验过程中产生的烧结、收缩、膨胀和鼓泡等现象及其产生时的相应温度。 根据灰熔融性温度的高低,通常把煤灰分成易熔、中等熔融、难熔和不熔四种,其熔融温度范围大致为: 易熔灰ST值在1160℃以下; 中等熔融灰ST值在1160~1350℃之间; 难熔灰ST值在1350~1500℃之间; 不熔灰ST值则高于1500℃。 一般把ST值为1350℃作为锅炉是否易于结渣的分界线,灰熔融性温度越高,锅炉越不易结渣;反之,结渣严重。7 煤灰熔融性测定的精密度 煤灰熔融性测定的精密度值见表1。(略)8 影响煤灰熔融性温度的因素8.1 粒度大小 煤灰粒度小,比表面积大,颗粒之间接触的机率也高,同时,还具有较高的表面活化能,因此,同一种煤灰,粒度小的比粒度大的熔融性温度低。例如某种煤的煤灰的软化温度在粒度小于600μm 时为1175℃;粒度小于250μm时为1165℃;粒度小于75μm时为1140℃。8.2升温速度 若在软化温前200℃左右,急剧升温比缓慢升温所测出的软化温度高。当升温速度缓慢时,煤灰中化学成分间相对有时间进行固相反应,因此,软化温度点相对在较低温度出现。8.3 气氛性质 煤灰的熔融性温度受气氛性质的影响最为显著,特别是含铁量大的煤灰更为明显。这主要是由于煤灰中铁在不同性质气氛中有不同形态,并进一步产生低熔融性的共熔体所致。因此要定期检查炉内气氛的性质,才能保证测定结果的可靠性,通常检查炉内气氛性质的方法有下列两种。参比灰锥法:此法简单易行,效果较好,被广泛采用。先选取具有氧化和弱还原性两种气氛下的煤灰熔融性温度的标准煤灰,制成灰角锥,而后置于炉中,按正常操作测定其四个特征温度,即变形温度(DT),软化温度(ST),半球温度(HT),流动温度(FT)。 当实测的软化温度(ST),半球温度(HT),流动温度(FT)与弱还原性气氛下的标准值相差不超过50℃时,则认为炉内气氛为弱还原性。如果超过50℃,则要根据实测值与氧化气氛或弱还原性气氛下的相应标准值的接近程度及封碳物质的氧化情况判断炉内气氛性质。气体分析法:用一根内径为3~5mm
什么叫溶媒?
现在有一个锑铋锌合金样品,其中锑含量大于50%,现在试了多种溶样酸都没办法溶解,求高手帮助。
请问各位老师污水中的溶解性镁、总镁,还有高温残留物(600度)都怎么检测啊?
有些化学试剂以及配成的溶液要避光保存,是见光分解还是氧化,浓度会降低吗?

今天收到客户一个实验,检测奥美拉唑镁肠溶片,溶出度实验,样品中有一个杂质未分开,希望安排售前实验,进行色谱柱的筛选。以辛烷基硅烷键和硅胶为填充剂,流动相是0.01M磷酸氢二钠(磷酸调pH=7.6)-乙腈=75:25,波长302nm,要求奥美拉唑峰与杂质I分离度大于2.0.下面是客户做的结果,实验室色谱柱筛选工作正在进行中……http://ng1.17img.cn/bbsfiles/images/2016/03/201603071349_586166_1987954_3.png
测定硫酸根的钡镁溶液如果与空气中二氧化碳反应生成沉淀是碳酸钡还是碳酸镁?
[b]问题:[b][b][b][/b][/b]艾司奥美拉唑镁肠溶片的检测,流动相是?[/b]答案:流动相: A:水-磷酸盐缓冲溶液-乙腈(80:10:10) B:乙腈-磷酸盐缓冲溶液-水(80:1:19)=======================================================================【活动内容】1、每个工作日上午10:00左右发布一个关于应用数据库的应用问答题,版友根据题目给出自己理解的答案。2、每个工作日下午15:10公布参考答案。【活动奖励】幸运奖:抽奖软件,当天随机抽取3个或5个回答正确的版友ID号(最后一个ID号,截止至下午15:00),每人奖励[color=#ff0000]2钻石币[/color](抽奖人数≤10,抽取3个版友;抽奖人数>10,抽取5个版友);中奖名单:lijing320323(注册ID:lijing320323)999youran(注册ID:999youran)dahua1981(注册ID:dahua1981)PAEs(注册ID:v2911392)吕梁山(注册ID:shih20j07)[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/09/201809041504163298_6848_1610895_3.png!w690x388.jpg[/img][img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/09/201809041504189792_3148_1610895_3.png!w690x388.jpg[/img]积分奖励:所有回答正确的版友奖励[color=#ff0000]10个积分[/color](幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次[/b][align=left][color=#ff0000][b]PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。[/b][/color][/align][align=left][color=#ff0000][b] 下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。[/b][/color][/align][align=center]=======================================================================[/align]方法:HPLC基质:药品应用编号:103783化合物:艾司奥美拉唑色谱柱:[url=http://www.dikma.com.cn/product/details-855.html]Platisil ODS 5μm 250 x 4.6mm[/url]样品前处理:有关物质供试品:精密称取20mg样品置于100mL容量瓶中,加10mL甲醇,振摇,加20mL磷酸盐缓冲溶液(每1000mL水中加入磷酸钠0.0137mol和磷酸氢二钠0.0551mol),超声使其溶解,用水稀释到100mL,混匀,过滤,取续滤液。色谱条件:色谱柱: Platisil ODS 250*4.6 mm,5 μm(Cat#:99503)流动相: A:水-磷酸盐缓冲溶液-乙腈(80:10:10) B:乙腈-磷酸盐缓冲溶液-水(80:1:19)磷酸盐缓冲溶液:1000mL水+磷酸二氢钠0.0052mol+磷酸氢二钠0.0315mol流速: 1.0 mL/min柱温: 30 ℃检测器: 302nm进样量: 20uL文章出处:天津应用实验室关键字:艾司奥美拉唑镁肠溶片、Platisil ODS、99503、HPLC摘要:Platisil ODS检测艾司奥美拉唑镁肠溶片。图谱:[img]http://www.dikma.com.cn/u/image/2017/01/05/1483598227111770.jpg[/img][img]http://www.dikma.com.cn/u/image/2017/01/05/1483598227527569.jpg[/img][img]http://www.dikma.com.cn/u/image/2017/01/05/1483598227109068.jpg[/img]
最近开展了封闭溶样测定微量金,结果总偏低,不知道大家在这方面有什么经验,不妨说出来交流一下!