请教各位:考马斯亮兰检测蛋白质中磷酸起什么作用?在配置考马斯亮兰时(称100mg考马斯亮兰G-250,溶于50ml95%的乙醇后,再加入120ml85%的磷酸,用水稀释至1L)其中,乙醇和磷酸起什么作用?可不可以改变磷酸的浓度?
采用考马斯亮蓝法测定提取液中的蛋白质需要准备那些试剂及仪器?
一、标准曲线一般用分光光度法测物质的含量,先要制作标准曲线,然后根据标准曲线查出所测物质的含量。因此,制作标准曲线是生物检测分析的一项基本技术。二、蛋白质含量测定方法 1. 凯氏定氮法2. 双缩脲法3. Folin-酚试剂法4. 紫外吸收法5. 考马斯亮蓝法三、考马斯亮蓝法测定蛋白质含量—标准曲线制作 (一)试剂: 1. 考马斯亮蓝试剂:考马斯亮蓝G—250 100 mg溶于50 ml 95%乙醇,加入100 ml 85% H3 PO4 ,雍蒸馏水稀释至1000 ml,滤纸过滤。最终试剂中含0.01%(W/V)考马斯亮蓝G—250,4.7%(W/V)乙醇,8.5%(W/V)H3 PO4 。2. 标准蛋白质溶液:纯的牛血清血蛋白,预先经微量凯氏定氮法测定蛋白氮含量,根据其纯度同0.15 mol/LNaCl配制成100 ug/ml蛋白溶液。(二)器材: 1. 722S型分光光度计使用及原理。2. 移液管使用。(三)标准曲线制作: 1. 试管编号0123456100ug/ml标准蛋白(ml)0.00.10.20.30.40.50.60.15mol/L NaCl (ml)10.90.80.70.60.50.4考马斯亮蓝试剂 (ml)5555555摇匀,1h内以1号管为空白对照,在595nm处比色A595nm2. 以A595nm 为纵坐标,标准蛋白含量为横坐标(六个点为10ug、20 ug、30 ug、40 ug、50 ug、60 ug),在坐标轴上绘制标准曲线。(1)利用标准曲线查出回归方程。(2)用公式计算回归方程。(3)或用origin作图 ,测出回归线性方程。即A595nm =a×X( )+6;一般相关系数应过0.999以上,至少2个9以上。(4)绘图时近两使点在一条直线上,在直线上的点应该在直线两侧。(四)蛋白质含量的测定: 样品即所测蛋白质含量样品(含量应处理在所测范围内),依照操作步骤1操作,测出样品的A595nm ,然后利用标准曲线或回归方程求出样品蛋白质含量。一般被测样品的A595nm 值在0.1—0.05之间,所以上述样品如果A595nm 值太大,可以稀释后再测A595nm值,然后再计算。(五)注意事项: 1. 玻璃仪器要洗涤干净。2. 取量要准确。3. 玻璃仪器要干燥,避免温度变化。4. 对照:用被测物质以外的物质作空白对照。蛋白质含量测定实验难度系数 0共 0 人点评打分实验材料结晶牛血清清蛋白 g—球蛋白试剂(盒)Na2CO3酒石酸钾钠蒸馏水硫酸铜钨酸钠钼酸钠磷酸硫酸锂液体溴NaOH酚酞仪器耗材可见光分光光度计旋涡混合器秒表[url=http://www.biomart.cn/equipm
请教一个问题:考马斯亮蓝法测总蛋白质含量,目标物中总蛋白含量大概在0.0001-0.06mg/g范围内,有合适的仪器推荐吗? 目前有一台普通的721型可见分光光度计,试测效果不佳。
大家好,请教各位一个问题: 文献报道,考马斯亮蓝G-250在游离状态下呈红色,最大光吸收在488nm;当它与蛋白质结合后变为青色,蛋白质-色素结合物在595nm波长下有最大光吸收。其光吸收值与蛋白质含量成正比,因此可用于蛋白质的定量测定。 但我按照文献配制的G-250(0.1mg/mL)是紫色的,用紫外光谱检测时超出量程,所以用二次水稀释一倍,检测其最大吸光度值,不在488nm,将其和一定浓度的牛血清白蛋白结合,发现其颜色并未变成青色,吸光度也不在595nm,而是随着蛋白浓度的增加红移。实验现象与文献完全不同,不知道是哪里出错了,请教各位! 很着急,请知情人解答疑惑,万分感谢!
最近小弟在做考法测蛋白质含量,结果出现与书本上不相符的一些东东,书本上是说考马斯亮蓝在游离态下呈红色的,可是我配出来的贮备液是呈现暗绿色做实测的时候:对照:蓝色样品:青色郁闷啊,不知是试剂问题还是水的问题请高手指点啊
用考马斯亮蓝法测定蛋白质含量,发现蛋白质与染色液混合后吸光度值很不稳定,在1h内时间越长,吸光度越来越低,与文献上的越来越高并趋于稳定有所差异,不知道是不是这个原因,做加标回收率很低,求大神指教到底是什么原因会导致这样的情况。
染色用的考马斯亮蓝染液弄到手上了,怎么弄掉啊,对身体有危害吗?http://simg.instrument.com.cn/bbs/images/brow/em09508.gif
考马斯亮蓝法测定蛋白质含量加标回收率在80%左右,怎么做都升不上去,请大神指教有可能的原因,样品是β环糊精,蛋白质含量在0.2%左右
[align=left][font=仿宋]考马斯亮蓝法检测样品中蛋白质含量需要的G250染液和BSA标准蛋白需要单独购买吗?有配套的吗?[/font][/align][font=仿宋][font=仿宋][/font][/font]
GS-Smart小型自动凝胶染色摇床在考马斯亮蓝染色实验中的应用考马斯亮蓝染色法(CBB染色法)是目前蛋白质染色实验中相当常用的方法,它既克服了氨基黑染色灵敏度不高的限制,号称目前灵敏度最高的蛋白质测定法之一,而又比硝酸银染色等其他方法更简便且更加容易操作,因而得到了广泛应用。考马斯亮蓝染色法的全实验过程有两个关键且耗时较长的步骤,分别是染色和脱色。通常,为了让蛋白凝胶能够充分的染色和脱色,一般会先后将CBB染色液、脱色液加入持续摇摆的脱色摇床工作池,再置入凝胶使其充分浸润洗涤,从而实现染色脱色。普通的脱色摇床除了工作池的摆动频率可以调节外,并没有其他参数可以设置,进液、换液和排液等步骤都必须由实验人员手动完成。而且启动后,由于工作池一般是持续不停的摆动,因而染色、脱色时间也只能靠实验人员自己把握。所以,普通考马斯亮蓝染色脱色实验一般都需要有实验人员值守。此外,为固定蛋白质和维持CBB在染色前的酸性环境,同时也为了去除前期电泳残留物质对染色的干扰,通常配置的CBB染色液或脱色液中有时会加入具有神经毒性的甲醇和强刺激性的乙酸,且配好的CBB染色液一般总体呈棕黑色(CBB R-250)。而普通脱色摇床的工作池完全敞开暴露,所以摆动过程中有可能溅出溢出CBB染色液、脱色液,还有可能挥发出有毒化合物。这样不仅容易造成污染,甚至可能产生安全隐患,进而危害实验人员的健康。鼎昊源GS-Smart小型自动凝胶染色摇床(又名自动凝胶染色仪)可以很好地解决以上普通考马斯亮蓝染色脱色实验所面临的问题,同时也能带来更多便利。首先,她的智能编程功能可以实现进液、换液、出液、定时摇动、废液回收的自动运行,全过程无需人员值守,从而真正全自动完成CBB染色脱色实验。其次,她配备了可封闭的染色池,能有效防止CBB染色液、脱色液溅出溢出,阻隔挥发物质,从而大大降低污染风险,保护实验人员的健康。染色池还有多款尺寸可选,甚至可以定制,从而尽可能多地满足不同科研工作者对考马斯亮蓝染色脱色实验的不同需求。第三,鼎昊源GS-Smart小型自动凝胶染色摇床操作起来也十分简单方便,只需“加入溶液、置入凝胶、设置管路程序、点击运行”四个简单的步骤,便可轻松搞定考马斯亮蓝染色、脱色的全过程,省时省力省心。另外,再值得一提的是,鼎昊源GS-Smart小型自动凝胶染色摇床还拥有国际外首创的机身与储液瓶一体化设计,与市场同类产品相比,减少了分散在外的瓶瓶罐罐,节省了实验室空间,同时也美化了整体外观。本文关键词:染色摇床,自动凝胶染色摇床,考马斯亮蓝染色,CBB染色
[b][font=宋体]摘要:[/font][/b][font=宋体]试样经乙酸溶解,经过滤后制备成测试溶液。经紫外法预测试,蛋白浓度较低,选择考马斯亮蓝法([/font]Braford[font=宋体]法)测定蛋白浓度。以[/font]BSA[font=宋体]溶液浓度绘制标准曲线,其线性相关系数达到[/font]0.99[font=宋体]以上。标定样品蛋白浓度时发现测量值超出标曲的有效计算范围。降低实验测试[/font]BSA[font=宋体]浓度和反应试剂体积,重新绘制微量蛋白浓度标准曲线,测定后可得蛋白浓度为[/font] 11.05μg/ml[font=宋体],玉米秸秆中蛋白含量为[/font]0.221%[font=宋体]。[/font][b][font=宋体]关键词:[/font][/b][font=宋体]蛋白质浓度;考马斯亮蓝法;玉米秸秆[/font][b]1 [font=宋体]蛋白质浓度测定方法对比[/font][/b](1) [font=宋体]双缩脲法:双缩脲是在大约[/font]180°C[font=宋体]条件下加热两个尿素分子,以达到释放出一个氨分子而获得的产物。在强碱性溶液中,缩二脲和硫酸铜形成紫色络合物,称为缩二脲反应。当底物中含有肽键时(多肽),试液中的铜与多肽配位,配合物呈紫色。可通过比色法分析浓度,在紫外可见光谱中的波长为[/font]540nm[font=宋体]。[/font](2) Folin[font=宋体]酚试剂法:[/font]Folin—[font=宋体]酚试剂中的磷钼酸盐[/font]—[font=宋体]磷钨酸盐被蛋白质中的酪氨酸和色氨酸残基还原,产生深蓝色(钼兰和钨兰的混合物)。在一定的条件下,蓝色深度与蛋白的量成正相关。这个测定法的优点是灵敏度高,比双缩脲法灵敏得多。[/font](3) [font=宋体]紫外法:蛋白质分子中含有共轭双键的酪氨酸、色氨酸等芳香族氨基酸。它们具有吸收紫外光的性质,其吸收高峰在[/font]280nm[font=宋体]波长处,且在此波长内吸收峰的光密度值与其浓度成正比关系,故可作为蛋白质定量测定的依据。[/font](4) [font=宋体]考马斯亮蓝法:也称[/font]Bradford[font=宋体]检测法,考马斯亮蓝[/font]G-250[font=宋体]在游离状态下呈红色,最大光吸收在[/font]488nm[font=宋体];当它与蛋白质结合后变为青色,蛋白质[/font]-[font=宋体]色素结合物在[/font]595nm [font=宋体]波长下有最大光吸收。其光吸收值与蛋白质含量成正比,因此可用于蛋白质的定量测定。[/font][b]2 [font=宋体]试剂和材料[/font]2.1 [font=宋体]试剂[/font][/b]1[font=宋体])[/font]BSA[font=宋体]粉末[/font]2[font=宋体])乙酸[/font]3[font=宋体])考马斯亮蓝试剂:([/font]Thermo CoomassiePlus Assay Reagent[font=宋体])[/font][b]2.2 [font=宋体]仪器设备[/font][/b]1) Amersham Biosciences Ultrospec 2100 [i]pro[/i][align=left]2) [font=宋体]分析天平[/font][/align][align=left]3) [font=宋体]涡旋振荡器[/font][/align][align=left]4) [font=宋体]离心机[/font][/align][align=left]5) [font=宋体]石英比色皿[/font][/align][b]3 [font=宋体]实验方法[/font]3.1 [font=宋体]配置样品溶液[/font][/b][font=宋体]称取粉碎均匀的样品[/font] 25mg [font=宋体]至[/font] 15ml [font=宋体]离心管中,加入[/font] 1%[font=宋体]乙酸水溶液[/font] 5ml[font=宋体],样品终浓度为[/font] 5mg/ml[font=宋体],颠倒混匀至样品完全溶解。[/font][b]3.2 [font=宋体]配置常规蛋白浓度标准品和样品[/font][/b][font=宋体]称取[/font]BSA [font=宋体]粉末[/font] 2mg [font=宋体]左右至[/font] 2ml [font=宋体]离心管中,加入[/font] 1%[font=宋体]乙酸水溶液[/font] 1ml[font=宋体],标准品母液终浓度为[/font] 2mg/ml[font=宋体]。用[/font] 1%[font=宋体]乙酸水将标准品分别稀释至表[/font]1[font=宋体]中标准蛋白浓度。[/font][b]3.3 [font=宋体]测试[/font][/b][font=宋体]用二次水做[/font]blank[font=宋体]。取[/font]200μl[font=宋体]考马斯亮蓝试剂与[/font]200μl[font=宋体]标准品[/font]/[font=宋体]样品混合,室温放置[/font]10[font=宋体]分钟,测定在[/font]595nm[font=宋体]波长吸收值。每个测试样品至少重复三次。[/font][b]3.4 [font=宋体]配置微量蛋白浓度标准品[/font][/b][font=宋体]称取[/font]BSA [font=宋体]粉末[/font] 2mg [font=宋体]左右至[/font] 2ml [font=宋体]离心管中,加入[/font] 1%[font=宋体]乙酸水溶液[/font] 1ml[font=宋体],标准品母液终浓度为[/font] 2mg/ml[font=宋体]。用[/font] 1%[font=宋体]乙酸水将标准品分别稀释至表[/font] 2 [font=宋体]中标准蛋白浓度。[/font][b]3.5 [font=宋体]微量蛋白浓度测试[/font][/b][font=宋体]用二次水做[/font]blank[font=宋体]。取[/font]750μl[font=宋体]考马斯亮蓝试剂与[/font]25μl[font=宋体]标准品[/font]/[font=宋体]样品混合,室温放置[/font]10[font=宋体]分钟,测定在[/font]595nm[font=宋体]波长吸收值。每个测试样品至少重复三次。[/font][b]4 [font=宋体]结果[/font]4.1 [font=宋体]绘制标准曲线[/font][/b][font=宋体]根据[/font] 125~1000 μg/ml OD595 [font=宋体]绘制标准曲线,获得线性相关曲线如图[/font] 1[font=宋体]。线性相关方程为[/font] y=0.0008x + 0.0522[font=宋体],[/font]R2=0.9937[font=宋体]。[/font][img=,415.15,219.75]file:///C:/Users/jiajia66/AppData/Local/Temp/msohtmlclip1/01/clip_image001.png[/img][align=center][b][font=黑体]图[/font]1 [font=黑体]常规浓度标准曲线[/font][/b][/align][b]4.2 [font=宋体]测定并计算蛋白浓度[/font][/b]经过分析检测,标准品和样品与亮蓝[font='Times New Roman',serif]G-250[/font]试剂反应后[font='Times New Roman',serif]OD595nm[/font]吸收峰为如下:[align=center][b][font=黑体]表[/font]1 [font=黑体]标准曲线测定[/font][/b][/align] [table=614][tr][td] [font=宋体]标准物([/font]BSA[font=宋体])[/font][font=宋体]浓度([/font]μg/ml[font=宋体])[/font] [/td][td] 0 [/td][td] 25 [/td][td] 125 [/td][td] 250 [/td][td] 500 [/td][td] 750 [/td][td] 1000 [/td][td] 1500 [/td][td] 2000 [/td][td] [font=宋体]样品[/font][font=宋体]([/font]5mg/ml[font=宋体])[/font] [/td][/tr][tr][td] OD(595nm) [/td][td] 0.348 [/td][td] 0.339 [/td][td] 0.466 [/td][td] 0.546 [/td][td] 0.737 [/td][td] 1.014 [/td][td] 1.160 [/td][td] 1.265 [/td][td] 1.399 [/td][td] 0.341 [/td][/tr][tr][td] [/td][td] 0.327 [/td][td] 0.345 [/td][td] 0.466 [/td][td] 0.589 [/td][td] 0.822 [/td][td] 0.992 [/td][td] 1.107 [/td][td] 1.257 [/td][td] 1.406 [/td][td] 0.350 [/td][/tr][tr][td] [/td][td] 0.309 [/td][td] 0.347 [/td][td] 0.471 [/td][td] 0.589 [/td][td] 0.821 [/td][td] 1.024 [/td][td] 1.187 [/td][td] 1.255 [/td][td] 1.433 [/td][td] 0.354 [/td][/tr][tr][td] [font=宋体]平均值[/font] [/td][td] 0.328 [/td][td] 0.343667 [/td][td] 0.467667 [/td][td] 0.574667 [/td][td] 0.793333 [/td][td] 1.01 [/td][td] 1.151333 [/td][td] 1.259 [/td][td] 1.412667 [/td][td] 0.348333 [/td][/tr][tr][td] [font=宋体]扣除[/font]blank [/td][td] [/td][td] 0.015667 [/td][td] 0.139667 [/td][td] 0.246667 [/td][td] 0.465333 [/td][td] 0.682 [/td][td] 0.823333 [/td][td] 0.931 [/td][td] 1.084667 [/td][td] [/td][/tr][/table][font='Times New Roman',serif] [/font]带入标准曲线由此计算可得样品中蛋白含量过低,超出标准曲线范围。因此采用微量浓度测定方法。[b]4.3 [font=宋体]绘制微量蛋白浓度标准曲线[/font][/b][font=宋体]根据[/font] 3~30 μg/mlOD595 [font=宋体]绘制标准曲线,获得线性相关曲线如图[/font] 1[font=宋体]。线性相关方程为[/font] y=0.0166x + 0.0845[font=宋体],[/font]R2=0.9906[font=宋体]。[/font][img=,393.4,205.15]file:///C:/Users/jiajia66/AppData/Local/Temp/msohtmlclip1/01/clip_image002.png[/img][align=center][b][font=黑体]图[/font]2 [font=黑体]微量浓度标准曲线[/font][/b][/align][b]4.4[font=宋体]测定并计算蛋白浓度[/font][/b][align=left][font=宋体]由此计算可得样品中蛋白浓度为[/font] 11.05 μg/ml[font=宋体],蛋白含量为[/font]0.221%[font=宋体]。[/font][/align][align=center][b][font=黑体]表[/font]2 [font=黑体]微量蛋白浓度标准曲线测定[/font][/b][/align] [table=613][tr][td] [font=宋体]标准物([/font]BSA[font=宋体])[/font][font=宋体]浓度([/font]μg/ml[font=宋体])[/font] [/td][td] 0 [/td][td] 3 [/td][td] 6 [/td][td] 12 [/td][td] 24 [/td][td] 30 [/td][td] [font=宋体]样品[/font][font=宋体]([/font]5mg/ml[font=宋体])[/font] [/td][/tr][tr][td] OD(595nm) [/td][td] 0.256 [/td][td] 0.365 [/td][td] 0.43 [/td][td] 0.561 [/td][td] 0.744 [/td][td] 0.828 [/td][td] 0.521 [/td][/tr][tr][td] [/td][td] 0.245 [/td][td] 0.371 [/td][td] 0.44 [/td][td] 0.557 [/td][td] 0.744 [/td][td] 0.811 [/td][td] 0.526 [/td][/tr][tr][td] [/td][td] 0.253 [/td][td] 0.361 [/td][td] 0.44 [/td][td] 0.564 [/td][td] 0.747 [/td][td] 0.816 [/td][td] 0.511 [/td][/tr][tr][td] [font=宋体]平均值[/font] [/td][td] 0.251333 [/td][td] 0.365667 [/td][td] 0.436667 [/td][td] 0.560667 [/td][td] 0.745 [/td][td] 0.818333 [/td][td] 0.519333 [/td][/tr][tr][td] [font=宋体]扣除[/font]blank [/td][td] [/td][td] 0.114334 [/td][td] 0.185334 [/td][td] 0.309334 [/td][td] 0.493667 [/td][td] 0.567 [/td][td] 0.268 [/td][/tr][/table]
AOAC 992.23杜马斯燃烧法检测谷物、油籽中粗蛋白质 英文版 pdf格式杜马斯法优于凯式定氮法[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=125929]AOAC 992.23杜马斯燃烧法检测谷物、油籽中粗蛋白质[/url]
中文名称: 托马斯杨 外文名: Young,Thomas 生卒年: 公元1773年~1829年 故居: 英国萨默塞特郡的米尔弗顿 洲: 欧洲 国别: 英国 省: 萨默塞特郡 托马斯杨,英国医生兼物理学家,光的波动说的奠基人之一。1773年6月13日托马斯杨生于英国萨默塞特郡的米菲尔顿一个富裕的贵格会教徒的家庭,是十个孩子中的老大。从小就有神童之称,兴趣十分广泛,两岁就学会了看书,十四岁时用拉丁文写过一篇自传,就在当时他已掌握了多种语言。在杨成年后,他对职业的选择受到了他叔父的影响,他的叔父是一位卓越的医生,杨在家庭同意下转到了医学方面。在十九岁时,他进入伦敦的圣巴塞罗缪医学院学医,21岁时,即以他的第一篇关于眼睛的调节机理的医学论文成为英国皇家学会会员。为了进一步深造,他到爱丁堡和剑桥继续学习,后来又到德国哥廷根去留学继续研究医学。在那里,他受到一些德国自然哲学家的影响,开始怀疑起光的微粒说。1797年回到英国,进入剑桥的伊曼纽尔学院继续攻读医学,1799年杨在剑桥大学完成了学习。那时,他的叔父已经去世,去世时留给他一笔巨大遗产,包括房屋、书籍、艺术品和一万英镑现款。这笔巨大遗产使他在经济上完全独立,帮助他度过了一生。1801年托马斯杨进行了著名的杨氏干涉实验,为光的波动说的复兴奠定了基础。1803年,杨已是知名的物理学家了,被聘为伦敦皇家学院自然哲学教授。1802年他被选为皇家学会的外事秘书,他担任这个职务一直到他去世。1818年他被任命为《航海天文历》的主持人,做了不少工作以改进实用天文学和航海援助工作。1829年5月10日托马斯杨在伦敦逝世。终年五十六岁。研究领域:托马斯.杨在物理学上最杰出的贡献是在光学和声学领域。在1973年发表的关于生理光学的论文《对视觉过程的观察》中,他研究了眼睛对距离的调节问题,并证明眼睛适应不同距离,是靠改变眼球水晶体的曲度来进行的。1800年,在继续进行这方面的实验中,形成了他对光的本质的看法,这一年他向皇家学会提出了《在声和光方面的实验和问题》的报告。他认为,声和光都是波的传播,光是在充满整个空间的以太流体中传播的弹性振动,由于以太极稀薄,所以光是以纵波形式传播的,光的颜色和不同频率的声音是类似的。他指了,在解释强光源和弱光源发出的光以同样的速度传播的问题上,用波动说比粒子说更容易,因为,光粒子为什么只以一个不变的速度运动,这是很难理解的。论文中关于声学的一部分特别重要。托马斯.杨在这部分分析了水波的干涉现象后指出,在声波迭加的情况下,会产生声音的加强和减弱、复合的声调和拍频。“干涉”这个术语,就是他最先提出的。 在1801年发表的一篇报告中,采用著名的杨氏干涉实验,托马斯.杨发展了惠更斯的光学理论,形成了波动光学的基本原理。他提出了光波的频率和波长的概念,并解释了牛顿环现象。在这篇论文中,他叙述了他所发现的“简单而普遍的规律”:“同一束光的两个不同部分,以不同的路径要末完全一样地,要末在方向上十分接近地进入眼睛,在光线的路程差是某个长度的整数倍的地方,光就增强,而在干涉区域的中间部分,光将最强。对于不同颜色的光束来说,这个长度是不同的。 他指出,牛顿环的明暗条纹,就是由不同界面反射出的光互相重合产生“干涉”的结果。位相相反的振动迭加起来就互相抵消,位相相同的则互相加强。他用实验的办法确证了他所提出的这一假设。他用紫外光投射到薄层上,使紫外光从上下两个界面反射产生干涉。由于紫外光是人眼所看不见的,他就让反射光落在涂有氯化银溶液的纸上,结果出现了黑环,从而证明了他的干涉原理。他精确地确定了各种色光的波长值。他指出:“根据各种实验的比较,组成极端红光的波的宽度,在空气中,似应假定约为三万六千分之一英寸,极端紫光的约为六万分之一英寸。” 在1803年11月24日的报告中,托马斯.杨把干涉原理应用于解释衍射现象。他知道,光能绕过不透明物体的边缘产生有色的影子,并认为这种衍射条纹是直接通过衍射缝的光和边界波的干涉产生的。在这篇论文中,他用光从较密介质反射时的半波损失,补充了他关于薄板颜色的理论。 此外,托马斯.杨在其他领域也做出了不菲的成就。他第一个测量了7种颜色光的波长,从生理角度说明了人眼的色盲现象;他还建立了三原色原理,指出一切色彩都可以从红、绿、蓝这三种原色的不同比例的混和而得到。托马斯杨对弹性力学很有研究,特别是对胡克定律和弹性模量。后人为了纪念杨氏的贡献,把纵向弹性模量(正应力与线应变之比)称为杨氏模量。他还首先使用运动物体的能量一词来代替活力。1814年他开始研究考古发现的古埃及石碑,他用了几年时间破译了碑上的文字,对考古学作出了贡献。作品:1、《自然哲学与机械工艺课程》(1807年)2、《医学文献介绍及实用疾病分类学》(1813年)3、《拉普拉斯天体力学原理阐明》(1821年)4、《声和光的实验和探索纲要》(1801年)5、《对视觉过程的观察》(1973年)6、《自然哲学讲义》(1807年)曾获奖项:1、1794年被选为英国皇家学会会员。2、当选为法国科学院院士。
各位:有没有使用过杜马斯仪的,就是燃烧法测定蛋白质的仪器,能谈谈您认为的有缺点吗?准确性有没有保证,能不能提高效率?我们在考虑是否不是买一台,谢谢。
杜马斯定氮仪的相关标准如下:1.中华人民共和国国家标准 杜马斯燃烧法测定饲料原料中的总氮含量2. 农业部标准 谷类、豆类粗蛋白含量的测定 杜马斯燃烧法3. 中华人民共和国出入境检验检疫行业标准 进出口食品和饲料中总氮及粗蛋白的检测方法 杜马斯燃烧法漏掉了最重要的标准:食品安全国家标准 食品中蛋白质的测定
ISO 16634.2:2006 杜马斯燃烧法测定谷物豆类研磨谷物产品油菜籽动物饲料中氮和蛋白质 国际标准 英文版 pdf格式杜马斯燃烧法优于传统凯式法。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=125919]ISO 16634.2:2006 杜马斯燃烧法测定谷物豆类研磨谷物产品油菜籽动物饲料中氮和蛋白质[/url]
为什么杜马斯法有存在的价值?它有什么优点和缺点?它能给我解决什么问题?奔着这三个问题,我大概说下杜马斯定氮仪的优势和劣势,并给您算笔小账。杜马斯法最大的优点有两个: 1.安全:样品只需要称量和包样后即可放进自动进样器开始试验,结果在电脑上自动显示。相比凯式法要进行的前期消解就容易溅烫到操作人员,而且实验室里的味道很大,对皮肤也不好。如果老师注重实验室安全,杜马斯法无疑是首选。 2.解放人力资源:通俗的讲就是高效。杜马斯法的前期样品称量和包样需要人员操作,样品进自动进样器后,人员就可以去做其他的了,所有结果会自动在电脑上显示,一个样品4分钟的分析时间,一两个小时候操作人员就可以直接打出数据,中间无需看守。假如我们一天要做50个样品,称量、包样和记录的时间约20秒一个样。50个样品的包样、记录时间20分钟足够。放入自动进样器、在电脑上输入重量和样品名称每个样品也要花大概20秒时间。50个样品也是20分钟。那么,这50个样品,只需要一个实验人员总共花费40分钟的时间就可以得出全部结果。(仪器平时基本不关,下班后处于休眠状态即可,第二天上班后很快就达到工作温度)50个样品如果用凯式法做,相信大家很熟悉需要花多长时间,3炉消解将近3个小时,进样后,检测期间人员要在旁边记录,不能做其他的事情,4分钟一个样品,要做3个半小时。算上数据输入记录等时间的话,前后要花7、8个小时,即一个工作人员一天的时间。可以说,每做50个样品,杜马斯法就能帮客户节省一个实验人员一天的工作时间。如果实验室一年做10000个样品(量超级大了),用杜马斯法就完全能解放一个工作人员。再假设实验室的样品量足够大,一台杜马斯定氮仪一天可以做100个样品来计算,一年即是30000个样品(工作日),可以解放出3个工作人员从事其他研究,如此一来,即使是工资费用就节省十几万元,更何况没有安全隐患,工作环境大大改善。这是假设样品量足够大。很多单位肯定没这么大的量,一般是一天只做十几个样品,一周做两三天,那么,十几个样品用杜马斯法要20分钟足够,凯式法的话,需要2个小时。也能是带来很大便利的。 杜马斯定氮仪的缺点是: 1.购置成本高:一台杜马斯定氮仪约合人民币大概50万,比凯式定氮仪贵很多。 2.做样成本高:一台杜马斯定氮仪的做样总耗材成本约合5-6元人民币(所有耗材都算上),也是凯式定氮仪做样成本的好几倍。但这只是硬件成本,考虑到人力资源的释放和安全隐患,总成本是低于凯式定氮仪的。 综上所述,对于样品量大的客户来说,杜马斯定氮仪的综合经济成本不比凯式定氮仪高,还可以营造绿色、安全的工作环境,数据结果准确,精度高,平行好。相关的国标也有,检测结果可以作为依据。非常适合样品量大的检测行业用户。所以。回到开头,杜马斯定氮仪存在的价值是因为它安全(绿色)、高效(解放了人)。它很适合经常做蛋白质检测的单位,或者应付继续大量蛋白质检测这样的突发事件。以上是我个人的一点见解,欢迎批评交流。
对于食品、谷物、肥料、动物饲料及相关产品,全氮和蛋白质含量的测定是非常重要的。目前,用于农产品的最常用的定氮方法是Kjeldahl于1883年提出的凯氏法,虽然后来经过改进,但是消化时间长、难以把有机物定量转变成氨以及严重的环境污染是此法存在的典型问题在过去的十年里,一种快速、精确、低成本、无污染的定氮方法很快的在欧美国家得到了广泛应用,成为凯氏法的替代方法, 即杜马斯燃烧定氮法(Combustion Nitrogen Analysis )。此法是Jean BaptisteDumas 于1831 年提出的,比凯氏定氮法早50 年,但是由于早期的定氮方法只能测定几个毫克的样品,使它在农产品等领域的实际应用中受到了极大的限制。近十年来,随着可以检测克级样品的杜马斯法快速定氮仪问世,拉开了其在食品、饲料、肥料、植物、土壤及临床等领域上广泛应用的序幕。本文着重介绍了Dumas 法的原理,杜马斯法与凯氏法的优劣,以及杜马斯法在国内外农产品领域中的应用。
有国产的杜马斯定氮仪吗? 价格多少?
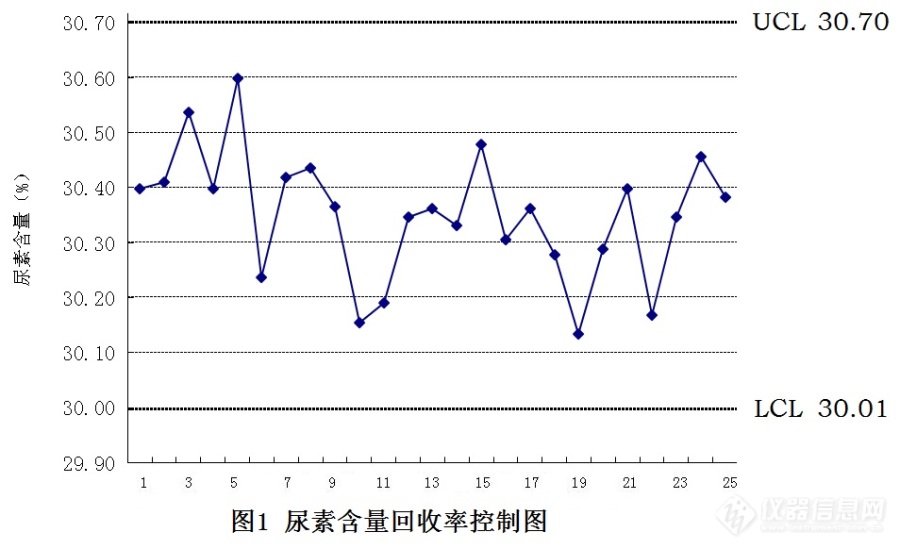
[align=center][b]杜马斯定氮仪关键测试验收指标初探[/b][/align][align=center]山西省产品质量监督检验研究院 曹仲杰 李学哲[sup]*[/sup][/align]摘要:杜马斯定氮仪是利用杜马斯高温燃烧法对样品中氮含量进行检测的一个专用化学分析仪器。本文主要讨论了在验收D100杜马斯定氮仪时,根据仪器生产企业的一般交货验收规定、验收用相关标准、仪器运行稳定性数理统计等,探究了杜马斯定氮仪含氮量检测的相关验收关键技术要求,为今后仪器验收工作探索了一些有益的经验。关键词:杜马斯定氮仪 验收 规定 标准 稳定性0 引言:汽车尾气所引发的环境污染已成为造成空气污染的主要原因。北京雾霾天气的成因存在争议,从政府公布的结论是20-30%的污染是来源于汽车尾气排放[sup][/sup]。尽管柴油车在我国机动车保有量中所占比例不到20%,但其排放的颗粒污染物(PM)和氮氧化物(NOx)分担率均超过60%[sup][/sup]。目前,SCR(Selective Catalytic Reduction的简称)技术已广泛推广使用,《柴油发动机氮氧化物还原剂尿素水溶液(AUS 32)》[sup][/sup]标准规定的目标值是32.5%的尿素水溶液(AUS32)。由于尿素水溶液(AUS32)主要成分是氮元素,氮含量的多少决定了产品的还原能力最佳效率问题,杜马斯定氮仪作为一款新型、高效、专用定氮仪由此应运而生。近日我单位新购进一台由山东海能科学仪器有限公司生产的D100杜马斯定氮仪,是引进、消化、吸收的正宗国产仪器。近期,发表在《中国招标》2016年第6期的 “2.8亿招标采购国产仪器为何遭排挤?”[sup][/sup]一文引起了人们对国产仪器相关问题的高度关注,人们对此纷纷发表议论,有关国产仪器的分析讨论热度空前,研究与进展、验证与评价等助推国产仪器发展的论文更是引人注目[sup][/sup]。但是一个不可忽略的事实是我国检测仪器贸易逆差不断,国产检测仪器处境尴尬[sup][/sup]。我们购置的D100杜马斯定氮仪是一个带有样品前处理装置,使用双通道TCD检测器,专用于氮元素检测的专业分析仪器。本文主要在该仪器验收工作的相关基础上,对有关验收测试时所作的一些关键指标做了相应的研究讨论,其目的就是为今后的国产仪器验收工作提供一定的基础参考资料。1 企业提供的仪器验收方法介绍1.1 仪器验收路径仪器验收主要分为5个步骤:仪器介绍 →开箱验收→仪器安装→仪器校准→测试验收① 仪器介绍:仪器简介,仪器特点,技术指标,测试原理等;② 开箱验收:清点配件及主要耗材并简单介绍用途③ 仪器安装:a)燃烧管、干燥管安装;b) 检查仪器通信是否正常;c) 气路联接、检查、检漏。④ 仪器校准⑤ 测试验收:样品制备、制作标准曲线、样品测试。样品测试阶段主要是按照GB 29518-2013中的规范性附录A的方法进行。标准规定每个样品至少做三次,只要三次独立测定结果的精密度和再现性符合标准要求,就达到验收目的,验收合格。具体在验收时可以多做几次,测试结果均要符合标准要求。1.2 仪器验收方法存在的缺陷讨论仪器验收用户最关心的是仪器的适用性,能否按相关标准进行规范检测不是仪器验收关键所在。如:标准规定做的三次独立测定,若第四次就出现问题,该如何处理?三次是不是就是最佳的结果,有没有可能能做N多次后结果的精密度和再现性也能符合标准要求,这样的结果可信度是不是更高?仪器若能达到这样的效果,我们为什么不去考证? 若能出现独立测试五次及以上的好的结果,对以后的能力验证、科学研究等应该是有益的,也可以考虑这样的结果在其他领域里存在有扩大仪器适用范围的可能。我们在仪器验收时,对样品测试方案做了一些调整,具体为:①8~9次的独立测定结果的精密度和再现性的标准符合性考证;② 连续20~25次独立测定结果的控制图法,监控所购仪器的分析系统的可靠性。2 调整后的测试验收结果分析 本仪器验收时的试验方法是按照GB 29518-2013中的规范性附录A的方法进行,这里对试验方法过程不在赘述。只对试验的结果进行讨论,以此来评价所购置的仪器的主要性能能否满足试验要求。2.18~9次独立测定的结果标准要求的是正常不少于3的独立测试结果。我们验收的要求是8~9次独立测定的结果,明显高于标准要求,我们这里考虑更多的是测试中会有各种情况发生,如果仪器的连续工作的可靠性差的话,是无法满足日常检验任务要求的。需要说明的是仪器验收我们只对重复性的结果进行了探讨。8~9次独立测定的具体结果见表1。表1 三组尿素水溶液氮含量平行实验的结果 [table][tr][td=1,2] [align=center]序号[/align] [/td][td=1,2] [align=center]样品[/align] [align=center]名称[/align] [/td][td=2,1] [align=center]第一组[/align] [/td][td=2,1] [align=center]第二组[/align] [/td][td=2,1] [align=center]第三组[/align] [/td][/tr][tr][td] [align=center]样品重量[/align] [align=center](mg)[/align] [/td][td] [align=center]氮含量[/align] [align=center](%)[/align] [/td][td] [align=center]样品重量[/align] [align=center](mg)[/align] [/td][td] [align=center]氮含量[/align] [align=center](%)[/align] [/td][td] [align=center]样品重量[/align] [align=center](mg)[/align] [/td][td] [align=center]氮含量[/align] [align=center](%)[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td=1,4] [align=center]天冬氨酸[/align] [align=center]N标准物质[/align] [/td][td] [align=center]150.90[/align] [/td][td] [align=center]10.566[/align] [/td][td] [align=center]151.48[/align] [/td][td] [align=center]10.444[/align] [/td][td] [align=center]150.11[/align] [/td][td] [align=center]10.550[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]150.16[/align] [/td][td] [align=center]10.593[/align] [/td][td] [align=center]149.54[/align] [/td][td] [align=center]10.502[/align] [/td][td] [align=center]150.32[/align] [/td][td] [align=center]10.452[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]149.38[/align] [/td][td] [align=center]10.528[/align] [/td][td] [align=center]149.97[/align] [/td][td] [align=center]10.684[/align] [/td][td] [align=center]149.70[/align] [/td][td] [align=center]10.545[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]149.03[/align] [/td][td] [align=center]10.438[/align] [/td][td] [align=center]150.59[/align] [/td][td] [align=center]10.608[/align] [/td][td] [align=center]149.73[/align] [/td][td] [align=center]10.587[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td=1,8] [align=center]尿素[/align] [align=center]水溶液[/align] [align=center]样品[/align] [/td][td] [align=center]103.87[/align] [/td][td] [align=center]14.324[/align] [/td][td] [align=center]98.15[/align] [/td][td] [align=center]14.566[/align] [/td][td] [align=center]97.07[/align] [/td][td] [align=center]14.340[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]101.14[/align] [/td][td] [align=center]14.290[/align] [/td][td] [align=center]96.09[/align] [/td][td] [align=center]14.576[/align] [/td][td] [align=center]100.82[/align] [/td][td] [align=center]14.433[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]103.28[/align] [/td][td] [align=center]14.365[/align] [/td][td] [align=center]96.66[/align] [/td][td] [align=center]14.505[/align] [/td][td] [align=center]96.67[/align] [/td][td] [align=center]14.285[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]100.56[/align] [/td][td] [align=center]14.331[/align] [/td][td] [align=center]95.29[/align] [/td][td] [align=center]14.481[/align] [/td][td] [align=center]94.55[/align] [/td][td] [align=center]14.488[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]97.66[/align] [/td][td] [align=center]14.255[/align] [/td][td] [align=center]104.02[/align] [/td][td] [align=center]14.524[/align] [/td][td] [align=center]99.53[/align] [/td][td] [align=center]14.351[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]103.43[/align] [/td][td] [align=center]14.264[/align] [/td][td] [align=center]101.79[/align] [/td][td] [align=center]14.448[/align] [/td][td] [align=center]100.69[/align] [/td][td] [align=center]14.438[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]105.52[/align] [/td][td] [align=center]14.371[/align] [/td][td] [align=center]96.07[/align] [/td][td] [align=center]14.507[/align] [/td][td] [align=center]96.11[/align] [/td][td] [align=center]14.378[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]101.15[/align] [/td][td] [align=center]14.339[/align] [/td][td] [align=center]98.98[/align] [/td][td] [align=center]14.532[/align] [/td][td] [align=center]96.77[/align] [/td][td] [align=center]14.356[/align] [/td][/tr][tr][td] [align=center]9[/align] [/td][td] [align=center] [/align] [/td][td] [align=center]101.43[/align] [/td][td] [align=center]14.299[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][/tr][tr][td] [align=center] [/align] [/td][td] [align=center]RSD[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]0.29[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]0.29[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]0.45[/align] [/td][/tr][/table]2.2N次测定结果的分析可靠性控制图例控制图是实验室监测质量监控常用的方法,检验工作应该是在满足控制图要求的情况下进行,若控制图发生问题,就要采取有效措施,去满足日常检验要求。所以我们进行了控制图法的检验验收工作。参照《常规控制图》[sup][/sup]标准,我们对检测的25组尿素含量检测的回收率数据进行重复性测试后,依据《数据的统计处理和解释正态样本离群值的判断和处理》[sup][/sup]标准,我们对测试后的尿素含量结果分别进行了计算,由此给出了25次测定结果的质量控制图,见图1。[img=,690,420]http://ng1.17img.cn/bbsfiles/images/2018/07/201807011005314498_5952_2345874_3.jpg!w690x420.jpg[/img]2.3 调整后的测试验收结果的分析讨论2.3.1 8~9次独立测定的结果说明对照GB 29518-2013中规范性附录A的精密度要求,标准要求的实验结果的相对偏差是1.0%,我们的3组重复性测试结果分别是:0.29%,0.29%,0.45%,均满足标准的小于1.0%的要求。说明验收的这台D100杜马斯定氮仪是满足我们预定的对立测试N次的结果要求的。2.3.2 N次测定结果的分析可靠性控制图的结果说明 从尿素含量回收率控制图上分析,我们的质量控制结果是符合要求的。可以确定为仪器验收时的质量控制要求是满足一般实验室的检验质检质量控制需求的。3 结束语本文主要在对D100杜马斯定氮仪进行开箱,组装,验收等一系列步骤的基础上对于其验收中测试验收工作相关问题进行了讨论。仪器验收领域的标准或规范等国家没有具体规定,2017年颁布的《分析化学仪器设备验证与综合评价指南》[sup][/sup]认证认可标准对于国产仪器的评价有了一定的指导意义,但是方案中对于测试过程中需要通过怎样的手段来完成验证,未做具体规定。我们就是在这次杜马斯定氮仪的测试验收中,通过多次独立测定和N次测定结果的控制图的试验佐证了仪器的可靠性,通过分析可靠性,有效指导了本次测试验收工作。仪器验收工作非常重要,希望多关注一些仪器验收的细节问题,在一定程度上,能够助推国产仪器更快、更好发展。参考文献[color=#cc0000](不完全版)[/color]1 张楫泽,刘憬然,孔漪宝. 北京雾霾现象与机动车尾气排放关系分析 北方环境. 2013(11):115-1172 邓华,余运波,贺泓. 银/氧化铝催化乙醇选择性还原氮氧化物过程中典型中间体的吸附态研究催化学报.2015(8):1312-13203 GB 29518-2013,柴油发动机氮氧化物还原剂尿素水溶液(AUS 32) [s].[/s]
请问一下,在有机元素分析中什么叫杜马斯高温分解原理?
麻烦一下,进口杜马斯定氮仪都值多少钱

[b][color=#cc0000]马克思[/color][color=#cc0000]名[/color][color=#cc0000]言[/color][color=#cc0000]——[/color][color=#cc0000]马斯科名[/color][/b][color=#cc0000][b]言 ![img=,521,477]https://ng1.17img.cn/bbsfiles/images/2022/10/202210201417579164_2317_1841897_3.jpg!w521x477.jpg[/img][/b][/color]
马斯克:将于2030年左右开建首座火星城市,即火星基地阿尔法
杜马斯定氮仪做个样品大概多少成本,使用过的告诉下啊
对于食品、谷物、乳制品、肥料、动物饲料、植物、烟草及相关产品,全氮和蛋白质含量的测定是非常重要的。传统凯氏定氮法作为工业标准已执行很多年,但繁复的操作步骤、耗时长、使用腐蚀性酸、难以把有机物定量转变成氨以及严重的环境污染较难满足当前检测发展的需求。在过去的十年多里,一种快速、精确、低成本、无污染、自动化高的定氮方法很快的在欧美国家得到了广泛应用,成为凯氏法的替代方法,即杜马斯(DUMAS)燃烧定氮法。杜马斯法目前已被很多组织认可,如: AOAC,ASBC, EBC, AACC和 ISO,成为法定的氮/ 蛋白质分析方法。在美国、加拿大和德国的某些领域,杜马斯法甚至作为唯一的定氮标准。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=86763]制备色谱技术—在天然产物分离中的应用(霍斯泰特曼&马斯顿)[/url]
AOAC 968.06杜马斯法测定饲料中粗蛋白质杜马斯法为燃烧法,优于凯式法。 [img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=125924]AOAC 968.06杜马斯法测定饲料中粗蛋白质[/url]
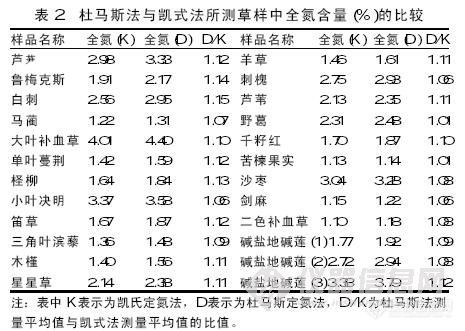
1 引 言 氮是植物需求量最大的矿物质营养元素,同时也是植物个体乃至自然生态系统和人工生态系统(包括农业系统)生长最常见的限制因子。在植物体中含有的氮,大部分是作为蛋白质、氨基酸、酰胺及其它与蛋白质有关的物质的组成而存在的,此外少部分作为硝酸态存在。 全氮是植物成分分析中非常重要的项目之一。全氮的测定方法有很多种,最经典的方法为凯氏定氮法,但是普通的凯氏法不便定量硝态氮,而其含量可能相当高。 此外,对-N=N-,http://www.dsddy.cn/Upload/UploadPic/201042612017583.jpg,-N=O, -NO2等的定量也是困难的。对于大量含有这些形态氮的样品,应采用各自的定量方法进行检测。但通常用能定量植物样品中大部分氮素的凯氏法所定量的氮作为全氮。若样品中含有较多硝态氮时,可用水杨酸硫酸分解法还原硝酸,这种方法比较烦琐。目前在欧美等发达国家广泛采用杜马斯燃烧法取代凯氏法。这种方法是使样品在高温纯氧环境中燃烧后,分离出氮气,并被热导检测器检测,检测出的结果包含了硝态氮。此法也因其快速,精确,无污染等优点而得到了广泛的认可。对两种定氮方法做一比较是非常必要的。以下简介杜马斯燃烧定氮法,并对两种方法测定几种植物样品中的全氮进行了对比。2 杜马斯燃烧定氮法 早在1833年,Jean Baptiste Dumas就开发出燃烧定氮法,后人定名为杜马斯(Dumas)法。该方法的发明比凯氏法还早50年,但是由于早期的杜马斯法只能检测几个毫克的样品,使它的实际应用受到了极大的限制,在随后的岁月里这种方法没有被广泛的应用开来。近十年来,随着可以检测克级样品的杜马斯法快速定氮仪问世,才拉开了其在食品、饲料、肥料、植物、土壤及临床等领域上广泛应用的序幕。目前,在西方国家的很多实验室都已用杜马斯法代替凯氏法检测全氮。http://ng1.17img.cn/bbsfiles/images/2010/12/201012032157_264274_1641058_3.jpg 凯氏定氮法需要较大的劳动强度和分析时间,且操作过程较为危险,产生化学废物污染环境。相比之下,杜马斯法有很大的优势:它不需要对样品做复杂的前处理,只要适当的粉碎;单个样品分析只要3-5分钟,可用自动进样器连续进样,不需要人看守;它不用有害试剂,不产生污染物质,对操作人员和环境都是安全的。表1归纳了两种方法的特点。3 实验部分3.1凯氏定氮法3.1.1原理利用浓酸溶液将有机物中的氮分解出来。均匀的样品在沸腾的浓硫酸中作用,形成硫酸铵。加入过量的碱于硫酸消解液中,将NH4+ 转变成NH3,然后蒸馏出NH3,用接受液吸收。通过测定接受液中氨离子的量来计算样品中氮的含量。3.1.2仪器全自动凯氏定氮仪。3.2杜马斯燃烧定氮法3.2.1原理样品在900℃~1200℃高温下燃烧,燃烧过程中产生混合气体,其中的干扰成分被一系列适当的吸收剂所吸收,混合气体中的氮氧化物被全部还原成分子氮,随后氮的含量被热导检测器检测。3.2.2仪器蛋白质测定仪 。3.2.3反应过程(基于ZDDN-II氮/蛋白质分析仪)样品在高温下燃烧,燃烧生成的气体被载气 CO2携带直接通过氧化铜(作为催化剂)而被完全氧化。此外,化合物中一定量的难氧化部分会被载气携带通过作为催化剂的氧化铜和铂混合物进一步氧化。燃烧生成的氮氧化物在钨上还原为分子氮,同时过量的氧被结合。用传感器控制最佳燃烧所需的氧气量,以保证氧气和钨的消耗量最少。用一系列的吸收剂将干扰成分如H2O、SO2、HX从被检测气流中除去。用TCD热导检测器来检测 CO2 载气流中的氮。用标准物质独立校正,被测样品中含氮量自动计算、打印和存储。4 结果与讨论凯氏法一个公认的局限性是它不能定量NO3-N (植物样品全氮的重要组成部分)( Silvertooth和Westerman,1988)。Sader等人(2004)发现NO3-N的存在会影响全氮含量。Simonne et al.(1995)和Etheridge et al.(1998)也证实,在分析植物样品时,杜马斯法得到的全氮值总是略微高于凯氏法的测定值。本实验也得到了同样的结果。http://ng1.17img.cn/bbsfiles/images/2010/12/201012032158_264275_1641058_3.jpg由表2可以看出,凯氏氮总是低于杜马斯氮,D/K的值均大于1。Sader等(2004)认为,凯氏氮与杜马斯氮在同类样品中呈线性相关,通过校正因子对硝态氮进行校正后,两种结果差异不显著。对于草类样品,凯氏氮低于杜马斯氮的程度是否与样品中硝态氮的含量有关及其相关性如何尚需进一步研究。此外,植物的不同部位以及生长的不同阶段其硝态氮的含量和分布会有所不同,用凯氏法及杜马斯法测得的总氮结果会有何等差异,在本文中未曾涉及,有待进一步探讨。5 结 论由于植物样品中多含有硝态氮,某些样品硝态氮的含量占全氮的10%以上,所以杜马斯法测定结果往往高于凯氏法的结果。可见杜马斯定氮法所得到的全氮结果更接近真值。而且,杜马斯法不需要消煮,大大缩短了工作时间,减少了实验的危险性,对环境没有任何污染。作者认为可以用杜马斯燃烧法进行植物样品中全氮的测定。