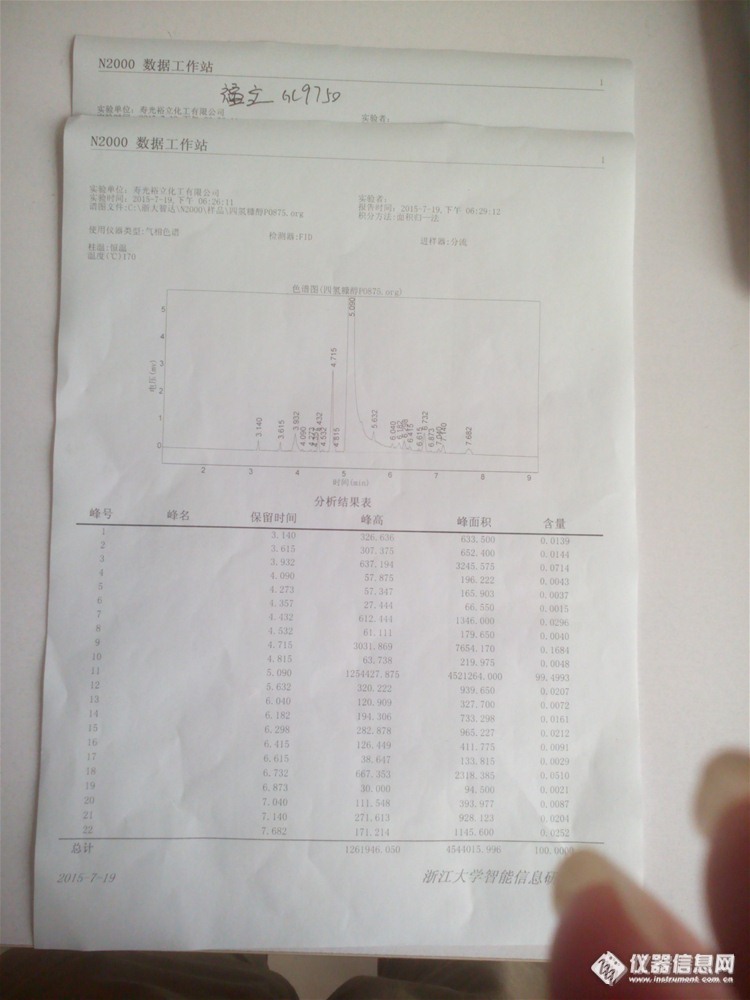
fid测%99.5四氢糠醇,分流,灵敏度,总流量怎么调,可以使糠醇不平顶,杂质也能测出来?求大神指导!??http://ng1.17img.cn/bbsfiles/images/2015/07/201507202058_556314_2864181_3.jpg
2009年10月6日,美国国际贸易委员会发布公告,决定于原产于中国的四氢糠醇实施的反倾销措施进行日落复审,以决定若取消反倾销措施,涉案产品在合理的、可预见的期限内是否会对美国国内产业造成实质性损害。 2003年7月18日,美国商务部对原产于中国的四氢糠醇进行反倾销调查,涉案产品海关编码为29321300。2004年6月18日,美国商务部对该案作出肯定性终裁,裁定中国涉案企业的倾销幅度为136.86%。2009年7月1日,美国商务部对该案进行反倾销日落复审立案调查。老美太霸道,对他们这种行径,表示强烈谴责.
如题,分析抗生素药中乙醇和四氢呋喃残留,大家都是怎么做的,交流一下,供学习,也请这里的专家指点一下柱子型号:规格:分析条件:温度——升温速率——温度保持时间等样品量:检测器是否用顶空顶空条件所用机器型号所用机器品牌及价格
本公司最近进了一批四氢呋喃废料,打算回收四氢呋喃,但是里面有醇类,具体不清楚是甲醇还是乙醇,上了精馏塔也只处理到含量93左右,水分比较高,而我们所需要得是无水得四氢呋喃,总感觉用片碱处理水分无法达到要求,0.05%以下,现在想请教有没有办法去除。
色谱柱再生的时候,需要用到四氢呋喃,异丙醇之类的,请教PEEK管能用吗?
甲醇,丙酮,仲丁醇,四氢呋喃用什么[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]柱子做比较好。用过HP-5 仲丁醇和四氢呋喃分离不好
GPC的废液---四氢呋喃-甲醇等--有回收的?我们单位好多这样的废液,不知道有没有单位要回收这些。有事联系.
含四氢呋喃或甲醇的流动相变浑浊是什么原因?
四氢呋喃纯化时蒸馏要氮气保护吗?我最近在做四氢呋喃的纯化,是用二苯甲酮、钠回流的,之前做好先用氢氧化钾干燥。等体系变墨绿色的时候就可以蒸馏出来了。我用干燥塔隔绝湿气,这时候要用氮气保护码 四氢呋喃有被氧化的机会。请给位高手指教!!!
请教各位,色谱级四氢呋喃里面是没有加入抗氧化剂的,那么一瓶四氢呋喃打开以后最多可以放置多久呀?还是打开以后要往里面充氮气?
用HPLC分析D异抗坏血酸及其钠盐,多元醇,乙二醇,丙二醇,甘油,丁四醇等,用什么色谱柱和检测器???
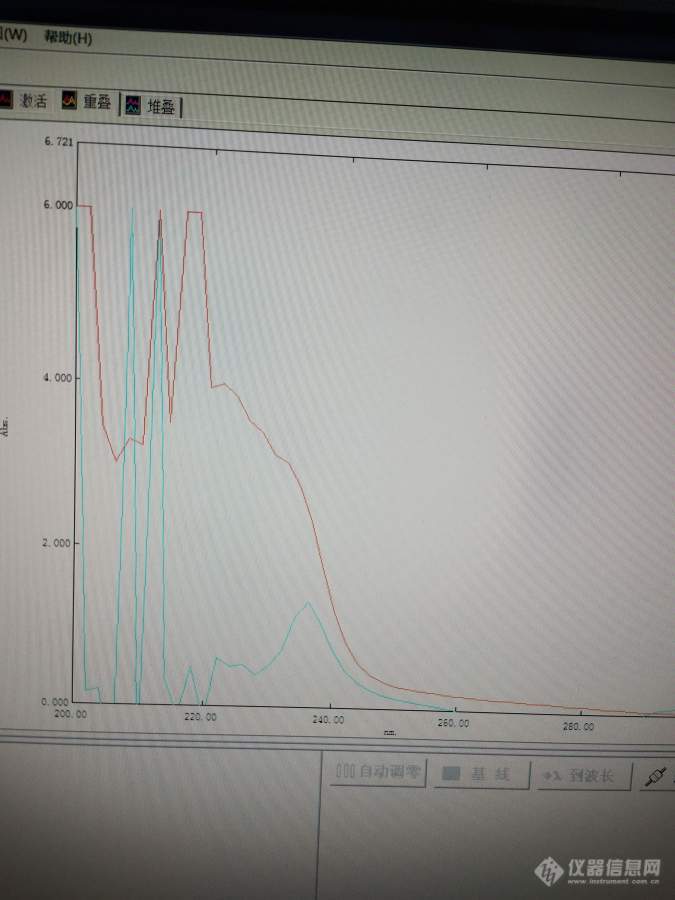
[color=#444444]请教一下,测紫外可见光谱的时候,为什么分析物在乙醇中出的峰和在四氢呋喃中出的峰不一样,在乙醇中只有一个包,而在四氢呋喃中会出现一个完整的峰,红色代表在乙醇中,蓝色代表在THF中,谢谢[/color][color=#444444][img=,675,900]https://ng1.17img.cn/bbsfiles/images/2019/08/201908021511251896_2446_1752342_3.jpg!w675x900.jpg[/img][/color]
如题!求助各位大侠了,我们公司GPC是WATERS的,由于新买的没用过,之前安装仪器的时候,对方工程师简单培训了一下,之后由于我们要做的是107胶的分子量测试,用甲苯溶解性会好一点,但是我们买的是四氢呋喃的柱子,我问过对方工程师可不可以用甲苯做流动相,对方说可以,但是要先用异丙醇冲洗,再换成甲苯,这几个星期我就用异丙醇冲洗柱子,发现压力突然增大(到3000多psi,1ml/min),当时我没在意,只以为是泵里面有空气,这样冲了2瓶异丙醇,并放置了3个多星期,后面发现压力还是这么大,就打电话到waters问,他们说不能用异丙醇做流动相,叫我赶紧换回去,我换回去以后压力变回700多psi。现在不敢测标样。问问各位达人:1、这柱子是不是已经不能用了?(我的是3根四氢呋喃柱)2、四氢呋喃柱能不能用甲苯做流动相?能的话怎么换?3、柱子大约多少钱?补充一下:柱子是WAT044225和WAT054460
FID使用时相关问题,我是在乙醇里加入等体积四氢呋喃、甲苯、氟苯浓度大概在百分之一,出峰顺序是四氢呋喃、乙醇、氟苯、甲苯,提高柱温以后,乙醇的含量减少了是怎么回事?相同样品,同样的注射量,恒温程序走的,当提升温度把柱温由60变到80,乙醇的积分面积百分数从90%下降到80%是因为什么,请各位大神解惑
各位大虾: 有谁有用GC测四氢呋喃纯度的方法的没?请不惜赐教!谢谢噢!
问题: 求助一下:阳离子交换柱能用使用四氢呋喃,异丙醇一类的溶剂吗?
求购1、草酸2、枸橼酸3.磷酸二氢钾4.四丁基硫酸氢铵5.磺基水杨酸为分析纯试剂6.甲醇(色谱纯)7.乙腈(色谱纯)8.异丙醇(色谱纯)9.异丙醇分析醇等若干,具体规格及数量见附件
请问GPC用甲醇做溶剂可以用四氢呋喃的柱子做吗?谢谢!
GB/T 14022.1—2009《工业糠醇》[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=180346]GBT 14022.1-2009工业糠醇.pdf[/url]
我们用甲醇(68%),磷酸二氢钠溶液(4%),四氢呋喃-异丙醇(117:155,28%),做精密度第三针的时候发现基线不行了,开始用水与甲醇冲柱子,发现基线出现很规则的波浪状的峰(一个大峰后连2-3个小峰,很规则),一直冲不平。这是怎么回事,是不是进气泡了或柱子不行了.用甲醇能冲平基线,但测定的时候样品为平头峰,且中间有分叉。我用的是戴安的机器
求助:中间体3-四氢呋喃甲醇液相分析方法,调不出来,大家谁能告知??气相很简单,但是想用液相定量。。
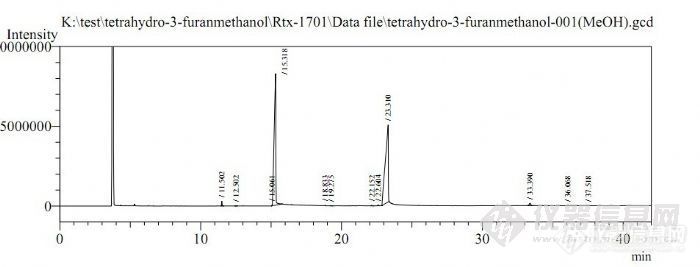
大家好,我在检测3-羟甲基四氢呋喃纯度的时候,因为对这个东西一点也不了解,也没有查到相应的资料,就先用了RTX-1701柱子检测,进样口:250,检测器(FID):300,分流比:20:1,线速度进样:1.0mL/min,升温程序:50(2)-10-250(20)),用甲醇稀释了一下,发现走得不怎么好,具体谱图如下,大家帮我看看,应该怎么做?知道的TX请不吝赐教,给我一个详细的分析方法,最好帮我也附张图谱!谢谢!比较着急!!!http://ng1.17img.cn/bbsfiles/images/2011/07/201107030846_302772_1973612_3.jpg
看到论坛上关于乙腈和甲醇的洗脱能力的疑问,特此发表下甲醇/水 乙腈/水 四氢呋喃/水10 相当于 6 相当于 420 12 1030 22 1740 32 2350 40 3060 50 3770 60 4580 73 5390 86 63100 100 72溶剂混溶性表溶 剂 极性指数 折光度20℃ 紫外截止波长 沸 点(℃) 黏 度(cPoise) 水中溶解度(%W/W) 乙酸 6.2 1.372 230 118 1.26 100 丙酮 5.1 1.359 330 56 0.32 100 乙腈 5.8 1.344 190 82 0.37 100 苯 2.7 1.501 280 80 0.65 0.18 正丁醇 4.0 1.394 254 125 0.73 0.43 四氯化碳 1.6 1.399 263 77 0.97 0.08 氯仿 4.1 1.466 245 61 0.57 0.815 [color=black
[font=宋体]抗体是一类免疫蛋白,可识别并结合特定抗原,在生物研究以及临床应用中,纯化得到高质量的抗体十分重要。[/font][font=宋体] [/font][font=宋体][b]? 凝胶过滤层析法[/b][/font][font=宋体]凝胶过滤层析法的原理是基于抗体分子的不同大小,利用不同孔径的凝胶过滤介质将目标分子(抗体)与较大分子(如蛋白质等杂质)分离开来。[/font][font=宋体] [/font][font=宋体]具体操作步骤如下:[/font][font=宋体][font=Calibri]1. [/font][font=宋体]将含有目标抗体的混合物加入到预先平衡好的凝胶柱中。[/font][/font][font=宋体][font=Calibri]2. [/font][font=宋体]使用缓冲液进行洗脱,较大分子无法通过凝胶柱而流出。[/font][/font][font=宋体][font=Calibri]3. [/font][font=宋体]目标抗体分子大小适中,可通过凝胶柱并被保留下来。[/font][/font][font=宋体][font=Calibri]4. [/font][font=宋体]最后使用洗脱缓冲液将目标抗体从凝胶柱中洗脱出来,得到纯化的抗体。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]? 亲和层析法[/b][/font][font=宋体]亲和层析法的原理是利用抗体分子与抗原之间的特异性结合来实现目标抗体的纯化。[/font][font=宋体] [/font][font=宋体]具体操作步骤如下:[/font][font=宋体][font=Calibri]1. [/font][font=宋体]将含有目标抗体的混合物加入到预先包含特异性结合配体[/font][font=Calibri]([/font][font=宋体]如蛋白[/font][font=Calibri]A[/font][font=宋体]、蛋白[/font][font=Calibri]G[/font][font=宋体]等[/font][font=Calibri])[/font][font=宋体]的亲和层析柱中。[/font][/font][font=宋体][font=Calibri]2. [/font][font=宋体]目标抗体与配体之间发生特异性结合。[/font][/font][font=宋体][font=Calibri]3. [/font][font=宋体]使用洗脱缓冲液将非特异结合的组分洗脱掉。[/font][/font][font=宋体][font=Calibri]4. [/font][font=宋体]最后使用洗脱缓冲液将目标抗体从亲和层析柱中洗脱出来,得到纯化的抗体。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]? 离子交换层析法[/b][/font][font=宋体]离子交换层析法的原理是利用目标抗体分子与离子交换柱中固定的离子之间的相互作用来实现纯化。[/font][font=宋体] [/font][font=宋体]具体操作步骤如下:[/font][font=宋体][font=Calibri]1. [/font][font=宋体]将含有目标抗体的混合物加入到预先平衡好的离子交换柱中。[/font][/font][font=宋体][font=Calibri]2. [/font][font=宋体]使用缓冲液进行洗脱,使与固定离子相同电荷的分子无法通过离子交换柱而流出。[/font][/font][font=宋体][font=Calibri]3. [/font][font=宋体]目标抗体由于表面电荷不同,能够通过离子交换柱被保留下来。[/font][/font][font=宋体][font=Calibri]4. [/font][font=宋体]最后使用洗脱缓冲液改变[/font][font=Calibri]pH[/font][font=宋体]或盐浓度等条件,将目标抗体从离子交换柱中洗脱出来,得到纯化的抗体。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]? 逆向相色谱法[/b][/font][font=宋体]逆向相色谱法的原理是利用目标抗体分子与逆向相色谱柱中固定的疏水基团之间的相互作用来实现纯化。[/font][font=宋体] [/font][font=宋体]具体操作步骤如下:[/font][font=宋体][font=Calibri]1. [/font][font=宋体]将含有目标抗体的混合物加入到预先平衡好的逆向相色谱柱中。[/font][/font][font=宋体][font=Calibri]2. [/font][font=宋体]使用缓冲液进行洗脱,使疏水性较低的分子无法通过逆向相色谱柱而流出。[/font][/font][font=宋体][font=Calibri]3. [/font][font=宋体]目标抗体由于表面疏水性不同,能够通过逆向相色谱柱被保留下来。[/font][/font][font=宋体][font=Calibri]4. [/font][font=宋体]最后使用洗脱缓冲液改变溶剂极性等条件,将目标抗体从逆向相色谱柱中洗脱出来,得到纯化的抗体。[/font][/font][font=宋体] [/font][font=宋体][b]抗体纯化方法的优缺点[/b][/font][font=宋体]凝胶过滤层析法:优点:[/font][font=宋体]简单易行,不需要特殊设备,适用于各种规模的实验室 缺点:[/font][font=宋体]分离效率低,只能实现较为粗略的纯化[/font][font=宋体]亲和层析法 优点:[/font][font=宋体]纯度高,效率高 缺点:[/font][font=宋体]需要特定的亲和试剂和配体,成本较高[/font][font=宋体]离子交换层析法 优点:[/font][font=宋体]选择性高,适用性强 缺点:[/font][font=宋体]需要根据不同抗体进行条件优化,操作较复杂[/font][font=宋体]逆向相色谱法 优点:[/font][font=宋体]选择性高,灵活性强 缺点:[/font][font=宋体]需要特定设备支持,操作条件较为复杂[/font][font=宋体] [/font][font=宋体]抗体纯化是一项关键技术,在抗体制备过程中十分重要。每种方法都有其特点和适用性,义翘神州可根据您的具体需求选择合适的抗体纯化方法,保证交付高质量、高纯度的纯化抗体。[/font][font=宋体] [/font][font=宋体][font=宋体]更多详情可以参看:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/antibody-purification[/font][/font]
[font=宋体][font=宋体]抗体纯化的原理是依据抗体的生物学特征,如抗体分子的电荷、大小、疏水性等,选用合适的方法将目标抗体分子从初始混合物中分离纯化出来。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗体纯化方法包括[/font][/font][b][font=宋体][font=宋体]亲和层析法、离子交换层析法、凝胶过滤层析法和疏水作用层析法[/font][/font][/b][font=宋体][font=宋体]等。选用何种纯化方法取决于抗体的来源、时间、成本以及抗体的最终用途等。[/font][/font][font=宋体] [/font][b][font=宋体][font=宋体]抗体纯化的方法及步骤[/font][/font][/b][font=宋体] [/font][font=宋体][font=宋体]抗体是一类免疫蛋白,可识别并结合特定抗原,在生物研究以及临床应用中,纯化得到高质量的抗体十分重要。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]一、凝胶过滤层析法[/font][/font][font=宋体][font=宋体]凝胶过滤层析法的原理是基于抗体分子的不同大小,利用不同孔径的凝胶过滤介质将目标分子(抗体)与较大分子(如蛋白质等杂质)分离开来。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]具体操作步骤如下:[/font][/font][font=宋体][font=Calibri]1. [/font][font=宋体]将含有目标抗体的混合物加入到预先平衡好的凝胶柱中。[/font][/font][font=宋体][font=Calibri]2. [/font][font=宋体]使用缓冲液进行洗脱,较大分子无法通过凝胶柱而流出。[/font][/font][font=宋体][font=Calibri]3. [/font][font=宋体]目标抗体分子大小适中,可通过凝胶柱并被保留下来。[/font][/font][font=宋体][font=Calibri]4. [/font][font=宋体]最后使用洗脱缓冲液将目标抗体从凝胶柱中洗脱出来,得到纯化的抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]二、[url=https://cn.sinobiological.com/resource/protein-review/protein-purification-by-ac][b]亲和层析法[/b][/url][/font][/font][font=宋体][font=宋体]亲和层析法的原理是利用抗体分子与抗原之间的特异性结合来实现目标抗体的纯化。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]具体操作步骤如下:[/font][/font][font=宋体][font=Calibri]1. [/font][font=宋体]将含有目标抗体的混合物加入到预先包含特异性结合配体[/font][font=Calibri]([/font][font=宋体]如蛋白[/font][font=Calibri]A[/font][font=宋体]、蛋白[/font][font=Calibri]G[/font][font=宋体]等[/font][font=Calibri])[/font][font=宋体]的亲和层析柱中。[/font][/font][font=宋体][font=Calibri]2. [/font][font=宋体]目标抗体与配体之间发生特异性结合。[/font][/font][font=宋体][font=Calibri]3. [/font][font=宋体]使用洗脱缓冲液将非特异结合的组分洗脱掉。[/font][/font][font=宋体][font=Calibri]4. [/font][font=宋体]最后使用洗脱缓冲液将目标抗体从亲和层析柱中洗脱出来,得到纯化的抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]三、离子交换层析法[/font][/font][font=宋体][font=宋体]离子交换层析法的原理是利用目标抗体分子与离子交换柱中固定的离子之间的相互作用来实现纯化。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]具体操作步骤如下:[/font][/font][font=宋体][font=Calibri]1. [/font][font=宋体]将含有目标抗体的混合物加入到预先平衡好的离子交换柱中。[/font][/font][font=宋体][font=Calibri]2. [/font][font=宋体]使用缓冲液进行洗脱,使与固定离子相同电荷的分子无法通过离子交换柱而流出。[/font][/font][font=宋体][font=Calibri]3. [/font][font=宋体]目标抗体由于表面电荷不同,能够通过离子交换柱被保留下来。[/font][/font][font=宋体][font=Calibri]4. [/font][font=宋体]最后使用洗脱缓冲液改变[/font][font=Calibri]pH[/font][font=宋体]或盐浓度等条件,将目标抗体从离子交换柱中洗脱出来,得到纯化的抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]四、逆向相色谱法[/font][/font][font=宋体][font=宋体]逆向相色谱法的原理是利用目标抗体分子与逆向相色谱柱中固定的疏水基团之间的相互作用来实现纯化。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]具体操作步骤如下:[/font][/font][font=宋体][font=Calibri]1. [/font][font=宋体]将含有目标抗体的混合物加入到预先平衡好的逆向相色谱柱中。[/font][/font][font=宋体][font=Calibri]2. [/font][font=宋体]使用缓冲液进行洗脱,使疏水性较低的分子无法通过逆向相色谱柱而流出。[/font][/font][font=宋体][font=Calibri]3. [/font][font=宋体]目标抗体由于表面疏水性不同,能够通过逆向相色谱柱被保留下来。[/font][/font][font=宋体][font=Calibri]4. [/font][font=宋体]最后使用洗脱缓冲液改变溶剂极性等条件,将目标抗体从逆向相色谱柱中洗脱出来,得到纯化的抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]抗体纯化是一项关键技术,在[url=https://cn.sinobiological.com/resource/antibody-technical/antibody-production][b]抗体制备[/b][/url]过程中十分重要。每种方法都有其特点和适用性,义翘神州可根据您的具体需求选择合适的抗体纯化方法,保证交付高质量、高纯度的纯化抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]更多[url=https://cn.sinobiological.com/resource/antibody-technical/antibody-purification][b]抗体纯化[/b][/url]详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/antibody-purification[/font][/font][font=宋体] [/font]
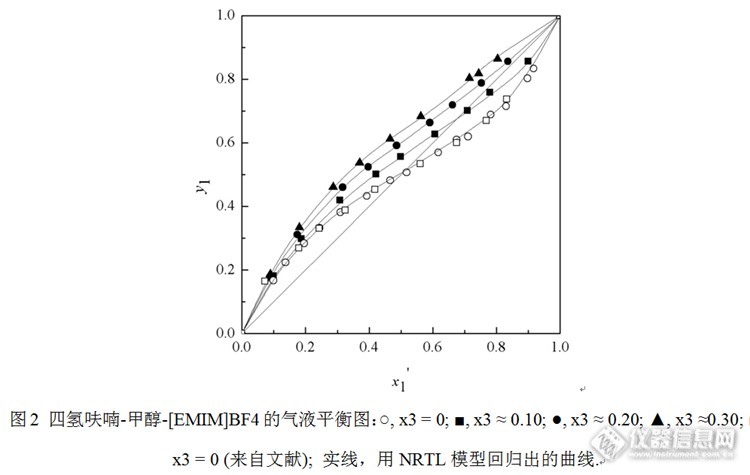
前言 本阶段进行了1-乙基-3-甲基咪唑四氟硼酸盐(4])、1-丁基-3-甲基咪唑四氟硼酸盐(4])、1-丁基-3-甲基咪唑六氟磷酸盐([PF[sub]6])、1-辛基-3-甲基咪唑六氟磷酸盐([PF[sub]6])对四氢呋喃-甲醇二元体系的气液平衡的影响,并对实验结果运用了NRTL模型进行了关联,关联结果良好。最后将关联的结果导入aspen plus模拟软件模拟了整个萃取精馏过程,为今后的工业应用提供基础的理论数据。1.1 气液平衡试验的流程1.1.1 试验设备及试剂试验所采用的主要试验仪器如下:[align=center]表1-1主要实验仪器[/align] [table=606][tr][td] [align=center]编号[/align] [/td][td] [align=center]仪器名称[/align] [/td][td] [align=center]生产厂家[/align] [/td][td] [align=center]量程及精度[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]Bs120s型 电子天平[/align] [/td][td] [align=center]德国sartorius公司[/align] [/td][td] [align=center]0.0001g[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]CE-2型汽液平衡数据测定仪[/align] [/td][td] [align=center]天津大学北洋化工实验设备有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]旋转蒸发仪[/align] [/td][td] [align=center]上海申顺生物科技有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]Sp6890型气相色谱仪[/align] [/td][td] [align=center]北京精科瑞达有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]N2000型 色谱工作站[/align] [/td][td] [align=center]浙江大学智达信息工程有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]真空干燥箱DZF-6020型[/align] [/td][td] [align=center]上海一恒科技有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][/table]另外还有烧杯、容量瓶、移液管、磁力搅拌器、微样进样针(1μL)等。试验中所采用的主要试验试剂如下:甲醇,四氢呋喃:北京化工厂,分析纯,质量分数≥99.8 %;本文共用到五种不同的离子液体,分别为:1-乙基-3-甲基咪唑四氟硼酸盐(BF[sub]4);1-丁基-3-甲基咪唑四氟硼酸盐(BF[sub]4);1-丁基-3-甲基咪唑六氟磷酸盐([PF[sub]6]);1-辛基-3-甲基咪唑六氟磷酸盐([PF[sub]6])。离子液体从上海成捷化学有限公司购买,产品的质量分数≥98%。1.1.2 试验流程 本文测定了四氢呋喃-甲醇共沸物系分别加入不同浓度的离子液体(BF[sub]4、BF[sub]4、[PF[sub]6]、[PF[sub]6])后的汽液相平衡数据。每个摩尔分数下的离子液体做10个浓度点,每个点取样5次,每个样品在色谱仪中出峰时间约为6分钟,然后根据色谱分析对应浓度,对五次平行试验结果进行平均得出最终浓度。整个操作的实验流程如图1.实验测定步骤如下:(1) 依据实验所要求的摩尔比将各个组分所需要的体积量和质量计算列表,然后以体积量为估计值,利用移液管在容量瓶中加入比体积量稍少体积的试剂,最后用分析天平通过滴管准确滴至所需质量。同样的方法加入其它组分。在全部组分加入完成后,摇匀,密封,静止以观察是否分层。容量瓶如装有含离子液体的溶液,需要用溶剂清洗回收离子液体。容量瓶用洗涤剂清洗,最后用去离子水润洗。配液过程用所用的烧杯,滴定管,移液管等如果用过不同的液体需要清洗烘干。(2) 用甘油作为导热剂,在测温套管中加入适量甘油,标准温度计插入套管中;(3) 对系统的气密性进行检查,保证试验装置的气密性不会有样品损失而影响平衡数据的测定,再加样进行实验;(4) 沸腾室内加入配制好的四氢呋喃-甲醇-离子液体混合溶液约70ml,打开冷却水,打开电源进行加热。采用逐步升温加热,开始时调节小电流(0.1A)控制加热温度,等到整个仪器预热完毕调大电流到0.2A稳定十分钟,继续调到0.3A左右持续稳定加热,以沸腾室内液体能沸腾为准适当调节电流。冷凝回流液控制在每秒1-3滴,待温度计度数不变,稳定回流30分钟左右以建立平衡状态;(5) 达到平衡后,读取温度计的温度并记录;(6) 应用1μL微量进样器直接从汽相取样口取出0.4μL试样,取液前应先进行5次以上的洗针操作,以保证针管内润湿同时减少误差。取液时应注意每次取液时尽量取同样的位置,取样量保持一致。每次取样后应尽快打入色谱仪中,打针时遵循快进快出原则,以免液体被气化。待将样品打入仪器中,尽快点采集数据进行分析。待所有的峰积分完成以后,稳定一分钟进行数据的记录和保存。重复上述过程,每个样品汽液相各测3-5个点取平均。同样的再次使用微量进样器从液相取样口取出0.4μL试样,也是进行色谱分析浓度,同样操作,记录数据;(7) 重复以上第六步的操作,进行下一数据点的测定,对每个点的汽液相至少分别测试五次,取相近的较为稳定的四针样品浓度进行平均,得出最后浓度;(8) 当样品的数据测试完成后,将电流调至零点,关闭加热电源,静置平衡釜至温度较低时,拆卸装置。平衡釜中的液体从液相口倒出,用低沸点的溶剂将平衡釜清洗1至2次。如果平衡釜内为二元样品,可直接将样品及洗液倒入废液瓶,若果为加入离子液体的三元样品,需将样品和洗液收集起来以回收里面的离子液体。清洗完平衡釜后,用电吹风开加热档吹10分钟以上,将平衡釜里面残留的溶剂吹干为止。(9) 将含有离子液体的废液加入蒸发瓶,安置到旋转蒸发仪上,固定。加热器应逐级升温,以防蒸发液暴沸,减压旋转蒸发维持3个小时以上,保证离子液体纯度。(10)每天实验结束后,首先关闭色谱加热,冷却色谱降温,待色谱中热导温度降至80度以下时,关闭仪器,关闭色谱工作站,最后关闭氢气。如检测含离子液体的三元组分物系,需注意色谱工作站的谱线是否出现峰值和面积减小,某些峰的检测能力下降等的异常,这是由于离子液体积存在仪器中衬管的棉花上,导致样品通过量减少。这时,需按照上述步骤完全关闭仪器,更换衬管的石棉并且对衬管进行清洗。注意在安装衬管时,衬管安装松紧要合适,过紧会顶碎衬管,过松会导致设备漏气。安装完成后,检查压力表示数与安装前是否一致,以确定是否漏气。[img=,512,436]http://ng1.17img.cn/bbsfiles/images/2015/09/201509281522_568298_2984502_3.jpg[/img]1.2 二元体系的气液相平衡 为了验证整个实验过程的可靠性,我们首先对四氢呋喃-甲醇体系的二元气液平衡数据进行了测定,测定的结果如下,实验结果与文献吻合度较高,说明我们的实验仪器可以用于含离子液体的三元体系的测定。[img=,547,623]http://ng1.17img.cn/bbsfiles/images/2015/09/201509281523_568299_2984502_3.jpg[/img] 由图三可以看出,在四氢呋喃-甲醇二元体系当中,101.3kPa下共沸点存在于四氢呋喃的含量为x1=0.512时,平衡温度为T=332.4K。实验结果表明此二元体系存在共沸现象,要分离需要采用特殊精馏的方法。而本文的目的就是为分离这个体系选取绿色有效的萃取剂。1.3带有四氟硼酸根的离子液体对四氢呋喃甲醇体系的气液平衡的影
GB/T 14022.2—2009《工业糠醇试验方法》[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=180347]GBT 14022.2-2009工业糠醇试验方法.pdf[/url]
有谁知道用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]检测四氢呋喃纯度的方法?急用!先说声谢谢了。[em0815] 中国心
有机溶剂(乙醇,四氢呋喃等溶剂)适合用什么极性柱子还是非极性柱子????为什么???

万古霉素是由链霉菌产生的、结构复杂的糖肽类抗生素,易溶于水,甲醇中极微溶解,乙醇或丙酮中几乎不溶.万古霉素主要抑制细菌细胞壁合成,由于万古霉素有较强的抗菌作用,在人医临床上也较少使用,而且同氨基糖苷类药物一样,具有严重耳毒性及肾毒性,故只宜在其他抗生素对病菌无效时才会被短期使用于抢救,也就是所谓的最后一线药物. 近年来,一些养殖者和饲料生产企业在动物饲喂过程或加工生产中,为追求利润,将万古霉素添加到饲料中应用,长期使用的后果是使需要万古霉素来治疗的一种能够致死的细菌产生抗药性,变异成万古霉素抗药性肠球菌(VRE),对人类生命安全造成了极大的威胁.因此,建立饲料中万古霉素的测定方法是非常必要的.1、适用范围适用于饲料中万古霉素的检测。2、提取称取1 g 均质样品于15 mL 离心管中,加入8 mL 乙酸提取液* 和4 mL 三氯甲烷;振荡4 min, 4,000 rpm下离心4 min,收集上清液;下层残留物用5 mL、5 mL 乙酸提取液重复提取两次,合并三次提取液;作为上样液,待净化。* 乙酸提取液:10% 乙酸溶液(用50% 甲醇水溶解)3、净化ProElut PXC 500 mg/12 mL (Cat.#68207)a 活化: 依次加入6 mL 甲醇,6 mL 水,流出液弃去;b 上样: 将上样液加入柱中,流出液弃去;c 淋洗: 依次用10 mL 水,3 mL 甲醇淋洗,流出液弃去;d 洗脱: 10 mL 10% 氨水(甲醇/ 水= 3/7)溶液洗脱,收集洗脱液;e 重新溶解:50 oC 下用减压蒸馏将洗脱液浓缩近干,然后用1% 乙酸重新定容至1 mL,上机供HPLC 分析。4、色谱条件色谱柱:Spursil C18 250 x 4.6 mm ID, 5 μm (Cat. #82001)流动相:50 mmol/L 磷酸二氢钾(1 L 磷酸二氢钾溶液需加入300 μL 磷酸)/ 乙腈= 92/8流速:1.0 mL/min 进样量:20 μL 柱温:30 oC 检测器: UV 210 nm5、添加回收结果5.1 添加水平为1.0 mg/kg 饲料中万古霉素检测的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041358_559009_2452211_3.pnghttp://ng1.17img.cn/bbsfiles/images/2015/08/201508041358_559010_2452211_3.png回收率:71.6%(注:被仪器的logo遮住了)5.2 添加水平为10.0 mg/kg 饲料中万古霉素检测的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041421_559012_2452211_3.png回收率:69.4%(注:被仪器的logo遮住了)5.3 饲料中万古霉素检测(空白样品)的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041422_559013_2452211_3.png5.4 万古霉素标准品10.0 mg/L 的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041423_559014_2452211_3.png5.5 万古霉素标准品1.0 mg/L 的液相色谱图http://ng1.17img.cn/bbsfiles/images/2015/08/201508041424_559015_2452211_3.png