孔雀石绿萃取中加入二甘醇有什么作用?
大家知道乙二醇单丁醚是哪个法规指令管控吗?
在检测水产品中孔雀石绿残留量的标准方法中,很多都要用到二甘醇、盐酸羟胺及对-甲苯磺酸,但不知它们的作用是什么,不知哪位知道,大家都来谈一谈啊
聚乙二醇[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]残留做二甘醇和乙二醇:药典用注射进样,由于,聚乙二醇杂峰很多,做不出来,我想改用顶空进样,可二甘醇和乙二醇的沸点很高,不知道可不可行?谢谢
大家好,有个任务要检测模拟提取磷酸盐溶液里的乙二醇和二甘醇残留量。 有两点请教大家: 1. 像这种水溶液只能用顶空进样吗? [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]柱能不能进水溶液 2. 用顶空的话,乙二醇沸点197,二甘醇沸点245,可以进行顶空
聚乙二醇在新型药剂的应用和质量控制摘要:聚乙二醇是常用的药用辅料,有不同的分子量规格。聚乙二醇在新型药剂中有广泛应用,其修饰的药物和纳米粒制剂可以有效提高药物利用度,减少副作用,提高病灶组织药物浓度。本文简单介绍了聚乙二醇化的新型药剂实例,比较了主要药典对聚乙二醇的质量控制方案,结合新的分析方法,介绍了聚乙二醇及其衍生物质量控制的快速简便方案。1聚乙二醇http://ng1.17img.cn/bbsfiles/images/2014/12/201412170937_527449_2265735_3.jpg图1 聚乙二醇结构和化学通式。 聚乙二醇(polyethylene,PEG)由环氧乙烷和水缩聚而成 (图1),n代表基本单元氧乙烯基的平均数目。低分子量的聚乙二醇为粘稠的液体,当平均分子量超过1000,聚乙二醇为白色的蜡状固体。在中国药典收录作为辅料的常用聚乙二醇辅料有分子量400、600、1000、1500、4000、6000共6种规格。聚乙二醇是传统的药用辅料,一般作为赋形剂使用,或者作为药物的分散剂。随着药物输送系统的发展,目前聚乙二醇在制药技术的应用主要有两个方面:药物的聚乙二醇修饰和修饰纳米粒的骨架结构1]。2聚乙二醇在新型药剂中的应用 聚乙二醇两端的羟基可以方便的被修饰(图1B R[sub]1[/sub]和R[sub]2[/sub]),如羟基甲基化形成聚乙二醇单甲醚,也可以用来直接和药物基团反应,形成药物和聚乙二醇复合物。大量实验和研究表明药物和聚乙二醇复合物是一种有效的药物输送手段,它可以有效延长药物的半衰期,增加药物溶解性,提高药物的安全性[[url=file:///M:/PEG-1.doc#_ENREF_2]2]。http://ng1.17img.cn/bbsfiles/images/2014/12/201412170940_527450_2265735_3.jpg 传统的抗肿瘤小分子是聚乙二醇修饰的主要目标。聚乙二醇修饰的柔红霉素(daunorubicin)改善药物的溶解性和水溶液稳定性,增加了药物在血液中的循环时间。在临床Ⅲ期治疗Kaposi[sup],[/sup]s肉瘤的研究中,对比阿霉素的治疗效果,聚乙二醇修饰的柔红霉素显著降低了毒性,减缓了中性中性粒细胞减少症[[url=file:///M:/PEG-1.doc#_ENREF_3]3]。与聚乙二醇修饰小分子药物相比,聚乙二醇修饰的蛋白质药物获得的进展更为引人关注。第一个上市的聚乙二醇修饰的蛋白质药物是腺苷脱氨酶,Enzon公司在1991年推出。聚乙二醇修饰蛋白质药物最成功的例子是[color=#323E32]安进([font='simsun','serif'][color=#323E32]Amgen[color=#323E32])推出的[font='simsun','serif'][color=#323E32]Neulasta[color=#323E32](培非格司亭)(聚乙二醇修饰的重组人粒细胞集落刺激因子(G-CSF)),[font='simsun','serif'][color=#323E32]Neulasta[color=#323E32]的销售额在推出的第一年就超过了原研药[color=#323E32]非格司亭。[font='simsun','serif'][color=#323E32]Neulasta[color=#323E32](培非格司亭)主要治疗多种癌症化疗导致的嗜中性白血球减少症,降低化疗病人的感染风险。从[color=#323E3
做二氯乙醇有没有注意要求,还有[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]加顶空方法。多谢
一直糊里糊涂的做,多方查证后得知,与大家分享:盐酸羟胺:作为还原剂,有助于防止待测物的降解;对甲苯磺酸:作为离子对试剂,有利于孔雀石绿形成离子对,增加乙腈对该物 质的提取效率;氧化铝:吸附样品中的油脂;二甘醇:消除乳化。
做生物样品的孔雀石绿的分析时,有加入加入二甘醇,在一次研讨会上有人提问加入二甘醇的作用?记忆中有个工程师说是仿暴沸!看了些书,我觉的可能是增加提取液的极性吧?大家有兴趣的来讨论下啊

本人在一家化工企业实习,最近在做一个课题,可是遇到很多问题,请各位师傅高手指点一下!以下是我的气相分析条件:柱子50米的hp-5 柱温180℃ 进样口280℃ 检测器300℃ 进样量0.4μL在2.980分出峰的是乙二醇,可是二乙二醇检测不出。当使用60米的柱子时,两种醇都可以检测出来,但是二乙二醇和碳酸乙烯酯的出峰时间非常相近,很难分离开,因此要做定量的话根本不准确。http://ng1.17img.cn/bbsfiles/images/2013/05/201305141847_440001_2729912_3.jpghttp://ng1.17img.cn/bbsfiles/images/2013/05/201305141853_440002_2729912_3.jpg这张色谱图是我使用升温程序做的峰,发现碳酸乙烯酯的峰成锯齿状。为什么会这样呢,是哪方面的问题呢?请大家指导一下,本人的QQ:806968887 非常感谢!
乙二醇、二甘醇和三甘醇取本品4g,精密称定。置 100ml量瓶中,取1,3-丁二醇0.004g,精密称定,置同一量瓶中,加丙酮使溶解,相同溶剂稀释至刻度,作为供试品溶液。取乙二醇0.0025g, 二甘醇0.004g,三甘醇0.004g,精密称定,置同一100ml量瓶中,取1,3-丁二醇0.004g,置 该量瓶中,加丙酮使溶解,相同溶剂稀释至刻度,作为对照品溶液。照[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法(通则0521)试验。以50%苯基-50% 甲基聚硅氧烷为固定液(液膜厚度1.0μm)的毛细管柱,起始 温度为40℃,以每分钟10℃的速率升温至60℃,维持5分钟,再以每分钟10℃的速率升温至170℃,维持0分钟,再以每分钟15℃的速率升温至280℃。维持60分钟(可根据具体情况调整)。检测器为氢火焰离子化检测器。检测器温度 290℃,进样口温度为270℃。取对照品溶液作为系统适用性 试验溶液,载气为氦气,流速5.0ml/min,分流比2:1,进 样体积1.0μl。乙二醇,二甘醇和三甘醇与内标1,3-丁二醇的分离度均不得小于2.0,各峰间的拖尾因子应符合规定,[color=#ff0000]乙二醇,二甘醇和三甘醇峰面积相对于内标1,3-丁二醇的峰面积相对标准偏差不得过5.0%[/color]。以1,3-丁二醇峰面积计算乙二醇,二甘醇和三甘醇的峰面积,以下式计算:[color=#ff0000]结果=(Ru / Rs) X (Cs X Cu)X F X100 [/color] 式中Ru为供试品溶液中各待测物质与内标的峰面积比率;Rs为对照品溶液中各对照物质(乙二醇,二甘醇和三 甘醇)与内标的峰面积比率; Cs为对照品溶液中各对照物质(乙二醇,二甘醇和三 甘醇)的浓度,ug/ml;Cu为供试品溶液中待测物质的浓度,mg/ml F为转换因子,103mg/g。(10的三次方 )依法检测,乙二醇,二甘醇和三甘醇均不得过0.01%。以上标红文字不能理解其含义,望解答,谢谢 !

检测甘油,有对照乙二醇、二甘醇,内标正己醇,条件:DB-624(30m*0.53mm 3.um),进样量1ul,分流比10:1,进样口200°,FID250°,程序:起始100(维持4′),以50°/min升120°(维持10′),再以50°/min升220°(维持6′).后加设降温和平衡时间。样品处理:系统适用性性乙二醇、二甘醇,内标正己醇各100mg稀释至100ml(系统储备液),精取1ml+4g甘油样品至100容量瓶, 所 有 溶剂都是色谱甲醇。 对照液:乙二醇、二甘醇,内标正己醇各50mg至100ml(标储液),取5ml稀释至25ml。问题:6月份同样方法检测,一切正常(当时柱子新买来活化后检1批乙醇,) 这两天同一根柱子检测(中间检测了3批乙醇),结果系统适用性乙二醇出不来峰了。正己醇和二甘醇峰面积无论是储备液还是系统适用性都没什么差异。储备液中的乙二醇有峰面积,但与之前浓度相当情况下峰面积小1/3,系统适用性就出不来了,对照液要算校正因子f,之前差不多2-3左右,现在超过10了。乙二醇的安剖瓶色标5ml有之前开启后密封冷藏的,也有新开的,两种情况都差不多,批号都是081226。http://ng1.17img.cn/bbsfiles/images/2012/07/201207251613_379663_2481522_3.jpg6月份的对照液,峰依次是:乙二醇--正己醇--二甘醇。http://ng1.17img.cn/bbsfiles/images/2012/07/201207251616_379664_2481522_3.jpg6月的系统适用性,7.8′乙二醇峰还是不错的,但这次此峰消失了。后面的正己醇、二甘醇相当浓度峰面积也相当。请问问题可能在哪里呢?
福立仪器做水质甲醇顶空,柱子聚乙二醇,水质顶空苯系物也用的同样的机器和柱子,两个项目做的话,总得换分流比,想问一下分流比调到多少,柱前压调到多少合适,可以做两个项目的,只有一个柱子,每次做很麻烦需要手动调节分流比,想找个好点的办法谢谢各位大神
玉米赤霉醇:盲目追求增重的危害· 什么是玉米赤霉醇 玉米赤霉醇又名“右环十四酮酚”,商品名字“畜大壮”,是玉米赤霉菌在生长过程中产生的次生代谢产物玉米赤霉烯酮的还原产物,属于雷索酸内酯类非甾体类同化激素。它是一种皮埋增重剂。· 食品中为什么会残留玉米赤霉醇玉米赤霉醇能直接或间接作用于脑下垂体和胰脏,提高体内生长激素和胰岛素水平,促进动物机体蛋白质的合成,提高饲料利用率,从而产生促增重作用。由于玉米赤霉醇作为牛羊增重剂效果好,经济回报高,部分违法者在畜禽养殖过程中使用玉米赤霉醇,导致玉米赤霉醇可能会残留在各种食用组织(如牛羊肉、动物肝脏、肾脏和血液等)中。· 玉米赤霉醇有哪些危害 玉米赤霉醇及其代谢产物具有雌激素类物质的生物活性,对促性腺激素结合受体、体外肝脏激素结合受体均有抑制作用。雌激素类物质的残留会引起人体性激素机能紊乱及影响第二性征的正常发育,在外部条件诱导下,可能致癌。玉米赤霉醇排出动物体外后,还可经饮水和食物造成二次污染及环境污染。· 玉米赤霉醇的检测方法 目前,玉米赤霉醇残留量的主要检测标准是推荐性国家标准GB/T 21982-2008《动物源食品中玉米赤霉醇、β-玉米赤霉醇、α-玉米赤霉烯醇、β-玉米赤霉烯醇、玉米赤霉酮和赤霉烯酮残留量检测方法,液相色谱-质谱/质谱法》,另外还有3个是农业部公告方法:农业部1025号公告-3-2008《动物性食品中玉米赤霉醇残留检测酶联免疫吸附法和气相色谱-质谱法》、农业部1025号公告-19-2008《动物源性食品中玉米赤霉醇类 药物残留检测 液相色谱-串联质谱法》和农业部1077号公告-6-2008《水产品中玉米赤霉醇类残留量的测定液相色谱-串联质谱法》。南京科捷高效液相色谱:LC600高效液相色谱仪(梯度配置) P600宝石恒流泵 2台UV600紫外检测器 1台7725i六通进样阀 1只进口C18柱 150x4.6 5u 1根WS600色谱工作站 1套主要特点:1 智能化---状态智能监测系统,人性化更强 2 自动化---自动控制及反馈功能,操作更便捷 3 网络化---多台仪器网络接口链接,平台更先进 4 高精度,高稳定性----全数字化信号系统有效的提高了仪器精度; 各部件长寿命的设计标准以及低能耗的运行有效地保证了仪器的稳定性

GDX能分开乙二醇和二甘醇么?从来没有做过,药典上要求用山梨醇硅藻土的柱子,而药典上要求的温度是160度,稍微不注意就把山梨醇给烤糊了,所以我想GDX不是能分离醇类的么?恰好15年前剩下两瓶GDX101,所以就给空柱子给填了刚开始看见两个不错的峰,觉得很高兴,谁知道一验证,得知那个前面的峰是乙醇峰,被污染的乙醇,而后面的主峰是需要的!把图给大家发上来,请大家给出一个主意,我现在不用毛细柱,因为要进带水的样,用填充柱,手里的填料有,GDX101.102.503.504.PEG-20M等,看看那个能把这两个醇给分开?==============================================================================================http://ng1.17img.cn/bbsfiles/images/2010/11/201011062037_257759_1621482_3.jpg=================================================================================================http://ng1.17img.cn/bbsfiles/images/2010/11/201011062038_257760_1621482_3.jpg
环氧乙烷和二氧六环 取本品1g,精密称定,置顶空瓶中,精密加入超纯水1.0ml,密封,摇匀,作为供试品溶 液。量取环氧乙烷300uL(相当于0.25g环氧乙烷),置含 50ml经过处理的聚乙二醇400(以60℃,1.5~2. 5kPa旋转蒸发6小时,除去挥发性成分)的100ml量瓶中,加入相同溶剂稀释至刻度,摇匀,作为环氧乙烷对照品贮备液,精密称取lg冷的环氧乙烷对照品贮备液,置含40ml经过处理的聚乙二醇400的50ml量瓶中,加相同溶剂稀释至刻度。精密称取10g,置含30ml水的50ml量瓶中,加水稀释至刻 度。精密量取10ml,置50ml量瓶中,加水稀释至刻度,摇匀,作为环氧乙烷对照品溶液。取二氧六环适量,精密称定,用水制成每1ml中含0.1mg的溶液,作为二氧六环对照品溶液。精密称取本品lg,置顶空瓶中,精密加入0.5ml 环氧乙烷对照品溶液及0.5ml 二氧六环对照品溶液,密封, 摇匀,作为对照品溶液。量取0.5ml环氧乙烷对照品溶液置 顶空瓶中,加入新鲜配制的0.001%乙醛溶液0.1ml及二氧六环对照品溶液0.1ml,密封,摇匀,作为系统适用性试验溶液,照[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url](通则0521)试验,以聚二甲基硅氧烷为固定液,起始温度为35℃,维持5钟,以每分钟5℃的 速率升温至180℃,然后以每分钟30℃的速率升温至 230℃,维持5分钟(可根据具体情况调整)。进样口温度为 150℃,检测器温度为250℃,顶空平衡温度为70℃,平衡时间为45分钟。取系统适用性试验溶液顶空进样,调节检测器灵敏度使环氧乙烷峰和乙醛峰的峰高约为满量程的 15%,乙醛峰和环氧乙烷峰之间的分离度不小于2.0,二氧六环峰高应为基线噪音的5倍以上,分别取供试品溶液及对照品溶液顶空进样,重复进样至少3次。环氧乙烷峰面积的相对标准偏差应不得过15%,二氧六环峰面积的相对标准偏差应不得过10%,按标准加入法计算,含环氧乙烷不得过0.0001%, 含二氧六环不得过0.001%。
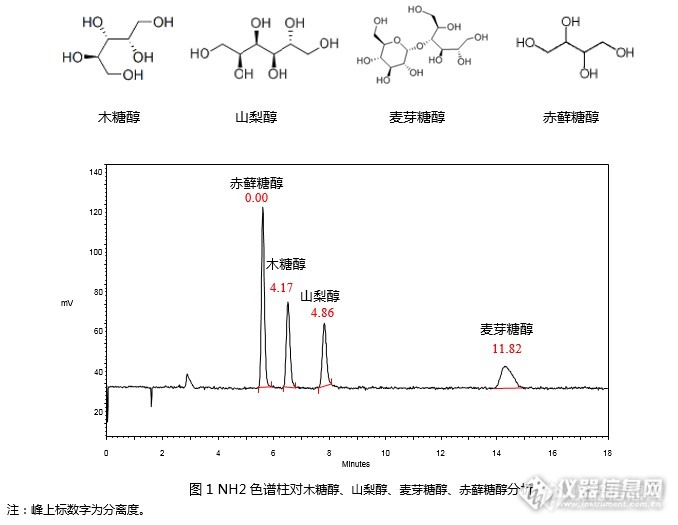
[align=center]GB 5009.279-2016 食品安全国家标准 食品中木糖醇、山梨醇、麦芽糖醇、赤藓糖醇的测定-NQAD[/align]《GB 5009.279-2016 食品安全国家标准食品中木糖醇、山梨醇、麦芽糖醇、赤藓糖醇的测定》第二法中推荐使用蒸发光散射检测器对4种糖醇进行检测。本实验室使用资生堂高灵敏度气溶胶通用型检测器NQAD对该项目进行检测。使用资生堂氨基柱CAPCELL PAK NH2 UG80 S5 4.6 mm i.d. × 250 mm(GQAD 05507)依据国标方法进行分析,可以实现4种糖醇的良好分析(见图1)。[img=,678,525]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030937_01_2222981_3.png[/img][img=,611,257]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030937_02_2222981_3.png[/img]进一步对标准曲线进行绘制,依据国家标准,以峰面积为纵坐标,标准工作液浓度为横坐标,以赤藓糖醇浓度为0.14 mg/mL, 0.21 mg/mL, 0.28 mg/mL, 0.35 mg/mL, 0.42 mg/mL, 0.49 mg/mL,木糖醇、山梨醇、麦芽糖醇浓度为0.10 mg/mL, 0.15 mg/mL, 0.20 mg/mL, 0.25 mg/mL, 0.30 mg/mL, 0.35 mg/mL的混合系列标准工作液,进行标准曲线绘制。如图2~5所示,赤藓糖醇在0.14 mg/mL~0.49 mg/mL浓度范围内,木糖醇、山梨醇、麦芽糖醇在0.1 mg/mL~0.35 mg/mL浓度范围内线性良好,相关系数R[sup]2[/sup]均在0.99以上。[img=,534,330]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030938_01_2222981_3.png[/img][img=,573,327]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030938_02_2222981_3.png[/img][img=,573,326]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030938_03_2222981_3.png[/img][img=,556,342]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030938_04_2222981_3.png[/img]注:图中色谱峰线条不平滑是由于图像在复制过程中解像度问题引起的。
[table=100%][tr][td=2,1,650][font=宋体][/font][align=center][b][size=5]产品概要[/size][/b][/align][size=5] 雌二醇[b](β-Estradiol)[/b]是应用广泛的甾类同化激素,被大量用于促进反刍动物的生长。但由于雌二醇存在明显的致癌性,欧美等国家已相继禁止或严格禁止使用。我国农业部第235号文件中规定,动物源性食品中雌二醇的残留限量为不得检出。由于[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url](GC)分析法样本前处理及测定操作繁琐且费用高,使推广应用受到限制。[/size][align=center][b][size=5]产品用途[/size][/b][/align][size=5] 可定性、定量检测动物组织(肌肉、肝脏、虾、鱼等)、尿液、饲料、奶粉等样本中雌二醇的残留量。[/size][align=center][b][size=5]产品性能参数[/size][/b][/align][size=5] [/size][table][tr][td][size=5]产品规格[/size][/td][td][size=5]96T[/size][/td][/tr][tr][td][size=5]适用范围[/size][/td][td][size=5]动物组织(肌肉、肝脏、虾、鱼等)、尿液和饲料,奶粉等[/size][/td][/tr][tr][td][size=5]检测时间[/size][/td][td][size=5]1.5个小时[/size][/td][/tr][tr][td][size=5]检测下限[/size][/td][td][size=5]鸡肉/肝、猪肉/肝、虾、鱼 :5ppb饲料 :80ppb尿液 :2.5ppb[/size][/td][/tr][tr][td][size=5]灵敏度[/size][/td][td][size=5]0.1ppb[/size][/td][/tr][tr][td][size=5]前处理流程[/size][/td][td][size=5]组织:均质、振荡离心、吹干、溶解、反萃取、振荡离心、吹干、复溶[/size][/td][/tr][tr][td][size=5]交叉反应率[/size][/td][td][size=5]雌 二 醇 :100%雌二醇-3甲醚:30%炔 雌 醇 :7%雌酚酮 :小于0.1%苯甲酸雌二醇 :小于0.1%雌 三 醇 :小于0.1%[/size][/td][/tr][tr][td][size=5]结果判定[/size][/td][td][size=5]定性:根据样本孔颜色与标准品孔颜色进行比对定量:运用酶标仪进行计算[/size][/td][/tr][/table][/td][/tr][tr][td=2,1][size=5][i][b]无锡康纳生物科技有限公司 0510-85191271,13771068995,杨小姐[/b][/i][/size][/td][/tr][/table]
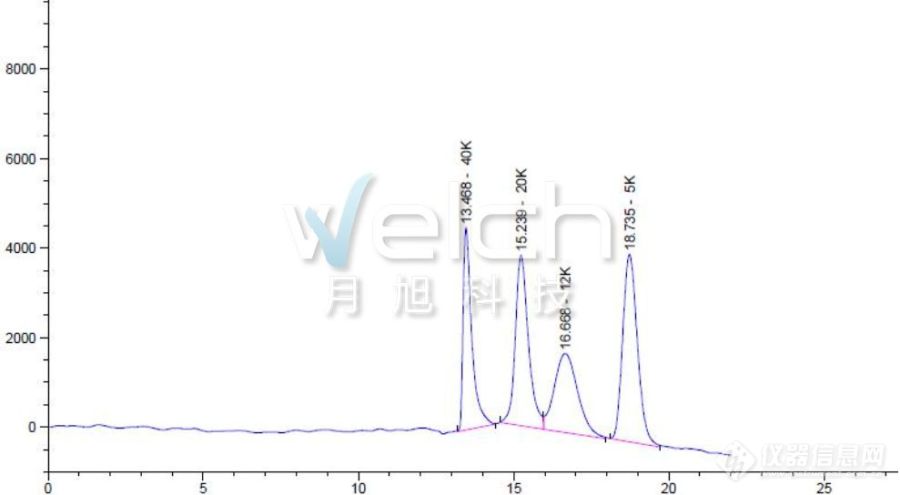
[b][/b][align=center][b]新增项目[/b][/align]最近在浏览国家药典委员会官网的时候,惊奇的发现聚乙二醇300,400,1000……全部的聚乙二醇品种药典方法都要修订了!在浏览了公示方法,发现原来是新增了一个项目,从2020版药典开始要标明重均分子量及分子量分布系数的标示值(按所附测定方法测定),那各位小伙伴了解分子量及分子量分布测定方法吗?这里就给大家详细讲讲。[b]2020版中国药典征求意见稿之分子量及分子量分布测定方法[/b]分别称取聚乙二醇600、聚乙二醇1000、聚乙二醇4000、聚乙二醇7000、聚乙二醇10000分子量对照品适量,加流动相溶解并稀释制成每1ml中约含2mg的溶液作为对照品溶液。称取样品适量,加流动相溶解并稀释制成每1ml中约含2mg的溶液作为供试品溶液。照分子排阻色谱法(通则0514)测定,采用适宜分离范围的凝胶色谱柱,以0.1mol/L硝酸钠溶液(含0.02%抑菌剂)为流动相,示差折光检测器;检测器温度35℃,柱温35℃,取对照品溶液各100μl注入液相色谱仪,记录色谱图,由GPC软件计算回归方程,线性相关系数R应不得小于0.99。取供试品溶液100μl,同法测定,根据回归方程计算供试品的重均分子量及分子量分布。供试品的重均分子量应为标示值的90%~110%,分布系数应为产品标示值的90%~110%。[b]什么是分子排阻色谱法[/b]分子排阻色谱法是根据待测组分的分子大小进行分离的一种液相色谱技术。分子排阻色谱法的分离原理为凝胶色谱柱的分子筛机制。色谱柱多以亲水硅胶、凝胶或经过修饰的凝胶如葡聚糖凝胶(Sephadex)和琼脂糖凝胶(Sepharose)等为填充剂,这些填充剂表面分布着不同孔径尺寸的孔,药物分子进入色谱柱后,它们中的不同组分按其分子大小进入相应的孔内,大于所有孔径的分子不能进入填充剂颗粒内部,在色谱过程中不被保留,最早被流动相洗脱至柱外,表现为保留时间较短;小于所有孔径的分子能自由进入填充剂表面的所有孔径,在色谱柱中滞留时间较长,表现为保留时间较长;其余分子则按分子大小依次被洗脱。[b]分子排阻色谱法应用案例[/b]月旭科技Xtimate SEC色谱柱是硅胶基质的分子排阻色谱柱,其色谱填料为高纯度、具有良好稳定性的硅胶微球表面键合亲水性聚合物。月旭科技采用特殊的表面修饰技术,确保了该填料具有良好的稳定性和批次重现性。Xtimate SEC色谱填料采用独特的化学键合技术,在硅胶表面键合了亲水性聚合物以及亲水性二醇基官能团,双重键合机制使水溶性高分子聚合物蛋白、生物酶、多肽等生物样品的非特异性吸附极小,因而可广泛应用于水溶性聚合物及生物大分子的分离和测定。月旭科技采用Xtimate SEC-300 (7.8*300mm,5μm)两根色谱柱串联的方式成功分离检测聚乙二醇40k,20k,12k,5k含量。[b]色谱柱:[/b]月旭Xtimate SEC-300 (7.8*300mm,5μm)两根色谱柱串联[b]流动相:[/b]高纯水[b]检测波长:[/b]示差检测器[b]柱温:[/b]柱温40℃,检测器40℃[b]流速:[/b]1.0ml/min[b]进样量:[/b]20μl[align=center][img=,690,379]https://ng1.17img.cn/bbsfiles/images/2019/10/201910160944591635_8915_932_3.jpg!w690x379.jpg[/img][/align][align=center][img=,414,40]https://ng1.17img.cn/bbsfiles/images/2019/10/201910160946105076_5570_932_3.png!w414x40.jpg[/img][/align]各位小伙伴想了解更多有关分子排阻色谱法的相关信息,请咨询月旭当地销售人员或拨打400-810-6969垂询。
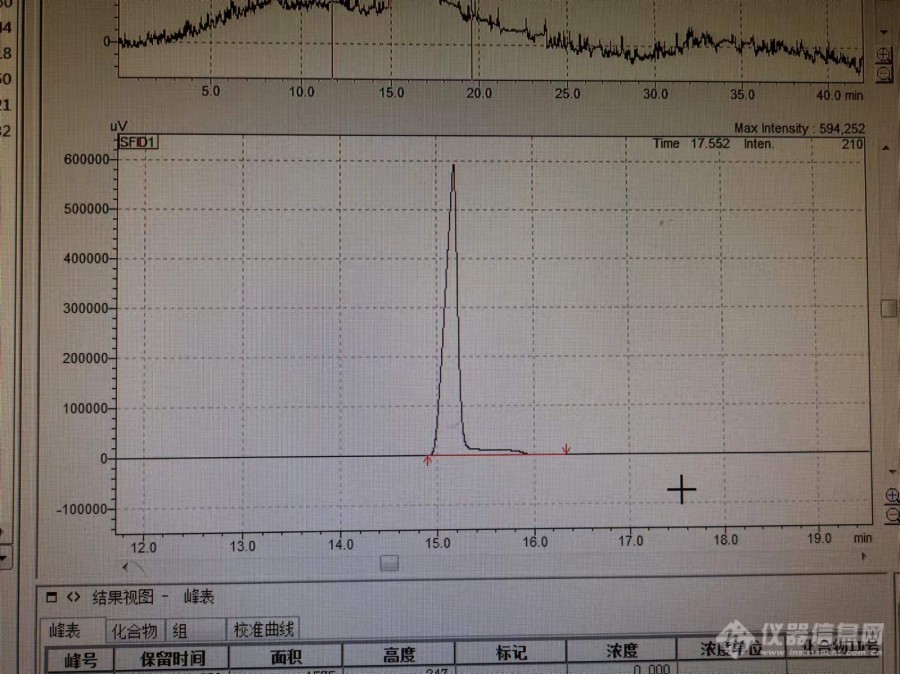
[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]检测乙二醇的纯度,柱子Rtx-624,进样量0.3微升,分流比200,升温程序:80℃(3min),5℃/min升至230℃,维持10min,现在有几个问题:(1)乙二醇需要用溶剂稀释吗?不稀释时信号值在500000左右,是不是有点大,柱子会过载吗?进样量已经尽可能小,分流比尽可能的最大了。这种情况怎么解决?(2)乙二醇的峰出现如下图的拖尾峰,该怎么解决?[img=,690,516]https://ng1.17img.cn/bbsfiles/images/2022/01/202201041402054285_3186_3347577_3.jpg!w690x516.jpg[/img]
[align=left][font='宋体'][size=24px]赤藓糖醇[/size][/font][font='宋体'][size=24px]的性质及国标测定方法[/size][/font][/align][size=24px]游臻[/size][size=24px]时 间:2021.[/size][size=24px]7[/size][align=center][font='黑体'][size=20px]赤藓糖醇的性质及国标测定方法[/size][/font][/align][size=16px]摘 要[/size][size=16px]:[/size][size=16px]赤藓糖醇,一种天然活性物质,被广泛应用于食品、医药保健品、日化产品和化工产品中。近年来,随着人们对于营养健康的关注度逐渐增加,学者对其理化及生物学特性研究的不断深入,赤藓糖醇的安全性得到证实,应用范围逐渐扩大。为此,本文对赤藓糖醇的理化特性[/size][size=16px]、[/size][size=16px]来源[/size][size=16px]、[/size][size=16px]提取方法[/size][size=16px]、[/size][size=16px]应用[/size][size=16px]、[/size][size=16px]检测方法[/size][size=16px]、[/size][size=16px]检测标准[/size][size=16px]进行了简要介绍,从机理和应用的角度阐述了赤藓糖醇在不同领域的研究。[/size][size=16px]因为[/size][size=16px]赤藓糖醇独特的代谢方式,使其被应用于糖尿病、葡萄糖不耐受症等特殊人群的功能食品中。赤藓糖醇的防龋性、抗氧化性、保湿性和不可燃性等特性使其在医药、日化领域的应用不断扩展。[/size][size=16px]关键词[/size][size=16px]:赤藓糖醇;性质;检测;应用;生产[/size][size=18px]一、[/size][size=18px]赤藓糖醇的理化性质[/size][size=18px]与生理性质[/size][font='宋体'][size=16px]1[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]赤藓糖醇的性质[/size][/font][size=13px]赤藓糖醇在自然界分布十分广泛,海藻、蘑菇以及甜瓜、葡萄、桃等水果类中均含有赤藓糖醇。由于细菌、真菌和酵母也能产生赤藓糖醇,所以在发酵食品果酒、啤酒、酱油中也存在,另外还存在于人和哺乳动物的体液中。赤藓糖醇为白色结晶的四碳多元醇类化合物,化学名称为[/size][size=13px]1,2,3,4-丁四醇,分子式为C4H10O4,分子量122.12,熔点126℃,沸点329~331℃,溶解热-97.4J/g,[/size][size=13px]其化学性质与山梨糖醇、甘露糖醇和木糖醇等糖醇相类似。[/size][font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]1][/size][/font][font='宋体'][size=14px](1) [/size][/font][font='宋体'][size=16px]赤藓糖醇的甜度[/size][/font][size=13px]赤[/size][size=13px]藓糖[/size][size=13px]醇与蔗糖的甜昧特性十分接近,爽净且无后苦味,甜度约为蔗糖的[/size][size=13px]70%~80%。[/size][size=13px]与其他甜味剂混合使用具有改善、协调味质[/size][size=13px]的[/size][size=13px]作用,如赤藓糖醇与高甜味剂甜菊[/size][size=13px]糖[/size][size=13px]苷以[/size][size=13px]1000:(1~7)混合使用,可有效掩盖甜菊[/size][size=13px]糖[/size][size=13px]苷[/size][size=13px]的后苦味;将[/size][size=13px]20%以上的赤藓糖醇与白砂糖并用,其后[/size][size=13px]味和甜味比白砂糖更为理想;溶液中[/size][size=13px]1%~3%的赤藓糖[/size][size=13px]醇能有效掩饰刺激性口味,改善溶液的口感和风味[/size][size=13px];与糖精,阿斯巴甜等甜味剂混合使用,甜味特性良好,可以掩盖人工合成甜味剂的不良味感。[/size][font='宋体'][size=14px](2) [/size][/font][font='宋体'][size=16px]赤藓糖醇的稳定性[/size][/font][size=13px]赤[/size][size=13px]藓糖醇在热[/size][size=13px],[/size][size=13px]酸,碱条件下[/size][size=13px]稳定,[/size][size=13px]适用的酸碱范围为[/size][size=13px]pH2~12,符合一般食品对酸碱的要求,由于不含羰基,所以在与氨基酸共存的情况下无美拉德反应发生。试验表明,赤藓糖醇在160℃高温条件下不会出现分解及热变色,避免高温加工过程食品出现的焦化。[/size][font='宋体'][size=14px](3) [/size][/font][font='宋体'][size=16px]赤藓糖醇的结晶性[/size][/font][size=13px]赤藓糖醇吸湿性低,结晶性好,易粉碎制得粉状产品,其吸湿性在糖醇及蔗糖等甜味剂中是最小的。温度为[/size][size=13px]20℃、相对湿度为90%的环境中,放置5d后的吸湿增[/size][size=13px]重,麦芽糖约为[/size][size=13px]17%,蔗糖约为10%,而赤藓糖醇仅为2 %左右。[/size][font='宋体'][size=14px](4) [/size][/font][font='宋体'][size=16px]赤藓糖醇的溶解热[/size][/font][size=13px]赤藓糖醇在[/size][size=13px]20℃时溶解度仅为37%,大约是山梨醇[/size][size=13px]溶解度的[/size][size=13px]50%,在制作高甜度食品时,为防止结晶析出,[/size][size=13px]保持食品的质构稳定,应和其他糖醇混合使用。赤藓糖醇溶解热高是葡萄糖的[/size][size=13px]3倍,为-96.86kJ/kg,溶于水会吸[/size][size=13px]收较多的能量,食用时有一种凉爽的口感特性。赤藓糖醇结晶性好,不吸潮,在[/size][size=13px]20℃、相对湿度为90%时仍不吸[/size][size=13px]潮,特别适用于加工巧克力糖果等食品。[/size][font='宋体'][size=14px](5) [/size][/font][font='宋体'][size=16px]赤藓糖醇的[/size][/font][font='宋体'][size=16px]渗透压[/size][/font][size=13px]由于赤藓糖醇分子小,分子量仅为蔗糖的[/size][size=13px]1/3左右,[/size][size=13px]能大大地降低水分活度。[/size][size=13px]25℃、36%的水溶液,水分活度[/size][size=13px]为[/size][size=13px]0.91;而赤藓糖醇渗透压高,20℃、15%的水溶液渗透[/size][size=13px]压为[/size][size=13px]1861mosm/kg,是蔗糖的3.2倍,山梨醇的1.8倍。赤[/size][size=13px]藓糖醇的这一特性有利于提高食品的防腐能力,延长食品的[/size][size=13px]保质[/size][size=13px]期。[/size][font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]2][/size][/font][font='宋体'][size=16px]2.赤藓糖醇的生理性质[/size][/font][font='宋体'][size=16px]([/size][/font][font='宋体'][size=16px]1)赤藓糖醇的代谢[/size][/font][font='宋体'][size=13px]赤藓糖醇在小肠易于吸收,大部分能进入血液中循环,仅有少量直接进入大肠中作为碳源发酵。由于人[/size][/font][font='宋体'][size=13px]体缺乏代谢赤藓糖醇的酶系,进入血液中的赤藓糖醇不能被消化降解,只能透过肾从尿液中排出体外,这一独特的代谢特征,决定了赤藓糖醇低热值的特性。据文献报道[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px],进入机体内的赤藓糖醇有约[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]经小肠吸收并从[/size][/font][font='宋体'][size=13px]尿液中排出,[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]左右进入大肠,进入大肠中的最多有[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]被细菌利用,其他经由粪便排出体外。由此得知,摄入的赤藓糖醇只有[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]代谢产能,为人体提供能量,而赤[/size][/font][font='宋体'][size=13px]藓糖醇的能量值为[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]k[/size][/font][font='宋体'][size=13px]cal/g[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]kcal/g[/size][/font][font='宋体'][size=13px],仅为蔗糖能量[/size][/font][font='宋体'][size=13px]的[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px],是所有多元糖醇甜味剂中能量最低的一[/size][/font][font='宋体'][size=13px]种。[/size][/font][font='宋体'][size=13px]由于进入机体的赤藓糖醇进入大肠的量很少,因此不会造成不吸收物质可能带来的腹泻及肠胃胀气等副作用,所以赤藓糖醇具有很高的耐受性,是糖醇中耐受性最高的一种。由于人体缺乏代谢赤藓糖醇的酶系,进入机体的赤藓糖醇大部分由尿液排出,其代谢途径与胰岛素无关或很少依赖胰岛素,所以对糖代谢没有影响。食用含赤藓糖醇的食品对糖尿病患者等糖限量的特殊消费群体是安全的。[/size][/font][font='宋体'][size=16px]([/size][/font][font='宋体'][size=16px]2)赤藓糖醇的非致龋齿特性[/size][/font][font='宋体'][size=13px]由于口腔中的细菌,特别是金黄链球菌[/size][/font][font='宋体'][size=13px]([/size][/font][font='宋体'][size=13px]Streptococcus mutans)[/size][/font][font='宋体'][size=13px]不能利用和发酵赤藓糖醇,所以不会引[/size][/font][font='宋体'][size=13px]起口腔牙表面[/size][/font][font='宋体'][size=13px]pH[/size][/font][font='宋体'][size=13px]值下降产生牙斑,导致龋齿。[/size][/font][size=18px]二[/size][size=18px]、[/size][size=18px]赤藓糖醇的生产[/size][font='宋体'][size=16px]1[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]化学法生产赤藓糖醇[/size][/font][font='宋体'][size=13px]化学合成法[/size][/font][font='宋体'][size=13px]是[/size][/font][font='宋体'][size=13px]由丁烯二醇与过氧化氢反应,其中丁烯二醇是由乙炔和甲醛先制成2[/size][/font][font='宋体'][size=13px]-[/size][/font][font='宋体'][size=13px]丁烯[/size][/font][font='宋体'][size=13px]-[/size][/font][font='宋体'][size=13px] 1,4 [/size][/font][font='宋体'][size=13px]-[/size][/font][font='宋体'][size=13px] 二 醇, 然后将其水溶液与活性镍催化剂混合并加[/size][/font][font='宋体'][size=13px]入[/size][/font][font='宋体'][size=13px]阻化剂氨水,在[/size][/font][font='宋体'][size=13px]0.5[/size][/font][font='宋体'][size=13px] M Pa压力下通[/size][/font][font='宋体'][size=13px]入[/size][/font][font='宋体'][size=13px]H[/size][/font][font='宋体'][size=13px]2[/size][/font][font='宋体'][size=13px]氢化,得到赤[/size][/font][font='宋体'][size=13px]藓[/size][/font][font='宋体'][size=13px]糖醇产品。以淀粉为原料的化学合成法是将淀粉用高碘酸法生成双醛淀粉,再经氧化裂解生成赤[/size][/font][font='宋体'][size=13px]藓[/size][/font][font='宋体'][size=13px]糖[/size][/font][font='宋体'][size=13px]醇[/size][/font][font='宋体'][size=13px]和其他衍生物[/size][/font][font='宋体'][size=13px]。[/size][/font][font='宋体'][size=13px]化学合成生产赤[/size][/font][font='宋体'][size=13px]藓[/size][/font][font='宋体'][size=13px]糖[/size][/font][font='宋体'][size=13px]醇[/size][/font][font='宋体'][size=13px]的工艺方法存在流程长、成本高、污染严重、条件要求高、产品安全性差等不足,无法与发酵法比拟,因此目前研究和应用最多的是以淀[/size][/font][font='宋体'][size=13px]粉为原料的发酵法来生产赤藓糖醇的工艺方法。[/size][/font][font='宋体'][size=16px]2[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]发酵法生产赤藓糖醇[/size][/font][font='宋体'][size=13px]发酵法是以淀粉水解葡萄糖为原料,经耐高渗酵母菌株发酵产生赤藓糖醇及少量的核糖醇,丙三醇等副产物,经分离,提取,精制,获得高纯度的赤藓糖醇产品。产品的收率大约为5[/size][/font][font='宋体'][size=13px]0%[/size][/font][font='宋体'][size=13px]。与化学合成法相比,具有条件温和,易于控制,环境友好,污染少,产品安全,原料来源丰富,成本低等优点,更易于实现规模生产。[/size][/font][font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]4][/size][/font][font='宋体'][size=18px]三[/size][/font][font='宋体'][size=18px]、[/size][/font][font='宋体'][size=18px]赤藓糖醇的应用[/size][/font][font='宋体'][size=16px]1[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]赤藓糖醇在食品工业的应用[/size][/font][font='宋体'][size=13px]赤藓糖醇经过急性、亚急性、慢性毒性试验等动物 试验以及人体试验确认安全无毒、食用安全性较好, 允许添加量较高,不易引起腹泻或胃肠等不适感。1990 年日本食品法规批准赤藓糖醇可直接作为食品配料; 1997年通过美国食品与药品管理局(FDA)批准,获美 国FDA安全食品配料(GRAS)认[/size][/font][font='宋体'][size=13px]证和允许在标签上标 注“有益于牙齿健康”;1999年世界粮农组织(FAO)和 世界卫生组织(WHO)联合组成的食品添加剂专家委员 会(JECFA)批准赤藓糖醇作为食用甜味剂,无需规定 ADI值;1999年澳大利亚和新西兰食品监督局(AN 、A)批准赤藓糖醇作为食用配料,我国在GB 2760-86标准 中也允许其在食品中应用。 [/size][/font][font='宋体'][size=13px]由于赤藓糖醇的热、酸稳定性好,在一般性食品加工条件下,几乎不会引起褐变或分解现象,在硬糖生产时高温熬煮也不会引起褐变。赤藓糖醇的热稳定性高使巧克力生产的精炼可以在更高的温度下进行,进一步促进巧克力风味的形成,改善产品的品质。赤藓糖醇的吸湿性差,在湿度为90%的环境也不易吸潮,这一特性对巧克力、口香糖等食品加工很有利。赤藓糖醇的高吸热性使得产品食用后具有持久的爽口清凉感觉,对改善口香糖、清凉性固体饮料和糖果的品质十分重要。赤藓糖醇甜味爽净,在与蛋白糖、甜菊糖等高甜度甜味剂复配时可有效地掩盖其后苦味;赤藓糖醇还可以降低酒精的异味,改善蒸馏酒和葡萄酒的口感与风味,在蔬菜汁饮料中使用,可有效地抑制蔬菜饮料特有的不良口味;在饮用咖啡时添加可有效地抑制咖啡的涩味。赤藓糖醇的耐热和耐酸等特性,使得巴氏高温或超高温等杀菌工艺对以赤藓糖醇为甜味剂的饮料外观品质均不会产生影响。[/size][/font][font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]5[/size][/font][font='宋体'][size=13px]][/size][/font][font='宋体'][size=16px]2[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]赤藓糖醇在医药生产的应用[/size][/font][font='宋体'][size=13px]赤藓糖醇的防龋特性是近年来赤藓糖醇的一个应用热点。张帆等通过体外的人工龋实验证实,赤藓糖醇和牛奶的混合液具有抑制变异链球菌在生物膜中黏附生长,促进脱矿牙釉质再矿化的作用,可以在一定程度是阻止龋病的发展。未来,赤藓糖醇-牛奶混合液,作为一种安全、营养的食品,极有可能成为替代加氟牛奶成为另一条防龋的有效途径。李维丹实验表明赤藓糖醇对牙周炎的主要致病菌牙龈卟啉单胞菌有明显抑制作用,并能降低其在牙骨质表面的黏附作用,为牙周病的防治提供了新的方向。[/size][/font][font='宋体'][size=13px]此外,赤藓糖醇还能抑制多种龋病致病链球菌及耐氟菌的生长和产酸。目前,越来越多的防龋产品使 用赤藓糖醇代替传统的氟化物和抗生素。赤藓糖的抗氧化性,不仅是添加到柠檬汁饮料中保护 VC,还可以应用为一种体内抗氧化剂,防止身体的氧化应激损伤。韩春妮等通过设计实验表明,赤藓糖醇可减轻 H2O2 对 PC12 细胞的氧化损伤程度,具有体外抗氧化损伤的作用,为赤藓糖醇应用于预防和治疗机体氧化应激引起的糖尿病及其并发症提供了理论基础。在链脲佐菌素诱导的糖尿病大鼠实验中,赤藓糖醇不仅是一种极好的自由基清除剂和抑制剂,还具有保护内 皮细胞层的作用。此外,研究还表明,赤藓糖醇对2,2-偶氮二异丁基脒二盐酸盐引起的大鼠溶血有抑制作用,对减轻高血糖症引起的血管损伤起到积极作用。此外,赤藓糖醇的吸湿性低、分散性好、口感优良、与各种药物兼容性好等特性,正越来越多的应用于药片包衣、药剂辅料、吸入剂药物载体或赋形剂等诸多领域[/size][/font][font='宋体'][size=13px]。[/size][/font][font='宋体'][size=16px]3[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]赤藓糖醇在日化品生产的应用[/size][/font][font='宋体'][size=13px]赤藓糖醇因其防龋齿性,促进牙菌斑分解,有利于维持口腔健康等优势已被应用于牙膏中, KAO(花王)、LG 竹盐炫润白系列牙膏都添加有赤藓糖醇。另外,赤藓糖醇不仅具有和甘油相同的保湿及改善肌肤粗糙的效果,而且黏稠性低、有清凉效果,已被日本资生堂用于多个系列的护肤品中[/size][/font][font='宋体'][size=13px]。[/size][/font][font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]6[/size][/font][font='宋体'][size=13px]][/size][/font][font='宋体'][size=18px]四[/size][/font][font='宋体'][size=18px]、[/size][/font][font='宋体'][size=18px]赤藓糖醇的检测[/size][/font][font='宋体'][size=16px]1[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]高效液相色谱法[/size][/font][font='宋体'][size=13px]根据[/size][/font][font='宋体'][size=13px]GB 26404-2011[/size][/font][font='宋体'][size=13px],[/size][/font][font='宋体'][size=13px]利用高效液相色谱仪和示差折光检测器,色谱条件为流动相是重蒸蒸馏水;色谱柱为[/size][/font][font='宋体'][size=13px]氢型大孔径阳离子交换树脂填充柱,树脂包含大网格磺化聚苯乙烯[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]二乙烯基苯[/size][/font][font='宋体'][size=13px]共聚物,交联度为[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px],颗粒大小为[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]微米;流速为[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]ml[/size][/font][font='宋体'][size=13px]/[/size][/font][font='宋体'][size=13px]min;柱温为6[/size][/font][font='宋体'][size=13px]0[/size][/font][font='宋体'][size=13px]摄氏度;进样量为1[/size][/font][font='宋体'][size=13px]0[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]L。[/size][/font][font='宋体'][size=13px]实验步骤为[/size][/font][font='宋体'][size=13px]准确称取0.25g 在105℃下干燥4h后的赤藓糖醇标准品[/size][/font][font='宋体'][size=13px],[/size][/font][font='宋体'][size=13px]精确至0.0001g[/size][/font][font='宋体'][size=13px],[/size][/font][font='宋体'][size=13px]转移至一个[/size][/font][font='宋体'][size=13px]50mL容量瓶中,用流动相溶解,稀释定容至刻度[/size][/font][font='宋体'][size=13px],[/size][/font][font='宋体'][size=13px]混匀后备用。色谱分析前,用0.45μm微孔滤膜过滤。[/size][/font][font='宋体'][size=13px]再[/size][/font][font='宋体'][size=13px]确称取2.0g在105℃下干燥4h后的赤藓糖醇试样[/size][/font][font='宋体'][size=13px],[/size][/font][font='宋体'][size=13px]精确至0.0001g[/size][/font][font='宋体'][size=13px],[/size][/font][font='宋体'][size=13px]转移至一个50mL容量瓶中,用流动相溶解,稀释定容至刻度,混匀后备用。色谱分析前,用0.45μm微孔滤膜过滤。[/size][/font][font='宋体'][size=13px]最后[/size][/font][font='宋体'][size=13px]在参考色谱条件下,分别对标准溶液和试样液进行色谱分析,记录60min的色谱图。赤藓糖醇的出峰时间根据标准品的出峰时间定性。重复实验两次,得到平均峰面积值[/size][/font][font='宋体'][size=13px]。[/size][/font][font='宋体'][size=13px]结果计算[/size][/font][font='宋体'][size=13px]赤藓糖醇含量以赤藓糖醇([/size][/font][font='宋体'][size=13px]C[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px]H[/size][/font][font='宋体'][size=13px]10[/size][/font][font='宋体'][size=13px]O[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px])的质量分数 w[/size][/font][font='宋体'][size=13px]1[/size][/font][font='宋体'][size=13px]计,数值以%表示,按公式计算:[/size][/font][font='宋体'][size=13px]式中: m[/size][/font][font='宋体'][size=13px]1[/size][/font][font='宋体'][size=13px]──称取的赤藓糖醇标准品质量的数值,单位为克(g); m[/size][/font][font='宋体'][size=13px]2[/size][/font][font='宋体'][size=13px]──称取的试样质量的数值,单位为克(g); A[/size][/font][font='宋体'][size=13px]1[/size][/font][font='宋体'][size=13px]──试样液色谱图中赤藓糖醇平均峰面积值的数值; A[/size][/font][font='宋体'][size=13px]2[/size][/font][font='宋体'][size=13px]──标准溶液色谱图中赤藓糖醇平均峰面积值的数值。[/size][/font][font='宋体'][size=13px] 实验结果以平行测定结果的算术平均值为准,平行测定结果的绝对差值不大于0.5%。[/size][/font][font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]7[/size][/font][font='宋体'][size=13px]][/size][/font][font='宋体'][size=16px]2[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]灼烧残渣的测定[/size][/font][font='宋体'][size=13px]准确称取2g试样,精确至0.0001g,置于800℃±25℃下灼烧至恒重的坩埚中,缓缓加热直至试 样完全碳化。将碳化的试样冷却,用0.5 mL的硫酸润湿残渣,继续加热至硫酸蒸汽逸尽,并在800℃ ±25℃的高温炉中灼烧残渣至恒重[/size][/font][font='宋体'][size=13px]灼烧残渣以质量分数[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]计,数值以[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]表示,按公式计算[/size][/font][font='宋体'][size=13px]式中:[/size][/font][font='宋体'][size=13px]m[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px]──残渣和空坩埚的质量的数值,单位为克(g);m[/size][/font][font='宋体'][size=13px]3[/size][/font][font='宋体'][size=13px]──空坩埚的质量的数值,单位为克(g);m──称取的试样质量的数值,单位为克(g)。[/size][/font][font='宋体'][size=13px]实验结果以平行测定结果的算术平均值为准,平行测定结果的绝对差值不大于[/size][/font][font='宋体'][size=13px]0.05%[/size][/font][font='宋体'][size=16px]3[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]还原糖(以葡萄糖计)的测定[/size][/font][font='宋体'][size=13px]准备[/size][/font][font='宋体'][size=13px]葡萄糖溶液:0.75mg/mL。费林溶液A:称取34.66 g硫酸铜(CuSO[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px]5H[/size][/font][font='宋体'][size=13px]2[/size][/font][font='宋体'][size=13px]O),溶于水中,完全溶解后,用水稀释至500 mL,贮存于密闭容器中。费林溶液B:称取173g酒石酸钾钠(KNaC[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px]H[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px]O[/size][/font][font='宋体'][size=13px]6[/size][/font][font='宋体'][size=13px]4H[/size][/font][font='宋体'][size=13px]2[/size][/font][font='宋体'][size=13px]O)和50g氢氧化钠(NaOH),溶于水中,完全溶解后,用水稀释至500 mL,贮存于橡胶塞玻璃瓶内。 [/size][/font][font='宋体'][size=13px] 分析步骤[/size][/font][font='宋体'][size=13px]为[/size][/font][font='宋体'][size=13px]准确称取约0.5 g试样,精确至 0.0001 g,转移至一个 20 mL 烧瓶中,加入2mL水,溶解、混合,此为试样液。移取2mL葡萄糖溶液,置于另一烧瓶中。分别往两个烧瓶中加入1mL费林溶液 A和1mL费林溶液 B,加热至沸腾后冷却。溶液形成红棕色沉淀。[/size][/font][font='宋体'][size=13px]若葡萄糖溶液反应液较试样液反应液混浊,则判定为合格。[/size][/font][font='宋体'][size=16px]4[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]核糖醇和丙三醇的测定[/size][/font][font='宋体'][size=13px]参考色谱条件同[/size][/font][font='宋体'][size=13px]赤藓糖醇测定的参考色谱条件。准确称取核糖醇标准品和丙三醇标准品各 0.025g,精确至0.0001g,转移至一个50mL容量瓶中,用流动相溶解,稀释定容至刻度,混匀后备用。色谱分析前,用0.45μm 微孔滤膜过滤。试样液制备:准确称取2.0g在105℃下干燥4h后的赤藓糖醇试样,精确至0.0001g,转移至一个50mL容量瓶中,用流动相溶解,稀释定容至刻度,混匀后备用。色谱分析前,用0.45μm微孔滤膜过滤。在参考色谱条件下,分别对标准溶液和试样液进行色谱分析,记录 60 min 的色谱图。核糖醇和丙三醇的出峰时间根据对应标准品的出峰时间定性。重复实验两次,得到平均峰面积值。[/size][/font][font='宋体'][size=13px]结果计算核糖醇和丙三醇的含量分别以质量分数w[/size][/font][font='宋体'][size=13px]3[/size][/font][font='宋体'][size=13px]和w[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px]计,数值均以%表示[/size][/font][font='宋体'][size=13px]式中:[/size][/font][font='宋体'][size=13px]m[/size][/font][font='宋体'][size=13px]5[/size][/font][font='宋体'][size=13px]──称取的核糖醇标准品质量的数值,单位为克(g);[/size][/font][font='宋体'][size=13px]m[/size][/font][font='宋体'][size=13px]0[/size][/font][font='宋体'][size=13px]──称取的试样质量的数值,单位为克(g);[/size][/font][font='宋体'][size=13px]A[/size][/font][font='宋体'][size=13px]3[/size][/font][font='宋体'][size=13px]──试样液色谱图中核糖醇平均峰面积值的数值;[/size][/font][font='宋体'][size=13px]A[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px]──标准溶液色谱图中核糖醇平均峰面积值的数值。[/size][/font][font='宋体'][size=13px]m[/size][/font][font='宋体'][size=13px]6[/size][/font][font='宋体'][size=13px]──称取的丙三醇标准品质量的数值,单位为克(g);[/size][/font][font='宋体'][size=13px]A[/size][/font][font='宋体'][size=13px]5[/size][/font][font='宋体'][size=13px]──试样液色谱图中丙三醇平均峰面积值的数值;[/size][/font][font='宋体'][size=13px]A[/size][/font][font='宋体'][size=13px]6[/size][/font][font='宋体'][size=13px]──标准溶液色谱图中丙三醇平均峰面积值的数值。[/size][/font][font='宋体'][size=13px]取两次平行测定结果的算术平均值为测定结果,平行测定结果的绝对差值不大于[/size][/font][font='宋体'][size=13px]0.01 %[/size][/font][font='宋体'][size=18px]五[/size][/font][font='宋体'][size=18px]、[/size][/font][font='宋体'][size=18px]赤藓糖醇的国家标准[/size][/font][font='宋体'][size=16px]1[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]在产品中的使用量[/size][/font][font='宋体'][size=13px]赤藓糖醇在国家标准中规定在产品中适量使用,没有明确的限制标准,这是因为赤藓糖醇安全性较高并且在产品中过量使用时反而会使产品的外观口感等质量指标大幅度下降,从而影响产品的销售。所以国标中对产品中赤藓糖醇的使用量并没有限制量。[/size][/font][font='宋体'][size=16px]2[/size][/font][font='宋体'][size=16px].[/size][/font][font='宋体'][size=16px]赤藓糖醇的质量标准[/size][/font][font='宋体'][size=13px]感官要求标准,[/size][/font][font='宋体'][size=13px]色泽[/size][/font][font='宋体'][size=13px]为[/size][/font][font='宋体'][size=13px]白色[/size][/font][font='宋体'][size=13px],[/size][/font][font='宋体'][size=13px]滋味[/size][/font][font='宋体'][size=13px]要求[/size][/font][font='宋体'][size=13px]有甜味[/size][/font][font='宋体'][size=13px],[/size][/font][font='宋体'][size=13px]组织状态[/size][/font][font='宋体'][size=13px]为[/size][/font][font='宋体'][size=13px]结晶性粉末或颗粒[/size][/font][font='宋体'][size=13px]理化指标为[/size][/font][font='宋体'][size=13px]赤藓糖醇[/size][/font][font='宋体'][size=13px](以[/size][/font][font='宋体'][size=13px] C[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px]H[/size][/font][font='宋体'][size=13px]10[/size][/font][font='宋体'][size=13px]O[/size][/font][font='宋体'][size=13px]4 [/size][/font][font='宋体'][size=13px]计,以干基计),w/% [/size][/font][font='宋体'][size=13px]:[/size][/font][font='宋体'][size=13px]99.5~100.5[/size][/font][font='宋体'][size=13px]干燥减量,[/size][/font][font='宋体'][size=13px]w/% ≤ 0.2 [/size][/font][font='宋体'][size=13px]灼烧残渣,w/% ≤ 0.1 [/size][/font][font='宋体'][size=13px]还原糖(以葡萄糖计),[/size][/font][font='宋体'][size=13px]w/% ≤ 0.3 [/size][/font][font='宋体'][size=13px]核糖醇和丙三醇(以干基计),[/size][/font][font='宋体'][size=13px]w/% ≤ 0.1 [/size][/font][font='宋体'][size=13px]铅([/size][/font][font='宋体'][size=13px]Pb)/(mg/kg) ≤ 1 [/size][/font][font='宋体'][size=13px]参考文献[/size][/font][font='宋体'][size=13px]:[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]肖素荣,李京东.赤藓糖醇的特性及应用[J].中国食物与营养,2008(05):26-28.[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]刘建军,赵祥颖,田延军,韩延雷,张家祥.低热值甜昧剂——赤藓糖醇[J].食品与发酵工业,2007(09):132-135.[/size][/font][font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]3]尤新.尤新食品发酵论文选[/size][/font][font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]M].北京:中国轻工业出版社,2005.272[/size][/font][font='宋体'][size=13px]-[/size][/font][font='宋体'][size=13px]274[/size][/font][font='宋体'][size=13px][[/size][/font][font='宋体'][size=13px]4[/size][/font][font='宋体'][size=13px]]李树东,宋微,魏春红,曹龙奎.发酵法生产赤藓糖醇的研究综述[J].农产品加工(创新[/size][/font][font='宋体'][size=13px]版),2009(12):50-52.[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]刘建军,赵祥颖,田延军,韩延雷,张家祥,李丕武.低热值甜味剂赤藓糖醇的研究现状及应用[J].中国酿造,2006(12):1-3+16.[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]李俊霖,郭传庄,王松江,王建彬,隋松森.赤藓糖醇的特性及其应用研究进展[J].中国食品添加剂,2019,30(10):169-172.[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]?[/size][/font][font='宋体'][size=13px]GB 26404-2011, 食品安全国家标准 食品添加剂 赤藓糖醇[s].[/s][/size][/font]
不知道哪位朋友能弄到 牙膏中的二甘醇的检测 的国家标准呢?我目前只有美国FDA提供了牙膏中二甘醇的GC-MS检测http://www.gzflm.com/Chinese/NewsInfo.asp?Action=Co&ID=88谢谢拉
喷了几次了,总是出现筛子孔。孔经常先在样品边缘出现,然后才在中间出现,并且需要等待几十秒才能透光。。。这是怎么回事,求指点!还有就是束流用大的还是用小的?样品时变形态高纯镁(沿挤压方向压缩的纯镁挤压棒),圆片厚度50-60微米双喷液是5.3g氯化锂+11.16g高氯酸镁+100mL乙二醇丁醚+500mL甲醇双喷温度-55℃~-30℃(这个温度段的都试过),电压100v,电流50毫安左右
请问各位专家,[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法如何检测聚醚(分子量大于400)中戊二醇含量?戊二醇沸点约在200度,若采用顶空进样是不是很难气化;如采用溶剂稀释直接进样聚醚会不会残留在色谱柱中?
供试品溶液制备:取本品1g,精密称定,置顶空瓶中,精密加入超纯水1.0ml, 密封,摇匀,作为供试品溶液。环氧乙烷对照贮备液制备:量取环氧乙烷300μl(相当于0.25g环氧乙烷),置含50ml经过滤处理的聚乙二醇400(以60℃,1.5~2.5kPa旋转蒸发6小时,除去挥发性成分)的100ml量瓶中,加入相同溶剂稀释至刻度,摇匀,作为环氧乙烷对照品贮备液。环氧乙烷对照品溶液制备:精密称取1g冷的环氧乙烷对照品贮备液,置含40ml经过处理的聚乙二醇400的50ml量瓶中,加相同溶剂稀释至刻度。精密称取10g,置含30ml水的50ml量瓶中,加水稀释至刻度。精密量取10ml,置50ml量瓶中,加水稀释至刻度,摇匀,作为环氧乙烷对照品溶液。二氧六环对照品溶液制备:取二氧六环适量,精密称定,用水制成每1ml中含0.1mg的溶液,作为二氧六环对照品溶液。混合对照品溶液制备:精密称取本品1g,置顶空瓶中,精密加入0.5ml环氧乙烷对照品溶液及0.5ml二氧六环对照品溶液,密封,摇匀,作为对照品溶液。系统适用性试验溶液制备:量取0.5ml环氧乙烷对照品溶液置顶空瓶中,加入新鲜配制的0.001%乙醛溶液0.1ml及二氧六环对照品溶液0.1ml,密封,摇匀,作为系统适用性试验溶液。试验条件:照气相色谱法试验,以聚二甲基硅氧烷为固定液,起始温度为35℃,维持5分钟,以每分钟5℃的速率升温至180℃,然后以每分钟30℃的速率升温至230℃,维持5分钟(可根据具体情况调整)。进样口温度150℃,检测器温度250℃,顶空瓶温度70℃,平衡时间为45分钟。取系统适用性试验溶液顶空进样,调节检测器灵敏度使环氧乙烷峰和乙醛峰的峰高约为满量程的15%,乙醛峰和环氧乙烷峰之间的分离度不小于2.0,二氧六环峰高应为基线噪音的5倍以上,分别取供试品溶液及对照品溶液顶空进样,重复进样至少3次。环氧乙烷峰面积的相对标准偏差应不得过15%,二氧六环峰面积的相对标准偏差应不得过10%,按标准加入法计算,环氧乙烷不得过0.0001%,二氧六环不得过0.001%。问题1:“相同溶剂稀释至刻度“是指水吗?问题2:求组计算过程或者指点一下,多谢。实在搞不清楚标准加入法的计算过程,一些人说要扣什么,已经糊涂了,灰常感谢。好人好报
我们的一个产品用到乙二醇甲醚,需对产品中的乙二醇甲醚的残留进行控制。方法如下:色谱柱:DB-624进样口温度:200,检测器温度:300柱温 40保持4min,10/min升温至200保持7min流速:4.0ml/min分流比:1:1顶空条件顶空瓶平衡温度:140,定量环温度:150,传输线温度:160我们遇到的问题是:乙二醇甲醚在这种条件下的响应很低,500ppm的限度下峰面积为41.2,50ppm限度下无响应。而乙二醇甲醚在药典里规定的限度为50ppm请问,我们应该怎么改进条件来检测乙二醇甲醚残留?
专家,你好!我想请教,用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测甲醇,每升不超过0.4克,柱子直径0.25~0.18mm的二乙烯苯-乙基乙烯苯型高分子多孔小球作为载体。请问柱长应选多少?高分子小球的直径为多少?谢谢!
现在要做一项溶残检测,同时含二氯甲烷、异丙醇和乙腈,在DB-624(30m*320um*1.8um)柱上异丙醇和乙腈完全重叠,在HP-INNOWax(30m*320um*0.25um)柱上异丙醇和二氯甲烷的分离度很低(小于1.0)。现在是顶空进样方式,分流比5:1,调节了流速等其他参数,都不能达到理想的分离效果,请教各位同仁有没有能较好分离这三种溶剂的色谱条件,多谢!
2010版药典中辅料丙二醇增加了有关物质的气相检查,其中有杂质一缩二丙二醇、二缩三丙二醇,但据了解,这两种东西均为异构体混合物,我们买了杂质对照品(均为色谱标准品),一缩二丙二醇、二缩三丙二醇均出好几个峰,且有的峰不能完全分离不知怎么理解标准中对其控制的要求?有做过的同仁,望不吝赐教!
我司客户要求提供甲基丙二酸二乙酯和丙二酸二乙酯产品中乙醇含量的具体数据,所以急需乙醇含量测定方法和参数。气相色谱条件1. 列的名称2. 列长度3. 柱内径4. 薄膜厚度5. 进样口温度(进口温度)6. 检测器温度7. 烘箱温度程序8. 载气流量9. 线速度10.分流比11.进样量顶空条件(如有需要)Thermostating时间Thermostation温度(顶空烤箱温度)循环温度(注射器,注射温度)传输线温度加压时间循环填充时间注射时间循环平衡时间矩阵沸点GC周期时间肯请各位高手不吝赐教,谢谢