请问如何分离乙醇、丙酮、异丙醇(样品由以上三者组成,且三者的质量百分数差不多)。我用毛细柱,试了很多不同的载气流量和不同的柱温,进样温度,检测器温度也没能分离好,只出现一个大的平顶峰。请问有哪位前辈可以为我提供分离条件。谢谢!
请问如何分离乙醇、丙酮、异丙醇(样品由以上三者组成,且三者的质量百分数差不多)。我用毛细柱,试了很多不同的载气流量和不同的柱温,进样温度,检测器温度也没能分离好,只出现一个大的平顶峰。请问有哪位前辈可以为我提供分离条件。谢谢!我用的是Elite 5MS的柱子。一定要用PEG20M(Carbowax20M)毛细柱才可分离吗?
用Fid检测器氯仿和甲醇,乙醇,丙酮,乙腈的出峰顺序是怎样的啊
求[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]中以下校正因子:水-乙醇 水-甲醇 水-丙酮 正丁醇-乙醇 正丁醇-甲醇 正丁醇-丙酮还有乙醇、甲醇、丙酮、正丁醇的密度表~~谢谢
各位老师好:请问,老师有检测过药物中异丙叉丙酮和二丙酮醇痕量残留的分析的经验么?请指教。谢谢
有谁用HP-INNOWAN色谱柱,FID检测器测定精甲醇中微量乙醇、丙酮含量?详细参数是什么,最好传个谱图上来,谢谢!
甲醇水为流动相一切正常;加上乙腈就出问题,泵压也出现规律性的波动,227nm紫外检测器也总是出规律性的峰;一开始以为是柱子问题,用甲醇水冲洗后一切正常,换流动相后,就是甲醇乙腈水三相为流动相时,又开始泵压和紫外检测器都是规律性的峰,这是怎么回事呢?在线过滤器超声过了 ,乙腈换了新的一瓶还是一样~~~是管路?该怎么清洗呢???
我们有发酵液,内含有丙酮、正丁醇、乙醇如何分离,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]参考条件
SOS!SOS!……测定卵磷脂中的丙酮和乙醇残留量,丙酮、乙醇中的水分.GC-FID和TCD顶空进样器HP-WAX测定丙酮和乙醇残留量30×0.32×0.5,我的检测限是10PPM,这个柱子行吗?两个不性的化,应该用个什么样的规格?Porapak Q柱子和GDX-102是一样的填料吧,都是高分子小球,测定水分可以吧,用2×4的可以吧[em0812] [em0812] [em0813] [em0813]
实验室要分离 丙酮 异丙醇 异丙醚 戊醇 水还有一些醇类杂志求推荐柱子我自己查了一下用安捷伦 115-2132 不知道行不行通常选柱子有啥依据没有啊谢谢!!!
[color=#444444]最近在做苯乙酮和1-苯乙醇的化学实验,想用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行分析,结果发现两个的沸点相差很近,请问这种情况下应该怎么样进行测试,[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的操作应该注意什么,苯乙酮的沸点是202.3度,1-苯乙醇的是203.4度,谢谢大家[/color]
请教各位大虾:液相色谱中为什么不用乙醇取代甲醇作常规溶剂?还有,丙酮与各溶剂的互溶性也很好,可为什么正反相交替的时候我们通常选择异丙醇却不用丙酮?
要测吡啶\丙酮\乙醇\DMF\乙二醇应选哪种型号色谱柱?
初步调研市售纯牛奶雌二醇(E2)和孕酮(P4)含量现状。方法:收集同季节6 个品牌(A、B、C、D、E 和F 品牌,各品牌随机采集6 个批号)共36 个批号市售纯牛奶,采用免疫化学发光分析法检测经硫酸酯酶水解的乳清总E2(TE2)和P4。结果:6 个品牌乳清TE2 差异无统计学意义;F 品牌乳清P4 高于C 品牌(P < 0.05),其余各品牌间差异均无统计学意义。36 个批号中,乳清TE2 和P4 最大值与最小值之比分别为2.32 和6.67。A、B、C、D、E 和F 品牌批号间乳清TE2 的最大值与最小值之比分别为1.38、1.60、1.82、1.79、2.17 和1.68,其P4的最大值与最小值之比分别为3.19、5.98、2.89、1.38、1.86 和1.67。6 个品牌的乳清TE2 和P4 均值的最大值与最小值之比分别为1.25 和3.05。结论:市售纯牛奶品牌间乳清P4 存在差异,且同品牌不同批号波动较大;批号间乳清TE2 也有一定差异。
不知道各位有没有人做过异丙基托品醇这种物质的检测,异丙基托品酮为异丙基托品醇的已知杂质,两者结构比较相近,在气相条件下难分离,在薄层条件也做过一次,两种物质比较难实现分离。忘各位能够提供一些实验方向能使两者实现分离。
研究表明,当流动相的A0.7的时候,基线噪声会显著增加,一般选择的吸收值0.5。当A1.0时,基本就不能用使了。对于示差折光检测器,主要考虑样品和流动相的折光率,这里不 再赘述。选用的溶剂粘度要低、沸点适中使用低粘度溶剂,可减小容质的传质阻力,降低柱压,利于提高柱效。从分离制备和色质连用考虑,沸点要适中,低沸点的溶剂有它的优点;但仅仅用 于分析,沸点太低,反而由于溶剂的挥发,造成保留时间的变化。尽量不用高毒性的溶剂不只是环境,单从我们自身的安全考虑,当然用低毒溶剂最好。溶剂对样品有足够的溶解力样品如果不能溶解在选用的溶剂里,还怎么分析?但如果样品在流动相里溶剂仍然不大,可以用样品的最佳溶剂先溶解,再用流动相稀释,就 可以了。知道了上面选择溶剂的一般原则,就不难理解为什么不同乙醇、丙醇做流动相的原因了,因 为它们的粘度大。 还有丙酮,虽然粘度和毒性较低、溶解度大、极性适中,但用于它的截至吸收波长为330nm, 所以不常用,如果样品的吸收大于330nm,其实用丙酮是一个不错的选择。
实验室做丁酮烯醇钠中间体检测,实验室用GC测试,乙醇做溶剂,丙酮的出峰时间和乙醇的太接近了,完全分离不出来,有啥好办法没?需要换溶剂吗?
测微生物代谢产物 甲醇、甲酸、丙酮酸、乳酸、乙酸、乙醇可以用什么检测?实验室有[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]、GC-MS。 测这些物质标曲怎么做了?浓度大概ppm级。标液溶剂一般是甲醇,那么我的甲醇又该如何检测了? 拜托各位前辈了
求助各位大神和老师,去哦长期以来被六通阀问题所困扰。我的气路有两路,一路是纯N2,一路是由N2配制的甲苯混合气,当我由纯载气切换至混合气时,会有一个向上凸起的峰,而当我由混合气切换至纯载气时,又会有一个向下的倒峰。我知道是两路气压不平衡所导致的,但是我想请问的是当出现向上的峰是纯载气的压力大还是混合气的压力大呢?并且有没有可能是空气流量太大导致切阀波动比较大?因为上次工程师来调过氢空比后就出现了这样的问题。下图是我实验中出现的部分问题图。[img=,690,310]https://ng1.17img.cn/bbsfiles/images/2022/08/202208021612139811_2409_3520668_3.jpg!w690x310.jpg[/img]
我用GC做双丙酮醇做出来两个峰,其中一个是丙酮,如何判断双丙酮醇的含量,应该是将丙酮这个峰和另外一个峰加起来吧!但我不知道原因,有谁帮我解释一下。谢谢!
如题,检测化合物为多溴联苯醚,标品溶剂为异辛烷,前处理要求必须用乙醇或丙酮,不能用异辛烷或正己烷。就怕影响定性或是定量啊!求大家帮助!
请问分析丙酮及其中的乙醇,甲醇含量。用分光光度法应该怎么分析?
在一些香精里会见到丙酮醇 2-Propanone, 1-hydroxy-,请问是来自于哪里??是否来自于丙二醇呢?(查资料说丙二醇脱氢可以生成丙酮醇))附件数据的10.65min的峰 -
请问如何定量分析?二丙酮醇分解温度较低,请问要选用什么样的溶剂作内标物呢?另外我在单独进样二丙酮醇时,一直会出现两个峰,请问如何解决?我们公司二丙酮醇的供应商拿来的检测报告上面写着纯度为99.8%,有谁知道他们是如何测出来的,而且上面的谱图是一个峰.可是我怎么做都是两个峰,请问有更好的条件分离吗?谢谢...急!~~
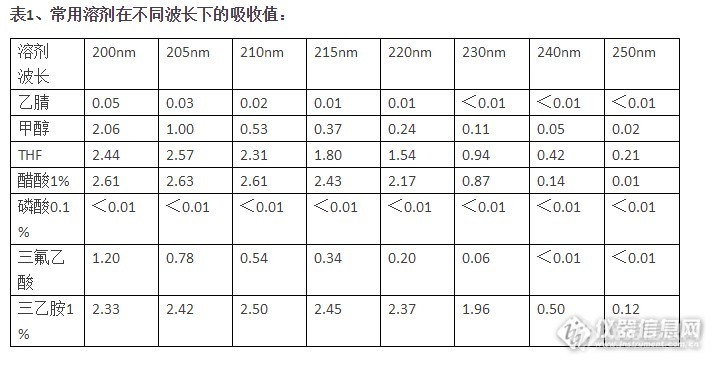
研究表明,当流动相的A0.7的时候,基线噪声会显著增加,一般选择的吸收值0.5。当A1.0时,基本就不能用使了。对于示差折光检测器,主要考虑样品和流动相的折光率,这里不 再赘述。选用的溶剂粘度要低、沸点适中使用低粘度溶剂,可减小容质的传质阻力,降低柱压,利于提高柱效。从分离制备和色质连用考虑,沸点要适中,低沸点的溶剂有它的优点;但仅仅用 于分析,沸点太低,反而由于溶剂的挥发,造成保留时间的变化。尽量不用高毒性的溶剂不只是环境,单从我们自身的安全考虑,当然用低毒溶剂最好。溶剂对样品有足够的溶解力样品如果不能溶解在选用的溶剂里,还怎么分析?但如果样品在流动相里溶剂仍然不大,可以用样品的最佳溶剂先溶解,再用流动相稀释,就 可以了。知道了上面选择溶剂的一般原则,就不难理解为什么不同乙醇、丙醇做流动相的原因了,因 为它们的粘度大。 还有丙酮,虽然粘度和毒性较低、溶解度大、极性适中,但用于它的截至吸收波长为330nm, 所以不常用,如果样品的吸收大于330nm,其实用丙酮是一个不错的选择。http://ng1.17img.cn/bbsfiles/images/2015/12/201512011315_575751_1858651_3.png
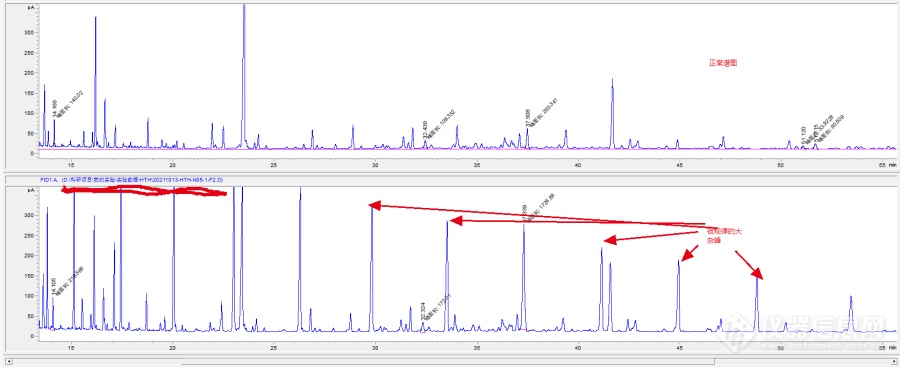
[img=[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]谱图,升温80-200-250-300-315度,检测器300°,690,281]https://ng1.17img.cn/bbsfiles/images/2021/11/202111031013369374_9410_5406430_3.png!w690x281.jpg[/img]如上图所示,萃取样品方法使用生物标志物法,空白实验无杂峰,样品实验如图中所示,有较大的杂峰,不知何原因,请各位大佬指教一二。思考如下:1.空白实验和样品实验除一个加样品,一个不加样品外,其他操作步骤均相同,样品瓶、试剂、量取仪器均同一套,如是污染的问题,但空白没污染2.这个样品之前也做过几次,均没有大杂峰出现,且是在一个样品袋里的样品,可能是样品本身的问题3.整个实验过程中,除萃取甲藻甾醇和烯酮组分,还萃取了烷烃组分,本次萃取的烷烃组分无异常。萃取顺序:先烷烃后甲藻甾醇和烯酮,如是样品问题,烷烃组分却没有异常4.此样品在仪器上测试两遍,中间间隔一周,测试结果相同。如是仪器问题,间隔一周中其他人使用该仪器无异常
有关苯乙酮的性质如下外观与性状:无色或淡黄色低熔点、低挥发性、有水果香味的固体。熔点(℃):19.7,相对密度(水=1):1.03(20℃),沸点(℃):202.3这么低熔点的物质在室温下(如现在20°左右)基本都是液体了,那么怎么配置30ug/ml的甲醇溶液呢?如何称量?如果用量筒,又怎么计算啊?
(1)饮用纯净水要适度。纯净水pH值呈弱酸性,而人体大多适宜喝呈弱碱性的水,老人、儿童及婴幼儿尤其不宜将纯净水作为通常饮用水大量、长期饮用,纯净水应与矿泉水交替着喝。 (2)定期全面地清洗、消毒饮水机。最好由专业清洗人员来清洗,冬季三个月一次,夏季一个半月一次。因为桶装水放入饮水机就与饮水机储水池和室内空[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]通,若饮水机本身污染,杂菌或绿苔就会进入大桶内。即使是合格的矿泉水、山泉水,进入杂菌后,在阳光和温度作用下,经过一段时间就可能形成绿苔,造成水的二次污染。 (3)加快桶装水更换速度。桶装水启封后,应在一周内饮用完,且在3天后不再饮用凉水,而应煮沸后再饮用。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=92808]丙酮 乙醇 氨的物理性质[/url]
顶空进样器中残留乙醇、丙酮的去除方法?