我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
大家好。我想问一下。 我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC 的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
在解红外光谱时常分不出来胺基(酰胺基)是与苯环相连的。还是在苯环侧链上。
各位老师好,我现在遇到一个方法,里面采用三羟甲基氨基甲烷作为缓冲液,但是待测物本身是没有酸碱性的,其杂质也没有酸碱性,为什么还要用缓冲液作为流动相的水相,也还是这个三羟甲基氨基甲烷有其他的用途?
大家好。我想问一下。 我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
对氨基环己甲酸乙酯的液相可以分析吗?如果可以,该如何让选择流动相?http://www.instrument.com.cn/bbs/images/upfile/200832223417.pdf
看到一段不理解的描述:当化合物只有氨基时,缓冲体系的选择十分简单,大多数氨基化合物在PH值小于9时都被质子化,所以所有PH值在7或更低的溶液均适合应用。请问各位老师,只有氨基的化合物是碱性化合物,ph不应该选碱性?使物质以分子形式存在更易分析?
我以前ph=6的缓冲流动相做这个系列的化合物的时候,即使接近纯水,峰都难以分开,后来调到ph=3的流动相后分离差不不多了,但实验现象却有点让人不踏实。听说有氨基酸专用柱,请问是专门用来分离氨基酸系列的化合物还是指这种含有氨基羧基两性基团的化合物?
求助按照GB/T 5009.97-2003国家标准,用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]FID检测器测定环已基氨基磺酸钠,标曲点有反应,进样品后就没显示啊,添加回收点也没反应。我样品是白酒和植物饮料
各位高手,我想请教一下,测定食品中甜蜜素(环已基氨基磺酸钠)的毛细管柱;最好能 请提供样品(饮料、果汁、糕点)的前处理和色谱柱使用条件。谢谢了啊,在线等答复~~
大家好!我是个新手,我现在在做一个化学品——3-环已胺基丙胺的含量分析我用的是标准样品,可是我所采用的方法在我们公司的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]上打不出原有浓度,所以求助大家给点宝贵意见。谁能提供一下关于该化学品——3-环已胺基丙胺的含量分析方法
磺胺药物对氨基苯磺酰胺的合成目的原理Ar-NHCOCH3 + 2HOSO2Cl → p-ClO2S-Ar-NHCOCH3+ HClp-ClO2S-Ar-NHCOCH3 + NH3 → p-CH3CONH-Ar-SO2NH2 + HClp-CH3CONH-Ar-SO2NH2 + H2O → p-H2N-Ar-SO2NH2 + CH2CO2H仪器药品乙酰苯胺(自制) 5g(0.037mol);氯磺酸(d=1.77) 22.5g(12.5ml,0.19mol);浓氨水(28%,d=0.9) 35ml 浓盐酸,碳酸钠。过程步骤(1)对乙酰氨基苯碘酰氯在100ml干燥的锥形瓶中,加入5g干燥的乙酰苯胺,在石棉网上用小火加热熔化。瓶壁上若有少量水气凝结,应用干净的滤纸吸去。冷却使熔化物凝结成块。将锥形瓶置于冰浴中冷却后,迅速倒入12.5ml氯磺酸,立即塞上带有氯化氢导气管的塞子。反应很快发生,若反应过于激烈,可用冰水浴冷却。待反应缓和后,旋摇锥形瓶使固体全溶,然后再在温水浴中加热10~15min使反应完全。将反应瓶在冷水中充分冷却后,于通风中在充分搅拌下,将反应液慢慢倒入盛75g碎冰的烧杯,用少量冷水洗涤反应瓶,洗涤液倒入烧杯中。搅拌数分钟,并尽量将大块固体粉碎,使成颗粒小而均匀的白色固体。抽滤收集,用少量冷水洗涤,压干,立即进行下一步反应。(2)对乙酰氨基苯磺酰胺将上述粗产物移入烧杯中,在不断搅拌中慢慢加入17.5ml浓氨水(在通风橱内),立即发生放热反应并产生白色糊状物。加完后,继续搅拌15min,使反应完全。然后加入19ml水,在石棉网上用小火加热10~15min,并不断搅拌,以除去多余的氨,得到的混合物可直接用于下一步合成。(3)对氨基苯磺酰胺(磺胺)将上述反应物放入圆底烧瓶中,加入3.5ml浓盐酸,在石棉网上用小火加热回流0.5h。冷却后,应得一几乎澄清的溶液,若有固体析出,应继续加热,使反应完全。如溶液呈黄色,并有极少量固体存在时,需加入少量活性炭煮沸10min,过滤。将滤液转入大烧杯中,在搅拌下小心加入粉状碳酸钠至恰呈碱性(约4g)。在冰水浴中冷却,抽滤收集固体,用少量冰水洗涤,压干。粗产物用水重结晶(每克产物约须12ml水),产量3~4g。熔点161~162℃。纯品对氨基苯磺酰胺为白色针状结晶,熔点163~164℃。注意事项1.氯磺酸对皮肤和衣服有强烈的腐蚀性,暴露在空气中会冒出大量氯化氢气体,遇水会发生猛烈的放热反应,甚至爆炸,故取用时需加小心。反应中所用仪器及药品皆需十分干燥,含有氯磺酸的废液不可倒入水槽,而应倒入废液缸中。工业氯磺酸常呈棕黑色,使用前宜用磨口仪器蒸馏纯化,收集148~150℃的馏分。2.酰磺酸于乙酰苯胺的反应非常剧烈,将乙酰苯胺凝结成快状,可使反应缓和进行,当反应过于激烈时,应适当冷却。3.在氯磺化过程中,将有大量氯化氢气体放出。为避免污染室内空气,装置应严密,导气管的末端要与接受器内的水面接近,但不能插入水中,否则可能倒吸而引严重事故!4.加入速度必须缓慢,必须充分搅拌,以免局部过热而使对乙酰胺基苯磺酰胺水解。这是实验成功的关键。5.尽量洗去固体所夹杂和吸附的盐酸,否则产物在酸性介质中放置过久,会很快水解,因此在洗涤后,应尽量压干,且在1~2h内将它转变为磺胺类化合物。6.粗制的对氨基苯磺酰氯久置容易分解,甚至干燥后也不可避免。若要得到纯品,可将粗产物溶于温热的氯仿中,然后迅速转移到事先温热的分液漏斗中,分出氯仿层,在冰水浴中冷却后即可析出晶体。纯品对氨基苯磺酰氯的熔点为149℃。7.为了节省时间,这一步的粗产物可不必分出。若要得到产品,可在冰水浴中冷却,抽滤,用冰水洗涤,干燥即可。粗品用水重结晶,纯品熔点为219~220℃。8.对乙酰胺基苯磺酰胺在稀酸中水解成磺胺,后者又与过量的盐酸形成水溶性的盐酸盐,所以水解完成后,反应液冷却时应无晶体析出。由于水解前溶液中氨的含量不同,加3.5ml盐酸有时不够,因此,在回流至固体全部消失前,应测一下溶液的酸碱性,若酸性不够,应补加盐酸回流一段时间。9.用碳酸钠中和滤液中的盐酸时,有二氧化碳产生,故应控制加热速度并不断搅拌使其逸出。磺胺是一两性化合物,在过量的碱溶液中也易变成盐类而溶解。故中和操作必须仔细进行,以免降低产量。分析思考 1.为什么在氯磺化反应完成以后处理反应混合物时,必须移到通风橱中,且在充分搅拌下缓缓倒入碎冰中?若在未倒完前冰就化完了,是否应补加冰块?为什么?2.为什么苯胺要乙酰化后在氯磺化?直接氯磺化行吗?3 .如何理解对氨基苯磺酰氨是两性物质?试用反应式表示磺胺与稀酸和稀碱的作用。
用氨基酸自动分析仪测定氨基酸含量,配制不同pH的柠檬酸钠缓冲液的作用是什么?是淋洗不同的氨基酸?如果用732阳离子树脂吸附氨基酸,用氨水来淋洗,测定氨基酸总量,原理上可行吗?谢谢!
一种含有苯胺基团和氮杂环结构的化合物,在HPLC测定纯度时存在一些疑问,希望行家能给予一些指教:这种化合物如果用甲醇/水:70/30流动相测定,纯度为94%(90/10也可,但保留时间太短);而如果用甲醇/水:90/10,用磷酸和氨水调节pH值到3.1左右作为流动相,测定的纯度变为60%左右。测了一下这个化合物的甲醇/水溶液的pH值为6.7左右,个人认为在这种情况下前一种方法更为准确,因为后一种方法会导致样品的不完全质子化,产生多峰。以上是实验现象和个人的想法,不知道是否正确,现在正对采用哪种方法非常的困惑,希望得到经验丰富人士的意见,谢谢。
现在合成一个化合物 萘环左边环有一个磺酸基,右边环1位是酚羟基 2位是氨基,对这个化合物液相分析,流动相PH4,出现两个峰,固体样品溶解后进样 前面峰是主要的峰,但是样品放了一会后再进样 就变成后面是主要的峰了,请问这两个峰都是我的产物么,这个化合物本身会有离子分子间转换么 ,查到有苯类带磺酸基和氨基说会形成内盐。
(2S,3S)-3-氨基-2-甲基-4-氧代氮杂环丁烷-1-磺酸(2S,3S)-3-amino-2-methyl-4-oxoazetidine-1-sulfonic acid谁有这个液相的检测纯度的方法,是氨曲南的起始物料N-氮杂环丁烷???
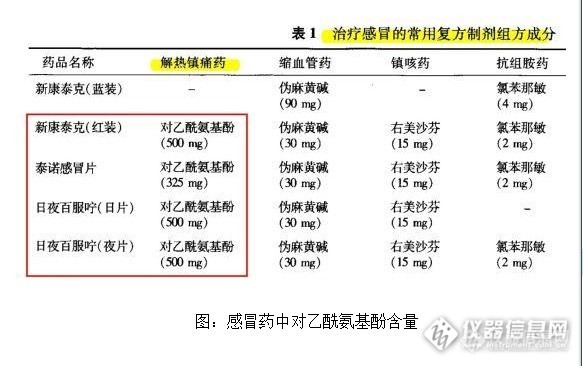
点击查看FDA声明原文 FDA警告,过量服用对乙酰氨基酚药物将会导致肝功能衰竭甚至死亡,高危人群包括在24小时内服用超过处方规定剂量药物的患者,同时服用超过一种含对乙酰氨基酚成分药物的患者,以及在服用含对乙酰氨基酚成分药物时饮用含酒精饮料的患者。 FDA自2011年起开始要求制药企业将对乙酰氨基酚的含量控制在每单位325毫克以内,但截止至2014年1月14日,市场上仍有部分单位对乙酰氨基酚含量超过325毫克的药物正在流通销售。 FDA表示,将在近期启动相关法律程序,禁止开具每单位对乙酰氨基酚含量超过325毫克的药物处方。 国内康泰克、百服宁等超标近54% 调查发现,国内多家知名品牌感冒药的对乙酰氨基酚含量高于每单位325毫克,包括新康泰克、百服宁等。 中美史克生产的新康泰克美扑伪麻片(红装),其每片对乙酰氨基酚含量同样是500毫克。 上海施贵宝制药有限公司生产的日夜百服咛、加合百服宁的每单位对乙酰氨基酚含量为500毫克,超出美国FDA规定含量上限54%。 此外,有多个品牌感冒药的单位对乙酰氨基酚含量达到美FDA规定的上限325毫克,它们分别是:白加黑、泰诺、银得菲。 其他品牌如快克、感康、康必得等单位对乙酰氨基酚含量在250毫克以内。 走访沪上多家药房后发现,最为常见的白加黑、新康泰克等感冒药均为处方药,需要处方及身份证才能购买。 大量非处方药含对乙酰氨基酚 不过,一药房工作人员提醒道,前述感冒药被转为处方药管理,并非缘于对乙酰氨基酚的过量,而是系其含有伪麻黄碱的缘故。 事实上,由于良好的镇痛祛热疗效,对乙酰氨基酚药物使用普及度很高,国内亦将其列为非处方药(OTC),即不需要持有医生处方即能买到,同时也能通过网络合法销售。 搜索淘宝等线上商城后发现,在网上不仅可以随意买到各种各样品牌的对乙酰氨基酚药品,而且购买数量亦完全没有限制。 沪上一医药销售人员表示,由于在各种药物中使用广泛,以及非处方药可以任意购买的缘故,患者容易同时购买多种含有对乙酰氨基酚的药物,导致患者在不知情的情况下过量服用。 根据FDA统计,在1998年至2003年间,对乙酰氨基酚过量服用是导致病人肝衰竭的主要原因。美国疾病控制中心在2007年也曾经发布报告称,全美每年有1600起急性肝功能衰竭,其中对乙酰氨基酚过量服用是最大缘由。 该销售人员解释道,美FDA长期以来都对药物中对乙酰氨基酚的含量作出规定,但因为非处方药的关系,仍有大量患者过量服用,所以FDA将对乙酰氨基酚的含量限制在325毫克以内,也是为了在不影响疗效的情况下尽可能的让患者减少服用,降低副作用。 FDA在此次声明中亦表示,将采取新的行动针对对乙酰氨基酚类的非处方药进行监管。 小知识:对乙酰氨基酚(扑热息痛) 对乙酰氨基酚是乙酰苯胺类解热镇痛药,别名有乙酰氨基酚、扑热息痛、醋氨酚、退热净等。该药具有解热镇痛作用,主要用于缓解轻、中度的疼痛,如关节痛、头痛、神经痛、牙痛及痛经等。 作为非处方药,虽然有质量稳定,疗效确切的优点,但该药的滥用,使用不当也会产生不良反应或严重的肝毒性和肾毒性。 此药对肝损害是最主要的不良反应,其次是引起肾衰,此外也可能导致血小板减少、哮喘发作等症状。 在无其他药物或无酒精干扰情况下,对乙酰氨基酚的安全剂量为:成人口服每次300-600毫克,最大日剂量不超过4000毫克,退热疗程不宜超过3天,镇痛疗程不宜超过5天。儿童12岁以下按体重每次10-15mg/kg,疗程不宜超过3天。 若患者饮酒或空腹或与其他药物有相互作用的药物合用时,应调低剂量或禁用。
用氨基柱做糖类化合物,加什么可以减轻拖尾,流动相是:乙氰:磷酸盐缓冲液。现在的情况是拖尾还是严重啊。怎么办呢?还有就是如何快速平衡色谱柱呢?
我们有个化合物,主框架是苯环,侧链是有酸,还有个氨基,像氨基酸,极性很大,90%的乙腈很快就出峰了,我是试过ph值为3.8和6.6的缓冲盐,峰形不似很好,想请问个为这种情况怎么办?如何选择缓冲盐,如何选择pH大小,
空气中五氯酚及其钠盐的测定方法 4-氨基安替比林比色法 1 原理五氯酚(钠)在酸性溶液中,在有氧化剂存在下,与4-氨基安替比林作用,生成蓝色安替比林染料,用二甲苯提取后,比色定量。2 仪器2.1 冲击式吸收管。2.2 抽气机。2.3 流量计,0~5L/min。 2.4 具塞比色管,10ml。2.5 pH计。2.6 分光光度计,5mm比色杯。3 试剂3.1 吸收液:五氯酚用0.006mol/L氢氧化钠溶液作吸收液。五氯酚钠用水作吸收液。3.2 柠檬酸盐缓冲溶液(pH5.6)。3.2.1 柠檬酸二钠溶液,0.1mol/L:称取21.0g柠檬酸(C6H8O7H2O)溶于200ml 1mol/L氢氧化钠溶液中,加水至1L。3.2.2 氢氧化钠溶液,0.1mol/L。3.2.3 量取69.3ml柠檬酸二钠溶液(3.2.1),加入30.7ml氢氧化钠溶液(3.2.2)配成pH值为5.6的缓冲溶液,用pH计测量并校正。3.3 4-氨基安替比林溶液,4g/L。3.4 铁氰化钾溶液,100g/L。3.5 二甲苯。3.6 标准溶液:称取五氯酚1.0000g,用100ml 0.6mol/L氢氧化钠溶液溶解,移入1000ml量瓶中,加水至刻度,此溶液1ml=1.0mg五氯酚,是为贮备液,贮于棕色瓶内。临用时量取10ml贮备液,用水稀释至100ml,配成1ml=100微克五氯酚的标准溶液。五氯酚钠标准溶液以水为溶剂配制。4 采样串联两个各装有10ml吸收液的冲击式吸收管,以3L/min的速度抽取75L空气。5 分析步骤5.1 对照试验:同采样,将吸收管装好吸收液带至现场,但不抽取空气,照样品分析。5.2 样品处理:用吸收管中的吸收液洗涤进气管内壁3次,从每个吸收管中分别量取5.0ml样品溶液于比色管中。5.3 标准曲线的绘制:按表72配制标准管。表72 五氯酚标准管的配制如测定五氯酚钠,则用五氯酚钠标准溶液,按上表配制。向标准管中各加入2ml柠檬酸盐缓冲溶液(3.2),0.25ml4-氨基安替比林溶液(3.3),摇匀,再加入0.25ml铁氰化钾溶液(3.4),摇匀,立即用2ml二甲苯(3.5)提取(加铁氰化钾与二甲苯间隔时间不超过30S),剧烈振摇100次,静置分层后,将二甲苯提取液放入5mm比色杯中,以二甲苯为对照,于波长580nm处比色,以五氯酚含量对吸光度作图,绘制标准曲线。5.4 测定:样品管操作同标准管,比色后由标准曲线上查出五氯酚的含量。6 计算X=2(C1+C2)/V0式中:X——空气中五氯酚(钠)的浓度,mg/m3;C1、C2——分别为第1、第2吸收管所取样品溶液中五氯酚(钠)含量,微克;V0——标准状况下的样品体积,L。7 说明7.1 本法的检测限为10微克/5ml。7.2 五氯酚-安替比林蓝色染料在二甲苯中可稳定1h,1h后吸光度有下降趋势,故应在1h内比色。7.3 五氯酚-安替比林蓝色染料在水溶液中极不稳定,显色30s后,吸光度即开始下降,故加入铁氰化钾溶液后应在30s内用二甲苯提取。7.4 温度对显色反应有影响,温度越高,吸光度下降幅度越大,因此要求配制标准管与样品管时的温差越小越好,最好不超过3~5℃。7.5 五氯酚贮备液于冰箱内可保存1个月。7.6 4-氨基安替比林溶液与铁氰化钾溶液于冰箱中保存可使用1周。7.7 酚对测定有干扰。当空气中酚与五氯酚(钠)浓度比在20∶1以下,样品管中酚含量在500微克以下时,改用pH4.2缓冲溶液(61.2ml 0.1mol/L柠檬酸二钠溶液与38.8ml 0.1mol/L盐酸溶液混合,用pH计测量并校正)可消除酚的干扰。超过此限量则干扰测定。
氨基柱是同时可以用于正相条件和反相条件的,但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻烦。对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。 过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。☆ 柱效检测:这是判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。流动相:10%乙酸乙酯+90%正己烷流速1.0标准溶液:乙苯(如乙苯找不到就用甲苯代替呗)+苯甲酸甲酯检测波长254nm这个方法特别适用于新购柱子(新购柱子往往保存在正相溶剂中)时即进行检测,也适合在柱子在准备放置相当长一段时间之前进行充分清洗后进行检测作为记录留档。在平常的使用过程中,如果分析物是固定重复的,我们当然可以从对分析物的分离分析情况来作出判断;但如果分析物和分析条件不同时,定期检测柱效可以避免柱效下降导致分离不佳再分析查找原因这样浪费人力物力的过程。不过特别要注意的是,当氨基柱(或氰基柱)在反相条件中使用时,如用该条件检测,请注意流动相的换相过渡问题。 ☆ 氨基柱的使用:需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5-10倍的柱体积的含0.5-1.0%NH3的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。☆ 氨基柱的清洗:简单说起来,正相条件下使用的氨基柱你就参照硅胶柱的清洗方法;反相条件下使用的氨基柱你就参照C18的清洗方法。※ 平时在正相条件下使用:首先用50倍柱体积的异丙醇清洗,因异丙醇粘度较大可适当放低流速;之后,用50倍的甲醇清洗;之后,用异丙醇过渡回到平常使用的正相流动相,即可。※ 平时在反相条件下使用:缓冲盐应及时冲洗,以及不能直接用纯甲醇冲洗缓冲盐等,属常识就不作特别交待了。用50倍纯甲醇冲洗;之后,用异丙醇过渡后,用二氯甲烷冲洗色谱柱;之后,再用异丙醇过渡回来到甲醇条件下。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等。
基质为聚合物的氨基柱有哪些品牌?
今天做对乙酰氨基酚,20ul定量环,进样60ul,出峰有严重的前延峰.但进样16\10ul,峰形良好. 反复测试了都这样? 难道进样体积能影响这么大?也就相差几ul啊?
试剂氨基钠的制备近白色或浅灰色固体。性质与氢氧化钠相似,是一碱性试剂。常用于脱卤化氢制备烯或炔类化合物,也可以用于Claise反应。久贮不当会大大影响活性,特别是氨基钠变成黄色或棕色后,表示已经有氧化物生成,可能发生爆炸。遇到此情况可用苯或甲苯将其覆盖,慢慢加入稀醇予以销毁。因此,氨基钠应该用时制备,不要久贮。在贮存或使用时,应注意防水,因遇水可引起爆炸。 制备方法如下: 取一500mL三口瓶,分别安装搅拌、导气管和带有钠石灰干燥管的冷凝管,导气管上接氢氧化钠干燥塔,再与氨气钢瓶连接。外用干冰和丙酮冷却,通入氨气使其冷却为液体氨,待液体氨达200mL时(大约为瓶的0.5体积,在反应过程中,要经常补加一些液体氨),取去导气管,瓶口用塞子塞住,并将干冰浴中的干冰换以木屑。加入0.2g硝酸铁。再取10g洁净的金属钠切成小块,在缓慢搅拌下,每次用铁丝刺一小块钠直接加入液体氨中。待钠全部作用,溶液由蓝变灰后,再加入另一小块钠。直到钠全部加完,并完全成氨基钠后(即由蓝溶液变为灰色悬浮物),反应即告完成。可直接用于下步反应。 如果氨基钠用于其他溶剂中反应,可将溶剂加入液氨中,让氨气挥发,最后在水浴中加热,逐渐除去残留的氨气。 整个制备的实验,应该在通风橱中进行。
[align=center][size=21px]氨基糖苷[/size][size=21px]类药物检测国内标准比较解读[/size][/align][size=18px]氨基糖苷类[/size][size=18px]药物[/size][size=18px]是一类抑制革兰氏阴性菌的抗生素,其[/size][size=18px]分子结构[/size][size=18px]中含有氨基糖苷键和氨基环己醇,[/size][size=18px]本身不具有发色基团,只有通过与衍生试剂反应才能用紫外或荧光检测,[/size][size=18px]由于其极性很强,分析时需要加离子对试剂才能在反相色谱柱上保留,可以使用高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法活[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱法检测,现将[/size][size=18px]国内[/size][size=18px]氨基糖苷类[/size][size=18px]药物相关[/size][size=18px]主要[/size][size=18px]检测方法标准[/size][size=18px]总结如下[/size][size=18px]:[/size][table][tr][td]序号[/td][td]标准名称[/td][td]检测原理[/td][td]药物数量、种类[/td][/tr][tr][td]1[/td][td]GB/T 21323-2007 动物组织中氨基糖苷类药物残留量的测定 高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱/质谱法[/td][td]试样用含0.4 mmol/L EDTA和2%三氯乙酸的磷酸盐缓冲溶液提取,经C18固相萃取柱净化,浓缩后使用七氟丁酸作为离子对试剂,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定。[/td][td]10 种:壮观霉素、潮霉素B、双氢链霉素、链霉素、丁胺卡那霉素、卡那霉素、安普霉素、妥布霉素、庆大霉素、新霉素[/td][/tr][tr][td]2[/td][td]GB/T 22995-2008 蜂蜜中链霉素、双氢链霉素和卡那霉素残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用 0.2 mol/L的磷酸盐缓冲溶液提取,用HLB和羧酸型固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定。[/td][td]3 种:链霉素、双氢链霉素、卡那霉素[/td][/tr][tr][td]3[/td][td]GB/T 21164-2007 蜂王浆中链霉素、双氢链霉素残留量测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法[/td][td]试样用庚烷磺酸钠-磷酸钠混合缓冲溶液提取,用C18固相萃取柱净化,高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]荧光法检测。[/td][td]2 种:链霉素、双氢链霉素[/td][/tr][tr][td]4[/td][td]GB/T 22945-2008 蜂王浆中链霉素、双氢链霉素和卡那霉素残留量的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用5%磷酸溶液提取,三氯乙酸沉淀蛋白,用苯磺酸型和羧酸型固相萃取小柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱测定。[/td][td]3 种:链霉素、双氢链霉素、卡那霉素[/td][/tr][tr][td]5[/td][td]农业部1077号公告-3-2008 水产品中链霉素残留量的测定 高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法[/td][td]试样5%三氟乙酸溶液提取,用C18固相萃取小柱净化,高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]荧光法检测。[/td][td]1 种:链霉素[/td][/tr][tr][td]6[/td][td]SN/T 1925-2007 进出口蜂产品中链霉素、双氢链霉素残留量的检测方法 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱法[/td][td]试样用pH=2的磷酸溶液提取,用阳离子交换柱和HLB固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱测定。[/td][td]2 种:链霉素、双氢链霉素[/td][/tr][tr][td]7[/td][td]SN/T 4778-2017 出口花粉中链霉素和双氢链霉素的测定方法 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱/质谱法[/td][td]用庚烷磺酸钠-磷酸钠混合缓冲溶液提取,三氯乙酸沉淀蛋白,用C18固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱测定。[/td][td]2 种:链霉素、双氢链霉素[/td][/tr][tr][td]8[/td][td]SN/T 5117-2019 进出口食用动物、饲料 链霉素类(链霉素、二氢链霉素)药物残留测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-质谱/质谱法[/td][td]试样用含0.4 mmol/L EDTA和2%三氯乙酸的磷酸二氢钾缓冲溶液提取,经HLB固相萃取柱净化,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-串联质谱仪测定,外标法定量。[/td][td]2 种:链霉素、双氢链霉素[/td][/tr][/table][size=18px]通过比较这些方法标准发现,由于氨基糖苷类药物极性强,水溶性好,一般用磷酸溶液等无机溶液提取;试样中的蛋白等杂质一般通过加入三氯乙酸及SPE法去除(HLB、C[/size][size=18px]18[/size][size=18px]小柱等)[/size][size=18px],[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]方法检测时要特别注意七氟丁酸等离子对试剂的使用,浓度不能过高,使用后要用大量水冲洗管路,否则出现残留后会对仪器灵敏度产生较大影响。[/size]
[font='Segoe UI'][color=#212529][font=Segoe UI]答:这是由氨基柱的特性造成的,因为氨基柱在分析糖类时,典型的流动相是[/font]60%~90%的乙腈水混合液,当在使用过程中,填料空隙处高浓度的氨基基团显碱性,导致硅胶和键合相缓慢的水解,随着时间的推移,脱落的键合相越来越多,就会导致目标物的保留时间发生变化,同时这也是氨基柱在反相条件下寿命变短的原因。[/color][/font]
氨基柱的使用和保养氨基柱是同时可以用于正相条件和反相条件的这一点很多用户都已经知道;但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。柱效检测:我用于判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,我可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。流动相:0%乙酸乙酯+90%正己烷 流速1.0标准溶液:乙苯(如乙苯找不动就用甲苯代替呗)+苯甲酸甲酯检测波长:254nm这个方法特别适用于新购柱子(新购柱子往往保存在正相溶剂中)时即进行检测,如有问题,可及时与供应商沟通。也适合在柱子在准备放置相当长一段时间之前进行充分清洗后进行检测作为记录留档。在平常的使用过程中,如果分析物是固定重复的,我们当然可以从对分析物的分离分析情况来作出判断;但如果分析物和分析条件不同时,定期检测柱效可以避免柱效下降导致分离不佳再分析查找原因这样浪费人力物力的过程。不过特别要注意的是,当氨基柱(或氰基柱)在反相条件中使用时,如用该条件检测,请注意流动相的换相过渡问题。 氨基柱的使用:需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5-10倍的柱体积的含0.5-1.0%NH3的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。氨基柱的清洗简单说起来,正相条件下使用的氨基柱你就参照硅胶柱的清洗方法;反相条件下使用的氨基柱你就参照C18的清洗方法。平时在正相条件下使用:首先用50倍柱体积的异丙醇清洗,因异丙醇粘度较大可适当放低流速;之后,用50倍的甲醇清洗;之后,用异丙醇过渡回到平常使用的正相流动相,即可。平时在反相条件下使用:缓冲盐应及时冲洗,以及不能直接用纯甲醇冲洗缓冲盐等,属常识就不作特别交待了。用50倍纯甲醇冲洗;之后,用异丙醇过渡后,用二氯甲烷冲洗色谱柱;之后,再用异丙醇过渡回来到甲醇条件下。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等Ultimate氨基柱的使用方法1.氨基柱既可以正相使用,也可以反相使用,但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,正常情况新氨基柱保存在正相环境中,例如LUNA 氨基柱保存在正己烷-乙腈(99:1)中。2. 正相使用2.1 新柱子可直接用流动相。推荐先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再根据流动相选用极性相近的氯仿或二氯甲烷以相同的流速冲10倍柱体积,最后换成流动相。2.2 正相使用时,不宜分析含醛基、羰基的化合物,不可用于还原糖的分析;流动相要彻底脱气,并不得含有羰基化合物和过氧化物(质量不好的乙醚、四氢呋喃含有少量)。2.3 任何时候更换流动相时都要确保新流动相与柱子原保存液可互溶。3 反相使用3.1 先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再依次以相同的流速相同的用量用氯仿、异丙醇、甲醇、甲醇-水(50:50)冲柱子。3.2 以0.5ml/min的流速用30倍柱体积的pH11.0的氢氧化钠(LUNA)水溶液冲柱子(注意pH值切不可超过11.0),立即用水(0.5ml/min的流速,30倍柱体积)冲洗,再换成流动相。3.3 配制流动相时,应各组分分别量取,比例较小的组分要精密量取,需调pH值时要精密到0.1。3.4 反相条件下使用时,要特别注意控制pH值范围,pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。最理想的pH范围在pH 3.0-7.03.5 如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。3.6 有一种情况是,当使用氨基柱进行酸性物质的分析时,酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。建议:用5-10倍的柱体积的含0.5-1.0%NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。4 色谱柱的冲洗:简单说起来,正相条件下使用的氨基柱就参照硅胶柱的清洗方法;反相条件下使用的氨基柱就参照C18的清洗方法。5 色谱柱的保存5.1 正相使用时,将柱子冲洗干净后,用正己烷-乙腈(99:1)保存。5.2 反相使用时,如短期不用,可用甲醇或乙腈保存;长期不用时需将甲醇依次用异丙醇、氯仿置换,最后用正己烷保存。6 色谱柱的再生6.1 方案1:依次用甲醇、异丙醇、氯仿、正己烷、氯仿、异丙醇、甲醇冲柱子(各以0.5ml/min的流速,20倍柱体积),再换流动相。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等。6.2 方案2:NH2柱用于反相条件时,NH2键会水解,尤其是在该柱子pH范围以外,在极端酸性和碱性条件下柱寿命会下降很快,如果在这个条件下使用需要清洗一下,需要用10倍柱体积溶液冲洗,如下:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水并保持95%乙腈/5%水继续冲洗,以低流速0.2-0.5mL/min过夜冲洗。6.3 方案3:柱子使用一定时间后,柱效下降,老化,也可清洗一下柱子恢复柱性能,清洗时依次用10倍柱体积的下列溶液冲洗:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水再走流动相即可
[em58] 本人做有机合成,通过2,4-二氨基苯甲醚的单酰化来合成2-氨基-4-乙酰氨基苯甲醚,但生成对位酰化物的同时,也形成邻位酰化物以及二酰化物,需要使用液相色谱方法进行分析,但尝试了甲醇,乙腈和水的不同配比流动相,始终无法将几个峰分开,上次根据一位大虾的建议尝试了乙腈与0.01M磷酸缓冲溶液的流动相,效果仍然不行,恳求各位大虾给与意见和方法,谢咯~~~~~~~!
氨基柱是同时可以用于正相条件和反相条件的这一点很多用户都已经知道;但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,对这一点的忽略可能会带给使用者一些麻烦。对于新购买到的柱子,首先请注意打开分析测试说明书,了解柱子的保存溶剂。如果保存溶剂与你将要使用的流动相极性不同不会互溶,请先用异丙醇过渡。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。柱效检测:我用于判断一个用户是否有经验的指标之一,是用户是否习惯配制一些柱效检测标准溶液。说到柱效检测,我可以向大家提供一个方法,而且很通用,你也可以用同样的标准溶液和流动相来检测硅胶柱和氰基柱。流动相:10%乙酸乙酯+90%正己烷 流速1.0标准溶液:乙苯(如乙苯找不动就用甲苯代替呗)+苯甲酸甲酯检测波长254nm这个方法特别适用于新购柱子(新购柱子往往保存在正相溶剂中)时即进行检测,如有问题,可及时与供应商沟通。也适合在柱子在准备放置相当长一段时间之前进行充分清洗后进行检测作为记录留档。在平常的使用过程中,如果分析物是固定重复的,我们当然可以从对分析物的分离分析情况来作出判断;但如果分析物和分析条件不同时,定期检测柱效可以避免柱效下降导致分离不佳再分析查找原因这样浪费人力物力的过程。不过特别要注意的是,当氨基柱(或氰基柱)在反相条件中使用时,如用该条件检测,请注意流动相的换相过渡问题。氨基柱的使用:需要注意的是,氨基柱的键合官能团氨丙基要比C18,C8柱的键合官能团C18,C8要容易水解,所以首先要做好其使用寿命稍逊的心理准备,特别是当你的使用条件是反相条件下时。反相条件下使用时,要特别注意控制PH值范围,PH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。所以,在使用后以及准备长时间放置该柱时,必要的清洗和将氨基柱保存于纯的有机溶剂中是很好的保养措施。有一种情况是,当使用氨基柱进行酸性物质如果汁的分析时(分析其中的糖份),酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。这时,Kromasil专家所给的建议是:用5-10倍的柱体积的含0.5- 1.0%NH3的50-50乙腈-水溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。氨基柱的清洗简单说起来,正相条件下使用的氨基柱你就参照硅胶柱的清洗方法;反相条件下使用的氨基柱你就参照C18的清洗方法。平时在正相条件下使用:首先用50倍柱体积的异丙醇清洗,因异丙醇粘度较大可适当放低流速;之后,用50倍的甲醇清洗;之后,用异丙醇过渡回到平常使用的正相流动相,即可。平时在反相条件下使用:缓冲盐应及时冲洗,以及不能直接用纯甲醇冲洗缓冲盐等,属常识就不作特别交待了。用50倍纯甲醇冲洗;之后,用异丙醇过渡后,用二氯甲烷冲洗色谱柱;之后,再用异丙醇过渡回来到甲醇条件下。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等LUNA氨基柱的使用方法1.氨基柱既可以正相使用,也可以反相使用,但是要注意到的是:正相溶剂和反相溶剂往往是不互溶的,正常情况新氨基柱保存在正相环境中,例如LUNA氨基柱保存在正己烷-乙腈(99:1)中。2. 正相使用2.1新柱子可直接用流动相。推荐先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再根据流动相选用极性相近的氯仿或二氯甲烷以相同的流速冲10倍柱体积,最后换成流动相。2.1正相使用时,不宜分析含醛基、羰基的化合物,不可用于还原糖的分析;流动相要彻底脱气,并不得含有羰基化合物和过氧化物(质量不好的乙醚、四氢呋喃含有少量)。2.3 任何时候更换流动相时都要确保新流动相与柱子原保存液可互溶。3 反相使用3.1先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再依次以相同的流速相同的用量用氯仿、异丙醇、甲醇、甲醇-水(50:50)冲柱子。3.2以0.5ml/min的流速用30倍柱体积的pH11.0的氢氧化钠(LUNA)水溶液冲柱子(注意pH值切不可超过11.0),立即用水(0.5ml/min的流速,30倍柱体积)冲洗,再换成流动相。3.3 配制流动相时,应各组分分别量取,比例较小的组分要精密量取,需调pH值时要精密到0.1。3.4反相条件下使用时,要特别注意控制pH值范围,pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。最理想的pH范围在pH3.0-7.03.5如果要使用的流动相中还含有缓冲盐类,建议在用分析流动相之前,先用不含缓冲盐的同比例流动相过渡,这样可避免缓冲盐在分析柱内的析出。3.6有一种情况是,当使用氨基柱进行酸性物质的分析时,酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。建议:用5-10倍的柱体积的含0.5-1.0%NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。4色谱柱的冲洗:简单说起来,正相条件下使用的氨基柱就参照硅胶柱的清洗方法;反相条件下使用的氨基柱就参照C18的清洗方法。5 色谱柱的保存5.1 正相使用时,将柱子冲洗干净后,用正己烷-乙腈(99:1)保存。5.2反相使用时,如短期不用,可用甲醇或乙腈保存;长期不用时需将甲醇依次用异丙醇、氯仿置换,最后用正己烷保存。6 色谱柱的再生6.1 方案1:依次用甲醇、异丙醇、氯仿、正己烷、氯仿、异丙醇、甲醇冲柱子(各以0.5ml/min的流速,20倍柱体积),再换流动相。这些清洗方法,主要是针对当样品中有杂质逐步吸附累积到填料上时的处理方法,色谱柱表现行为为诸如柱压增高柱效降低等。6.2方案2:NH2柱用于反相条件时,NH2键会水解,尤其是在该柱子pH范围以外,在极端酸性和碱性条件下柱寿命会下降很快,如果在这个条件下使用需要清洗一下,需要用10倍柱体积溶液冲洗,如下:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水并保持95%乙腈/5%水继续冲洗,以低流速0.2-0.5mL/min过夜冲洗。6.3方案3:柱子使用一定时间后,柱效下降,老化,也可清洗一下柱子恢复柱性能,清洗时依次用10倍柱体积的下列溶液冲洗:95%水/5%乙腈THF四氢呋喃95%乙腈/5%水再走流动相即可