卫办监督函〔2011〕561号各有关单位: 根据《食品安全法》及其实施条例的规定,我部组织制定了《食品添加剂 庚酸烯丙酯》等71项食品安全国家标准(征求意见稿)。现征求你部门意见并向社会公开征求意见(征求意见稿可从卫生部网站http://www.moh.gov.cn下载),请于2011年8月16日前以传真或电子邮件形式反馈我部。 传 真:010-67711813 电子信箱:gb2760@gmail.com. 二○一一年六月十四日 附件:《食品添加剂 庚酸烯丙酯》等71项食品安全国家标准(征求意见稿) 序号 标准名称 1 食品添加剂 庚酸烯丙酯 2 食品添加剂 苯甲醛 3 食品添加剂 月桂酸乙酯 4 食品添加剂 肉豆蔻酸乙酯 5 食品添加剂 乙酸香茅酯 6 食品添加剂 丁酸香叶酯 7 食品添加剂 乙酸丁酯 8 食品添加剂 乙酸己酯 9 食品添加剂 乙酸辛酯 10 食品添加剂 乙酸癸酯 11 食品添加剂 顺式-3-己烯-1-醇乙酸酯(又名乙酸叶醇酯) 12 食品添加剂 乙酸异丁酯 13 食品添加剂 丁酸戊酯 14 食品添加剂 丁酸己酯 15 食品添加剂 顺式-3-己烯醇丁酸酯(又名丁酸叶醇酯)[/siz
根据《食品安全法》规定,卫生部组织制(修)订了《食品添加剂 庚酸烯丙酯》等71项食品安全国家标准。但是,可乐使劲地搜,愣是没有搜到这71项标准http://simg.instrument.com.cn/bbs/images/brow/em09501.gif哪位童鞋有,有标准的赶紧上传啊,上传有大奖噢!http://ng1.17img.cn/bbsfiles/images/2011/06/201106221433_300960_0_3.jpghttp://ng1.17img.cn/bbsfiles/images/2011/06/201106221434_300961_0_3.jpghttp://ng1.17img.cn/bbsfiles/images/2011/06/201106221434_300963_0_3.jpg【奖励】:上传相关附件者每人视情况加2-20分! 针对标准提出意见者视情况另加2-20分!新闻链接:http://www.instrument.com.cn/news/20110621/063465.shtml
请问我用6890N[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url],柱子为FFAP测定小分子脂肪酸,但现在突然出现平头峰和叉峰(裂峰)是怎么回是呀?怎么才能解决?只有异丁酸\异戊酸\己酸\庚酸和2-乙基丁酸出现上述情况,而乙酸\丙酸\丁酸和琥珀酸等不会有上述现象.请教专家!!1谢谢你的赐教!!!
[color=#444444]看了很多文献的报道,使用[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]分析体液中未衍生化的氨基酸时,他们都使用离子对试剂全氟酸(例如全氟庚酸、全氟丁酸等),但是我现在希望不使用任何离子对试剂的帮助,通过反相液相色谱柱进行分离氨基酸,并通过质谱进行定性定量分析。我想问的问题就是我的方案的可行性有多大,有意义吗?(因为如果我的想法可行的话,国外为什么很多报道还是使用离子对试剂呢?)[/color][color=#444444]希望大家帮我多提宝贵意见,谢谢。[/color]
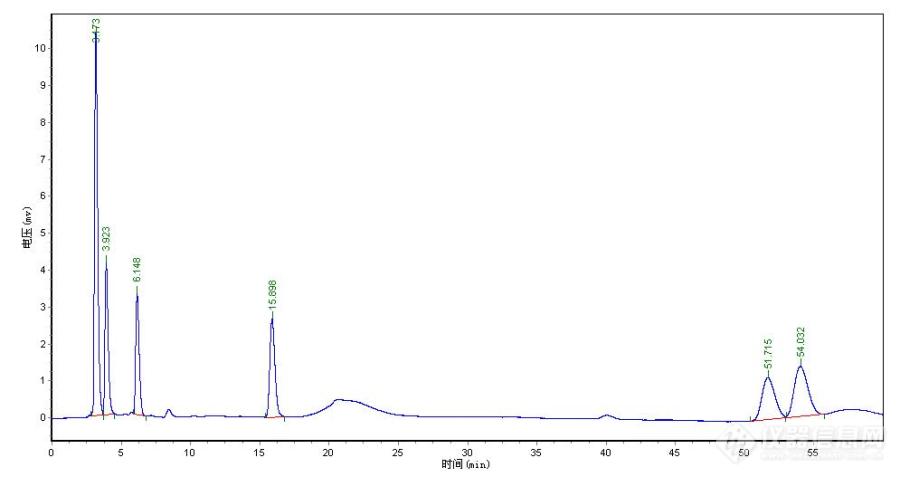
流动相用的是0.015mol/L 磷酸二氢钾 用磷酸调pH=2.5 和甲醇以 97:3 混合标准样用的是混标 十种酸 甲酸 乙酸 丙酸 异丁酸 丁酸 异戊酸 戊酸 异己酸 己酸 庚酸配的标准样浓度以乙酸记是100mg/L 现在出的图有六个峰 请问怎么确定哪种峰是对应的哪种物质?为什么有的酸没有峰?还有是不是有一种各种酸的出峰表可以对比的?[img=,690,365]https://ng1.17img.cn/bbsfiles/images/2019/09/201909291638034804_4574_1773263_3.jpg!w690x365.jpg[/img]
之前用庚酸做内标检测辛酸含量时,发现后进的样会受先进的样干扰。后来分别单独进辛酸和庚酸,发现辛酸里面会跑出庚酸的峰,庚酸里面会跑出辛酸的峰(都在1%左右),新开的辛酸、庚酸也是这样,基本可以排除辛酸庚酸被污染的可能。但是只进溶剂氯仿的话,不会有杂质峰。垫圈、衬管、柱子都换了新的,也没改善,不知道哪出了问题?
用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定辛酸钠含量色谱条件与系统适用性试验: 用酸改性聚乙二醇(20M)毛细管柱。注温160℃,火焰离子化检测器,检测器温度230℃,气化室温度230℃,载气(氮气)流速为每分钟35ml。辛酸峰与庚酸峰的分离度应大于1.5,辛酸峰的拖尾因子应为0.95~1.20。辛酸对照品溶液连续进样5次,所得辛酸峰与庚酸峰面积之比的相对标准偏差(RSD)应不大于5%。
GC,我用色谱柱TG-624 检测三乙胺、乙酸异丙酯和庚烷的混合样,分离总是不好。该如何调节?
以乙烷为溶剂的戊酸甲酯(2.0%),己酸甲酯(2.5%),庚酸甲酯(3.0%,辛酸甲酯(3.5)混合液共得到5个峰。可以用其中一种酯的保留时间减去溶剂保留时间来得到调整保留时间吗?

10,抽取5个版友);中奖名单:langyabeilei(注册ID:langyabeilei)zengzhengce163(注册ID:zengzhengce163)WUYUWUQIU(注册ID:wulin321)dahua1981(注册ID:dahua1981)999youran(注册ID:999youran)http://ng1.17img.cn/bbsfiles/images/2016/07/201607111533_600018_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/07/201607111533_600019_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================浓香型白酒分析方法:GC基质:标准溶液应用编号:101196化合物:乙醛; 丙醛; 异丁醛; 丙酮; 甲酸乙酯; 乙酸乙酯+ 乙缩醛; 甲醇; 2- 丁酮; 2- 甲基丁醛; 3- 甲基丁醛; 乙醇; 丙酸乙酯; 异丁酸乙酯; 二乙氧基异丁烷; 2- 戊酮; 仲丁醇; 丁酸乙酯; 正丙醇;. 异戊酸乙酯;二乙氧基-2- 甲基丁烷; 二乙氧基-3- 甲基丁烷; 异丁醇; 乙酸异戊酯; 仲戊醇; 戊酸乙酯; 正丁醇; 异戊醇; 己酸乙酯; 正戊醇; 3- 羟基丁酮; 己酸丙酯; 2- 庚醇;庚酸乙酯; 乳酸乙酯; 正己醇; 己酸丁酯; 辛酸乙酯; 乙酸;糠醛; 苯甲醛; 壬酸乙酯; 丙酸; 2.3- 丁二醇;( 左旋); 辛醇; 异丁酸; 2.3- 丁二醇;( 内消旋); 己酸己酯; 癸酸乙酯; 正丁酸; 异戊酸;正戊酸;正己酸; 苯丙酸乙酯; β- 苯乙; 庚酸; 十四酸乙酯; 辛酸; 棕榈酸乙酯; 油酸乙酯; 亚油酸乙酯固定相:DM-WAX色谱柱/前处理小柱:DM-WAX 30m x 0.25mm x 0.25um色谱条件:柱温:37 ℃ ( 2 min ) - 70 ℃, 3 ℃/min ;70 ℃ ( 1min) - 130 ℃, 6 ℃/min ;130 ℃- 220 ℃, 10 ℃/min ;220 ℃ ( 10 min ) 载气:高纯氮, 1mL/min 进样:260 ℃, 分流比30:1 检测:FID, 260 ℃文章出处:CFO00011关键字:白酒,食品,GC,DM-Wax, 乙醛; 丙醛; 异丁醛; 丙酮; 甲酸乙酯; 乙酸乙酯+ 乙缩醛; 甲醇; 2- 丁酮; 2- 甲基丁醛; 3- 甲基丁醛; 乙醇; 丙酸乙酯; 异丁酸乙酯; 二乙氧基异丁烷; 2- 戊酮; 仲丁醇; 丁酸乙酯; 正丙醇;. 异戊酸乙酯;二乙氧基-2- 甲基丁烷; 二乙氧基-3- 甲基丁烷; 异丁醇; 乙酸异戊酯; 仲戊醇; 戊酸乙酯; 正丁醇; 异戊醇; 己酸乙酯; 正戊醇; 3- 羟基丁酮; 己酸丙酯; 2- 庚醇;庚酸乙酯; 乳酸乙酯; 正己醇; 己酸丁酯; 辛酸乙谱图:http://www.dikma.com.cn/Public/Uploads/images/DM-Wax-1%20copy.png图例:1. 乙醛;2. 丙醛;3. 异丁醛;4. 丙酮;5. 甲酸乙酯;9. 乙酸乙酯+ 乙缩醛;10. 甲醇;11. 2- 丁酮;12. 2- 甲基丁醛;13. 3- 甲基丁醛;14. 乙醇;15. 丙酸乙酯;16. 异丁酸乙酯;17. 二乙氧基异丁烷;18. 2- 戊酮;19. 仲丁醇;20. 丁酸乙酯;21. 正丙醇;25. 异戊酸乙酯;26. 二乙氧基-2- 甲基丁烷;27. 二乙氧基-3- 甲基丁烷;29. 异丁醇;30. 乙酸异戊酯;31. 仲戊醇;32. 戊酸乙酯;33. 正丁醇;36. 异戊醇;38. 己酸乙酯;40. 正戊醇;41. 3- 羟基丁酮;43. 己酸丙酯;44. 2- 庚醇;45. 庚酸乙酯;46. 乳酸乙酯;47. 正己醇;48. 己酸丁酯;49. 辛酸乙酯;51. 乙酸;52. 糠醛;55. 苯甲醛;56. 壬酸乙酯;57. 丙酸;58. 2.3- 丁二醇;( 左旋);59. 辛醇;60. 异丁酸;61. 2.3- 丁二醇;( 内消旋);62. 己酸己酯;63. 癸酸乙酯;64. 正丁酸;65. 异戊酸;66. 正戊酸;68. 正己酸;69. 苯丙酸乙酯;70. β- 苯乙;71. 庚酸;74. 十四酸乙酯;76. 辛酸;79. 棕榈酸乙酯;85. 油酸乙酯;86. 亚油酸乙酯
做脂肪酸甲酯化,除了用正庚烷作为溶剂还可以用什么?环己烷可以吗?在线等,急急急!好友回复:考虑到毒性问题 使用正己烷正庚烷好一些,其实就是萃取 没必要用毒性很大的溶剂大家说说~
利用顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定甲乙丙丁戊5种醇,分别测试了下正戊烷、正庚烷、丙酮、乙酸乙酯都能够与这5种醇分开,乙酸乙酯我已经选来做稀释剂,其他三种合适做内标物质吗?
柱温:37 ºC ( 2 min ) - 70 ºC, 3ºC/min ;70 ºC ( 1min) - 130 ºC, 6ºC/min ;130 ºC - 220 ºC, 10 ºC/min ;220 ºC ( 10 min )载气:高纯氮, 1mL/min进样:260 ºC, 分流比30:1检测:FID, 260 ºChttp://www.dikma.com.cn/Public/Uploads/images/DM-Wax-1%20copy.png1. 乙醛;2. 丙醛;3. 异丁醛;4. 丙酮;5. 甲酸乙酯;9. 乙酸乙酯+ 乙缩醛;10. 甲醇;11. 2- 丁酮;12. 2- 甲基丁醛;13. 3- 甲基丁醛;14. 乙醇;15. 丙酸乙酯;16. 异丁酸乙酯;17. 二乙氧基异丁烷;18. 2- 戊酮;19. 仲丁醇;20. 丁酸乙酯;21. 正丙醇;25. 异戊酸乙酯;26. 二乙氧基-2- 甲基丁烷;27. 二乙氧基-3- 甲基丁烷;29. 异丁醇;30. 乙酸异戊酯;31. 仲戊醇;32. 戊酸乙酯;33. 正丁醇;36. 异戊醇;38. 己酸乙酯;40. 正戊醇;41. 3- 羟基丁酮;43. 己酸丙酯;44. 2- 庚醇;45. 庚酸乙酯;46. 乳酸乙酯;47. 正己醇;48. 己酸丁酯;49. 辛酸乙酯;51. 乙酸;52. 糠醛;55. 苯甲醛;56. 壬酸乙酯;57. 丙酸;58. 2.3- 丁二醇;( 左旋);59. 辛醇;60. 异丁酸;61. 2.3- 丁二醇;( 内消旋);62. 己酸己酯;63. 癸酸乙酯;64. 正丁酸;65. 异戊酸;66. 正戊酸;68. 正己酸;69. 苯丙酸乙酯;70. β- 苯乙;71. 庚酸;74. 十四酸乙酯;76. 辛酸;79. 棕榈酸乙酯;85. 油酸乙酯;86. 亚油酸乙酯
在体育界,对于睾丸激素的滥用越来越需要一个新的检测方法。 目前,GC-MS被用来从尿液中检测排泄物的睾丸激素/表睾(甾)酮比值。 当T/E的比例超过6:1的时候,传统上被认为是确证为睾丸素的管理。 这个比值被接受,由于世界流行的T/E比例低于该比例。但是, 有少部分的天然的就超过了6:1, 这样一些无辜者就被错误的判别成了有罪。 以下工作揭示了天然和合成的睾丸素荷尔蒙在C13方面的差异。这个应用文章揭示了传统的测试方法的失败,和使用GC-C-IRMS方法分析的成功。睾丸激素庚酸酯,丙酸睾丸甾酮库存是从日本获得。参比类固醇,吉拉德氏试剂T(羧甲基,三甲基氨基氯化酰胺)和铋酸盐是从Sigma公司获得。Sephadex LH-20是AB公司产品,Sep-pakcartridges来自waters。B-葡(萄)糖苷酸酶/芳香基硫酸酯酶是从Sigma和Boehringer Mannheim公司获得。所有的试剂均是分析6级。关于这个研究的志愿者5个中国男子(年龄:19-22)参与这个研究。在肌肉注射250mg庚酸睾丸酮之前的两天,收集尿样。在注射后的最初四天里,收集两个尿样(20ml),虽然只有每天清晨收集的样品用于分析。清晨点的尿样在第5-9天收集,后面依次是第11,13,15天。
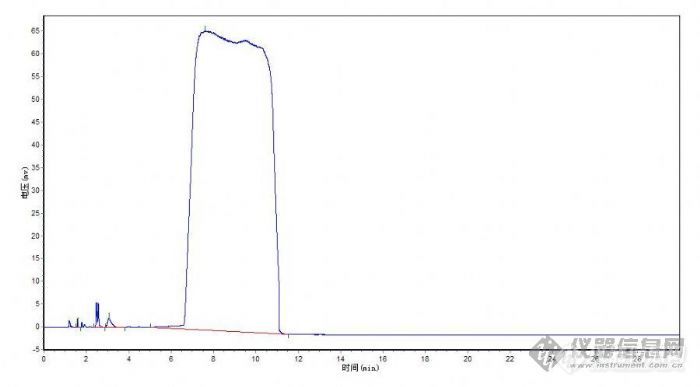
[img]http://ng1.17img.cn/bbsfiles/images/2008/11/200811171501_118902_1635634_3.jpg[/img]样品:7-氯-2-氧代庚酸乙酯检测条件:进样口温度250,初始温度100,保持5,以10的速度上升至230,保持5,FID检测器,280度,进样量0.2ul
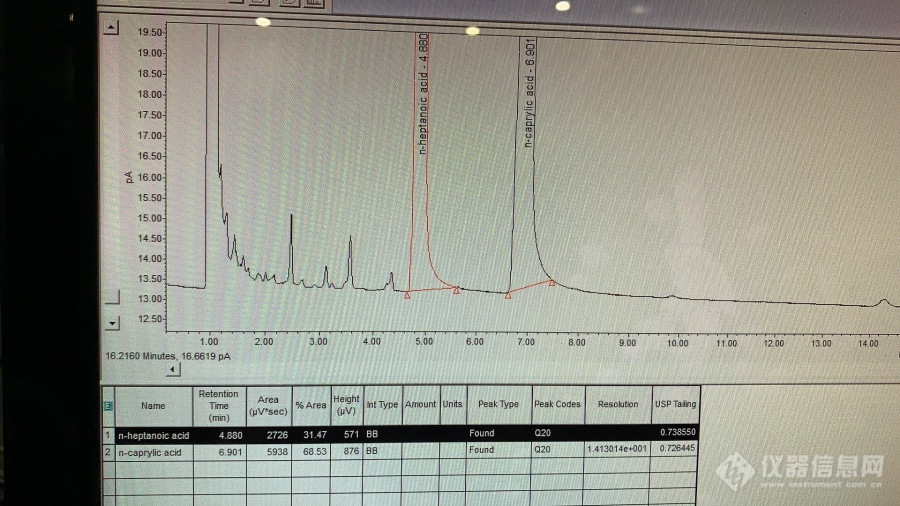
各位大神,请教一下药典通则里面的辛酸钠测定,要求[color=#333333]色谱条件与系统适用性试验为 用酸改性聚乙二醇(20M)毛细管柱,柱温160℃,火焰离子化检测器,检测器温度230℃,气化室温度230℃,载气(氮气)流速为每分钟35ml。辛酸峰与庚酸峰的分离度应大于1.5,辛酸峰的拖尾因子应为0.95~1.20,辛酸对照品溶液连续进样5次,所得辛酸峰与庚酸峰面积之比的相对标准偏差(RSD)应不大于5%。[/color][color=#333333]我这边色谱柱用的是J&W DB-FFAP(30×0.32×0.50)[color=#333333]柱温160℃,火焰离子化检测器,检测器温度230℃,气化室温度230℃,流速3.5ml/min,分流比10:1,出的峰分离度只有0.7~0.8左右,达不到要求的0.95,应该怎么处理?[/color][/color][color=#333333][color=#333333]ps:因为配制的时候浓度比药典规定的小4倍,所以进样量为4μl。[/color][/color][color=#333333][color=#333333][img=,690,387]https://ng1.17img.cn/bbsfiles/images/2019/08/201908261137379899_2144_2576605_3.jpg!w690x387.jpg[/img][/color][/color]
透明质酸分子量100万以上,配成溶液最高浓度约1%,能通过离心变得更浓吗?最近做蛋白质和透明质酸溶液,完全溶解最高浓度也只有1%多,查到超滤的方法可以做的更浓。刚接触这个领域,今天打电话咨询了一个公司的超滤杯,回复不用离心机、不用加压,就在里面有个转子,配合磁力搅拌器就能使用,不太靠谱吧? 有没有谁用过适合实验室小规模实验用的超滤仪器,也不是十分贵的,推荐一下!介绍超滤方面的知识也行。
对SCFA进行衍生化处理(酯化),在前处理过程中就加入了内标,上机内标浓度均为5ppm, SCFA-酯是自己酯化的,然后建立了标曲,标曲中内标响应特别稳定,大概50万左右,做回收率的时候设置低、中、高三个浓度水平,分别在水样和乳清粉(不含脂肪酸)中测定其回收率,每个组设置三个重复,组内三个重复的内标响应特别稳定,水样中内标响应较稳定,均在44万左右,但乳清粉中低、中、高三个浓度水平(0.5,2.5,20ppm)内标响应相差很大,分别在5万,13万,30万左右,请问可能是什么原因造成的(内标为2-乙基丁酸,也试过庚酸做内标,情况一致,加样的体积都在500微升,基本可以排除加样不准确的问题)
近日某公司一纸订单挖出了白酒乙醇勾兑的冰山一角,一时间整个行业保持集体缄默,我们到底喝的是啥?“酒精”还是“粮食精” 亟待标准出台,真假还是以脂类成分为主 迪马白酒分析应用可以给大家一个参考浓香型白酒分析方法: GC基质: 标准溶液固定相: DM-WAX色谱柱/前处理小柱: DM-WAX 30m x 0.25mm x 0.25um商品编号: 7521色谱条件: 柱温:37 oC ( 2 min ) - 70 oC, 3oC/min ;70 oC ( 1min) - 130 oC, 6oC/min ; 130 oC - 220 oC, 10 oC/min ;220 oC ( 10 min )载气:高纯氮, 1mL/min进样:260 oC, 分流比30:1检测:FID, 260 oC作者: 迪马科技http://www.dikma.com.cn/Public/Uploads/images/DM-Wax-1%20copy.png图例1. 乙醛;2. 丙醛;3. 异丁醛;4. 丙酮;5. 甲酸乙酯;9. 乙酸乙酯+ 乙缩醛;10. 甲醇;11. 2- 丁酮;12. 2- 甲基丁醛;13. 3- 甲基丁醛;14. 乙醇;15. 丙酸乙酯;16. 异丁酸乙酯;17. 二乙氧基异丁烷;18. 2- 戊酮;19. 仲丁醇;20. 丁酸乙酯;21. 正丙醇;25. 异戊酸乙酯;26. 二乙氧基-2- 甲基丁烷;27. 二乙氧基-3- 甲基丁烷;29. 异丁醇;30. 乙酸异戊酯;31. 仲戊醇;32. 戊酸乙酯;33. 正丁醇;36. 异戊醇;38. 己酸乙酯;40. 正戊醇;41. 3- 羟基丁酮;43. 己酸丙酯;44. 2- 庚醇;45. 庚酸乙酯;46. 乳酸乙酯;47. 正己醇;48. 己酸丁酯;49. 辛酸乙酯;51. 乙酸;52. 糠醛;55. 苯甲醛;56. 壬酸乙酯;57. 丙酸;58. 2.3- 丁二醇;( 左旋);59. 辛醇;60. 异丁酸;61. 2.3- 丁二醇;( 内消旋);62. 己酸己酯;63. 癸酸乙酯;64. 正丁酸;65. 异戊酸;66. 正戊酸;68. 正己酸;69. 苯丙酸乙酯;70. β- 苯乙;71. 庚酸;74. 十四酸乙酯;76. 辛酸;79. 棕榈酸乙酯;85. 油酸乙酯;86. 亚油酸乙酯酒中的酸和酯方法: GC基质: 标准溶液固定相: DM-FFAP色谱柱/前处理小柱: DM-FFAP 50m x 0.25mm x 0.25um商品编号: 7672色谱条件: 柱温:70 oC - 240 oC, 12oC/min ( 3 min )载气:H2, 28psi, 240 oC进样方式:不分流, 1.0 μL, 保持0.5 min, 240 oC检测:FID作者: 迪马科技http://www.dikma.com.cn/Public/Uploads/images/CFR00500.png图例1. 辛酸乙酯;2. 乙酸;3. 丙酸;4. 异丁酸;5. 3- 癸醇;6. 癸酸乙酯;7. 月桂酸乙酯;8. 顺式- 内酯;9. 2- 苯乙醇;10. 反式内酯;11. 肉豆蔻酸甲酯;12. 肉豆蔻酸乙酯;13. 辛酸;14. 棕榈酸乙酯;15. 癸酸;16. 月桂酸;17. 香兰素
[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LCMS[/color][/url]分析中TFA,甲酸,乙酸哪个更常用啊
聚氯乙烯和醋酸纤维滤膜,哪个更容易消解?请消解过的说一下,谢谢!!!
[align=center][b]保留指数应用(14)----直链脂肪酸乙酯计算保留指数2(非极性柱子)[/b][/align][b] [/b]保留指数作为[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。前面三篇分别探讨了利用直链饱和脂肪酸甲酯(FAME,Fat AcidMethyl Ester)计算极性和非极性柱子计算保留指数,以及利用直链脂肪酸乙酯计算极性柱子的保留指数的相关问题。本篇主要探讨利用直链脂肪酸乙酯(FAEE, Fat Acid Ethyl Ester)来计算非极性柱子的保留指数。并讨论和用正构烷烃计算保留指数的区别和相关性。 附:保留指数基本概念保留指数retention index或KovatsIndex(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。保留指数(RI)的计算公式如下:I=100Z+100[logt’[sub]R(x)[/sub]-logt’[sub]R(z)[/sub]]/ [logt’[sub]R(z+1)[/sub]- logt’[sub]R(z)[/sub]] (恒温分析) (1)式中:t’[sub]R[/sub]为校正保留时间 Z和Z+1分别为目标化合物(X)流出前后的正构烷烃所含碳原子的数目 这里:t’[sub]R(z)[/sub] t’[sub]R(x)[/sub] t’[sub]R(z+1)[/sub], 一般正构烷烃所含碳原子的数目Z大于4.以上的保留指数(RI)的计算只用于恒温分析。对于沸点范围较宽的复杂组分混合物的分析,一般采用程序升温的方法。在程序升温时,组分的保留指数的测定有所不同。两者有差异,需要校正。1963年Van Den Dool 等经过推算(详细的推导过程略)引入线性程序升温保留指数的概念。I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]] (线性程序升温) (2) 式中:T[sub]R(x)[/sub][sub],[/sub]T[sub]R(z)[/sub][sub],[/sub]T[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留温度。且T[sub]R(z)[/sub]T[sub]R(x)[/sub]T[sub]R(z+1)[/sub][sub]。[/sub][sub] [/sub] 一般讲,保留温度的测量比保留时间的测定要麻烦一点。由于保留温度和保留时间通常具有高度的相关性,所以用保留时间代替上式中的保留温度来进行计算保留指数。I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温) (3)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留时间。且RT[sub]R(z)[/sub]RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub][b]保留指数与保留时间的转换[/b]从I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/ [T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]](3)式可以导出:T[sub]R(x)[/sub]= [I[sup]T[/sup]-100Z]*[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]]/100+T[sub]R(z) [/sub](4)[sub] [/sub][align=center][b](14)直链饱和脂肪酸乙酯(FAEE)计算保留指数2(非极性柱子)[/b][/align]一般是使用正构烷烃来计算化合物的保留指数,但也有人使用直链饱和脂肪酸甲酯或乙酯及某些系列化合物(例如苯系列等)来计算保留指数。脂肪酸乙酯很常见,可能更容易得到。如果使用直链饱和脂肪酸乙酯(FAEE)计算保留指数,把公式(3)改成I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温) (5)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1的直链饱和脂肪酸乙酯保留时间。且RT[sub]R(z)[/sub] RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub]或者:I[sup]RT[/sup]=100(Z+N)+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/ [RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]](线性程序升温) (6)式中:N为调整的碳数(为了和正构烷计算保留指数校正对应)[b]1试验部分[/b]1.1 仪器与装置美国安捷伦6890N/5973I[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪。1.2样品和标样、试剂所用香气化合物标准品均来自Sigma-Aldrich等主要试剂公司,少数为实验室内部精制标样。C6-C24正构烷混合标准物来自上海安谱,直链饱和脂肪酸乙酯标品来自上海甄准。TBME来自安谱。1.3 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MS条件1.3.1 色谱条件:色谱柱:HP-Innowax (60m×0. 25 mm ( i.d.)×0.25μm)毛细管柱;升温程序: 60℃保持0 min,以3 ℃/min升至250℃,保持26 min;载气(He, 纯度99.999%以上)流速1.9 mL/min 进样口温度250℃,分流进样,分流比20:1,进样量1ul;1.3.2质谱条件: 电子轰击(EI)离子源;电子能量70eV;传输线温度280℃;离子源温度230℃;四级杆温度150℃。SCAN扫描范围:29-400。EMV:1655V。1.4 标样配制正构烷混合标准混合物,直链饱和脂肪酸乙酯标准混合物和香气化合物化合物标准稀释配制在TBME中,约0.1%浓度。[b]2 结果与讨论[/b]采用正构烷保留时间和利用公式(5)和(6)计算脂肪酸乙酯(FAEE)保留指数(正构烷形式),结果如表1。[align=center]表1 正构烷和直链饱和脂肪酸乙酯(FAEE)测定的保留时间和其保留指数对照表[/align][align=center](非极性柱子)[/align][align=left][table=620][tr][td=4,1]正构烷保留指数[/td][td=6,1]直链饱和脂肪酸乙酯(FEMA)非极性柱子保留指数[/td][/tr][tr][td]保留时间[/td][td]定义保留指数[/td][td]保留时间[/td][td]定义保留指数[/td][td]校正定义保留指数[/td][td]正构烷计算的保留指数[/td][/tr][tr][td]正构烷[/td][td]正构烷碳数[/td][td]RT(min)[/td][td]RI[/td][td]FAEE[/td][td]FEMA碳数[/td][td]RT(min)[/td][td]Rifaee (N=1)[/td][td]RIfaee_c (N=1.8)[/td][td]RIa[/td][/tr][tr][td]正庚烷[/td][td]7[/td][td]2.258[/td][td]700[/td][td]丁酸乙酯[/td][td]6[/td][td]2.924 [/td][td]600[/td][td]780[/td][td]785[/td][/tr][tr][td]正辛烷[/td][td]8[/td][td]3.061[/td][td]800[/td][td]戊酸乙酯[/td][td]7[/td][td]4.260 [/td][td]700[/td][td]880[/td][td]888[/td][/tr][tr][td]正壬烷[/td][td]9[/td][td]4.442[/td][td]900[/td][td]己酸乙酯[/td][td]8[/td][td]6.141 [/td][td]800[/td][td]980[/td][td]986[/td][/tr][tr][td]正癸烷[/td][td]10[/td][td]6.437[/td][td]1000[/td][td]庚酸乙酯[/td][td]9[/td][td]8.416 [/td][td]900[/td][td]1080[/td][td]1082[/td][/tr][tr][td]碳11烷[/td][td]11[/td][td]8.866[/td][td]1100[/td][td]辛酸乙酯[/td][td]10[/td][td]11.026 [/td][td]1000[/td][td]1180[/td][td]1183[/td][/tr][tr][td]碳12烷[/td][td]12[/td][td]11.483[/td][td]1200[/td][td]壬酸乙酯[/td][td]11[/td][td]13.626 [/td][td]1100[/td][td]1280[/td][td]1282[/td][/tr][tr][td]碳13烷[/td][td]13[/td][td]14.113[/td][td]1300[/td][td]癸酸乙酯[/td][td]12[/td][td]16.093 [/td][td]1200[/td][td]1380[/td][td]1378[/td][/tr][tr][td]碳14烷[/td][td]14[/td][td]16.688[/td][td]1400[/td][td]碳11酸乙酯[/td][td]13[/td][td]18.612 [/td][td]1300[/td][td]1480[/td][td]1480[/td][/tr][tr][td]碳15烷[/td][td]15[/td][td]19.114[/td][td]1500[/td][td]碳12酸乙酯[/td][td]14[/td][td]20.965 [/td][td]1400[/td][td]1580[/td][td]1580[/td][/tr][tr][td]碳16烷[/td][td]16[/td][td]21.442[/td][td]1600[/td][td]碳13酸乙酯[/td][td]15[/td][td]23.160 [/td][td]1500[/td][td]1680[/td][td]1678[/td][/tr][tr][td]碳17烷[/td][td]17[/td][td]23.658[/td][td]1700[/td][td]碳14酸乙酯[/td][td]16[/td][td]25.292 [/td][td]1600[/td][td]1780[/td][td]1778[/td][/tr][tr][td]碳18烷[/td][td]18[/td][td]25.767[/td][td]1800[/td][td]碳15酸乙酯[/td][td]17[/td][td]27.305 [/td][td]1700[/td][td]1880[/td][td]1877[/td][/tr][tr][td]碳19烷[/td][td]19[/td][td]27.777[/td][td]1900[/td][td]碳16酸乙酯[/td][td]18[/td][td]28.074 [/td][td]1800[/td][td]1980[/td][td]1976[/td][/tr][tr][td]碳20烷[/td][td]20[/td][td]29.695[/td][td]2000[/td][td]碳17酸乙酯[/td][td]19[/td][td]31.152 [/td][td]1900[/td][td]2080[/td][td]2080[/td][/tr][tr][td]碳21烷[/td][td]21[/td][td]31.529[/td][td]2100[/td][td]碳18酸乙酯[/td][td]20[/td][td]32.905 [/td][td]2000[/td][td]2180[/td][td]2179[/td][/tr][tr][td]碳22烷[/td][td]22[/td][td]32.282[/td][td]2200[/td][td] [/td][td] [/td][td] [/td][td] [/td][td] [/td][td] [/td][td] [/td][/tr][/table] [/align][align=left]2.1正构烷和直链饱和脂肪酸乙酯测定的非极性柱子的保留时间和其保留指数对比2.1.1从上面的表可以看出,在线性程序升温时候,直链饱和脂肪酸乙酯化合物的非极性柱子保留时间也是基本随碳数等距离增加,和正构烷的出峰时间的趋势一样。2.1.2直链饱和脂肪酸乙酯化合物的非极性柱子保留时间和正构烷保留时间的碳数差不多相差1-2。[b][u]而不是脂肪酸甲酯的整数值。也不是极性柱子的碳数相差4-5。[/u][/b]2.1.3直链饱和脂肪酸乙酯化合物的非极性柱子保留指数加约180和相同碳数的正构烷保留指数很接近。[b][u]不是极性柱子保留指数加约440和相同碳数的正构烷保留指数很接近。也不是直链饱和脂肪酸甲酯化合物的非极性柱子的保留指数加500和相同碳数的正构烷保留指数很接近的情况。[/u][/b]****************************************************************************2.2 部分挥发性香气化合物乙酸酯的非极性柱子保留指数举例用公式(3),(5)和(6)来计算部分挥发性香气化合物保留指数。[/align][align=center]表2部分挥发性香气化合物乙酸酯的非极性柱子保留指数举例[/align][table=520][tr][td]保留时间[/td][td]正构烷计算保留指数[/td][td]FEMA计算保留指数[/td][td]FEMA计算校正保留指数[/td][/tr][tr][td]化合物名称[/td][td]RT(min)[/td][td]RI[/td][td]Rifaee (N=1)[/td][td]RIfaee_c (N=1.8)[/td][/tr][tr][td]butyl acetate[/td][td]3.043[/td][td]800[/td][td]609[/td][td]789[/td][/tr][tr][td]Hexanol[/td][td]3.804[/td][td]855[/td][td]666[/td][td]846[/td][/tr][tr][td]alpha-pinene[/td][td]5.124[/td][td]935[/td][td]765[/td][td]945[/td][/tr][tr][td]ehthyl capronoate[/td][td]5.323[/td][td]945[/td][td]757[/td][td]937[/td][/tr][tr][td]benzyl alcohol[/td][td]6.712[/td][td]1012[/td][td]825[/td][td]1005[/td][/tr][tr][td]Limonene[/td][td]6.931[/td][td]1021[/td][td]835[/td][td]1015[/td][/tr][tr][td]gamma-terpinene[/td][td]7.759[/td][td]1055[/td][td]871[/td][td]1051[/td][/tr][tr][td]Linalool[/td][td]8.440 [/td][td]1083[/td][td]901[/td][td]1081[/td][/tr][tr][td]PEA[/td][td]8.586[/td][td]1089[/td][td]907[/td][td]1087[/td][/tr][tr][td]methyl salicylate[/td][td]10.528[/td][td]1164[/td][td]881[/td][td]1061[/td][/tr][tr][td]geranial[/td][td]12.680 [/td][td]1246[/td][td]1064[/td][td]1244[/td][/tr][tr][td]Triactin[/td][td]14.509[/td][td]1316[/td][td]1136[/td][td]1316[/td][/tr][tr][td]Caroyphenen[/td][td]16.875[/td][td]1409[/td][td]1231[/td][td]1411[/td][/tr][tr][td]amyl cinnamic aldehyde[/td][td]22.318[/td][td]1640[/td][td]1461[/td][td]1641[/td][/tr][tr][td]Tonalide[/td][td]26.661[/td][td]1845[/td][td]1667[/td][td]1847[/td][/tr][tr][td]Benzyl Cinnamate[/td][td]30.638[/td][td]2052[/td][td]1883[/td][td]2063[/td][/tr][/table]从表2看出,直链饱和脂肪酸乙酯计算挥发性香气化合物的非极性柱子的保留指数加约[b][u]18[/u][/b]0(FAEE校正保留指数,[b][u]N=1.8[/u][/b])和相同碳数的正构烷保留指数很接近。[b][u]而不是极性柱子的保留指数加440(FAEE校正保留指数,N=4.4)和相同碳数的正构烷保留指数很接近。比极性柱子的乙酯计算的保留指数值偏差小一些。[/u][/b]在实际应用中可以考虑相互参照参考或甚至相互代用。

紫苏梗中迷迭香酸含量检测 紫苏梗药材为唇形科植物紫苏的干燥茎。秋季采割,除去杂质,晒干,即可。主要药物功效有理气、止痛、安胎等。可治疗胸膈痞闷、胃脘疼痛、嗳气呕吐、安胎保胎等疑难病证。 紫苏梗中主要药物成分有迷迭香酸,而该成分含量比较低,药典中有严格的限量标准。下面我们就来检测紫苏梗中迷迭香酸含量,采用的方法是高效液相色谱法。实验部分【原理】 精密称取适量紫苏梗样品经60%丙酮溶解,超声提取后注入高效液相色谱系统,C18色谱柱分离,紫外检测器检测,外标法(保留时间定性,峰面积定量)计算,得出该样品中迷迭香酸含量。【仪器及试剂】 仪器:高效液相色谱仪(紫外检测器+等度泵+柱温箱+在线脱气机等),超声波清洗仪,溶剂过滤器,电子天平(0.0001),药典筛(三号筛)等。 试剂:甲醇(色谱纯), 丙酮(分析纯),甲酸溶液(分析纯),超纯水等。【样品制备】 对照品溶液制备:准确称取迷迭香酸对照品2mg于50ml容量瓶中,加60%丙酮溶液溶解、定容,配制成40ug/ml迷迭香酸对照品溶液,备用。 供试品溶液制备:取紫苏梗样品适量,充分粉碎后过药典筛三号筛,准确称取过筛粉末0.5g,置具塞锥形瓶中,精密加入60%丙酮25ml,密塞,称定重量并记录,超声处理30分钟,放冷,再次称定重量,用60%丙酮补足减少的重量,摇匀,0.45um微膜滤过,待测。【色谱条件】检测器:紫外检测器检测波长:330nm色谱柱:Promosil C18 ( 250 mm X 4.6mm,5μm )流动相:甲醇:0.1%甲酸溶液=40:60(V:V)流速:1.0ml/min柱温:30℃进样量:10μl【色谱图】对照品溶液色谱图:http://ng1.17img.cn/bbsfiles/images/2015/09/201509101148_565579_2536753_3.png供试品溶液色谱图:http://ng1.17img.cn/bbsfiles/images/2015/09/201509101149_565580_2536753_3.png【计算及结果】http://ng1.17img.cn/bbsfiles/images/2015/09/201509101149_565581_2536753_3.png 经计算该紫苏梗样品中迷迭香酸含为0.11%,含量还是不错的,略高于药典中规定的不小于0.10%的限量,符合药典要求。按药典要求,属于合格品。 该方法检测该项目,检测时间虽然有点长,但样品中被测成分后紧挨着一个干扰物,采用缩短检测时间的方法它们两很容易粘合在一起,影响它们的分离度及检测准确性,所以这个时间已算比较短的了。【结论】 该方法对药典方法略作修改,得到了不错的检测效果,该方法适合该样品中迷迭香酸含量检测。
[em09512]如题!按照要求,试用期满3个月的标准品是需要更换的。我们使用的是自己配制的标准品。使用甲醇做溶剂,溶质有1克左右的丙二醇、0.25克左右的乙酸丙酯、0.25克左右的苯乙烯、0.25克左右的甲苯、0.45克左右的异丙醇和0.25克左右的庚烷,依次加入甲醇中。之前也是同样的配制方法,可是现在走[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]下来的结果里面,除了庚烷的相应值加倍,其他的都没怎么变化。曾怀疑是庚烷变质的原因,使用新采购的庚烷却还是同样的结果。这影响到了我们的分析结果,使得烷烃类的物质的含量较以前变化很大。请教高手,到底是为什么呢?
[align=center][b]保留指数应用(13)----直链脂肪酸乙酯计算保留指数1(极性柱子)[/b][/align][b] [/b]保留指数作为[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]定性一个强有力的辅助手段,在天然香精油,香气香味材料,香精产品等的分析鉴定中广泛应用。当然应用范围远不止这些。对于异构体,同系物和结构特征相似的化合物,由于其质谱图非常相似,谱库检索结果匹配度,排列次序都很接近,检索给出的顺序也不一定正确。但它们的保留时间可能会不同,但保留时间只能在特定色谱条件下不变,而保留指数在固定相相同下有可比性。虽然在相同的柱子上和相同的色谱条件下,两个不同的化合物的保留指数有可能相同。但两个化合物同时具有相同的保留指数(或保留时间)和相同的质谱图的不可能性极小。虽然保留时间也可以帮助确认,但保留时间会随着柱子使用的不同阶段新旧等因素而变化,但保留指数是和固定相为主要因素的一个值,相对比较固定不变。所以才有保留指数辅助定性更具有优势。在谱库检索的基础上,用保留指数来确认结果。是一种很重要的手段。前面两篇探讨了利用直链饱和脂肪酸甲酯(FAME)计算保留指数的相关问题。本篇主要探讨利用直链脂肪酸乙酯(FAEE, Fat Acid Ethyl Ester)来计算保留指数。并讨论和用正构烷烃计算保留指数的区别和相关性。 附:保留指数基本概念保留指数retention index或KovatsIndex(RI或KI)概念是由Kovats在1958年提出。是把组分的保留值用两个分别前后靠近它的正构烷烃来标定(这比仅用一个参比物质的相对保留值定向更为精确)。正构烷烃的保留指数规定为等于该烷烃分子中碳原子数的100倍。例如正己烷的RI为600,正庚烷为700,正十五烷为1500.正构烷烃的RI与所用的色谱柱,柱温及其它操作条件无关。保留指数(RI)的计算公式如下:I=100Z+100[logt’[sub]R(x)[/sub]-logt’[sub]R(z)[/sub]]/ [logt’[sub]R(z+1)[/sub]- logt’[sub]R(z)[/sub]] (恒温分析) (1)式中:t’[sub]R[/sub]为校正保留时间 Z和Z+1分别为目标化合物(X)流出前后的正构烷烃所含碳原子的数目 这里:t’[sub]R(z)[/sub] t’[sub]R(x)[/sub] t’[sub]R(z+1)[/sub], 一般正构烷烃所含碳原子的数目Z大于4.以上的保留指数(RI)的计算只用于恒温分析。对于沸点范围较宽的复杂组分混合物的分析,一般采用程序升温的方法。在程序升温时,组分的保留指数的测定有所不同。两者有差异,需要校正。1963年Van Den Dool 等经过推算(详细的推导过程略)引入线性程序升温保留指数的概念。I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]] (线性程序升温) (2) 式中:T[sub]R(x)[/sub][sub],[/sub]T[sub]R(z)[/sub][sub],[/sub]T[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留温度。且T[sub]R(z)[/sub]T[sub]R(x)[/sub]T[sub]R(z+1)[/sub][sub]。[/sub][sub] [/sub] 一般讲,保留温度的测量比保留时间的测定要麻烦一点。由于保留温度和保留时间通常具有高度的相关性,所以用保留时间代替上式中的保留温度来进行计算保留指数。I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温) (3)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1正构烷的保留时间。且RT[sub]R(z)[/sub]RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub][b]保留指数与保留时间的转换[/b]从I[sup]T[/sup]=100Z+100[T[sub]R(x)[/sub]-T[sub]R(z)[/sub]]/ [T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]](3)式可以导出:T[sub]R(x)[/sub]= [I[sup]T[/sup]-100Z]*[T[sub]R(z+1)[/sub]-T[sub]R(z)[/sub]]/100+T[sub]R(z) [/sub](4)[sub] [/sub][align=center][b](13)直链饱和脂肪酸乙酯(FAEE)计算保留指数1(极性柱子)[/b][/align]一般是使用正构烷烃来计算化合物的保留指数,但也有人使用直链饱和脂肪酸甲酯或乙酯及某些系列化合物(例如苯系列等)来计算保留指数。脂肪酸乙酯很常见,可能更容易得到。如果使用直链饱和脂肪酸乙酯(FAEE)计算保留指数,把公式(3)改成I[sup]RT[/sup]=100Z+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/[RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]] (线性程序升温) (5)式中:RT[sub]R(x)[/sub][sub],[/sub]RT[sub]R(z)[/sub][sub],[/sub]RT[sub]R(z+1)[/sub]分别代表组分及碳数为Z,Z+1的直链饱和脂肪酸乙酯保留时间。且RT[sub]R(z)[/sub] RT[sub]R(x)[/sub]RT[sub]R(z+1)[/sub][sub]。[/sub]或者:I[sup]RT[/sup]=100(Z+N)+100[RT[sub]R(x)[/sub]-RT[sub]R(z)[/sub]]/ [RT[sub]R(z+1)[/sub]-RT[sub]R(z)[/sub]](线性程序升温) (6)式中:N为调整的碳数(为了和正构烷计算保留指数校正对应)[b]1试验部分[/b]1.1 仪器与装置美国安捷伦6890N/5973I[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪。1.2样品和标样、试剂所用香气化合物标准品均来自Sigma-Aldrich等主要试剂公司,少数为实验室内部精制标样。C6-C24正构烷混合标准物来自上海安谱,直链饱和脂肪酸乙酯标品来自上海甄准。TBME来自安谱。1.3 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MS条件1.3.1 色谱条件:色谱柱:HP-Innowax (60m×0. 25 mm ( i.d.)×0.25μm)毛细管柱;升温程序: 60℃保持0 min,以3 ℃/min升至250℃,保持26 min;载气(He, 纯度99.999%以上)流速1.9 mL/min 进样口温度250℃,分流进样,分流比20:1,进样量1ul;1.3.2质谱条件: 电子轰击(EI)离子源;电子能量70eV;传输线温度280℃;离子源温度230℃;四级杆温度150℃。SCAN扫描范围:29-400。EMV:1655V。1.4 标样配制正构烷混合标准混合物,直链饱和脂肪酸乙酯标准混合物和香气化合物化合物标准稀释配制在TBME中,约0.1%浓度。[b]2 结果与讨论[/b]采用正构烷保留时间和利用公式(5)和(6)计算脂肪酸乙酯(FAEE)保留指数(正构烷形式),结果如表1。[align=center]表1 正构烷和直链饱和脂肪酸乙酯(FAEE)测定的保留时间和其保留指数对照表[/align][table=619][tr][td=4,1]正构烷保留指数[/td][td=6,1]直链饱和脂肪酸乙酯(FAEE)保留指数[/td][/tr][tr][td]保留时间[/td][td]定义保留指数[/td][td]保留时间[/td][td]定义保留指数[/td][td]校正定义保留指数[/td][td]正构烷计算的保留指数[/td][/tr][tr][td]正构烷[/td][td]正构烷碳数[/td][td]RT(min)[/td][td]RI[/td][td]FAEE[/td][td]FAEE碳数[/td][td]RT(min)[/td][td]RIfaee[/td][td]RIfaee_c (N=4.4)[/td][td]RIa[/td][/tr][tr][td]正辛烷[/td][td]8[/td][td]4.112[/td][td]800[/td][td]乙酸乙酯[/td][td]4[/td][td]4.631[/td][td]400[/td][td]840[/td][td]881[/td][/tr][tr][td]正壬烷[/td][td]9[/td][td]4.76[/td][td]900[/td][td]丙酸乙酯[/td][td]5[/td][td]5.457[/td][td]500[/td][td]940[/td][td]960[/td][/tr][tr][td]正癸烷[/td][td]10[/td][td]5.92[/td][td]1000[/td][td]丁酸乙酯[/td][td]6[/td][td]6.582[/td][td]600[/td][td]1040[/td][td]1035[/td][/tr][tr][td]碳11烷[/td][td]11[/td][td]7.811[/td][td]1100[/td][td]戊酸乙酯[/td][td]7[/td][td]8.541[/td][td]700[/td][td]1140[/td][td]1127[/td][/tr][tr][td]碳12烷[/td][td]12[/td][td]10.515[/td][td]1200[/td][td]己酸乙酯[/td][td]8[/td][td]12.034[/td][td]800[/td][td]1240[/td][td]1245[/td][/tr][tr][td]碳13烷[/td][td]13[/td][td]13.89[/td][td]1300[/td][td]庚酸乙酯[/td][td]9[/td][td]15.059[/td][td]900[/td][td]1340[/td][td]1331[/td][/tr][tr][td]碳14烷[/td][td]14[/td][td]17.659[/td][td]1400[/td][td]辛酸乙酯[/td][td]10[/td][td]19.265[/td][td]1000[/td][td]1440[/td][td]1441[/td][/tr][tr][td]碳15烷[/td][td]15[/td][td]21.575[/td][td]1500[/td][td]壬酸乙酯[/td][td]11[/td][td]22.432[/td][td]1100[/td][td]1540[/td][td]1522[/td][/tr][tr][td]碳16烷[/td][td]16[/td][td]25.369[/td][td]1600[/td][td]癸酸乙酯[/td][td]12[/td][td]26.683[/td][td]1200[/td][td]1640[/td][td]1632[/td][/tr][tr][td]碳17烷[/td][td]17[/td][td]29.263[/td][td]1700[/td][td]碳11酸乙酯[/td][td]13[/td][td]30.723[/td][td]1300[/td][td]1740[/td][td]1740[/td][/tr][tr][td]碳18烷[/td][td]18[/td][td]32.914[/td][td]1800[/td][td]碳12酸乙酯[/td][td]14[/td][td]34.141[/td][td]1400[/td][td]1840[/td][td]1835[/td][/tr][tr][td]碳19烷[/td][td]19[/td][td]36.421[/td][td]1900[/td][td]碳13酸乙酯[/td][td]15[/td][td]37.765[/td][td]1500[/td][td]1940[/td][td]1940[/td][/tr][tr][td]碳20烷[/td][td]20[/td][td]39.78[/td][td]2000[/td][td]碳14酸乙酯[/td][td]16[/td][td]41.099[/td][td]1600[/td][td]2040[/td][td]2041[/td][/tr][tr][td]碳21烷[/td][td]21[/td][td]42.996[/td][td]2100[/td][td]碳15酸乙酯[/td][td]17[/td][td]44.418[/td][td]1700[/td][td]2140[/td][td]2146[/td][/tr][tr][td]碳22烷[/td][td]22[/td][td]46.086[/td][td]2200[/td][td]碳16酸乙酯[/td][td]18[/td][td]48.758[/td][td]1800[/td][td]2240[/td][td]2250[/td][/tr][tr][td]碳23烷[/td][td]23[/td][td]49.055[/td][td]2300[/td][td]碳17酸乙酯[/td][td]19[/td][td]50.623[/td][td]1900[/td][td]2340[/td][td]2355[/td][/tr][tr][td]碳24烷[/td][td]24[/td][td]51.906[/td][td]2400[/td][td]碳18酸乙酯[/td][td]20[/td][td]53.551[/td][td]2000[/td][td]840[/td][td]2460[/td][/tr][tr][td] [/td][td] [/td][td] [/td][td] [/td][/tr][/table]2.1正构烷和直链饱和脂肪酸乙酯测定的保留时间和其保留指数对比2.1.1从上面的表可以看出,在线性程序升温时候,直链饱和脂肪酸乙酯化合物的保留时间也是基本随碳数等距离增加,和正构烷的出峰时间的趋势一样。2.1.2直链饱和脂肪酸乙酯化合物的保留时间和正构烷保留时间的碳数差不多相差4-5。[b][u]而不是脂肪酸甲酯的整数值。[/u][/b]2.1.3直链饱和脂肪酸乙酯化合物的保留指数加440和相同碳数的正构烷保留指数很接近。[b][u]而不是直链饱和脂肪酸甲酯化合物的保留指数加500和相同碳数的正构烷保留指数很接近的情况。[/u][/b]****************************************************************************2.2 部分挥发性香气化合物保留指数举例用公式(3),(5)和(6)来计算部分挥发性香气化合物保留指数。[table=520][tr][td]保留时间[/td][td]正构烷计算保留指数[/td][td]FAEE计算保留指数[/td][td]FEMA计算校正保留指数[/td][/tr][tr][td]化合物名称[/td][td]RT(min)[/td][td]RI[/td][td]RIfaee[/td][td]RIfaee_c (N=4.4)[/td][/tr][tr][td]ethyl acetate[/td][td]4.631[/td][td]881[/td][td]400[/td][td]840[/td][/tr][tr][td]Ethanol[/td][td]5.166[/td][td]935[/td][td]495[/td][td]905[/td][/tr][tr][td]alpha-pinene[/td][td]6.526[/td][td]1032[/td][td]595[/td][td]1035[/td][/tr][tr][td]butyl acetate[/td][td]6.658[/td][td]1039[/td][td]604[/td][td]1044[/td][/tr][tr][td]Limonene[/td][td]10.515[/td][td]1200[/td][td]757[/td][td]1197[/td][/tr][tr][td]isoamyl alcohol[/td][td]10.852[/td][td]1210[/td][td]766[/td][td]1206[/td][/tr][tr][td]ehthyl capronoate[/td][td]12.034[/td][td]1245[/td][td]805[/td][td]1245[/td][/tr][tr][td]Hexanol[/td][td]16.001[/td][td]1356[/td][td]822[/td][td]1362[/td][/tr][tr][td]Linalool[/td][td]23.483[/td][td]1549[/td][td]1125[/td][td]1565[/td][/tr][tr][td]PG[/td][td]24.729[/td][td]1581[/td][td]1154[/td][td]1593[/td][/tr][tr][td]Caroyphenen[/td][td]24.924[/td][td]1586[/td][td]1158[/td][td]1598[/td][/tr][tr][td]methyl salicylate[/td][td]31.271[/td][td]1755[/td][td]1316[/td][td]1756[/td][/tr][tr][td]benzyl alcohol[/td][td]35.999[/td][td]1888[/td][td]1451[/td][td]1891[/td][/tr][tr][td]Triactin[/td][td]41.999[/td][td]2069[/td][td]1627[/td][td]2067[/td][/tr][/table]从表2看出,直链饱和脂肪酸乙酯计算挥发性香气化合物的保留指数加[b][u]44[/u][/b]0(FAEE校正保留指数,[b][u]N=4.4[/u][/b])和相同碳数的正构烷保留指数很接近。在实际应用中可以考虑相互参照参考或甚至相互代用。但乙酸乙酯的保留指数值相差比较大,偏差较大。(下次讨论非极性柱子上面用直链脂肪酸乙酯来计算保留指数。并讨论和用正构烷烃计算保留指数的区别和相关性。)
如题,七氟正丁酸和庚磺酸钠混合溶液能上质谱吗?
请问:七氟正丁酸和庚烷磺酸钠混合溶液能上质谱吗?
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。 产品编号 产品名称 纯度 SLF0170庚酸-GCS99%SLF0171庚酸乙酯-GCS99%SLF0172癸二酸二丁酯-GCS99%SLF0173癸二酸二辛酯-GCS99%SLF0174环丁砜-GCS99%SLF0175环己醇-GCS99%SLF0176环己酮-GCS99%SLF0177环己烷-GCS,试剂,无证书99%SLF0178环戊醇-GCS99%SLF0179环戊烷-GCS99%SLF0180环氧氯丙烷-GCS99%SLF0181己二酸-GCS99%SLF0182己酸丁酯-GCS99%SLF0183己酸甲酯-GCS99%SLF0184己酸乙酯-GCS,试剂,无证书99%SLF0185甲胺-GCS99%SLF0186甲醇-GCS,试剂,无证书99%SLF0187甲基苯-GCS99%SLF0188甲基吡啶-GCS99%SLF0189甲基丁基甲酮-GCS99%SLF0190甲基环己烷-GCS99%SLF0191甲基环戊烷-GCS99%SLF0192甲基叔丁基醚-GCS99%SLF0193甲基叔戊基醚-GCS99%SLF0194甲基戊基甲酮-GCS99%SLF0195甲基异丙基甲酮-GCS99% 坛墨质检现有员工79人,办公室面积450平米,实验室1650平米;销售、客服、财务及行政人员35人,实验室工作人员21人,库房14人,市场部8人。实验仪器设备:气相色谱、液相色谱、气质联用、液质联用、离子色谱、紫外分光光度计,原子吸收、ICP-OES和ICP-MS;库房面积450平米,库房工作人员12人,现货产品5万个,坛墨质检自主研发的产品近3000个,已申报国标345项,填补国内空白的产品达到65项。坛墨质检是国内唯一提供标准溶液定制服务的标准物质研制单位,定制范围:特殊浓度定制、特殊溶剂定制、混标定制。
我们单位最近的业务很多,99.999%的氮气不到半个月就用一瓶(带两台色谱同时工作),导致成本上升很大.请问如果用瓶装气、氮气发生器、三气一体发生器,哪个更划算?[em33]
测氨氮的纳氏试剂是自己配还是买成品更划算更方便呢?如果是直接买成品,一般是多少钱呢?什么牌子的?有没有推荐店铺呢?感谢!!