哪位朋友有丙酮氰醇含量测定的方法([url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法),可否给我上传一个,谢谢!
请问分析丙酮及其中的乙醇,甲醇含量。用分光光度法应该怎么分析?
低本底总α检测法实验中加丙酮或者无水乙醇的作用
我想测定发酵液中丁醇,丙酮和乙醇还有乙酸和丁酸,现有岛津GC-2010plus,柱子DB-FFAP((30 m × 0 . 53 mm × 0 . 5μm); :进样量: 1μL,进样温度:220 0C;载气流量: 4.8m1/min;恒压模式:25磅/英寸;分流比为20:1;程序升温: 初始温度为 50℃,维持 2 min,第 1次程序升温 5 ℃/min至 170℃,维持 1 min,第2次程序升温20℃/min至 210 ℃,维持 2 min。检测器温度:240 ℃ , 氢气流量:40.0mL/min, 空气流量:250m1/min;内标物:异丁醇。不知这个条件对乙酸和丁酸的分离度怎么样?长期进水样是不是特别影响柱子,能给出好的意见吗?谢谢!
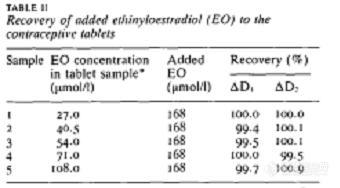
炔诺酮中炔雌醇的测定1 绪论采用各种已报道的方法测定避孕药片中乙炔雌二醇(EO)。这些方法包括分光光度法,高压液相色谱,薄层色谱和比色法。Corti等人用二阶导紫外分光测定二元混合物的雌激素和孕激素,相对标准偏差 5%以内。Ebeletal等人报告说,有几个方法确定EO的口服避孕药片,包括利用直接,差分 derivative紫外分光法和直角多项式法。作者报告说,后者的方法得到了最可靠的结果。最近, 事实已经证明,应用分光光度法的衍生技术是非常有益的,在解决光谱重叠, 消除来自其他样品不相干吸收。不过,在某些情况下,衍生的技术无法应付的干扰,尤其是当[size
【作者】 马铭研; 周丹丹; 于治国;【机构】 沈阳药科大学药学院; 沈阳药科大学药学院 辽宁沈阳110016; 辽宁沈阳110016;【摘要】 目的:比较研究大鼠尾静脉注射与局部皮肤给予酮咯酸氨丁三醇的药动学行为。方法:采用HPLC法,色谱柱:Dia-monsil C18柱(200mm×4.6mm,5μm);流动相:甲醇-水-三乙胺-冰醋酸(80∶19.9∶0.02∶0.08);流速:1.0mL.min-1;柱温:30℃;检测波长:313nm。结果:酮咯酸氨丁三醇在0.2~100mg.L-1范围内与峰面积呈良好的线性关系(r=0.999 0),日内RSD为2.3%~5.1%,日间RSD为2.2%~12.2%,萃取回收率为86.8%~96.2%,注射剂和凝胶剂的T1/2α分别为(0.4±0.3)h,(2.9±2.6)h;T1/2β分别为(2.7±2.0)h,(9.0±8.5)h。结论:本试验建立的方法操作简单,方法灵敏、特异,结果准确。酮咯酸在大鼠体内药动学行为符合二房室模型;外用给药透皮吸收良好。【谱图】 http://ng1.17img.cn/bbsfiles/images/2012/08/201208142206_383898_1609970_3.jpg
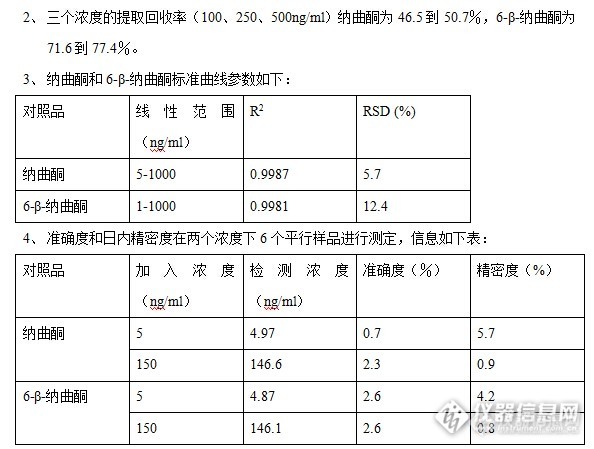
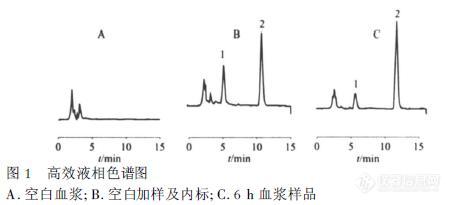
血清中纳曲酮及其代谢物6-β-纳曲酮醇的高效液相色谱分析 纳曲酮是一种阿片受体拮抗剂,其用于酒精中毒治疗及阿片类药物依赖已有几十年的历史,一些临床试验已证明纳曲酮是一种有效的酒精中毒辅助用药。临床已经证明纳曲酮相比安慰剂能够减少嗜酒复发率和对酒精的渴望。服用纳曲酮后经过快速和广泛的肝脏代谢由酶将酮还原为主要代谢物6-β-纳曲酮醇及其他代谢产物:(如下图)http://ng1.17img.cn/bbsfiles/images/2014/12/201412302127_530344_2184412_3.jpg 与纳曲酮相比6-β-naltrexol阿片受体拮抗剂作用较弱,但其仍对于疗效有贡献,因为其在体内浓度甚至高于纳曲酮。纳曲酮及其代谢物大多是以共轭形式存在。在肝硬化及其他严重的肝脏疾病中这种纳曲酮到6-β-naltrexol的代谢会有减少。随着药物治疗临床检测的发展,本次试验意于开发一种纳曲酮到6-β-naltrexol在人体血清中的同时检测手段。材料与方法:纳曲酮、6-β-纳曲酮醇、色谱甲醇纳曲酮和6-β-纳曲酮醇储备溶液制备成含1 mg/ml的甲醇溶液。储备溶液用于制备标准曲线溶液,浓度范围0-1ug/ml, 所有的校准标准,空白和质量控制样品, 均配置在空白血清中;所有缓冲液,制备用去离子水。临床采样:样品来自87个酗酒后的受试者,酗酒者采用双盲实验,设安慰剂对照组和药物治疗组,来评估对酒精依赖的作用。入选标准为18-65岁酒精依赖者。纳曲酮(盐酸纳曲酮)是每天早上50毫克口服,为期三个月。血液样品收集于服药后约2-4小时,空白血清样品采集于第一周、第二周和第八周,并使其凝固,离心(4000转[font=Times New Rom
热解吸做voc中丁酮和甲醇峰分不开?用的是wax柱子,请问各位老师还能怎么分离开?第一个峰是丙酮,第二峰是乙酸乙酯,第三个峰是溶剂甲醇峰覆盖目标丁酮。[img]https://ng1.17img.cn/bbsfiles/images/2018/11/201811171633448269_6611_3333718_3.png[/img]
我们有发酵液,内含有丙酮、正丁醇、乙醇如何分离,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]参考条件
我们需做苯乙酮还原成苯乙醇的反应无副反应,想测其转化率。以前都是用的是面积归一法做,但他想用更精确点的办法解决,请问除了内标法外,是不是可以用测出那两种物质的响应因子来解决?还是用面积归一法就可以了?测响应因子该怎么测?
火焰法测海水中的锌用甲基异丁基酮提纯 请问怎么提纯?
三氯杀螨醇在丙酮中的稳定性 关于在有机溶剂中农药稳定性问题,有人发现:三氯杀螨醇标液在棕色小瓶室温下持续6个小时的稳定性试验,三氯杀螨醇在丙酮中迅速降解。大家平时实验时有没有发现这种现象?
版友求助:聚乙烯醇(药用辅料)的残留溶剂测定中,为什么供试溶液中检测出内标物(丙酮)的峰面积会变小?
有人在实验室做完丙酮氰醇的实验室吗?按照指标测定其纯度,硫酸含量,氢氰酸含量,水分含量,这东西听说狠毒,在做的过程中会不会挥发害人,看网上报道很可怕的,有经验的能否告知宝贵的测试经验?
我在用测试乙醇丙酮等等挥发性物质,ICP老是熄火(稀释至少100倍),不知道大家如何测试这些物质的重金属含量的?谢谢
今年,单位要拓展检测能力范围,要开始检测“黄曲霉毒素B1、脱氧雪腐镰刀菌烯醇、玉米赤霉烯酮”了,要求在液质上建立方法,毒性太大,如果操作有哪些注意事项----心有余悸,求破解!
【讨论】做醇类物质通常用什么柱子,而做酮呢?最近常做醇或酮类物质杂质分析,而且杂质含量很低,也不知自己检测量对不对?我做醇和酮一般都用DB-1 的柱子,但我看别人好象也用HP-1和HP-5,希望有高手能发表一哈建议,到底用哪种柱子最好???
想要分析水中溶解的挥发性物质,丁酮及甲醇。我使用的机子是岛津GC-17A,inj:110,col:40度,2度/分到50度,50度保持时间5分,DET:300度。出来的峰重合在一齐,不知道有什么方法让他们分离!!
Fapas 鸡蛋中喹诺酮和氟喹诺酮的测定 02200 有木有一起的啊? 大家讨论一下结果?
请问六氟异丙醇进高效液相色谱前可以用什么针筒式滤膜过滤呢?
求异丙醇和丙酮的单纯用岛津顶空溶残法区别,出峰位置都是3.7左右
请问,分析杂醇油需具备什么样的色谱条件,另外请介绍六、八、十通阀等的进样原理,可使样品气切换到不同的柱子吗?
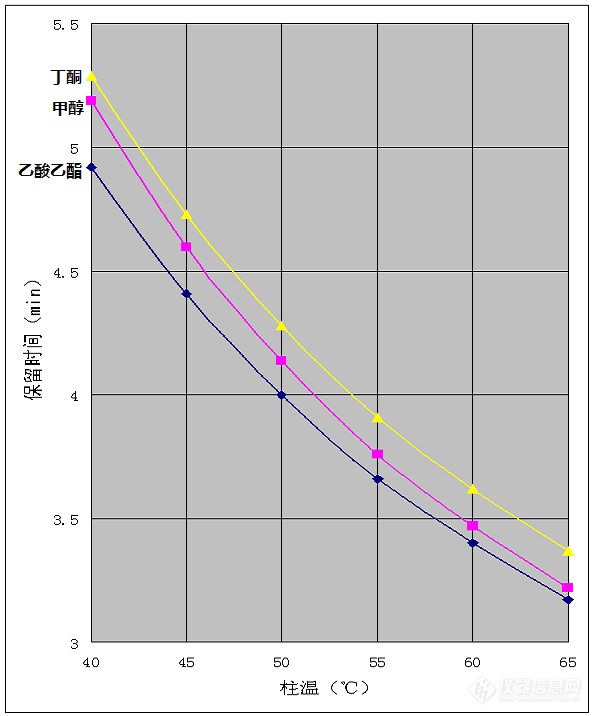
溶剂残留分析是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的重要应用之一,在药品、食品、包装等领域都是必测的项目。常见溶剂中涉及到的检测目标物经常有乙酸乙酯、甲醇、丁酮,以及二甲苯异构体这几项。最近看到 @m3091333、@p3109800、@Insm_c1196d2b 等多人发帖子讨论相关问题,我从原理上进行了一些解释,但终究纸上谈兵,于是找别的实验室要了这几种试剂,用实践检验了一下。首先,如果二甲苯异构体不要求分离,用624柱可以很容易的解决问题,这里就不讨论了。如果要求乙苯、对二甲苯、间二甲苯、邻二甲苯四种异构体分离,用624柱是无法完成的。因为二甲苯异构体色散力差异非常小,只能靠诱导力的差异分离,不同异构体在强极性柱上的极化率不同,乙苯极化率最低,其次是对二甲苯、间二甲苯,邻二甲苯极化率最大,出峰时间也随极化率的增加而延长。而624柱的极性比较弱,不能产生足够的极化作用,特别是对二甲苯与间二甲苯的极化差异非常小,无法实现分离。这个问题是由分子结构决定的,无论怎么调节色谱条件都不能解决。要想解决只能换强极性柱,常见的就是聚乙二醇柱,包括各种wax柱和FFAP柱等。三氟丙基柱也是强极性的,可以分离二甲苯异构体,但是这种柱很少使用。在聚乙二醇类的色谱柱上,乙酸乙酯、甲醇、丁酮三种目标物分离困难,各种类型的聚乙二醇柱选择性略有差异,但这三种物质都是较为接近的,想要分离是不太容易的。但是这三种物质与聚乙二醇固定相之间的作用力存在本质上的差异,因此通过调整柱温条件是可以分离的。下面三幅图是用60米*0.53mm*1um的INNOWAX柱分离乙酸乙酯、甲醇、丁酮的效果,柱温分别是40℃、50℃、60℃。[img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157168864_5041_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157170984_7926_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157172914_736_2204387_3.png!w690x796.jpg[/img]图中很明显,柱温低时甲醇与丁酮出峰时间接近分不开,高温时甲醇与乙酸乙酯出峰时间接近分不开,温度适中时三者可以实现分离。虽然未达到基线分离,但分离度都超过1,用来定量是完全可以的。这是找别人借的一根旧柱子,柱效只有4万塔板,如果是新柱子柱效应该能达到七八万塔板,分离度肯定更高,如果是0.32mm口径的柱子分离就更没问题了。要强调的是,能够实现分离的条件并不是完全靠盲目尝试获得的。我们看一看三种目标物的保留时间随柱温的变化就能发现其中的规律,见下图:[img=,594,716]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022156374904_6999_2204387_3.png!w594x716.jpg[/img]图中可以看出,三种目标物的保留时间都是随温度升高而减小的,但是减小的幅度却并不相同。甲醇的保留时间随温度升高而减小的幅度明显大一些。这是因为甲醇具有羟基,与聚乙二醇固定相的相互作用力以氢键为主,氢键的强度随温度升高而迅速减弱。而乙酸乙酯、丁酮与聚乙二醇固定相的作用力都是以诱导力和取向力为主,这种力是由分子偶极矩决定的,受温度的影响要小一些。甲醇峰位置在乙酸乙酯与丁酮之间,温度升高时保留时间都减小,但甲醇减小更多,于是甲醇与乙酸乙酯靠的更近,与丁酮的分离度提高。温度降低时保留时间都增大,但甲醇增大更多,于是甲醇与丁酮靠的更近,与乙酸乙酯的分离度提高。用其他的柱子,如DB-wax或者FFAP时,各组分之间的相对位置会有差别,甚至有时出峰顺序都会变,但是保留时间随温度变化的这种规律仍然是适用的。所以遇到分不开的情况,一定不要盲目的乱试一通,也不用盲目的换柱子,一定要把问题想明白,有针对性的优化条件。最后要强调的是,这里虽然是以溶剂检测为例讨论了如何只用一根柱子就实现分离,但实际样品很复杂,并不是每次都能通过这种优化实现全部分离目的。所以色谱实验室配备多种不同极性的色谱柱是非常重要的。特别是做复杂样品时,即使谱图上看起来分离不错,最好也能用另外一种柱子进行一次验证,以免实际样品中有干扰物共流出,造成假阳性。
热脱附的冷肼填料是Tenax TA (应该是20mg)推荐的一级解吸条件:样品管脱附温度300℃,脱附流量40ml/min 脱附10min,冷肼5℃。这样算起来冷肼Tenax TA在5℃通过的流量有400ml丙酮,异丙醇是否穿透了?所以想看看Tenax TA 对丙酮,异丙醇在不同温度下的安全采样体积数据或者上哪里可以查?
不知道各位有没有人做过异丙基托品醇这种物质的检测,异丙基托品酮为异丙基托品醇的已知杂质,两者结构比较相近,在气相条件下难分离,在薄层条件也做过一次,两种物质比较难实现分离。忘各位能够提供一些实验方向能使两者实现分离。
[color=#444444]最近在做苯乙酮和1-苯乙醇的化学实验,想用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行分析,结果发现两个的沸点相差很近,请问这种情况下应该怎么样进行测试,[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的操作应该注意什么,苯乙酮的沸点是202.3度,1-苯乙醇的是203.4度,谢谢大家[/color]
用甲醇钠制得丁酮烯醇钠,计算收率的时候用什么方法来确定干燥品中丁酮烯醇钠的占比是多少呢?
有做过HJ895-2017 水质 甲醇和丙酮的吗?为什同样的标曲绘制出来,丙酮可以,甲醇却不行?
求[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]中以下校正因子:水-乙醇 水-甲醇 水-丙酮 正丁醇-乙醇 正丁醇-甲醇 正丁醇-丙酮还有乙醇、甲醇、丙酮、正丁醇的密度表~~谢谢
频那酮和甲醇要分离 液相怎么做啊 什么条件呢