今天我们聊一款小众的色谱柱-氨基色谱柱,如果大家在实际使用过程中有遇到,可以参考。在高效液相色谱(HPLC)中,氨基色谱柱(NH2柱)是一种常用于正相和亲水性相互作用液相色谱(HILIC)的色谱柱。它通常用于分离糖类、脂溶性维生素、核苷酸和水溶性维生素等物质。 01.氨基色谱柱的组成 1)色谱柱管:色谱柱管通常是由不锈钢制成管状结构,用于容纳填料。 2)填料:通常由硅胶或聚合物基质组成。在氨基色谱柱中,填料是在硅胶或聚合物基质上键合了氨基(-NH2)官能团的球形颗粒。这些颗粒具有均匀的孔径分布,允许不同大小的分子进入孔隙内部。氨基官能团提供了亲水性相互作用和弱阴离子交换的特性,适合于分离极性化合物。 02.氨基色谱柱的分离机制 1)HILIC模式:在这种模式下,氨基色谱柱用作亲水性相互作用色谱柱,适用于糖类、糖醇等化合物的分析。流动相通常是水和有机溶剂(如乙腈)的混合物,通过调整流动相中水和有机溶剂的比例,可以控制分析物的保留行为。在HILIC模式下,氨基色谱柱的氨基提供了与极性化合物相互作用的位点,通过氢键和偶极-偶极相互作用实现保留 。 2)弱阴离子交换模式:在酸性流动相条件下,填料表面带正电荷,适用于水溶性维生素或核苷酸类的分析。这种模式下,氨基色谱柱的氨基官能团可以作为弱阴离子交换位点,通过离子交换作用保留带负电荷的分析物 。 3)正相模式:氨基色谱柱也可以在正相色谱中使用,分析酸性物质、烃类化合物、维生素A和D等。在正相色谱中,通常使用非极性流动相,氨基柱的氨基官能团可以与分析物形成氢键或其他极性相互作用 。(较少) 03.氨基色谱柱使用的注意事项 1)使用前: a. 检查色谱柱包装和标签:确保色谱柱没有物理损伤,确认色谱柱的规格和填料类型符合实验需求。 b. 阅读说明书:[font=&]仔细阅读色谱柱的使用说明书,了解色谱柱的pH稳定性范围、最大操作压力等参数。 c. 系统冲洗:使用适当的溶剂冲洗色谱系统,确保系统中没有气泡和污染物。 d. 色谱柱平衡:柱子需要用流动相平衡,直到基线稳定。HILIC模式下,通常需要平衡4~5小时。(有些甚至过夜平衡)注:如果上一个试验是无机盐的流动相试验,需要对仪器进行充分的冲洗,怕产生盐析;同理,如果是做了氨基柱的试验换成无机盐试验,也是要充分冲洗。 2)使用中: a. 流动相组成:确保流动相组成适合分析物和色谱柱,严格控制pH值在色谱柱的允许范围内(通常是pH 2-8)。注:如果是是无机盐与有机相的混合流动相,要注意加入的先后顺序,可能会有结晶析出 b. 样品溶解性:样品应在流动相中完全溶解,避免在柱上沉淀。 c. 流速控制:设置合适的流速,以获得最佳分离效果。 d. 样品负载:避免超载,以保持色谱峰形和分辨率。 e. 温度控制:根据需要调整柱温,以优化分离效果。 3)使用后: a. 柱子清洗:分析完成后,使用适当的溶剂冲洗色谱柱,以去除可能的污染物。 注:如果是含有无机盐-有机相的流动相 这个冲洗要先含有较多水的有机相进行冲洗(如95%水-乙腈),除盐→然后再转到高有机相冲洗(如95%乙腈水),除杂→再过渡置换成保存溶液 一般不要使用100%水冲洗色谱柱,氨基会水解。 b. 柱子保存:短期内如果不用,可以用与流动相相同组成的溶剂保存。长期不用,建议用色谱柱出厂时的保存液(如100%异丙醇)保存。 c.记录使用情况:记录色谱柱的使用情况,包括分析的样品、使用条件和色谱柱表现,以便于追踪柱效和寿命。 04.氨基色谱柱使用的局限性 1)pH值限制:氨基色谱柱的氨基官能团对pH值较为敏感,通常推荐的pH值使用范围是2-8。超出这个范围可能会加速氨基官能团的水解,从而缩短色谱柱的使用寿命。 2)溶剂兼容性:在反相条件下使用时,需要注意流动相中水的比例和pH值,因为高比例的水和极端的pH值可能导致官能团水解。 3)样品极性:氨基色谱柱对极性化合物的分离效果较好,但对非极性化合物的分离能力相对较弱。 4)样品负载:样品浓度和负载量不宜过高,以避免超载现象,导致色谱峰形变宽和分辨率下降。 5)温度敏感性:虽然适当的温度升高可以提高某些极性化合物的溶解度和分离效率,但过高的温度可能会加速色谱柱的老化。 6)缓冲盐类:如果流动相中含有缓冲盐,需要特别注意在分析前后使用不含盐的流动相进行适当的过渡,以避免盐类在柱内的析出。 7)保存溶剂:新购买的氨基柱的保存溶剂可能与使用的流动相不互溶(可能出厂保存在正相溶剂中,一般要用异丙醇置换),需要使用适当的溶剂进行过渡。 https://ng1.17img.cn/bbsfiles/images/2024/10/202410081129146844_2050_3203140_3.png!w490x14.jpg 总结一下:氨基色谱柱(NH2柱)在高效液相色谱(HPLC)中的角色有点像个分类专家,它通过分子的极性来区分它们。这种色谱柱是由不锈钢管和特殊填料构成的,填料上的氨基官能团能够与极性分子亲和,帮助我们把不同的分子分开。使用时,得注意几点:首先,pH值要控制在2到8之间,这样氨基官能团才能稳定工作。其次,样品要在流动相中溶解得好,免得在柱子里堵路。流速和温度也要适当调整,以保证分离效果。用完以后,别忘了用合适的溶剂冲洗,短期保存可以用流动相,长期的话最好用出厂时的保存液。氨基色谱柱虽然对极性分子分离有一手,但对非极性分子就不太灵了,而且它的分辨率和灵敏度可能不如其他类型的色谱柱。所以,如果你的样品极性很强,氨基色谱柱是个好选择,但要是分子大小差不多,或者你需要高分辨率和灵敏度,那就可能得考虑其他色谱柱了。总的来说,氨基色谱柱是个实用的工具,特别适合分析那些对环境条件敏感的极性分子。
承接上回,我们说了一下氨基色谱柱的原理、构造、分离机制、使用过程中的注意事项及它的局限性,今天主要说说它的维护保养和相关的注意事项,色谱柱固有一死,但好的操作还是能延缓它的生命周期的。 01.氨基色谱柱的维护由于氨基柱是一款既可以正相使用,也可以反相使用,但是我们要注意到的是:正相溶剂和反相溶剂往往是不互溶的,正常情况新氨基柱出厂时保存在正相环境中(如Luna的氨基柱保存在正己烷-乙腈(99:1)中)。 1)正相体系的维护 a. 推荐先用正己烷-乙腈(99:1)以0.5ml/min的流速冲10倍柱体积,再根据流动相选用极性相近的氯仿或二氯甲烷以相同的流速冲10倍柱体积,最后换成你实验的流动相。 b. 正相使用时,不宜分析含醛基、羰基的化合物,不可用于还原糖的分析;流动相要彻底脱气,并不得含有羰基化合物和过氧化物(质量不好的乙醚、四氢呋喃含有少量)。 c. 任何时候更换流动相时都要确保新流动相与柱子原保存液可互溶。d. 使用前要确认仪器是否耐受正相溶剂,如果泵相关的密封圈组件不耐受,会造成损害。 2)反相体系的维护以上述色谱柱保存在正相溶剂正己烷-乙腈(99:1)为例,一般用以下方法进行置换操作: a. 在进行过渡置换前,需要把仪器的整个系统都用异丙醇冲洗(你需要测柱效涉及的管路),包括检测器,保证仪器是无水的一个状态。 b. 由于新的氨基柱保存在正己烷-乙腈(99:1)中,与反相流动相是不互溶的,因此如果使用反相的方法,[color=#595959]必须用至少10倍柱体积的异丙醇冲洗过渡(至少2h,0.5mL/min),以除去正相保存溶液。过渡过程中注意因异丙醇粘度较大,会导致柱压很高,适当调低流速即可。 c. 再用至少10倍柱体积95%水-5%乙腈(或甲醇)冲洗(不含缓冲盐的流动相可省去)过渡,最后用流动相平衡。(可能每家色谱柱会有不同,但是就是不建议用100%的水去过渡色谱柱) d. 用完后洗柱时,必须先用95%水冲洗至少10倍柱体积,除去所用缓冲盐(不含缓冲盐的流动相可省去)。然后保存于乙腈/水(80:20)溶液(一个月内)中。长期不用的话,建议用异丙醇保存(一个月以上)。(不同厂家的色谱柱可按照说明书执行)其他:当使用氨基柱进行酸性物质的分析时,酸性物质的存在意味着质子的存在,可能会使略带负电荷的氨基官能团质子化,导致使用一段时间后对于某些类的分析物保留性质有所改变或表现在柱效下降。---------建议用10-15倍的柱体积的为pH=11 NH3的乙腈-水(50:50)溶液冲洗该柱(冲洗后当然要再用不含碱的流动相洗去多余氨),之后再进行分析这类酸性分析物时建议在流动相中略微添加少许氨如0.1%。 注:反相条件下使用时,要特别注意控制pH值范围(根据你色谱柱耐受使用pH),pH值越低越有发生水解的危险,流动相中水的比例越高当然也越有发生水解的危险。 02.氨基色谱柱的注意事项[font=PingFang SC, system-ui, -apple-system, BlinkMacSystemFont, Helvetica Neue, Hiragino Sans GB, Microsoft YaHei UI, Microsoft YaHei, Arial, sans-serif]关于它的注意事项,前面也上一篇也基本涵盖了使用中的注意事项和它自身的一些局限性的事项,这里就不再重复阐述,详见高效液相色谱基础篇|关于氨基色谱柱使用的小知识。这里只是再次提醒大家在使用过程中强调注意的几点: 1.如果用正相体系,确保仪器可耐受; 2.如果用反相体系,仪器要充分的平衡; 3.如果柱子保存是正相溶剂,仪器也要充分的过渡,以免溶液分层造成检测器波动; 4. 如果是反相体系,流动相平衡时间要长(至少6个小时跑不了,我一般都过夜平衡) 5. 及时记录色谱柱状态,做好维护管理;如果氨基水解了,一般较难再生,建议更换。 https://ng1.17img.cn/bbsfiles/images/2024/10/202410081133544526_2231_3203140_3.png!w490x14.jpg 总结一下:氨基色谱柱的维护保养其实挺讲究的。首先,你得搞清楚你的柱子是正相用还是反相用,因为这俩用的溶剂不互溶。如果是正相,就用正己烷-乙腈之类的冲一冲,换成氯仿或者二氯甲烷再冲冲,最后换成你的流动相。正相的时候别用那些含醛基、羰基的化合物,也别分析还原糖。反相的话就稍微复杂了点,先得用异丙醇把仪器整个系统冲洗一遍,确保无水状态。然后,因为新柱子有些是正相溶剂里保存的,所以得用异丙醇过渡,至少冲个两小时,避免正相溶剂在仪器中与其他溶液分层。接着用不含缓冲盐的水-乙腈(或甲醇)冲洗,最后用流动相平衡。用完记得先用95%的水冲洗,再保存在乙腈/水溶液中,长期不用的话就用异丙醇。还要注意的是,如果你分析的是酸性物质,氨基柱可能会质子化,影响保留性质或者柱效。这时可以用pH=11的NH3的乙腈-水溶液冲洗,分析时流动相里稍微加点氨。最后,使用前要注意仪器是否耐受正相溶剂,反相体系要充分平衡,柱子保存的如果是正相溶剂,仪器也要充分过渡。反相体系的流动相平衡时间要长,至少得过夜。同时也要及时记录柱子的状态,做好维护。如果氨基水解了,那柱子就差不多该换了。
需要用HLCP分析糖类物质,但组里是C18柱,不好用来分析糖类,所以请教以下几种柱子大概的价格,看看老板能不能给买,谢谢各位!sugar SH1011(shodx,srnmDx300mm)氨基色谱柱还有这个是[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]用的柱子:AminoPac PA10
蒸发光散射检测器要求聚合物基质的氨基柱,但是Waters的BEH技术也是硅胶基氨基色谱柱,请问原理在哪里?硅胶基氨基色谱柱用在蒸发光散射检测器上柱流失致其背景很高。!
月旭科技官网上的qq以及客服人员怎么都不在线啊,想咨询他们的氨基柱情况,有知道去哪里咨询吗
如题:对氨基苯磺酰胺与对氨基苯磺酸在亚硝酸盐的测定中有区别吗?为什么水中亚硝酸盐的测定GB/T5750。5-2006中用到的是对氨基苯磺酰胺;而食品GB/T5009.34-2008中用到的却要求是对氨基苯磺酸.我们检测水的时候也是用对氨基苯磺酸,你们说对检测结果会有影响吗
1,现在准备分析含2,3单糖的寡糖,waters氨基柱比较贵,4660,能推荐其他厂家的、质量还行的氨基柱吗,比如原装kromasil的怎样?2,想配制总价在100-160K 的液相,做前期探索实验;单泵,手动进样,紫外检测器,配国产柱温箱;如果条件许可想换四元泵。(大实验室另有Agilent1100,自动进样,四元泵,紫外阵列,荧光)。岛津LC-20A相对便宜,服务好像不太好,岛津以前的质量还行(以前课题组一GC用了10多年),现在不知道怎样?。Agilent比较贵。选择岛津还是Agilent比较好?大家帮助分析一下。
最近老师要求让我买根氰基色谱柱,不知道是否适合分离生物样品?
在解红外光谱时常分不出来胺基(酰胺基)是与苯环相连的。还是在苯环侧链上。
求助五羟基色氨酸的紫外光谱图,急用。多谢各位大虾的帮助,先谢了!
磺胺药物对氨基苯磺酰胺的合成目的原理Ar-NHCOCH3 + 2HOSO2Cl → p-ClO2S-Ar-NHCOCH3+ HClp-ClO2S-Ar-NHCOCH3 + NH3 → p-CH3CONH-Ar-SO2NH2 + HClp-CH3CONH-Ar-SO2NH2 + H2O → p-H2N-Ar-SO2NH2 + CH2CO2H仪器药品乙酰苯胺(自制) 5g(0.037mol);氯磺酸(d=1.77) 22.5g(12.5ml,0.19mol);浓氨水(28%,d=0.9) 35ml 浓盐酸,碳酸钠。过程步骤(1)对乙酰氨基苯碘酰氯在100ml干燥的锥形瓶中,加入5g干燥的乙酰苯胺,在石棉网上用小火加热熔化。瓶壁上若有少量水气凝结,应用干净的滤纸吸去。冷却使熔化物凝结成块。将锥形瓶置于冰浴中冷却后,迅速倒入12.5ml氯磺酸,立即塞上带有氯化氢导气管的塞子。反应很快发生,若反应过于激烈,可用冰水浴冷却。待反应缓和后,旋摇锥形瓶使固体全溶,然后再在温水浴中加热10~15min使反应完全。将反应瓶在冷水中充分冷却后,于通风中在充分搅拌下,将反应液慢慢倒入盛75g碎冰的烧杯,用少量冷水洗涤反应瓶,洗涤液倒入烧杯中。搅拌数分钟,并尽量将大块固体粉碎,使成颗粒小而均匀的白色固体。抽滤收集,用少量冷水洗涤,压干,立即进行下一步反应。(2)对乙酰氨基苯磺酰胺将上述粗产物移入烧杯中,在不断搅拌中慢慢加入17.5ml浓氨水(在通风橱内),立即发生放热反应并产生白色糊状物。加完后,继续搅拌15min,使反应完全。然后加入19ml水,在石棉网上用小火加热10~15min,并不断搅拌,以除去多余的氨,得到的混合物可直接用于下一步合成。(3)对氨基苯磺酰胺(磺胺)将上述反应物放入圆底烧瓶中,加入3.5ml浓盐酸,在石棉网上用小火加热回流0.5h。冷却后,应得一几乎澄清的溶液,若有固体析出,应继续加热,使反应完全。如溶液呈黄色,并有极少量固体存在时,需加入少量活性炭煮沸10min,过滤。将滤液转入大烧杯中,在搅拌下小心加入粉状碳酸钠至恰呈碱性(约4g)。在冰水浴中冷却,抽滤收集固体,用少量冰水洗涤,压干。粗产物用水重结晶(每克产物约须12ml水),产量3~4g。熔点161~162℃。纯品对氨基苯磺酰胺为白色针状结晶,熔点163~164℃。注意事项1.氯磺酸对皮肤和衣服有强烈的腐蚀性,暴露在空气中会冒出大量氯化氢气体,遇水会发生猛烈的放热反应,甚至爆炸,故取用时需加小心。反应中所用仪器及药品皆需十分干燥,含有氯磺酸的废液不可倒入水槽,而应倒入废液缸中。工业氯磺酸常呈棕黑色,使用前宜用磨口仪器蒸馏纯化,收集148~150℃的馏分。2.酰磺酸于乙酰苯胺的反应非常剧烈,将乙酰苯胺凝结成快状,可使反应缓和进行,当反应过于激烈时,应适当冷却。3.在氯磺化过程中,将有大量氯化氢气体放出。为避免污染室内空气,装置应严密,导气管的末端要与接受器内的水面接近,但不能插入水中,否则可能倒吸而引严重事故!4.加入速度必须缓慢,必须充分搅拌,以免局部过热而使对乙酰胺基苯磺酰胺水解。这是实验成功的关键。5.尽量洗去固体所夹杂和吸附的盐酸,否则产物在酸性介质中放置过久,会很快水解,因此在洗涤后,应尽量压干,且在1~2h内将它转变为磺胺类化合物。6.粗制的对氨基苯磺酰氯久置容易分解,甚至干燥后也不可避免。若要得到纯品,可将粗产物溶于温热的氯仿中,然后迅速转移到事先温热的分液漏斗中,分出氯仿层,在冰水浴中冷却后即可析出晶体。纯品对氨基苯磺酰氯的熔点为149℃。7.为了节省时间,这一步的粗产物可不必分出。若要得到产品,可在冰水浴中冷却,抽滤,用冰水洗涤,干燥即可。粗品用水重结晶,纯品熔点为219~220℃。8.对乙酰胺基苯磺酰胺在稀酸中水解成磺胺,后者又与过量的盐酸形成水溶性的盐酸盐,所以水解完成后,反应液冷却时应无晶体析出。由于水解前溶液中氨的含量不同,加3.5ml盐酸有时不够,因此,在回流至固体全部消失前,应测一下溶液的酸碱性,若酸性不够,应补加盐酸回流一段时间。9.用碳酸钠中和滤液中的盐酸时,有二氧化碳产生,故应控制加热速度并不断搅拌使其逸出。磺胺是一两性化合物,在过量的碱溶液中也易变成盐类而溶解。故中和操作必须仔细进行,以免降低产量。分析思考 1.为什么在氯磺化反应完成以后处理反应混合物时,必须移到通风橱中,且在充分搅拌下缓缓倒入碎冰中?若在未倒完前冰就化完了,是否应补加冰块?为什么?2.为什么苯胺要乙酰化后在氯磺化?直接氯磺化行吗?3 .如何理解对氨基苯磺酰氨是两性物质?试用反应式表示磺胺与稀酸和稀碱的作用。
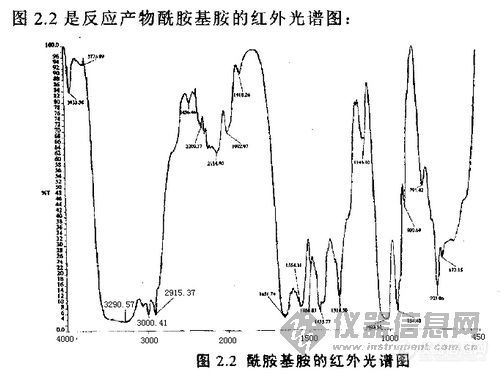
间苯二甲胺 和 己二酸反应生成 酰胺基胺,可是红外光谱上只能看见仲酰胺基的特征吸收峰,为什么看不到伯胺的峰?3000.41和2915.37处是不是伯胺吸收峰?是不是往后挪了?[img]http://ng1.17img.cn/bbsfiles/images/2009/06/200906080958_154498_1608859_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2009/06/200906080958_154497_1608859_3.jpg[/img]
请问老师,如果用光谱的方法进行盐水溶液中的苯胺和多胺(2,2-二氨基二苯基甲烷,2,4-二氨基二苯基甲烷,4,4-二氨基二苯基甲烷,N-甲基二氨基二苯基甲烷)含量的测定,它们的吸收峰是多少???
请帮忙推荐几款用于氨基,表面活性剂分析用色谱柱,需要明确的参数和价格,谢谢
请问老师:如何分析盐水溶液中的苯胺和多胺(2,2-二氨基二苯基甲烷,2,4-二氨基二苯基甲烷,4,4-二氨基二苯基甲烷,N-甲基二氨基二苯基甲烷)含量??含量在几个到几十个PPM
[align=center][b]新型氨基键合色谱柱对《2015版中国药典》乳糖含量测定方法的建立[/b][/align][b] 摘要 目的:[/b]本文根据《2015版中国药典》四部乳糖项下含量测试方法,采用高效液相色谱-示差折光检测器(HPLC-RI) 法对乳糖与蔗糖进行了液相色谱分检测方法研究,建立了乳糖含量测定的HPLC法。实验过程中考察了月旭公司三种不同类型的氨基键合硅胶色谱柱对乳糖和蔗糖的保留及分离情况。[b]结果:[/b]结果表明:按照《2015版中国药典》四部乳糖项下的条件,流动相为乙腈:水=70 : 30(v/v),使用月旭Xtimate[sup][/sup]Lactose-NH[sub]2 [/sub]氨基色谱柱(5 μm, 4.6×300 mm) 对两种物质的分离度为3.03,实现了乳糖和蔗糖的良好分离,且各物质峰形良好,峰面积的RSD仅为1.13%,远小于药典规定的2.0%,保留时间稳定。[b]结论:[/b]本文建立的方法完全满足《2015版中国药典》四部项目乳糖含量测定的要求。[b]1引言[/b][color=#333333]乳糖是一种双糖,英文名称为[/color][color=#333333]Lactose[/color][color=#333333];由一分子[/color][color=#333333]β-D-[/color][color=#333333]半乳糖和一分子[/color][color=#333333]α-D-[/color][color=#333333]葡萄糖在[/color][color=#333333]β-1[/color][color=#333333],[/color][color=#333333]4-[/color][color=#333333]位形成糖苷键相连,如图[/color][color=#333333]1[/color][color=#333333]所示。分子式[/color][color=#333333]C[sub]12[/sub]H[sub]22[/sub]O[sub]11[/sub][/color][color=#333333],摩尔质量[/color][color=#333333]342.3[/color][color=#333333]。有两种端基异构体:[/color][color=#333333]α-[/color][color=#333333]乳糖和[/color][color=#333333]β-[/color][color=#333333]乳糖,在水溶液中可互相转化。[/color][color=#333333]α-[/color][color=#333333]乳糖很容易结合一分子结晶水。[/color]乳糖作为一种药用辅料,以填充剂或稀释剂的形式广泛应用于片剂、胶囊、颗粒剂和冻干产品中。然而,一般药用乳糖来源于牛奶,可能存在可引起过敏反应的杂蛋白。因此,《2015版中国药典》在“有关物质”和“含量测定”项目中,药典对色谱条件的规定为:用氨基键合色谱硅胶为填充剂;以乙腈-水(70 : 30)为流动相;示差检测器检测;柱温为45 [sup]o[/sup]C,检测器温度为40[sup] o[/sup]C。但是,实验过程中发现,用市面上普通氨基键合硅胶色谱填料进行该项目的测试定时,经常会遇到以下问题:(1)柱效达不到5000的理论塔板数,不能满足《2015版中国药典》要求;(2)蔗糖和乳糖的分离度不能达到基线分离;(3)峰面积的RSD不能达到2.0%以下,无法对乳糖进行准确的定量。究其原因,是因为普通氨基键合硅胶色谱填料存在氨基基团容易在酸性条件下质子化、并且在氨基键合硅胶色谱填料在高比例水相色谱条件下容易水解脱落等问题。[align=center][img=,255,190]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230853_01_2451449_3.png[/img][/align][align=center]图1:乳糖分子化学结构式[/align]本文基于上述乳糖在液相色谱含量测定过程中存在的问题,进行了氨基官能团键合工艺的改进,从而开发了新型Xtimate[sup][/sup]Lactose-NH[sub]2[/sub]氨基色谱填料。该氨基键合硅胶色谱填料采用独特的键合工艺,所制备的填料增强了氨基基团在硅胶表面的键合稳定性,使得氨基基团的耐水性大大提高,氨基基团更不容易从硅胶表面脱落,从而解决了《2015版中国药典》乳糖含量测定存在的上述众多问题。[b]2 实验部分 2.1.主要仪器与试剂[/b]高效液相色谱仪(Agilent 1260,美国安捷伦公司) 洁盟牌超声波清洗器(深圳市洁盟清洗设备有限公司);XW-80A涡旋混合仪振荡器(海门市其林贝尔仪器制造有限公司);月旭Xtimate[sup][/sup]Lactose-NH[sub]2[/sub]氨基色谱柱(5μm, 4.6×300 mm)、月旭Ultimate[sup][/sup]XB-NH[sub]2[/sub]氨基色谱柱(5μm, 4.6×250 mm)以及月旭Topsil[sup][/sup]NH[sub]2[/sub]氨基色谱柱(5μm, 4.6×250mm),上述三种氨基色谱柱均购于浙江月旭材料科技有限公司。乳糖和蔗糖对照品 (含量大于99.0%) 购于中国食品药品检定研究院。乙腈为 HPLC 级,购于德国 Merck 公司,实验用水为娃哈哈超纯水(杭州娃哈哈集团有限公司)。[b]2.2 方法色谱条件色谱柱:[/b]月旭Xtimate[sup][/sup] Lactose-NH[sub]2[/sub]氨基色谱柱(5μm, 4.6×300 mm),月旭Ultimate[sup][/sup]XB-NH[sub]2[/sub]氨基色谱柱(5μm, 4.6×250 mm)以及月旭Topsil[sup][/sup]NH[sub]2[/sub]氨基色谱柱(5μm, 4.6×250 mm)[b]流动相:[/b]乙腈 : 水=70 : 30[b]柱温:[/b]柱温45 [sup]o[/sup]C,检测池40 [sup]o[/sup]C[b]流速:[/b]1.0 ml/min[b]进样量:[/b]10 μL[b] 2.3溶液的制备2.3.1[/b]混合对照溶液取乳糖对照品与蔗糖对照品各适量,精密称定,加水溶解并稀释制成每lmL各含l.0 mg的溶液。分别取10 μL混合对照品溶液,注入液相色谱仪,考察各种氨基色谱柱的色谱性能和分离情况。[b]2.3.2[/b]供试品溶液取供试品,精密称量,加水溶解并定量稀释制成每1mL约含乳糖1mg的溶液,精密量取10 μL,注入液相色谱仪。[b]3结果与分析[/b]图2为使用月旭常规的Ultimate[sup][/sup] XB-NH[sub]2[/sub]氨基色谱柱对乳糖和蔗糖混合对照溶液的测定效果图。由图1可以发现:使用常规的Ultimate[sup][/sup] XB-NH[sub]2[/sub]氨基色谱柱进行该项目的测定时,其乳糖的柱效为8466,满足《2015版中国药典》乳糖检测项下对柱效规定为5000的要求。进一步进行测定,连续进样五针混合对照混合溶液,如图3所示。发现峰面积的RSD为2.72%,大于《2015版中国药典》规定的2.0%。因而综合判断,常规的Ultimate[sup] [/sup]XB-NH[sub]2[/sub]氨基色谱柱无法满足《2015版中国药典》项下乳糖含量测定的要求。[align=center][img=,506,386]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230857_02_2451449_3.png[/img][/align][align=center]1,蔗糖;2,乳糖[/align][align=center]图2. 采用月旭Ultimate[sup][/sup]XB-NH[sub]2[/sub]测定混合对照溶液色谱图[/align][align=center][img=,543,428]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230857_01_2451449_3.png[/img][/align][align=center]1,蔗糖;2,乳糖[/align][align=center]图3. 混合对照溶液连续进样5针色谱图(月旭Ultimate[sup][/sup]XB-NH[sub]2[/sub]色谱柱)[/align]图4为使用月旭Topsil[sup][/sup] NH[sub]2[/sub]氨基色谱柱对乳糖对照溶液的测定效果图。由根据图3的测定结果,发现使用常规的Topsil[sup][/sup] NH[sub]2[/sub]氨基色谱柱进行该项目的测定时,其乳糖的柱效为5259,勉强满足《2015版中国药典》对色谱柱的柱效规定为5000的要求。进一步进行测定,连续进样5针,如图5所示。发现峰面积的RSD为2.53%,仍然大于《2015版中国药典》规定的2.0%。因而综合判断,采用月旭常规的Topsil[sup][/sup] NH[sub]2[/sub]氨基色谱柱无法满足《2015版中国药典》药典项下乳糖含量测定的要求。[align=center][img=,519,392]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230900_01_2451449_3.png[/img][/align][align=center]1,蔗糖;2,乳糖[/align][align=center]图4. 采用月旭Topsil[sup][/sup]NH[sub]2[/sub]测定混合对照溶液色谱图[/align][align=center][img=,479,365]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230904_01_2451449_3.png[/img][/align][align=center]1,蔗糖;2,乳糖[/align][align=center]图5. 混合对照溶液连续进样5针色谱图(月旭Topsil[sup][/sup]NH[sub]2[/sub]色谱柱)[/align]图6为使用月旭Xtimate[sup][/sup]Lactose-NH[sub]2[/sub]氨基色谱柱对乳糖对照溶液的测定效果图。根据图5的测定结果,发现使用经过改进键合的Xtimate[sup][/sup]Lactose-NH[sub]2[/sub]氨基色谱柱进行该项目的测定时,其乳糖的柱效为8932,完全满足《2015版中国药典》对柱效规定为5000的要求。进一步进行测定,连续进样5针,如图7所示。发现峰面积的RSD为1.14%,小于《2015版中国药典》规定的2.0%。因而综合判断,经过改进的稳定性更好,耐水性更强的月旭常规的Xtimate[sup][/sup]Lactose-NH[sub]2[/sub]氨基色谱柱非常适合《2015版中国药典》项下乳糖含量测定的要求。[align=center][img=,481,351]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230905_01_2451449_3.png[/img][/align][align=center]1,蔗糖;2,乳糖[/align][align=center]图6. 采用月旭Xtimate[sup][/sup]Lactose-NH[sub]2[/sub]氨基柱测定混合对照溶液色谱图[/align][align=center][img=,534,403]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230906_01_2451449_3.png[/img][/align][align=center]1,蔗糖;2,乳糖[/align][align=center]图7. 混合对照溶液连续进样5针色谱图(月旭Xtimate[sup][/sup]Lactose-NH[sub]2[/sub]色谱柱)[/align][b]4 结论[/b] 采用月旭Xtimate[sup][/sup]Lactose-NH[sub]2[/sub]氨基色谱柱按照《2015版中国药典》的要求对乳糖进行测定。系统适用性试验中,乳糖与蔗糖的分离度达到3.03,乳糖的理论塔板数为8932,满足药典要求(药典规定乳糖峰的理论塔板数不低于5000),并且连续5针进样峰面积RSD为1.14%,小于《2015版中国药典》规定的不超过2.0%,均满足药典要求。因此,本文建立的方法能够作为《2015版中国药典》乳糖含量测定的质控方法。
求3-氨基-5正丙胺基-1,2,4-三氮唑标准品,CS号也不知道是多少
想请教一下各位网友,我用苯胺衍生二甲氨基甲酰氯,但是随着衍生时间延长,以及苯胺用量,衍生物峰面积一直在增加,做不到反应彻底,有什么解决方法吗
在做偶氮测试时,4氨基偶氮苯按纺织品方法BS EN14362做回收率测试,上机测试时只有检出苯胺,没有苯二胺出现。而且苯二胺在做回收率的时候,竟然没有检测到,哪位仁兄有碰到这样的问题。其它各种的偶氮的回收率都很好,都可以达到要求!
2,4,6-三氨基三嗪是不是三聚氰胺?
想请教一下各位网友,我用苯胺衍生二甲氨基甲酰氯,但是随着衍生时间延长,以及苯胺用量,衍生物峰面积一直在增加,做不到反应彻底,有什么解决方法吗
我们知道,做禁用偶氮染料,一旦检出苯胺就必须进行4-氨基偶氮苯的确认,但是确认4-氨基偶氮苯会发现苯胺物质仍然存在,怎么确认该苯胺除了全是是4-氨基苯胺分解而来,还是部分?或者4-氨基苯胺分解而来?
硫化氢的对氨基二甲基苯胺物质冻结成块了,这该怎么配?
大家好!我是个新手,我现在在做一个化学品——3-环已胺基丙胺的含量分析我用的是标准样品,可是我所采用的方法在我们公司的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]上打不出原有浓度,所以求助大家给点宝贵意见。谁能提供一下关于该化学品——3-环已胺基丙胺的含量分析方法
用TLC检测苯胺基乙腈和苯胺基乙酸钾,应该使用那种染色剂呢?基本的显色剂碘或者硫酸是否可以?
RT:10版药典对乙酰氨基酚中的对氨基酚及有关物质、对氯苯乙酰胺检测有个朋友公司开始做这个项目,药典采用的是C8色谱柱朋友想买热电的柱子,不知道有没有同行采用热电的柱子做过?有的话帮忙发一张图谱看看,谢谢!QQ:342832185
测定水质中的硫化物,所配的试剂中,有一个是对氨基二甲基苯胺,买的是国外的试剂,用过一段时间后发现里面全都变的如黑沥青似的黏黏的,不知道是保存的哪个环节出了问题?(我们用的是黑色塑料瓶子,拧的很严,通风,干燥.)[em0810]
3-氨基-5正丙胺基-1,2,4-三氮唑CS号是多少?
想用GB8538.41-87对二乙氨基苯胺分光光度法做水中硫化物,可对二乙氨基苯胺怎么也买不到,商家说根本没有这个药,????疑惑.请高手指点而亚甲蓝分光光度法测定水中硫化物,用的是对氨基二甲基苯胺.这两中方法的原理都是在酸性条件下和三氯化铁生成亚甲蓝染料.用的药是一样的吗?请高手指点.十分感谢
[size=2][font=宋体]2-氨基苯酚-4-磺酰胺的国标或行标[/font][/size][size=2][font=宋体][/font][/size]