中文通用名称:鱼藤酮 英文通用名称:rotenone 化学名称:[2R-(2α,6aα,12aα)]-1,2,12,12a-四氢-8,9-二甲氧基-2-(1-甲基乙烯基)[1]苯并吡喃[3,4-b]糠酰[2,3-h][1]苯并吡喃-6(6aH)-酮 化学结构式 理化性质:鱼藤酮可从鱼藤根的萃取液中结晶得到。纯品为无色六角板状晶体,熔点163℃(同质二晶型的熔点181℃)。几乎不溶于水(100℃水中溶解度15毫克/升),微溶于矿油和四氯化碳,易溶于极性有机溶剂,在氯仿中溶解度最大(472克/升)。遇碱消旋,易氧化,尤其在光或碱存在下氧化快,而失去杀虫活性。在干燥情况下比较稳定。 毒性:按我国农药毒性分级标准,鱼藤酮属中等毒。原药大鼠急性经口LD5124.4毫克/公斤,急性经皮LD50≥2050毫克/公斤。 作用特点:鱼藤酮是一种历史比较久的植物性杀虫剂,具选择性,无内吸性,见光易分解,在空气中易氧化,在作物上残留时间短,对环境无污染,对天敌安全。该药剂杀虫谱广,对害虫有触杀和胃毒作用。本品能抑C-谷氨酸脱氢酶的活性,而使害虫死亡。该药剂能有效地防治蔬菜等多种作物上的蚜虫,安全间隔期为3天。 制剂:2.5%鱼藤酮乳油 2.5%鱼藤酮乳油 理化性质及规格:2.5%鱼藤酮乳油含有效成分鱼藤酮2.5%,外观为淡黄至棕黄色液体,比重0.91,pH≤8.5,闪点29℃,低温易析出结晶,高于80℃易变质。 毒性:大鼠急性经口LD50176.6毫克/公斤,大鼠急性经皮≥2086毫克/公斤。 登记情况及厂家:2.5%鱼藤酮乳油已在我国获得老品种登记,登记号为PD91105,登记厂家为广东省云浮县云城农药厂、广东省广州农药厂,登记号为PD91105-2,批准登记作物和防治对象为叶菜类蔬菜的蚜虫。 (记者 佚名)
各位大虾:哪位有苦参碱,鱼藤酮的检验方法或经验介绍?有没有标准品?另,哪里有苯达松、苯硫磷的标准样?最好是国产的。
请问哪位老师用气相检测过农残中的鱼藤酮,能指教下方法吗?
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=87706]薄层色谱法分离鱼藤中异黄酮类化合物 [/url]
附件请参考。
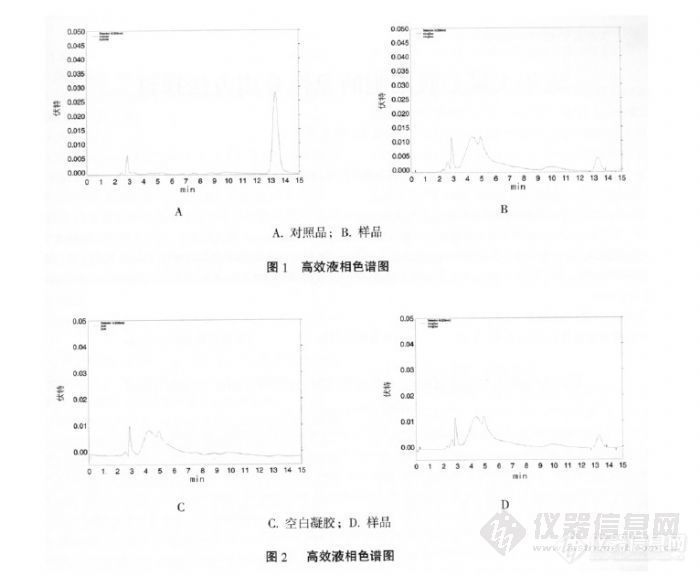
【作者】 李燕; 刘新;【Author】 LI Yan,et al (Department of Natural Medicinal Chemistry,College of Pharmacy,Chongqing Medical University)【机构】 重庆医科大学药学院天然药物化学教研室药物重庆市高校工程研究中心;【摘要】 目的:建立RP-HPLC法测定雷公藤外用凝胶中雷公藤甲素的含量。方法:采用Diamonsil C18色谱柱(250mm×4.6mmi.d,5μm),检测波长为220nm,流动相为甲醇∶水(46∶54),流速1ml/min,柱温为室温。结果:在10.24~51.20μg/ml间,雷公藤甲素的浓度与峰面积积分值呈良好的线性关系(r=0.9997),方法回收率为98.3%,RSD为0.23%(n=5)。结论:此方法准确、简便,可用于雷公藤甲素外用凝胶中雷公藤甲素的含量测定。 更多还原【Abstract】 Objective:To develop an HPLC method for the assay of the content of triptolide in triptolide gel. Methods:The content of triptolide was measured by HPLC on Diamonsil C18 column(250mm×4.6mm i.d,5μm)using methanol-water(46∶54,v/v)as mobile phase,at a flow rate of 1.0ml/min. The UV detection was set at 220nm. Results:The calibration curve was proved to be linear in the range of 10.24~51.20μg/ml with a regression coeficient of 0.999 7. The average recovery of the method was 98.3%;RSD was 0.23%(n=5).... 更多还原【关键词】 高效液相色谱法; 雷公藤甲素; 凝胶; 【Key words】 HPLC; Triptolide; Gel; http://ng1.17img.cn/bbsfiles/images/2012/08/201208061038_381720_2352694_3.jpg
雷公藤红素(celastrol)主要来源于卫矛科雷公藤属的雷公藤Tripterygium wilfordii Hook. f.,同时也存在于南蛇藤、独子藤等植物中[1],蜂蜜中也有发现[2]。雷公藤多生于背阴多湿的山坡、山谷、溪边灌木林中,主要分布于中国东南沿海等地,朝鲜、日本亦有少数分布。雷公藤始载于《本草纲目拾遗》,在我国具有悠久的药用历史,以根入药,味苦、辛,性凉,有大毒,具有祛风、解毒、杀虫的功效。现代医学研究发现,雷公藤对肿瘤、类风湿关节炎、系统性红斑狼疮、免疫性肾病等多种疾病的治疗效果显著,是较为可靠的免疫抑制类中药,被称为“中草药免疫剂”[3]。从雷公藤根部提取出的雷公藤总苷包含多种活性单体成分,其药理活性良好,素有“中草药激素”之称[4]。雷公藤红素是首个从雷公藤根皮中分离得到的天然活性产物,是一种具有醌甲基结构的去甲木栓烷型五环三萜(图1),具有抗肿瘤、抗炎、抗风湿、抗肥胖等作用,常用于治疗各种肿瘤、类风湿关节炎、2型糖尿病等[5-6]。 图片 文献计量学是一门定量分析知识载体的交叉科学,是集数学、统计学、文献学为一体,注重量化的综合性知识体系。通过使用CiteSpace软件对文献进行可视化分析,能够准确把握研究现状,探索新的研究方向。雷公藤红素自2007年被Cell杂志列为最有可能、最值得开发为现代药物的5种天然化合物之一以来[7],备受关注。本研究采用文献计量学方法,对现存的中英文有关雷公藤红素文献进行可视化处理,旨在呈现相关知识的结构、规律和分布等情况,形成对雷公藤红素的全面认知,有利于解读当前雷公藤红素的研究现状和未来发展趋势,帮助研究者更清晰、透彻地理解雷公藤红素发展现状,并为该领域的今后研究提供有价值的参考依据。 1 资料与方法 1.1 数据来源 在中国知网(China National Knowledge Infrastructure,CNKI)数据库和Web of Science(WOS)数据库,分别以“雷公藤红素”和“celastrol”为检索词进行文献检索,检索年限为2000年1月1日—2023年6月30日,分别得到中文文献744篇、英文文献1 254篇。 1.2 数据筛选 人工剔除掉数据库中的重复文献、图书、报纸文章、会议论文、成果报告以及不相关的内容。 1.3 数据可视化 将CNKI及WOS的文献分别以Refwork及文本格式导出,并以download_*.txt命名。使用CiteSpace 6.1.R4对得到的数据进行去重、格式转化。设置CiteSpace的参数:(1)时间分区(time slicing):时间段为2000年1月1日—2023年6月30日,时间切片为1;(2)节点类型(node types):分别选择“作者(author)”“研究机构((institution)”“关键词(keyword)”进行分析;(3)阈值选择(selection criteria):g-index(k=25),Top N=50,Top N%=10.0%;(4)剪切方式(pruning):“作者”“研究机构”分析选择“pathfinder”“pruning sliced networks”,“关键词”分析选择再加上“pruning the merged network”。对转化的数据进行可视化分析,探究其发文量、作者共现性、研究机构共现性、关键词共现性、关键词爆发时间、关键词聚类、研究方向等。 2 结果与分析 2.1 发文趋势 分析相关论文的发文趋势有助于了解该学科的研究现状、成长速度及未来发展方向。本研究旨在深入了解雷公藤红素的发展状况,通过对CNKI和WOS数据库中的中英文文献进行系统统计,时间跨度覆盖了2000年1月1日—2023年6月30日,筛选去重后获得了中文文献674篇、英文文献1 147篇。从图2中可以清晰地观察到,近20年来雷公藤红素相关文献的年发文量经历了不同的阶段,整体趋势呈现出稳定增长,同时英文文献的数量明显高于中文文献。具体而言,可将发文量的变化分为3个主要阶段。第1阶段跨越了2000—2007年,这一时期的发展相对平稳,研究逐渐积累。第2阶段,从2008—2017年,呈现了渐进的增长态势,显示了雷公藤红素领域受到持续关注并逐渐成熟。第3阶段自2018—2022年,是一个迅猛增长的时期,且为该领域的广泛研究爆发期。需要注意的是,由于本研究截至2023年6月30日,数据统计仅覆盖到112篇,因此出现下降趋势,但并不影响前述趋势的有效性。第2阶段的增长可能与2007年Cell杂志将雷公藤红素列为最有可能也最值得开发为现代药物的5种天然化合物之一,引发广泛关注有关[7]。总地来看,雷公藤红素相关文献的年发文量呈现出上升的趋势,背后的原因可能是随着中医药现代化进程的发展推动,中医药的认可度不断提升,相关领域的研究与应用蓬勃发展。作为具有巨大潜力的天然活性成分,雷公藤红素受到越来越多研究者的关注和探索。这一趋势有望在未来继续,为该领域的研究提供有力支持。 图片 2.2 国家、机构、作者分析 2.2.1 国家分布情况 分析文献作者所在国家的分布情况有助于了解各国对雷公藤红素的研究热度,同时也有助于研究雷公藤红素的植物基原和国家影响因素。全球范围内,共有59个国家和地区参与雷公藤红素的研究,发文量前12的国家见图3。中国的发文量远超其他国家和地区,这可能是因为雷公藤红素主要来源于雷公藤或南蛇藤的根皮、茎和叶,且雷公藤属于中国传统中药,故相较于其他国家,中国对雷公藤红素的研究投入相对更多,也更关注其潜在应用和价值。此外,美国和韩国也在雷公藤红素研究中发挥了重要作用,分别贡献了220篇和63篇文献。这表明雷公藤红素的研究具有国际性的合作和影响,不仅受到中国的关注,还在全球范围内也引起了广泛兴趣。综上所述,各国在雷公藤红素研究领域的贡献不仅反映了该领域的热度,还反映了雷公藤红素作为一种有潜力的天然活性成分的国际重要性。 图片 2.2.2 作者合作网络 在CNKI数据库中,共有674篇文献涵盖了503位作者,其中发文最多的作者是张振海(7篇)。作者合作网络见图4-A,共包含503个节点和638条连线,密度为0.005 1。张振海、陈彦和瞿鼎等作者构成了1个核心的合作团队,专注于雷公藤红素给药系统及抗癌药理作用的研究。总体而言,其他作者尚未形成规模较大且完整的合作研究团队,这可能不利于雷公藤红素研究的协作发展。在WOS数据库中,共有1 147篇文献涵盖了405位作者,其中发文最多的作者是Gao Wei(17篇),主要关注雷公藤红素的生物合成研究。作者合作网络如图4-B所示,包含405个节点和371条连线,密度为0.004 5。Gao Wei、Su Ping和Huang Luqi等作者构成了另1个核心合作团队,在研究雷公藤红素药理作用的同时,更加侧重雷公藤红素的生物合成研究。总体上看,其他作者合作研究团队已有雏形,预示着雷公藤红素的研究具有巨大的发展潜力和希望。 图片 2.2.3 机构合作网络 CNKI数据库中发文量最多的机构是南京中医药大学(7篇)和南京中医药大学附属中西医结合医院(7篇),其次是苏州大学附属第一附属医院(6篇)。推测可能是由于江苏省为雷公藤主要产地之一,且该地机构对雷公藤红素研究较为重视。中文文献研究机构合作网络见图5-A,包含409个节点和211条连线,说明尚未形成完善的合作机构团队,机构间的合作研究较少,有待加强各机构间的团队合作以推动相关研究。WOS数据库中发文量最多的机构是Chinese Academy of Sciences(56篇),其次是Sichuan University(30篇)、China Academy of Chinese Medical Sciences(29篇)。英文文献研究机构合作网络见图5-B,包括405个节点和371条连线,密度为0.004 5。英文文献发表机构间的合作在上述机构的带领下,形成了庞大且完整的机构合作网络,有利于机构间的相关经验交流与合作互补,进而促进雷公藤红素的研究发展。 图片 2.3 关键词分析 关键词是文献的总结凝练,通过分析关键词能够快速地了解论文主旨,有效掌握研究热点和研究方向。 2.3.1 关键词共现分析 对CNKI数据库中雷公藤红素相关文献的关键词进行可视化共现分析,结果如图6-A所示。该关键词共现图谱中包含276个节点和403条连线,排名前30的高频关键词见表1。通过分析共现图谱和高频关键词可知,与雷公藤红素相关的前5高频关键词为凋亡、雷公藤、细胞凋亡、雷公藤甲素、增殖,出现频率分别为41、34、30、24、19次。这表明药理作用、活性成分、化合物来源均是当下研究的热点。出现频率前30的关键词可分为6个大类。(1)药理作用:药理作用是雷公藤红素研究的重点内容,相关高频关键词共有17个,包括药理作用、作用机制、多发性骨髓瘤、凋亡、细胞凋亡、增殖、乳腺癌、小胶质细胞、胶质瘤、抗肿瘤、肝癌、细胞增殖、细胞周期、内皮细胞、巨噬细胞、成纤维细胞、代谢组学。说明中文文献中药理作用研究的热点是抗肿瘤、抗炎、抗风湿。(2)化学成分:探究雷公藤红素相类似的化学成分是对雷公藤红素研究的拓展,相关高频关键词有5个,包括雷公藤红素、雷公藤甲素、含量测定、化学成分和雷公藤次碱。雷公藤甲素、雷公藤次碱与雷公藤红素均为雷公藤总苷的组成成分,具有相似的化学结构和药理活性,可以为新药源的开发提供思路。(3)植物基原:植物基原的探寻是雷公藤红素研究工作的重要部分,相关高频关键词有3个,包括雷公藤、昆明山海棠、南蛇藤。雷公藤红素主要来自于雷公藤,探究雷公藤红素的植物基原可以拓展其获取途径,选取质最优、量最大的基原植物进行培养,丰富雷公藤红素资源。(4)研究方法:研究方法的选择对研究结果有巨大影响,相关高频关键词有2个,包括分子对接、综述。说明前人对雷公藤红素的总结阐述较多,倾向于用分子对接的方法进行研究。(5)中药:雷公藤红素主要来源于中国传统药材雷公藤,相关高频关键词有2个,包括中药、中医药。表明雷公藤红素研究的背景与传统中药的关联。(6)给药系统:雷公藤红素的给药系统是近年来的新兴热点,对应的相关高频关键词为体外释放。雷公藤红素具有良好的抗肿瘤、抗风湿、抗炎活性,但其人体吸收率较低。以何种方式更好地利用雷公藤红素,成为目前亟待解决的问题。 图片 图片 对WOS数据库中雷公藤红素相关文献的关键词进行可视化分析,如图6-B所示,该关键词共现图谱包括204个节点和294条连线,节点数量较中文文献略少,排名前30的高频关键词见表2。通过分析共现图谱和高频关键词可知,英文研究中频率前5的关键词是activation、celastrol、expression、apoptosis、NF-κB,出现频率分别为213、187、184、179、143次。说明英文文献同样注重雷公藤红素的药理作用。可以大致分为5个大类。(1)药理作用:药理作用是雷公藤红素研究的重点内容,相关高频关键词共有21个,包括activation、expression、apoptosis、NF-κB、growth、inhibition、cells、oxidative stress、inflammation、cancer、induction、mechanisms、obesity、rheumatoid arthritis、down regulation、pathway、disease、cancer cells、proliferation、therapy、autophagy。说明英文文献中涉及的雷公藤红素药理作用主要包括抗肿瘤、抗肥胖、抗炎、抗风湿。与中文文献相比,英文文献雷公藤红素相关药理作用关键词更多,种类也更丰富。除此之外,英文文献与通路相关的高频关键词多于中文文献,说明对雷公藤红素在细胞层面通过信号通路对机体产生影响的研究更多。(2)化学成分:化学成分是雷公藤红素研究的基础,相关高频关键词有4个,包括celastrol、triptolide、identification、triterpene。相较于中文文献稍少,但是提到了雷公藤红素所属的三萜类成分。同时中文文献侧重报道雷公藤红素的含量测定,而英文文献侧重于雷公藤红素的检测鉴定。(3)研究方法:研究方法的选择是雷公藤红素研究中必不可少的一环,出现3个高频关键词,分别为in vitro、design、mice。相较于中文文献采用软件手段的分子对接和综述,英文文献更倾向于使用动物实验相关研究手段,2种研究方式各有优劣,应取长补短。(4)给药系统:给药系统是雷公藤红素近年来的研究热点,出现1个相关高频关键词,为nanoparticles。相较于中文文献报道的体内释放,英文文献显示已经形成较成熟的纳米给药系统。(5)植物基原:植物基原是雷公藤红素探究的重要部分,出现1个相关高频关键词,为Tripterygium wilfordii,与国内研究相比,国外在植物基原方面研究较少,这可能是因为中药材雷公藤主产于中国,国内研究有地理优势和历史渊源。这些关键词共现和高频关键词分析有助于更深入地了解英文文献中对雷公藤红素研究的关注点和趋势,为未来的研究提供了重要线索。 图片 2.3.2 关键词热点聚类分析 将关系较为紧密的关键词进行聚类分析,有助于将研究热点可视化呈现。“聚类#”后的数字越小,说明该类研究的规模越大。本研究将CNKI检索到的与雷公藤红素相关的关键词进行可视化聚类分析,见图7-A。此聚类模块值(Q)=0.762 5,Q>0.5,平均轮廓值(S)=0.980,S>0.7,说明聚类结果合理显著。将7个聚类模块分为3大类。(1)药理作用:该大类包含了聚类#0(凋亡)、聚类#2(增殖)、聚类#5(抗肿瘤)、聚类#6(抑制作用)4个小聚类,主要反映了雷公藤红素在抗肿瘤药理作用方面的研究。研究表明雷公藤红素对肺癌、肝癌、胃癌、宫颈癌、乳腺癌、卵巢癌、黑素瘤、神经胶质瘤等多种肿瘤细胞具有良好的抑制作用[8]。Ni等[9]发现,雷公藤红素能够下调抗凋亡蛋白B淋巴细胞瘤-2(B-cell lymphoma-2,Bcl-2)和生存素(survivin)的表达,并有效阻断p65亚基的核转位,通过上调p27表达、调控核因子-κB(nuclear factor-κB,NF-κB),诱导肿瘤细胞周期阻滞和凋亡,从而达到抗肿瘤作用。梁柳春等[10]发现,雷公藤红素还有抗炎及免疫抑制、抗肥胖、神经保护等药理作用。(2)药物资源:该大类包括聚类#1(雷公藤)、聚类#3(中药)。雷公藤甲素主要来源于雷公藤和南蛇藤等传统中药,这些药材一直以来都在中医药中有着重要的地位。(3)化学成分:该大类包括聚类#4(雷公藤甲素),是雷公藤总苷的主要成分之一,雷公藤总苷被称为“中草药激素”,其组成成分还包括雷公藤晋碱和雷公藤次碱等萜类活性成分,具有治疗类风湿性关节炎、糖尿病肾病、紫癜性肾炎、系统性红斑狼疮等疾病的功效[11]。这些聚类分析结果有助于更清晰地了解雷公藤红素研究的热点和不同方向,为未来的研究提供了重要的指导。 图片 将WOS数据库中雷公藤红素相关文献关键词进行可视化聚类分析,见图7-B,Q=0.766 9,Q>0.5,S=0.893,S>0.7,说明聚类结果合理显著,具有实际意义。将10个聚类分为药理作用、药物资源2大类。(1)药理作用:该大类包括聚类#0(oxidative stress)、聚类#1(extracellular vesicles)、聚类#2(rheumatoid arthritis)、聚类#3(endoplasmic reticulum stress)、聚类#4(expression)、聚类#5(breast cancer)、聚类#7(inhibition)、聚类#9(activation)、聚类#10(growth)。这些关键词反映了英文文献中对雷公藤红素药理作用的研究广泛。研究表明,雷公藤红素在抗肿瘤、抗炎、抗风湿等领域有着丰富的研究内容。与中文文献相比,英文文献在雷公藤红素药理作用领域的研究范围更广泛,研究方向更多元化。(2)药用植物资源:该大类包括聚类#6(Tripterygium wilfordii)和聚类#8(Tripterygium wilfordii Hook. f.),二者含义相同,均代表雷公藤,为其拉丁名的不同写法。这表明中英文文献在药物资源领域研究报道均较为深入,同时药物基原在国内外均有较高关注度。 2.3.3 聚类热点时间分析 为了更好地展示不同时间段的热门研究方向,将图7-A的中文关键词聚类图转化为关键词聚类时间线图(图8)时间线图聚焦于不同聚类在时间维度上的分布,有利于发现不同时期的研究热点。由图8可知,2007年以前以雷公藤红素的聚类#5(抗肿瘤)和聚类#6(抑制作用)研究为主;2007年以后,聚类#0(凋亡)、聚类#1(雷公藤)、聚类#2(增殖)、聚类#3(中药)、聚类#4(雷公藤甲素)相关研究逐渐增多,且聚类#0(凋亡)的研究持续时间较长,表明这一方向的研究在不同时期都备受关注。将图7-B的英文关键词聚类图转化为关键词聚类时间线图(图9)。由图9可知,在2007年以前,WOS数据库中雷公藤红素相关的研究数量和方向较CNKI数据库更多,如聚类#10(growth)和聚类#9(activation),且全部11个聚类研究持续性均较好。总体上相较于雷公藤红素相关中文文献关键词聚类时间线图,英文的时间线图聚类更多,分布更密集,每个聚类持续时间更长。这些时间线图提供了关于雷公藤红素研究的时间演变趋势的重要信息,有助于更全面地了解不同时期的研究热点和发展方向。 图片 图片 2.3.4 关键词突现分析 关键词突现分析是将某段时间内频次变化高的关键词筛选出来,展现关键词出现的起止年份以及突变强度,可以清晰地表现出研究热点和发展趋势,预测雷公藤红素未来发展情况。WOS数据库中的雷公藤红素研究突现关键词更全面,更具有代表性,故以WOS数据库中英文研究关键词突现图为例分析雷公藤红素研究热点的变化。如图10所示,共包含25个突现关键词。其中强度最大的是“triterpene”,为10.7,持续时间为2010—2014年。2007年雷公藤红素被Cell期刊列为最有可能也是最值得开发为现代药物的5种天然化合物之一,其主要药效基团是位于A/B环上的醌甲基等结构。雷公藤红素所属三萜类化合物存在于大多数植物体内,具有多种生物活性,这也可能是“triterpene”关键词强度很高的原因之一。 图片 持续时间最长的突现关键词是“cancer cells”,从2009年持续到2018年。这说明雷公藤红素自被发现以来,其抗肿瘤作用一直备受关注,作为热点研究方向经久不衰。同时突现关键词中还有“heat shock”“kappa b activation”“inhibitor”等与抗肿瘤相关。雷公藤红素已被发现对肺癌、肝癌、胃癌、宫颈癌、乳腺癌、卵巢癌、黑素瘤、神经胶质瘤等多种肿瘤细胞具有良好的抑制作用。“drug delivery”和“delivery”分别成为2018年和2019的突现关键词,说明在雷公藤红素药理作用研究较为完善的基础上,大量学者开始关注给药系统的研究。尽管雷公藤红素具有良好的药理活性,但其口服生物利用度较低,毒性较大,导致其临床应用受到限制,因此给药系统成为近年来新的研究热点。靶向叶酸受体和线粒体的载体雷公藤红素聚酰胺-胺树枝状聚合物、透明质酸包被的线粒体靶向脂质体、尺寸可控的雷公藤红素纳米颗粒等相关研究陆续出现,能够在降低雷公藤红素自身毒性、提高口服生物利用度的同时,丰富雷公藤红素给药系统[12-14]。这些研究进展为雷公藤红素更广泛的应用提供了可能性。 2.4 高被引文献分析 文献引用量是反映当前研究情况和未来发展方向的重要指标。CNKI数据库中引用次数排名前10的雷公藤红素相关文献见表3。其中被引频次最多的是出自《中华肿瘤杂志》的“雷公藤红素抑制血管生成的实验研究”,被引170次,该研究通过测定雷公藤红素对血管内皮细胞株增殖的影响,观察其对血管内皮细胞株迁移、小管形成和鸡胚尿囊膜血管生成的影响,发现雷公藤红素可以抑制血管内皮细胞的增殖、迁移和小管形成,并具有抑制鸡胚尿囊膜血管生成的作用,该研究说明雷公藤红素具有明显抑制血管生成的作用。抗肿瘤作为雷公藤红素最重要的药理作用之一,除了被引频次第1的文献外,被引频次第2、5的文献“雷公藤红素抑制血管内皮细胞株增殖的体外研究”和“雷公藤红素对U937细胞Notch 1、NF-κB信号蛋白通路的调控作用”都与抗肿瘤作用相关,说明雷公藤红素抑制肿瘤生长的作用及其机制一直是研究的重点方向。 图片 被引频次排第4的文献是出自《中华结核和呼吸杂志》的“雷公藤红素抑制支气管哮喘小鼠气道炎症的实验研究”,共被引用61次。该研究发现雷公藤红素可减少哮喘模型小鼠肺组织炎性细胞浸润,降低肺组织干细胞因子蛋白表达强度,证实雷公藤红素具有支气管抗炎作用。另外2篇文献“雷公藤红素对小鼠的免疫抑制作用及其对IL-6 mRNA表达影响的研究”和“雷公藤红素对类风湿关节炎滑膜成纤维细胞中RANKL、OPG及炎性因子表达的影响”同样涉及雷公藤红素的抗炎作用和作用机制。 出自《中草药》的“HPLC法测定雷公藤及其片剂中雷公藤红素”一文中建立了快速高效的雷公藤红素HPLC测定方法,为进一步研究雷公藤红素的化学成分提供了理论基础。“环境胁迫对雷公藤中雷公藤红素含量的影响”则探讨了水分、光照、土壤氮含量的轻度胁迫对雷公藤幼苗中雷公藤红素含量的影响,为提高雷公藤药材品质提供参考。“雷公藤红素的研究进展”为综述性论文,内容丰富广泛,涵盖了雷公藤红素提取工艺、含量分析、药理活性等多项内容。该文被引量较多,较为经典,对雷公藤未来的研究具有参考意义。 WOS数据库中引用量前10的英文文献如表4所示。被引频次最多的文献是2010年在Cancer and Metastasis Reviews杂志发表的“Regulation of survival,proliferation,invasion,angiogenesis,and metastasis of tumor cells through modulation of inflammatory pathways by nutraceuticals”,被引用170次。该研究探索了饮食与健康之间的联系,对饮食习惯预防癌症进行着重分析,讨论包含雷公藤红素在内的香料、豆类、水果、坚果、蔬菜等食物通过调节炎症途径影响肿瘤细胞的生存、增殖、侵袭、血管生成和转移。该文献阐述了肿瘤形成的原因和抑制肿瘤的方式,有助于更好地理解雷公藤红素的抗肿瘤作用。值得一提的是,英文文献被引频次第2、4、5、6、8、10亦与雷公藤红素抗肿瘤的药理作用相关,且多数提到了抗肿瘤通路,说明雷公藤红素抗肿瘤研究一直是一个备受关注且不断深入的研究热点。 图片 “Treatment of obesity with celastrol”揭示了雷公藤红素通过增强瘦素敏感性,抑制食物摄入,阻断能量消耗的减少,从而显著减轻了高瘦素血症饮食诱导的肥胖小鼠体质量,该文献被引频次排名第3位。肥胖一直是人类长期面临的问题之一,也是雷公藤红素未来研究方向之一。“Celastrols as inducers of the heat shock response and cytoprotection”被引342次,该研究发现雷公藤红素能够刺激基因转录,该功能类似于热应激的动力学激活热休克转录因子,从而对致命细胞应激表现出细胞保护作用。该研究表明雷公藤红素有望成为一类新的热休克反应调节剂。排名第5的文献“Chemical and biological approaches synergize to ameliorate protein-folding diseases”被引313次,该研究证明通过使用小分子蛋白稳定调节因子,可以增强先天细胞蛋白稳态,有望改善功能性蛋白失

作者:王艳芝; (吉林省双辽市中医院药剂科;)摘要:目的:建立高效液相法测定雷公藤片中雷公藤甲素的方法。方法:采用Diamonsil-C18(4.6 mm×200 mm,5μm)色谱柱;流动相:甲醇-水(60∶40);检测波长:218 nm;流速:1.3 ml/min。结果:雷公藤甲素在0.047 6~0.476 0μg范围内与峰面积呈良好的线性关系(r=0.999 1),平均回收率为99.08%,RSD=0.75%。结论:本方法简便、准确、重现性好,可用于雷公藤片中雷公藤甲素的质量控制。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208201417_384706_1606903_3.jpg
乙蒜素,鱼藤酮,藜芦碱,苦参碱,苦皮藤素,蛇床子,香芹酚,大蒜素,烟碱,烯效唑,甲哌嗡,吲哚丁酸,菇类蛋白多糖,葡聚烯糖。
据新华社华盛顿10月18日电 (记者任海军)美国明尼苏达大学研究人员日前报告说,小鼠模型显示在传统中药中有悠久使用历史的天然植物产品——雷公藤甲素对治疗胰腺癌有效。 此前有研究表明,胰腺癌细胞可能含有过多HSP70蛋白,后者能保护癌细胞免于死亡。明尼苏达大学研究人员发现,雷公藤甲素可降低胰腺癌细胞中的HSP70浓度,进而减少小鼠体内的肿瘤细胞。 不过,由于雷公藤甲素不溶于水,它在小鼠体内的作用不甚理想。研究人员于是对雷公藤甲素进行加工,最终得到一种水溶性、注射用新药明尼甲素,后者可以更有效地运输到胰腺癌细胞。 研究人员在胰腺癌细胞系以及移植了人类胰腺肿瘤的小鼠中测试了新药。他们发现,该药对杀灭肿瘤细胞及缩小肿瘤效果极佳。
(按笔划顺序排列) 八角莲、八里麻、千金子、土青木香、山莨菪、川乌、广防己、马桑叶、马钱子、六角莲、天仙子、巴豆、水银、长春花、甘遂、生天南星、生半夏、生白附子、生狼毒、白降丹、石蒜、关木通、农吉痢、夹竹桃、朱砂、米壳(罂粟壳)、红升丹、红豆杉、红茴香、红粉、羊角拗、羊踯躅、丽江山慈姑、京大戟、昆明山海棠、河豚、闹羊花、青娘虫、鱼藤、洋地黄、洋金花、牵牛子、砒石(白砒、红砒、砒霜)、草乌、香加皮(杠柳皮)、骆驼蓬、鬼臼、莽草、铁棒槌、铃兰、雪上一枝蒿、黄花夹竹桃、斑蝥、硫磺、雄黄、雷公藤、颠茄、藜芦、蟾酥。
[size=15px][font=宋体]金黄色葡萄球菌([/font][font=&]Staphylococcus aureus[/font][font=宋体])是医院感染最常见的病原体,已成为全球主要的公共卫生威胁之一。随着“超级细菌”耐甲氧西林金黄色葡萄球菌([/font][font=&]MRSA[i][/i][/font][font=宋体])的出现和迅速传播,治疗金黄色葡萄球菌感染变得愈发困难,临床上迫切需要发现新的超级抗生素来应对超级细菌的威胁。[/font][font=&][/font][/size] [size=15px][font=宋体][b]天然产物雷公藤红素[i][/i]在体外和体内均能有效对抗[/b][/font][b][font=&]MRSA[/font][font=宋体],且雷公藤红素靶向Δ[/font][font=&]1-[/font][font=宋体]吡咯啉[/font][font=&]-5-[/font][font=宋体]羧酸脱氢酶(Δ[/font][font=&]1-Pyrroline-5-Carboxylate Dehydrogenase[/font][font=宋体],[/font][font=&]P5CDH[/font][font=宋体])发挥抗[/font][font=&]MRSA[/font][font=宋体]作用。机制上,[/font][font=宋体]雷公藤红素通过与[/font][font=&] P5CDH [/font][font=宋体]结合诱导氧化应激[i][/i]并抑制[/font][font=&] DNA [/font][font=宋体]合成。[/font][/b][font=宋体]这项研究的结果表明雷公藤红素是一种有前途的先导化合物,并证实[/font][font=&] P5CDH [/font][font=宋体]是开发抗[/font][font=&] MRSA [/font][font=宋体]新型药物的潜在靶点。[/font][/size] [size=15px][b][font=&]1[/font][font=宋体]、雷公藤红素在体外表现出对抗[/font][font=&] MRSA [/font][font=宋体]的强效活性[/font][font=&][/font][/b][/size] [size=15px][font=宋体]作者首先通过[/font][b][font=宋体]体外实验[/font][/b][font=宋体]发现雷公藤红素对[/font][font=&]MRSA USA300[/font][font=宋体]表现出显著的抗菌活性,最低杀菌浓度([/font][font=&]MBC[/font][font=宋体])为[/font][font=&]8μg mL ?1[/font][font=宋体],在浓度为[/font][font=&]1[/font][font=宋体]和[/font][font=&]2 μg mL[/font][font=&]?[/font][font=&]1[/font][font=宋体]时,雷公藤红素完全抑制了菌株的生长,根据[/font][font=&]MBC[/font][font=宋体]和[/font][font=&]MIC[/font][font=宋体]值确认雷公藤红素是一种很有前途的抗[/font][font=&] MRSA[/font][font=宋体]药物[/font][font=宋体]。[/font][font=&][/font][/size] [align=center] [/align] [size=15px][b][font=&]2[/font][font=宋体]、雷公藤红素在不同感染模型中表现出潜在的治疗能力[/font][font=&][/font][/b][/size] [size=15px][font=宋体]作者通过[/font][b][font=宋体]体内实验[/font][/b][font=宋体]评估雷公藤红素在[/font][font=&]3[/font][font=宋体]种不同感染模型(大蜡螟幼虫模型和两种小鼠感染模型)中的治疗能力,发现雷公藤红素提高了被[/font][font=&]MRSA USA300[/font][font=宋体]感染的大蜡螟幼虫的存活率,改善小鼠的[/font][font=&]MRSA[/font][font=宋体]皮肤感染,提高[/font][font=&]MRSA[/font][font=宋体]菌血症[i][/i]模型的存活率。这些结果表明雷公藤红素具有优异的体内抗[/font][font=&]MRSA[/font][font=宋体]活性[/font][font=宋体]。[/font][font=&][/font][/size] [align=center][img=图片,1,]data:image/svg+xml,%3C%3Fxml version='1.0' encoding='UTF-8'%3F%3E%3Csvg width='1px' height='1px' viewBox='0 0 1 1' version='1.1' xmlns='http://www.w3.org/2000/svg' xmlns:xlink='http://www.w3.org/1999/xlink'%3E%3Ctitle%3E%3C/title%3E%3Cg stroke='none' stroke-width='1' fill='none' fill-rule='evenodd' fill-opacity='0'%3E%3Cg transform='translate(-249.000000, -126.000000)' fill='%23FFFFFF'%3E%3Crect x='249' y='126' width='1' height='1'%3E%3C/rect%3E%3C/g%3E%3C/g%3E%3C/svg%3E[/img][/align][align=center] [/align] [size=15px][b][font=&]3[/font][font=宋体]、多组学分析发现新型抗[/font][font=&] MRSA [/font][font=宋体]靶点[/font][font=&][/font][/b][/size] [size=15px][font=宋体]接着研究人员[/font][b][font=宋体]通过转录组学、蛋白质组学和代谢组学分析了[/font][font=&]MRSA[/font][font=宋体]治疗后的细胞变化[/font][/b][font=宋体],揭示了雷公藤红素抗[/font][font=&]MRSA[/font][font=宋体]活性的可能靶点,多组学分析表明雷公藤红素上调应激反应[i][/i]和氧化磷酸化,而下调氨基酸和核苷酸、天冬氨酸、谷氨酸和嘧啶代谢的生物合成。这些代谢通路与[/font][font=&]Δ1-[/font][font=宋体]吡咯啉[/font][font=&]-5-[/font][font=宋体]羧酸脱氢酶([/font][font=&]P5CDH, [/font][font=宋体]由[/font][font=&]rocA[/font][font=宋体]基因编码)相关。因此,作者推测[/font][font=&]P5CDH[/font][font=宋体]是抗菌药物开发的潜在靶点 [/font][/size] [size=15px][b][font=&]4[/font][font=宋体]、[/font][font=&]P5CDH [/font][font=宋体]是一个潜在的抗菌靶点[/font][font=&][/font][/b][/size] [size=15px][b][font=宋体]为了进一步确定[/font][font=&]P5CDH[/font][font=宋体]作为潜在的抗菌靶点,作者构建了[/font][font=&]MRSA USA300 rocA[/font][font=宋体]敲除菌株和补充菌株(Δ[/font][font=&]:: rocA [/font][font=宋体])[/font][/b][font=宋体],发现[/font][font=&]rocA[/font][font=宋体]缺失显著损害细菌生长,而补充菌株在生长方面与[/font][font=&]WT[/font][font=宋体]相同。此外,突变后雷公藤红素对[/font][font=&]MRSA[/font][font=宋体]的[/font][font=&]MIC[/font][font=宋体]由[/font][font=&]1[/font][font=宋体]变为[/font][font=&]8[/font][font=宋体]μ[/font][font=&]g mL[/font][font=&]?[/font][font=&]1[/font][font=宋体],而补充[/font][font=&]rocA[/font][font=宋体]基因后又恢复到[/font][font=&]1[/font][font=宋体]μ[/font][font=&]g mL[/font][font=&]?[/font][font=&]1[/font][font=宋体],说明雷公藤红素的抗菌活性部分是通过抑制[/font][font=&]P5CDH[/font][font=宋体]来实现的[/font][/size] [size=15px][b][font=&]5[/font][font=宋体]、雷公藤红素与[/font][font=&]P5CDH[/font][font=宋体]直接结合[/font][font=&][/font][/b][/size] [size=15px][b][font=宋体]由于蛋白质组学分析中雷公藤红素并没有显著影响[/font][font=&]P5CDH[/font][font=宋体]的表达,因此研究推测雷公藤红素通过靶向[/font][font=&]P5CDH[/font][font=宋体]并影响其功能来发挥抗菌活性。[/font][/b][font=宋体]接着通过分子对接、[/font][font=&]BLI[/font][font=宋体]、[/font][font=&]CETSA[/font][font=宋体]、圆二色谱和酶活性测定,证实雷公藤红素能够直接结合影响[/font][font=&]P5CDH[/font][font=宋体],影响其酶活 [/font][/size] [size=15px][b][font=&]6[/font][font=宋体]、[/font][font=&]K205A[/font][font=宋体]和[/font][font=&]E208A[/font][font=宋体]是[/font][font=&]P5CDH[/font][font=宋体]与雷公藤红素的关键结合位点[/font][font=&][/font][/b][/size] [size=15px][font=宋体]接着,[/font][b][font=宋体]作者采用了分子对接和定点诱变技术揭示雷公藤红素结合位点[/font][/b][font=宋体]。分子对接成功预测出[/font][font=&]3[/font][font=宋体]个结合位点,分别为[/font][font=&]Lys205[/font][font=宋体]([/font][font=&]K205A[/font][font=宋体])、[/font][font=&]Glu208[/font][font=宋体]([/font][font=&]E208A[/font][font=宋体])和[/font][font=&]Asp209[/font][font=宋体]([/font][font=&]D209A[/font][font=宋体])。随后,作者构建了三个突变质粒并表达相关蛋白。[/font][b][font=&]BLI[/font][font=宋体]分析显示[/font][font=&]K205[/font][font=宋体]和[/font][font=&]E208[/font][font=宋体]突变后雷公藤红素结合能力显著降低,且不再抑制其酶活,表明[/font][font=&]K205[/font][font=宋体]和[/font][font=&]E208[/font][font=宋体]是结合的关键残基[/font][/b][/size] [size=15px][b][font=&]7[/font][font=宋体]、雷公藤红素促进氧化损伤[/font][font=&][/font][/b][/size] [size=15px][font=宋体]有文献报道[/font][font=&]P5CDH[/font][font=宋体]通过影响[/font][font=&]P5C-Pro[/font][font=宋体]循环的平衡进而对产生[/font][font=&]ROS[/font][font=宋体]至关重要,[/font][b][font=宋体]作者推测雷公藤红素可能通过氧化损伤发挥抗菌作用。通过对[/font][font=&]WT [/font][font=宋体]或[/font][font=&] Δ:: rocA [/font][font=宋体]组、[/font][font=&]Δ rocA[/font][font=宋体]组菌株采用雷公藤红素或乙醛酸([/font][font=&]P5CDH[/font][font=宋体]抑制剂)[/font][/b][font=宋体],发现雷公藤红素扰乱[/font][font=&]P5C-Pro[/font][font=宋体]循环的平衡。此外,[/font][font=&]ΔrocA[/font][font=宋体]、雷公藤红素或抑制剂处理组的[/font][font=&]ROS[/font][font=宋体]水平升高。其中,雷公藤红素治疗组[/font][font=&]ROS[/font][font=宋体]升高最为显著,可能是因为雷公藤红素是一种多途径抗菌剂,可以通过多种方式刺激[/font][font=&]ROS[/font][font=宋体]生成。结果表明氧化损伤是雷公藤红素重要的抗菌机制[/font][/size] [size=15px][b][font=&]8[/font][font=宋体]、雷公藤红素诱导细菌死亡[/font][font=&][/font][/b][/size] [size=15px][font=宋体]为研究雷公藤红素处理后[/font][font=&]MRSA[/font][font=宋体]死亡情况,作者用[/font][font=&]DAPI[/font][font=宋体]标记细胞中的[/font][font=&]DNA[/font][font=宋体],在[/font][font=&]ΔrocA[/font][font=宋体]、雷公藤红素或抑制剂处理组均观察到染色体凝聚,提示有细菌死亡发生,特别是雷公藤红素处理的细菌出现了凋亡小体形成和萎缩等细菌死亡形态学特征。在[/font][font=&]TUNEL[/font][font=宋体]染色实验中,与未接受药物处理的[/font][font=&]WT[/font][font=宋体]细胞相比,雷公藤红素处理的[/font][font=&]WT[/font][font=宋体]细菌荧光较强,提示有[/font][font=&]DNA[/font][font=宋体]双链断裂出现 [/font][/size] [size=15px][b][font=&]9[/font][font=宋体]、雷公藤红素抑制[/font][font=&]DNA[/font][font=宋体]合成[/font][font=&][/font][/b][/size] [size=15px][font=宋体]前面多组学结果发现雷公藤红素影响谷氨酸和嘧啶代谢的生物合成,该过程与[/font][font=&]DNA[/font][font=宋体]合成密切相关,[/font][b][font=宋体]作者推测雷公藤红素可能通过抑制[/font][font=&]DNA[/font][font=宋体]合成发挥抗[/font][font=&]MRSA[/font][font=宋体]活性。[/font][/b][font=宋体]结果显示,用雷公藤红素或抑制剂和[/font][font=&]ΔrocA[/font][font=宋体]组处理的细菌中[/font][font=&]NADP+/NADPH[/font][font=宋体]比率降低,表明[/font][font=&]5-[/font][font=宋体]磷酸核糖的合成受到抑制。[/font][font=&]Asp[/font][font=宋体]是嘌呤和嘧啶合成的重要前体,作者发现[/font][font=&]Glu[/font][font=宋体]和[/font][font=&]Asp[/font][font=宋体]的减少。此外,作者观察到[/font][font=&]DNA[/font][font=宋体]含量下降。考虑到[/font][font=&]DNA[/font][font=宋体]能够影响蛋白质的表达,作者也观察到[/font][font=&]ΔrocA[/font][font=宋体]、雷公藤红素或抑制剂处理组的蛋白质含量均显著降低,表明[/font][font=&]P5CDH[/font][font=宋体]能够影响蛋白质的合成。总之,雷公藤红素可以抑制[/font][font=&]DNA[/font][font=宋体]合成来对抗[/font][font=&]MRSA[/font][/size] [size=15px][b][font=宋体]总结[/font][font=&][/font][/b][/size] [size=15px][font=宋体]该研究表明,雷公藤红素对标准和临床耐甲氧西林金黄色葡萄球菌菌株表现出强大的抗菌活性,并且耐药性发展水平较低。这种抗菌活性的机制被认为是基于与[/font][font=&]P5CDH[/font][font=宋体]的竞争性结合,从而激活多种途径。雷公藤红素是开发用于对抗耐甲氧西林金黄色葡萄球菌相关感染的新型抗生素药物的有希望的候选药物[/font][/size]
[align=center][size=24px]千金藤素的提取和纯化[/size][/align][align=center][/align][align=left]摘要:本研究从中药山乌龟中提取得到含千金藤素的提取液;该提取液用键合硅胶层析柱进行纯化,得到含量大于99%的千金藤素,该方法简单、环保、经济且具备工业放大可行性。[/align][align=left][/align][table][tr][td][align=left][font='calibri'][size=13px]样品名称[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]别名[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]结构式[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]分子量[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]CAS号[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]药物功效[/size][/font][/align][/td][/tr][tr][td][align=left][font='calibri'][size=13px]千金藤素[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]千金藤碱[/size][/font][/align][/td][td][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115068700_8263_3120214_3.png[/img][/align][/td][td][align=left][font='calibri'][size=13px]606.71[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]481-49-2[/size][/font][/align][/td][td][align=left]抗炎,抗肿瘤;抑制冠状病毒复制的倍数为15393倍*[/align][/td][/tr][/table][align=left]*:[font='helvetica'][size=9px][color=#333333]2022年5月10日,中国科学家发现的新冠治疗新药获得国家发明专利授权。专利说明书显示,10μM(微摩尔/升)的千金藤素抑制冠状病毒复制的倍数为15393倍。美国学者之后也在《科学》发表论文证实,千金藤素的数据在其研究的26种药物中数据亮眼,而且优于已经获批上市的瑞德西韦和帕罗韦德。[/color][/size][/font][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115069773_3887_3120214_3.jpeg[/img][/align][align=left][font='helvetica'][size=13px][color=#333333]实验部分[/color][/size][/font][/align][align=left]1. [font='helvetica'][size=13px][color=#333333]样品提取:取中药材山乌龟片,用研钵捣碎至粉末,称取5g于具塞锥形瓶中,加入200ml甲醇,超声提取20min,静置冷却。[/color][/size][/font][/align][align=left]2. [font='helvetica'][size=13px][color=#333333]色谱分析:将提取液用甲醇稀释2倍后,过0.45um膜,进[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用仪[/color][/url]进行色谱分析,色谱条件如下:[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]色谱柱:Bioseps AQ C18, 2.1*100mm, 3um, 100[/color][/size][/font][font='calibri'][size=13px][color=#333333]?[/color][/size][/font][font='helvetica'][size=13px][color=#333333] [/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]流动相:甲醇:0.1%TEA=80:20(V/V)[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]检测波长:282nm[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]流速:0.3ml/min;[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]柱温:35℃[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]进样量:1ul[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]质谱电压:3000V, 扫描范围150~1500m/z, Pos-TIC模式[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]提取液检测[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]检测图:[/color][/size][/font][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115073934_9473_3120214_3.png[/img][/align][align=left]3. 层析纯化:将提取液过0.45μm的膜,进制备[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]进行纯化。制备色谱工艺参数如下:[/align][align=left]层析填料:Bioseps-Flash C18, 20-45μm,100[font='calibri']?[/font];[/align][align=left]填装规格:20×250mm;[/align][align=left]进样体积:10ml (折合样品500mg)[/align][align=left]洗脱液:甲醇:水=85:15(V/V)[/align][align=left]洗脱流速:18mL/min [/align][align=left]收集方式:紫外检测282nm, 35-39.5min [/align][align=left]4. 后处理:馏分35℃下减压旋蒸除去甲醇,冷冻干燥,得白色固体,称重为1.23mg.[/align][align=left]5. 纯化检测,经[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LCMS[/color][/url]检测,样品纯度为97.2%, 检测[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LCMS[/color][/url]图如下:[/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115077303_9982_3120214_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115078485_5049_3120214_3.png[/img][/align][align=left]小结:[/align][align=left]1. 由纯品质量折算山乌龟中千金藤素的含量约为0.246%;[/align][align=left]2. 该工艺使用的层析填料为大粒径键合硅胶,有利于放大至规模化生产,建议的生产设备配置如下:[/align][align=left]DAC 800, 系统耐压2MPa,配置集成化层析控制柜,符合GMP生产要求,产能估算,每日分离提取液160L,折合中药样品8kg,可得千金藤素纯品20g.[/align][align=left][/align]
1、雷公藤红素抑制CML细胞增殖作者首先进行了网络药理学分析,以评估在治疗CML方面最有效的天然产物。通过对3882种天然产物进行了网络药理学分析,发现从传统中药“雷公藤”(Tripterygium wilfordii)根皮中提取的五环三萜雷公藤红素在抑制CML方面排名第一。为了验证网络药理学筛选的可靠性,作者在CML细胞中进行细胞活力测定。选择18β-甘草次酸作为阴参,因为它与雷公藤红素的结构最相似,但在3882 种天然产物中预测得分不高,选择17-AAG(HSP90抑制剂,已有文章报道HSP90是雷公藤红素的靶点)和TKI 药物伊马替尼作为阳参。结果表明雷公藤红素、17-AAG和伊马替尼均能有效抑制CML细胞增殖,而18β-甘草次酸几乎不影响细胞生长。作者进一步开展细胞实验,发现雷公藤红素对K562和K562T315I细胞表现出抗增殖活性,诱导细胞凋亡。尽管对雷公藤红素的研究很深入,但尚未系统地鉴定出雷公藤红素在CML中的直接蛋白质靶点,尤其是在耐药性CML细胞中 雷公藤红素抑制CML细胞增殖2、雷公藤红素处理后 K562T315I 细胞的转录组和蛋白质组学分析接着,作者通过RNA 测序发现富集的通路包括铁死亡、蛋白水解调节、响应p53介导的DNA损伤等。作者还进行了蛋白质组学分析雷公藤红素对K562T315I细胞中蛋白质表达水平的调节,下调蛋白主要富集于DNA和RNA代谢途径以及 DNA损伤反应,以及蛋白质加工途径。MCODE分析发现“对DNA损伤刺激的反应”和“对未折叠蛋白的反应”分别是最具特征性的途径。雷公藤红素与其已知靶标HSP90的相互作用可能是“对未折叠蛋白的反应”上调的关键贡献事件。而目前尚未有报道称雷公藤红素的直接蛋白质靶标与“对DNA损伤刺激的反应”途径有关( 雷公藤红素处理后 K562T315I 细胞的定量蛋白质组学分析3、雷公藤红素处理后 K562T315I 细胞的CETSA-MS分析作者接着检测了K562T315I细胞中celastrol处理后可溶性蛋白质水平的变化,在雷公藤红素处理后鉴定了178种差异溶解蛋白质,主要位于DNA中心区域,包括细胞核和线粒体,更具体地说是在DNA损伤位点。此外,“分子伴侣复合物”中溶解度降低,这可能是由于雷公藤红素和HSP90之间的互作所致 雷公藤红素处理后 K562T315I细胞的CETSA-MS分析4、雷公藤红素诱导 K562T315I 细胞DNA损伤对 K562T315I细胞经雷公藤红素处理后总蛋白和可溶性蛋白水平变化的系统分析表明,雷公藤红素主要诱导K562T315I细胞中的DNA损伤和未折叠蛋白反应。因此,作者进行了实验来验证这些观察结果。结果显示雷公藤红素显著诱导γ-H2AX(DNA损伤的常见标志物)的表达,并降低DNA损伤修复相关蛋白FANCD2水平,彗星试验进一步证实了雷公藤红素促进的DNA损伤( 雷公藤红素诱导 K562T315I细胞DNA损伤5、雷公藤红素在K562T315I细胞中的靶点鉴定然后,作者在细胞裂解物中开展质谱耦合等温剂量反应-细胞热位移分析(MS-ITDR-CETSA)实验,以确定雷公藤红素的直接蛋白质靶标,特别是那些参与DNA损伤反应的蛋白质靶标。在检测到的3393种蛋白质中,有12种蛋白质表现出热稳定性的显著变化,代表了最有潜力且可信度高的靶标蛋白质。值得注意的是,雷公藤红素的已知靶标HSP90 (HSP90AA1和HSP90AB1) 的热稳定性仅表现出很小的变化,并且没有超过阈值。对这12个潜在靶标和定量蛋白质组学以及CETSA-MS分析的差异蛋白进行PPI分析,发现 YY1均为最紧密相关的蛋白质。因此,YY1与所有这些DEP/DSP的关联节点数量最多,并且可能是与DNA损伤相关的最重要的靶标。现有研究表明,YY1作为转录因子,可以调节参与DNA修复和细胞存活的各种蛋白质的表达,以响应DNA损伤。此外,HMCES已被确定为通过屏蔽脱碱基位点来保护基因组完整性免受氧化碱基损伤的关键蛋白。因此,作者继续通过蛋白质印迹结合细胞热位移分析(WB-CETSA)验证了celastrol与YY1和HMCES的互作。同样,报道的阳性对照HSP90蛋白也显示出明显的热稳定性增加( 雷公藤红素在K562T315I细胞中的靶点鉴定6、雷公藤红素与YY1和HMCES相互作用的验证为了进一步验证celastrol与YY1和HMCES的直接相互作用,合成了可点击炔烃标签功能化celastrol探针(Cel-P),该探针保留了celastrol对K562T315I细胞的抑制活性。利用该探针开展Pulldown实验发现Cel-P 能够成功地从细胞中拉下HMCES和HSP90蛋白,但由于尚不清楚的原因,在蛋白质印迹膜上的下拉样本中未检测到YY1。随后,表达并纯化重组YY1(rYY1)蛋白,发现随着Cel-P浓度的增加,rYY1的标记以剂量依赖性方式增加 雷公藤红素与YY1和HMCES相互作用的验证7、雷公藤红素通过靶向YY1和HMCES诱导DNA损伤在验证了celastrol与YY1和HMCES之间的相互作用后,作者继续在K562T315I细胞中敲低 YY1或HMCES。结果显示YY1或HMCES的敲低显著增加了DNA损伤的发生率,同时影响细胞生长,增强细胞对celastrol的敏感性。此外,与HMCES相比,YY1敲低对细胞的影响更为显著,表明YY1发挥着更为重要的作用。对接分析显示,与HMCES相比,celastrol对YY1的亲和力略强,且Celastrol与YY1上的Leu132和Val316形成氢键,与HMCES的Glu127、Arg130和Arg137形成氢键 雷公藤红素通过靶向 YY1 和 HMCES 诱导 DNA 损伤鉴于YY1在雷公藤红素诱导的DNA损伤反应中发挥关键作用,作者对YY1蛋白进行了进一步实验。发现YY1过表达对细胞生长没有显著影响,但减轻了雷公藤红素引起的细胞死亡和DNA损伤,且通过裂解的PARP1和Caspase-3水平发现YY1表达与雷公藤红素诱导的细胞凋亡呈负相关。使用双荧光素酶报告基因发现雷公藤红素显著抑制了YY1的转录活性,BLI结合试验发现celastrol 可以与 rYY1 结合(图8)。图8 YY1在雷公藤红素诱导的 K562T315I细胞DNA损伤和细胞死亡中起关键作用总结研究使用多组学方法对雷公藤红素的作用机理进行了系统研究,利用蛋白质组范围的无标记靶标反卷积方法MS-CETSA来识别雷公藤红素的蛋白质靶标。研究不仅验证了雷公藤红素通过靶向HSP90来诱导未折叠蛋白反应,而且还发现它通过直接靶向耐药 K562T315ICML 细胞中的YY1和HMCES来诱导DNA损伤(图9)。研究有助于更好地理解雷公藤红素的多方面机制。研究提供了一种有效的系统药理学工作流程范例,该范例集成了网络药理学分析、蛋白质丰度和溶解度测量以及 MS-CETSA,以揭示任何天然产物或活性化合物的作用机理。
1.藤茶是茶吗? 答:准确的说藤茶不属茶。藤茶(Ampelopsis grossede)属葡萄科蛇葡萄属显齿蛇葡萄种的多年生藤本植物,又称端午茶、藤婆茶、白茶、白茶饼、甘露茶,主要分布于湖北、福建、云南、广东、广西、江西、湖南、贵州等地,藤茶含有丰富的黄酮类化合物、酚性物质、有机酸、酸类、甙类、蛋白质、维生素C等物质,还含有钾、钙、镁、铁、锌等多有微量元素。藤茶性凉、无毒、安全,味甘甜,具有消炎、抑菌、镇痛、降脂、祛痰、祛湿、止咳、抗癌、抗高血压等作用,对治疗感冒发热、咽喉肿痛、黄疸肝炎、高血压、高血脂等有一定疗效,是一种具有独特保健功效和饮用价值的野生天然类茶植物代用茶。2.藤茶同普通茶有什么区别? 答:普通茶叶一般含茶碱,咖啡碱,茶多酚,其主要是提神,软化血管,存在多种禁忌,如晚上不能多喝,易失眠,不可与各类药物同用;还有包括儿童,妇女,中老年人等都不可多用; 而藤茶的主要成份是黄酮及各种微量元素,营养物质;聚多种功效于一身,几乎没有任何禁忌,老少皆宜。同时还可以与各类中西药同用,辅助中西药更好地发挥药效;
[color=black][b]藤青泡腾片提取工艺研究[/b][/color]藤青泡腾片是以闽产药食资源为基础制成的复方制剂,处方由藤茶、青果、葛花、甘草[font=times new roman]4[/font]味药材组成,具有调节血脂,保护化学性肝损伤的作用。传统中药煎煮繁琐,携带不便,气味较苦,将其制成泡腾片,携带、服用方便,崩解速度快,提高其生物利用度、临床疗效。本处方中各味药的主要有效成份为黄酮,水溶性较好,且二氢杨梅素等在热水中的溶解度大,因此采用水为提取溶液进行加热提取,成本低、实验条件简单。采用正交试验的方法考察各因素对总黄酮、浸膏得率的影响,获得最佳提取工艺。1.1[font=宋体][b]仪器与试药[/b][/font](1)实验仪器[font=times new roman] [/font][table][tr][td]电子分析天平[font=times new roman]XS105[/font][/td][td]METTLER TOLEDO[/td][/tr][tr][td]电子调温电热套[font=times new roman]98-1-B[/font]型[/td][td]天津市泰斯特仪器有限公司[/td][/tr][tr][td]电热恒温水浴锅[font=times new roman]HWS24[/font][/td][td]上海一恒科学仪器有限公司[/td][/tr][tr][td]常压恒温干燥箱[font=times new roman]XMTD-822[/font][/td][td]上海精宏实验设备有限公司[/td][/tr][tr][td]紫外分光光度计[font=times new roman]UV9100[/font][/td][td]北京瑞利分析仪器公司[/td][/tr][tr][td][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]([font=times new roman]200 μL[/font]、[font=times new roman]1000 μL[/font])[/td][td]GILSON[/td][/tr][/table](2)实验试药葛花[font=times new roman] [/font]产地:安徽[font=times new roman] [/font]北京三和药业有限公司[font=times new roman] [/font]藤茶(产地:广西)、青果(产地:广东)、甘草(产地:甘肃)[table][tr][td]芦丁对照品[/td][td]批号:[font=times new roman]100080-20708[/font]中国[font=宋体]食品[/font]药品[font=宋体]检[/font]定[font=宋体]研究院[/font][/td][/tr][tr][td]甲醇[font=times new roman] (AR)[/font][/td][td]国药集团化学试剂有限公司[/td][/tr][tr][td]亚硝酸钠[font=times new roman](AR)[/font][/td][td]上海联试化工试剂有限公司[/td][/tr][tr][td]硝酸铝[font=times new roman](AR)[/font][/td][td]上海展云化工有限公司[/td][/tr][tr][td]氢氧化钠[font=times new roman](AR)[/font][/td][td]上海联试化工试剂有限公司[/td][/tr][/table] [font=times new roman][size=13px]1.2 [/size][/font][size=13px]泡腾片提取工艺条件的研究[/size]1.2.1[font=宋体][b]正交试验筛选[/b][/font]称取藤茶、葛花、青果、甘草各[font=times new roman]0.5[/font]倍处方量为[font=times new roman]1[/font]份,共[font=times new roman]9[/font]份,以加水量([font=times new roman]A[/font]),提取时间([font=times new roman]B[/font]),提取次数([font=times new roman]C[/font])为考察因素,按表[font=times new roman]1[/font]的因素水平进行[font=times new roman]L9[/font][font=times new roman][size=21px]([/size][/font][font=times new roman]3[/font][font=times new roman]4[/font][font=times new roman][size=21px])[/size][/font]正交试验,根据总黄酮含量、浸膏得率进行评价,考察最佳提取工艺条件。1.2.1.1[font=宋体][b]水提取液浸膏得率的测定[/b][/font]吸取1.2.1项下提取的每份药液[font=times new roman]15 ml[/font],转移到干燥蒸发皿内,置于水浴锅内蒸发水份至流浸膏后,放入烘箱于[font=times new roman]100[/font]℃烘干到恒重,称重,记录结果并计算,结果见表[font=times new roman]2[/font]1.2.1.2[font=宋体][b]水提取液总黄酮的含量测定[/b][/font]对照品溶液的制备:称芦丁对照品适量,精密称定,加甲醇溶解并定量稀释至每1 ml含[font=times new roman]0.2 mg[/font]的芦丁溶液,制得对照品溶液。供试品溶液的制备:取上述[font=times new roman]9[/font]份提取物各[font=times new roman]1[/font] [font=times new roman]ml[/font],于[font=times new roman]50[/font] [font=times new roman]ml[/font]容量瓶中,并用水稀释至刻度。芦丁对照品标准曲线制备:精密吸取芦丁对照品溶液[font=times new roman]0.0[/font],[font=times new roman]1.0[/font],[font=times new roman]2.0[/font],[font=times new roman]3.0[/font],[font=times new roman]4.0[/font],[font=times new roman]5.0[/font],[font=times new roman]6.0[/font] [font=times new roman]ml[/font],分别置[font=times new roman]25 ml[/font]([font=times new roman]V[/font][font=times new roman]3[/font])量瓶中,加水至[font=times new roman]6 ml[/font],加入1 ml的[font=times new roman]5%[/font] NaNO2,混匀,放置[font=times new roman]6min[/font],往容量瓶里加入1 ml的[font=times new roman]10%A[/font]l[font=times new roman](NO[/font][font=times new roman]3[/font][font=times new roman])[/font][font=times new roman]3[/font],混匀后静置[font=times new roman]6min[/font],加入[font=times new roman]10[/font] ml NaOH试液,混匀,加蒸馏水至刻度,混匀,静置[font=times new roman]15[/font]分钟,以[font=times new roman]0.0 ml[/font]对照品溶液制备的溶剂为空白对照,在[font=times new roman]510nm[/font]波长下测定各组的吸光度值。以吸光度为纵坐标[font=times new roman]([/font][font=times new roman][i]A[/i][/font][font=times new roman])[/font],浓度为横坐标([font=times new roman]mg/ml[/font]),绘制标准曲线,结果见图[font=times new roman]1[/font]。样品测定:吸取待测溶液[font=times new roman]10 ml[/font]([font=times new roman]V[/font][font=times new roman]2[/font])于[font=times new roman]25 ml[/font]容量瓶中,照芦丁对照品标准曲线制备自“加入[font=times new roman]1 ml[/font]的[font=times new roman]5%[/font] NaNO2”起,在波长[font=times new roman]510nm[/font]下测定样品的吸光度,([font=times new roman][i]X[/i][/font])。根据标准曲线求出样品中总黄酮的含量[img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009212136303003_5694_2166779_3.png[/img][color=black]结果计算:[/color][color=black] [/color][color=black] [/color][color=black]X—[/color][font=宋体][color=black]试样中总黄酮百分含量,以芦丁[/color][/font][color=black](C[/color][color=black]27[/color][color=black]H[/color][color=black]30[/color][color=black]O[/color][color=black]16[/color][color=black])[/color][font=宋体][color=black]计, [/color][/font][color=black]g/100g[/color][font=宋体][color=black]([/color][/font][color=black]ml[/color][font=宋体][color=black]);[/color][/font][color=black]C—[/color][font=宋体][color=black]标准曲线上读出供试品溶液中总黄酮的浓度,[/color][/font][color=black]mg/ml[/color][font=宋体][color=black];[/color][/font][color=black]V[/color][color=black]1[/color][color=black]—[/color][font=宋体][color=black]试样定容体积,[/color][/font][color=black]ml[/color][font=宋体][color=black];[/color][/font][color=black]V[/color][color=black]2[/color][color=black]—[/color][font=宋体][color=black]吸取供试液体积,[/color][/font][color=black]ml[/color][font=宋体][color=black];[/color][/font][color=black]V[/color][color=black]3[/color][color=black]—[/color][font=宋体][color=black]显色定容体积,[/color][/font][color=black]ml[/color][font=宋体][color=black];[/color][/font][color=black]M—[/color][font=宋体][color=black]试样取样量,[/color][/font][color=black]g(ml)[/color][font=宋体][color=black]。[/color][/font][color=black]结果见表[/color][font=times new roman][color=black]2[/color][/font][color=black],表[/color][font=times new roman][color=black]3. [/color][/font][font=times new roman][color=red] [/color][/font][align=center]表[font=times new roman]1 [/font]提取正交试验因素水平表[/align][table][tr][td=1,2][align=center]水平[/align][/td][td=3,1][align=center]因素[/align][/td][/tr][tr][td][align=center]A[font=宋体]加水量[/font]([font=宋体]倍[/font])[/align][/td][td][align=center]B[font=宋体]提取时间[/font](h)[/align][/td][td][align=center]C[font=宋体]提取次数[/font][/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]10[/align][/td][td][align=center]0.5[/align][/td][td][align=center]1[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]15[/align][/td][td][align=center]1.0[/align][/td][td][align=center]2[/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]20[/align][/td][td][align=center]1.5[/align][/td][td][align=center]3[/align][/td][/tr][/table]注:以[font=times new roman]D[/font]因素为误差项[color=black]图[/color][font=times new roman][color=black]1[/color][/font][color=black]芦丁标准品标准曲线 [/color][align=center][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009212136306476_9524_2166779_3.png[/img][size=16px] [/size][/align]采用加权平均法对浸膏得率、总黄酮含量进行综合评估,由于含量对泡腾片疗效的影响较大,因此,分别给予浸膏得率、总黄酮含量[font=times new roman]40%[/font]、[font=times new roman]60%[/font]的权重进行分配。浸膏的率越高,患者最终单次的给药量越多,较低较好,以最低得率[font=times new roman]19.808%[/font]为最高得分,而总黄酮为主要有效成份,宜越高越好,故以[font=times new roman]1.969[/font]为最高得分。以序号[font=times new roman]1[/font]为例计算综合评分:[font=times new roman](19.808/19.808)*0.4+(0.796/1.969)*0.6=0.643[/font],同理,可求得其余各综合评分,结果见表[font=times new roman]2.[/font] 表[font=times new roman]2[/font]提取正交试验结果([font=times new roman][i]n[/i][/font][font=times new roman]=9[/font])[table][tr][td][align=center]序号[/align][/td][td][align=center]A[/align][/td][td][align=center]B[/align][/td][td][align=center]C[/align][/td][td][align=center]D[/align][/td][td][align=center]浸膏得率[font=times new roman](%)[/font][/align][/td][td][align=center]总黄酮含量[font=times new roman](g)[/font][/align][/td][td][align=center]综合评分[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]19.808 [/align][/td][td][align=center]0.796 [/align][/td][td][align=center]0.643 [/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]2[/align][/td][td][align=center]2[/align][/td][td][align=center]29.159 [/align][/td][td][align=center]1.109 [/align][/td][td][align=center]0.610 [/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]3[/align][/td][td][align=center]3[/align][/td][td][align=center]3[/align][/td][td][align=center]34.835 [/align][/td][td][align=center]1.499 [/align][/td][td][align=center]0.684 [/align][/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]33.656 [/align][/td][td][align=center]1.490 [/align][/td][td][align=center]0.689 [/align][/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]2[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]37.467 [/align][/td][td][align=center]1.854 [/align][/td][td][align=center]0.776 [/align][/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]23.851 [/align][/td][td][align=center]0.978 [/align][/td][td][align=center]0.630 [/align][/td][/tr][tr][td][align=center]7[/align][/td][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]3[/align][/td][td][align=center]2[/align][/td][td][align=center]40.161 [/align][/td][td][align=center]1.969 [/align][/td][td][align=center]0.797 [/align][/td][/tr][tr][td][align=center]8[/align][/td][td][align=center]3[/align][/td][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]3[/align][/td][td][align=center]26.402 [/align][/td][td][align=center]1.099 [/align][/td][td][align=center]0.635 [/align][/td][/tr][tr][td][align=center]9[/align][/td][td][align=center]3[/align][/td][td][align=center]3[/align][/td][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]34.196 [/align][/td][td][align=center]1.544 [/align][/td][td][align=center]0.702 [/align][/td][/tr][tr][td][align=center]K1[/align][/td][td][align=center]1.94 [/align][/td][td][align=center]2.13 [/align][/td][td][align=center]1.91 [/align][/td][td][align=center]2.12 [/align][/td][td] [/td][td] [/td][td] [/td][/tr][tr][td][align=center]K2 [/align][/td][td][align=center]2.10 [/align][/td][td][align=center]2.02 [/align][/td][td][align=center]2.00 [/align][/td][td][align=center]2.04 [/align][/td][td] [/td][td] [/td][td] [/td][/tr][tr][td][align=center]K3[/align][/td][td][align=center]2.13 [/align][/td][td][align=center]2.02 [/align][/td][td][align=center]2.26 [/align][/td][td][align=center]2.01 [/align][/td][td] [/td][td] [/td][td] [/td][/tr][tr][td][align=center]R[/align][/td][td][align=center]0.07 [/align][/td][td][align=center]0.04 [/align][/td][td][align=center]0.12 [/align][/td][td][align=center]0.04 [/align][/td][td][align=center] [/align][/td][td][align=center] [/align][/td][td][align=center] [/align][/td][/tr][/table][align=center]表[font=times new roman]3[/font]提取正交试验方差分析[/align][table][tr][td][align=center]方差来源[/align][/td][td][align=center]离差平方和[/align][/td][td][align=center]自由度[/align][/td][td][align=center]F[font=宋体]值[/font][/align][/td][td][align=center]均方[/align][/td][td][align=center]显著性[/align][/td][/tr][tr][td][align=center]加水量[/align][/td][td][align=center]0.007349[/align][/td][td][align=center]2[/align][/td][td][align=center]3.2139[/align][/td][td][align=center]0.003675[/align][/td][td] [/td][/tr][tr][td][align=center]提取时间[/align][/td][td][align=center]0.002731[/align][/td][td][align=center]2[/align][/td][td][align=center]1.1945[/align][/td][td][align=center]0.001366[/align][/td][td] [/td][/tr][tr][td][align=center]提取次数[/align][/td][td][align=center]0.02189[/align][/td][td][align=center]2[/align][/td][td][align=center]9.5733[/align][/td][td][align=center]0.01095[/align][/td][td][align=center]**[/align][/td][/tr][tr][td][align=center]误差[/align][/td][td][align=center]0.002287[/align][/td][td][align=center]2[/align][/td][td][align=center]1.0000 [/align][/td][td][align=center]0.001143[/align][/td][td] [/td][/tr][/table]由表[font=times new roman]3[/font]可知,根据水提取液中总黄酮含量与浸膏得率进行评估,各因素对结果的影响大小:提取次数[font=times new roman][/font]加水量[font=times new roman][/font]提取时间,即主要影响因素是提取次数,其次是加水量,提取时间影响最小。以实验结果为参考,结合实际生产情况,最终确定提取工艺为:加水[font=times new roman]20[/font]倍量,每次提取[font=times new roman]0.5h[/font],提取[font=times new roman]3[/font]次。1.2.2[font=宋体][b]提取正交验证实验[/b][/font]根据以上所选最佳提取工艺条件,加水[font=times new roman]20[/font]倍量,每次提取[font=times new roman]0.5h[/font],提取[font=times new roman]3[/font]次,平行[font=times new roman]3[/font]份,对水提取液的浸膏得率与总黄酮含量进行测定,按[font=times new roman]1.2.1.2[/font]项下的方法计算综合评分后,求平均得分,结果见表[font=times new roman]4.[/font][align=center]表[font=times new roman]4[/font]提取正交实验验证结果([font=times new roman][i]n[/i][/font][font=times new roman]=3[/font])[/align][table][tr][td][align=center]编号[/align][/td][td][align=center]浸膏得率(%)[/align][/td][td][align=center]总黄酮含量(g)[/align][/td][td][align=center]综合评分[/align][/td][td][align=center]平均得分[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]37.3[/align][/td][td][align=center]2.036[/align][/td][td][align=center]0.833[/align][/td][td=1,3][align=center]0.830[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]38.1[/align][/td][td][align=center]2.038[/align][/td][td][align=center]0.829[/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]37.4[/align][/td][td][align=center]2.021[/align][/td][td][align=center]0.828[/align][/td][/tr][/table]由表[font=times new roman]4[/font]可知,[font=times new roman]3[/font]份平行实验最终的平均得分为[font=times new roman]0.830[/font],接近于正交设计中的[font=times new roman]A3B1C3[/font]综合评分,且评分最高,有良好的重复性和较高的准确率,所筛选的提取工艺条件基本稳定,可作为藤青泡腾片的提取方法。小结与讨论在提取工艺的探讨过程中,用正交试验的方法研究加水量、提取时间、提取次数对药液浸膏得率和总黄酮含量的影响,获得最适提取条件为:[font=times new roman]20[/font]倍量水,提取[font=times new roman]3[/font]次,每次提取[font=times new roman]0.5h[/font]。试验中发现,青果为橄榄的干燥果实,本处方中用量较少,为方便称取,同时提高没食子酸等有效成份的提取率,宜先将其进行粉碎;藤茶、葛花密度小,提取过程中浮于水面,应将其充分润湿,使其浸没于水中,以免影响各成份的提取率;若直接加热煎煮,提取过程中水分蒸发严重,实验结果重现性差,宜采用冷凝回流的方法进行提取。

紫藤鲜花香气成分的研究紫藤又名朱藤、藤罗, 豆科紫藤属落叶藤本树种, 分布于我国西北,华北及长江流域诸省。喜缠绕上升, 花序总状下垂, 花期4、5月, 花蓝紫色, 先叶开放, 穗大而美, 具芳香, 花粉为扁球形, 观赏价值高, 广泛应用于园林、庭院绿化及盆景用材。紫藤不仅是早春观花植物,而且有着较高的经济价值, 其花含芳香油, 可用于提取紫藤鲜花油, 花瓣用糖渍制糕点, 根皮和花药用, 能解毒驱虫, 止吐泻, 花穗治腹水;此外,从其种子中提取所得的紫藤凝集素,在临床免疫和细胞遗传研究中也有一定的应用前景。人们研究植物芳香成分多以浸膏或净油为对象, 由于受萃取溶剂的干扰, 影响到香气的真实性。固相微萃取技术属于非溶剂型萃取法,是一种新的采样技术,其装置简单、操作方便,能与其它分析仪器联用,对挥发性和半挥发性的有机物进行分析测定,特别适用于现场分析,目前已在环保、医药、食品、香料等领域得到广泛应用, 并取得良好的效果。但目前未见用SPME 研究紫藤鲜花香气成分的研究报道。本实验在室温下,采用固相微萃取吸附富集紫藤鲜花的香气成分,然后用GC/MS分析,为全面了解紫藤鲜花的香气成分,对紫藤的进一步研究及开发利用, 更好地开发利用我国紫藤资源提供科学依据。 1 实验部分1.1 材料与仪器紫藤鲜花采自浙江工业大学校园内,采集后立即进行分析。手动固相微萃取进样器,美国Supelco 公司制造;30 µm 聚二甲基硅氧烷(PDMS)萃取纤维头, 美国Supelco 公司制造;GC3800 / MS Saturn 2000气相色谱-质谱联用仪,配有液体化学源(色谱级乙腈为化学源反应试剂),美国Varian公司制造。1.2 SPME取样[/
藤黄【英文名】Gamboge【别名】玉黄、月黄。【来源】药材基源:为藤黄科植物藤黄的树脂。拉丁植物动物矿物名:Garcinia hanburyi Hook.f.采收和储藏:在开花之前,在离地3m处将茎干的皮部作螺旋状的割伤,伤口内插一竹简,盛受流出的树脂,加热蒸干,用刀刮下,即可。【原形态】藤黄 常绿乔木,高约15-18m。小枝四棱形。单叶对生,几无柄;叶片薄革质,阔披针形,长9-13cm,先端尖,基部楔形,全缘或微波状。花单生或为聚啊伞花序;两性与单性花黄存;花绿白色,无梗;萼片5,花瓣5;雄花通常2-3朵簇生,雄蕊多数,花丝短,花药1室,横裂;雌花具退化雄蕊12枚,其基部合生而环绕子房周围,子房上位,平滑无毛,柱头盾形,为不整齐之裂片或瘤块,4室。浆果,径约2cm。种子4颗。花期11月,果熟期次年2-3月。【生境分布】生态环境:原产柬埔寨及马来西亚,印度、泰国、越南亦产。资源分布:现我国广东、广西有引种栽培。【栽培】野生【性状】性状鉴别 树脂为不规则的圆柱形或块状,棕红色或橙色,外被黄绿色粉霜,可见纵条纹。质硬脆,较易击碎,破面有空隙,具蓝褐色略带蜡样光泽。味辛,有毒。以半透明、色红黄者为佳。【化学成份】藤黄树含藤黄酸(gambogic acid),别藤黄酸(allogambogic acid),新藤黄酸(neogambogic acid)。【药理作用】1.抗菌作用:其种子衣中的色素--藤黄宁对金黄色葡萄球菌有抑制作用,体外的有效浓度为1∶10000;对若干真菌、草分支杆菌、人型结核杆菌效力很豹,对大肠杆菌亦无效闭。新藤黄宁也有抗金黄色葡韵球菌的作用。异构体(异藤黄宁及异新藤黄宁)的抗原虫作用较其母体有效(藤黄宁或新藤黄宁通过肠管时可异构化)。藤黄索在体外对非致病性原虫有抑制作用,特别是β-及γ-藤黄素效力较强。抗原虫与抗菌作用,并不平行。α1-及γ-藤黄素在各方面(如抑制革兰氏阳性细菌之能力、对小鼠人工感染葡萄球菌的保护作用、在血清或金属离干存在时的反应、对热及酸碱度的稳定性等)皆与α2-及β-藤黄素相似。2.其他作用与毒性:β-及α1-藤黄索在超过治疗量时可引起小鼠腹泻(β-藤黄索致泻力更强)。对小鼠的急性毒性(半数致死量,mg/kg)为:α1-及γ-藤黄素皮下注射均为277;腹腔注射分别为87.1及77.18;静脉注射分别为108.4及108,这些数值与α2-及β-藤黄素的毒性栖差甚微。【炮制】制藤黄:1.先用豆腐一大块,平铺于盘内,中间挖一不透底的槽,将藤黄放人,再用豆腐盖严,置于笼屉内,放入锅中,将此锅再坐于大锅内,隔水加热,蒸至藤黄溶化,取出,冷却凝固,去豆腐晒干。2.先将藤黄放入磁罐内,加入比藤黄多10倍量的鲜荷叶煎汁,将罐放入锅中,隔水加热40-60分钟,至罐内溶液呈紫红色时,倒入铜锅内再煎,浓缩成糊状,晒干。(每藤黄斤约用荷 叶半斤煎法,去渣)3.将藤黄加入鲜山羊血中,置铜锅内,加水同煮5-6小时,去山羊血晾干。(每藤黄1斤,用鲜山羊血半斤)【性味】酸;涩;凉;有毒【功能主治】消肿;攻毒;止血;杀虫;祛腐剑疮。主痈疽肿毒;溃疡;湿疮;肿癣;顽癣;跌打肿痛;创伤出血及烫伤【用法用量】外用:适量,研末调敷、磨汁涂或熬督涂。内服:0.03-0.06g,入丸剂
[align=center][font='times new roman'][size=20px] [/size][/font][font='times new roman'][size=20px]藤青泡[/size][/font][font='times new roman'][size=20px]腾片成型工艺研究[/size][/font][/align][size=16px]为了提高产品疗效,质量的稳定性,将复方提取液制成泡腾片,通过摸索性试验,用崩解速度、发泡数量、[/size][size=16px]pH[/size][size=16px]值以及口感为评价标准[/size][size=16px],[/size][size=16px]筛选稀释剂、崩解剂、粘合剂、[/size][size=16px]矫[/size][size=16px]味剂的种类,确定各自用量,[/size][size=16px]探索[/size][size=16px]藤青泡[/size][size=16px]腾片[/size][size=16px]最佳组[/size][size=16px]方及配比[/size][size=16px]。[/size][font='times new roman'][size=20px]仪器与试药[/size][/font][size=16px]([/size][size=16px]1[/size][size=16px])[/size][size=16px]实验仪器[/size][table][tr][td][size=16px]常压恒温干燥箱[/size][size=16px] XMTD-822[/size][/td][td][size=16px]上海精宏实验设备有限公司[/size][/td][/tr][tr][td][size=16px]单冲压片机[/size][size=16px] TDP-1.5[/size][/td][td][size=16px]上海超亿制药机械设备有限公司[/size][/td][/tr][/table][size=16px]([/size][size=16px]2[/size][size=16px])[/size][size=16px]实验试[/size][size=16px]药[/size][size=16px] [/size][table][tr][td][size=16px]柠檬酸[/size][size=16px] (AR) [/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]无水乙醇[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]酒石酸[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]碳酸氢钠[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]碳酸钠[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]无水乳糖[/size][size=16px] [/size][/td][td][size=16px]Aladdin Industrial [/size][size=16px]Inc[/size][/td][/tr][tr][td][size=16px]聚乙烯吡咯烷酮[/size][size=16px]K30[/size][/td][td][size=16px]上海展云化工有限公司[/size][/td][/tr][tr][td][size=16px]甘草甜素(食用级)[/size][/td][td][size=16px]陕西帕尼尔生物科技有限公司[/size][/td][/tr][tr][td][size=16px]甜菊糖苷(食用级)[/size][/td][td][size=16px]南通华康甜菊糖有限公司[/size][/td][/tr][tr][td][size=16px]阿斯巴甜(食用级)[/size][/td][td][size=16px]Aladdin Industrial [/size][size=16px]Inc[/size][/td][/tr][tr][td][size=16px]硬脂酸镁[/size][size=16px] [/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]PEG6000[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][/table][font='times new roman'][size=20px]成型工艺处方的筛选[/size][/font][font='times new roman'][size=18px]崩解剂的筛选与优化[/size][/font][size=16px]([/size][size=16px]1[/size][size=16px])崩解剂的种类筛选[/size][size=16px]按表[/size][size=16px]9[/size][size=16px]中的组份进行制软材,压片,崩解实验,以筛选崩解剂种类。[/size][align=center][/align][align=center][size=16px]表[/size][size=16px]9[/size][size=16px]不同种类崩解剂的制剂考察[/size][/align][table][tr][td][align=center][size=16px]样品[/size][/align][/td][td][align=center][size=16px]稠[/size][size=16px]浸膏[/size][size=16px](g) [/size][/align][/td][td][align=center][size=16px]酸材[/size][size=16px](g) [/size][/align][/td][td][align=center][size=16px]碱材[/size][size=16px](g)[/size][/align][/td][td][align=center][size=16px]结果[/size][/align][/td][/tr][tr][td][align=center][size=16px]1[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]柠檬酸[/size][size=16px]1.1[/size][/align][/td][td][align=center][size=16px]碳酸钠[/size][size=16px]0.9[/size][/align][/td][td][align=center][size=16px]易吸湿,气泡多,崩解快[/size][/align][/td][/tr][tr][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]柠檬酸[/size][size=16px]1.1[/size][/align][/td][td][align=center][size=16px]碳酸氢钠[/size][size=16px]0.9[/size][/align][/td][td][align=center][size=16px]易吸湿,气泡量适中,崩解快[/size][/align][/td][/tr][tr][td][align=center][size=16px]3[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]酒石酸[/size][size=16px]1.1[/size][/align][/td][td][align=center][size=16px]碳酸钠[/size][size=16px]0.9[/size][/align][/td][td][align=center][size=16px]较不吸湿,气泡多,崩解快[/size][/align][/td][/tr][tr][td][align=center][size=16px]4[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]酒石酸[/size][size=16px]1.1[/size][/align][/td][td][align=center][size=16px]碳酸氢钠[/size][size=16px]0.9[/size][/align][/td][td][align=center][size=16px]较不吸湿,气泡量适中,崩解快[/size][/align][/td][/tr][/table][size=16px]结果表明,样品[/size][size=16px]4[/size][size=16px]的效果较好。[/size][size=16px]([/size][size=16px]2[/size][size=16px])崩解剂的用量优化[/size][size=16px]为了获得崩解剂的最佳用量,以表[/size][size=16px]9[/size][size=16px]中样品[/size][size=16px]4[/size][size=16px]为基础,查阅相应文献崩解剂的用量大多在[/size][size=16px]20%-40%[/size][size=16px],酸碱比例在[/size][size=16px]1:1-1.2:1[/size][size=16px]之间,[/size][size=16px]故设计[/size][size=16px]表[/size][size=16px]10[/size][size=16px],不同崩解剂的用量及酸碱比例,根据片剂的崩解速度,得到最佳用量及酸碱比例。[/size][align=center][size=18px]表[/size][size=18px]10[/size][size=16px]崩解剂的用量及酸碱比例优化[/size][/align][table][tr][td][align=center][size=16px]样品[/size][/align][/td][td][align=center][size=16px]崩解剂占片[/size][/align][align=center][size=16px]重比例[/size][size=16px](%)[/size][/align][/td][td][align=center][size=16px]酸碱比例[/size][/align][/td][td][align=center][size=16px]崩解时间([/size][size=16px]s[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]结果[/size][/align][/td][/tr][tr][td][align=center][size=16px]5[/size][/align][/td][td][align=center][size=16px]20[/size][/align][/td][td][align=center][size=16px]1:1[/size][/align][/td][td][align=center][size=16px]55[/size][/align][/td][td][align=center][size=16px]泡量适中[/size][size=16px],部分颗粒[/size][size=16px]不[/size][size=16px]崩解[/size][/align][/td][/tr][tr][td][align=center][size=16px]6[/size][/align][/td][td][align=center][size=16px]20[/size][/align][/td][td][align=center][size=16px]1.2:1[/size][/align][/td][td][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]泡量适中[/size][size=16px],崩解较完全[/size][/align][/td][/tr][tr][td][align=center][size=16px]7[/size][/align][/td][td][align=center][size=16px]30[/size][/align][/td][td][align=center][size=16px]1:1[/size][/align][/td][td][align=center][size=16px]49[/size][/align][/td][td][align=center][size=16px]气泡较多,部分颗粒[/size][size=16px]不[/size][size=16px]崩解[/size][/align][/td][/tr][tr][td][align=center][size=16px]8[/size][/align][/td][td][align=center][size=16px]30[/size][/align][/td][td][align=center][size=16px]1.2:1[/size][/align][/td][td][align=center][size=16px]47[/size][/align][/td][td][align=center][size=16px]气泡较多,崩解较完全[/size][/align][/td][/tr][tr][td][align=center][size=16px]9[/size][/align][/td][td][align=center][size=16px]40[/size][/align][/td][td][align=center][size=16px]1:1[/size][/align][/td][td][align=center][size=16px]47[/size][/align][/td][td][align=center][size=16px]气泡多,部分颗粒[/size][size=16px]不[/size][size=16px]崩解[/size][/align][/td][/tr][tr][td][align=center][size=16px]10[/size][/align][/td][td][align=center][size=16px]40[/size][/align][/td][td][align=center][size=16px]1.2:1[/size][/align][/td][td][align=center][size=16px]45[/size][/align][/td][td][align=center][size=16px]气泡多,崩解较完全[/size][/align][/td][/tr][/table][size=16px]由上表可知,崩解剂中酸微过量时崩解完全,比例为[/size][size=16px]1.2:1[/size][size=16px]时较好;当崩解剂在片重中的比例增加时,崩解时间减小,但变化幅度较小,且崩解剂比例增加时,溶液的[/size][size=16px]p[/size][size=16px]H[/size][size=16px]值减小,对胃伤害较大,故选用[/size][size=16px]崩解剂占片重[/size][size=16px]比例[/size][size=16px]20%[/size][size=16px],酸碱比例为[/size][size=16px]1.2:1[/size][size=16px]为[/size][size=16px]最[/size][size=16px]宜。[/size][font='times new roman'][size=18px]稀释剂的选择[/size][/font][size=16px]由于泡腾片溶解以后溶液[/size][size=16px]应该[/size][size=16px]澄清,因此稀释剂应[/size][size=16px]能溶于水[/size][size=16px]的,[/size][size=16px]本实验[/size][size=16px]主要考虑可溶性淀粉、乳糖、糖粉,由于[/size][size=16px]藤青泡[/size][size=16px]腾片的提取液味较苦,加入糖粉后,挤压制[/size][size=16px]粒比较[/size][size=16px]困难,乳糖[/size][size=16px]易过筛[/size][size=16px]制粒,可压性强,故选用乳糖作为稀释剂。[/size][font='times new roman'][size=18px]粘合剂的选择[/size][/font][size=16px]常用的粘合剂有乙醇、淀粉浆、[/size][size=16px]PVP[/size][size=16px]。本实验分别用无水乙醇、[/size][size=16px]10%[/size][size=16px]淀粉浆、[/size][size=16px]5%[/size][size=16px]聚乙烯吡咯烷酮[/size][size=16px]K30[/size][size=16px]乙醇溶液作为粘合剂,分别与酸材、[/size][size=16px]碱材混匀[/size][size=16px],过[/size][size=16px]20[/size][size=16px]目筛挤压制粒,[/size][size=16px]6[/size][size=16px]0[/size][size=16px]℃[/size][size=16px]干燥[/size][size=16px]30min[/size][size=16px],压片。乙醇作为粘合剂,干燥以后颗粒较散,[/size][size=16px]细分较多[/size][size=16px],流动性较差,片重差异较大,淀粉[/size][size=16px]浆[/size][size=16px]粘合性较差,压片时容易出现松片,聚乙烯吡咯烷酮[/size][size=16px]K30[/size][size=16px]颗粒不易结块,崩解良好,故选聚乙烯吡咯烷酮[/size][size=16px]K30[/size][size=16px]作粘合剂。[/size][font='times new roman'][size=18px]润滑剂的选择[/size][/font][size=16px] [/size][size=16px]湿法制粒时,在压片前通常需要加入适当的润滑剂,以改善颗粒的流动性,[/size][size=16px]使[/size][size=16px]片重[/size][size=16px]均匀[/size][size=16px],片剂[/size][size=16px]外表[/size][size=16px]光滑。本实验[/size][size=16px]对[/size][size=16px]硬脂酸镁、[/size][size=16px]聚乙二醇[/size][size=16px]6000[/size][size=16px]进行对比试验[/size][size=16px],[/size][size=16px]根据[/size][size=16px]休止角与堆积密度[/size][size=16px]的大小[/size][size=16px],[/size][size=16px]比较两者[/size][size=16px]对颗粒流动性的影响[/size][size=16px]。[/size][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009241643187478_4227_2166779_3.jpeg[/img][size=16px]3.2.4[/size][size=16px].1[/size][size=16px]休止角的测定[/size][size=16px]用固定[/size][size=16px]圆锥底法[/size][size=16px]进行[/size][size=16px]测量[/size][size=16px],把漏斗固定[/size][size=16px]于[/size][size=16px]铁架台上,下方放置一张滤纸,[/size][size=16px]漏斗下端出口垂直于滤纸表面且对准圆心,调节[/size][size=16px]高度约[/size][size=16px]4cm[/size][size=16px],把加入润滑剂的药物颗粒[/size][size=16px]从上口[/size][size=16px]倒入漏斗中,直到铺满[/size][size=16px]整张[/size][size=16px]滤纸为止,测[/size][size=16px]量[/size][size=16px]圆锥的高度,如图[/size][size=16px]3[/size][size=16px],计算休止角:[/size][size=16px]atgθ[/size][size=16px]= h/r[/size][size=16px],平行测定[/size][size=16px]3[/size][size=16px]次,结果见表[/size][size=16px]11.[/size][size=16px]图[/size][size=16px]3 [/size][size=16px]流动角测定装置[/size][size=16px] [/size][size=16px]堆积密度的测定[/size][size=16px] [/size][size=16px]取一只[/size][size=16px]20 ml[/size][size=16px]量筒,洗净,干燥,称重,将颗粒从距[/size][size=16px]瓶口正[/size][size=16px]上方约[/size][size=16px]5cm[/size][size=16px]处流下,直至量筒内颗粒堆积至[/size][size=16px]20 ml[/size][size=16px]刻度处,称量[/size][size=16px]出量筒[/size][size=16px]总重量,求得颗粒重量,平行测[/size][size=16px]3[/size][size=16px]次,取平均值,根据重量与体积计算堆积密度,结果见表[/size][size=16px]11.[/size][align=center][size=16px]表[/size][size=16px]11[/size][size=16px]润滑剂对颗粒流动性影响考察[/size][/align][table][tr][td][align=center][size=16px]样品[/size][/align][/td][td][align=center][size=16px]药物颗粒量[/size][size=16px](g)[/size][/align][/td][td][align=center][size=16px]硬脂酸镁([/size][size=16px]g[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]PEG6000(g)[/size][/align][/td][td][align=center][size=16px]休止角[/size][size=16px]([/size][size=16px]℃[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]堆积密度[/size][size=16px](g/cm[/size][font='times new roman'][size=16px]3[/size][/font][size=16px])[/size][/align][/td][/tr][tr][td][align=center][size=16px]11[/size][/align][/td][td][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]0[/size][/align][/td][td][align=center][size=16px]0[/size][/align][/td][td][align=center][size=16px]37.6[/size][/align][/td][td][align=center][size=16px]0.53[/size][/align][/td][/tr][tr][td][align=center][size=16px]12[/size][/align][/td][td][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]0[/size][/align][/td][td][align=center][size=16px]27.9[/size][/align][/td][td][align=center][size=16px]0.60 [/size][/align][/td][/tr][tr][td][align=center][size=16px]13[/size][/align][/td][td][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]0[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]28.1[/size][/align][/td][td][align=center][size=16px]0.59[/size][/align][/td][/tr][/table][size=16px]由[/size][size=16px]上表堆积密度可知,加入润滑剂以后,粉体的堆积度明显增大,即粉体的流动性、填充性得到改善,压片过程中可减小片重差异,同时减小粉体间的孔隙率,增强可压性;而休止角方面,[/size][size=16px]在没有加[/size][size=16px]任何润滑剂的时候,休止角大,流动性[/size][size=16px]不好[/size][size=16px],且压片后表面粗糙无光泽,不符合生产要求,加入硬脂酸镁、[/size][size=16px]PEG6000[/size][size=16px]后,流动性[/size][size=16px]得到提高[/size][size=16px],片重差异减小,片剂表面光滑,但硬脂酸镁崩解后在溶液表面形成一层薄膜,有浑浊感,故[/size][size=16px]以[/size][font='arial'][size=16px][color=#333333]聚乙二醇[/color][/size][/font][size=16px]6000[/size][size=16px]作为润滑剂。在实验过程中发现,在相同重量的颗粒中,随着加入润滑剂的增加,片剂表面变光滑,但崩解时间也相应延长,实验表明,当用量为[/size][size=16px]2%[/size][size=16px]时,表面光滑,崩解性能良好。[/size][font='times new roman'][size=18px]矫[/size][/font][font='times new roman'][size=18px]味剂的选择[/size][/font][size=16px]矫[/size][size=16px]味剂种类选择[/size][size=16px] [/size][size=16px]由于[/size][size=16px]藤青泡[/size][size=16px]腾片提取液的苦味较强,需[/size][size=16px]采用[/size][size=16px]合适的[/size][size=16px]矫[/size][size=16px]味剂[/size][size=16px]进行矫正[/size][size=16px]。本实验中,主要考察了蔗糖、阿斯巴甜、甜菊糖苷以及甘草甜素对苦味的改善情况,结果表明,蔗糖由于甜度小,制剂过程中加入量大,不符合生产要求;阿斯巴甜甜度较大,但加入后[/size][size=16px]药物[/size][size=16px]变硬结块,难以挤压制粒;甜菊糖苷,甜度大,服用后涩味明显,不宜作为[/size][size=16px]矫[/size][size=16px]味剂,甘草甜素甜度大,服用后喉间有回甘,[/size][size=16px]且藤青泡[/size][size=16px]腾片原料药中含有甘草,故选用甘草甜素作为[/size][size=16px]矫[/size][size=16px]味剂。[/size][size=16px]矫[/size][size=16px]味剂用量优化[/size][size=16px]甘草甜素甜度较大,且个人口感差异较大,因此在[/size][size=16px]矫[/size][size=16px]味剂限量范围内,设计添加量为[/size][size=16px]0.45%[/size][size=16px],[/size][size=16px]0.90%[/size][size=16px],[/size][size=16px]1.8[/size][size=16px]0[/size][size=16px]%[/size][size=16px]三个梯度甜度的[/size][size=16px]藤青泡[/size][size=16px]腾片,在人群中进行口感调查,以[/size][size=16px]0-10[/size][size=16px]分进行评价,口感满意度越好,分值越高,最后[/size][size=16px]求平均[/size][size=16px]得分,获得最受大众接受甜度。结果见表[/size][size=16px]12.[/size][align=center][size=16px]表[/size][size=16px]12[/size][size=16px]不同甜度口感满意度调查结果[/size][size=16px]([/size][size=16px]n[/size][size=16px]=16[/size][size=16px])[/size][/align][table][tr][td][align=center][size=16px]样品[/size][/align][/td][td][align=center][size=16px]矫[/size][size=16px]味剂添加量[/size][/align][/td][td][align=center][size=16px]总得分[/size][/align][/td][td][align=center][size=16px] [/size][size=16px]平均得分[/size][/align][/td][td][align=center][size=16px]备注[/size][/align][/td][/tr][tr][td][align=center][size=16px]14[/size][/align][/td][td][align=center][size=16px]0.45%[/size][/align][/td][td][align=center][size=16px]87[/size][/align][/td][td][align=center][size=16px]5.44[/size][/align][/td][td][align=center][size=16px]苦味强烈[/size][/align][/td][/tr][tr][td][align=center][size=16px]15[/size][/align][/td][td][align=center][size=16px]0.90%[/size][/align][/td][td][align=center][size=16px]107[/size][/align][/td][td][align=center][size=16px]6.69[/size][/align][/td][td][align=center][size=16px] [/size][size=16px]酸味较明显[/size][/align][/td][/tr][tr][td][align=center][size=16px]16[/size][/align][/td][td][align=center][size=16px]1.80%[/size][/align][/td][td][align=center][size=16px]115[/size][/align][/td][td][align=center][size=16px]7.19[/size][/align][/td][td][align=center][size=16px] [/size][size=16px]酸度适宜,无苦涩感[/size][/align][/td][/tr][/table][size=16px]由[/size][size=16px]上表可知,在甘草甜[/size][size=16px]素加入[/size][size=16px]量较少时,药物提取液的苦味较明显,随添加量增加,苦味被覆盖,酒石酸的味道明显,当加入量为[/size][size=16px]1.8%[/size][size=16px]时,口感满意。[/size][font='times new roman'][size=20px]藤青泡[/size][/font][font='times new roman'][size=20px]腾片成型工艺路线[/size][/font][font='times new roman'][size=20px][color=#ff0000] [/color][/size][/font][align=center][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009241643189568_2916_2166779_3.jpeg[/img][/align][font='times new roman'][size=20px]藤青泡[/size][/font][font='times new roman'][size=20px]腾片处方工艺[/size][/font][size=16px](1)[/size][size=16px]处方:[/size][size=16px] [/size][size=16px] [/size][size=16px][color=#ff0000] [/color][/size][table][tr][td][align=center][size=16px]藤茶[/size][/align][/td][td][align=center][size=16px]60[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]葛花[/size][/align][/td][td][align=center][size=16px]30[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]青果[/size][/align][/td][td][align=center][size=16px]2[/size][size=16px]0[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]甘草[/size][/align][/td][td][align=center][size=16px]12[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]酒石酸[/size][/align][/td][td][align=center][size=16px]42.5g[/size][/align][/td][/tr][tr][td][align=center][size=16px]碳酸氢钠[/size][size=16px]([/size][size=16px]外加[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]30.6g[/size][/align][/td][/tr][tr][td][align=center][size=16px]乳糖[/size][/align][/td][td][align=center][size=16px]247[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]甘草甜素[/size][/align][/td][td][align=center][size=16px]8.5g[/size][/align][/td][/tr][tr][td][align=center][size=16px]PEG6000([/size][size=16px]外加[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]9[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]5%PVP[/size][/align][/td][td][align=center][size=16px]适量[/size][/align][/td][/tr][/table][size=16px]共制成泡腾片([/size][size=16px]0.45g/[/size][size=16px]片)[/size][size=16px] [/size][size=16px] [/size][size=16px] 1000[/size][size=16px]片[/size][size=16px](2)[/size][size=16px]制备工艺[/size][size=16px]:[/size][size=16px]将藤茶、葛花、青果、甘草加水煎煮三次,每次[/size][size=16px]30[/size][size=16px]分钟,分次滤过,合并滤液,浓缩成流浸膏,放冷,加乙醇适量,静置,取上清液,回收乙醇,浓缩成稠膏,备用。加入酒石酸、乳糖、甘草甜素,混匀,以[/size][size=16px]5%PVP[/size][size=16px]乙醇溶液为粘合剂,制粒,干燥,整粒,加入[/size][size=16px]PEG6000[/size][size=16px]和碳酸氢钠,混匀,压制成[/size][size=16px]1000[/size][size=16px]片,即得。[/size][font='times new roman'][size=20px]小结与讨论[/size][/font][size=16px]通过[/size][size=16px]对泡腾片[/size][size=16px]组[/size][size=16px]方及配比的探讨[/size][size=16px],最终[/size][size=16px]得到[/size][size=16px]最[/size][size=16px]适[/size][size=16px]配方为:崩解剂[/size][size=16px]15.7%[/size][size=16px],酒石酸与碳酸氢钠比例[/size][size=16px]1.2:1[/size][size=16px],[/size][size=16px] [/size][size=16px]稀释剂乳糖[/size][size=16px]53.2%[/size][size=16px],粘合剂[/size][size=16px]PEG6000 1.9%[/size][size=16px],[/size][size=16px]矫[/size][size=16px]味剂甘草甜素[/size][size=16px]1.8%[/size][size=16px],[/size][size=16px]PVP[/size][size=16px]适量,按[/size][size=16px]3.4[/size][size=16px]项下的制备工艺进行制备。实验过程中发现,由于黄酮会与碱性崩解剂碳酸氢钠发生化学反应,所制的颗粒颜色变深,导致酸碱软材颜色不一致,压片后出现花斑,因此碳酸氢钠采用外加法,即在压片前加[/size][size=16px]入、混合后压片;由于浸膏中含有部分多糖,解热条件下粘度增加,干燥过程中温度不宜过高;润滑剂的用量需适量,过少表面粗糙,片重差异较大,过多会导致崩解迟缓;本实验过程中,用单冲压片机进行压片,使前需进行试压,调整好进样量、压力后在进行压片,以免出现顶车现象,损坏电机,手动压片时尽量转动速度均匀;由于空气湿度、[/size][size=16px]温度对泡腾[/size][size=16px]片的影响较大,整个生产过程,相对湿度[/size][size=16px]不宜超过[/size][size=16px]45%[/size][size=16px],温度在[/size][size=16px]15℃-25℃[/size][size=16px]为宜。[/size]
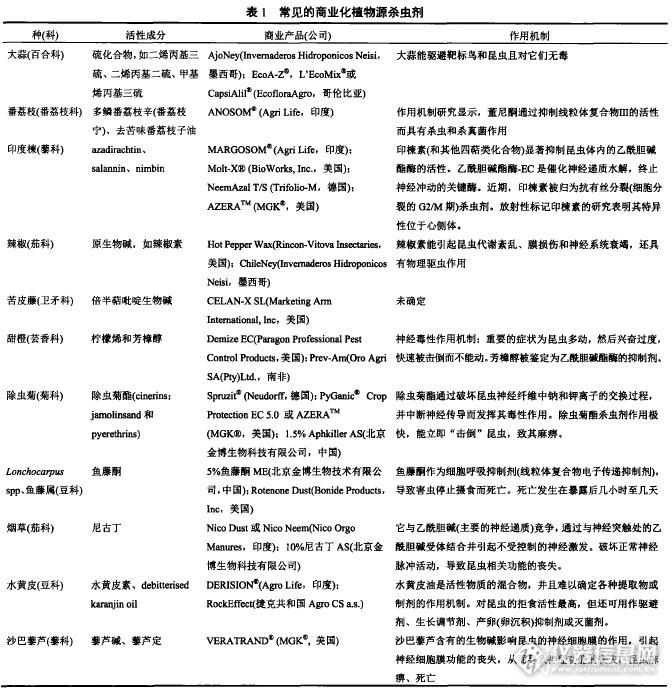
在欧洲用植物防治昆虫可追溯到3000多年前。起初,人们以一些芳香植物和其提取物或汤液防治害虫,特别是作为驱避剂对付肠虫或外寄生虫等讨厌的昆虫,也用植物来保护贮存的粮食或食物免受仓储害虫的危害。第一个商业化植物源杀虫剂出现在17世纪,当人们发现烟草叶中的尼古丁能杀死豆象虫后,开发上市。1850年左右,一种叫做鱼藤酮的植物源杀虫剂问世了,它是从鱼藤的根中提取获得。第二次世界大战之后,在欧洲廉价的合成杀虫剂(有机氯和有机磷酸盐)的出现(主要由部分化武制剂脱毒而成),使商业化植物源杀虫剂的进一步发展受到限制。http://ng1.17img.cn/bbsfiles/images/2017/03/201703261604_01_1623180_3.jpghttp://ng1.17img.cn/bbsfiles/images/2017/03/201703261604_02_1623180_3.jpg注:相关内容摘自《世界农药》
[size=15px][font=宋体]雷公藤([/font][font=&]Tripterygium wilfordii[/font][font=宋体])在我国多地均有分布,具有悠久的药用历史,广泛用于治疗类风湿关节炎[i][/i],在《本草纲目》等有记载。雷公藤红素([/font][font=&]Celastrol[/font][font=宋体])是从雷公藤植物中提取的一种生物活性分子,对于治疗自身免疫疾病和肿瘤等有显著作用,已被证明具有抗炎特性,然而,其作用机制尚未完全阐明。[/font][font=&][/font][/size] [size=15px][b][font=&]1[/font][font=宋体]、[/font][font=&]COMMD3/8 [/font][font=宋体]复合物缺乏会损害体液免疫[/font][font=&][/font][/b][/size] [size=15px][font=&][font=宋体]COMMD3[/font][/font][/size][font=宋体][back=url(&]和[/back][/font][font=&][font=宋体][back=url(&]COMMD8[/back][/font][/font][font=宋体][back=url(&]是[/back][/font][font=&][font=宋体][back=url(&]COMMD[/back][/font][/font][font=宋体][back=url(&]蛋白家族成员,在诱导体液免疫反应过程中形成了介导[/back][/font][font=&][font=宋体][back=url(&]B[/back][/font][/font][font=宋体][back=url(&]细胞迁移所必需的异二聚体,在调节免疫反应方面起着重要作用。作者构建了[/back][/font][font=&][font=宋体][back=url(&]Commd3[/back][/font][/font][font=宋体][back=url(&]基因敲除小鼠(在没有另一个蛋白的情况下,[/back][/font][font=&][font=宋体][back=url(&]COMMD3[/back][/font][/font][font=宋体][back=url(&]或[/back][/font][font=&][font=宋体][back=url(&]COMMD8[/back][/font][/font][font=宋体][back=url(&]蛋白会被蛋白酶体降解),发现[/back][/font][font=&][font=宋体][back=url(&]COMMD3[/back][/font][/font][font=宋体][back=url(&]缺失导致生发中心([/back][/font][font=&][font=宋体][back=url(&]germinal center[/back][/font][/font][font=宋体][back=url(&],[/back][/font][font=&][font=宋体][back=url(&]GC[/back][/font][/font][font=宋体][back=url(&])的[/back][/font][font=&][font=宋体][back=url(&]B[/back][/font][/font][font=宋体][back=url(&]细胞数量降低。[/back]为了分析[/font][font=&]COMMD3[/font][font=宋体]缺乏对免疫细胞的整体影响,作者通过质谱流式([/font][font=&]CyTOF[/font][font=宋体])和[/font][font=&]scRNA-seq[/font][font=宋体]均发现[/font][font=&]Commd3[/font][font=宋体]缺失降低[/font][font=&]GC B [/font][font=宋体]细胞的比例。这些发现表明[/font][font=&]B[/font][font=宋体]细胞受到[/font][font=&]COMMD3/8[/font][font=宋体]复合物缺乏的选择性影响[/font][font=宋体]。[/font][font=&][/font] [align=center] [/align] [size=15px][b][font=&]2[/font][font=宋体]、[/font][font=&]COMMD3/8 [/font][font=宋体]复合物缺乏可缓解关节炎[/font][font=&][/font][/b][/size] [size=15px][font=宋体]鉴于[/font][font=&]COMMD3/8[/font][font=宋体]复合物在体液免疫反应中的重要作用以及[/font][font=&]B[/font][font=宋体]细胞靶向疗法在类风湿关节炎([/font][font=&]RA[/font][font=宋体],[/font][font=&]Rheumatoid Arthritis[/font][font=宋体])中的已知疗效,作者利用胶原诱导性关节炎[i][/i]([/font][font=&]CIA[/font][font=宋体],一种[/font][font=&]RA[/font][font=宋体]小鼠模型)来测试[/font][font=&]COMMD3/8[/font][font=宋体]复合物在自身免疫性疾病中的作用。结果显示[/font][font=&]COMMD3/8[/font][font=宋体]复合物缺失还改善了[/font][font=&]CIA[/font][font=宋体],且在[/font][font=&]B[/font][font=宋体]细胞中表达的[/font][font=&]COMMD3/8[/font][font=宋体]复合物在[/font][font=&]CIA[/font][font=宋体]发病机制中起着重要作用。结果表明针对[/font][font=&]COMMD3/8[/font][font=宋体]复合物可能是治疗自身免疫性疾病的有前途的策略[/font][/size] [align=center] [/align] [size=15px][b][font=&]3[/font][font=宋体]、雷公藤红素靶向抑制[/font][font=&]COMMD3[/font][font=宋体]与[/font][font=&]COMMD8[/font][font=宋体]结合[/font][font=&][/font][/b][/size] [size=15px][font=宋体]接着,为了寻找[/font][font=&]COMMD3[/font][font=宋体]与[/font][font=&]COMMD8[/font][font=宋体]结合的有效抑制剂,[/font][/size][font=宋体][size=15px]研究人员通过天然产物化合物库[/size][/font][size=15px][font=宋体]([/font][font=&]2555[/font][font=宋体]种化合物)开展筛选,鉴定出雷公藤红素([/font][font=&]Celastrol[/font][font=宋体])是一种破坏[/font][font=&]COMMD3/8[/font][font=宋体]复合物的最有效的化合物,并通过生物发光共振能量转移([/font][font=&]BRET[/font][font=宋体])分析和[/font][font=&]CO-IP[/font][font=宋体]验证了雷公藤红素抑制[/font][font=&]COMMD3[/font][font=宋体]和[/font][font=&]COMMD8[/font][font=宋体]结合。此外,雷公藤红素处理加速了[/font][font=&]COMMD3[/font][font=宋体]和[/font][font=&]COMMD8[/font][font=宋体]的降解[/font][/size] [align=center] [/align] [size=15px][b][font=&]4[/font][font=宋体]、[/font][/b][/size][size=15px][b][font=宋体]雷公藤红素[/font][/b][/size][size=15px][b][font=宋体]与[/font][font=&] COMMD3 [/font][font=宋体]上的[/font][font=&] C170 [/font][font=宋体]共价结合[/font][font=&][/font][/b][/size][size=15px][font=宋体]雷公藤红素在[/font][font=&]C6[/font][font=宋体]处有一个亲电位点,半胱氨酸残基的亲核硫醇基团已证实可在此发生反应形成共价键。为了测试[/font][font=&] C6 [/font][font=宋体]原子是否参与了雷公藤红素与[/font][font=&] COMMD3/8 [/font][font=宋体]复合物的相互作用,作者获得了二氢雷公藤红素(雷公藤红素衍生物),其中[/font][font=&]C6[/font][font=宋体]位被还原并且失去了进行亲核加成的能力,发现二氢雷公藤红素不会破坏活细胞或纯化形式的[/font][font=&]COMMD3/8 [/font][font=宋体]复合物,表明雷公藤红素可能与[/font][font=&]COMMD3[/font][font=宋体]或[/font][font=&]COMMD8[/font][font=宋体]上的半胱氨酸残基形成共价键,从而解离[/font][font=&]COMMD3/8 [/font][font=宋体]复合物。[/font][font=&][/font][/size] [size=15px][font=宋体]在[/font][font=&]COMMD3[/font][font=宋体]和[/font][font=&]COMMD8[/font][font=宋体]上的半胱氨酸残基中,[/font][font=&]COMMD3[/font][font=宋体]上的[/font][font=&]C170[/font][font=宋体]是位于[/font][font=&]COMM[/font][font=宋体]结构域内的唯一半胱氨酸残基,两个[/font][font=&]COMMD[/font][font=宋体]蛋白通过该结构域相关联。作者,将[/font][font=&]COMMD3[/font][font=宋体]上[/font][font=&]170[/font][font=宋体]位的[/font][font=&]C[/font][font=宋体]突变为[/font][font=&]A[/font][font=宋体],发现含有[/font][font=&] COMMD3 C170A[/font][font=宋体]的[/font][font=&]COMMD3/8[/font][font=宋体]复合物不再被活细胞中的雷公藤红素解离,表明[/font][font=&]COMMD3[/font][font=宋体]上的[/font][font=&]C170[/font][font=宋体]可能作为雷公藤红素的结合位点。进一步分子对接发现与[/font][font=&]C170[/font][font=宋体]结合的雷公藤红素很可能被埋在[/font][font=&]COMMD3[/font][font=宋体]和[/font][font=&]COMMD8[/font][font=宋体]的[/font][font=&]COMM [/font][font=宋体]结构域之间的界面形成的疏水腔中,用雷公藤红素处理的纯化[/font][font=&] COMMD3/8 [/font][font=宋体]复合物的质谱鉴定发现[/font][font=&]C170[/font][font=宋体]是该结构域内雷公藤红素的唯一共价结合位点。总之,这些发现表明雷公藤红素可能通过与[/font][font=&] COMMD3 [/font][font=宋体]上的[/font][font=&]C170[/font][font=宋体]共价结合来解离[/font][font=&] COMMD3/8 [/font][font=宋体]复合物[/font][/size] [align=center] [/align] [size=15px][b][font=&]5[/font][font=宋体]、[/font][font=&][b][font=宋体]雷公藤红素[/font][/b][/font][font=宋体]重现[/font][font=&] COMMD3/8 [/font][font=宋体]复合物缺乏症[/font][font=&][/font][/b][/size] [size=15px][font=宋体]接下来,作者想知道雷公藤红素是否能重现[/font][font=&]COMMD3/8[/font][font=宋体]复合物缺乏所导致的功能性后果。结果显示,雷公藤红素抑制小鼠[/font][font=&] B [/font][font=宋体]细胞对[/font][font=&]CXCR4[/font][font=宋体]和[/font][font=&]EBI2[/font][font=宋体]刺激的趋化性迁移,这与[/font][font=&]COMMD3/8 [/font][font=宋体]复合物作为趋化因子受体信号传导的正调节剂的作用一致。此外,与[/font][font=&]COMMD3/8[/font][font=宋体]复合物缺乏的情况一样,雷公藤红素可阻止[/font][font=&]B[/font][font=宋体]细胞中[/font][font=&]GRK6[/font][font=宋体]介导的配体激活的[/font][font=&]CXCR4[/font][font=宋体]磷酸化。质谱流式([/font][font=&]CyTOF[/font][font=宋体])显示使用雷公藤红素治疗可选择性降低[/font][font=&]GC B[/font][font=宋体]细胞的比例,同时保持其增殖能力,这与在他莫昔芬[i][/i]诱导的[/font][font=&]Commd3[/font][font=宋体]缺失的小鼠中观察到的情况一样[/font][/size] [align=center] [/align] [size=15px][font=宋体]先前的研究表明,雷公藤红素治疗可抑制[/font][font=&]CIA[/font][font=宋体]的发展。作者证实在[/font][font=&]CIA[/font][font=宋体]发作时开始使用雷公藤红素治疗可阻止疾病进展。并重现[/font][font=&]COMMD3/8[/font][font=宋体]复合物缺乏对[/font][font=&]CIA[/font][font=宋体]中体液免疫反应的影响,降低血清中[/font][font=&] TIIC [/font][font=宋体]特异性抗体的滴度以及[/font][font=&]GC B[/font][font=宋体]细胞数量,而不会影响引流淋巴结中[/font][font=&]T H17[/font][font=宋体]和[/font][font=&]Treg[/font][font=宋体]细胞丰度,这些发现进一步表明雷公藤红素具有[/font][font=&]B[/font][font=宋体]细胞选择性作用。总体而言,雷公藤红素治疗表型模拟了[/font][font=&]COMMD3/8[/font][font=宋体]复合物的缺陷[/font][/size] [align=center] [/align] [size=15px][b][font=&]6[/font][font=宋体]、[/font][font=&]COMMD3[/font][font=宋体]的[/font][font=&]C170A[/font][font=宋体]突变消除了雷公藤红素的活性[/font][font=&][/font][/b][/size] [size=15px][font=宋体]接着,作者发现[/font][font=&]COMMD3[/font][font=宋体]的[/font][font=&]C170A[/font][font=宋体]突变使[/font][font=&]COMMD3/8[/font][font=宋体]复合物对雷公藤红素具有抗性。为了验证[/font][font=&]COMMD3/8[/font][font=宋体]复合物是雷公藤红素的真正靶标,作者生成了表达来自内源性[/font][font=&]Commd3[/font][font=宋体]基因座的[/font][font=&]COMMD3 C170A[/font][font=宋体]的小鼠,并测试雷公藤红素在这些小鼠中的作用是否被消除。结果显示,从[/font][font=&]COMMD3 C170A/C170A[/font][font=宋体]小鼠中分离的[/font][font=&]B[/font][font=宋体]细胞在[/font][font=&]CXCR4[/font][font=宋体]和[/font][font=&]EBI2[/font][font=宋体]介导的趋化反应以及[/font][font=&]GRK6[/font][font=宋体]介导的[/font][font=&]CXCR4[/font][font=宋体]磷酸化中表现出对雷公藤红素的完全抗性。此外,雷公藤红素治疗不会抑制突变小鼠的体液免疫反应。质谱流式([/font][font=&]CyTOF[/font][font=宋体])和[/font][font=&]scRNA-seq[/font][font=宋体]分析均表明,在免疫的突变小鼠中,雷公藤红素治疗不会显著影响任何可检测到的免疫细胞群。此外,[/font][font=&]COMMD3 C170A/C170A[/font][font=宋体]小鼠的[/font][font=&]CIA[/font][font=宋体]进展和[/font][font=&]TIIC[/font][font=宋体]诱导的体液免疫反应并未受到雷公藤红素治疗的抑制,这进一步证实了这些小鼠对雷公藤红素的无反应性。这些发现表明[/font][font=&]COMMD3/8[/font][font=宋体]复合物是雷公藤红素的主要分子靶点[/font][/size]
2月25日,美国底特律,通用汽车公司宣布腾中重工无法如约完成收购公司旗下悍马品牌,并将启动关闭悍马业务的有关程序。如此一来,折腾了大半年时间、在国内外闹得沸沸扬扬的悍马入川一事,可以说是正式以失败告终。在腾中重工收购悍马这一消息正甚嚣尘上的时候,笔者曾经发表过一篇题为《悍马入川渐生谣言:公关沟通三大要点》的评论文章,指出腾中方面在对此事件进行的公关沟通中存在着极大的问题,并由此导致了谣言满天飞的舆论危机。尽管这一事件由始至终均有炒作嫌疑,但从目前来看,腾中重工耗费许多精力与财力聘请专门的财务顾问、法律顾问和公关公司,最后仍是得不偿失。从公共关系的角度来看,作为一起受到国内外广泛关注的企业收购案,腾中买马的最终失败,与其在公关沟通方面所犯下的诸多错误有极大关系。在与政府、公众等多方利益相关者进行的公关沟通中,腾中方面一直采取的是遮遮掩掩的态度,即对作为重要沟通渠道的媒体奉行消极回避和刻意隐瞒的沟通策略。由此所导致的外界种种猜测,使得此次收购事件逐渐变味,让腾中重工陷入了十分严重的舆论困境。在长达大半年的买马计划失败之后,腾中重工和更多希望通过收购世界性品牌实现国际化发展的中国企业都应该吸取的教训是:要想完成一项收购计划并非有钱就能搞定,收购这一行为涉及到众多的利益相关群体,不是企业之间的私下交易,而是一种公众行为,企业必须要学会运用正确的公共关系手段与包括政府、客户、媒体等在内的多种利益相关者进行良好的沟通。首先,企业必须认识到主动沟通的重要性。对于企业收购而言,需要面对的外部沟通核心元素是媒体,因为媒体在很大程度上影响着消费者、供应商、经销商甚至是政府人士对于收购事件的了解和认识。企业在对待媒体时,应该坚持主动、及时、坦诚的原则,此前媒体报道中所出现的“媒体打探腾中重工背景一时无果”、“公关公司负责人员电话多数时候无人接听”、“记者所发采访邮件毫无回音”等情况,企业在进行公关沟通时需要引以为戒。其次,要针对性地解答媒体所关心的问题。通过研究过往众多企业-全球品牌网-收购案例,我们可以很清楚地看到,外界对于收购方的实力和整合能力的质疑,是企业在进行收购时常常会面临的一个问题,此次腾中买马遇到的最大问题也正是这个。媒体关心的问题其实无非是这样一些:比如收购方为什么要买?被收购方为什么要卖?双方的成交价格是多少?收购方的资金如何而来?被收购企业的未来是怎样?所有问题都需要提前拟定答案,把握沟通的主动权,而不是像腾中重工此前三缄其口,任由各种猜测议论甚嚣尘上。第三是要未雨绸缪防范危机的出现。在力求主动、及时、正面传递相关信息的同时,企业还需要随时关注媒体动向,启动实时信息监控机制,对一些可能出现的负面报道给予及时处理,将潜在的危机消除在萌芽状态。在腾中重工此前的公关沟通中,由于缺乏相应的准备而导致各种真假难辨的不利传言迅速发展,形成了潜在的舆论危机,实际上已经对企业及相关人士造成了相当大的伤害。
好了伤疤忘了疼,黄曲霉毒素已经离我们远去
[size=20px][color=#93c6bc][b]鉴别[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size][font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体](1)本品横切面:最外层为表皮,外被厚角质层,或为木栓层。皮层散有纤维和[color=var(--weui-LINK)]石细胞[i][/i][/color]。中柱鞘纤维束新月形,其内侧常为2~5列石细胞,并切向延伸与射线中的石细胞群连接成环。维管束外韧型。韧皮射线向外渐宽,可见锥形或分枝状石细胞;韧皮部细胞大多颓废,有的散有1~3个纤维。木质部导管单个散在或数个切向连接。髓细胞壁稍厚,纹孔明显。薄壁细胞含淀粉粒和草酸钙针晶。[/font] [font=宋体] [/font][font=宋体]粉末黄褐色或灰褐色。表皮细胞黄色或黄棕色,断面观类圆形或矩圆形,直径24~78[/font][font=宋体]μ[/font][font=宋体]m[/font][font=宋体],被有角质层。石细胞淡黄色或黄色,类方形、梭形、椭圆形或不规则形,壁较厚,孔沟明显。皮层纤维微黄色或黄色,直径27~70[/font][font=宋体]μ[/font][font=宋体]m[/font][font=宋体],壁极厚,胞腔狭窄。草酸钙针晶细小,存在于薄壁细胞中。[/font] [font=宋体](2)取本品粉末2g,加乙醇25ml,加热回流1小时,滤过,滤液蒸干,残渣加乙醇1ml使溶解,作为供试品溶液。另取[color=var(--weui-LINK)]青藤碱[i][/i][/color]对照品,加乙醇制成每1ml含1mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各5[/font][font=宋体]μ[/font][font=宋体]l[/font][font=宋体],分别点于同一硅胶G薄层板上,以甲苯-乙酸乙酯-甲醇-水(2: 4:2:1)10℃以下放置的上层溶液为展开剂,置浓氨试液预饱和20分钟的展开缸内展开,取出,晾干,依次喷以碘化铋钾试液和亚硝酸钠乙醇试液。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。[/font] [font=宋体][/font] [size=20px][color=#93c6bc][b]检查[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [b][font=宋体][/font] [font=宋体][/font] [font=宋体][/font] [font=宋体][/font][/b] [font=宋体][b]水分[/b] 不得过13.0%(通则0832第二法)。[/font] [b][font=宋体]总灰分[/font][/b][font=宋体] [/font][font=宋体]不得过6.0% (通则2302)。[/font] [b][font=宋体]【含量测定】[/font][/b][font=宋体] 照高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法(通则0512)测定。[/font] [b][font=宋体]色谱条件与系统适用性试验[/font][/b][font=宋体] [/font][font=宋体]以[color=var(--weui-LINK)]十八烷基硅烷键合硅胶[i][/i][/color]为填充剂;以甲醇-磷酸盐缓冲液(0.005mol/L磷酸氢二钠溶液,以0.005mol/L的磷酸二氢钠调节pH值至8.0,再以1%三乙胺调节pH值至9.0)(55:45)为[color=var(--weui-LINK)]流动相[i][/i][/color];检测波长为262nm。理论板数按青藤碱峰计算应不低于1500。[/font] [b][font=宋体]对照品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取青藤碱对照品适量,精密称定,加甲醇制成每1ml含0.5mg的溶液,即得。[/font] [b][font=宋体]供试品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取本品粉末(过三号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入70%乙醇20ml,密塞,称定重量,超声处理(功率250W,频率20kHz)20分钟,放冷,再称定重量,用70%乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。[/font] [b][font=宋体]测定法[/font][/b][font=宋体] [/font][font=宋体]分别精密吸取对照品溶液与供试品溶液各5[/font][font=宋体]μ[/font][font=宋体]l[/font][font=宋体],注入[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],测定,即得。[/font] [font=宋体]本品按干燥品计算,含青藤碱(C[sub]19[/sub]H[sub]23[/sub]NO[sub]4[/sub])不得少于0.50%。[/font] [font=宋体] [/font]
近年来,有机食品越来越流行,很多人到超市买东西也只挑有机。而商家也趁机大肆宣传有机食品不使用化学添加物、纯天然、更营养、更安全,不少消费者趋之若鹜。不过,有机食品是不是真的更好呢?它值得人们的爱吗? 有机食品在生产和加工中不使用人工合成的化学物质,如化肥、化学农药、化学生长调节剂。但它是否会因此更安全呢?未必。 首先,有机食品在生产过程中是允许使用农药的,包括一些植物源和动物源的杀菌剂、杀虫剂,如天然除虫菌素、鱼藤酮类等;还有一些矿物来源的杀真菌剂、杀虫剂等,如石灰水、波尔多液等。尽管跟人工合成农药来源不同,但它们同样具有毒性,也并非完全不残留,如果不清洗干净就吃下去,对身体同样可能有安全风险。 其次,有机食品会有天然毒素的风险。一些植物性食物,为了预防天敌,会产生天然的毒素;而且,有机食品也有被霉菌毒素污染的风险。 另外,有机化肥有重金属和病菌污染的风险。有机蔬果使用植物性堆肥或是动物排泄物。这就带来了一个问题:动物牲畜体内都有病菌和重金属,会随着粪便排出,用这些肥料种植出来的蔬果,就可能沾染上大肠杆菌、沙门氏菌等,可能引发食用者的感染甚至死亡。 所以,有机食品并不一定更安全,关键在种植是否规范。只要规范种植,常规食品和有机食品都是安全的。
参照标准GB/T20770-2008检测了啶虫脒、硫双威、甲硫威、鱼藤酮、毒死蜱,使用LC-MS/MS检测,在做单标的时候峰型都还不错,可是配置混标后毒死蜱的峰有些裂,不知怎么改善?

10,抽取5个版友);中奖名单:999youran(注册ID:999youran)捌道巴拉巴巴巴(注册ID:v3082413)千层峰(注册ID:jxyan)m3071659(注册ID:m3071659)牛一牛(注册ID:v2700892)http://ng1.17img.cn/bbsfiles/images/2016/11/201611091512_616152_0_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/11/201611091512_616153_0_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================雷公藤原料药中雷公藤内酯甲的测定方法:HPLC基质:药品应用编号:101595化合物:雷公藤内酯甲固定相:Diamonsil C18(2)色谱柱/前处理小柱:Diamonsil 5μm C18(2), 250 x 4.6mm样品前处理:1 样品准备/提取 (1) 精密称取0.2000 g 本品细粉,加入60 mL 乙酸乙酯,超声5 min,静置10 min; (2) 精密量取15 mL 上层清夜,作为上样液待净化。 2 SPE 柱净化——ProElut Al-N 3 g/20 mL (1)活 化: 用40 mL 乙酸乙酯活化,流出液弃去; (2)上 样: 将上样液加入柱中,收集流出液; (3)洗 脱: 用10 mL 乙酸乙酯洗脱,收集流出液,与(2)中流出液合并; (5)重新溶解: 在40 ℃下用减压蒸馏将流出液浓缩至近干,然后用流动相重新 定容至1 mL。色谱条件:色谱柱: Diamonsil C18(2) 250×4.6mm ID,5μm(Cat.#99603) 流 速: 1.0 mL/min 检测器: UV 210 nm 柱 温: 30 ℃ 进样量: 20 μL 流动相: 乙腈 : 水=8 : 2文章出处:迪马科技应用实验室关键字:雷公藤,原料药,雷公藤内酯甲,Diamonsil C18(2),99603摘要:适用于雷公藤原料药中雷公藤内酯甲的检测。谱图:http://www.dikma.com.cn/Public/Uploads/images/leigongteng1.PNGhttp://www.dikma.com.cn/Public/Uploads/images/leigongteng2.PNG图例:1 雷公藤内酯甲
【作者】 叶秀波; 谭淑娴;【机构】 广州市海珠区中医医院; 广州市海珠区妇幼保健院;【摘要】 目的建立藤己微乳喷雾剂中青藤碱的含量测定方法。方法采用高效液相色谱法,色谱条件以Diamonsil C18柱(250mm×4.6 mm,5μm)为色谱柱,流动相为甲醇-水(60∶40),加入0.3%的三乙胺,检测波长为265nm,流速1.0mL/min,柱温为室温。结果青藤碱在质量浓度为2.24~35.84μg/mL范围内线性关系良好(r=0.9998),平均回收率为100.10%,RSD=1.74%(n=6)。结论该方法其操作简便可行,准确度高,重现性好,可作为该制剂的质控方法。 更多还原【关键词】 高效液相色谱法; 藤己微乳; 喷雾剂; 青藤碱;
湖南商务及外经外贸部门官员和专家近日表示,7月29日起正式执行的欧盟新的食品中农药残留标准,将成为我国茶叶出口的新门槛。 相关专家指出,欧盟新施行的有关茶叶农药残留最高限量标准(MRL)有两个显著特点:一是茶叶的MRL标准出现9个变化。在新标准附录Ⅱ中,有关茶叶的5种农药MRL标准加严,分别为二溴乙烷、二嗪磷、滴丁酸、氟胺氰菊酯和敌敌畏。 二是新增一些与茶叶生产关系密切的MRL标准。新标准附录Ⅲ新增170种农药,大多是新农药。如,印楝素、鱼藤酮和除虫菊素属于植物性农药,以往一般不予控制,但此次也被列入名单;西玛津是一种三均氮类除草剂,在我国茶叶生产中应用很普遍。值得关注的是,新标准中硫元素和铜元素的MRL分别为5毫克/千克和40毫克/千克,将对我国广为应用的石硫合剂和铜杀菌剂产生一定影响。 有关人士认为,迅速对相关农药降解动态展开研究、分析茶叶中相关物质残留状况,严格按照国际标准选用农药,是当前我国茶叶跨越出口壁垒的有效措施。
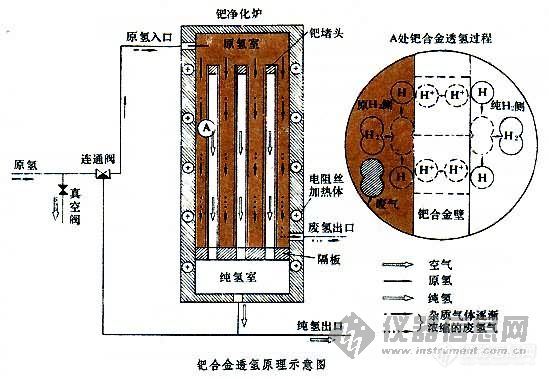
透氢材料 hydrogen penetrating materials 在一定的温度和氢压力差条件下,只让氢气透过的材料,主要用于制取高纯氢(又称超纯氢),纯度可达99.99999%,因而也称氢净化材料。透氢材料在半导体材料、原子能等工业部门及高纯金属、化学分析等科学研究部门中广泛应用。透氢材料中在工业上得到大量实际应用的是钯合金。英国人格雷厄姆(T.Graham)于1866年在实验时发现钯具有很高的吸氢能力。金属钯吸收的氢最多可达本身体积的2800倍,在温度为 300℃以上真空中,可把吸收的氢放出。钯及其合金的透氢功能就是由此特性决定的。纯钯由于吸氢后变形,因而未能得到应用。1956年美国人亨特(J.B.Hunter)制成钯银合金,解决了变形问题,于是出现了使用氢扩散透过钯合金制取超纯氢的技术。以后,日本人山本勇三和後藤良亮等人制成钯银金多元合金,用这种合金制造了超纯氢净化装置。英国、联邦德国、苏联和中国等国家也先后研制出钯合金材料并制造了超纯氢净化装置。 钯同银、金、钌、钇、钐、镝等制成的合金不仅提高了钯的强度,而且还能增强它的透氢性能。实用的钯合金透氢材料有:纯钯和钯银合金,多用作小型纯氢源的超纯氢发生器的阴极材料。钯银、钯银金,以及在钯银金中加入铂、钌、铑、铁、镍的合金,多用于高温热扩散的氢净化装置。含有稀土元素钇或钐等的二元合金,透氢能力和硬度均高,很有发展前途,但因抗氧化性和焊接性能差,尚未在工业中应用。另外,镍和15-24镍金合金虽可透过少量氢气,但因工作温度高(700℃以上),而且透氢速率低,在工业中也很少应用。 钯合金透氢原理和装置如图所示。制取纯氢的过程是:首先将净化装置系统抽空,清除管道系统和装置内部的气体杂质。同时加热钯净化炉,达到400~500℃后停止抽真空,关闭真空阀和连通阀,打开原氢阀门,引入的原氢(具有高的压力)透过钯合金壁进入内表面(即纯氢侧),通过纯氢流量计流出。其他气体(氧、氮等)仍留在原氢侧。原氢流从钯净化炉上部往下流动,杂质气体不断富集,从废氢出口排出。氢透过钯合金时的透氢速率与原氢侧和纯氢侧之间的压力差的平方根成正比,与加热温度呈指数函数关系,与钯合金的厚度成反比。为延长钯合金的使用寿命,加热温度一般在400~450℃之间,不得超过500℃。氢气压力差不应过高,常为6~10kgf/cm2。被净化的原氢中含有一氧化碳和不饱和的烃类,容易使钯合金中毒。因这些物质中的碳渗入钯合金后,在低温时以石墨状态析出,会使钯合金变脆,降低它的透气性能。硫和卤族元素也是有害物质。加热温度如低于310℃,钯合金将吸收大量的氢,发生部分α─→β相转变(若纯钯则全部转变为β相),使合金体积增大11%左右,容易使钯合金产生裂纹而破裂,所以低温时应避免氢与钯合金接触。 [img]http://ng1.17img.cn/bbsfiles/images/2006/11/200611272056_33837_1634962_3.jpg[/img]