[align=center][size=24px][b]松脂酸(松香酸)测定方法[/b][/size][/align] 松香酸用于发酵工业,并且可用作肥皂和造纸工业的填料。松香酸为三环二萜类化合物。在含水乙醇中得单斜片状结晶。熔点172~175℃,旋光度-102°(无水乙醇)。不溶于水,溶于乙醇、苯、氯仿、乙醚、丙酮、二硫化碳以及稀氢氧化钠水溶液。为天然松香树脂的主要成分。本测定方法是建立松香中松脂酸测定,液体原药松脂酸铜中松脂酸测定;文献报道,[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法测定松脂酸铜需要加入盐酸,[font=宋体]将松脂酸铜衍生转化为松脂酸,图[/font][font='Times New Roman','serif']1[/font][font=宋体]列出了其可能的转化途径,确定松脂酸铜实际测定对象为松脂酸。厂家送过来的原药是盐酸处理过的所以我们直接检测就行。[/font][align=center][img=,589,168]https://ng1.17img.cn/bbsfiles/images/2023/08/202308150859397658_4592_3963412_3.jpg!w589x168.jpg[/img][/align][align=center][b][font=宋体]图[/font][font='Times New Roman','serif']1 [/font][/b][font=宋体][b]松脂酸铜转化为松脂酸[/b][/font][/align][align=left][b]实验方法[/b][/align][align=left][/align][align=left][font='Times New Roman','serif']1[/font][font=宋体]试剂:乙腈(色谱级),磷酸(分析纯);盐酸分析纯[/font][font=&] [font='Times New Roman','serif']2[/font][font=宋体][url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]条件:[/font][font='Times New Roman','serif']LC-20AT [/font][font=宋体]波长:[/font][font='Times New Roman','serif']245nm [/font][font=宋体];进样量:[/font][font='Times New Roman','serif']5μL[/font][font=宋体]色谱柱型号:[/font][font='Times New Roman','serif']Agilent Eclipse XDB-C18(2.1 mm×100mm, 2.7 μm), [/font][font=宋体]柱温:[/font][font='Times New Roman','serif']30.5 [/font][font=宋体]℃,流动相条件如表[/font][font='Times New Roman','serif']1[/font][font=宋体]:[/font][/font][/align][align=center][font=&][font=宋体]表1 流动相洗脱程序[/font][/font][/align][align=center][font=&][font=宋体][img=,559,298]https://ng1.17img.cn/bbsfiles/images/2023/08/202308151105132742_2164_3963412_3.jpg!w559x298.jpg[/img][/font][/font][/align][align=left][font='Times New Roman','serif']3 [/font][font=宋体]标准品配制:称取一定量的松脂酸,用乙腈[/font][font='Times New Roman','serif']:0.1%[/font][font=宋体]磷酸([/font][font='Times New Roman','serif']V/V=70:30[/font][font=宋体])溶解,定容,得到浓度为[/font][font='Times New Roman','serif']200 μg/mL[/font][font=宋体],待测。[/font][/align][font=宋体][/font][align=center][img=,534,242]https://ng1.17img.cn/bbsfiles/images/2023/08/202308150902130177_1955_3963412_3.jpg!w534x242.jpg[/img]图2 标准品色谱图[/align][align=left][font='Times New Roman','serif']4[/font][font=宋体]样品制备:[/font][/align][align=left][font='Times New Roman','serif']4.1[/font][font=宋体]松香用研钵研碎,称取一定量的样品,用乙腈[/font][font='Times New Roman','serif']:0.1%[/font][font=宋体]磷酸([/font][font='Times New Roman','serif']V/V=70:30[/font][font=宋体])超声溶解,定容至[/font][font='Times New Roman','serif']50 mL[/font][font=宋体],然后过滤待测。[/font][/align][align=center][img=,532,236]https://ng1.17img.cn/bbsfiles/images/2023/08/202308150904090783_7851_3963412_3.jpg!w532x236.jpg[/img][/align][align=center]图3 松香样1色谱图[/align][align=center][/align][align=center][img=,498,227]https://ng1.17img.cn/bbsfiles/images/2023/08/202308150904412965_7172_3963412_3.jpg!w498x227.jpg[/img][/align][align=center]图4 松香样2色谱图[/align][align=left]4.2 称取一定量的液体原药,用乙腈:0.1%磷酸(V/V=70:30)溶解,定容至50mL, 过0.45μm滤膜,待测。[/align][align=center][img=,560,254]https://ng1.17img.cn/bbsfiles/images/2023/08/202308150908303829_927_3963412_3.jpg!w560x254.jpg[/img]图5 原药1色谱图[/align][align=center][img=,513,235]https://ng1.17img.cn/bbsfiles/images/2023/08/202308150908401428_7495_3963412_3.jpg!w513x235.jpg[/img]图6 原药2色谱图[img=,690,516]https://ng1.17img.cn/bbsfiles/images/2023/08/202308150914267479_9450_3963412_3.jpg!w690x516.jpg[/img]图7 松香(1和2)样品图[/align][align=left]结论:从松香质地能看出来松香2 质地要优于松香1,松香1中松香酸含量44.3%,松香2中松香酸含量88.5%,原药1含量12.5%,原药2中含量42.1%。后来联系客户说松香1是湿地松得到的,松香2是马尾松得到的。不同植物得到的松香差异比较明显。[/align][font='Times New Roman','serif'][/font][align=left][font=宋体][/font][/align][align=center][/align][align=left][/align][align=left][/align]
求:特戊酸、特戊酸氯甲酯、特戊酰氯的分析方法

[b][color=#006580]1 [/color][font=宋体][color=#006580]前言[/color][/font][/b][align=left][font=宋体]人们通常将从植物里制取的油称作植物油,植物油的最主要来源是一年生植物,例如大豆、玉米、花生等,这些油料生长在温带地区。也有来源于多年生的油料树种,例如橄榄、椰子等,这些油料生长在热带地区。植物油的种类繁多,习惯上是按照不同植物油料种类进行的分类。近年来,由于发展中国家的收入和人口增长及亚洲和其他地区快速扩张的食品加工业的刺激,使全球植物油消费和贸易的增长远远超过大多数其他农产品。在过去[/font]10[font=宋体]年中,世界范围的植物油消费以平均每年[/font]4.2%[font=宋体]的速度增长[/font][sup][1][/sup][font=宋体]。[/font][/align][font=宋体]食用油脂中最主要的成分是脂肪酸,构成脂肪酸的有饱和、不饱和及特殊脂肪酸,还有几何及位置异构体等,其生理作用按种类不同而异[/font][sup][2][/sup][font=宋体]。因此,油脂的营养价值主要取决于它的脂肪酸组成及其配比,脂肪酸决定油脂的品质,必需的脂肪酸对人类的健康作用日趋重要,油脂的成分分析也越来越得到人们的重视[/font][sup][3-5][/sup][font=宋体]。必需脂肪酸是组织细胞的组成成分,在体内参与磷脂的合成,并以磷脂的形式存在于线粒体和细胞膜中,必需脂肪酸和胆固醇的关系极为密切,只有当胆固醇与必需的脂肪酸结合时,才能在体内转运正常代谢,起到预防动脉硬化、高胆固醇血症和高血脂症等。人们生活中离不开食用油,食用油品质的好坏,直接影响到人们的身体健康。由于食用油的植物来源不同,所含脂肪酸的种类及含量也各不相同。曾有人认为:只有富含多不饱和脂肪酸的植物油对人体有益,植物油中主要含有油酸和亚油酸,这是人体所必需的不饱和脂肪酸。但研究表明,人体对油脂中饱和类、单烯类、多烯类脂肪酸需保持合理的比例,单一的天然动、植物油都不可能满足人体需要[/font][sup][6-7][/sup][font=宋体]。[/font][font=宋体]对食用油的分析与研究通过测定主要物理、化学参数包括折光率、熔点、碘值、皂化值和非皂化物含量报道较多[/font][sup][8-9][/sup][font=宋体],本文采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法分析食用植物油中的脂肪酸的组成及相对含量,为合理利用食用油提供科学依据。[/font][b][color=#006580]2 [/color][font=宋体][color=#006580]实验部分:[/color][/font]2.1 [font=宋体]仪器与试剂[/font][/b][align=center][img=,690,469]https://ng1.17img.cn/bbsfiles/images/2020/07/202007241336393030_6748_3299836_3.jpg!w690x469.jpg[/img][/align]SP-3530[font=宋体]型[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url](北分瑞利),配[/font]FID[font=宋体]检测器,填充柱注样器,填充柱[/font]20%DEGS[font=宋体]([/font]φ3*2m[font=宋体]),[/font]BF-3000[font=宋体]色谱工作站(北分瑞利),水浴锅。[/font][font=宋体]氢氧化钾,三氟化硼,甲醇,正己烷,氯化钠,无水硫酸钠,均为分析纯。[/font][font=宋体]氢氧化钾[/font]-[font=宋体]甲醇溶液:约[/font]0.5mol/L[font=宋体]三氟化硼[/font]-[font=宋体]甲醇溶液:质量分数[/font]12%-15%[b]2.2 [font=宋体]甲酯化反应[/font][/b][font=宋体]用移液管吸取油样[/font]0.35mL[font=宋体],置于[/font]50mL[font=宋体]圆底烧瓶中,加入[/font]6mL[font=宋体]氢氧化钾[/font]-[font=宋体]甲醇溶液([/font]0.5mol/L[font=宋体]),然后将冷凝管固定于烧瓶上,水浴锅加热到[/font]60[font=宋体]℃[/font][font=宋体]左右时,将烧瓶置于水浴中,继续加热回流约[/font]30min[font=宋体]后,油滴消失,用移液管从冷凝管顶部加入[/font]6mL[font=宋体]三氟化硼[/font]-[font=宋体]甲醇溶液于沸腾溶液内,继续煮沸[/font]2min[font=宋体],经冷凝管顶部加入[/font]4mL[font=宋体]正己烷,继续煮沸[/font]1min[font=宋体],停止加热,冷却至室温后取下冷凝管,加入少量饱和氯化钠溶液并清摇烧瓶数次,继续加入氯化钠溶液至烧瓶顶部,静置分层后吸取上层溶液于小试管中,经无水硫酸钠去除痕量水,置于[/font]4[font=宋体]℃[/font][font=宋体]冰箱冷藏待分析。[/font][b]2.3 [font=宋体]色谱条件[/font][/b][font=宋体]柱温:[/font]200[font=宋体]℃[/font][font=宋体],[/font]FID[font=宋体]检测器温度:[/font]270[font=宋体]℃[/font][font=宋体],进样口温度:[/font]250[font=宋体]℃[/font][font=宋体]载气流速:[/font]30mL/min[font=宋体],进样量:[/font]1uL[font=宋体]。[/font][b]2.4 [font=宋体]色谱条件的选择[/font][/b][font=宋体]在色谱柱和检测器选定的情况下,柱温和载气流速对色谱分离和测定结果影响最大,因此,本方法对此两个条件进行了选择。[/font][b]2.4.1[font=宋体]温度的选择[/font][/b][font=宋体]温度的选择主要是柱温的选择,其它如载气流速、进样量大小等条件固定不变。只改变柱温的实验结果见表[/font]1[font=宋体]。[/font][align=left][font=宋体]表[/font]1 [font=宋体] 改变柱温的色谱分离结[/font][/align][table][tr][td] [b][font=宋体]柱 温[/font][/b] [/td][td] [b][font=宋体]亚油酸含量[/font]/%[/b] [/td][td] [b][font=宋体]分离度[/font][/b] [/td][td] [b][font=宋体]理论塔板数[/font][/b] [/td][/tr][tr][td] 190 [font=宋体]℃[/font] [/td][td] 32. 98 [/td][td] 1.77 [/td][td] 217 [/td][/tr][tr][td] 200 [font=宋体]℃[/font] [/td][td] 33. 57 [/td][td] 1. 78 [/td][td] 224 [/td][/tr][tr][td] 210 [font=宋体]℃[/font] [/td][td] 33. 59 [/td][td] 1. 76 [/td][td] 218 [/td][/tr][/table][font=宋体]从表[/font]1[font=宋体]中看出,选择不同的柱温所得结果有一定的差别,同时可以看出[/font]200[font=宋体]℃[/font][font=宋体]时,分离度与理论塔板数均达到最大。因此我们选择以[/font]200[font=宋体]℃[/font][font=宋体]作为本实验的柱温。[/font][b]2.4.2[font=宋体]载气流速的选择[/font][/b][font=宋体]固定其他条件,柱温选择[/font]200[font=宋体]℃[/font][font=宋体],只改变载气([/font]N[sub]2[/sub][font=宋体])的流速,得到实验结果如表[/font]2[font=宋体]。[/font] [table][tr][td] [b][font=宋体]载气流速[/font][/b] [/td][td] [b][font=宋体]亚油酸含量[/font]/%[/b] [/td][td] [b][font=宋体]分离度[/font][/b] [/td][td] [b][font=宋体]理论塔板数[/font][/b] [/td][/tr][tr][td] 25 mL/min [/td][td] 33. 52 [/td][td] 1. 78 [/td][td] 221 [/td][/tr][tr][td] 30 mL/min [/td][td] 33.57 [/td][td] 1. 78 [/td][td] 223 [/td][/tr][tr][td] 35 mL/min [/td][td] 33. 59 [/td][td] 1. 77 [/td][td] 221 [/td][/tr][/table][align=left][font=宋体]表[/font]2 [font=宋体]改变载气流速的色谱分离结果[/font][/align][font=宋体]从表[/font]2[font=宋体]中可看出[/font],[font=宋体]选择不同的载气流速所得实验结果也有所不同,同时可看出当载气流速为[/font]30mL/min[font=宋体]时,理论塔板数与分离度均达最大。因此,我们选择载气流速为[/font]30mL/min[font=宋体]。[/font][b]2.5 [font=宋体]数据处理[/font][/b][font=宋体]应用峰面积归一化法计算植物油中脂肪酸成分的相对百分含量[/font][font=宋体][/font][font=宋体][b][color=#006580]3 [/color][font=宋体][color=#006580]结果与讨论[/color][/font]3.1 [font=宋体]分离与定性[/font][/b][font=宋体]使用填充柱[/font]20%DEGS[font=宋体]([/font]φ3*2m[font=宋体])做分析柱,在实验过程中,除了亚麻酸与花生酸两个组分的分离情况不理想外,其他组分的分离度均合格,由于亚麻酸与花生酸不是我们要求的鉴定植物油品质的重要组分,所以忽略它们的分离效果,我们认为选用的填充柱分离效果可以满足要求。我们根据脂肪酸甲酯的出峰规律确定每种脂肪酸的相对保留时间,并根据保留时间对植物油各组分定性。各脂肪酸甲酯的保留时间见表[/font]3[font=宋体]和图[/font]1[font=宋体]。[/font][/font][align=left][font=宋体]表[/font]3 [font=宋体]各脂肪酸甲酯的保留时间[/font][/align][table][tr][td] [b][font=宋体]脂肪酸甲酯[/font][/b] [/td][td] [b][font=宋体]保留时间[/font]/min[/b] [/td][td] [b][font=宋体]脂肪酸甲酯[/font][/b] [/td][td] [b][font=宋体]保留时间[/font]/min[/b] [/td][/tr][tr][td] [font=宋体]豆蔻酸[/font] [/td][td] 2.248 [/td][td] [font=宋体]花生酸[/font] [/td][td] 13.175 [/td][/tr][tr][td] [font=宋体]棕榈酸[/font] [/td][td] 3.787 [/td][td] [font=宋体]花生烯酸[/font] [/td][td] 16.293 [/td][/tr][tr][td] [font=宋体]硬脂酸[/font] [/td][td] 6.582 [/td][td] [font=宋体]山嵛酸[/font] [/td][td] 20.785 [/td][/tr][tr][td] [font=宋体]油酸[/font] [/td][td] 7.745 [/td][td] [font=宋体]芥酸[/font] [/td][td] 23.911 [/td][/tr][tr][td] [font=宋体]亚油酸[/font] [/td][td] 9.518 [/td][td] [font=宋体]花生四烯酸[/font] [/td][td] 37.143 [/td][/tr][tr][td] [font=宋体]亚麻酸[/font] [/td][td] 12.502 [/td][td] [/td][td] [/td][/tr][/table][align=center][font=宋体][img=,690,369]https://ng1.17img.cn/bbsfiles/images/2020/07/202007241339021229_7868_3299836_3.jpg!w690x369.jpg[/img][/font][/align][align=center][font=宋体]图[/font]1 [font=宋体]菜籽油中脂肪酸的色谱图[/font][/align][b]3.2 [font=宋体]样品的检测与重现性[/font][/b][font=宋体]我们对四种油样进行了分析之后发现,菜籽油中含有[/font]15%[font=宋体]左右的芥酸,这可以作为区别于其他植物油的特征酸。分析所得各种油样中脂肪酸含量如表[/font]4[font=宋体]。[/font][align=left][font=宋体]表[/font]4 [font=宋体]油样中脂肪酸含量表[/font]/%[/align][table=558][tr][td] [/td][td] [b][font=宋体]花生油[/font][/b] [/td][td] [b][font=宋体]芝麻油[/font][/b] [/td][td] [b][font=宋体]米糠油[/font][/b] [/td][td] [b][font=宋体]菜籽油[/font][/b] [/td][/tr][tr][td] [font=宋体]豆蔻酸[/font] [/td][td] 0.01 [/td][td] 0.03 [/td][td] 0.35 [/td][td] 0.09 [/td][/tr][tr][td] [font=宋体]棕榈酸[/font] [/td][td] 12.29 [/td][td] 9.53 [/td][td] 20.46 [/td][td] 4.75 [/td][/tr][tr][td] [font=宋体]硬脂酸[/font] [/td][td] 3.01 [/td][td] 4.21 [/td][td] 1.28 [/td][td] 1.75 [/td][/tr][tr][td] [font=宋体]油酸[/font] [/td][td] 41.75 [/td][td] 39.58 [/td][td] 42.59 [/td][td] 37.58 [/td][/tr][tr][td] [font=宋体]亚油酸[/font] [/td][td] 37.83 [/td][td] 45.69 [/td][td] 33.57 [/td][td] 34.24 [/td][/tr][tr][td] [font=宋体]亚麻酸[/font] [/td][td] 0.97 [/td][td] 0.18 [/td][td] 0.16 [/td][td] 0.93 [/td][/tr][tr][td] [font=宋体]花生酸[/font] [/td][td] 0.64 [/td][td] 0.38 [/td][td] 0.81 [/td][td] 0.90 [/td][/tr][tr][td] [font=宋体]花生烯酸[/font] [/td][td] 0.43 [/td][td] 0.02 [/td][td] 0.05 [/td][td] 3.92 [/td][/tr][tr][td] [font=宋体]山嵛酸[/font] [/td][td] 3.07 [/td][td] 0.27 [/td][td] 0.22 [/td][td] 0.29 [/td][/tr][tr][td] [font=宋体]芥酸[/font] [/td][td] — [/td][td] — [/td][td] — [/td][td] 15.28 [/td][/tr][tr][td] [font=宋体]花生四烯酸[/font] [/td][td] — [/td][td] 0.11 [/td][td] 0.51 [/td][td] 0.16 [/td][/tr][/table][font=宋体]在分析植物油中脂肪酸含量时,我们对样品进行了[/font]5[font=宋体]次重复性实验,结果显示每种物质保留时间稳定;同时从精密度试验[/font]5[font=宋体]个平行样品检测结果来看,实验重现性很好,相对标准偏差[/font]RSD[font=宋体]都小于[/font]3%[font=宋体],数据稳定。[/font]5[font=宋体]次重复性检测结果如表[/font]5[font=宋体]。样品结果以米糠油为例,以峰面积计算。[/font][font=宋体]表[/font]5[font=宋体]样品重复性检测结果(峰面积)[/font] [table=580][tr][td] [/td][td] [b][font=宋体]第一次[/font][/b] [/td][td] [b][font=宋体]第二次[/font][/b] [/td][td] [b][font=宋体]第三次[/font][/b] [/td][td] [b][font=宋体]第四次[/font][/b] [/td][td] [b][font=宋体]第五次[/font][/b] [/td][td] [b]RSD[/b] [/td][/tr][tr][td] [font=宋体]豆蔻酸[/font] [/td][td] 21133 [/td][td] 20873 [/td][td] 21585 [/td][td] 20917 [/td][td] 20675 [/td][td] 1.64% [/td][/tr][tr][td] [font=宋体]棕榈酸[/font] [/td][td] 1237737 [/td][td] 1204285 [/td][td] 1256353 [/td][td] 1290316 [/td][td] 1274722 [/td][td] 2.67% [/td][/tr][tr][td] [font=宋体]硬脂酸[/font] [/td][td] 77532 [/td][td] 76358 [/td][td] 80254 [/td][td] 79324 [/td][td] 77537 [/td][td] 1.99% [/td][/tr][tr][td] [font=宋体]油酸[/font] [/td][td] 2575974 [/td][td] 2531684 [/td][td] 2497351 [/td][td] 2603186 [/td][td] 2583451 [/td][td] 1.68% [/td][/tr][tr][td] [font=宋体]亚油酸[/font] [/td][td] 2030792 [/td][td] 2104584 [/td][td] 2086473 [/td][td] 1984532 [/td][td] 2005875 [/td][td] 2.52% [/td][/tr][tr][td] [font=宋体]亚麻酸[/font] [/td][td] 9519 [/td][td] 9437 [/td][td] 9658 [/td][td] 9932 [/td][td] 9421 [/td][td] 2.20% [/td][/tr][tr][td] [font=宋体]花生酸[/font] [/td][td] 49264 [/td][td] 47358 [/td][td] 48506 [/td][td] 46872 [/td][td] 47691 [/td][td] 1.98% [/td][/tr][tr][td] [font=宋体]花生烯酸[/font] [/td][td] 3100 [/td][td] 3058 [/td][td] 3134 [/td][td] 3194 [/td][td] 3257 [/td][td] 2.46% [/td][/tr][tr][td] [font=宋体]山嵛酸[/font] [/td][td] 13568 [/td][td] 12985 [/td][td] 13790 [/td][td] 13652 [/td][td] 13831 [/td][td] 2.52% [/td][/tr][tr][td] [font=宋体]花生四烯酸[/font] [/td][td] 30031 [/td][td] 31205 [/td][td] 30810 [/td][td] 29403 [/td][td] 31328 [/td][td] 2.68% [/td][/tr][/table][b][color=#006580]4 [/color][font=宋体][color=#006580]结论[/color][/font][/b] [font=宋体]用本文提出的方法制备脂肪酸甲酯衍生物,衍生化反应速度较快,酯化效率高,方法简便,适于处理大批量使用植物油样品,实验得到[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]图分离效果符合要求,易于定性,面积归一法定量方法可靠,对各种食用植物油检测有重要意义。常见的植物油脂肪酸组成和营养特色各不相同,花生油、芝麻油易于吸收,米糠油是一种新兴油种,营养价值较高,菜籽油虽然价格比较低廉,但含有芥酸等对身体有害的物质。[/font][b][font=宋体][color=#006580]参考文献:[/color][/font][/b][1][font=宋体]回瑞华,侯冬岩,李铁纯,李学成,刘晓媛,雷磊,国艳秋[/font].[font=宋体]食用植物油中脂肪酸的分析[/font].[font=宋体]鞍山师范学院学报,[/font]2006-12[font=宋体],[/font]8[font=宋体]([/font]6[font=宋体]):[/font]19-21.[2][font=宋体]李永和[/font].[font=宋体]对食用油脂营养价值的新认识[/font][J].[font=宋体]中国油脂,[/font]1997[font=宋体],[/font]22[font=宋体]([/font]4[font=宋体]):[/font]13-15.[3][font=宋体]景淑华,付渝滨[/font].[font=宋体]羟肪酸快速测定食用油主要营养必需脂肪酸[/font][J]. [font=宋体]色谱,[/font]1998[font=宋体],[/font]16[font=宋体]([/font]1[font=宋体]):[/font]53-55.[4] [font=宋体]陈希中[/font].[font=宋体]食品防腐剂山梨酸和苯甲酸的[/font]GC[font=宋体]内标法测定[/font][J].[font=宋体]食品发酵工业[/font],1997[font=宋体],[/font]23[font=宋体]([/font]3[font=宋体]):[/font]39-41.[5][font=宋体]李相仁[/font],[font=宋体]胡永明[/font].[font=宋体]海蒿子中脂肪酸组成的研究[/font][J].[font=宋体]青岛师范学院学报,[/font]1998[font=宋体],[/font]15[font=宋体]([/font]2[font=宋体]):[/font]43-44.[6][font=宋体]陈智斌,陈媛,张立伟[/font].[font=宋体]合理选择食用油对预防疾病的作用[/font][J].[font=宋体]粮油食品,[/font]2001[font=宋体],([/font]2[font=宋体]):[/font]56-58.[7][font=宋体]金霞,余纲哲[/font].[font=宋体]食用油脂与人体健康[/font][J].[font=宋体]生物学通报,[/font]2000[font=宋体],[/font]35[font=宋体]([/font]2[font=宋体]):[/font]13-15.[8][font=宋体]中华人民共和国国家标准,食品卫生检验方法理化部分[/font][M].[font=宋体]北京[/font].[font=宋体]中国标准出版社,[/font]1997[9][font=宋体]李文智[/font].[font=宋体]食用油酸价和过氧化值快速检测试纸法的评价[/font][J].[font=宋体]粮油食品科技,[/font]2002[font=宋体],[/font]10[font=宋体]([/font]5[font=宋体]):[/font]40-41.[font=宋体][/font]
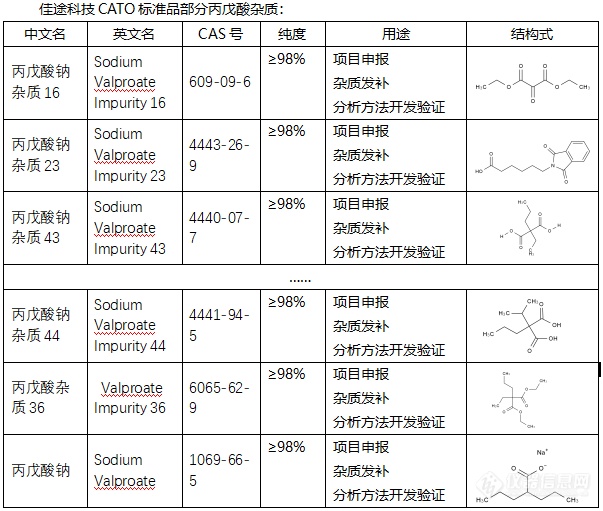
[font=宋体]◇关于[/font][font=微软雅黑]丙戊酸杂质[/font][font=微软雅黑]丙戊酸杂质[/font][font=微软雅黑]是[/font][font=Arial][color=#1f1f1f][font=宋体]是一种镇痉药物[/font][/color][/font][font=宋体][color=#1f1f1f],[/color][/font][font=Arial][color=#1f1f1f][font=宋体]丙戊酸钠[/font][/color][/font][font=宋体][color=#1f1f1f]的机制原理是[/color][/font][font=Arial][color=#1f1f1f][font=宋体]通过增加[/font][/color][/font][font=宋体][color=#1f1f1f]抑制[/color][/font][font=Arial][color=#1f1f1f][font=宋体]中枢神经系统的[/font][/color][/font][font=宋体][color=#1f1f1f]作用[/color][/font][font=Arial][color=#1f1f1f][font=宋体],[/font][/color][/font][font=宋体][color=#1f1f1f]就可以降低[/color][/font][font=Arial][color=#1f1f1f][font=宋体]神经细胞的兴奋性,[/font][/color][/font][font=宋体][color=#1f1f1f]随之降低[/color][/font][font=Arial][color=#1f1f1f][font=宋体]突触传递和脑电活动[/font][/color][/font][font=宋体][color=#1f1f1f]。[/color][/font][font=Arial][color=#1f1f1f][font=宋体]丙戊酸钠主要[/font][/color][/font][font=宋体][color=#1f1f1f]有以下五个好处:[/color][/font][font=宋体][color=#333333]一[/color][/font][font=Arial][color=#333333][font=宋体]、[/font][/color][/font][font=Arial][color=#1f1f1f][font=宋体]有效控制癫痫的症状[/font][/color][/font][font=宋体][color=#1f1f1f];[/color][/font][font=宋体][color=#1f1f1f]二[/color][/font][font=Arial][color=#333333][font=宋体]、[/font][/color][/font][font=Arial][color=#1f1f1f][font=宋体]缓解肌肉的痉挛和僵直,改善患者的运动功能[/font][/color][/font][font=宋体][color=#1f1f1f]。[/color][/font][font=宋体][color=#1f1f1f]三[/color][/font][font=Arial][color=#333333][font=宋体]、[/font][/color][/font][font=Arial][color=#1f1f1f][font=宋体]可以稳定躁狂患者的情绪[/font][/color][/font][font=宋体][color=#1f1f1f];[/color][/font][font=宋体][color=#1f1f1f]四[/color][/font][font=Arial][color=#333333][font=宋体]、[/font][/color][/font][font=Arial][color=#1f1f1f][font=宋体]用于治疗痉挛型疼痛[/font][/color][/font][font=宋体][color=#1f1f1f];[/color][/font][font=宋体][color=#1f1f1f]五[/color][/font][font=Arial][color=#333333][font=宋体]、[/font][/color][/font][font=Arial][color=#1f1f1f][font=宋体]可以减轻炎症反应,缓解疼痛和肿胀等症状[/font][/color][/font][font=宋体][color=#1f1f1f]。[/color][/font][font=宋体][font=Calibri]CATO[/font][font=宋体]标准品提供的[/font][/font][font=微软雅黑]丙戊酸杂质[/font][font=微软雅黑],[/font][font=Arial][color=#1f1f1f][font=宋体]丙戊酸钠的应用[/font][/color][/font][font=宋体][color=#1f1f1f]十分广泛,但是[/color][/font][font=微软雅黑]在临床上[/font][font=Arial][color=#1f1f1f][font=宋体]治疗癫痫[/font][/color][/font][font=宋体][color=#1f1f1f]有显著的效果。[/color][/font][img=,603,511]https://ng1.17img.cn/bbsfiles/images/2024/02/202402042151222095_2072_6381607_3.png!w603x511.jpg[/img]
想要分别测定一下月桂酸甲酯、肉豆蔻酸甲酯、棕榈酸甲酯和硬脂酸甲酯的含量,想内标法定量,请问选择哪种内标物比较合适呢?现在的试剂98%纯以上,可不可以互相作为内标还是另外选择一种呢?第一次做[url=https://insevent.instrument.com.cn/t/Mp]气相[/url],还请知情人士相助。
如题,本人想用GC-MS测植物的代谢物,加入脂肪酸甲酯系列混合物辅助定性,请问用饱和的和不饱和的脂肪酸甲酯有区别吗?还是都可以呢?我对利用保留指数定性不是很明白,或者有谁能给详细解释一下具体如何算嘛。谢谢!
[color=#444444]我用辛酸甲酯methyloctanoate (C9H18O2) 做[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的内标物,绘制不同分析物的标准曲线,各个分析物的相对校正因子差别很大。实验室人告诉我,如果分析物和内标结构差不多,那么校正因子越接近1。这是对的,不过有的化合物化学式差不多,结构却相差很多,这样校正因子差别也很大,我要如何判断我做出来的标准曲线和相对校正因子是对的呢?[/color][color=#444444]比如,我用辛酸甲酯做内标,测了两个化合物,苯乙酸(C8H8O2,含苯环和羧酸)和香兰素(C8H8O3,含苯环,羰基,甲氧基和羟基)。其中苯乙酸相对辛酸甲酯差别不是很大,而香兰素差别就大了。所以他们的标准曲线分别是y=0.7311x-0.0525 R2=0.99998,y-1.1526x-0.1764 R2=0.9982。不知道它们的校正因子对不对?有大神帮忙分析一下吗?[/color]
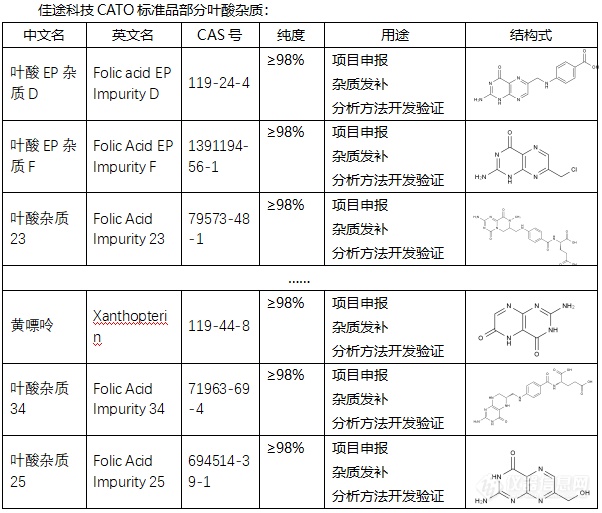
[font=宋体]◇叶酸杂质[/font][font='Segoe UI'][color=#05073b][font=Segoe UI] 叶酸杂质通常是指在叶酸的生产或保存过程中产生的非目标化合物。这些杂质可能会影响叶酸的纯度和效果,因此在叶酸的生产和质量控制过程中需要严格控制其含量。叶酸杂质有多种类型,每一种都具有不同的化学特性,如[/font]CAS号、分子式、分子量等。例如,有一种叶酸杂质CAS号为82778-08-3,分子式为C7H7ClN6HCl,分子量为247.08。另一种叶酸杂质G的CAS号为6810-75-9,英文名称为Folinic Acid Impurity G。此外,叶酸杂质5的CAS号为873397-19-4,纯度为98% HPLC。[/color][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的叶酸全套的杂质[/font][/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[img=,602,513]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182015587706_5356_6381607_3.png!w602x513.jpg[/img][/font][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供叶酸全套[/font][/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
请大侠门指点一下配脂肪酸甲酯的标液用什么溶剂?买了芥酸,木焦油酸等标准固体的物质,我称了0。1克标准物,用异辛-烷定容10ML,进样气相色谱芥酸没有出峰,木焦油酸溶解不了。为什么呢?
如题,求助一篇松脂酸铜的具体分析方法!
SH/T 0831-2010生物柴油中脂肪酸甲酯及亚麻酸甲酯含量的测定 气相色谱法
丁酸戊酯丁酸异戊酯异丁酸戊酯异丁酸异戊酯这四个从质谱上 有什么明显的区别吗? 公司没有这些原料 我没法进仪器区分 是刚才分析样品是看到的一个峰,区分不开到底是啥, 大家支支招 还是要我把谱图上传 都可以的。。。。上个附件,RT:12.577 大家有空帮忙看看 这个到底是什么??
[b][font=宋体]问题描述:根据[/font]NY/T 1723[font=宋体]富马酸二甲酯的测定方法,方法检出限是[/font]0.05mg/kg[font=宋体],折算后标准溶液最低点需要做到[/font]10ng/mL[font=宋体],但目前我们实验室只能做到[/font]50ng/mL[font=宋体]。因为食品中富马酸二甲酯是禁止添加的,如何才能做到检出限满足标准要求呢?[/font][font=宋体]解答:[/font][/b][font=宋体]([/font]1[font=宋体])对于非法添加物质的检测,无论是在制作标准曲线,还是在做加标回收等质控,都必须将检测限作为一个重要的关注点。通常将[/font]3[font=宋体]倍信噪比的色谱峰浓度作为化合物的检测限。[/font][font=宋体]([/font]2[font=宋体])由于富马酸二甲酯在紫外吸收本身不是太强,单位浓度的在液相色谱中的响应不是太高,获得达到低的检测限([/font]0.05mg/kg[font=宋体])是一个难题。总体的解决办法是采取措施去提高富马酸二甲酯的信噪比。[/font][font=宋体]([/font]3[font=宋体])改善富马酸二甲酯的信噪比,可以通过以下措施:[/font]a.[font=宋体]更换有机相种类。甲醇的紫外截至波长为[/font]205nm[font=宋体],在[/font]220nm[font=宋体]波长处吸收度大于[/font]0.2AU[font=宋体]。在[/font]NY/T 1723-2009[font=宋体]《食品中富马酸二甲酯的测定[/font] [font=宋体]高效液相色谱法》中流动相甲醇的比例为[/font]55%[font=宋体],其背景吸收为[/font]0.11AU[font=宋体]左右,远高于[/font]0.05AU[font=宋体]的要求。而乙腈在[/font]220nm[font=宋体]处的吸光度比较低。流动相背景吸光度的降低有利于提高富马酸二甲酯的信噪比。[/font]b.[font=宋体]选择粒径更小的色谱柱。色谱柱的粒径越小,则色谱峰的峰宽越窄,信噪比越大。当然,粒径越小带来一个不利影响就是柱压越高。对富马酸二甲酯的检测,可以选择比标准更小一点粒径的色谱柱,即粒径为[/font]3.5μm[font=宋体]的色谱柱。[/font]c.[font=宋体]加大进样量。在不影响化合物在色谱柱保留行为及改变峰形的前提下,增大进样量有利于提高化合物色谱峰的信噪比。[/font][font='微软雅黑','sans-serif'][color=black][back=white]领取更多《实战宝典》请进:[url]http://instrument-vip.mikecrm.com/2bbmrpI[/url][/back][/color][/font][font='微软雅黑','sans-serif'][color=black][back=white] [/back][/color][/font]
请问一下哪位高手做过动植物油脂中脂肪酸甲酯的测定因为脂肪酸甲酯有70多种同分异构体所以没办法一一分开请问各为高手怎么样才能把这70多种物质分开呢.还有就是你们用的是什么检测器什么条件呢?谢谢各位.
PC(碳酸丙烯酯),EC(碳酸乙烯酯),DMC(碳酸二甲酯),DEC(碳酸二乙酯),EMC(碳酸甲乙酯)混合物可以用GCMS 测试吗?还是GCFID
基于高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法-紫外检测器(high-performance liquid chromatography -ultraviolet detector,HPLC-UVD )检测松脂酸铜在火龙果、豇豆和杧果3种果蔬中的农药残留的分析方法。原理为盐酸将松脂酸铜转化为松脂酸,用石油醚超声提取,提取液蒸干后使用乙腈定容,通过HPLC-UVD对样品进行定量测定。结果表明,松脂酸铜的相关系数R2为0.999 6,平均回收率在77% ~ 108%,相对标准偏差均小于5%,线性关系良好,方法的检出限(limit of detection,LOD)为0.03 mg/kg,定量限(limit of quantitation,LOQ )为0.1 mg/kg。该方法简便、准确、快速,可满足果蔬中松脂酸铜残留检测灵敏度和准确度的要求,其他果蔬样品中的松脂酸铜残留也可参照该方法进行分析。详见[font=&][color=#666666]10.13995/j.cnki.11-1802/ts.030912[/color][/font]
各位大神好。在线急等。。。脂肪酸甲酯,难道不是碳12以上的混合物吗?为什么客户说他就要测脂肪酸甲酯,而且含量低于百分之一,怎么做啊到底。我把油酯化后,不就出的油中各个酸的含量吗。那怎么看脂肪酸甲酯?都有哪些酸面积加一块?并且能低于百分之一!?感觉不对啊。哪里出问题了?
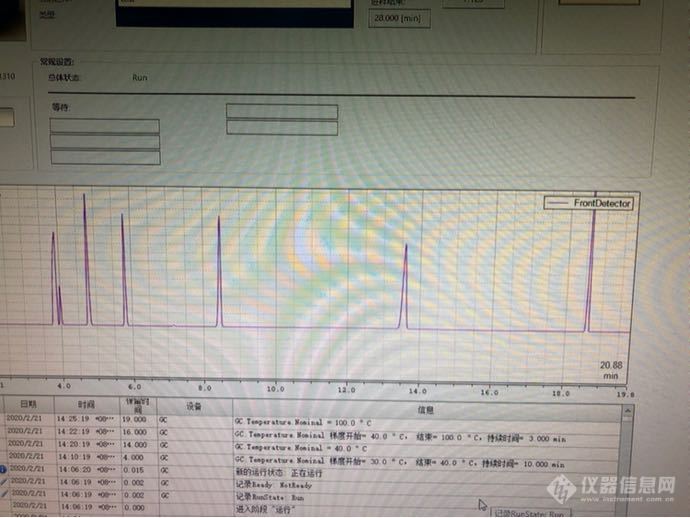
我买的坛墨的7种饱和脂肪酸酯类化合物混标!甲酸甲酯 乙酯 乙酸甲乙丙丁戊酯。现在问题来了。我甲酸乙酯和乙酸甲酯一直分不开 。下面是我条件:30 度保持4min 以1 度/min 升到40度 30度/min到100。后面都没问题 甲酸甲酯我温度低一点也能和cs2分开。可是甲酸乙酯和乙酸甲酯...分不开。那我怎么做呢?是不是要单独做一个乙酸甲酯曲线方法验证。柱子是 ffap 30 0.32 0.25[img=,690,517]https://ng1.17img.cn/bbsfiles/images/2020/02/202002211425479329_4319_2990176_3.png[/img]
日本植物油中酸价的标准酸价的国标和行标又是怎样的?急!!急
最近在做酯交换法合成碳酸二甲酯,碳酸丙烯酯跟甲醇反应,产物为丙二醇和碳酸二甲酯,定量分析不知如何分析。求助,仪器条件及内标物选定,谢谢啦!
哪位老师用LC或LCMSMS做过松香酸?乙腈,水,难调配,C18柱,峰形很难看,柱压、信号都非常怪异;药典加入25%的四氢呋喃,本人不想加,但摸不到头绪。好友回复:做梯度洗脱,LCMSMS最好走梯度,仅做标样中的松香酸,也要走梯度,液质质走梯度分离效果好
在这个测定中,我国是不是规定了花生油、葵花籽油、米糠油POV ≤20mmol/kg,其他食用油POV ≤12mmol/kg,精炼植物油POV ≤mmol/kg ? 还有油脂氧化酸败还可引起酸价AV和羰基价CGV上升,我国规定的食用植物油总CGV ≤20mmol/kg,精炼食用植物油 ≤10mmol/kg ?那酸价的标准是用CGV的标准还是用AV的标准啊?AV有标准的吗?
脂肪酸甲酯是极性化合物吗,为什么检测时多选用强极性色谱柱?
求助采用内标法气相测谱检测甲醛、丙烯酸甲酯、醋酸甲酯,内标物选什么?稀释剂选什么?进样、检测、柱温如何设置?急求!!谢谢!!
分享一个不常见的农药松脂酸铜的高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法-紫外检测器检测方法。样品利用盐酸衍生生成松脂酸,通过HPLC-UVD对松脂酸进行定量,间接定量松脂酸铜。结果表明,松脂酸铜的相关系数R2为0.999 6,平均回收率在77% ~ 108%,相对标准偏差均小于5%,线性关系良好,方法的检出限(limit of detection,LOD)为0.03 mg/kg,定量限(limit of quantitation,LOQ )为0.1 mg/kg。该方法简便、准确、快速,可满足果蔬中松脂酸铜残留检测灵敏度和准确度的要求,其他果蔬样品中的松脂酸铜残留也可参照该方法进行分析。 详见王美然等,食品与发酵工业,2022.
关于此类物质的 laman资料太少,我急用可是查不到相关资料。急求Ga(镓),Ga2O3(氧化镓)WO3(氧化钨)和Ga2(WO4)3(钨酸镓)的峰值区或者laman图谱,谢谢了!!!!!!!!!!!!!
关于此类物质的 laman资料太少,我急用可是查不到相关资料。急求Ga(镓),Ga2O3(氧化镓)WO3(氧化钨)和Ga2(WO4)3(钨酸镓)的峰值区或者laman图谱,谢谢了!!!!!!!!!!!!!
[b][font=宋体]采用高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]级甲醇、正己烷和硫酸(H2SO4)进行原位酯交换反应。 用于FAMES分析的[u]内标[/u]1,3-二氯苯购自Sigma-Aldrich(36708-1g)。 [u]FAMES分析方法的校准[/u]是用FAMES标准混合物进行的,该标准混合物含有C4-C24范围内的饱和脂肪酸、单不饱和脂肪酸和多不饱和脂肪酸。[/font][font=等线]1.[/font][font=等线]脂质检测的具体方法:[/font][font=宋体]微藻中油脂提取的方法为原位酯交换法[/font][font=宋体]脂质分析采用:[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]质谱仪[/font][font=等线]2.[/font][font=等线]需要的标准品和耗材:[/font][font=宋体]药品:高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]级甲醇;浓硫酸;正己烷;[/font][font=宋体]标准品:FAMES标准混合物[/font][/b]
用内标法测碳酸二甲酯的量,该用什么内标物呢,请高人指点。
各位老师好。我使用的是安捷伦GC7890B-MS7000C[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪,HP-5ms毛细管柱(30 m×250 um×0.25 um)。目前打算用这台仪器做软体动物和浮游植物的脂肪酸测定,已经购买了37种脂肪酸甲酯(可定性定量)和十九烷酸甲酯作为内标使用,甲酯化方法参考国标《GBT17376-2008动植物油脂脂肪酸甲酯制备》和《GBT21514-2008饲料中脂肪酸含量的测定》。但是目前有一个疑问,就是在甲酯化的过程,脂肪酸和脂肪酸甲酯存在一个转化效率的问题,如何解决这样一个问题?我在网上找了一遍,发现有一种叫做回收率指示物的东西,好像可以得到这个效率。对此我有几个疑问。第一,对于这个脂肪酸甲酯实验,老师们有没有推荐的回收率指示的标准品?或者有更好的办法能够解决这个问题?第二,有没有做过脂肪酸甲酯相关实验的老师,请问大家采取的甲酯化方式是否和我相同,可否分享一下,为什么选择这种甲酯化方法?欢迎交流