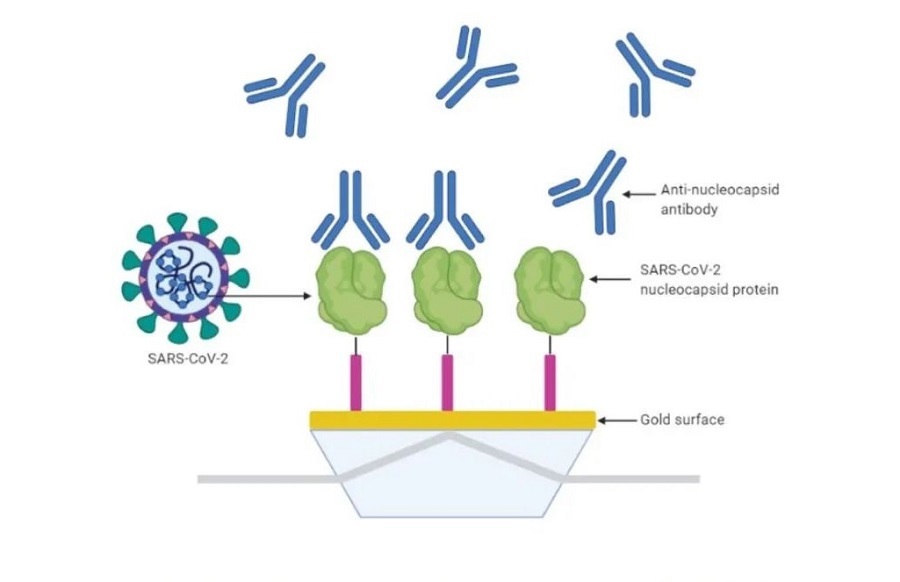
中央:大规模开展核酸和抗体检测
section data-role=" outer" label=" Powered by 135editor.com" section data-role=" outer" label=" Powered by 135editor.com" section data-role=" paragraph" class=" _135editor" section class=" _135editor" data-tools=" 135编辑器" data-id=" 32290" section style=" clear: both padding: 0px border: 0px none margin: 5px 0px box-sizing: border-box " section style=" border-top-width: 2.5px border-top-style: solid border-color: #ef7060 font-size: 1em font-weight: inherit text-decoration: inherit color: #fefefe box-sizing: border-box " section style=" border: 0px rgb(239, 112, 96) margin: 2px 0px 0px overflow: hidden padding: 0px color: inherit box-sizing: border-box " section style=" display: inline-block font-size: 1em font-weight: inherit text-align: inherit text-decoration: inherit color: inherit border-color: rgb(239, 112, 96) font-family: inherit box-sizing: border-box " section class=" 135brush" data-bcless=" darken" data-brushtype=" text" style=" display: inline-block line-height: 1.4em padding: 5px 10px height: 32px vertical-align: top font-weight: bold float: left color: inherit border-color: rgb(212, 43, 21) background: rgb(239, 112, 96) font-family: inherit box-sizing: border-box !important " “应检尽检、愿检尽检” /section section class=" assistant" style=" display: inline-block vertical-align: top width: 0px height: 32px border-top: 32px solid rgb(239, 112, 96) border-right: 32px solid transparent border-top-right-radius: 4px border-bottom-left-radius: 2px color: inherit overflow: hidden box-sizing: border-box !important " /section /section /section /section /section /section p style=" text-align:justify text-indent: 32px " 中央应对新冠肺炎疫情工作领导小组22日召开会议。会议指出,做到“四早”首要是早发现。做好常态化防控要加快提升检测能力,大规模开展核酸和抗体检测。要加快提升检测技术,抓紧增加更简便、更高效准确的检测设备生产,广泛配备到医院、口岸等急需方面,扩大商业化应用,做到对重点人群应检尽检,对复工复产中人员聚集的单位、场所优先做到愿检尽检。 /p p style=" text-align:center text-indent: 0em " img src=" https://img1.17img.cn/17img/images/202004/uepic/eeda61a4-d35e-478a-87f7-b8ac2e7e5303.jpg" title=" image001.jpg" alt=" image001.jpg" width=" 312" height=" 326" data-ratio=" 1.0440097799511003" data-w=" 409" style=" caret-color: red max-height: 100% width: 312px height: 326px " / span style=" caret-color: red " /span /p p style=" text-align:justify text-indent: 32px " 目前主要的检测方法就是核酸检测、抗体检测和抗原检测,但是国家药监局目前仍然没有批准抗原检测产品(敏感性不及核酸),所以我们暂不进行讨论。截至2020年4月23日,国家药品监督管理局应急审批批准30个新冠病毒检测试剂,其中包括19个核酸检测试剂和11个抗体检测试剂。从技术角度出发,现有的检测技术可以满足大部分需求,但仍然存在一些局限性,因此加快提升检测技术是关键。 /p section class=" _135editor" data-tools=" 135编辑器" data-id=" 32290" section style=" clear: both padding: 0px border: 0px none margin: 5px 0px box-sizing: border-box " section style=" border-top-width: 2.5px border-top-style: solid border-color: #ef7060 font-size: 1em font-weight: inherit text-decoration: inherit color: #fefefe box-sizing: border-box " section style=" border: 0px rgb(239, 112, 96) margin: 2px 0px 0px overflow: hidden padding: 0px color: inherit box-sizing: border-box " section style=" display: inline-block font-size: 1em font-weight: inherit text-align: inherit text-decoration: inherit color: inherit border-color: rgb(239, 112, 96) font-family: inherit box-sizing: border-box " section class=" 135brush" data-bcless=" darken" data-brushtype=" text" style=" display: inline-block line-height: 1.4em padding: 5px 10px height: 32px vertical-align: top font-weight: bold float: left color: inherit border-color: rgb(212, 43, 21) background: rgb(239, 112, 96) font-family: inherit box-sizing: border-box !important " 核酸检测准确度低,容易出现假阴性 /section section class=" assistant" style=" display: inline-block vertical-align: top width: 0px height: 32px border-top: 32px solid rgb(239, 112, 96) border-right: 32px solid transparent border-top-right-radius: 4px border-bottom-left-radius: 2px color: inherit overflow: hidden box-sizing: border-box !important " /section /section /section /section /section /section p style=" text-align:justify text-indent: 2em " 核酸检测是确诊新冠肺炎的“金标准”,目前是最可靠的筛查和确认手段,主要是利用实时荧光定量PCR(RT-PCR)技术,相比于抗体检测灵敏度高。 strong 但是阳性率还是较低只有30%至50%。 /strong 主要的原因是样本处理、试剂质量问题以及方法学本身的问题综合导致,因此这也为技术厂商提供一定的仪器试剂发展方向。 /p section class=" _135editor" data-tools=" 135编辑器" data-id=" 32290" section style=" clear: both padding: 0px border: 0px none margin: 5px 0px box-sizing: border-box " section style=" border-top-width: 2.5px border-top-style: solid border-color: #ef7060 font-size: 1em font-weight: inherit text-decoration: inherit color: #fefefe box-sizing: border-box " section style=" border: 0px rgb(239, 112, 96) margin: 2px 0px 0px overflow: hidden padding: 0px color: inherit box-sizing: border-box " section style=" display: inline-block font-size: 1em font-weight: inherit text-align: inherit text-decoration: inherit color: inherit border-color: rgb(239, 112, 96) font-family: inherit box-sizing: border-box " section class=" 135brush" data-bcless=" darken" data-brushtype=" text" style=" display: inline-block line-height: 1.4em padding: 5px 10px height: 32px vertical-align: top font-weight: bold float: left color: inherit border-color: rgb(212, 43, 21) background: rgb(239, 112, 96) font-family: inherit box-sizing: border-box !important " 抗体检测技术存在滞后性 /section section class=" assistant" style=" display: inline-block vertical-align: top width: 0px height: 32px border-top: 32px solid rgb(239, 112, 96) border-right: 32px solid transparent border-top-right-radius: 4px border-bottom-left-radius: 2px color: inherit overflow: hidden box-sizing: border-box !important " /section /section /section /section /section /section p style=" text-align:justify text-indent: 32px " 抗体检测属于免疫学检测方法,主要是看样本中有没有病毒相关蛋白或者相关抗体。主要使用的是 strong 胶体金方法 /strong ,类似于血糖仪的检测场景,该类检测最大的优势在于方便快捷,能够有效突破现有检测技术对人员、场所的限制。 strong 但抗体检测主要存在窗口期时间较长的局限性 /strong ,新型冠状病毒侵入人体5-7天后才会出现IgM抗体,然后在10-15天后出现IgG抗体,所以最大的缺点就是 strong 容易导致漏诊的情况出现 /strong 。 /p section class=" _135editor" data-tools=" 135编辑器" data-id=" 32290" section style=" clear: both padding: 0px border: 0px none margin: 5px 0px box-sizing: border-box " section style=" border-top-width: 2.5px border-top-style: solid border-color: #ef7060 font-size: 1em font-weight: inherit text-decoration: inherit color: #fefefe box-sizing: border-box " section style=" border: 0px rgb(239, 112, 96) margin: 2px 0px 0px overflow: hidden padding: 0px color: inherit box-sizing: border-box " section style=" display: inline-block font-size: 1em font-weight: inherit text-align: inherit text-decoration: inherit color: inherit border-color: rgb(239, 112, 96) font-family: inherit box-sizing: border-box " section class=" 135brush" data-bcless=" darken" data-brushtype=" text" style=" display: inline-block line-height: 1.4em padding: 5px 10px height: 32px vertical-align: top font-weight: bold float: left color: inherit border-color: rgb(212, 43, 21) background: rgb(239, 112, 96) font-family: inherit box-sizing: border-box !important " 新冠检测技术进展各有亮点 /section section class=" assistant" style=" display: inline-block vertical-align: top width: 0px height: 32px border-top: 32px solid rgb(239, 112, 96) border-right: 32px solid transparent border-top-right-radius: 4px border-bottom-left-radius: 2px color: inherit overflow: hidden box-sizing: border-box !important " /section /section /section /section /section /section p style=" text-align:justify text-indent: 32px " 近期处于热议中的雅培ID NOW COVID-19检测试剂,官方称可在5分钟内获得新冠阳性结果。但该方法的检测限相比于荧光定量PCR高,即灵敏度较低。此后,它的检测准确率又被美国白宫质疑,基于NEAR技术(切口酶扩增反应技术)的核酸检测方法,虽有速度和灵敏度的优势,但短序列的设计确实存在高假阳性的可能。 strong 因此后续的升级款是否会在准确率方向进行提升值得期待 /strong 。 /p p style=" text-align:center " img src=" https://img1.17img.cn/17img/images/202004/uepic/af9ed3cc-e20c-4f26-ab18-e10431250c3a.jpg" title=" image002.jpg" alt=" image002.jpg" style=" width:auto max-width: 100% max-height: 100% " data-ratio=" 1.0268817204301075" data-w=" 186" / /p p style=" text-align:center text-indent: 0em " 雅培ID NOW设备 /p p style=" text-align:justify text-indent: 32px " 罗氏在三月中旬推出的用于检测该疾病病毒活性的 strong 高通量PCR检测系统 /strong cobas 6800/8800,据悉将显著提高现有的SARS-CoV-2检测能力,可在3个半小时内提供多达96个检测结果,在24小时内,cobas 6800和8800系统可分别提供1,440和4,128个检测结果。系统无人值守时间分别长达8小时(cobas 6800系统)和4小时(cobas 8800系统),提高了工作效率和灵活性。 strong 只是目前cobas SARS-CoV-2检测尚未获得FDA许可或批准,在大规模检测过程中,高通量是检测仪器必要的。 /strong /p p style=" text-align:justify text-indent: 32px " 近日,麻省理工学院称其开发的核酸检测系统绕开PCR扩增、采用等温扩增技术RPA,有望在一小时内实现病毒检测。 /p p style=" text-align:justify text-indent: 32px " 检测试剂不是万能的,不同的方法,具有不同的特点,针对不同的景,也有其局限性。中国对抗体的定位是核酸阴性的补充确诊手段,疫情防控的目的是发现所有的感染者。通过核酸、抗体检测方式联合应用,缩短检测窗口期,提高阳性检出率,在新冠肺炎的辅助诊断方面,具有十分重要的作用,毕竟不是所有的机构都适合做核酸检测。 /p section class=" _135editor" data-tools=" 135编辑器" data-id=" 32290" section style=" clear: both padding: 0px border: 0px none margin: 5px 0px box-sizing: border-box " section style=" border-top-width: 2.5px border-top-style: solid border-color: #ef7060 font-size: 1em font-weight: inherit text-decoration: inherit color: #fefefe box-sizing: border-box " section style=" border: 0px rgb(239, 112, 96) margin: 2px 0px 0px overflow: hidden padding: 0px color: inherit box-sizing: border-box " section style=" display: inline-block font-size: 1em font-weight: inherit text-align: inherit text-decoration: inherit color: inherit border-color: rgb(239, 112, 96) font-family: inherit box-sizing: border-box " section class=" 135brush" data-bcless=" darken" data-brushtype=" text" style=" display: inline-block line-height: 1.4em padding: 5px 10px height: 32px vertical-align: top font-weight: bold float: left color: inherit border-color: rgb(212, 43, 21) background: rgb(239, 112, 96) font-family: inherit box-sizing: border-box !important " 核酸检测商业化应用 /section section class=" assistant" style=" display: inline-block vertical-align: top width: 0px height: 32px border-top: 32px solid rgb(239, 112, 96) border-right: 32px solid transparent border-top-right-radius: 4px border-bottom-left-radius: 2px color: inherit overflow: hidden box-sizing: border-box !important " /section /section /section /section /section /section p style=" text-indent: 33px " span style=" font-size: 15px letter-spacing: 1px background: white " 在大规模检测的政策环境下,检测仪器与试剂的 /span 生产成本及销售价格也是大家所关注的。目前市面上 span style=" font-size: 15px letter-spacing: 1px background: white " 新冠核酸检测的成本较高,在某平台上单次检测价格是 /span span style=" font-size: 15px letter-spacing: 1px background: white font-family: Helvetica, sans-serif " 200-300 /span span style=" font-size: 15px letter-spacing: 1px background: white " 元不等。要知道扩大检测规模后,谁能保证每个人只筛查一次,这样的投入不论是个人、企业还是政府而言,都可能是一种负担。 strong 那么研发更加低廉的核酸检测试剂与平台也会是当下厂商面临的发展方向。 /strong /span /p p style=" text-align:center " img src=" https://img1.17img.cn/17img/images/202004/uepic/13f4bbf3-173a-4d95-be24-be6716586678.jpg" title=" image003.jpg" alt=" image003.jpg" width=" 552" height=" 227" style=" max-width: 100% max-height: 100% width: 100% height: 227px " data-ratio=" 0.41040462427745666" data-w=" 692" / /p p style=" text-align:center text-indent: 0em " 某平台核酸检测服务价格在200-300不等 /p p style=" text-align:justify text-indent: 2em " 截止发稿前,笔者发现 strong 华大基因 /strong 在电商平台拼多多已经开卖核酸检测服务,24h即可出具电子版本检测报告。 /p p style=" text-align:center " img src=" https://img1.17img.cn/17img/images/202004/uepic/fdf55210-f682-4935-9e82-50360e2ef09b.jpg" title=" 华大基因.拼多多.jpg" alt=" 华大基因.拼多多.jpg" width=" 187" height=" 283" style=" max-width: 100% max-height: 100% width: 187px height: 283px " data-ratio=" 1.44" data-w=" 750" / /p section class=" _135editor" data-tools=" 135编辑器" data-id=" 32290" section style=" clear: both padding: 0px border: 0px none margin: 5px 0px box-sizing: border-box " section style=" border-top-width: 2.5px border-top-style: solid border-color: #ef7060 font-size: 1em font-weight: inherit text-decoration: inherit color: #fefefe box-sizing: border-box " section style=" border: 0px rgb(239, 112, 96) margin: 2px 0px 0px overflow: hidden padding: 0px color: inherit box-sizing: border-box " section style=" display: inline-block font-size: 1em font-weight: inherit text-align: inherit text-decoration: inherit color: inherit border-color: rgb(239, 112, 96) font-family: inherit box-sizing: border-box " section class=" 135brush" data-bcless=" darken" data-brushtype=" text" style=" display: inline-block line-height: 1.4em padding: 5px 10px height: 32px vertical-align: top font-weight: bold float: left color: inherit border-color: rgb(212, 43, 21) background: rgb(239, 112, 96) font-family: inherit box-sizing: border-box !important " 未来新冠检测应用场景带来的市场“福利” /section section class=" assistant" style=" display: inline-block vertical-align: top width: 0px height: 32px border-top: 32px solid rgb(239, 112, 96) border-right: 32px solid transparent border-top-right-radius: 4px border-bottom-left-radius: 2px color: inherit overflow: hidden box-sizing: border-box !important " /section /section /section /section /section /section p style=" text-indent: 33px " span style=" font-size: 15px letter-spacing: 1px " 目前各方判断,新冠病毒有可能成为类似流感病毒一样和人类长期共存的病毒。因此 /span 当新冠检测规模扩大,甚至下沉到社区,必然会产生巨大的样本检测量,理论上就要求检测仪器必须满足 strong 现场大规模快速检测、准确度高 /strong 、 strong 操作简单、自动化程度高价格低、便携小型化、价格低廉 /strong 等特点。此外,企业想要把握这次市场“福利”,不仅要尽可能满足上述仪器试剂的发展要求,也要保证仪器试剂的 strong 产能足够高 /strong ,满足大规模检测的需求。 /p section class=" _135editor" data-tools=" 135编辑器" data-id=" 86318" section class=" _135editor" data-tools=" 135编辑器" data-id=" 86318" data-color=" #ef7060" section class=" layout" style=" margin: 0px auto " section class=" " style=" margin-top: 2em padding-top: 0.5em padding-bottom: 0.5em font-size: 1em font-weight: inherit line-height: 22.4px border-style: solid none none border-top-width: 1px border-top-color: rgb(204, 204, 204) text-decoration: inherit color: rgb(166, 166, 166) box-sizing: border-box font-family: inherit " section class=" " style=" margin-top: -1.2em text-align: center border: none line-height: 1.4 box-sizing: border-box " span class=" 135brush" data-brushtype=" text" style=" padding: 8px 23px border-radius: 25px color: rgb(255, 255, 255) font-weight: inherit text-decoration: inherit border-color: rgb(17, 17, 17) background-color: rgb(17, 17, 17) font-family: inherit " 后记: /span /section /section /section /section /section p style=" text-indent: 32px " 据悉目前核酸等温扩增仪器的最新进展是,在某些针对贫困地区的设备甚至不需要电即可在常温或温水里运行(目前处于研究阶段)。这也为仪器试剂厂商指出了一定的技术方向。如果能实现该项技术,那么核酸检测的应用场景将被进一步扩大,市场机遇也会随之而来。 /p /section /section /section