阿德福韦酯是由美国Gilead Science公司开发的新型核苷类抗乙型病毒性肝炎药物,已在国外进行了Ⅱ、Ⅲ期临床试验。国外的临床研究资料表明,阿德福韦能有效地抑制HBV DNA的复制,使HBV DNA滴度迅速降低,而且在出现拉米夫定耐药的患者中阿德福韦能继续有效地抑制变异株。我国药品监督管理局于2000年12月批准该药在中国进行临床试验,目前,Ⅰ期临床试验已结束,Ⅱ期临床试验也已在2002年12月正式启动。 一、作用机制 阿德福韦酯是腺嘌呤磷酸酯化合物阿德福韦的前药,其分子式为C20H32N5O8P,分子量为501.48。口服后,在体内转化为阿德福韦发挥抗病毒作用。阿德福韦是单磷酸腺苷的核苷酸类似物,在体内通过细胞激酶作用被磷酸化为具有活性作用的二磷酸阿德福韦,二磷酸阿德福韦抑制HBV DNA多聚酶或逆转录酶作用机制包括:(1)竞争脱氧腺苷三磷酸底物;(2)终止病毒DNA链延长。二磷酸阿德福韦对HBV DNA多聚酶的抑制常数为0.1mmol/L;对人类DNA多聚酶α和γ的抑制作用较弱,其抑制常数分别为1.18mmol/L和0.97mmol/L,因此,治疗剂量对正常细胞没有毒性。 二、药效和毒理 在体外实验中,阿德福韦抑制HBV转染人肝细胞瘤细胞株HepG2和HB611细胞病毒复制的半数抑制浓度(IC50)分别为0.2~2.5mmol/L和0.2~1.2mmol/L。二磷酸阿德福韦在细胞内的T1/2为30h,故作用较持久,可以每天给药一次。 拉米夫定耐药株涉及HBV DNA聚合酶M552V、M552I、L528M、L552M/M552V位点的突变。在体外实验中发现这些突变体对阿德福韦仍敏感,与野生株比较,它们的抑制常数增加了不到2.2倍,而拉米夫定对变异株的抑制常数则增加了8~25倍。这些资料表明,阿德福韦可以治疗对拉米夫定耐药的HBV,而且与拉米夫定联合治疗可以有效控制对拉米夫定的耐药。同时,体外实验也发现阿德福韦对泛昔洛韦耐药株也较敏感。 在体内实验中,发现阿德福韦能有效地抑制鸭乙型肝炎病毒和土拨鼠肝炎病毒(WHV)的复制。给予慢性感染WHV的成年土拨鼠每日口服5mg/kg、15mg/kg的阿德福韦或安慰剂治疗12周,治疗后5mg/kg剂量组WHV DNA水平减少了260倍,而15mg/kg剂量组则下降了1000倍以上。 四、国外临床研究进展 阿德福韦已在美国、欧洲、澳大利亚及东南亚进行了Ⅱ、Ⅲ期临床试验。临床试验涉及HBeAg阳性和考虑有前C区变异的HBeAg阴性的慢性乙型肝炎患者、对拉米夫定耐药的代偿性肝病患者、合并人类免疫缺陷病毒感染的拉米夫定耐药患者、肝移植前或移植后对拉米夫定耐药的失代偿性肝病患者。 早期进行的针对HBeAg阳性、ALT异常或正常的二项双盲、安慰剂对照的Ⅱ期临床试验,疗程为12周,并随访24周。ALT异常临床研究的患者,接受剂量为5mg/d、30mg/d和60mg/d。治疗12周后,5mg剂量组血清HBV DNA较基线下降1 Log10,30mg和60mg剂量组血清HBV DNA下降3~4 Log10,而安慰剂组无显著变化;36周后,30mg和60mg剂量组HBeAg转阴率为27%,HBeAg血清转化率为20%,血清转化率增高与基线时ALT水平呈正相关。ALT正常的临床研究患者,接受剂量为30mg/d。治疗12周后,30mg剂量组血清HBV DNA较基线下降3Log10,而安慰剂组无显著变化。所有接受治疗的患者在治疗12周后进行基因检测,没有发现与阿德福韦耐药有关的变异产生。在这二项研究中,30mg和60mg剂量组均出现部分患者的肾功能损害,表现为尿素氮和肌酐的升高,出现肾功能损害的比例与剂量呈正相关,故在以后的延续试验中以10mg剂量组而代替60mg剂量组。 在一项随机、双盲、安慰剂对照的临床试验中,共有515例HBeAg阳性的患者进入研究。在前48周,患者被随机分入阿德福韦30mg组(173例)、阿德福韦10mg组(172例)或安慰剂组(170例)。48周后,30mg组接受安慰剂治疗至96周,安慰剂组接受阿德福韦10mg治疗至96周,10mg组则再次随机按1:1接受安慰剂或继续阿德福韦10mg治疗至96周。所有患者在第一次随机前6月内接受第一次肝活检,在治疗48周、96周后接受第二、三次肝活检。所有患者治疗96周后随访24周。治疗48周后,10mg组和30mg组组织学改善率(组织学改善定义为Knodell坏死炎症计分下降32分,且Knodell肝纤维化计分无恶化)分别为53%和59%,显著高于安慰剂组25%;10mg组和30mg组治疗后血清HBV DNA较基线时下降3.52 Log10和4.76 Log10,安慰剂组为0.55 Log10;10mg组HBeAg阴转率为24%,HBeAg血清转化率为12%,显著高于安慰剂组的6%和11%;10mg组ALT复常率为48%,安慰剂组则为16%。研究中,发现基线ALT水平与肝组织学改善和HBeAg血清转化呈正相关。另一项随机、双盲、安慰剂对照的临床试验,共有185例考虑有前C区变异的HBeAg阴性的患者按2:1比例进入阿德福韦10mg组或安慰剂组。治疗48周后,10mg组组织学改善率为64%,显著高于安慰剂组33%;10mg组治疗后血清HBV DNA较基线时下降3.91 Log10,51%患者HBV DNA转阴,安慰剂组HBV DNA较基线时下降1.35 Log10,没有患者HBV DNA转阴;10mg组ALT复常率为72%,著高于安慰剂组29%。目前本项研究仍在进行中。 五、耐药和病毒变异 阿德福韦较少产生耐药的分子学基础包括:(1)阿德福韦与自然底物dATP在结构上非常相像;(2)阿德福韦具有灵活的开链连接;(3)具有磷酸键。 629例患者在治疗48周后接受了病毒变异的检测,结果未发现产生阿德福韦耐药的病毒变异。2003年美国肝病年会上,Gilead公司报道,238例患者在治疗96周时有4例发现N236T位点的变异,发生率为1.7%,并证实N236T变异与阿德福韦耐药有关。另一可能与阿德福韦耐药有关的A181V位点突变,96周时的发生率为0.8%。另外一项研究是早期进行的针对HBeAg阳性、ALT异常或正常的二项双盲、安慰剂对照研究的延续。患者在治疗中没有出现血清转化,也没有出现与治疗相关的毒性反应,患者自愿继续接受治疗。剂量开始为30mg/d,后改为10mg/d。在长达136周的观察中,阿德福韦对野生株和前C区变异的慢性乙型肝炎具有持续的抗病毒作用,而且没有发现与阿德福韦耐药相关的病毒变异。 七、国内的研究状况 我国食物药品监督管理局于2000年12月批准该药在中国进行Ⅰ期临床试验。2001年6月~9月进行Ⅰ期临床试验,Ⅰ期临床试验包括3个研究方案:(1)在健康中国男性志愿者中,对单次口服阿德福韦片剂的安全性和耐受性进行评估的一项Ⅰ期、单中心、随机、双盲、安慰剂对照的研究;(2)在健康中国男性志愿者中,对阿德福韦片剂的药代动力学进行评估的一项Ⅰ期、单中心、开放、拉丁方设计的研究;(3)在健康中国志愿者中,就连续6d,1次/d,口服阿德福韦片剂的安全性、耐受性和药代动力学进行评估的一项Ⅰ期、单中心、随机、双盲、安慰剂对照的研究。I期研究结果显示在健康中国志愿者中口服阿德福韦片剂的安全性、耐受性良好;10mg剂量下,未观察到肾功能损害;药代动力学参数与国外研究结果相似。2002年10月国家药品监督管理局批准该药在中国进行Ⅱ期临床试验。Ⅱ期临床试验在中国的总病例数为480例,均为HBeAg阳性、HBV DNA阳性、ALT增高的患者。全国有12个中心参与。目前,Ⅱ期临床试验已在2002年12月正式启动,2003年2月底已完成最后一例患者入组。
45.80646.423是丁酸香茅酯 还是 阿芬美酯?糊涂了 http://simg.instrument.com.cn/bbs/images/brow/em06.gif
各位大哥,在沒有塑料燒杯的情況下,怎麽趕走氫氟酸阿?我們公司的ICP霧化室耐不了氫氟酸的阿! 救救!
[color=black]复方盐酸阿替卡因注射液为复方制剂,是盐酸阿替卡因与肾上腺素的灭菌水溶液,作为口腔用局部麻醉剂,适用于涉及切骨术及粘膜切开的外科手术过程。[/color][color=black] [/color][img=,156,99]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211036489419_4502_2297_3.jpg!w156x99.jpg[/img][align=center][/align][align=left][b][color=black]盐酸阿替卡因(Articaine hydrochloride M.W.:320.84)[/color][/b][/align][align=center][b][color=black] [/color][/b][/align][color=black]在现有国家药品标准(YBH17082004-2015Z)分析方法中,流动相添加了离子对试剂-庚烷磺酸钠,并在pH为2.0的强酸条件下进行相应分析,不利于色谱柱的使用寿命。大曹三耀实验室参考USP方法,以冰醋酸水溶液-乙腈作为流动相,选用CAPCELL PAK C18 MGII色谱柱,实现了复方盐酸阿替卡因注射液中盐酸阿替卡因的定量和有关物质的良好分析(复方盐酸阿替卡因注射液由客户提供)。[/color][color=black]CAPCELLPAK C18 MGII[/color][color=black]液相色谱柱,其采用高纯度硅胶作为基质,通过减少硅胶微细孔的数量来增大有效比表面积;并且采用新包被技术Ultimate Polymer Coating,实现了对硅醇基极大程度的封锁,兼具分离性能和普适性能,通用性非常好。[/color][align=left][b][color=#0070c0]实验方法[/color][/b][/align][align=left][img=,500,358]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211037456969_5082_2297_3.jpg!w730x523.jpg[/img][/align][align=left]图1[color=black]盐酸阿替卡因[/color]对照品及供试品溶液[/align][align=left][img=,500,248]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211038541919_2603_2297_3.jpg!w572x284.jpg[/img][/align][align=center][/align][align=center][/align][color=black]为进行有关物质分析,该实验将注射液样品以流动相稀释100倍,作为有关物质供试品溶液,再将该有关物质供试品溶液以流动相进一步稀释100倍,作为自身对照溶液。以冰醋酸水溶液-乙腈作为流动相,选用CAPCELL PAK C18 MGII色谱柱,通过调整流动相比例及柱温,最终在18%乙腈、柱温30℃条件下实现了盐酸阿替卡因供试品溶液及对照品的良好分析。[/color]如图2、3,使用CAPCELL PAK C18 MGII色谱柱进行分析,盐酸阿替卡因和有关物质均能得到良好分析结果,主峰与峰前杂质得到了良好分离,分离度为1.90(见表1)[img=,400,311]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211045536855_9516_2297_3.jpg!w574x447.jpg[/img][img=,400,295]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211045540875_8483_2297_3.jpg!w698x516.jpg[/img][align=left] 图2 [color=black]盐酸阿替卡因[/color]有关物质供试品溶液及空白 图3 自身对照溶液[/align][align=center][/align][align=left]表1 有关物质结果详表[/align][align=left][img=,600,323]https://ng1.17img.cn/bbsfiles/images/2019/03/201903211042513275_6690_2297_3.jpg!w786x424.jpg[/img][/align][align=center][/align]综上实验结果,使用CAPCELL PAK C18 MGII S5 4.6mm i.d.×250 mm色谱柱,以冰醋酸水溶液-乙腈为流动相体系,在30°C柱温条件下,能够实现复方盐酸阿替卡因注射液中盐酸阿替卡因的定量和有关物质的良好分析。[color=black] [/color]
聚甲基丙烯酸叔丁酯薄膜的二维红外相关谱分析[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=151883]聚甲基丙烯酸叔丁酯薄膜的二维红外相关谱分析[/url]
催化合成丁二酸二丁酯第一章 绪论1.1 概要羧酸酯是一类重要的化工原料,低级的酯一般都是水果香味,可作香料(如醋酸异戊酯有香蕉味,戊酸乙酯有苹果香味等)。液态的酯能溶解很多有机物,故常用作溶剂。有些酯还可用作塑料、橡胶的增塑剂。丁二酸二丁酯是一种新型塑料工业的增塑剂,该增塑剂为无色透明液体,常用作有机合成中间体、食物添加剂、气象色谱固定液,是一种昆虫驱避剂,用于驱除蟑螂、蚂蚁等害虫,它的合成与其它酯类化合物一样,由相应的酸和醇通过酯化反应而制得.以往的酯化反应多采用浓硫酸做催化剂,而浓硫酸有腐蚀性,使得酯化反应副反应多、后处理困难、产品色泽较差,同时,在后处理过程中还会产生大量的含硫废水污染环境.为解决浓硫酸作催化剂时的缺点,人们已研究了其它催化剂来代替浓硫酸,但对于丁二酸二丁酯的合成研究的较少,虽有人将TiO2/S042- 固体超强酸用于催化合成丁二酸二丁酯,但该催化剂的制备较为复杂,成本较高,不利于工业化生产.随着人们环保意识的增强,对于酯化反应的催化剂进行了广泛的研究,作者曾注意到结晶硫酸氢钠是一种常见的结晶无机盐,保管、运输、使用均很方便,又能克服无机酸的强腐蚀性,因此作者将研究把硫酸氢钠直接用于催化合成丁二酸二丁酯,主要研究该物质的增塑剂性能和合成该物质所使用的催化剂。
用Wax柱子做丙烯酸丁酯的样品测定,死活分离不出丙酸丁酯,后来问了另一家做相同产品的公司,他们说用FFAP柱子能分离出来,我们就照做了,可是还没分离出来。搞得我现在严重怀疑是我们买的丙酸丁酯有问题,买的是国药的GCS丙酸丁酯,批号是O2789,有人遇到同样的问题吗?
乙二醇经高碘酸与品红阿硫酸反应,最终为什么得不到紫红色化合物?而环氧乙烷检测试验中制乙二醇标准曲线的时候,滴加盐酸的作用是什么?不知道谁能解开我这样的疑惑?谢谢了
前处理有时加入少量低浓度的醋酸铵的目的是啥阿,另外有个标准当基质为水类时,直接乙腈提取,若为油类时先加正己烷分散,再加70%乙腈提取,是因为乙腈不能溶解油类基质吗,先拿正己烷分散,然后再拿乙腈从正己烷中萃取出目标物质?
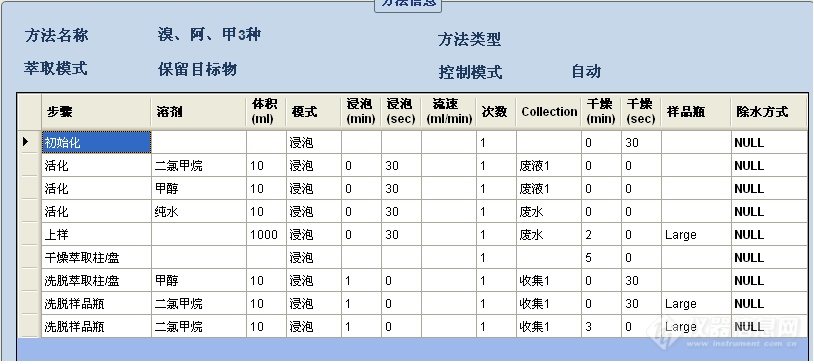
[align=center][font='times new roman'][size=13px]水中阿特拉津、甲萘威、溴氰菊酯的测定[/size][/font][/align][font='times new roman'][size=13px]前言[/size][/font]阿特拉津又名莠去津,是一种除草广谱、[color=#000000]持效期长[/color]的除草剂,[color=#000000]对一般常见[/color]杂草都有一定的防除作用。甲萘威又名西维因,是氨基甲酸酯类杀虫剂中第一个大量生产的品种,是一种杀虫广谱、[color=#000000]高效低毒[/color]的杀虫剂。溴氰菊酯[color=#000000]是菊酯类杀虫剂中毒性最高的一种,其[/color][font='arial'][color=#000000][back=#ffffff]触杀作用迅速,击倒力强[/back][/color][/font][color=#000000],[/color][font='arial'][color=#000000][back=#ffffff]被广泛用于各类害虫的防治。[/back][/color][/font][font='arial'][color=#000000][back=#ffffff]农业生产中不可避免的会用到各种农药除虫除草,但农药的大量、违规使用都会造成水体和环境的污染,所以建立一套快速处理、富集水中阿特拉津、甲萘威、溴氰菊酯并检测的方法是非常有必要的。[/back][/color][/font]本文使用 Sepaths UP 柱膜通用全自动固相萃取系统对水中阿特拉津、甲萘威、溴氰菊酯进行固相萃取富集,用高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url]进行检测。经过试验, Sepaths UP 柱膜通用全自动固相萃取系统对1L水中阿特拉津、甲萘威、溴氰菊酯萃取富集后的[color=#000000]回收率均在[/color][size=13px][color=#000000]76.37[/color][/size][color=#000000][back=#ffffff]%[/back][/color][color=#000000][back=#ffffff]~[/back][/color][size=13px][color=#000000]92.72[/color][/size][color=#000000][back=#ffffff]%之间[/back][/color][color=#000000][back=#ffffff],[/back][/color][color=#000000][back=#ffffff]重现性[/back][/color][color=#000000][back=#ffffff]RSD均[/back][/color][color=#000000][back=#ffffff]在[/back][/color][size=13px][color=#000000]2.06[/color][/size][color=#000000][back=#ffffff]%[/back][/color][color=#000000][back=#ffffff]~[/back][/color][size=13px][color=#000000]4.79[/color][/size][color=#000000][back=#ffffff]%之间[/back][/color]。试验得到较好的回收率和良好的重现性,说明全自动固相萃取系统可靠稳定,适用于大体积水中的阿特拉津、甲萘威、溴氰菊酯样品前处理。关键词:阿特拉津,溴氰菊酯,甲萘威,[font='times new roman'][size=13px]1试验过程[/size][/font][font='times new roman'][size=13px]1.1仪器与试剂[/size][/font]Sepaths UP 柱膜通用全自动固相萃取系统;LC600 二元高压梯度高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url];[color=#000000]阿特拉津标液(3μg/mL,甲醇);甲萘威标液(100μg/mL,甲醇);溴氰菊酯标液(100μg/mL,甲醇);[/color]甲醇(色谱纯);二氯甲烷(色谱纯);乙腈(色谱纯);自来[color=#000000]水;[/color][color=#000000]超纯水;[/color]C18固相萃取膜。[font='times new roman'][size=13px]1.2混合标准工作液的配制[/size][/font]分别取一定量的阿特拉津、甲萘威、溴氰菊酯标液于10mL容量瓶中,用甲醇定容,配置成浓度分别为0.6μg/mL、10μg/mL、10μg/mL的混合标准工作液。[font='times new roman'][size=13px]1.3试验方法[/size][/font][font='times new roman'][size=13px]1.3.1[/size][/font][font='times new roman'][size=13px]样品准备[/size][/font]取1L自来水样品,加入10mL甲醇和50μL的混合标准工作液,使待测水样中阿特拉津、甲萘威、溴氰菊酯的加标浓度分别为0.03μg/L、0.5μg/L、0.5μg/L,将样品混匀待处理。[font='times new roman'][size=13px]1.3.2 [/size][/font][font='times new roman'][size=13px]固相萃取[/size][/font][font='times new roman'][size=13px]及浓缩[/size][/font]按照图1所示的方法进行Sepaths UP方法编辑,并加载方法到相应通道,进行样品的固相萃取。收集洗脱液到收集瓶中,进行氮吹浓缩[color=#000000]并置换溶剂为甲醇,用流动相([/color][color=#000000]甲醇:水= 3:2)[/color][color=#000000]定容到1[/color][color=#000000].0 [/color][color=#000000]mL,待检测。[/color][img]https://ng1.17img.cn/bbsfiles/images/2022/10/202210101020135278_870_5237388_3.png[/img][align=center][size=12px]图1 [/size][size=12px]水中阿特拉津、甲萘威、溴氰菊酯的[/size][size=12px]SPE富集方法[/size][/align][align=center][/align][font='times new roman'][size=13px]1[/size][/font][font='times new roman'][size=13px].[/size][/font][font='times new roman'][size=13px]3.3[/size][/font][font='times new roman'][size=13px] [/size][/font][font='times new roman'][size=13px]HPLC测定水中阿特拉津、甲萘威、溴氰菊酯[/size][/font]色谱柱:Promosil C18,5μm,[color=#000000]4.6mm*1[/color]50mm;[color=#ff0000] [/color]波长:225nm(阿特拉津、甲萘威),230nm(溴氰菊酯);流[color=#000000]速:1.0mL[/color]/min;进样量:20μL;流动相:甲醇:水= 3:2(阿特拉津、甲萘威),乙腈:水= 9:1(溴氰菊酯);[font='times new roman'][size=13px]2试验结果[/size][/font][font='times new roman'][size=13px]2.1水中阿特拉津、甲萘威、溴氰菊酯色谱图[/size][/font][font='times new roman'][size=13px]2.1.1水中阿特拉津、甲萘威、溴氰菊酯标品色谱图[/size][/font]图2、图3为取50μL的混合标准工作液[color=#000000]用流动相([/color][color=#000000]甲醇:水= 3:2)[/color][color=#000000]定容到1[/color][color=#000000].0 [/color][color=#000000]mL检测,阿特拉津、甲萘威、溴氰菊酯[/color]标品出峰色谱图,图2依次为[color=#000000]甲萘威、阿特拉津[/color]标品出峰色谱图,出峰时间分别为5.5min、7.8min,图3为溴氰菊酯标品出峰色谱图,出峰时间为5.6min。[align=center][img]" style="max-width: 100% max-height: 100% [/img][/align][align=center][size=12px]图2 甲萘威与阿特拉津标品出峰色谱图[/size][/align][align=center][/align][align=center][img]" style="max-width: 100% max-height: 100% [/img][/align][align=center][size=12px]图3 溴氰菊酯标品出峰色谱图[/size][/align][align=center][/align][font='times new roman'][size=13px]2.1.2水中阿特拉津、甲萘威、溴氰菊酯加标样品色谱图[/size][/font]图4为甲萘威与阿特拉津加标样品出峰色谱图,出峰时间依次为5.5min、7.8min,图5为溴氰菊酯加标样品出峰色谱图,出峰时间为5.6min。[align=center][img]" style="max-width: 100% max-height: 100% [/img][/align][align=center][size=12px]图4 [/size]甲萘威与阿特拉津加标样品出峰色谱图[/align][align=center][/align][align=center][img]" style="max-width: 100% max-height: 100% [/img][/align][align=center][size=12px]图5 [/size]溴氰菊酯加标样品出峰色谱图[/align][align=center][/align][font='times new roman'][size=13px]2.2[/size][/font][font='times new roman'][size=13px] [/size][/font][font='times new roman'][size=13px]HPLC测定水中阿特拉津、甲萘威、溴氰菊酯回收率[/size][/font][color=#000000]HPLC测定自来水中阿特拉津、甲萘威、溴氰菊酯回收率计算结果如下表,[/color][color=#000000]萃取富集[/color][color=#000000]后的回收率均在[/color][size=13px][color=#000000]76.37[/color][/size][color=#000000][back=#ffffff]%[/back][/color][color=#000000][back=#ffffff]~[/back][/color][size=13px][color=#000000]92.72[/color][/size][color=#000000][back=#ffffff]%之间[/back][/color][color=#000000][back=#ffffff],[/back][/color][color=#000000][back=#ffffff]重现性[/back][/color][color=#000000][back=#ffffff]RSD[/back][/color][color=#000000][back=#ffffff]在[/back][/color][size=13px][color=#000000]2.06[/color][/size][color=#000000][back=#ffffff]%[/back][/color][color=#000000][back=#ffffff]~[/back][/color][size=13px][color=#000000]4.79[/color][/size][color=#000000][back=#ffffff]%之间。[/back][/color][align=center][size=12px][color=#000000]表1 自来水中阿特拉津、甲萘威、溴氰菊酯的回收率[/color][/size][/align][table][tr][td=1,2][align=left][size=13px][color=#000000]名称[/color][/size][/align][align=right][size=13px][color=#000000]编号[/color][/size][/align][/td][td=6,1][align=center][size=13px][color=#000000]回收率(%)[/color][/size][/align][/td][td=1,2][align=center][size=13px][color=#000000]平均[/color][/size][/align][align=center][size=13px][color=#000000](%)[/color][/size][/align][/td][td=1,2][align=center][size=13px][color=#000000]RSD[/color][/size][/align][align=center][size=13px][color=#000000](%)[/color][/size][/align][/td][/tr][tr][td][align=center][size=13px][color=#000000]1[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]2[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]3[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]4[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]5[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]6[/color][/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=13px][color=#000000]阿特拉津[/color][/size][/font][/align][/td][td][align=center][size=13px][color=#000000]83.99[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]81.15[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]86.19[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]85.08[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]78.33[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]76.37[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]81.85[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]4.79[/color][/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=13px][color=#000000]甲萘威[/color][/size][/font][/align][/td][td][align=center][size=13px][color=#000000]89.25[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]87.76[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]86.50[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]85.99[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]92.72[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]92.10[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]89.06[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]3.19[/color][/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=13px][color=#000000]溴氰菊酯[/color][/size][/font][/align][/td][td][align=center][size=13px][color=#000000]84.23[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]88.18[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]89.25[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]87.76[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]86.50[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]85.99[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]86.99[/color][/size][/align][/td][td][align=center][size=13px][color=#000000]2.06[/color][/size][/align][/td][/tr][/table][font='times new roman'][size=13px]3结论与讨论[/size][/font]使用Sepaths UP 柱膜通用全自动固相萃取系统将1L自来水中阿特拉津、甲萘威、溴氰菊酯同时富集处理、分批测定回收率,得回收率均在[size=13px][color=#000000]76.37[/color][/size][color=#000000][back=#ffffff]%[/back][/color][color=#000000][back=#ffffff]~[/back][/color][size=13px][color=#000000]92.72[/color][/size][color=#000000][back=#ffffff]%之间[/back][/color][color=#000000][back=#ffffff],[/back][/color][color=#000000][back=#ffffff]重现性[/back][/color][color=#000000][back=#ffffff]RSD[/back][/color][color=#000000][back=#ffffff]在[/back][/color][size=13px][color=#000000]2.06[/color][/size][color=#000000][back=#ffffff]%[/back][/color][color=#000000][back=#ffffff]~[/back][/color][size=13px][color=#000000]4.79[/color][/size][color=#000000][back=#ffffff]%之间[/back][/color],回收率[color=#000000]高[/color]、重现性良好[color=#000000],说明[/color][color=#000000]此方法适用于[/color]大体积自来水中阿特拉津、甲萘威、溴氰菊酯的富集、检测。
各位专家,大家好,我现在用GC112A分析乙酸丁酯和2,3-丁二醇,柱子用的是SE-30和SE-54,2,3-丁二醇沸点为181左右,乙酸丁酯为126.1,可是乙酸丁酯的峰在2,3-丁二醇后面,而且分离度不够,不能大于1.5,我采用了各种升温程序都不行,有谁能告诉我怎么办么??
WS/T 161-1999 作业场所空气中丙烯酸丁酯的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]测定方法 标准类别:国内食品标准 - 卫生标准 WS/T 161-1999 GB/T17092-1997 GB 8773-88 车间空气中丙烯酸甲脂卫生标准 谁有这些标准啊???、
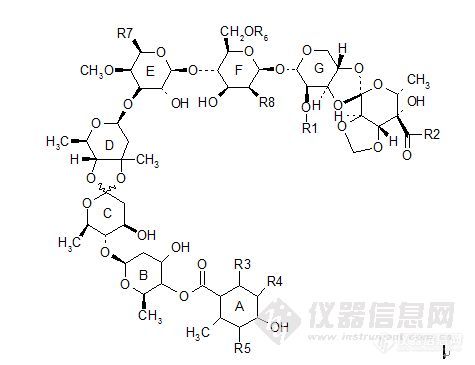
【中文名称】阿维霉素;卑霉素【英文名称】avilamycin;Surmax【结构或分子式】 http://ng1.17img.cn/bbsfiles/images/2012/03/201203112053_353986_1855403_3.jpg 【相对分子量或原子量】1404.24(阿维霉素A);1376.19(阿维霉素B)【用途】 主要对革兰氏阳性菌有效,而对革兰氏阴性菌效果差。其中以阿维霉素A的活性最高,特别是对梭菌、链球菌和杆菌有效;而阿维霉素B对葡萄球菌的活性最高。用量:用于4月龄以内的仔猪,每吨饲料20~40g;6月龄的猪每吨饲料加10~20g。【制备或来源】 由Streptomyces viridochromogenes发酵生产的甲基羟基甲氧基苯甲酸(DCIEA)的一种酯。是低聚糖抗生素orthosomycin类的总称。约有A、A′、B、C、D、D2、E、F、G、H、I、J、K等十多个组分。【生产单位】略
用凯氏定氮法测蛋白质时,最后滴定用0.05mol/l的硫酸标准滴定溶液或者0.05mol/l的盐酸标准滴定溶液滴定,这两种标液怎配制阿
有没有人搞过壬二酸的分析阿
关于乙醇、乙酸乙酯、甲基异丁酮、甲苯、丁酸乙酯、异戊酸乙酯、乙酸-2-甲基-1-丁醇酯、己酸乙酯、异戊酸异戊酯、异丁酸异戊酯、己酸烯丙酯、紫罗兰酮、肉桂酸异丙酯13种物质的气相方法,这13种物质能否一针全部出来,用什么柱子合适,FID对它们是不是都有响应?希望各路高手路过能留下点意见和相关资料,不胜感激!
分析氯甲酸乙酯,内标是乙酸异丁酯,固定液为DNP,请问该用什么载体合适?
(1)原理试样经处理后,在pH6左右的溶液中,镉离子与二硫腙形成配合物,并经乙酸丁酯萃取分离,导入原子吸收仪中,原子化以后,吸收228.8nm共振线,其吸收值与镉含量成正比,与标准系列比较定量。(2)试剂 氨水、混合酸、1g/L二硫腙-乙酸丁酯溶液(称取0.1g二硫腙,加10mL三氯甲烷溶解后,再加乙酸丁酯稀释至100rnL,临用时配制)、2mo1/L柠檬酸钠缓冲液(称取226.3g柠檬酸钠及48.46g柠檬酸,加水溶解,必要时加温助溶,冷却后加水稀释至500mL,临用前用1g/L二硫腙-乙酸丁酯溶液处理以降低空白值)、镉标准储备溶液和标准使用液的配制与碘化钾-4-甲基戊酮-2法中的相同。(3)仪器原子吸收分光光度计。(4)分析步骤①试样处理对于谷类要去除其中的杂物及尘土,必要时除去外壳。对于豆类,取可食部分洗净晾干,切碎充分混匀。②样品消化称取5.00g上述试样,置于250mL高型烧杯中,加15mL混合酸,盖上表面皿,放置过夜,再于电热板或电砂浴上加热。消化过程中,注意勿使干涸,必要时可加少量硝酸,直至溶液澄明无色或微带黄色。冷后加25mL水煮沸,除去残余的硝酸至产生大量白烟为止,如此处理两次,放冷。以25mL水分数次将烧杯内容物洗入125mL分液漏斗中。取与处理样品相同量的混合酸、硝酸按同一操作方法做试剂空白试验。③萃取分离 吸取0、0.25mL、0.50mL、1.50mL、2.50mL、3.50mL、5.0mL镉标准使用液(相当于0、0.05μg、0.1μg、0.3μg、0.5μg、0.7μg、1.0μg镉)。分别置于125mL分液漏斗中,各加盐酸(1+11)至25mL。向试样品处理溶液、试剂空白液及镉标准溶液各分液漏斗中各加5mL柠檬酸钠缓冲液(2mol/L),以氨水调节pH至5~6.4,然后各加水至50mL,混匀。再各加5.0mL二硫腙-乙酸丁酯溶液(1g/L),以氨水调节pH至5~6.4,然后各加水至501mL,混匀。再各加5.0mL二硫腙-乙酸丁酯溶液(1g/L),振摇2min,静置分层,弃去下层水相,将有机层放入具塞试管中,备用。④测定测定方法与碘化钾-4-甲基戊酮-2法中的相同。⑤结果计算 样品中镉的含量按下式进行计算。X=/(m×1000)式中,X为试样中镉的含量,mg/kg;A1为测定用试样液中镉的质量,μg;A2为试剂空白液中镉的质量,μg;m为试样质量或体积,g或mL。计算结果保留两位有效数字。⑥精密度 在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的15%。
关于游离脂肪酸检测,我将游离脂肪酸丁酯化处理,使用硫酸/正丁醇然后发现检测结果丁酸丁酯含量很高,我做了空白以及拿没有丁酸的标品做丁酯化都发现有丁酸丁酯,这丁酸丁酯是怎样产生的啊?有什么方法避免这种情况发生?丁酸是我很重要的目标分析物这样就很难对其定量。(我完成了丁酯化的[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]GC-MS[/color][/url]方法开发换方法不可能了)急需大神解答。
请问大家都是用什么方法检测没食子酸丙酯的含量的阿?偶现在用的是国标,采用的是分光光度计显色法,没食子酸丙酯标准物显色为紫黑色,可是我的样品按照国标处理后最后显色呈橙黄色,在540nm下仍旧有一定的吸光值,请问这样的检测结果能是正确的结果吗?如果有用[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]检测的,请问你们的处理条件和检测条件是什么呢?
请问,1000克含有35%甲苯40%乙酸丁酯15%乙酸乙酯10%乙醇的有机溶剂可以溶解多少克硝酸纤维素酯?如果要减小以上溶液的表面张力在不改变溶液透明有光泽的前提下,应该加哪一种表面活性剂?
长风破浪会有时,直挂云帆济沧海。出处 《 行路难》【唐】李白金樽清酒斗十千,玉盘珍羞直万钱。停杯投箸不能食,拔剑四顾心茫然。欲渡黄河冰塞川,将登太行雪满山。闲来垂钓碧溪上,忽复乘舟梦日边。行路难,行路难,多歧路,今安在。长风破浪会有时,直挂云帆济沧海。试验方法与步骤:精密称取本品内容物细粉适量(约相当于阿德福韦酯20mg),置20ml量瓶中,加4ml乙腈,振摇使溶解,并用0.05mol/L的磷酸二氢钾溶液稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液;精密量取供试品溶液1ml,置200ml量瓶中,加溶剂稀释至刻度,摇匀,作为对照溶液。照高效液相色谱法(中国药典2010年版二部附录 V D)测定,用十八烷基硅烷键合硅胶为填充剂;流动相A为0.05mol/L的磷酸二氢钾溶液,流动相B为乙腈;流速为每分钟1.0ml,按下表进行线性梯度洗脱;检测波长为216nm,分别取阿德福韦对照品、阿德福韦单酯对照品和阿德福韦酯对照品适量,用溶剂溶解并定量稀释制成每1ml中约含阿德福韦5μg、阿德福韦单酯20μg和阿德福韦酯10μg的混合对照品溶液,取10μl注入液相色谱仪,记录色谱图,阿德福韦酯峰的保留时间约为15分钟,理论板数按阿德福韦酯峰计算应不低于10000,阿德福韦、阿德福韦单酯和阿德福韦酯三者之间的分离度应符合规定。取对照溶液10μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%,立即精密量取供试品溶液、对照溶液和混合对照品溶液各10μl,分别注入液相色谱仪,记录色谱图。供试品溶液色谱图如有杂质峰,除溶剂峰外,阿德福韦按外标法以峰面积计算,不得过0.5%;阿德福韦单酯按外标法以峰面积计算,不得过2.0%;其他单个杂质峰面积不得大于对照溶液主峰面积(0.5%);其他各杂质峰面积的和不得大于对照溶液主峰面积的4倍(2.0%)。时间(分钟)流动相A(%)流动相B(%)0802018020106040256040303565403565458020508020色谱柱信息:Ultimate xB-C18 4.6*250 PN:00201-31043 SN:211202195典型色谱图:h
摘 要 本文以去离子水为萃取剂,通过加电膜萃取装置萃取了乙酸丁酯中的无机阴离子。在600V直流电压的作用下,8 ml乙酸丁酯中的四种无机阴离子通过聚丙烯中空纤维膜孔内的有机液膜进入膜内的100 μl 去离子水中。萃取完成后,使用离子色谱对萃取液进行分析。本文优化了影响萃取过程的因素,如施加电压、搅拌速度以及萃取时间。最佳萃取条件为:施加电压为600V,搅拌速度为600rpm,萃取时间为5分钟。该方法成功应用于乙酸丁酯实际样品的测定,无机阴离子的线性范围为0.01 mg/L-1mg/L,加标回收率为97-102%。实验结果表明,该方法快速有效,并可应用于其他微溶性有机物中无机阴离子的测定。关键词 无机阴离子;乙酸丁酯;加电中空纤维膜萃取;离子色谱 最近15年来,中空纤维膜萃取技术作为一种样品前处理方法,被广泛应用于环境分析、药物分析以及食品和饮料检测等重要领域。中空纤维膜萃取技术具有样品无需处理即可直接进样,对分析物具有预富集作用,基体消除,成本低廉,易与气相色谱、高效液相色谱、毛细管电流和离子色谱联用等优点。但分析物穿透中空纤维膜壁上的支撑液膜的运输机理是基于被动扩散,因此,常常需要花费超过30分钟甚至长达一小时的时间才能达到萃取平衡。为了克服传统的中空纤维膜萃取技术耗时的缺点,2005年挪威的Pedersen-Bjergaard和Rasmussen首次提出了一种称为加电中空纤维膜萃取的新型样品前处理方法。短短5分钟内,碱性药物在300V直流电压的作用下能够成功地穿过一层薄薄的有机液膜进入到300 μl 接收相中。与传统基于被动扩散的膜萃取技术相比,电动力迁移在加电中空纤维膜萃取中起到了主导作用,因此在很短的时间内就能取得良好的萃取效果。随后,Pedersen-Bjergaar小组又将这种新型的加电中空纤维膜萃取方法应用于更多种类的碱性药物、酸性药物、肽类和氯酚类物质的萃取 。他们建立了加电中空纤维膜萃取过程的理论模型并考察了影响加电中空纤维膜萃取效率的参数 。此外,新加坡的Lee小组使用加电中空纤维膜萃取技术从羊水、血清、口红和尿样中萃取了铅离子。目前为止,加电中空纤维膜萃取技术一直应用于液-液-液三相萃取体系,而本实验首次将加电中空纤维膜萃取应用于液-液两相萃取体系。我们曾经使用在线中空纤维膜萃取-离子色谱法测定了乙酯乙酯的无机阴离子,但该方法的萃取时间长达半小时,并且使用了柱切换技术,装置复杂,操作繁琐,仪器成本高。而本实验使用加电中空纤维膜萃取技术仅需要短短5分钟就能完成萃取,并且装置简单,操作简便,成功应用于乙酸丁酯中无机阴离子的测定。
乙酸对叔丁基环己酯 和乙酸邻叔丁基环己酯如何区分?谢谢
我们在做阿奇霉素的释放度的检测,具体的方法是0.1mol/L的盐酸2小时,然后再加入0.2mol/L的磷酸盐,调节Ph至6.8,45分钟,去溶液适量,滤过,去续滤液1ml,加0.1mol/L的盐酸4ml,加硫酸(75→100)5ml,显色,放冷后在测紫外!我们遇到的问题是,加硫酸后不显色!!后来也确定了是磷酸盐的问题,我想问的是磷酸盐是怎么对显色反应起到干扰作用的,(有问题的磷酸盐是能够把药品完全溶解的),同时还想问的是:加入硫酸显色的原理是怎样的!
老师你好,在微波消解这方面我是个新兵,求教各位微波消解后如何赶酸?(在消解罐中不加水赶?罐中加水赶?消解液倒至三角瓶中加水赶?)酸度如何控制?(消解液中的液体主要是酸吗?)如何定容(用载流定容还是纯水定容)?样品消解不完全如何处理?(是否同一批次消解完全样品也需要处理?),我要做的是食品样品中的砷、铅、镉、汞等。另外,消解后的样品检测结果不平行,空白也不平行是何原因?回收率也很低?
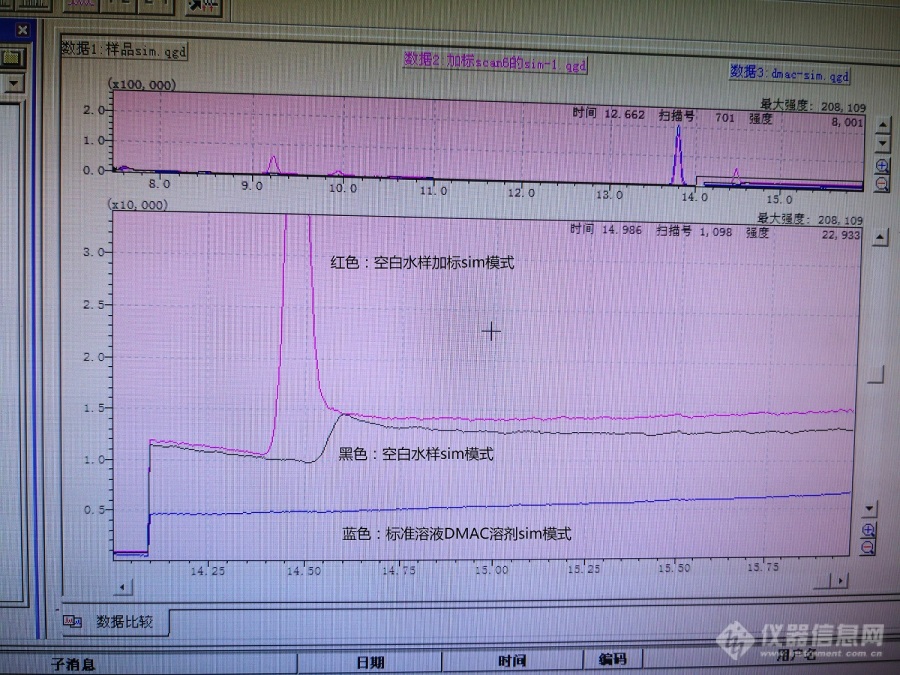
[font=宋体]用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]新建水样中乙酸丁酯等检测方法,柱子[/font]wax[font=宋体],程序升温[/font]60[font=宋体]℃([/font]8.5min[font=宋体])[/font]-5[font='微软雅黑','sans-serif']℃[/font][font='微软雅黑','sans-serif']/min-70℃-10℃/min-200℃-20℃/min-250℃[/font][font=宋体]([/font][font='微软雅黑','sans-serif']5min[/font][font=宋体]),乙酸丁酯出峰时间[/font][font='微软雅黑','sans-serif']14.6min[/font][font=宋体]。用母液(溶剂[/font][font='微软雅黑','sans-serif']DMAC[/font][font=宋体])进样峰型都很好。但是进样线性溶液(取母液用水稀释)、加标样品(母液加水样)以及溶剂水,基线就会在乙酸丁酯位置出现突越(见下图[/font][font='微软雅黑','sans-serif']14.6min[/font][font=宋体])。调整升温速率,突越总是跟乙酸丁酯一起。也老化过柱子,没有改善。请教各位老师,该突越是基线问题还是有杂质干扰,该如何去除。[/font][font=宋体][img=,656,491]https://ng1.17img.cn/bbsfiles/images/2020/03/202003261051583378_4789_2332103_3.jpg!w690x517.jpg[/img][/font]
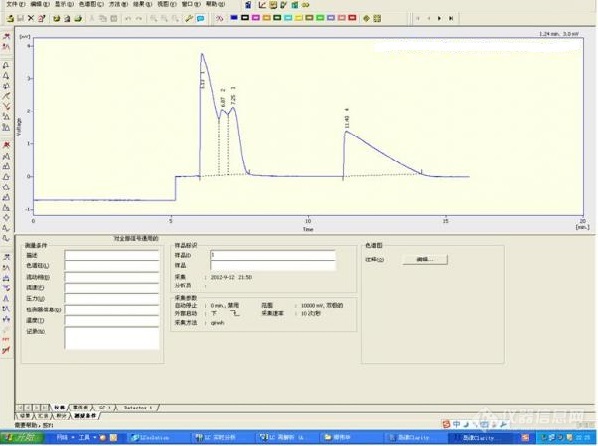
[color=#444444] 体系:[/color][color=#444444]乙酸/正丁醇/乙酸正丁酯/水;[/color][color=#444444]质量分数:均为25%[/color][color=#444444]沸点:乙酸119℃,正丁醇118℃,乙酸正丁酯126℃,水100℃。[/color][color=#444444] 分析条件:[/color][color=#444444]1. 色谱柱:DB-FFAP (30×0.25×0.25)[/color][color=#444444]2. 检测器:TCD[/color][color=#444444]载气流量:N2,0.25ml/min[/color][color=#444444]进样口温度:150℃[/color][color=#444444]柱温箱温度:120℃[/color][color=#444444]检测器温度:220℃[/color][color=#444444]图上可以看出:[/color][color=#444444]1, 基线发生瞬间跳动,一般基本上是漂移吧,为什么我这会突然发生阶跃式的跳动?分析原因是不是载气流量太低,可能载气流量发生不稳定,导致基线发生跳动?[/color][color=#444444]2, 由于有四元组分,前三个峰没有完全分开,而色谱柱分离效率跟载气流量,柱温关系最大,载气流量已经很低了,而且柱温也低于乙酸正丁酯的沸点,是不是也不能再低了。考虑能不能采用程序升温的方法,有没有可能将峰分开?如果可以的话,程序升温建议应该如何设置?[/color][color=#444444]求高手。[/color][color=#444444][img=,598,446]https://ng1.17img.cn/bbsfiles/images/2019/09/201909271014211801_6141_1752329_3.jpg!w598x446.jpg[/img][/color]
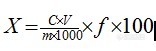
[align=center]医用胶中α-氰基丙烯酸正丁酯的测定[/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]品控部:赵杨瑞[/align][b]1.原理[/b] 试样经二氯甲烷溶解定容,采用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]测定,保留时间定性,峰面积外标法定量。实验方法参考史迎杰等[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱法测定医用胶粘剂中α-氰基丙烯酸正丁酯的含量。[b]材料与方法[/b]2.1仪器设备 [url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]:配FID检测器,分析天平:感量为0.0001g 。2.2试剂二氯甲烷:分析纯。α-氰基丙烯酸正丁酯标准品。[b]试样处理[/b]3.1 样品配制:准确称取样品50mg(精确至0.00001g),置于50mL容量瓶中,加入二氯甲烷溶解定容,摇匀。3.2[b] [/b]色谱条件:3.2.1色谱柱:(5%-苯基)-甲基聚硅氧烷为固定相的毛细管色谱柱,柱长30m,内径0.25mm,膜厚0.25μm或同种极性的色谱柱;3.2.2流速:1.0mL/min ;3.2.3进样体积1.0μL;分流比:50:1。3.2.4柱温:程序升温,初始温度120℃保持3 min,以5℃/min的速率升温至180℃,保持2 min;进样口温度:120℃;检测器:200℃。3.3外标法计算公式:[align=center][img=,156,51]http://ng1.17img.cn/bbsfiles/images/2017/09/201709110853_01_2904018_3.png[/img][/align]式中:X-样品中α-氰基丙烯酸正丁酯的含量,% C-由标准曲线所得样品溶液各组分浓度,mg/ mL; V-定容体积,mL;m-称样质量g;f-稀释倍数。 两次测试结果的相对误差小于10%即为测试平行。[b]4实验结果[/b]4.1外标法标准曲线线性的确定准确称量α-氰基丙烯酸正丁酯标准品约105mg,精密称定,置于10 mL容量瓶,加入二氯甲烷溶解定容,摇匀,配置成浓度为10.5mg/ml的标准品储备液,再精密配制成8.0mg/mL,4.0mg/mL,2.0mg/mL,1.0mg/mL的标准品溶液,置于进样小瓶中,密封。测定氰基丙烯酸正丁酯浓度与峰面积的相关性,确定相关系数及线性范围,标准曲线见图1。可见,α-氰基丙烯酸正丁酯在1.0-10.5mg/mL范围内,Y=227330X-124184,R[sup]2[/sup]=0.9976506;含量与色谱峰面积呈显著的线性关系,可满足定量分析的需要。[align=center][img=,610,423]http://ng1.17img.cn/bbsfiles/images/2017/09/201709110854_01_2904018_3.png[/img][/align][align=center] 图1 α-氰基丙烯酸正丁酯标准曲线[/align]4.2检出限取0.5mg/mL和1.0mg/mL标准溶液梯度稀释进样,至S/N=3±1,确定出α-氰基丙烯酸正丁酯的最低检出限0.5%。4.3加标回收及重复性 对样品进行加标回收实验,加标浓度设1.0mg/mL,回收率结果见图2,可见对样品进行的加标回收率在95.8%左右。对样品进行重复性实验结果见图3,结果可见,RSD为1.011%,由图2和图3结果表明本实验方法能够满足分析要求。[align=center][img=,575,101]http://ng1.17img.cn/bbsfiles/images/2017/09/201709110855_01_2904018_3.png[/img][/align][align=center]图2 α-氰基丙烯酸正丁酯样品加标回收率结果[/align][align=center][img=,586,451]http://ng1.17img.cn/bbsfiles/images/2017/09/201709110855_02_2904018_3.png[/img] [/align][align=center] 图3 α-氰基丙烯酸正丁酯重复性实验[/align][align=left][b]5.结论[/b][/align]综上所述:医用胶中α-氰基丙烯酸正丁酯的测定方法学从线性、重复性、回收率、准确度、最低检出限均符合分析要求。本方法的α-氰基丙烯酸正丁酯的检出限为0.5%,本方法可以用于医用胶中α-氰基丙烯酸正丁酯的测定。
我用的是岛津GC-14C型的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url],检测器是FID,柱子是SGE的AC10(中等极性),工作站是浙大N2000,现要测定丁酸,溶剂为乙醚,我设置的仪器参数如下:COL为100, SPL为180, FID为200。进样后发现只有乙醚的峰,丁酸不知道去那里了,不知道有哪位前辈做过,给我指点一下,谢谢!!