做荧光检测时,需要配置各种氨基酸不同浓度的溶液,在配制时有的不溶于水中,如何解决?
有人知道荧光增白剂2氨基2苯乙烯含量如何测定吗
摘 要:目的:用高效液相柱后衍生荧光检测系统测定水果、蔬菜中氨基甲酸酯类农残的残留量;方法:采用甲醇:水为流动相梯度洗脱,Ultimate XB-C18, 4.6×250mm,5μm色谱柱分离,激发波长为330nm、发射波长为465nm;结果:该方法平均回收率为72.91%~114.96%,RSD为1.094%~1.377%,在信噪比S:N=3的条件下,其空白回收检测限在0.01~0.06ppm范围内。结论:该方法对水果、蔬菜中氨基甲酸酯农残含量结果稳定,重现性好,可操作性强,适用于水果、蔬菜中氨基甲酸酯农残残留量的定性定量检测。关键词:氨基甲酸酯;水果、蔬菜;高效液相色谱法氨基甲酸酯类农药是目前我国使用量较大的杀虫剂之一,是继有机磷、有机氯类农药后发展较为迅速的一类高效、广谱杀虫剂,主要应用于粮食、蔬菜和水果上。氨基甲酸酯类杀虫剂的杀虫作用机制为抑制昆虫神经传导的重要物质乙酰胆碱酯酶,氨基甲酸酯类农药进入虫体后 ,与乙酰胆碱酯酶结合 ,形成氨基甲酰化酶 ,使乙酰胆碱酯酶无法水解乙酰胆碱,致使神经突触部位乙酰胆碱大量积累,对突触后膜产生连续不断的刺激作用,昆虫在连续不断的神经刺激下,出现兴奋、痉挛、最后瘫痪、死亡。其具有较强的杀虫效果、分解速度快、代谢迅速,残留期短等特点,此外还常被作为杀菌剂、除草剂和生长调节剂。由于其广泛利用于各种农作物,残留在蔬菜、水果等农作物的氨基甲酸酯类农残严重危害到人体的健康,同时也对地下水产生了严重的污染。本方法在国标NY/T 781 -2008蔬菜和水果中有机磷、有机氯、拟除虫菊酯和氨基甲酸酯类农药多残留的测定的基础上,结果公司的高效液相色谱仪LC310仪器特点,优化色谱条件,重新研究建立了测定水果、蔬菜中氨基甲酸酯类农残检测的高效液相柱后衍生色谱法,该方法简便、快速,实用性强,回收率良好,检测结果稳定可靠。1 实验:1.1 仪器和试药1.1.1 仪器 LC310高效液相色谱仪(包括LC-P310高压恒流泵、FLD荧光检测器、柱后衍生泵,水解泵,均为江苏天瑞仪器股份有限公司产品);电子天平(赛多利斯);超声波清洗器(张家港神科超声);超纯水机(南京易普易达);食品加工器;匀浆机;氮吹仪。1.1.2 试剂氨基甲酸酯农残对照品(浓度均≥96.00%);固相萃取柱;OPA稀释液、邻苯二甲醛、氢氧化钠、巯基乙醇,均为分析纯;甲醇、乙腈、二氯甲烷(色谱纯);氯化钠(140度烘烤4小时);水(超纯水,自制);水果、蔬菜购买至菜市场。注:柱后衍生试剂 OPA试剂制备:1.将945mlOPA稀释剂倒入试剂瓶,留5ml第五步用。2.盖上瓶盖,打开进气阀,开启气源。使惰性气体喷射满全瓶。持续冒泡10分钟3.将100mgOPA溶解于10ml色谱纯甲醇中。4.关闭气源,打开瓶盖。将OPA溶液倒入已经去氧的稀释液中。5.溶解2g巯基乙醇与第一步留下的5mlOPA稀释液中并倒入试剂瓶。6.盖上瓶盖,打开气源,使其喷射几分钟后关闭气阀。轻轻摇动试剂使其完全混匀。固相萃取柱:氨基柱(Aminopropyl),容积6mL,填充物500mg。1.2 色谱条件色谱柱:Ultimate XB-C18,4.6×250mm,5μm,月旭材料(上海)公司;流动相A:甲醇流动相B:水流速:0.8 ml/min柱温:30℃进样量:10μL荧光检测激发波长:330nm;发射波长:465nm;水解试剂0.05mol/L氢氧化钠;水解温度100℃;水解流速为0.3mL/min衍生试剂OPA;衍生温度35℃;衍生流速为0.3mL/min时间梯度程序如下:T(min)流动相A流动相B030701045[align
各位师兄师姐,有没有拿二级测氨基糖苷类(我做庆大霉素、依替米星和阿米卡星)吗?柱子和流动相用的什么呀?七氟丁酸实验室不给用,HPLC实验室只有紫外和荧光检测器,不能做ELSD和FID。我的课题刚上手,好多不太懂,老师催着摸方法,好纠结。。。谢谢各位师兄师姐~
大家好。我想问一下。 我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC 的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
有人检测过氨基寡糖素吗,有什么好方法吗,谢谢
大家好。我想问一下。 我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC 的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊 同时我还想问一下氨基和异硫氰基的反应原理及条件?
大家好。我想问一下。 我的做1,4-对氨基苯与FITC(异硫氰酸荧光素)反应的时候。其条件完全是按照蛋白质的氨基与FITC的条件。即氨基与异硫氰根的反应条件进行的。但是却标记不上。不知道是不是苯环上的氨基具有惰性?还是反应条件不适合?有哪位高手指教一下!谢谢啊
1 主题内容与适用范围 本标准规定了用 2,3-二氨基萘(DAN)荧光法测定饲料中硒的方法。 本标准适用于配合饲料、预混合料、浓缩饲料和单一饲料中硒的测定。在萃取液中检测范围为 0.001~0.1 μ g/ mL (以Se计)。 2 引用标准 GB 1.4 标准化工作导则 化学分析方法标准编写规定 GB 6682 实验室用水规格 3 方法原理 先将试样中有机物破坏,使硒游离出来,在微酸性溶液中硒( IV)和2.3-二氨基萘(DAN)生成4.5-苯基苯并硒二唑,用环己烷直接在生成络合物的同一酸度溶液中萃取,用荧光光度计测定其荧光强度。 4 试剂 实验室用水应符合 GB 6682中二级用水的规格,使用试剂除特殊规定外,应为分析纯。 4.1 高氯酸 优级纯( ρ 1.67g/ mL )。 4.2 硝酸 优级纯( ρ 1.42g/ mL )。 4.3 环己烷 ρ 0.778~0.80g/ mL 。 4.4 盐酸 优级纯(1+3)。 4.5 盐酸 C ( HCl ) =0.1mol/L。 4.6 氨水 ρ 0.90g/ mL 。 4.7 盐酸羟胺-乙二胺四乙酸二钠(EDTA)溶液 称取 10gEDTA溶于500mL水中,加入25g盐酸羟胺使其溶解,用水稀至1000mL。 4.8 2,3-二氨基萘(DAN)溶液 称取 DAN0.1g于150mL烧杯中,加入100mL0.1mol/L盐酸使其溶解,转移到250mL分液漏斗,加入20mL环己烷(4.3)振荡1min,待分层后弃去环己烷,水相重复用环己烷处理2~3次。水相放入棕色瓶中上面加盖3mm厚的环己烷,于暗处保存,此液可使用数周。 4.9 硒标准贮备溶液 称取硒粉(纯度 99%以上)25mg(精确至0.01mg),入100mL烧杯中,加入10mL硝酸加热溶解,冷至室温,用水转移至1000mL容量瓶中并稀至刻度,摇匀,此液 1mL含25.00 μ g的硒。 4.10 硒标准工作溶液 吸取( 4.9)溶液1.00mL、入50mL高型烧杯中按分析步骤消化至高氯酸冒烟 5min,取下稍冷,加1mL水和1mL盐酸(4.4)摇匀,放置10min用盐酸(4.5)转移至250mL容量瓶中并稀至刻度摇匀,此液1.00mL含硒0.1μg。 4.11 甲酚红 0.4g/L水溶液,称取0.1g甲酚红入400mL烧杯中,加少许水加氨水(4.6)使其溶解用水稀至250mL,摇匀。 5 仪器、设备 5.1 荧光光度计 激发波长 365~385nm,荧光发射波长520~525nm,1cm石英比色杯。 5.2 实验室用样品粉碎机 标准分析筛孔径( 0.42、0.25mm)。 5.3 分析天平分度值0.0001g。 5.4 可调温电炉(600W)或电热板(3000W)。 5.5 高型烧杯50mL和相应大小的表面皿。 5.6 具塞比色管50mL。 5.7 刻度吸量管2mL、10mL。 6 试样的制备 取已粉碎至 0.42mm的试样40~50g入250mL烧杯中加水至能搅动的糊状,在搅拌器上搅10~15min,倒在小搪瓷盘中铺平,放入烘箱70℃烘干,粉碎机上磨至0.25mm,混匀装入密封容器中备用,防止试样成分变化。 7 分析步骤 7.1 试样测定(配合饲料、浓缩料、单一饲料) 称取已制备好的试样约 1g,精确至0.0001g(≤0.4 μ gSe),放入50mL高型烧杯中,用少量水润湿试样加硝酸(4.2)10mL,轻摇烧杯使试样散开,加盖表面皿放到电热板(5.4)上低温加热见反应开始(泡沫开始上冒),切断电源或取下待剧烈反应缓解(气泡不上涌)后再放到电热板上煮沸至硝酸体积减少到5mL左右,取下稍冷加入5mL高氯酸(4.1)继续加热至剧烈小气泡冒完,高氯酸冒烟;取下稍冷,用水吹洗表面皿和杯壁,去掉表面皿,将烧杯置电热板上先低温蒸发水分,再升温至高氯酸冒烟并保持5~10min,取下稍冷,加入1mL水和1mL盐酸(4.4),摇匀,放置10min,水稀至30mL左右,加二滴甲酚红(4.11),用氨水(4.6)中和至黄色,再用盐酸(4.4)中和至橙色(pH1.5~2),加入3mL盐酸羟胺溶液(4.7)摇匀,用盐酸(4.5)转移到50mL比色管中(5.6),加2mLDAN 溶液(4.8),盖好塞子,摇匀,松动塞子,置于100℃水中保持5min。取出放入冷水中迅 速冷却至室温,用盐酸(4.5)稀至50mL,加5mL环己烷(4.3)振荡1min,静置分层后,用吸管小心吸取上部环已烷入1cm石英杯中,置入荧光光度计内于激发波长375~380nm,发射波长520~525nm测其荧光强度,在标准曲线上查得试料中硒的含量。 同时做空白试验(消化时应戴防护眼镜)。 7.2 高含量硒样品(预混合料)的测定 对于每千克含硒在 1mg以上含有机物的样品,按(7.1)进行至加入1mL水和1mL盐酸(4.4)摇匀,放置10min后将消化液稀释至足够体积,然后取部分溶液(Se≤0 .4 μ g)进行测定。对于以石粉为载体的预混料,称取1~5g样品(精确到0.0001g),于 250mL烧杯中,加入20mL水和25mL硝酸(4.2)(逐滴加入硝酸至气泡不发生后再全部加入),盖表面皿,置电热板上煮沸,低温沸腾30min,取下冷却,用水转移到100~500mL容量瓶中稀释至刻度,摇匀,取部分澄清液(Se≤0.4 μ g)入50mL高型烧杯中,加入5mL高氯酸(4.1),以下按7.1 加高氯 酸后程序进行。 7.3 工作曲线的绘制 取 0.00,0.50,1.00,1.50,2.00,3.00mL硒标准溶液(4.10),分别入50mL具塞比色管中,加入3mL盐酸羟胺溶液(4.7)、2滴甲酚红指示剂(4.11),以下按7.1用氨水中和起操作进行,以下按7.1用氨水中和起操作进行,以硒量为横坐标,荧光强度为纵从标,绘制工作曲线。 8 分析结果计算和表述 硒的含量( mg/kg)按下式计算: Se ( mg/kg)= m 1 V 0 /( m 0 V 1 ) 式中: m 1 ── 自工作曲线上查得的硒量,μ g; V 0 ── 试液的总体积, mL ; V 1 ── 分取试液的体积, mL ; m 0 ── 试料的质量, g。 所得结果应表示至三位小数: 0.001mg/kg。 9 允许差 室内每个试样应称两份试料进行测定,以其算术平均值为分析结果,其间分析结果的相对偏差应不大于下表所列允许差。 硒含量,mg/kg 允许偏差,% ≤0.100 40 >0.100~0.200 30 >0.200~0.400 20 >0.400 15
PCR荧光仪和全自动氨基酸分析仪各用什么来表示仪器的技术指标?
1.1概述1.1.1氨基酸基本的理化性质 一、基本物理学性质 包括基本组成和结构、溶解性、酸碱性质、立体化学、熔点、沸点、光学行为、旋光性、疏水性等。 (一)溶解性质根据氨基酸侧链与水相互作用的程度可将氨基酸分作几类。含有脂肪族和芳香族侧链的氨基酸,如Ala、Ile、Leu、Met、Pro、Val及Phe、Tyr,由于侧链的疏水性,这些氨基酸在水中的溶解度均较小;侧链带有电荷或极性集团的氨基酸,如Arg、Asp、Glu、His、Lys和Ser、Thr、Asn在水中均有比较大的溶解度;但根据电荷及极性分析也有一些例外,如脯氨酸属于带疏水基团的氨基酸,但在水中却有异常高的溶解度。 (二)氨基酸的疏水性 氨基酸的疏水性,是影响氨基酸溶解行为的重要因素,也是影响蛋白质和肽的物理化学性质(如结构、溶解度、结合脂肪的能力等)的重要因素。 按照物理化学的原理,疏水性可被定义为:在相同的条件下,一种溶于水中的溶质的自由能与溶于有机溶剂的相同溶质的自由能相比所超过的数值。估计氨基酸侧链的相对疏水性的最直接、最简单的方法就是实验测定氨基酸溶于水和溶于一种有机溶剂的自由能变化。 一般用水和乙醇之间自由能变化表示氨基酸侧链的疏水性,将此变化值标作△G′。 不同氨基酸的△G′值如下表所示。当氨基酸的△G′值为正时,其侧链具有疏水性,倾向于处在蛋白分子的内部; △G′为负时,其侧链是亲水的,倾向于处在蛋白分子的表面。需要注意的是,赖氨酸通常是蛋白质分子中亲水性的氨基酸残基,但它的△G′是正值,这是由于它的侧链含有优先选择有机环境的4个-CH2-基。 (三)氨基酸的光学性质 氨基酸中的苯丙氨酸、酪氨酸、色氨酸分子中由于有共轭体系,因此可以吸收近紫外光。它们的最大吸收波长(λmax)分别为260nm、275nm、278nm;在吸收最大波长光线的时候还会发出荧光。
液相色谱柱后衍生荧光检测做氨基甲酸酯为何同一浓度的对照品每3小时间隔进样,发现对照品峰面积越来越低,从原来的15934858,变成10334905。新配了对照品还是不行。因为连续进样了3天,会不会是仪器的原因??仪器也需要休息了啊??
各位大侠:新来小弟请教各位,氨基酸全自动分析仪能否检测氨基酸里面的微量元素?谢谢!
[color=#444444]自动氨基酸分析仪测素丸子里的氨基酸的样品前处理的方法 或者同类也行[/color]
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=155679]小麦籽粒氨基酸碳氮稳定同位素的测定与分析[/url]………………………………………………………………………………[color=#00008B]【目的】利用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-燃烧-同位素比值质谱仪(gas chromatography-combustion-isotope ratio masss pectrometry,GC-C-IRMS)测定小麦籽粒氨基酸碳氮稳定同位素组成。【方法】以小麦临汾50744为材料,水解得到其籽粒蛋白质氨基酸,将氨基酸标准样品以及小麦籽粒氨基酸衍生化为N-新戊酰基,O-异丙醇(N-pivaloyl-isopropyl,NPP)氨基酸酯,利用GC-C-IRMS测定其碳氮稳定同位素组成。【结果】氨基酸标准样品的碳氮同位素组成分析表明,NPP氨基酸酯的平均重现性δ^13C为0.47‰,δ^15N为0.28‰,并没有产生大的同位素分馏,因此δ^13C和δ^15N都能得到满意的测定结果。运用GC-C-IRMS测定了小麦临汾50744籽粒蛋白质氨基酸的稳定碳氮同位素的自然丰度,其中δ^13C的变化范围在-28.7‰到-34.7‰,δ^15N的变化范围为-6.2‰到9.5‰。采用系统聚类分析进行分类,根据δ^13C可以将氨基酸分为两类 根据δ^15N可以将氨基酸分为三类。【结论】运用GC-C-IRMS结合NPP氨基酸酯衍生物可以测定小麦籽粒氨基酸的稳定碳氮同位素,这对于揭示氨基酸代谢途径的差异以及逆境胁迫下氨基酸的合成差异具有重要的意义。[/color]
日本味之素氨基酸质量控制标准。就是俗称的AJI92。适合于氨基酸生产企业以及药厂原料入厂检验。以下是下载地址。http://www.instrument.com.cn/download/shtml/111107.shtml
在味精中添加甜蜜素(环己基氨基磺酸)后,为什么甜蜜素检测不出来?
请问有用氨基柱检测肾上腺素、去甲肾上腺素、多巴胺的吗氨基柱可以检测这些极性大的生物碱吗
精氨酸是机体蛋白合成的底物,并且可以转化为许多生物活性物质以调节细胞生化功能,精氨酸在增强机体的免疫力、细胞分裂、伤口复原、激素分泌、血管紧张性、胰岛素敏感度和内皮功能等各种生理过程中,也都有着重要的角色。中国科学院亚热带农业生态研究所印遇龙研究员带领的团队就精氨酸的研究与美国Texas A&M大学进行了长期合作,发现精氨酸是幼龄仔猪限制性氨基酸。但是精氨酸的吸收与赖氨酸等拮抗,因此,对精氨酸及其内源性合成调控研究具有极大的应用价值和实践意义。通过进行断奶仔猪动物实验,研究了精氨酸和精氨酸生素在提高仔猪生长性能和维护健康的作用。研究表明,与基础日粮组相比,添加精氨酸和精氨酸生素可以有效缓解仔猪断奶应激,促进肠道生长;精氨酸生素试验组仔猪腹泻率降低了18%。同时,试验结果还表明,精氨酸或者精氨酸生素通过促进肠道粘膜HSP70表达,防止肠道细胞凋亡,维护肠道粘膜形态。因此,精氨酸或精氨酸生素可以作为断奶仔猪日粮中一种功能性添加物,以提高仔猪的生长性能和维护仔猪肠道健康。在此基础上,中国科学院亚热带农业生态过程重点实验室自主研发了一种新型功能性氨基酸-精氨酸生素(AAA, Arginine activator additive)。该研究成果已于2010年8月发表在SCI收录期刊《氨基酸》(amino acids)39卷3期上
做水果蔬菜中氨基甲酸酯类农残用761方法过氨基柱,上液质检测,最近发现用的1.7um和1.6um的UPLC柱特别容易堵,不知道是不是色素除的不干净的原因,一般进两百多针就得换分析柱前面的筛板,要不压力就10000多PSI了
氨基酸分析技术的特点与内涵文章来源:国家产品质量安全与法信息中心网 添加时间:2009-7-19 3:13:19 点击:1510摘要:在传统蛋白质分析技术基础上,结合现代分析仪器技术发展优势,针对氨基酸分析技术难点及存在问题,概括比较分析评价当前氨基酸分析技术特点。关键词:蛋白质 氨基酸 分析技术 研究进展1 前言迄今为止,自然界中已发现180多种氨基酸,其中参与蛋白质合成的氨基酸只有20多种,称为基本氨基酸。氨基酸主要有两种存在形式,一种是以游离态存在于生理体液(血浆、尿)、食品(酒、饮料)中;另一种是以结合态存在于肽和蛋白质中。蛋白质在乳中含量为3.0%~3.5%,是乳的主要成分,对乳品的理化特性和营养价值有重要的影响。由于国标法对蛋白的检测是通过检测样品含氮量而得到的,实际上是将样品消化分解,经蒸馏碱吸收后,测定的挥发性“氨基氮”,因而部分不法商贩用添加外源动植物蛋白粉或脲等含氮化合物(虚“氮”)来增加原料乳的氮含量,钻传统检测方法表征“虚氮”的漏洞,以蒙混过关。这些掺入水解动物蛋白或者含氮化合物的乳粉因其氨基酸的组成不合理,根本不能代表动、植物蛋白,不易消化,所以营养价值低下,导致人体吸收利用率降低,严重地影响到婴幼儿的生长发育和智力水平。因此,对氨基酸分析方法的研究与改进逐渐得到各国家、全社会的高度重视。在一般情况下,质量监督检验单位在市场上抽到产品进行检验所得的数据中,蛋白质含量实际上是用总氮含量表示的,所以在加工企业常规检验时、含氮化合物、水解动物蛋白等杂蛋白是测不出来的,因此需要建立快速分析、测定乳制品中蛋白质、氨基酸的检测方法,保障乳制品的质量与安全。,1958年,Spackman等首先提出了用阳离子交换色谱与柱后茚三酮衍生结合的方法分析蛋白质中的氨基酸,实现了氨基酸分析的自动化。其后,人们不断地发展新的氨基酸分析方法,柱前衍生反相高效液相色谱法、高效阴离子交换色谱-积分脉冲安培检测法、毛细管电泳法、蛋白质芯片技术等相继应用于氨基酸分析。现已是多种氨基酸分析方法并存、互补。本文就目前应用于氨基酸分析的主要方法作一比较分析。,,2 氨基酸分析技术的光谱分析优势及特点利用光谱探针方法定量分析蛋白质的研究在国际上十分活跃,其中,对有机染料(包括显色剂和荧光染料)结合分光光度法和金属离子-有机染料(包括显色剂和荧光染料)结合分光光度法的研究倍受重视。 2.1 有机染料结合分光光度技术因为有机染料结合分光光度法测定蛋白质操作简便,比较灵敏,又不需特别的仪器,方法应用比较广泛。现在研究较多的可作为探针的染料分子中,大部分都含有带正电荷的亲水性基团如羟基、磺酸基、酚羟基及不带电荷的疏水性基团,如苯环。这类方法的基础是在溶液pH小于等电点时,蛋白质的肽键亚胺和N端氨基质子化成阳离子,若有阴离子染料存在时,由于电荷作用,蛋白质便与染料结合沉淀或改变结合染料的光吸收特性,借染料颜色的减褪或变化的程度测定蛋白质的含量。已经应用的染料有酸性橙红、考马斯亮蓝G-250、溴甲酚绿、溴甲酚紫、埃铬青R和溴酚蓝。2.2金属离子-有机染料结合分光光度技术近几年发展了利用金属离子和有机染料特别是荧光染料形成配合物体系结合光光度法来测定蛋白质含量。金属离子与含有-OH或C=O的有机染料相遇时,氧原子中的孤对电子可顺利进人杂化轨道,形成稳定的配合体系,在酸性条件下,该体系遇到结构不对称的蛋白质分子时,互相极化产生静电作用而结合成新的大分子团,改变了原体系的光谱性能,从而能定量测定蛋白质的含量。该方法具有灵敏度高、线性范围广、干扰离子少、操作简单、快速及适用于常规应用等特点。2.3 荧光光度分析技术荧光法是定量测定蛋白质的另一种常用方法通常比分光光度法更灵敏。常用的方法有内源荧光法、荧光探针法、荧光偏振、时间分辨荧光法及激光诱导时间分辨免疫分析法。2.3.1 内源荧光分析技术蛋白质中存在着Tyr、Trp、phe残基,能够吸收270~300 nm的紫外光而发出紫外荧光。当测定体系中加入小分子配体(SM)时,SM与蛋白质发生相互作用,会导致蛋白质荧光的猝灭,利用SM对蛋白质内源荧光的猝灭这一现象可以确定蛋白质与SM的作用类型及其结合部位等。2.3.2 外源荧光分析技术对于蛋白质的研究仅利用其内源荧光是不够的,需要通过外源荧光性质的研究才能获得更多关于蛋白质分子的各种信息,这就使得荧光探针对蛋白质分析有着极其重要的意义,这已成为蛋白质微量检测及溶液的构相分析中不可缺少的手段之一。在外源荧光法中,又可分为有机荧光探针法和稀土荧光探针法。作为一个好的荧光探针应满足以下条件:探针分子与蛋白质分子的某一微区必需有特异性的结合,并且结合比较牢固;探针的荧光必须对环境条件敏感;蛋白质分子与探针结合后不影响其原来的结构和特性。在满足这些条件的基础上可进行蛋白质的测定和与金属离子结合的计量化学等。与光度法类似,蛋白质在和某些具有荧光特性的染料结合后,能引起荧光强度的变化,并且在一定浓度范围内与蛋白质浓度成正比,因此可用于蛋白质的测定。利用这些化合物在不同蛋白质分子中量子产率、峰位及谱带的变化,就可探测蛋白质分子结合区的极性、疏水性的大小,从而推论构象的稳定情况及变化等。2.3.3 荧光偏振分析技术利用荧光体在转动扩散速度上的差异而导致偏振荧光的差别,建立了荧光偏振测定法。利用荧光偏振还可以研究:酶与荧光底物的结合程度;蛋白质聚合与解离;蛋白质从螺旋到无规卷曲的研究。,3 氨基酸分析技术的色谱分析优势及特点3.1 柱后衍生高效阳离子交换色谱分析技术高效阳离子交换色谱(HPCEC)-柱后茚三酮衍生光度检测分离测定氨基酸是一种经典的氨基酸分析方法。此方法是利用氨基酸在酸性条件下形成阳离子而在阳离子交换柱中分离,分离后的氨基酸用茚三酮衍生、紫外可见光检测器检测。该方法以阳离子交换树脂为固定相、酸性缓冲液流动相,在柱后流出液中加入茚三酮使氨基酸生成具有可见光吸收的衍生物进行检测,具有重现性好、仪器稳定、结果可靠、适合于大量常规样品分析等优点。另外,由于衍生化反应发生在氨基酸与其物质分离之后,因而避免了其他物质的干扰,适合复杂样品中氨基酸的分析。其缺点是仪器复杂、体积大、费用高。此外,由于脯氨酸的测定波长在440nm,而其他氨基酸的测定波长为570nm,因脯氨酸不能和其他氨基酸同时测定。氨基酸分析自动仪就是基于阳离子交换色谱分离、柱后茚三酮衍生光度检测技术设计的。商品化的自动氨基酸分析仪是在20世纪60年代初问世,目前的自动氨基酸分析仪已实现了程控自动化和数据处理电脑化,分析时间已缩短至1 h以内。氨基酸自动分析仪实际上属专门用来分析氨基酸的高效液相色谱仪,其优点是高压、快速、灵敏,试剂和样品用量少、重现性好、分析结果稳定。广泛用于食品、医学、农业以及微生物等领域。3.2 柱前衍生反相高效液相色谱分析技术近20年来,柱前衍生反相高效液相色谱法(RP-HPLC)分析氨基酸得到了迅速发展,逐渐取代柱后衍生高效阳离子交换色谱(HPCEC)在许多领域中的应用。RP-HPLC分析方法更加快速灵敏。与专业氨基酸分析的自动分析仪不同,HPLC仪适用性更广、更灵活。RP-HPLC要求将氨基酸在柱前转化为适于反相色谱分离并能被灵敏检测的衍生物,柱前衍生的关键在于衍生试剂的选择。选择衍生试剂的标准是能与各氨基酸定量反应,每种氨基酸只生成一种化合物且产物有一定的稳定性,不产生或易于排除干扰物,操作简单,色谱分离分辨率高、检测灵敏度高,分析时间短,便于实现自动化和使产物能在不同型号的高效液相色谱仪上测定。目前比较常用的柱前衍生试剂有邻苯二甲醛(OPA)、异硫氰酸苯酯(PITC)、氯甲酸芴甲酯(FMOC-Cl)及丹酰氯(Dansyl-Cl)。衍生后的氨基酸一般键合在C18柱上,利用液液分配原理进行分离。流动相多以乙酸盐或磷酸盐缓冲液为主,以乙腈、甲醇或四氢氟喃为调节剂。由于氨基酸衍生物仍保留着两性化合物的特点,除改变调节剂之外,还可通过调节缓冲液pH值、离子强度、柱温等使之达到理想的分离。当然,不同衍生物所选用的柱型、流动相以及氨基酸的洗脱时间和顺序不尽相同。柱前衍生反相高效液相色谱法可用于分析蛋白质水解液、生理体液和食品等样品中的氨基酸。当与质谱技术结合时,采用电离喷雾质谱(ESI-MS)或电离喷雾串联质谱(ESI-MS/MS)联用技术方式,借助计算机的联机检索,可以实现高通量筛选和鉴定蛋白质混合体系。目前,,蛋白质组研究的高效液相色谱-质谱联用的方式有一维色谱-质谱联用技术、多维色谱-质谱联用技术以及亲和色谱-质谱联用技术等。一维色谱-质谱技术仅能分析一些不太复杂的蛋白质体系,而对复杂的多肽混合物常不能满足分离的要求。多维色谱分离的方法在某种程度上满足了对复杂蛋白质混合分离鉴定的要求。,,,3.3 两种氨基酸直接分析技术大多数氨基酸不具备生色团,因此无法利用分光光度法直接检测,故需采用化学衍生技术,使之生成可在紫外或可见光区有吸收的化合物,或者采用荧光法检测。但对于分析工作者来讲,尤其是在新化合物研制的过程中,面对多种未知的降解物,如采
下载了好多有用的资料,也尝试做点贡献,呵呵。不过我是新人,好像还不能发附件....有需要的和正在做或者想做的,留下邮箱我会尽快把资料给你发过去的有分析氨基酸、氨基甲酸酯、黄曲霉素、草甘膦与甲氨磷酸AMPA、氨基糖苷类抗生素、多种残留霉菌毒素、生物多胺、水中百草枯和杀草快、聚醚类抗生素、贝类毒素、PKU与MSUD、磺胺类物质、溴酸盐、甲醛,不同物质方法不同。最好写下你需要哪一种的。[color=#DC143C][B]hotdoglet:非常感谢楼主的慷慨分享![/B][/color]
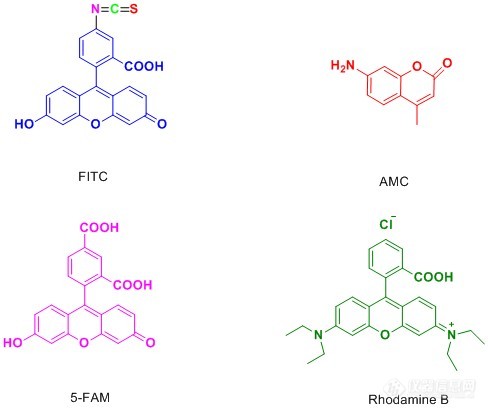
荧光标记所依赖的化合物称为荧光物质。荧光物质是指具有共轭双键体系化学结构的化合物,受到紫外光或蓝紫光照射时,可激发成为激发态,当从激发态恢复基态时,发出荧光。荧光标记技术指利用荧光物质共价结合或物理吸附在所要研究分子的某个基团上,利用它的荧光特性来提供被研究对象的信息。荧光标记的无放射物污染,操作简便等优点,使得荧光标记物在许多研究领域的应用日趋广泛。荧光标记物质在蛋白的功能研究、药物筛选等领域也有着广泛的应用。人们利用利用荧光标记的多肽来检测目标蛋白的活性,并将其发展的高通量活性筛选方法应用于疾病治疗靶点蛋白的药物筛选和药物开发(例如,各种激酶、磷酸酶、肽酶等)。因此,多肽的荧光修饰,同样是多肽合成领域的重要内容。下面是一些常用的多肽修饰荧光物质:[align=center][img=,488,412]https://ng1.17img.cn/bbsfiles/images/2018/12/201812201531359566_2467_3531468_3.jpg!w488x412.jpg[/img][/align]下面是一些荧光物质的激发光波长和发射光波长[align=center][img=,572,527]https://ng1.17img.cn/bbsfiles/images/2018/12/201812201531560487_1473_3531468_3.jpg!w572x527.jpg[/img][img=,572,296]https://ng1.17img.cn/bbsfiles/images/2018/12/201812201531563837_2721_3531468_3.jpg!w572x296.jpg[/img][/align]1.FITC修饰异硫氰酸荧光素(FITC)具有比较高的活性,通常来说,在固相合成过程中引入该种荧光基团相对于其他荧光素要更容易,并且反应过程中不需要加入活化试剂。我们公司合成的FITC修饰的多肽通常主要有两种形式:(1)在整条肽链末端接入FITC,并且在FITC之前接入一分子的Acp(6-氨基己酸),也称烷基间隔器。反应中FITC与肽链上裸露的-NH2反应,Acp的接入提供了六个碳的直链空间,大大降低了反应的空间位阻,提高了反应效率,降低了反应难度。其次,FITC还与多肽结构中的-SH,侧链-NH2反应,Acp的加入也降低了这种副反应发生的可能。此外,多肽在酸性环境条件下切割时,在N端接入FITC的多肽需要经历环化作用来形成荧光素,这种过程通常都会伴随最后一个氨基酸的切除,而烷基间隔器Acp的接入就避免了这一情况的发生。(2)在整条肽中的某个Lys侧链接入FITC,Lys侧链为末端为-NH2的四碳直链烷基,直接起到了降低空间位阻的作用。这种修饰方式能够灵活的在整条肽中任何位置进行FITC修饰,而不仅仅局限于末端。我们所采用的FITC修饰多肽的两种形式,都具有操作简便,成功率高,容易分离纯化等优点。[align=center][img=,670,486]https://ng1.17img.cn/bbsfiles/images/2018/12/201812201532383561_827_3531468_3.jpg!w670x486.jpg[/img][/align]2.AMC修饰7-氨基-4-甲基香豆素(AMC)是一种应用广泛的荧光标记试剂,例如,酶的痕量测定,酶的鉴定,激光染料的制备等多种用途,此外,C端用香豆素修饰的泛素分子也是研究蛋白质泛素化过程的重要探针。与其他荧光染料不同的是,AMC修饰多肽分子是从C端进行:(1)AMC与肽链C端第一个氨基酸反应 (2)固相合成整条肽链(从第二个氨基酸开始),并且保留整条肽链的侧链保护基和最后一个氨基保护基;(3)液相缩合AA-AMC与全保护的肽链;(4)切除保护基,完成肽链的修饰。[align=center][img=,514,326]https://ng1.17img.cn/bbsfiles/images/2018/12/201812201533275550_1867_3531468_3.jpg!w514x326.jpg[/img][/align]国肽生物提供5(6)-FAM,FITC,CY5,RhodamineB,PNA,EDNAS/dabcyl,Biotin等各种修饰的高质量多肽。国肽生物具有成熟的荧光标记多肽技术,优良的纯化生产工艺,定制荧光修饰的多肽,国肽生物是值得信任的品牌。成功案例:序列Cy5-betaA-YNDEDPEKEKRIKELELLLMSTENELKGQQAL,CY5进行修饰。HPLC分析:[align=center][img=,562,256]https://ng1.17img.cn/bbsfiles/images/2018/12/201812201534177890_6619_3531468_3.jpg!w562x256.jpg[/img][/align]MS分析:[align=center][img=,562,236]https://ng1.17img.cn/bbsfiles/images/2018/12/201812201534424203_4797_3531468_3.jpg!w562x236.jpg[/img][/align]合肥国肽生物官网[img=,220,52]https://ng1.17img.cn/bbsfiles/images/2018/12/201812201535194030_1002_3531468_3.jpg!w220x52.jpg[/img]
高效液相色谱法(HPLC)分析氨基酸概况杜文力 孟冲 史志军河北医药 Hebei Medical Journal 药品检测2004年1 月 第 26卷 第1 期, Jan 2004 , Vol 26 No 1随着氨基酸的广泛应用 ,对氨基酸的检测分析水平也不断提高。目前 ,氨基酸含量检测主要应用氨基酸 自动分析仪和HPLC。随着 HPLC 的发展 ,使用高效液相色谱技术分析氨基酸获得迅速发展 ,由于 HPLC技术无需特殊反应装置 ,具有高效、简便、快速、准确和价格低廉等优点 ,已在许多实验室部分或全部的代替了氨基酸自动分析仪 ,广泛应用于多种生物样品内氨基酸的检测。HPLC已成为一种较为理想的检测氨基酸的方法。实验所用色谱柱常采用 C18柱 、C8柱以及CN 柱 ,检测器使用紫外 、荧光或电化学 。流动相常采用强极性溶剂 ,如水、乙腈 、甲醇以及磷酸盐缓冲液。不同种类、不同离子强度的缓冲液均可影响到氨基酸容量因子 ,此时缓冲液的 pH值对容量因子的影响不大,但应注意当 pH7 对柱固定相有裂解作用。洗脱一般采用二级或三级梯度洗脱方式 ,洗脱程序明显影响分离效果

为什么甲氨基阿维菌素苯甲酸盐标准品会有这么多杂质峰?[img]http://ng1.17img.cn/bbsfiles/images/2018/04/201804231728132335_5892_3399169_3.jpg[/img]
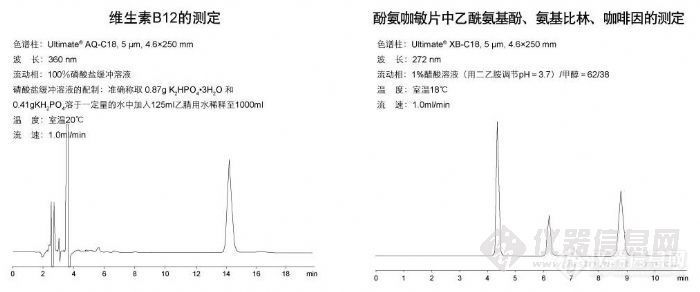
维生素B12的测定和酚氨咖敏片中乙酰氨基酚、氨基比林、咖啡因的测定http://ng1.17img.cn/bbsfiles/images/2009/11/200911021850_180185_1896702_3.jpg
有没有办法在一个样品能同时分析糖,氨基酸,甾醇,维生素的?液相了解的不多,可能问题都问的很傻,望高人指点
求助6-氨基青霉素烷酸中蛋白质检测 ,也就是6-APA中蛋白质含量检测,有做过的给说下吧,谢谢