苯乙酸是医药、农药、香料等有机合成的中间体。在医药工业中用于青霉素、地巴唑等药物的生产。苯乙酸经氯化、酯化得到α-氯代苯乙酸乙酯,用于稻丰散和乙基稻丰散的生产,这两种农药是广谱性有机磷杀虫剂。苯乙酸本身也是农药植物生长激素。苯乙酸广泛存在于葡萄、草莓、可可、绿茶、蜂蜜等中。苯乙酸在低浓度时具有甜蜂蜜味,在1ppm以下仍具有甜味,是一种重要的香料成分。苯乙酸还具有很强的杀菌作用。
[color=#444444]甲酰基苯乙酸甲酯的色谱含量测试中。由于甲酰基苯乙酸甲酯会有醇酮互变性质,在液相色谱(乙腈:水=50:50)下出现三个峰。但是在LC——MS下从第一个峰开始到第三个峰这之间所有的时间都出现了M+1峰(包括峰之间的)。谁能告诉我这是怎么回事。[/color][color=#444444]有哪个大侠做过甲酰基苯乙酸甲酯的含量测试的,求指导。[/color]
目前所做项目需要液相检测联苯乙腈(原料)和联苯乙酸(产物),但两者出峰时间一致,已尝试多种方法进行混合样分离,但始终只有一个尖峰显示,没有任何分离趋势,目前试过的方法有:甲醇:0.05%磷酸水=70:30(C-18长柱);乙腈:水=70:30;乙腈:0.1%氨水水溶液=70:30(NX-C18);甲醇:0.1%醋酸水=55:45(C18短柱)。求助是否有可行的方法能够较好的分离两种物质。谢谢。
求助各位同行:苯乙酸的国标或行标(HGB3444-62)全文.多谢了.我的邮箱:zjp9933@163.com
[font=Helvetica Neue,Helvetica,PingFang SC,Tahoma,Arial,sans-serif][size=14px][color=#333333]4-羟基苯乙酸酯[/color][/size][/font],[font=Helvetica Neue,Helvetica,PingFang SC,Tahoma,Arial,sans-serif][size=14px][color=#999999]CAS No.:[b]58556-55-1[/b][/color][/size][/font][font=Helvetica Neue,Helvetica,PingFang SC,Tahoma,Arial,sans-serif][size=14px][color=#999999]分子式:C[sub]1[/sub][sub]0[/sub]H[sub]1[/sub][sub]2[/sub]O[sub]3[/sub][/color][/size][/font]
如题,在合成中有一步反应是用邻羟基苯乙酸制备其二钠盐,其中产物中可能含有的成分有邻羟基苯乙酸、邻羟基苯乙酸的一钠盐、二钠盐,请问如何建立检测方法将其分离呢?谢谢! 试过液相的方法,但是分不开,也试过双相滴定,但是里面还有过量的NaOH,影响结果,也试过用酚羟基的显色反应,但这个又太灵敏了,无法定量。请大家指导一下吧。
[color=#444444]求助一下啊!!!![/color][color=#444444]我做的羟基苯乙酸去送样,结果GC分析人员做出了两个峰,做了两次都是这样。[/color][color=#444444]我的样品应该是纯的,是分析方法不对,还是其它什么原因啊?有没有哪个遇到这个的情况呢?求助哈[/color]
完全按GB29708-2013的方法处理,衍生化后质谱检不出五氯苯乙酸酯,不知道哪里有问题!请做过这个项目的指点。
[color=#d40a00][size=2]维权声明:本文为[font=Times New Roman]11093661[/font]原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。[/size][/color] 青霉素发酵过程中利用液相分析对发酵液中的苯乙酸,效价检测存在着很是矛盾的主体,那就是发酵过程中的效价检测是批量检测,在检测过程中青霉素效价有高有低,这样就不利于药典中规定的标准品与待测品的含量大致相同的规定,这就不可能每做一个样品就做一个标准,这样不实际也不利于节约成本的。那么就需要我们做一个线性范围来使在实际检测的过程中的效价范围在线性范围类,这样就有利于测样的准确性。本人通过长期反复工作实践发现在青霉素发酵过程中发酵液的稀释倍数在100倍以上时,出现了这样一个情况:在检测效价的过程中对苯乙酸检测的结果很不稳定,特别是长期工作的液相更是如此,本人在工作中试验发现原因主要是基线的漂移造成了这个现象。而检测苯乙酸对生产发酵中的地位相当重要,苯乙酸是青霉素发酵过程中的主要原材料之一,而苯乙酸的多少又决定了发酵水平高低。所以说苯乙酸的检测也同样重要。 而效价,苯乙酸是同时检测出来的,如果稀释倍数大于100后解决了效价检测的准确性得到了提高,但是苯乙酸的检测准确性也就低了。所以这个矛盾主体也就出现了。本人在长期的检测中实践发现如果分开来检测,也就是两次检测,而对于两次检测过程中的效价与苯乙酸两种物质稀释倍数采取不同的稀释倍数这样有利于检测结果的准确性。或者对苯乙酸检测采取[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]检测同时稀释倍数根据苯乙酸残量的多少采取不同的稀释倍数这样有利于检测结果的准确性,重现性。而根据本人了解某特大型青霉素发酵公司也就是只是对效价采取的稀释倍数的不同,这样提高了效价的准确性而导致了苯乙酸残量的检测的准确性也就降低了,导致发酵水平无法与成都某特大型青霉素发酵公司的水平相比较。这就说明了苯乙酸检测尤为重于效价检测。而分两次检测或气,液相同时检测这样不利于成本降低,本人通过长期的摸索,比较发现利用苯乙酸的多少来决定稀释倍数后,再根据效价的高低采取不同的标准品的含量,这样就利于检测的准确性与成本的降低——相当于分段检测。 本人事先声明这个纯属个人自己摸索试验得出的结论,在实际生产,检测中虽然得到了应用,但由于自己的试验结果,水平有限所以具体过程没有完全介绍,十分抱歉。
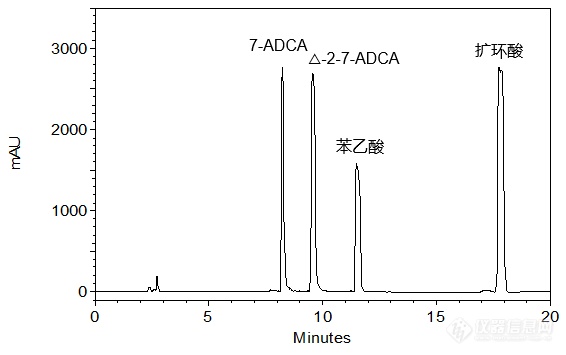
[align=center][b]4种头孢中间体的共同分析[/b][/align][align=right][b]——7-ADCA、△-2-7-ADCA、苯乙酸及扩环酸的分析[/b][/align][align=right][b][/b][/align]客户提供了7-ADCA(7-氨基去乙酰氧基头孢烷酸),△-2-7-ADCA、苯乙酸及扩环酸原料,希望本实验室依据客户所提供的色谱条件筛选合适的C[sub]18[/sub]色谱柱,实现以上4种化合物的稳定良好分析。本实验室参考客户提供的色谱条件,首先尝试使用经过聚合物包被处理的中等极性色谱柱——CAPCELL PAK C[sub]18[/sub] MGII对客户所提供样品进行分析,使用PDA检测器进行检测。如图1,在高浓度大体积进样的情况下,各色谱峰发生严重过载现象,出现平头峰;如图2,降低进样体积至5 μL可得到相对良好峰形,且各组分间能够得到良好分离,分离度均在10.0以上(结果详见表1)。[align=center][img=,566,355]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101537444868_8925_2222981_3.png!w566x355.jpg[/img][/align][align=center]图1 CAPCELL PAK C[sub]18 [/sub]MGII色谱柱分析结果(进样量:50 μL)[/align][align=center][img=,575,365]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101545063985_5910_2222981_3.png!w575x365.jpg[/img][/align][align=center]图2 CAPCELL PAK C[sub]18 [/sub]MGII色谱柱分析结果(进样量:5 μL)[/align][align=center] [/align][align=center]表1 CAPCELL PAK C[sub]18[/sub] MGII分析结果详表(进样量:5 μL)[/align][align=center][img=,553,136]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101537465105_7074_2222981_3.png!w553x136.jpg[/img][/align][align=center][/align][align=left][img=,579,319]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101545307700_4011_2222981_3.png!w579x319.jpg[/img][/align][align=left][/align][align=left]为使客户有更多色谱柱选择,本实验室也尝试了能够在纯水系流动相下稳定使用的高极性色谱柱——CAPCELL PAK C[sub]18[/sub] AQ进行分析。如图3,几种头孢中间体的整体保留有所增强,而高浓度上样仍会出现与MGII色谱柱相似的过载现象;如图4,降低进样体积进行分析,可得到良好结果,同时发现扩环酸有一定程度的拖尾(见表2)。[/align][align=center][/align][align=center][img=,527,377]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101546103944_1716_2222981_3.png!w527x377.jpg[/img][/align][align=center]图3 CAPCELL PAK C[sub]18 [/sub]AQ色谱柱分析结果(进样量:50 μL)[/align][align=center][img=,525,374]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101546123571_3070_2222981_3.png!w525x374.jpg[/img][/align][align=center]图4 CAPCELL PAK C[sub]18 [/sub]AQ色谱柱分析结果(进样量:5 μL)[/align][align=center] [/align][align=center]表2 CAPCELL PAK C[sub]18 [/sub]AQ分析结果详表(进样量:5 μL)[/align][align=center][img=,558,135]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101546125551_7090_2222981_3.png!w558x135.jpg[/img][/align][align=center][/align][align=left][img=,577,319]http://ng1.17img.cn/bbsfiles/images/2018/05/201805101547424196_8227_2222981_3.png!w577x319.jpg[/img][/align][align=left][/align][align=left]综上实验结果,使用中等极性色谱柱CAPCELL PAK C[sub]18 [/sub]MGII S5 4.6 mm i.d. × 250 mm和高极性色谱柱CAPCELL PAK C[sub]18[/sub] AQ S5 4.6 mm i.d. × 250 mm,以磷酸盐缓冲液(pH 6.0)-乙腈为流动相体系,在30°C柱温条件下进行梯度分析,均能够实现7-ADCA、△-2-7-ADCA、苯乙酸和扩环酸的良好分离,其中,CAPCELL PAK C[sub]18[/sub] MGII色谱柱所得峰形更佳。[/align]
有没有老师做过苯乙醇和乙酸苯乙醇的TLG分离的。在展开剂方面给点意见吧。
用YC/T207-2014方法,测混合标液,苯乙烯 2-乙氧基乙基乙酸酯 邻-二甲苯分离不好还,出现了重合峰情况,用谱库搜出来是间二甲苯,邻二甲苯甲苯去哪里了呢?[img]https://ng1.17img.cn/bbsfiles/images/2022/12/202212221658210017_6074_5898744_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2022/12/202212221658214942_5520_5898744_3.png[/img]
用YC/T207-2014方法,测混合标液,苯乙烯 2-乙氧基乙基乙酸酯 邻-二甲苯分离不好还,出现了重合峰情况,用谱库搜出来是间二甲苯,邻二甲苯甲苯去哪里了呢?![img]https://ng1.17img.cn/bbsfiles/images/2022/12/202212221603511087_6024_5898744_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2022/12/202212221603511511_1108_5898744_3.png[/img]
======在 2006-11-13 13:46:31 wangjiangli0123来信中写道:======请问 电离电位是多少 苯乙烯 的 乙酸丁酯的 还有十一烷的======================================
做的五氯苯酚,酯化后上机2ppm 浓度峰强度仅有70000多,远低于基线600000,这是哪里出的问题,方法检出限可是0.05ppm,这是用SIM做的原因吗?
《ChP2005》二部中,羟苯乙酯的鉴别:取本品约0.1g,加乙醇2ml使溶解,煮沸,加硝酸汞试液0.5ml,放置后逐渐生成沉淀,上清液显红色。开始是发生水解反应,可是水解产物与醋酸汞反应原理是什么?
【求助】请教苯乙烯、苯甲醛、环氧苯乙烷TLC同时展开的展开剂和显色剂是什么?或者只展开苯乙烯,环氧苯乙烷的展开剂和显色剂。本人最近在做苯乙烯的环氧化,需用TLC跟踪,想请教各位上述问题。
色谱柱DB23和DB-5都试过,都没有标准品峰进样口温度230,检测器温度250,柱温:60℃,以10℃/min程序升温至120℃,恒温1min,以10℃/min程序升温至200℃,恒温2min,进样量1uL;标准品为1uL苯乙醇溶于2ml乙酸乙酯溶剂峰正常,相同条件下苯乙酮标准品也有峰。为什么1-苯乙醇标准品不出峰???
[color=#444444]最近在做苯乙酮和1-苯乙醇的化学实验,想用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行分析,结果发现两个的沸点相差很近,请问这种情况下应该怎么样进行测试,[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的操作应该注意什么,苯乙酮的沸点是202.3度,1-苯乙醇的是203.4度,谢谢大家[/color]
室温下,在重水或氯仿中测聚苯乙烯、聚丙烯酸的碳谱(浓度约200mg/ml),信号是又矮又宽的包,有没有办法使信号变得尖锐?尝试过升高温度(升高至70度),加三乙胺(溶液最终的ph值未知)作谱,没什么变化。
最近做苯系物甚是郁闷,顶空FID做得时候,发现几乎不出峰,响应值很小,于是直接液体进样,然后...间对二甲苯完全重叠,苯乙烯和邻二甲苯重叠,由于二甲苯只要求算总量,现在的问题就是苯乙烯和邻二甲苯能不能分开!我们用的是安捷伦7890A,进样口温度180,柱温120保持1分钟,10每分钟升到200保持5分钟,检测器FID220,用的柱子是DB624,求解是不是柱子的问题?
[align=center][font='times new roman'][size=16px]苯乙烯[/size][/font][font='times new roman'][size=16px]-[/size][/font][font='times new roman'][size=16px]马来酸共聚物[/size][/font][font='times new roman'][size=16px]及其应用[/size][/font][/align] 苯乙烯与马来酸酐的[back=#ffffff]共聚物[/back][back=#ffffff]苯乙烯[/back][back=#ffffff]-[/back][back=#ffffff]马来酸([/back][back=#ffffff]SMA[/back][back=#ffffff])[/back][back=#ffffff]首先由[/back][back=#ffffff]Alfred[/back][back=#ffffff]和[/back][back=#ffffff]Lavin[/back][back=#ffffff]在[/back][back=#ffffff]1945[/back][back=#ffffff]年制[/back][back=#ffffff]备。[/back][back=#ffffff]之后[/back][back=#ffffff],[/back][back=#ffffff]Mayo[/back][back=#ffffff]等提出[/back][back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]共聚体系是典型的交替共聚模型[/back][back=#ffffff],[/back][back=#ffffff]具有强吸电子基团的马来酸酐与具有给电子基团[/back][back=#ffffff]的[/back][back=#ffffff]苯乙烯是一对电荷转移复合物,在自由基引发体系中具有很好的交替共聚特征,但是传统的自由基聚合会导致[/back][back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]的聚合不可控且分子量分布较宽等问题,限制了[/back][back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]共聚物[/back][back=#ffffff]的应用,“活性”[/back][back=#ffffff]/[/back][back=#ffffff]可控自由基聚合法为[/back][back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]的合成提供了解决方案,[/back][back=#ffffff]但是也有着显著区别。[/back][back=#ffffff]对于[/back][back=#ffffff]A[/back][back=#ffffff]TRP[/back][back=#ffffff]法,马来酸酐会与催化剂中金属离子发生反应,导致催化剂失效,因此只能采取光引发等无金属[/back][back=#ffffff]A[/back][back=#ffffff]TRP[/back][back=#ffffff]法合成。对于[/back][back=#ffffff]N[/back][back=#ffffff]MP[/back][back=#ffffff]法,由于聚合所需的温度较高,只能得到[/back][back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]的无规[/back][back=#ffffff]则[/back][back=#ffffff]共聚物。利用[/back][back=#ffffff]R[/back][back=#ffffff]AFT[/back][back=#ffffff]法可以较好地进行共聚,并且可以得到交替共聚物。在实际的聚合反应体系中,苯乙烯与马来酸酐的交替共聚速率远大于苯乙烯的自聚速率,并且马来酸酐的自聚能力很低,因此在苯乙烯过量的情况下,会首先形成[/back][back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]交替共聚物,此后再是苯乙烯的自聚,最终可形成具有[/back][back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]交替和[/back][back=#ffffff]苯乙烯[/back][back=#ffffff]自聚的嵌段共聚物[/back][back=#ffffff]。[/back] [back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]的一个重要优势在于马来酸酐中酸酐基团的高反应活性,可以在较温和的条件下发生酯化、酰胺化等反应,因此可以引入新的功能性基团,得到改性的[/back][back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]衍生物,这大大拓展了其应用范围[/back][back=#ffffff]。[/back][back=#ffffff]由于[/back][back=#ffffff]S[/back][back=#ffffff]MA[/back][back=#ffffff]及其衍生物具有独特的两亲性和生物相容性,已经被大量应用于膜蛋白增溶提取、药物递送和新材料合成等领域。[/back] [align=center][font='times new roman'][size=16px]S[/size][/font][font='times new roman'][size=16px]MA[/size][/font][font='times new roman'][size=16px]与膜蛋白质[/size][/font][/align] 在多细胞生物中,膜蛋白约占总蛋白质的三分之一。它们在细胞间信号传导和跨细胞膜转运中发挥着重要作用。2009年Knowles等首次报道了SMA共聚物可以直接将生物膜溶解成脂质纳米圆盘(SMALPs),既保留了圆盘内的蛋白质,又确保了膜蛋白稳定的天然脂质环境。此后,使用SMA共聚物的无去污剂增溶方法被大量应用于从生物膜中直接提取蛋白质和脂质。 目前为止,研究人员发现对于苯乙烯与马来酸组成比为3:1或2:1的共聚物结构对于膜的溶解最有效。以3:1的SMA为例简要描述其增溶机制,首先在阶段1中,苯乙烯单元穿透到磷脂双分子层的疏水部分且马来酸酐与亲水性头基结合,此时SMA从一开始紧凑且聚集的构象转变为解聚、延伸的构象,SMA已经插入到磷脂双分子层中。在阶段2中,SMA在磷脂双层中达到饱和状态,此时SMALPs形成,并与SMA饱和的磷脂双层共存。在第3阶段,SMA饱和的磷脂双层完全转化为SMALPs,磷脂双层全部溶解,SMA分布在磷脂双层中,过量的SMA附着在双层周围,生物膜实现增溶。 [align=center] [/align][align=center][font='times new roman'][size=16px]S[/size][/font][font='times new roman'][size=16px]MA[/size][/font][font='times new roman'][size=16px]衍生物[/size][/font][/align] 随着对SMA增溶机制的深入研究发现,SMA的分子量、化学组成与衍生基团的类型等会影响膜蛋白的提取效率与选择性。此外,由于SMA中马来酸的存在,酸的质子化或者与金属阳离子的络合会导致SMA变得过于疏水而无法维持纳米圆盘的结构,比如Mg[font='times new roman'][sup][size=16px]2[/size][/sup][/font][font='times new roman'][sup][size=16px]+[/size][/sup][/font]的浓度高于10 mM或pH低于6时通常会导致SMA沉淀,从而导致SMALPs分解。为了解决上述问题,研究人员开发了大量SMA衍生物,增加了对于pH与金属阳离子(Cu[font='times new roman'][sup][size=16px]2[/size][/sup][/font][font='times new roman'][sup][size=16px]+[/size][/sup][/font]、Mg[font='times new roman'][sup][size=16px]2[/size][/sup][/font][font='times new roman'][sup][size=16px]+[/size][/sup][/font]、Ca[font='times new roman'][sup][size=16px]2[/size][/sup][/font][font='times new roman'][sup][size=16px]+[/size][/sup][/font])的耐受性,为膜蛋白与膜脂的研究提供了更多的选择。例如,Brady等发现2-丁氧基乙醇功能化的SMA衍生物可以促进膜蛋白从蓝藻类囊体膜的提取,而未功能化的SMA基本上是无效的,且较长的疏水性烷氧基乙氧基化物侧链可以提高增溶效率。Burridge等同时合成了SMA-Glu/AE/Neut/Pos四种衍生物,所有的SMA衍生物都能够与以棕榈酰油酰磷脂酰胆碱制备的脂质体反应,形成不同尺寸的SMALPs,都显示出稳定的物理特性,在较宽pH范围和高达100 mM Mg[font='times new roman'][sup][size=16px]2+[/size][/sup][/font]下也可以发挥作用。Lindhoud等通过2-氨基乙硫醇对SMA的部分衍生化,合成了SMA-SH,其可以溶解生物膜,同时SMA-SH中的巯基基团可以与其它活性基团进行衍生化得到新的功能化SMA衍生物,进而实现膜蛋白的选择性提取与纯化,为SMA的应用提供了新思路。 除了对SMA进行衍生化用于提高对膜蛋白的提取效率与选择性之外,部分研究人员也探索了SMA共聚物本身的性质,比如苯乙烯与马来酸酐的比例、链的长度与化学组成分布等,以提高形成SMALPs的能力与稳定性。例如,Cunningham等报道了一种迭代RAFT聚合法合成了具有窄分子量分布与化学组成分布的SMA共聚物。在深入研究之后发现分子量分布与化学组成是影响膜增溶的两个主要因素,宽分子量分布的SMA共聚物,往往具有较高的链长,影响SMA的活性。事实上,较短链长的SMA更有利于SMALPs的形成,因为长链SMA会导致聚合物自身的缠绕,此外长链会同时参与多个SMALPs的形成,进一步影响增溶效率。 [align=center][font='times new roman'][size=16px]S[/size][/font][font='times new roman'][size=16px]MA[/size][/font][font='times new roman'][size=16px]与膜脂[/size][/font][/align] SMA及其衍生物已经广泛应用于膜蛋白的提取与研究。事实上,SMALPs也是用于研究蛋白质周围局部脂质环境的优良体系,但是相关的报道较膜蛋白要少。 Juarez等[font='times new roman'][sup][size=16px][95][/size][/sup][/font]用SMA从两种菌株(野生型N2和细菌抗性菌株agmo-1)中提取脂质,然后通过薄层色谱法和质谱法进行表征,发现从细菌抗性菌株agmo-1中提取的脂质含有醚连接的(O-烷基链)脂质,与仅含有酯连接的(O-酰基)脂质的野生型N2菌株相反。这与细菌抗性菌株agmo-1中功能性烷基甘油单加氧酶(AGMO)的丧失保持一致。此外,与传统的脂质提取方法(需要有机溶剂的方法)相比,SMA可用于生物活体中脂质的提取而不影响其活性,证明了SMA在脂质组学的研究中具有良好潜力。 Rehan等采用电喷雾离子化质谱(ESI-MS)法分析了由SMA提取的人体平衡核苷转运蛋白-1(hENT1)中的脂质组成,因为hENT1是一种需要脂质膜来维持其结构和功能的蛋白质,其周围脂质双层的组成对其活性和稳定性至关重要。分析结果发现,每个hENT1-SMALPs中含有16个磷脂酰胆碱(PC)和2个磷脂酰乙醇胺(PE)脂质分子。除此之外,研究发现使用SMA比使用洗涤剂溶解的hENT1更加稳定。
我吹扫浓度苯乙烯配0.5 1.02.5 5.0 10.0 20.0后面几个点线性很差 而且我质控前面加了清洗 发现清洗的苯乙烯浓度也是其他清洗的4倍。吹扫不急 苯系物浓度有残留吗 还是我浓度配的太高了 其他参数 都是999 就苯乙烯..
请教α-甲基苯乙烯,邻甲基苯乙烯,2-甲基苯乙烯,3-甲基苯乙烯,4-甲基苯乙烯,是不同的物质吗?,物质结构

作者:http://d.g.wanfangdata.com.cn/Images/head_pic.gif张琰 http://d.g.wanfangdata.com.cn/Images/head_pic.gif陈文秋 http://d.g.wanfangdata.com.cn/Images/head_pic.gif余敏灵 Author:Zhang Yan Chen Wenqiu Yu Minling 作者单位:四川省眉山市人民医院,四川,眉山,620010 四川省乐山食品药品检验所,四川,乐山,614000摘要: 目的 建立测定羟苯乙酯中水杨酸含量的方法 .方法 采用反相高效液相色谱法,Diamonsil C18柱(250mm×4.6 mm,5μm),以0.05mol/L磷酸二氢钠缓冲液(pH=3.4)-乙腈(50:50)为流动相,检测波长为297 mm.结果水杨酸质量浓度在0.51~13.26 μg/mL范围内与峰面积呈良好的线性关系,平均回收率为99.0%,RSD=0.8%(n=6).结论 该法简便、准确、快速,适用于羟苯乙酯中水杨酸的含量测定.http://ng1.17img.cn/bbsfiles/images/2012/08/201208201739_384784_2379123_3.jpg
请教一下,最近废气经常遇到苯乙烯和三苯或者其他挥发性有机物一起采样的情况,对采样频次有些纠结。有哪些排放标准里苯乙烯可以只采1个小时均值,不需要按照恶臭类排放标准采3-4个频次的。
二苯乙内酰脲又称苯妥英,水中的二苯乙内酰脲从何而来,水中二苯乙内酰脲高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]质谱法测定相关标准吗
据外媒报道,近日部分德国媒体报道称,珍珠奶茶含有多种致癌成分,严重危害人体健康。此消息一出,德国珍珠奶茶专卖店的生意变得异常惨淡,部分店家甚至面临关门歇业的境地。 如何检测苯乙酮、溴化物及苯乙烯等致癌物?
我国苯乙烯供应结构悄然变化 从2005年开始,国产苯乙烯供应增长速度,超过国内需求的增长速度,进口量下降,近两年维持了这一趋势。 产业发展重心应由扩能转向提高竞争力 国内苯乙烯市场受国际原油和纯苯价格波动影响较大。2007年国际油价一直高位徘徊,为苯乙烯价格提供有力支撑。同时,下游ABS等增长依然强劲,对苯乙烯市场起到拉动作用。 由于2007年我国苯乙烯新增产能仅为16万吨,且新增产能尚未有效释放,因此产量基本与2006年持平。同年上海高桥20万吨/年ABS装置、扬子石化金浦橡胶有限公司10万吨/年SBR装置、台湾台塑石化公司20万吨/年PS装置等几套苯乙烯下游装置投产,使我国苯乙烯供应紧张的形势加剧。2007年我国苯乙烯市场仍以卖方市场为主导,高位行情成主流。同时,供应紧张也使我国2007年苯乙烯的进口量在近年逐年下降的趋势下又创新高,达310万吨。 苯乙烯是苯用量最大的衍生物,也是最基本的芳烃化学品。苯乙烯主要用于生产聚苯乙烯(占其需求量约2/3),也可用于制取苯乙烯—丁二烯(丁苯)橡胶(SBR)、ABS和苯乙烯—丙烯腈(SAN)树脂、不饱和聚酯等,此外,苯乙烯也是生产涂料、染料、合成医药的重要原料。 供应结构已发生变化 长期以来,我国苯乙烯产不足需,缺口较大,每年需大量进口,并呈逐年增加趋势。1995年我国苯乙烯的进口量只有30.58万吨,进口量从1996年~1997年40万吨/年上升到1999年103万吨、2000年116万吨、2001年150万吨、2002年179.8万吨,2003年进口量达266.06万吨,2004年和2005年进口量分别达到288.90万吨和281.2万吨。进口/表观消费量比例由2002年66.92%增加到2003年73.85%、2004年74.70%,2005年进口依存度开始下降至69.44%,产量仍满足不了国内对苯乙烯的需求。1999年~2005年进口年均增长率达到23%。在苯乙烯大量进口的同时,还有较多的苯乙烯下游产品进口,对国内市场冲击较大。 近年来,随着一批大型苯乙烯装置的投产,我国苯乙烯供应紧张的形势有所缓解。进入2006年后,我国苯乙烯进口量继续减少,而且下降幅度越来越大,全年进口量为234.3万吨,比2005年同期下降16.7%,这表明我国苯乙烯供应格局已经悄然发生变化,即从2005年开始我国自身的苯乙烯供应增长速度首次超过需求的增长速度,进口出现下降,并维持了这一发展趋势。预计未来几年,随着我国一些大型苯乙烯新扩建装置的陆续建成投产,进口量还会逐渐减少。 近期内扩能趋势 2007~2010年仍是我国苯乙烯产能的大规模增长期,一些新建和扩建项目仍将陆续进行。预计到2008年我国苯乙烯总生产能力将达到约400万吨/年,2010年将达到约600万吨/年,届时我国苯乙烯市场供需矛盾将得到根本缓解。 苯乙烯需求的持续强劲增长,是我国苯乙烯生产不断扩能的原动力。2007年~2008年是我国苯乙烯产能的大规模增长期,而经过新一轮扩能高峰后,预计到2010年,我国苯乙烯市场供需矛盾将得到根本缓解,供需将基本平衡或略有缺口。 将重心由扩能转向提高竞争力 世界苯乙烯的生产能力已经出现过剩的态势。按照目前我国的扩能计划,2010年供需矛盾将得到根本缓解,因此,目前我国苯乙烯产业应该开始将重心由扩能转向提高竞争力。 一是要实现规模化生产,降低成本。我国现已建成上海赛科50万吨/年和惠州中海壳牌56万吨/年规模化装置,但我国大多数苯乙烯装置能力仍偏小,未达到规模生产的要求,加上有些装置生产技术相对落后,生产成本高,经济效益差,缺乏竞争力。 二是应尽快采用先进技术对现有装置进行技术改造,逐步提高装置的生产规模和工艺技术水平,增加产量,降低生产成本,进一步增强我国苯乙烯产品在国内外市场的竞争力。
从2005年开始,国产苯乙烯供应增长速度,超过国内需求的增长速度,进口量下降,近两年维持了这一趋势。 产业发展重心应由扩能转向提高竞争力 国内苯乙烯市场受国际原油和纯苯价格波动影响较大。2007年国际油价一直高位徘徊,为苯乙烯价格提供有力支撑。同时,下游ABS等增长依然强劲,对苯乙烯市场起到拉动作用。 由于2007年我国苯乙烯新增产能仅为16万吨,且新增产能尚未有效释放,因此产量基本与2006年持平。同年上海高桥20万吨/年ABS装置、扬子石化金浦橡胶有限公司10万吨/年SBR装置、台湾台塑石化公司20万吨/年PS装置等几套苯乙烯下游装置投产,使我国苯乙烯供应紧张的形势加剧。2007年我国苯乙烯市场仍以卖方市场为主导,高位行情成主流。同时,供应紧张也使我国2007年苯乙烯的进口量在近年逐年下降的趋势下又创新高,达310万吨。 苯乙烯是苯用量最大的衍生物,也是最基本的芳烃化学品。苯乙烯主要用于生产聚苯乙烯(占其需求量约2/3),也可用于制取苯乙烯—丁二烯(丁苯)橡胶(SBR)、ABS和苯乙烯—丙烯腈(SAN)树脂、不饱和聚酯等,此外,苯乙烯也是生产涂料、染料、合成医药的重要原料。 供应结构已发生变化 长期以来,我国苯乙烯产不足需,缺口较大,每年需大量进口,并呈逐年增加趋势。1995年我国苯乙烯的进口量只有30.58万吨,进口量从1996年~1997年40万吨/年上升到1999年103万吨、2000年116万吨、2001年150万吨、2002年179.8万吨,2003年进口量达266.06万吨,2004年和2005年进口量分别达到288.90万吨和281.2万吨。进口/表观消费量比例由2002年66.92%增加到2003年73.85%、2004年74.70%,2005年进口依存度开始下降至69.44%,产量仍满足不了国内对苯乙烯的需求。1999年~2005年进口年均增长率达到23%。在苯乙烯大量进口的同时,还有较多的苯乙烯下游产品进口,对国内市场冲击较大。 近年来,随着一批大型苯乙烯装置的投产,我国苯乙烯供应紧张的形势有所缓解。进入2006年后,我国苯乙烯进口量继续减少,而且下降幅度越来越大,全年进口量为234.3万吨,比2005年同期下降16.7%,这表明我国苯乙烯供应格局已经悄然发生变化,即从2005年开始我国自身的苯乙烯供应增长速度首次超过需求的增长速度,进口出现下降,并维持了这一发展趋势。预计未来几年,随着我国一些大型苯乙烯新扩建装置的陆续建成投产,进口量还会逐渐减少。 近期内扩能趋势 2007~2010年仍是我国苯乙烯产能的大规模增长期,一些新建和扩建项目仍将陆续进行。预计到2008年我国苯乙烯总生产能力将达到约400万吨/年,2010年将达到约600万吨/年,届时我国苯乙烯市场供需矛盾将得到根本缓解。 苯乙烯需求的持续强劲增长,是我国苯乙烯生产不断扩能的原动力。2007年~2008年是我国苯乙烯产能的大规模增长期,而经过新一轮扩能高峰后,预计到2010年,我国苯乙烯市场供需矛盾将得到根本缓解,供需将基本平衡或略有缺口。 将重心由扩能转向提高竞争力 世界苯乙烯的生产能力已经出现过剩的态势。按照目前我国的扩能计划,2010年供需矛盾将得到根本缓解,因此,目前我国苯乙烯产业应该开始将重心由扩能转向提高竞争力。 一是要实现规模化生产,降低成本。我国现已建成上海赛科50万吨/年和惠州中海壳牌56万吨/年规模化装置,但我国大多数苯乙烯装置能力仍偏小,未达到规模生产的要求,加上有些装置生产技术相对落后,生产成本高,经济效益差,缺乏竞争力。 二是应尽快采用先进技术对现有装置进行技术改造,逐步提高装置的生产规模和工艺技术水平,增加产量,降低生产成本,进一步增强我国苯乙烯产品在国内外市场的竞争力。