硒(Se)非金属,是人体必需微量元素之一,遍布各组织器官和体液,肾中浓度最高,对提高免疫力和预防癌症非常重要。男性体内的硒多集中在睾丸及前列腺、输精管中,会随精液一起排出体外。由于人体内硒不存在长期贮藏硒的器官,机体所需的硒应该不断从饮食中得到足够量的硒,硒浓度的平衡对许多器官、组织的生理功能有着重要的保护作用和促进作用。当硒缺乏的时候,就很容易导致人体免疫能力下降,威胁人类健康和生命的四十多种疾病都与人体缺硒有关,如癌症、心血管病、肝病、白内障、胰脏疾病、糖尿病、生殖系统疾病等症状。有人认为自己缺硒,就盲目补硒。把高硒食物当做营养品来长期服用,使人体处在一个高硒状态。其实盲目补硒是不可取的,人体长期处在高硒状态下表现为皮肤痛觉迟钝、四肢麻木、头昏眼花、食欲不振、头发脱落、指甲变厚、皮疹、皮痒、面色苍白、胃肠功能紊乱、消化不良等症状。
猪蹄中由于富含胶原蛋白,因此常常被认为是增加皮肤弹性、让皮肤更年轻态的给力食材。胶原纤维层仅仅是皮肤许多次层中的一个组成部分,皮肤是否处于健康、有弹性、有水分的正常状态,往往并不仅仅取决于胶原蛋白的多少,还与其他诸多成分紧密相关。因此,仅仅靠补充胶原蛋白就想获得“美白有弹性,光滑又滋润”的皮肤,并不靠谱。胶原蛋白是一种大分子蛋白质,而人体能够吸收的只有蛋白质和一部分小分子多肽,像胶原蛋白这样的大分子进入人体后,胃、胰脏等消化器官就会分泌胃蛋白酶、胰蛋白酶等将大分子结构的胶原蛋白切碎、打散成为甘氨酸、脯氨酸和羟脯氨酸等或小分子多肽,再根据人体对不同氨基酸的需要,重组为新的蛋白质。而新的蛋白质可能是酶、可能是身体器官组成部分、可能是激素……也就是说,胶原蛋白进入人体后,不可能直接变成皮肤中的胶原蛋白,对皮肤的影响,自然也微乎其微。因此吃猪蹄能美白的作用,大多数属于安慰剂作用。 看到这里,或许你在也不爱吃猪蹄了?
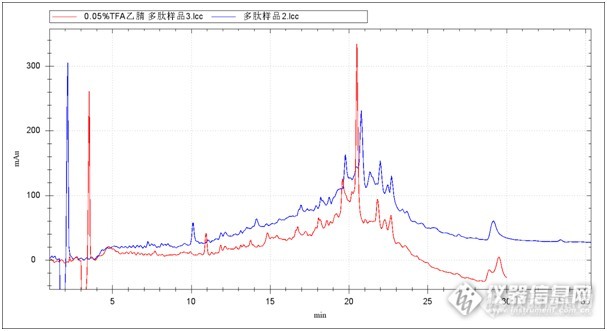
建立测定某多肽HPLC法 多肽是人体自身存在而且必需的活性物质,是人体的重要组成物质、营养物质,它广泛分布于人体各部位,特别是在大脑里,几乎对所有的细胞都有调节作用。人体缺失了多肽,免疫系统及各功能系统就可能发生紊乱,就会出现各种慢性病。多肽还具有抗菌、抗肿瘤、增强传统抗生素对耐药菌的活性、促进创伤愈合等多项生物学功能。这也就成为其在医药、食品防腐、保健品及化妆品等领域具有广阔的应用前景。 蛋白质的生理功能主要由肽来完成,有人甚至说肽是生命的统帅,对生命非常重要。所以肽及多肽的生产、合成也是非常重要的。当然测定工作也是很重要的。 某药物研究所通过药物机理成功的合成了某营养成分--某多肽,由于涉及到一些保密成分,暂时定义为“多肽X”。以下测定实验就是一是为了测定多肽,二是为了通过对某药品中多肽的测定,以便对该多肽成分制备提取提供可行性方法及理论数据。1 实验概述1.1 实验目的a.为了测定多肽。b.为了通过对某药品中多肽的测定,以便对该多肽成分制备提取提供可行性方法及理论数据。1.2 实验要求a. 梯度基线漂移不超过20mAu,分离度好。b. 定性定量分析结果准确可靠。c. 通过对某药品中多肽的测定,完善色谱条件(主要是流动相和检测波长的确定),为该多肽X的制备提取做工作。1.3 实验原理以乙腈和水为流动相,加入阴离子对试剂三氟乙酸,与多肽的质子化氨基结合,以提高多肽样品的保留值。1.4 实验环境1.4.1仪器设备:高效液相色谱仪(梯度洗脱泵,紫外检测器)手动进样器1.4.2环境:温度:24℃湿度:45%2 实验方案2.1色谱条件(参考):色谱柱:STC C18(250*4.6,5um)波长:210nm流动相A:0.1%三氟乙酸(TFA)的乙腈溶液流动相B:0.1%三氟乙酸(TFA)的水溶液http://ng1.17img.cn/bbsfiles/images/2013/08/201308311139_461282_2369266_3.png[font

[font=Helvetica][size=10.5pt][color=#333333]国肽生物是一家专业从事多肽产品的研发、生产和销售以及多肽技术转让的高新技术企业。BP公司成立之初,便成功收购了国内几家多肽、抗体公司,是目前国内的专业多肽合成、抗体制备、蛋白表达的规模型生产企业。国肽生物专长于荧光标记肽、同位素标记肽、人工胰岛素、药物肽、化妆品肽、长肽困难肽等产品的合成与研发,致力于学术水平的科研提升,搭建学术交流平台,促进前沿、专业的学术知识推广,推动多肽在生物医学材料等领域的研究与应用[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]多肽是一种与生物体内各种细胞功能都相关的生物活性物质,它的分子结构介于氨基酸和蛋白质之间,是由多种氨基酸按照一定的排列顺序通过肽键结合而成的化合物。多肽是涉及生物体内各种细胞功能的生物活性物质的总称,常常被应用于功能分析、抗体研究、尤其是药物研发等领域。多肽合成技术的出现,让这些多肽的应用领域变得更宽。[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]多肽的固相合成[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]多肽的合成是氨基酸重复添加的过程,通常从C端向N端(氨基端)进行合成。多肽固相合成的原理是将目的肽的第一个氨基酸C端通过共价键与固相载体连接,再以该氨基酸N端为合成起点,经过脱去氨基保护基和过量的已活化的第二个氨基酸进行反应,接长肽链,重复操作,达到理想的合成肽链长度,最后将肽链从树脂上裂解下来,分离纯化,获得目标多肽。[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]1、Boc多肽合成法[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]Boc方法是经典的多肽固相合成法,以Boc作为氨基酸α-氨基的保护基,苄醇类作为侧链保护基,Boc的脱除通常采用三氟乙酸(TFA)进行。多肽合成时将已用Boc保护好的N-α-氨基酸共价交联到树脂上,TFA切除Boc保护基,N端用弱碱中和。[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]肽链的延长通过二环己基碳二亚胺(DCC)活化、偶联进行,最终采用强酸氢氟酸(HF)法或三氟甲磺酸(TFMSA)将合成的目标多肽从树脂上解离。在Boc多肽合成法中,为了便于下一步的多肽合成,反复用酸进行脱保护,一些副反应被带入实验中,例如多肽容易从树脂上切除下来,氨基酸侧链在酸性条件不稳定等。[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]2、Fmoc多肽合成法[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]Carpino和Han以Boc多肽合成法为基础发展起来一种多肽固相合成的新方法——Fmoc多肽合成法。[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]Fmoc多肽合成法以Fmoc作为氨基酸α-氨基的保护基。其优势为在酸性条件下是稳定的,不受TFA等试剂的影响,应用温和的碱处理可脱保护,所以侧链可用易于酸脱除的Boc保护基进行保护。[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]肽段的最后切除可采用TFA/二氯甲烷(DCM)从树脂上定量完成,避免了采用强酸。同时,与Boc法相比,Fmoc法反应条件温和,副反应少,产率高,并且Fmoc基团本身具有特征性紫外吸收,易于监测控制反应的进行。Fmoc法在多肽固相合成领域应用越来越广泛。[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]肽是指由两个或两个以上的氨基酸脱水缩合而成的化合物。最简单的肽由两个氨基酸组成,称二肽。含多个氨基酸的肽称多肽。含50个氨基酸以上的多肽,通常称为蛋白质。肽广泛存在于动物、植物和微生物中,有重要的生理作用,对生物的生长发育、细胞分化、大脑活动、肿瘤病变、免疫防御、生殖控制以及抗衰老等方面都有特殊的功能。如谷胱甘肽是某些酶的辅酶,对体内的氧化还原过程起重要作用。许多激素属于多肽,如催产素、加压素、胰高血糖素以及促肾上腺皮质激素等,能调节机体代谢。由下丘脑分泌的激素调节因子也是多肽,它们控制着其他内分泌腺释放激素的活动。近年来在高等动物脑中发现的脑啡肽(五肽)有镇痛作用。微生物产生的许多抗生素如多粘菌素、短杆菌肽等都是肽类,有很强的抗菌作用。多肽指许多氨基酸单位用肽键互相连接构成的长链。肽和蛋白质没有严格的界限,一般把只含有数十个或更少个氨基酸单位的多肽叫做肽,把氨基酸单位比较多的多肽叫蛋白质。常把多肽中的氨基酸单位叫做氨基酸残基,因为这些单位在互相连接时已失去分子的一部分,而不是完整的氨基酸了。只有肽链两端的氨基酸残基才含有自由的α-氨基或自由的α-羧基。有自由α-氨基的末端残基叫做氨基末端(或N端)残基,有自由α-羧基的末端残基叫做羧基末端(或C端)残基。给多肽命名时按照从N端到C端残基的顺序,书写时也按这个顺序。如SerGlyTryAlaLeu这个五肽含有5个氨基酸残基和4个肽键,叫做丝氨酰甘氨酰酪氨酰丙氨酰亮氨酸。肽广泛存在于动植物组织中,其中有许多肽在生物体内有特殊的功能,统称生物活性肽。近年来发现:几乎所有生命科学的重大理论,如免疫防御、生殖控制、肿瘤病变、抗衰防老等都涉及有关的活性肽。这些理论问题无不与临床医学实践密切相关,所以生物活性肽在实际应用上也具有重要意义。生物活性肽的种类很多。如可刺激肾上腺皮质发育的促肾上腺皮质激素是39肽,可使子宫收缩的催产素为九肽,具有吗啡活性的两种重要的脑啡肽均为五肽。许多抗菌素也是肽类物质。又如生长因子受控于基因,在细胞发育过程中起调节和控制作用。这类重要物质为多肽。表皮生长因子含有50个氨基酸残基,神经生长因子由118个氨基酸残基组成。[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333][img=,486,246]https://ng1.17img.cn/bbsfiles/images/2020/06/202006161554536697_4085_3531468_3.jpg!w486x246.jpg[/img][/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]国肽生物主要提供:多肽合成、多肽定制、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、美容肽、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。[/color][/size][/font][font=Helvetica][size=10.5pt][color=#333333]详情请咨询国肽生物[/color][/size][/font]
糖肽是什么包含一个叫做聚糖的碳水化合物的多肽(氨基酸分子)被称为糖肽(Glycopeptides)。由于聚糖在所有生物体细胞中无所不在,并且糖肽有保持健康和防止疾病作用,糖生物学领域出现了分子等方面的研究。【合肥国肽生物】此外,还开发出治疗某些感染类型的糖肽类抗生素。糖肽是通过肽合成过程生产出来的。在此过程中,聚糖绑定多肽,并与其它聚糖结合氨基酸联系在一起,直到产生一个链。新产生的多肽随后通过糖基化绑定蛋白质和脂质。这一酶催化过程让糖肽影响细胞之间的生化沟通。因此,这些多肽在生物体生命过程中有很重要的生物学作用。细胞产生皮肤和有机组织,并有抵御疾病,帮助身体保持体内平衡等作用。糖生物学试图确定糖肽的分子结构,并进一步探索这些多肽在与人体其它相关细胞和分子中的功能。通过确定糖肽结构,进一步了解它们的机制,糖生物学领域工作者能生产出有助于促进健康和延长寿命的治疗方法。例如,糖肽包含一种特质-在癌细胞扩散前必须被分解;因此,了解糖肽结构能让科学家创造一种防止糖肽变质和抑制癌细胞扩散的方法。糖肽抗生素是一种专门开发出来用于抵御特定类型细菌(对青霉素等常见治疗形式抵抗)的抗生素。例如,万古霉素就是一种常见的糖肽类抗生素,可用于治疗肠道发炎。这种疾病通常是由肠道有害细菌导致,而万古霉素能杀死这些细菌。不过,从糖肽提取的抗生素没有抵御病毒感染的功效。这些药物通常通过静脉注射,或口服药片治疗肠道感染。由于糖肽类药物一般被视为抵抗菌株的最后治疗手段,在病人开始感觉好转的情况下也应坚持完整个疗程。否则,再次感染会加剧,并且更难治疗。糖肽抗生素并非没有副作用。如果大剂量给予,这种药会导致皮疹,或通过呼吸道肌肉收紧而干扰呼吸。糖肽连键的主要类型有两种:一,N-糖肽键,是指β-构型的N-乙酰葡糖胺异头碳与天冬酰胺的γ-酰胺N原子共价连接而成的N-糖苷键。二,O-糖肽键,是指单糖的异头碳与羟基氨基酸的羟基O原子共价结合而成的O-糖苷键。我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:17718122172;17718122684;17730030476;17718122397多肽及蛋白质的人工合成多肽及蛋白质的人工合成,指以氨基酸为原料,用化学方法合成多肽或蛋白质。以氨基酸为原料,用化学方法合成多肽或蛋白质。其目的是:①确证天然多肽或蛋白质的结构;②生产天然的、在生物体内含量极微但有医疗或其他生物效用的多肽;③改变部分结构,研究其结构与功能的关系,并设计更有效的药物。
多肽合成技术主要采用多肽合成仪,以固相合成为反应原理,在密闭的防爆玻璃反应器中使氨基酸按照已知顺序(序列,一般从C端-羧基端 向 N端-氨基端)不断添加、反应、合成,操作最终得到多肽载体。固相合成法,大大的减轻了每步产品提纯的难度。为了防止副反应的发生,参加反应的氨基酸的侧链都是保护的。羧基端是游离的,并且在反应之前必须活化。固相合成方法有两种,即Fmoc和tBoc。由于Fmoc比tBoc存在很多优势,现在大多采用Fmoc法合成,但对于某些短肽,tBoc因其产率高的优势仍然被很多企业所采用。【请移步百度搜“[b]合肥国肽生物[/b]”即可】具体合成由下列几个循环组成:(1)去保护:Fmoc保护的柱子和单体必须用一种碱性溶剂(piperidine)去 除氨基的保护基团。(2)激活和交联:下一个氨基酸的羧基被一种活化剂所活化。活化的单体与游离的氨基反应交联,形成肽键。在此步骤使用大量的超浓度试剂驱使反应完成。循环:这两步反应反复循环直到合成完成。(3)洗脱和脱保护:多肽从柱上洗脱下来,其保护基团被一种脱保护剂(TFA) 洗脱和脱保护。多肽的分类多肽有生物活性多肽和人工合成多肽两种。1、生物活性肽生物活性肽(Bioactive Peptides ,BAP)是对生物机体的生命活动有益或是具有生理作用的肽类化合物,是一类相对分子质量小于6000Da , 具有多种生物学功能的多肽。生物活性肽具有多种人体代谢和生理调节功能,易消化吸收,有促进免疫、激素调节、抗菌、抗病毒、降血压、降血脂等作用,是当前国际食品界最热门的研究课题和极具发展前景的功能因子。2、人工合成多肽固相多肽合成方法(SPPS),由于其合成方便,迅速,成为多肽合成的首选方法,而且带来了多肽有机合成上的一次**,并成为了一支独立的学科——固相有机合成,固相合成的发明同时促进了肽合成的自动化。世界上第一台真正意义上的多肽合成仪出现在1980年代初期。基于将单个N-α保护氨基酸反复加到生长的氨基成份上,合成一步步地进行, 通常从合成链的C端氨基酸开始,接着的单个氨基酸的连接通过用DCC,混合炭酐, 或N-carboxy酐方法实现。Carbodiimide方法包括用DCC做连接剂连接N-和C-保护氨基酸。重要的是, 这种连接试剂促接N保护氨基酸自己炭基和C保护氨基酸自由氨基间的缩水,形成肽链, 同时产出N,N?/FONT-dyaylcohercylurea副产物。多肽合成方法1、酸酐法在多肽合成中,最初考虑应用酸酐要追溯到1881年Theodor Curtius对苯甲酰基氨基乙酸合成的早期研究。从氨基乙酸银与苯甲酰氯的反应中,除获得苯甲酰氨基乙酸外,还得到了BZ-Glyn-OH(n=2-6)。早期曾认为,当用苯甲酰氯处理时,N-苯甲酰基氨基酸或N-苯甲酰基肽与苯甲酸形成了活性中间体不对称酸酐。 大约在70年后,Theodor Wieland利用这些发现将混合酸酐法用于现代多肽合成。目前,除该方法外,对称酸酐以及由氨基酸的羧基和氨基甲酸在分子内形成的N-羧基内酸酐(NCA,Leuchs anhydrides)也用肽缩合。最后应该提到,不对称酸酐常常参与生化反应中的酰化反应。2、混合酸酐法有机羧酸和无机酸皆可用于混合酸酐的形成。然而,仅有几个得到了广泛的实际应用,多数情况下,采用氯甲酸烷基酯。过去频繁使用的氯甲酸乙酯,目前主要被氯甲酸异丁酯所替代。由羧基组分和氯甲酸酯起始形成的混合酸酐,其氨解反应的区域选择性依赖依赖于两个互相竞争的羰基的亲电性和(或)空间位阻。在由N保护的氨基酸羧酸盐(羧基组分)和氯甲酸烷基酯(活化组分,例如源于氯甲酸烷基酯)形成混合酸酐时,亲核试剂胺主要进攻氨基酸组分的羧基,形成预期的肽衍生物,并且释放出游离酸形式的活性成分。3、酰基叠氮物法酰基叠氮物法早在1902年就被引入到肽化学中,因此它是最古老的缩合方法之一。在碱性水溶液中,除了与酰基叠氨缩合的游离氨基酸和肽以外,氨基酸酯可用于有机溶剂中。与其他许多缩合方法不同的是,它不需要增加辅助碱或另一等当量的氨基组分来捕获腙酸。 长期以来,一直认为叠氮物法是唯一不发生消旋的缩合方法,随着可选择性裂解的氨基酸保护基引入,该方法经历了一次大规模的复兴。该方法的起始原料分别是晶体状的氨基酸酰肼或肽酰肼64,通过肼解相应的酯很容易得到。4、对称酸酐法Nα-酰基氨基酸的对称酸酐是用于肽键形成的高活性中间体。与混合酸酐法多肽合成相反,它与胺亲核试剂的反应没有模棱两可的区域选择性。但肽缩合产率最高,为50%(以羧基组分计)。虽然由对称酸酐氨解形成的游离Nα-酰基氨基酸可以和目标肽一起,通过饱和碳酸氢钠溶液萃取回收,但在最初,这种方法的实用价值极低。对称酸酐可以用Nα-保护氨基酸与光气,或方便的碳二亚胺反应制得。两当量的Nα-保护氨基酸与-当量的碳二亚胺反应有利于对称酸酐的形成,对称酸酐可以分离出来,也可不经纯化而直接用于后面的缩合反应。基于Nα-烷氧羰基氨基酸的对称酸酐对水解稳定,可采用类似上述纯化混合酸酐的方法进行纯化。[img=,690,300]https://ng1.17img.cn/bbsfiles/images/2019/04/201904221451156040_1751_3531468_3.jpg!w690x300.jpg[/img]我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:17718122172;17718122684;17730030476;17718122397
国肽生物是一家专业从事多肽产品的研发、生产和销售以及多肽技术转让的高新技术企业。BP公司成立之初,便成功收购了国内几家多肽、抗体公司,是目前国内的专业多肽合成、抗体制备、蛋白表达的规模型生产企业。国肽生物专长于荧光标记肽、同位素标记肽、人工胰岛素、药物肽、化妆品肽、长肽困难肽等产品的合成与研发,致力于学术水平的科研提升,搭建学术交流平台,促进前沿、专业的学术知识推广,推动多肽在生物医学材料等领域的研究与应用。[img=,690,300]https://ng1.17img.cn/bbsfiles/images/2019/05/201905091358562505_4016_3531468_3.jpg!w690x300.jpg[/img]我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:17718122172;17718122684;17730030476;17718122397
蛋白质与多肽蛋白质粉 人类的营养物质有许多种类,最为重要的为蛋白质,碳水化合物和脂肪,其它则是微量营养物质,如维生素、电解质和微量元素等。虽然每一种营养物质对人体来说都是不可或缺的,但绝大多数的营养学家都会有充分的理由认为,真正最重要的营养物质是蛋白质。一、蛋白质是构成人体的基本物质。 蛋白质是由氨基酸通过肽链相连而构成的,它是人体包括骨骼、肌肉、皮肤和脑的重要物质基础,同时氨基酸也是生成核酸的基本物质。我们知道,核酸既形成遗传密码,也是体内储存能量的基本物质。因而从根本上说,人体是由蛋白质组成的。构成人体蛋白质的生理功能概括有如下三个方面:1)人体组织的主要构成成份:如肌肉、骨骼、血液、皮肤、神经、肝、心等等。2)具有特殊生理功能:可以这样说,人类的一切生理活动都与蛋白质有关。如酶蛋白能催化机体的一切化学反应,包括蛋白质、脂肪、碳水化合物的消化等;载脂蛋白运送脂肪;血红蛋白运送氧;激素蛋白调节代谢与生理活动包括情感;血浆白蛋白调节渗透压、运输金属离子、胆红素和抗生素等。3)供给机体能量:成年人每日约需要更新400g蛋白质,每克蛋白质彻底分解能释放出约4 Kcal的热量。4)为机体提供氮原料:人体内所必需的嘧啶、嘌呤、肌酸、胆碱、肾上腺素、肉碱、牛磺酸等,都是以多肽、氨基酸为原料的。表1. 世界粮食组织(FAD)和世界卫生组织(WHO)根据中国人的体质和膳食结构推荐的中国人蛋白质的摄入量(RNLs)。年 龄蛋白质RNL(g/d) 初生—6个月 1.5-3 1岁 35 3岁 45 5岁 55 7岁 60 9岁 65 10-16岁 75-85 成年女性 65 成年男性 75 妊娠 +15 乳母 +20 根据统计资料:由于贫困、工作紧张、精神压力、减肥节食、以及肠胃疾病、癌症、贫血、肾病、各种结核病、肝硬化、腹水、烧伤、失血等,以及老龄人均不同程度地存在着蛋白质的摄入不足。 上世纪80年代以来,我国营养学家对7个省18个贫困地区,1万名学龄前儿童进行了为期4年的连续调查,发现营养不良现象非常严重,其中蛋白质的摄入量不足WHO规定的60%。近年社会医学工作调查,在发达地区由于生活节奏加快,精神压力异常增加,以及办公室白领阶层的减肥节食,也导致蛋白质摄入不足,代谢异常的人群增加。二、蛋白质缺乏的体征和临床症状 单纯的蛋白质营养不良又叫加西长病,这或许是来源于非洲的单词,单纯的能量不足时叫消瘦;临床上通常把这两种现象叫单纯性蛋白质能量营养不良症或PEM。单纯的PEM症在临床上较少见到,但在慢性消耗性疾病患者中则常见,尤其是在癌症患者和艾滋病的患者中几乎占到90%以上。 现代都市和贫困地区存在着相当数量的蛋白质营养不良族群,他们的临床表现主要是能量损失或不足,如体力不支、睡眠不安、怕冷、怕热、性冷淡、无法进行正常的体力劳动和运动,其次为肌肉组织萎缩、皮肤松驰;腿部、脸部易水肿、脂肪肝、无名皮疹、伤口愈合不良、记忆力下降、视力减弱等。再者免疫力低下易感冒、感染。在做血检时通常会发现这些族群的血浆蛋白处于正常值的下限,其中白蛋白、转铁蛋白、甲状腺素结合前体蛋白和视轴蛋白(retinol-binding protein)均处于低水平时,患者易于感染各种疾病并且出现早衰症状,如果是儿童则感染后死亡率增加30%-40%,对于这类人群WHO的专家最好的建议就是迅速补充优质(或全价)的蛋白质。三、优质蛋白质和劣质蛋白质的区别。 要弄清楚何为优质蛋白质?何为劣质蛋白质?我们要引入什么是必需氨基酸的概念。营养生理学家、生化学家发现构成人体蛋白质的氨基酸共有21种,而这些氨基酸中其中有4种是可以由体内含碳和含氮底物自己合成的,被称为非必需氨基酸,还有10个必需的氨基酸,是人类机体无法制造需要从饮食中摄取的,另有7个是介于这两者之间的被称为条件必需氨基酸。表2. 必需、条件必需和非必需氨基酸 必需氨基酸条件必需氨基酸 非必需氨基酸 亮氨酸牛黄酸 丙氨酸 异亮氨酸酪氨酸 谷氨酸 缬氨酸甘氨酸 天冬氨酸 赖氨酸丝氨酸 天冬酰胺 苯丙氨酸(酪氨酸)脯氨酸 蛋氨酸(半胱氨酸)谷氨酰酸 苏氨酸 胱氨酸 色氨酸 组氨酸 精氨酸 虽然蛋白质广泛存在于许多动物性和植物性食物中,但是必需氨基酸的构成异差很大,WHO把“蛋白质其组成恰好符合人体需要”的蛋白质称为理想蛋白质,在自然界这种理想的蛋白质普遍认为是鸡蛋蛋白,因此就把鸡蛋蛋白作为衡量蛋白质优劣的参照蛋白,科学家把它作为一把尺子来衡量各种蛋白质,并制定出标准,以4种必需氨基酸为最低限来决定其优劣,即色氨酸、苏氨酸、赖氨酸或者蛋氨酸(半胱氨酸)。 通过比较科学发现,肉、鱼、蛋、牛奶、乳酪含有优质蛋白,大豆、花生、豌豆也含有较多的高质量蛋白。进一步研究发现它们都不够完美,因而要求大家对优质的动物性蛋白和植物性蛋白进行了科学搭配才是最完美的全价蛋白质(complete protein)。表3. 部分高质量蛋白

多肽合成是一个固相合成顺序顺序一般从C端(羧基端)向N端(氨基端)合成。过去的多肽合成是在溶液中进行的称为液相合成法。从1963年Merrifield发展成功了固相多肽合成方法以来,经过不断的改进和完善,到今天固相法已成为多肽和蛋白质合成中的一个常用技术,表现出了经典液相合成法无法比拟的优点,从而大大的减轻了每步产品提纯的难度。多肽合成总的来说分成两种:固相合成和液相多肽合成。【详情请咨询合肥国肽生物】多肽合成技术 Merrifield首次提出了固相多肽合成方法(SPPS)以来,此技术的优势受大众青睐,所以目前大众比较长使用的多肽合成技术手段就是固相合成技术。固相合成肽技术是液相合成肽技术的升华。液相合成技术,也可进行多肽的合成,通常此方法会导致消旋的副反应,或在强碱存在时形成5(4H)-oxaylones和N-acylurea而受到影响。庆幸地是,这些副反应能最小化,但是还不能完全消除。固相多肽合成原理 1963年,Merrifield提出了固相多肽合成方法,由于其合成方便,迅速,成为多肽合成的首选方法,而且带来了多肽有机合成上的一次**,并成为了一支独立的学科——固相有机合成,固相合成的发明同时促进了肽合成的自动化。 例如,国肽生物多肽合成主要是采用Fmoc合成法。Fmoc合成法采用Fmoc为α-氨基的保护基,侧链保护采用苄醇类。合成时将一个Fmoc-氨基酸衍生物共价交联到树脂上,用碱脱除Fmoc,用三乙胺中和游离的氨基末端,然后通过DCC活化、偶联下一个氨基酸,脱保护多采用HF法或TFMSA(三氟甲磺酸)法。多肽合成服务种类 多肽合成服务通常有线性肽合成服务、多种难肽合成服务、修饰肽合成服务、以及部分多肽合成公司还会提供多肽定制服务,定制出有针对性的合成肽。 目前有多肽合成公司提供的线性肽合成可达100个氨基酸,在修饰肽合成上,能提供常见修饰,磷酸化(Ser/Thr/Tyr),环化(酰胺环/二硫键环),荧光标记(5(6)-FAM,FITC,CY5,RhodamineB,PNA,EDNAS/dabcyl等),生物素标记(Biotin,Lys(Biotin))/复合抗原(MAP)/含D型氨基酸,及各种氨基酸衍生物均可合成。多肽产物纯度选择 常见的质谱级多肽纯度,一般要求95% 用于抗体筛选纯度,一般85%即可 NMR和结晶试验中,纯度一般98% 粗品肽,一般50%即可用于多肽筛选[img=,690,120]https://ng1.17img.cn/bbsfiles/images/2019/07/201907051044484496_5504_3531468_3.jpg!w690x120.jpg[/img]国肽生物主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com
多肽,多肽定制,多肽合成-合肥国肽生物是一家专业从事多肽产品的研发、生产和销售以及多肽技术转让的高新技术企业。BP公司成立之初,便成功收购了国内几家多肽、抗体公司,是目前国内的专业多肽合成、抗体制备、蛋白表达的规模型生产企业。详情请咨询www.bankpeptide.com定制多肽种类一、特殊类别多肽:订书肽、同位素标记多肽、磷酸肽、环肽、二硫键多肽、糖肽、药物肽、化妆品肽等二、修饰肽:磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC、CMK、FMK等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、RGD环肽等三、特殊氨基酸多肽:可以将种类繁多的非天然氨基酸合成到多肽上。四、合成方法:多肽固相合成、多肽液相合成、点击化学、一锅法合成等服务内容标准肽:链长至 150个氨基酸,毫克至克级,纯度最高可达99%。不同纯度范围:粗肽、脱盐、75% 、 85% 、90%、95%、98%、99%。常规修饰肽:乙酰化,酰胺化,生物素标记肽,磷酸化肽,D型氨基酸修饰肽等。特殊修饰肽:磺酸化肽(Sulfated-tyrosine),环肽(二硫键环化,首尾环化),荧光标记肽(FITC,Dabcyl/Edans,Dansyl,FAM,Abz/Dnp,Rhodamine等),甲基化多肽(Lys(Me2),Lys(Me),Lys(Me3),Arg(Me),Arg(Me2) -Symetrical,Arg(Me2) -Asymetrical),同位素标记肽(Heavy Isotope Labeled Peptides)、拟肽(peptoid)和点击化学用多肽(Peptides for Click Chemistry)。药用肽,大批量肽。协助客户建立科研肽库。抗原多肽及其与蛋白的交联:KLH,BSA, OVA服务流程确定合成序列,我们将在12小时内容提供准确报价。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:17718122172;17718122684;17730030476;17718122397

国肽生物 提供 多肽合成、多肽修饰、cGMP多肽、目录肽、药物肽/化妆品肽、多肽文库构建、中间体定制及合成、抗体服务、氨基酸、糖肽、订书肽、多肽核酸等.详情请咨询合肥国肽生物多肽合成服务种类多肽合成服务通常有线性肽合成服务、多种难肽合成服务、修饰肽合成服务、以及部分多肽合成公司还会提供多肽定制服务,定制出有针对性的合成肽。目前有多肽合成公司提供的线性肽合成可达150个氨基酸,在修饰肽合成上,能提供常见修饰,磷酸化(Ser/Thr/Tyr),环化(酰胺环/二硫键环),荧光标记(5(6)-FAM,FITC,CY5,RhodamineB,PNA,EDNAS/dabcyl等),生物素标记(Biotin,Lys(Biotin))/复合抗原(MAP)/含D型氨基酸,及各种氨基酸衍生物均可合成。多肽产物纯度选择常见的质谱级多肽纯度,一般要求95%用于抗体筛选纯度,一般85%即可NMR和结晶试验中,纯度一般98%粗品肽,一般50%即可用于多肽筛选国肽生物 提供 多肽合成、多肽修饰、cGMP多肽、目录肽、药物肽/化妆品肽、多肽文库构建、中间体定制及合成、抗体服务、氨基酸、糖肽、订书肽、多肽核酸等优越的领先技术合成方法(固相合成/液相合成)修饰性多肽(常见的N端修饰,C端修饰及其他特殊修饰)偶联技术(KLH,BSA,OVA偶联)首位环化技术,3个磷酸化,3对二硫键胰岛素工艺提供技术转让服务优质的产品服务合成质量:毫克至克级甚至kg合成纯度:Crude,脱盐,70%, 75%, 80%,85%, 90%, 95%,98%,99%定制长度:2-150个氨基酸免费提供:合格的HPLC和MS,COA文件,质量控制包含合格的纯度,合成的质量,分子量,溶解度等((如有特殊需要,可提供核磁,红外,紫外,元素分析,水分含量测定以及氨基酸分析服务))交货期限:1-30个长度最快1-2周交货合成数量:月通量可达8000-10000条药用肽,大批量肽。协助客户建立科研肽库。抗原多肽及其与蛋白的交联:KLH,BSA, OVA服务流程确定合成序列,我们将在12小时内容提供准确报价。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:0551-62626599[img=,690,522]https://ng1.17img.cn/bbsfiles/images/2019/07/201907181006059901_2592_3531468_3.jpg!w690x522.jpg[/img][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2019/07/201907181006182915_5959_3531468_3.jpg!w690x517.jpg[/img]
多肽合成又叫肽链合成,是一个固相合成顺序一般从C端(羧基端)向N端(氨基端)合成。过去的多肽合成是在溶液中进行的称为液相合成法。多肽的合成主要分为两条途径:化学合成多肽和生物合成多肽。请移步百度搜“合肥国肽生物”即可多肽合成的原理多肽合成就是如何把各种氨基酸单位按照天然物的氨基酸排列顺序和连接方式连接起来。由于氨基酸在中性条件下是以分子内的两性离子形式(H3+NCH(R)COO-)存在,因此,氨基酸之间直接缩合形成酰胺键的反应在一般条件下是难于进行的。氨基酸酯的反应活性较高。在100℃下加热或者室温下长时间放置都能聚合生成肽酯,但反应并没有定向性,两种氨基酸a1和a2的酯在聚合时将生成a1a2…、a1a1…、a2a1…等各种任意顺序的混合物。为了得到具有特定顺序的合成多肽,采用任意聚合的方法是行不通的,而只能采用逐步缩合的定向多肽合成方法。一般是如下式所示,即先将不需要反应的氨基或羧基用适当的基团暂时保护起来,然后再进行连接反应,以保证多肽合成的定向进行。式中的X和Q分别为氨基和羧基的保护基,它不仅可以防止乱接副反应的发生,还具有能消除氨基酸的两性离子形式,并使之易溶于有机溶剂的作用。Q在有的情况下也可以不是共价连接的基团,而是由有机强碱(如三乙胺)同氨基酸的羧基氢离子组成的有机阳离子。Y为一强的吸电子基团,它能使羧基活化,而有利于另一氨基酸的自由氨基,对其活化羧基的羧基碳原子进行亲核进攻生成酰胺键。由此所得的连接产物是N端和C端都带有保护基的保护肽,要脱去保护基后才能得到自由的肽。如果肽链不是到此为止,而是还需要从N端或C端延长肽链的话,则可以先选择性地脱去X或Q,然后再同新的N保护氨基酸(或肽)或C保护的氨基酸(或肽)进行第二次连接,并依次不断重复下去,直到所需要的肽链长度为止。对于长肽的多肽合成来说,一般有逐步增长和片段缩合两种伸长肽链的方式,前者是由起始的氨基酸(或肽)开始。每连接一次,接长一个氨基酸,后者则是用N保护肽同C保护肽缩合来得到两者长度相加的新的长肽链。对于多肽合成中含有谷氨酸、天冬氨酸、赖氨酸、精氨酸、组氨酸、半胱氨酸等等带侧链功能团的氨基酸的肽来说,为了避免由于侧链功能团所带来的副反应,一般也需要用适当的保护基将侧链基团暂时保护起来。多肽合成方法分类多肽的合成主要分为两条途径:化学合成多肽和生物合成多肽。化学合成主要是以氨基酸与氨基酸之间缩合的形式来进行。在合成含有特定顺序的多肽时,由于多肽合成原料中含有官能度大于2的氨基酸单体,多肽合成时应将不需要反应的基团暂时保护起来,方可进行成肽反应,这样保证了多肽合成目标产物的定向性。多肽的化学合成又分为液相合成和固相合成。多肽液相合成主要分为逐步合成和片段组合两种策略。逐步合成简洁迅速,可用于各种生物活性多肽片段的合成。片段组合法主要包括天然化学连接和施陶丁格连接。近年,多肽液相片段合成法发展迅速,在多肽和蛋白质合成领域已取得了重大突破。在多肽片段合成法中,根据多肽片段的化学特定性或化学选择性,多肽片段能够自发进行连接,得到目标多肽。因为多肽片段含有的氨基酸残基相对较少,所以纯度较高,且易于纯化。多肽的生物合成方法主要包括发酵法、酶解法,随着生物工程技术的发展,以DNA重组技术为主导的基因工程法也被应用于多肽的合成。多肽的固相合成多肽的合成是氨基酸重复添加的过程,通常从C端向N端(氨基端)进行合成。多肽固相合成的原理是将目的肽的第一个氨基酸C端通过共价键与固相载体连接,再以该氨基酸N端为合成起点,经过脱去氨基保护基和过量的已活化的第二个氨基酸进行反应,接长肽链,重复操作,达到理想的合成肽链长度,最后将肽链从树脂上裂解下来,分离纯化,获得目标多肽。1、Boc多肽合成法Boc方法是经典的多肽固相合成法,以Boc作为氨基酸α-氨基的保护基,苄醇类作为侧链保护基,Boc的脱除通常采用三氟乙酸(TFA)进行。多肽合成时将已用Boc保护好的N-α-氨基酸共价交联到树脂上,TFA切除Boc保护基,N端用弱碱中和。肽链的延长通过二环己基碳二亚胺(DCC)活化、偶联进行,最终采用强酸氢氟酸(HF)法或三氟甲磺酸(TFMSA)将合成的目标多肽从树脂上解离。在Boc多肽合成法中,为了便于下一步的多肽合成,反复用酸进行脱保护,一些副反应被带入实验中,例如多肽容易从树脂上切除下来,氨基酸侧链在酸性条件不稳定等。2、Fmoc多肽合成法Carpino和Han以Boc多肽合成法为基础发展起来一种多肽固相合成的新方法——Fmoc多肽合成法。Fmoc多肽合成法以Fmoc作为氨基酸α-氨基的保护基。其优势为在酸性条件下是稳定的,不受TFA等试剂的影响,应用温和的碱处理可脱保护,所以侧链可用易于酸脱除的Boc保护基进行保护。肽段的最后切除可采用TFA/二氯甲烷(DCM)从树脂上定量完成,避免了采用强酸。同时,与Boc法相比,Fmoc法反应条件温和,副反应少,产率高,并且Fmoc基团本身具有特征性紫外吸收,易于监测控制反应的进行。Fmoc法在多肽固相合成领域应用越来越广泛。多肽液相分段合成随着多肽合成的发展,多肽液相分段合成(即多肽片段在溶液中依据其化学专一性或化学选择性,自发连接成长肽的合成方法)在多肽合成领域中的作用越来越突出。其特点在于可以用于长肽的合成,并且纯度高,易于纯化。多肽液相分段合成主要分为天然化学连接和施陶丁格连接。天然化学连接是多肽分段合成的基础方法,局限在于所合成的多肽必须含半光氨酸(Cys)残基,因而限定了天然化学连接方法的应用范围。天然化学连接方法的延伸包括化学区域选择连接、可除去辅助基连接、光敏感辅助基连接。施陶丁格连接方法是另一种基础的片段连接方法,其为多肽片段连接途径开拓了更广阔的思路。正交化学连接方法是施陶丁格连接方法的延伸,通过简化膦硫酯辅助基来提高片段间的缩合率。其他多肽合成方法1、氨基酸的羧内酸酐法(NCA)氨基酸的羧内酸酐的氨基保护基也可活化羧基。NCA的原理:在碱性条件下,氨基酸阴离子与NCA形成一个更稳定的氨基甲酸酯类离子,在酸化时该离子失去二氧化碳,生成二肽。生成的二肽又与其他的NCA结合,反复进行。NCA适用于短链肽片段的多肽合成,其周期短、操作简单、成本低、得到产物分子量高,在目前多肽合成中所占比例较大,技术也较为通用。2、组合化学法20世纪80年代,以固相多肽合成为基础提出了组合化学法,即氨基酸的构建单元通过组合的方式进行连接,合成出含有大量化合物的化学库,并从中筛选出具有某种理化性质或药理活性化合物的一套多肽合成策略和筛选方案。组合化学法的多肽合成策略主要包括:混合-均分法、迭代法、光控定位组合库法、茶叶袋法等。组合化学法的最大优点在于可同时合成多种化合物,并且能最大限度地筛选各种新化合物及其异构体。3、酶解法酶解法是用生物酶降解植物蛋白质和动物蛋白质,获得小分子多肽。酶解法因其多肽产量低、投资大、周期长、污染严重,未能实现工业化生产。酶解法获得的多肽能够保留蛋白质原有的营养价值,并且可以获得比原蛋白质更多的功能,更加绿色,更加健康。4、基因工程法基因工程法主要以DNA重组技术为基础,通过合适的DNA模板来控制多肽的序列合成。有研究者通过基因工程法获得了准弹性蛋白-聚缬氨酸-脯氨酸-甘氨酸-缬氨酸-甘氨酸肽(VPGVG)。利用基因工程技术生产的活性多肽还有肽类抗生素、干扰素类、白介素类、生长因子类、肿瘤坏死因子、人生长激素,血液中凝血因子、促红细胞生成素,组织非蛋白纤溶酶原等。基因工程法合成多肽具有表达定向性强,安全卫生,原料来源广泛和成本低等优点,但因存在高效表达,不易分离,产率低的问题,难以实现规模化生产。5、发酵法发酵法是从微生物代谢产物中获得多肽的方法。虽然发酵法的成本低,但其应用范围较窄,因为现在微生物能够独立合成的聚氨基酸只有ε-聚赖氨酸(ε-PL)、γ-聚谷氨酸(γ-PGA)和蓝细菌肽。[align=center][img=,770,348]https://ng1.17img.cn/bbsfiles/images/2019/03/201903151633244062_8177_3531468_3.jpg!w770x348.jpg[/img][/align]请移步百度搜“合肥国肽生物”即可我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。
合肥国肽生物科技有限公司(简称:国肽生物TM)成立于2014年,是一家专业从事多肽产品的研发、生产和销售以及多肽技术转让的国家级高新技术企业。BP公司成立之初,便成功收购了国内几家多肽、抗体公司,是目前国内最大的专业多肽合成、抗体制备、蛋白表达的规模型生产企业。 国肽生物专长于荧光标记肽、同位素标记肽、人工胰岛素、药物肽、化妆品肽、长肽困难肽等产品的合成与研发,致力于学术水平的科研提升,搭建学术交流平台,促进前沿、专业的学术知识推广,推动多肽在生物医学材料等领域的研究与应用。公司产品广泛应用于药物研发,抗体的制备(包括单抗与双抗),荧光分子探针的构建以及细胞透膜研究、活体成像、新型材料研发和质谱分析等研究领域;目前我们已经与军科院、天津药物研究所、中科院物理研究所等研究机构,清华、北大、复旦等高校,以及国外著名药企建立了长期友好的合作交流关系。 国肽生物以科技创新为动力,提升企业核心竞争力。公司拥有一支由行业内领军人才组成的研发创新团队,硕士研发人员占企业员工总数的15%以上,同时公司还邀请国内外顶级生物医学科学家担任科学顾问。公司成立首年,通过多肽生产设施的精细改良、多肽研发工艺的自主创新,突破了多肽产品快速化、规模化生产技术瓶颈,获得了7项实用新型专利和2项发明专利。 国肽生物公司配备了一流的多肽合成、纯化、冻干、质量检测与分析等精密仪器,从美国、日本等国引进了[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用仪[/color][/url]、超高压液相色谱、紫外分光光度计等专用设备,以多肽合成与研发为核心,搭建起全产业链产品分析检测平台,为广大客户提供专业可靠的多肽及相关产品理化性质分析,纯度分析,质谱分析,CHN元素含量分析,红外,紫外光谱分析等分析检测服务。 国肽生物的创立,源自于公司对多肽行业未来发展的认同,公司秉承“质量第一,服务至上”的经营理念,带着行业责任感与使命感,立志于在全球范围内树立一个民族品牌,重新引领肽行业的健康、快速发展。

国肽生物 提供 多肽合成、多肽修饰、蛋白多肽、cGMP多肽、多肽化学合成、目录肽、药物肽/化妆品肽、多肽文库构建、中间体定制及合成、抗体服务、氨基酸、糖肽、订书肽、多肽核酸等多肽及蛋白质的人工合成多肽及蛋白质的人工合成,指以氨基酸为原料,用化学方法合成多肽或蛋白质。以氨基酸为原料,用化学方法合成多肽或蛋白质。其目的是:①确证天然多肽或蛋白质的结构;②生产天然的、在生物体内含量极微但有医疗或其他生物效用的多肽;③改变部分结构,研究其结构与功能的关系,并设计更有效的药物。[img=,625,151]https://ng1.17img.cn/bbsfiles/images/2019/06/201906190944309669_566_3531468_3.jpg!w625x151.jpg[/img]我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。详情请咨询合肥国肽生物www.bankpeptide.com
合肥国肽生物科技有限公司(简称:国肽生物TM)成立于2014年,是一家专业从事多肽产品的研发、生产和销售以及多肽技术转让的高新技术企业。BP公司成立之初,便成功收购了国内几家多肽、抗体公司,是目前国内的专业多肽合成、抗体制备、蛋白表达的规模型生产企业。国肽生物专长于荧光标记肽、同位素标记肽、人工胰岛素、药物肽、化妆品肽、长肽困难肽等产品的合成与研发,致力于学术水平的科研提升,搭建学术交流平台,促进前沿、专业的学术知识推广,推动多肽在生物医学材料等领域的研究与应用。公司产品广泛应用于药物研发,抗体的制备(包括单抗与双抗),荧光分子探针的构建以及细胞透膜研究、活体成像、新型材料研发和质谱分析等研究领域国肽生物按照客户定制要求供应高品质普通多肽。我们拥有成熟的多肽合成纯化方法,利用SPPS方法和液相合成方法为客户提供高品质多肽。我们的服务特点是:1. 纯度:我们提供粗品肽和纯度纯度为70%,75%,80%,85%,90%,95%,98%,99%的纯品多肽。2.脱盐和转盐:根据客户要求,我们可以对多肽进行脱TFA盐处理,也可以转为醋酸盐。3.交货期限:30个氨基酸之内,一般2-3周,最快1-2周。4.质量控制:每条多肽都免费提供合格的HPLC,MS和COA文件。5.售后服务:1-2周内可以提出异议,我们免费复测,不合格免费退货,1-3个月内使用不合格可以免费提供复测,样品免费保存3个月。国肽生物根据客户要求,供应各种修饰型多肽。1.磷酸化的Ser、Tyr和Thr修饰的多肽:我们提供单磷酸化和多磷酸化多肽服务,目前我们已经能够提供四个磷酸化位点修饰的多肽。2.5(6)-FAM,FITC,CY5,RhodamineB,PNA,EDNAS/dabcyl等荧光标记修饰的多肽:荧光标记修饰多肽技术是我们国肽生物的代表性多肽合成技术,我们的这项技术已经相当成熟。3.生物素Biotin,Lys(Biotin)修饰的多肽:生物素是维生素B2的组成部分,Biotin,Lys(Biotin)修饰的多肽也是客户经常定制的多肽。我们提供生物素修饰的多肽已经有将近100%的成功率。4.含有一对或多对二硫键修饰的多肽:二硫键在蛋白质的结构稳定中起到重要作用,目前我们已经能够为客户提供四对二硫键修饰的多肽。5.含有同位素C13,N15修饰的多肽:同位素标记的多肽主要应用于医学和生物学领域,通常价格较高,为了满足客户需要,我们接受微克级的同位素多肽定制。6.含有特殊氨基酸修饰的多肽:例如,D型氨基酸,氨基酸衍生物,脂肪族羧酸等等,都在我们接受的定制范围内。国肽生物提供150个氨基酸以内的长肽合成服务。多肽合成过程中,肽链过长时,经常会出现缺残基,氨基酸缩合困难等情况,基于这些现象,我们开发了三种有效提高反应成功率的方案:1. 微波合成法:对于合成过程中出现的一些难以缩合的氨基酸,我们采用微波法进行合成,该方法效果显著,并且大大缩短了反应时间。2. 片段合成法:当某些多肽用常规合成方法合成困难,我们也会采用将多肽中某一段的某几个氨基酸缩合之后作为一个整体缩合到肽链上去,这种方法也能够解决许多合成中存在的问题。3.酰肼合成法:酰肼法合成多肽的方法是将固相合成的 N末端Cys 多肽和 C末端多肽酰肼之间的化学选择性反应形成酰胺键而实现多肽的连接,该方法根据肽链中Cys的位置,将整条肽链分成多条序列分别合成,最终经过液相缩合反应得到目标肽,显著地提高了最终产物纯度,广泛适用于含有Cys的长链多肽的合成。国肽生物拥有成熟的长肽合成工艺,能够根据客户定制的多肽序列,快速有效地设计合成方案并迅速开始合成,更快更好的为客户提供所需的服务是我们不变的坚持。详情请咨询合肥国肽生物www.bankpeptide.com
http://www.people.com.cn/mediafile/pic/20110923/57/3100742272053981481.jpg这是人体肺泡的内部色彩增强显微照片。其实肺泡就是一个空腔,在这里血液和气体进行物质交换,人体代谢二氧化碳,吸入新鲜氧气。
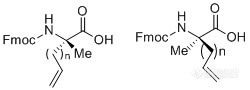
[align=center]全国多肽合成方法_北京多肽合成_上海多肽合成技术[/align]生物体内的多种生命进程调节都是通过蛋白质与蛋白质之间的相互作用来实现的。例如病毒的自组装,细胞的生长,分裂,分化等过程。而通常蛋白-蛋白相互作用的界面太大,从而使小分子药物很难对其进行靶向定位,达到高效特异性地阻断这种相互作用,展现良好的治疗效果。蛋白类药物因为很难顺利通过细胞膜所以也达不到直接靶向细胞内相互作用的效果,因此,研究者们开始寻求一种能够克服这两种药物缺点的既能够进入细胞膜又能特异性靶向蛋白-蛋白相互作用的新的药物分子。研究表明,具有α-螺旋结构和富含正电荷的多肽可以穿过细胞膜。但是一旦从母体分离就不能保持其原有的二级结构,构象的不稳定导致其与蛋白质的结合作用减弱,而普通的线性多肽不能穿过细胞膜且容易被水解。经过不断尝试,Verdine等发展了一种新型结构的多肽,这种多肽被称为订书肽,它是一种全碳支架的具有α-螺旋结构的多肽,全碳支架稳定α-螺旋结构,增强了多肽分子与蛋白质的相互作用,并且订书肽能够穿过细胞膜,不容易被水解,相比于之前的小分子药物和蛋白类药物,具有更高的药理活性。订书肽的合成与普通多肽合成的区别在于在固相合成肽链过程中引入两个含有α-甲基,α-烯基的非天然氨基酸,然后两个非天然氨基酸之间发生烯烃复分解反应环化构成稳定α-螺旋结构构象的全碳支架,进而合成订书肽。[align=center][img=,250,90]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041627034238_7646_3531468_3.jpg!w250x90.jpg[/img][/align]上图为两种不同构型的含有α-甲基,α-烯基的非天然氨基酸的一般结构。这种类型的氨基酸合成方法一般为:[align=center][img=,674,282]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041627250927_145_3531468_3.jpg!w674x282.jpg[/img][/align]订书肽的一般合成路线为:[align=center][img=,674,452]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041627446037_6078_3531468_3.jpg!w674x452.jpg[/img][/align]国肽生物始终坚持客户至上的经营理念,通过长久的实验累积,不断优化合成条件和纯化工艺,已经具备了成熟的订书肽合成工艺,具有了向全球提供高品质的订书多肽的能力,能够充分满足客户的各种研发需要。成功案例:合成下列结构订书肽[align=center][img=,560,298]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041628020314_7677_3531468_3.jpg!w560x298.jpg[/img][/align]HPLC分析:[align=center][img=,598,256]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041629267089_1992_3531468_3.jpg!w598x256.jpg[/img][/align]MS分析:[align=center][img=,598,236]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041629448117_2524_3531468_3.jpg!w598x236.jpg[/img][/align]合肥国肽生物官网:http://www.bankpeptide.com[img=,220,52]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041630056938_3130_3531468_3.jpg!w220x52.jpg[/img]翻译:translation:Peptide Synthesis Method_Peptide Synthesis_Peptide Synthesis TechnologyThe regulation of multiple life processes in an organism is achieved through the interaction between proteins and proteins. For example, self-assembly of viruses, cell growth, division, differentiation and the like. Usually, the interface of protein-protein interaction is too large, so that it is difficult for small molecule drugs to target them, and the interaction is effectively and specifically blocked, showing good therapeutic effects. Because protein drugs are difficult to pass through the cell membrane, they do not directly target intracellular interactions. Therefore, researchers have begun to seek a solution that can overcome the shortcomings of these two drugs and enter the cell membrane and specific targets. A new drug molecule that interacts with protein-proteins.Studies have shown that polypeptides with alpha-helical structures and positively charged can cross cell membranes. However, once it is separated from the mother, its original secondary structure cannot be maintained. The instability of the conformation causes its binding to proteins to be weakened, while the ordinary linear polypeptide cannot pass through the cell membrane and is easily hydrolyzed. After repeated attempts, Verdine et al. developed a novel structure of a peptide called a staple peptide, which is an all-carbon scaffold with an α-helical structure and an all-carbon scaffold that stabilizes the α-helical structure. The interaction between the polypeptide molecule and the protein is enhanced, and the peptide can pass through the cell membrane and is not easily hydrolyzed, and has higher pharmacological activity than the previous small molecule drugs and protein drugs.The synthesis of a peptide is different from the synthesis of a common polypeptide by introducing two unnatural amino acids containing an α-methyl group, an α-alkenyl group, and then an olefin metathesis reaction between two unnatural amino acids. Cyclization constitutes a full carbon scaffold that stabilizes the conformation of the α-helical structure, thereby synthesizing the book peptide.[align=center][img=,250,90]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041632306548_5671_3531468_3.jpg!w250x90.jpg[/img][/align]The top panel shows the general structure of an unnatural amino acid containing alpha-methyl, alpha-alkenyl groups in two different configurations. This type of amino acid synthesis is generally:[align=center][img=,674,282]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041632550117_8499_3531468_3.jpg!w674x282.jpg[/img][/align]The general synthetic route for a peptide is:[align=center][img=,674,452]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041633232025_6374_3531468_3.jpg!w674x452.jpg[/img][/align]National Peptide Biotechnology always adheres to the customer-oriented business philosophy. Through long-term experimental accumulation, continuous optimization of synthesis conditions and purification processes, it has a mature synthesis process of peptides, and has the ability to provide high-quality peptides to the world. Can fully meet the various research and development needs of customers.success case:Synthesis of the following structural peptides[align=center][img=,560,298]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041633554208_919_3531468_3.jpg!w560x298.jpg[/img][/align]HPLC analysis:[align=center][img=,598,256]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041634221078_9006_3531468_3.jpg!w598x256.jpg[/img][/align]MS analysis:[align=center][img=,598,236]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041634490741_8433_3531468_3.jpg!w598x236.jpg[/img][/align][color=#333333]Bankpeptide biological technology co.,LTD:http://www.bankpeptide.com[/color][color=#333333][img=,220,52]https://ng1.17img.cn/bbsfiles/images/2019/01/201901041635507626_7416_3531468_3.jpg!w220x52.jpg[/img][/color]

多肽合成方法分类多肽的合成主要分为两条途径:化学合成多肽和生物合成多肽。化学合成主要是以氨基酸与氨基酸之间缩合的形式来进行。在合成含有特定顺序的多肽时,由于多肽合成原料中含有官能度大于2的氨基酸单体,多肽合成时应将不需要反应的基团暂时保护起来,方可进行成肽反应,这样保证了多肽合成目标产物的定向性。多肽的化学合成又分为液相合成和固相合成。【合肥国肽生物】多肽液相合成主要分为逐步合成和片段组合两种策略。逐步合成简洁迅速,可用于各种生物活性多肽片段的合成。片段组合法主要包括天然化学连接和施陶丁格连接。近年,多肽液相片段合成法发展迅速,在多肽和蛋白质合成领域已取得了重大突破。在多肽片段合成法中,根据多肽片段的化学特定性或化学选择性,多肽片段能够自发进行连接,得到目标多肽。因为多肽片段含有的氨基酸残基相对较少,所以纯度较高,且易于纯化。多肽的生物合成方法主要包括发酵法、酶解法,随着生物工程技术的发展,以DNA重组技术为主导的基因工程法也被应用于多肽的合成。多肽的固相合成多肽的合成是氨基酸重复添加的过程,通常从C端向N端(氨基端)进行合成。多肽固相合成的原理是将目的肽的第一个氨基酸C端通过共价键与固相载体连接,再以该氨基酸N端为合成起点,经过脱去氨基保护基和过量的已活化的第二个氨基酸进行反应,接长肽链,重复操作,达到理想的合成肽链长度,最后将肽链从树脂上裂解下来,分离纯化,获得目标多肽。1、Boc多肽合成法Boc方法是经典的多肽固相合成法,以Boc作为氨基酸α-氨基的保护基,苄醇类作为侧链保护基,Boc的脱除通常采用三氟乙酸(TFA)进行。多肽合成时将已用Boc保护好的N-α-氨基酸共价交联到树脂上,TFA切除Boc保护基,N端用弱碱中和。肽链的延长通过二环己基碳二亚胺(DCC)活化、偶联进行,最终采用强酸氢氟酸(HF)法或三氟甲磺酸(TFMSA)将合成的目标多肽从树脂上解离。在Boc多肽合成法中,为了便于下一步的多肽合成,反复用酸进行脱保护,一些副反应被带入实验中,例如多肽容易从树脂上切除下来,氨基酸侧链在酸性条件不稳定等。2、Fmoc多肽合成法Carpino和Han以Boc多肽合成法为基础发展起来一种多肽固相合成的新方法——Fmoc多肽合成法。Fmoc多肽合成法以Fmoc作为氨基酸α-氨基的保护基。其优势为在酸性条件下是稳定的,不受TFA等试剂的影响,应用温和的碱处理可脱保护,所以侧链可用易于酸脱除的Boc保护基进行保护。肽段的最后切除可采用TFA/二氯甲烷(DCM)从树脂上定量完成,避免了采用强酸。同时,与Boc法相比,Fmoc法反应条件温和,副反应少,产率高,并且Fmoc基团本身具有特征性紫外吸收,易于监测控制反应的进行。Fmoc法在多肽固相合成领域应用越来越广泛。多肽液相分段合成随着多肽合成的发展,多肽液相分段合成(即多肽片段在溶液中依据其化学专一性或化学选择性,自发连接成长肽的合成方法)在多肽合成领域中的作用越来越突出。其特点在于可以用于长肽的合成,并且纯度高,易于纯化。多肽液相分段合成主要分为天然化学连接和施陶丁格连接。天然化学连接是多肽分段合成的基础方法,局限在于所合成的多肽必须含半光氨酸(Cys)残基,因而限定了天然化学连接方法的应用范围。天然化学连接方法的延伸包括化学区域选择连接、可除去辅助基连接、光敏感辅助基连接。施陶丁格连接方法是另一种基础的片段连接方法,其为多肽片段连接途径开拓了更广阔的思路。正交化学连接方法是施陶丁格连接方法的延伸,通过简化膦硫酯辅助基来提高片段间的缩合率。其他多肽合成方法1、氨基酸的羧内酸酐法(NCA)氨基酸的羧内酸酐的氨基保护基也可活化羧基。NCA的原理:在碱性条件下,氨基酸阴离子与NCA形成一个更稳定的氨基甲酸酯类离子,在酸化时该离子失去二氧化碳,生成二肽。生成的二肽又与其他的NCA结合,反复进行。NCA适用于短链肽片段的多肽合成,其周期短、操作简单、成本低、得到产物分子量高,在目前多肽合成中所占比例较大,技术也较为通用。2、组合化学法20世纪80年代,以固相多肽合成为基础提出了组合化学法,即氨基酸的构建单元通过组合的方式进行连接,合成出含有大量化合物的化学库,并从中筛选出具有某种理化性质或药理活性化合物的一套多肽合成策略和筛选方案。组合化学法的多肽合成策略主要包括:混合-均分法、迭代法、光控定位组合库法、茶叶袋法等。组合化学法的最大优点在于可同时合成多种化合物,并且能最大限度地筛选各种新化合物及其异构体。3、酶解法酶解法是用生物酶降解植物蛋白质和动物蛋白质,获得小分子多肽。酶解法因其多肽产量低、投资大、周期长、污染严重,未能实现工业化生产。酶解法获得的多肽能够保留蛋白质原有的营养价值,并且可以获得比原蛋白质更多的功能,更加绿色,更加健康。4、基因工程法基因工程法主要以DNA重组技术为基础,通过合适的DNA模板来控制多肽的序列合成。有研究者通过基因工程法获得了准弹性蛋白-聚缬氨酸-脯氨酸-甘氨酸-缬氨酸-甘氨酸肽(VPGVG)。利用基因工程技术生产的活性多肽还有肽类抗生素、干扰素类、白介素类、生长因子类、肿瘤坏死因子、人生长激素,血液中凝血因子、促红细胞生成素,组织非蛋白纤溶酶原等。基因工程法合成多肽具有表达定向性强,安全卫生,原料来源广泛和成本低等优点,但因存在高效表达,不易分离,产率低的问题,难以实现规模化生产。5、发酵法发酵法是从微生物代谢产物中获得多肽的方法。虽然发酵法的成本低,但其应用范围较窄,因为现在微生物能够独立合成的聚氨基酸只有ε-聚赖氨酸(ε-PL)、γ-聚谷氨酸(γ-PGA)和蓝细菌肽。[img=,457,333]https://ng1.17img.cn/bbsfiles/images/2019/04/201904221507346400_2482_3531468_3.jpg!w457x333.jpg[/img]我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:17718122172;17718122684;17730030476;17718122397
国肽生物美容多肽相关产品乙酰基六肽-8三肽-1铜棕榈酰三肽-1棕榈酰四肽-7棕榈酰五肽-4棕榈酰六肽;脂肽乙酰基五肽-1乙酰基八肽-1棕榈酰三肽-3/5寡肽-1五肽-18乙酰基四肽-5详情请咨询合肥国肽生物http://www.bankpeptide.com/product.do?id=4b2b73e8-69b0-4b10-ab40-d6834d1afe1f国肽生物主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等
国肽生物是一家专业从事多肽产品的研发、生产和销售以及多肽技术转让的高新技术企业。BP公司成立之初,便成功收购了国内几家多肽、抗体公司,是目前国内的专业多肽合成、抗体制备、蛋白表达的规模型生产企业。国肽生物根据客户要求,供应各种修饰型多肽。1.磷酸化的Ser、Tyr和Thr修饰的多肽:我们提供单磷酸化和多磷酸化多肽服务,目前我们已经能够提供四个磷酸化位点修饰的多肽。2. 5(6)-FAM,FITC,CY5,RhodamineB,PNA,EDNAS/dabcyl等荧光标记修饰的多肽:荧光标记修饰多肽技术是我们国肽生物的代表性多肽合成技术,我们的这项技术已经相当成熟。3.生物素Biotin,Lys(Biotin)修饰的多肽:生物素是维生素B2的组成部分,Biotin,Lys(Biotin)修饰的多肽也是客户经常定制的多肽。我们提供生物素修饰的多肽已经有将近100%的成功率。4.含有一对或多对二硫键修饰的多肽:二硫键在蛋白质的结构稳定中起到重要作用,目前我们已经能够为客户提供四对二硫键修饰的多肽。5.含有同位素C13,N15修饰的多肽:同位素标记的多肽主要应用于医学和生物学领域,通常价格较高,为了满足客户需要,我们接受微克级的同位素多肽定制。6.含有特殊氨基酸修饰的多肽:例如,D型氨基酸,氨基酸衍生物,脂肪族羧酸等等,都在我们接受的定制范围内。国肽生物提供150个氨基酸以内的长肽合成服务。多肽合成过程中,肽链过长时,经常会出现缺残基,氨基酸缩合困难等情况,基于这些现象,我们开发了三种有效提高反应成功率的方案:1. 微波合成法:对于合成过程中出现的一些难以缩合的氨基酸,我们采用微波法进行合成,该方法效果显著,并且大大缩短了反应时间。2. 片段合成法:当某些多肽用常规合成方法合成困难,我们也会采用将多肽中某一段的某几个氨基酸缩合之后作为一个整体缩合到肽链上去,这种方法也能够解决许多合成中存在的问题。3.酰肼合成法:酰肼法合成多肽的方法是将固相合成的 N末端Cys 多肽和 C末端多肽酰肼之间的化学选择性反应形成酰胺键而实现多肽的连接,该方法根据肽链中Cys的位置,将整条肽链分成多条序列分别合成,最终经过液相缩合反应得到目标肽,显著地提高了最终产物纯度,广泛适用于含有Cys的长链多肽的合成。国肽生物拥有成熟的长肽合成工艺,能够根据客户定制的多肽序列,快速有效地设计合成方案并迅速开始合成,更快更好的为客户提供所需的服务是我们不变的坚持。国肽生物按照客户定制要求供应高品质普通多肽。我们拥有成熟的多肽合成纯化方法,利用SPPS方法和液相合成方法为客户提供高品质多肽。我们的服务特点是:1. 纯度:我们提供粗品肽和纯度纯度为70%,75%,80%,85%,90%,95%,98%,99%的纯品多肽。2.脱盐和转盐:根据客户要求,我们可以对多肽进行脱TFA盐处理,也可以转为醋酸盐。3.交货期限:30个氨基酸之内,一般2-3周,最快1-2周。4.质量控制:每条多肽都免费提供合格的HPLC,MS和COA文件。5.售后服务:1-2周内可以提出异议,我们免费复测,不合格免费退货,1-3个月内使用不合格可以免费提供复测,样品免费保存3个月。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:0551-62626599[img=,690,311]https://ng1.17img.cn/bbsfiles/images/2019/04/201904111437129214_3530_3531468_3.jpg!w690x311.jpg[/img]
未婚女性,想了解一下ICP辐射有多大,对人体的危害有多大,穿市场上普通的防辐射服管用吗?我是做稀土分析的,废气对人体的危害大还是辐射对人体的辐射大。马上要结婚了,很想知道
1.多肽合成的基本原理?多肽固相合成法是多肽合成化學的一個重大的突破。它的最大特點是不必純化中間產物,合成過程可以連續進行,進而為多肽合成的自動化奠定了基礎。目前全自動多肽的合成,基本都是固相合成。其基本過程如下:基於Fmoc化學合成,先將所要合成的目標多肽的C-端氨基酸的羧基以共價鍵形式與一個不溶性的高分子樹脂相連,然後以這一氨基酸的氨基作為多肽合成的起點,同其他的氨基酸已經活化的羧基作用形成肽鍵,不斷重複這一過程,即可得到多肽。根據多肽的氨基酸組成不同,多肽後處理方式不同,純化方式也有差異。2.做免疫用的多肽多長為合適?答:一般約10-15個氨基酸,當然長一些免疫效果好一些,不過合成費用也會增加。MAP多肽則希望長度在15aa以上,效果較好。另外,10aa以下的多肽免疫效果比較差。3.免疫用多肽的純度需要很高嗎?答:一般而言, 免疫用Peptide,70-85%即可。4.我們合成的多肽溶解性不好,多肽就有問題對嗎?答:很難準確預測一個多肽的溶解性及合適的溶劑是什麼。如果多肽難以溶解就認為多肽合成有問題這個觀念並不正確。5.多肽狀態是如何?如何保存儲存?答:我們提供的多肽是粉末狀,一般為灰白色,組成不同,多肽粉末的顏色有差異,多肽一般長期保存需要避光保存,並應保存在-20度,短期可以保存在4度。可以短時間的話是以室溫運輸。6.如何溶解多肽?答:溶解多肽是非常複雜的事情,一般很難一下子確定合適的溶劑。通常是先取一點試驗,在沒有確定合適的溶劑前千萬不要合部溶解。下列方法有助於您選擇合適的溶劑:(1)判定多肽的電荷特定,設定酸性氨基酸Asp(D),Glu(E)和C端COOH為-1;鹼性氨基酸Lys(K),Arg(R),His(H)及N端NH2為+1,其他氨基酸的電荷為0。計算出將電荷數。(2)如果淨電荷數 0,多肽為鹼性,用水溶解:如果不溶解或溶解性不大,加入醋酸(10%以上);如果多肽還不能溶解,加入少量TFA(25ul)溶解,然後加入500ul水稀釋。(3)如果淨電荷數0,多肽為酸性,用水溶解;如果不溶解或溶解性不大,加入氨水(25ul)溶解,然後加入500ul水稀釋。(4)如果淨電荷數=0,多肽為中性,一般需要用有機溶劑如乙腈,甲醇或異丙醇,DMSO等溶解。還有人建議需要尿素來溶解疏水性很大的多肽。7.非HPLC純化的多肽中有哪些雜質?答:粗品和脫鹽級別的多肽中多肽和非多肽類雜質:如非全長多肽和多肽後處理的一些原料如DTT、TFA等8.HPLC純化的多肽有哪些雜質?答:經過HPLC純化的多肽,仍會有一些一些雜質存在,其中的雜質主要是短肽和微量TFA。9.多長的多肽為合適?答:多肽合成需要考慮多肽的長度,電荷,親疏水性等因素。長度越長,合成粗品的純度和產率都隨著降低,純化的難度和無法合成的幾率就會大些。當然多肽功能區的序列是無法改變的,但是為了多肽的順利合成,有時不得不在功能取的上下游增加一些輔助氨基酸,以改善多肽的溶解性和親疏水性。如果多肽太短,合成也可能有問題,主要問題是合成的多肽在後處理過程中有一定的難度,5肽以下的多肽,一般要有疏水的氨基酸,否則後處理難度加大。15個氨基酸殘基以下的多肽一般都可以得到滿意的產率和得率。10.如何從多肽序列中判定多肽的溶解性?(1)多肽中如果含有高比例的疏水性很強的氨基酸如和Leu,Val,IIe,Met,Phe和Trp,多肽很難溶解與水性溶液中或根本不可能溶解。這些氨基酸無論是純化或合成,都有可能有問題。(2)一般情況下疏水性氨基酸的比例50%,不能連續5個連續aa為疏水性,帶電荷的氨基酸的(正電荷K,R,H,N-terminus,負電荷D,E,C- terminus)的比例達到20%,在多肽的N或C短如果能增加極性氨基酸,也可以改善溶解性。11.為什麼含有Cys,Met,或Trp的多肽難合成?答:含有Cys, Met,或Trp的多肽難以合成,同時難以獲得高純度的產品。主要因為這些基團不穩定,易氧化。這些多肽的使用和儲存都需要特別注意,避免反復開啟蓋子。12.為什麼有些多肽的合成產率或純度會比較低?答:多肽合成與引子合成有比較大的區別,不能合成的引子很少,但是不能合成的多肽經常有。如Val,Ile,Tyr,Phe,Trp,Leu,Gln,和Thr這些氨基酸比鄰或重複時,多肽鏈在合成過程中不能完全舒展溶解,合成效率下降。以下幾種情形,合成效率和產物的純度都比較低,如:重複Pro,Ser-Ser,重複Asp,4個連續Gly等.13.多肽是如何純化的?答:多肽純化一般使用反相柱(如C8,C18等),214nm。緩衝體系通常為含TFA的溶劑,pH 2.0 。Buffer A為含0.1%TFA in ddH2O,Buffer B為1%TFA/ACN/ pH 2.0。純化前用Buffer A溶解;如果溶解不好,用Buffer B溶解後,然後用Buffer A稀釋;對疏水性強的多肽,有時還需要加入少量的Formic Acid或醋酸。HPLC分析多肽粗產物,如果多肽不長(15aa以下),一般會有主峰,主峰通常為全長產物;對於20aa以上的長肽,如果沒有主峰,HPLC需搭配Mass來判定分子量,進而確定哪個峰是所要合成的多肽。

[font=宋体][font=宋体]多肽合成是一个固相合成顺序一般从[/font]C[font=宋体]端[/font][font=Calibri]([/font][font=宋体]羧基端[/font][font=Calibri])[/font][font=宋体]向[/font][font=Calibri]N[/font][font=宋体]端[/font][font=Calibri]([/font][font=宋体]氨基端[/font][font=Calibri])[/font][font=宋体]合成。过去的多肽合成是在溶液中进行的称为液相合成法。从[/font][font=Calibri]1963[/font][font=宋体]年[/font][font=Calibri]Merrifield[/font][font=宋体]发展成功了固相多肽合成方法以来,经过不断的改进和完善,到今天固相法已成为多肽和蛋白质合成中的一个常用技术,表现出了经典液相合成法无法比拟的优点,从而大大的减轻了每步产品提纯的难度。多肽合成总的来说分成两种:固相合成和液相多肽合成。【详情请咨询国肽生物】[/font][/font][font=宋体][font=宋体]多肽的固相合成[/font][font=宋体][font=宋体]多肽的合成是氨基酸重复添加的过程,通常从[/font]C[font=宋体]端向[/font][font=Calibri]N[/font][font=宋体]端[/font][font=Calibri]([/font][font=宋体]氨基端[/font][font=Calibri])[/font][font=宋体]进行合成。多肽固相合成的原理是将目的肽的第一个氨基酸[/font][font=Calibri]C[/font][font=宋体]端通过共价键与固相载体连接,再以该氨基酸[/font][font=Calibri]N[/font][font=宋体]端为合成起点,经过脱去氨基保护基和过量的已活化的第二个氨基酸进行反应,接长肽链,重复操作,达到理想的合成肽链长度,最后将肽链从树脂上裂解下来,分离纯化,获得目标多肽。[/font][/font][font=宋体]1[font=宋体]、[/font][font=Calibri]Boc[/font][font=宋体]多肽合成法[/font][/font][font=宋体]Boc[font=宋体]方法是经典的多肽固相合成法,以[/font][font=Calibri]Boc[/font][font=宋体]作为氨基酸α[/font][font=Calibri]-[/font][font=宋体]氨基的保护基,苄醇类作为侧链保护基,[/font][font=Calibri]Boc[/font][font=宋体]的脱除通常采用三氟乙酸[/font][font=Calibri](TFA)[/font][font=宋体]进行。多肽合成时将已用[/font][font=Calibri]Boc[/font][font=宋体]保护好的[/font][font=Calibri]N-[/font][font=宋体]α[/font][font=Calibri]-[/font][font=宋体]氨基酸共价交联到树脂上,[/font][font=Calibri]TFA[/font][font=宋体]切除[/font][font=Calibri]Boc[/font][font=宋体]保护基,[/font][font=Calibri]N[/font][font=宋体]端用弱碱中和。[/font][/font][font=宋体][font=宋体]肽链的延长通过二环己基碳二亚胺[/font](DCC)[font=宋体]活化、偶联进行,最终采用强酸氢氟酸[/font][font=Calibri](HF)[/font][font=宋体]法或三氟甲磺酸[/font][font=Calibri](TFMSA)[/font][font=宋体]将合成的目标多肽从树脂上解离。在[/font][font=Calibri]Boc[/font][font=宋体]多肽合成法中,为了便于下一步的多肽合成,反复用酸进行脱保护,一些副反应被带入实验中,例如多肽容易从树脂上切除下来,氨基酸侧链在酸性条件不稳定等。[/font][/font][font=宋体]2[font=宋体]、[/font][font=Calibri]Fmoc[/font][font=宋体]多肽合成法[/font][/font][font=宋体]Carpino[font=宋体]和[/font][font=Calibri]Han[/font][font=宋体]以[/font][font=Calibri]Boc[/font][font=宋体]多肽合成法为基础发展起来一种多肽固相合成的新方法——[/font][font=Calibri]Fmoc[/font][font=宋体]多肽合成法。[/font][/font][font=宋体]Fmoc[font=宋体]多肽合成法以[/font][font=Calibri]Fmoc[/font][font=宋体]作为氨基酸α[/font][font=Calibri]-[/font][font=宋体]氨基的保护基。其优势为在酸性条件下是稳定的,不受[/font][font=Calibri]TFA[/font][font=宋体]等试剂的影响,应用温和的碱处理可脱保护,所以侧链可用易于酸脱除的[/font][font=Calibri]Boc[/font][font=宋体]保护基进行保护。[/font][/font][font=宋体][font=宋体]肽段的最后切除可采用[/font]TFA/[font=宋体]二氯甲烷[/font][font=Calibri](DCM)[/font][font=宋体]从树脂上定量完成,避免了采用强酸。同时,与[/font][font=Calibri]Boc[/font][font=宋体]法相比,[/font][font=Calibri]Fmoc[/font][font=宋体]法反应条件温和,副反应少,产率高,并且[/font][font=Calibri]Fmoc[/font][font=宋体]基团本身具有特征性紫外吸收,易于监测控制反应的进行。[/font][font=Calibri]Fmoc[/font][font=宋体]法在多肽固相合成领域应用越来越广泛。[/font][/font][font=宋体]多肽合成服务种类[/font][font=宋体]多肽合成服务通常有线性肽合成服务、多种难肽合成服务、修饰肽合成服务、以及部分多肽合成公司还会提供多肽定制服务,定制出有针对性的合成肽。[/font][font=宋体][font=宋体]目前有多肽合成公司提供的线性肽合成可达[/font]150[font=宋体]个氨基酸以内,在修饰肽合成上,能提供常见修饰,磷酸肽,[/font][font=Calibri]RGD[/font][font=宋体]环肽,荧光标记肽([/font][font=Calibri]Cy3[/font][font=宋体]、[/font][font=Calibri]Cy5[/font][font=宋体]、[/font][font=Calibri]Fitc[/font][font=宋体]、[/font][font=Calibri]AMC[/font][font=宋体]等),生物素标记肽[/font][font=Calibri]/[/font][font=宋体]复合抗原([/font][font=Calibri]MAP[/font][font=宋体])[/font][font=Calibri]/[/font][font=宋体]含[/font][font=Calibri]D[/font][font=宋体]型氨基酸[/font][font=Calibri],[/font][font=宋体]及各种氨基酸衍生物均可合成。[/font][/font][font=宋体]多肽产物纯度选择[/font][font=宋体][font=宋体]常见的质谱级多肽纯度,一般要求[/font]95%[/font][font=宋体][font=宋体]用于抗体筛选纯度,一般[/font]85%[font=宋体]即可[/font][/font][font=宋体]NMR[font=宋体]和结晶试验中,纯度一般[/font][font=Calibri]98%[/font][/font][font=宋体][font=宋体]粗品肽,一般[/font]50%[font=宋体]即可用于多肽筛选[/font][/font][font=宋体][font=宋体]国肽生物主要提供:多肽合成、多肽定制、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽([/font]Cy3[font=宋体]、[/font][font=Calibri]Cy5[/font][font=宋体]、[/font][font=Calibri]Fitc[/font][font=宋体]、[/font][font=Calibri]AMC[/font][font=宋体]等)、目录肽、偶联蛋白([/font][font=Calibri]KLH[/font][font=宋体]、[/font][font=Calibri]BSA[/font][font=宋体]、[/font][font=Calibri]OVA[/font][font=宋体]等)、美容肽、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、[/font][font=Calibri]RGD[/font][font=宋体]环肽等。详情请咨询国肽生物[/font][/font][/font][font=宋体][font=宋体][font=宋体][img=,690,143]https://ng1.17img.cn/bbsfiles/images/2020/09/202009091456152918_1632_3531468_3.jpg!w690x143.jpg[/img][/font][/font][/font]

[font=宋体][size=10.5000pt][font=宋体]多肽固相合成法是多肽合成化学的一个重大的突破。它的最大特点是不必纯化中间产物,合成过程可以连续进行,进而为多肽合成的自动化奠定了基础。目前全自动多肽的合成,基本都是固相合成。其基本过程如下:[/font] [/size][/font][font=宋体][size=10.5000pt][font=宋体]基于[/font]Fmoc[font=宋体]化学合成,先将所要合成的目标多肽的[/font][font=Calibri]C-[/font][font=宋体]端氨基酸的羧基以共价键形式与一个不溶性的高分子树脂相连,然后以这一氨基酸的氨基作为多肽合成的起点,同其它的氨基酸已经活化的羧基作用形成肽键,不断重复这一过程,即可得到多肽。【详情请咨询国肽生物】根据多肽的氨基酸组成不同,多肽后处理方式不同,纯化方式也有差异。 [/font][/size][/font][font=宋体][size=10.5000pt]1.[font=宋体]做免疫用的多肽多长为合适[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]一般约[/font]10-15[font=宋体]个氨基酸,当然长一些免疫效果好一些,不过合成费用也会增加。[/font][font=Calibri]MAP[/font][font=宋体]多肽则希望长度在[/font][font=Calibri]15aa[/font][font=宋体]以上,效果较好。另外,[/font][font=Calibri]10aa[/font][font=宋体]以下的多肽免疫效果比较差。 [/font][/size][/font][font=宋体][size=10.5000pt]2.[font=宋体]免疫用多肽的纯度需要很高吗[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]一般而言,免疫用[/font]Peptide[font=宋体],[/font][font=Calibri]70-85%[/font][font=宋体]即可。 [/font][/size][/font][font=宋体][size=10.5000pt]3.[font=宋体]我们合成的多肽溶解性不好,多肽就有问题对吗[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]很难准确预测一个多肽的溶解性及合适的溶剂是什么。如果多肽难以溶解就认为多肽合成有问题这个观念并不正确。[/font] [/size][/font][font=宋体][size=10.5000pt]4.[font=宋体]多肽状态是如何[/font][font=Calibri]?[/font][font=宋体]如何保存储存[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]我们提供的多肽是粉末状,一般为灰白色,组成不同,多肽粉末的颜色有差异,多肽一般长期保存需要避光保存,并应保存在[/font]-20[font=宋体]度,短期可以保存在[/font][font=Calibri]4[/font][font=宋体]度。可以短时间的话是以室温运输。 [/font][/size][/font][font=宋体][size=10.5000pt]5.[font=宋体]如何溶解多肽[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]溶解多肽是非常复杂的事情,一般很难一下子确定合适的溶剂。通常是先取一点试验,在没有确定合适的溶剂前千万不要合部溶解。[/font] [font=宋体]下列方法有助于您选择合适的溶剂:[/font] [/size][/font][font=宋体][size=10.5000pt](1)[font=宋体]判定多肽的电荷特定,设定酸性氨基酸[/font][font=Calibri]Asp(D),Glu(E)[/font][font=宋体]和[/font][font=Calibri]C[/font][font=宋体]端[/font][font=Calibri]COOH[/font][font=宋体]为[/font][font=Calibri]-1[/font][font=宋体];碱性氨基酸[/font][font=Calibri]Lys(K),Arg(R),His(H)[/font][font=宋体]及[/font][font=Calibri]N[/font][font=宋体]端[/font][font=Calibri]NH2[/font][font=宋体]为[/font][font=Calibri]+1,[/font][font=宋体]其它氨基酸的电荷为[/font][font=Calibri]0[/font][font=宋体]。计算出将电荷数。 [/font][/size][/font][font=宋体][size=10.5000pt](2)[font=宋体]如果净电荷数[/font][font=Calibri]0[/font][font=宋体],多肽为碱性,用水溶解:如果不溶解或溶解性不大,加入醋酸[/font][font=Calibri](10%[/font][font=宋体]以上[/font][font=Calibri])[/font][font=宋体];如果多肽还不能溶解,加入少量[/font][font=Calibri]TFA(25ul)[/font][font=宋体]溶解,然后加入[/font][font=Calibri]500ul[/font][font=宋体]水稀释。 [/font][/size][/font][font=宋体][size=10.5000pt](3)[font=宋体]如果净电荷数[/font][font=Calibri]0[/font][font=宋体],多肽为酸性,用水溶解;如果不溶解或溶解性不大,加入氨水[/font][font=Calibri](25ul)[/font][font=宋体]溶解,然后加入[/font][font=Calibri]500ul[/font][font=宋体]水稀释。 [/font][/size][/font][font=宋体][size=10.5000pt](4)[font=宋体]如果净电荷数[/font][font=Calibri]=0[/font][font=宋体],多肽为中性,一般需要用有机溶剂如乙腈,甲醇或异丙醇,[/font][font=Calibri]DMSO[/font][font=宋体]等溶解。还有人建议需要尿素来溶解疏水性很大的多肽。[/font][/size][/font][font=宋体][size=10.5000pt]6.[font=宋体]非[/font][font=Calibri]HPLC[/font][font=宋体]纯化的多肽中有哪些杂质[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]粗品和脱盐级别的多肽中多肽和非多肽类杂质:如非全长多肽和多肽后处理的一些原料如[/font]DTT[font=宋体]、[/font][font=Calibri]TFA[/font][font=宋体]等。 [/font][/size][/font][font=宋体][size=10.5000pt]7.HPLC[font=宋体]纯化的多肽有哪些杂质[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]经过[/font]HPLC[font=宋体]纯化的多肽,仍会有一些一些杂质存在,其中的杂质主要是短肽和微量[/font][font=Calibri]TFA[/font][font=宋体]。 [/font][/size][/font][font=宋体][size=10.5000pt]8.[font=宋体]多长的多肽为合适[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]多肽合成需要考虑多肽的长度,电荷,亲疏水性等因素。长度越长,合成粗品的纯度和产率都随着降低,纯化的难度和无法合成的几率就会大些。当然多肽功能区的序列是无法改变的,但是为了多肽的顺利合成,有时不得不在功能取的上下游增加一些辅助氨基酸,以改善多肽的溶解性和亲疏水性。如果多肽太短,合成也可能有问题,主要问题是合成的多肽在后处理过程中有一定的难度,[/font]5[font=宋体]肽以下的多肽,一般要有疏水的氨基酸,否则后处理难度加大。[/font][font=Calibri]15[/font][font=宋体]个氨基酸残基以下的多肽一般都可以得到满意的产率和得率。 [/font][/size][/font][font=宋体][size=10.5000pt]9.[font=宋体]如何从多肽序列中判定多肽的溶解性[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt](1)[font=宋体]多肽中如果含有高比例的疏水性很强的氨基酸如和[/font][font=Calibri]Leu,Val,IIe,Met,Phe[/font][font=宋体]和[/font][font=Calibri]Trp[/font][font=宋体],多肽很难溶解与水性溶液中或根本不可能溶解。这些氨基酸无论是纯化或合成,都有可能有问题。 [/font][/size][/font][font=宋体][size=10.5000pt](2)[font=宋体]一般情况下疏水性氨基酸的比例[/font][font=Calibri]50%[/font][font=宋体],不能连续[/font][font=Calibri]5[/font][font=宋体]个连续[/font][font=Calibri]aa[/font][font=宋体]为疏水性,带电荷的氨基酸的[/font][font=Calibri]([/font][font=宋体]正电荷[/font][font=Calibri]K,R,H,N-terminus,[/font][font=宋体]负电荷[/font][font=Calibri]D,E,C- terminus)[/font][font=宋体]的比例达到[/font][font=Calibri]20%[/font][font=宋体],在多肽的[/font][font=Calibri]N[/font][font=宋体]或[/font][font=Calibri]C[/font][font=宋体]短如果能增加极性氨基酸,也可以改善溶解性。 [/font][font=Calibri]11.[/font][font=宋体]为什么含有[/font][font=Calibri]Cys,Met,[/font][font=宋体]或[/font][font=Calibri]Trp[/font][font=宋体]的多肽难合成[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]含有[/font]Cys,Met[font=宋体],或[/font][font=Calibri]Trp[/font][font=宋体]的多肽难以合成,同时难以获得高纯度的产品。主要因为这些基团不稳定,易氧化。这些多肽的使用和储存都需要特别注意,避免反复开启盖子。 [/font][/size][/font][font=宋体][size=10.5000pt]10.[font=宋体]为什么有些多肽的合成产率或纯度会比较低[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]多肽合成与引子合成有比较大的区别,不能合成的引子很少,但是不能合成的多肽经常有。如[/font]Val,Ile,Tyr,Phe,Trp,Leu,Gln,[font=宋体]和[/font][font=Calibri]Thr[/font][font=宋体]这些氨基酸比邻或重复时,多肽链在合成过程中不能完全舒展溶解,合成效率下降。以下几种情形,合成效率和产物的纯度都比较低,如:重复[/font][font=Calibri]Pro,Ser-Ser[/font][font=宋体],重复[/font][font=Calibri]Asp[/font][font=宋体],[/font][font=Calibri]4[/font][font=宋体]个连续[/font][font=Calibri]Gly[/font][font=宋体]等。 [/font][/size][/font][font=宋体][size=10.5000pt]11.[font=宋体]多肽是如何纯化的[/font][font=Calibri]? [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]多肽纯化一般使用反相柱[/font]([font=宋体]如[/font][font=Calibri]C8[/font][font=宋体],[/font][font=Calibri]C18[/font][font=宋体]等[/font][font=Calibri])[/font][font=宋体],[/font][font=Calibri]214nm[/font][font=宋体]。缓冲体系通常为含[/font][font=Calibri]TFA[/font][font=宋体]的溶剂,[/font][font=Calibri]pH2.0[/font][font=宋体]。[/font][font=Calibri]Buffer A[/font][font=宋体]为含[/font][font=Calibri]0.1%TFA in ddH2O[/font][font=宋体],[/font][font=Calibri]Buffer B[/font][font=宋体]为[/font][font=Calibri]1%TFA/ACN/pH2.0[/font][font=宋体]。纯化前用[/font][font=Calibri]Buffer A[/font][font=宋体]溶解;如果溶解不好,用[/font][font=Calibri]Buffer B[/font][font=宋体]溶解后,然后用[/font][font=Calibri]Buffer A[/font][font=宋体]稀释;对疏水性强的多肽,有时还需要加入少量的[/font][font=Calibri]Formic Acid[/font][font=宋体]或醋酸。[/font][font=Calibri]HPLC[/font][font=宋体]分析多肽粗产物,如果多肽不长[/font][font=Calibri](15aa[/font][font=宋体]以下[/font][font=Calibri])[/font][font=宋体],一般会有主峰,主峰通常为全长产物;对于[/font][font=Calibri]20aa[/font][font=宋体]以上的长肽,如果没有主峰,[/font][font=Calibri]HPLC[/font][font=宋体]需搭配[/font][font=Calibri]Mass[/font][font=宋体]来判定分子量,进而确定哪个峰是所要合成的多肽。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体][img=,690,143]https://ng1.17img.cn/bbsfiles/images/2020/07/202007091611507608_3379_3531468_3.jpg!w690x143.jpg[/img][/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]国肽生物主要提供:多肽合成、多肽定制、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、美容肽、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。详情请咨询国肽生物[/font][/size][/font]

合肥国肽生物科技有限公司(简称:国肽生物TM)成立于2014年,是一家专业从事多肽产品的研发、生产和销售以及多肽技术转让的高新技术企业。BP公司成立之初,便成功收购了国内几家多肽、抗体公司,是目前国内的专业多肽合成、抗体制备、蛋白表达的规模型生产企业。 国肽生物专长于荧光标记肽、同位素标记肽、人工胰岛素、药物肽、化妆品肽、长肽困难肽等产品的合成与研发,致力于学术水平的科研提升,搭建学术交流平台,促进前沿、专业的学术知识推广,推动多肽在生物医学材料等领域的研究与应用。公司产品广泛应用于药物研发,抗体的制备(包括单抗与双抗),荧光分子探针的构建以及细胞透膜研究、活体成像、新型材料研发和质谱分析等研究领域;目前我们已经与军科院、天津药物研究所、中科院物理研究所等研究机构,清华、北大、复旦等高校,以及国外著名药企建立了长期友好的合作交流关系。 国肽生物以科技创新为动力,提升企业核心竞争力。公司拥有一支由行业内领军人才组成的研发创新团队,硕士研发人员占企业员工总数的15%以上,同时公司还邀请国内外生物医学科学家担任科学顾问。公司成立首年,通过多肽生产设施的精细改良、多肽研发工艺的自主创新,突破了多肽产品快速化、规模化生产技术瓶颈,获得了7项实用新型专利和1项发明专利。 国肽生物公司配备了一流的多肽合成、纯化、冻干、质量检测与分析等精密仪器,从美国、日本等国引进了[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url][url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用仪[/color][/url]、超高压液相色谱、紫外分光光度计等专用设备,以多肽合成与研发为核心,搭建起全产业链产品分析检测平台,为广大客户提供专业可靠的多肽及相关产品理化性质分析,纯度分析,质谱分析,CHN元素含量分析,红外,紫外光谱分析等分析检测服务。 国肽生物的创立,源自于公司对多肽行业未来发展的认同,公司秉承“品质优先,服务至上”的经营理念,带着行业责任感与使命感,立志于在全球范围内树立一个民族品牌,重新引领肽行业的健康、快速发展。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:17718122172;17718122684;17730030476;17718122397[img=,690,161]https://ng1.17img.cn/bbsfiles/images/2019/04/201904031458225876_4973_3531468_3.jpg!w690x161.jpg[/img]国肽生物根据客户要求,供应各种修饰型多肽。1.磷酸化的Ser、Tyr和Thr修饰的多肽:我们提供单磷酸化和多磷酸化多肽服务,目前我们已经能够提供四个磷酸化位点修饰的多肽。2. 5(6)-FAM,FITC,CY5,RhodamineB,PNA,EDNAS/dabcyl等荧光标记修饰的多肽:荧光标记修饰多肽技术是我们国肽生物的代表性多肽合成技术,我们的这项技术已经相当成熟。3.生物素Biotin,Lys(Biotin)修饰的多肽:生物素是维生素B2的组成部分,Biotin,Lys(Biotin)修饰的多肽也是客户经常定制的多肽。我们提供生物素修饰的多肽已经有将近100%的成功率。4.含有一对或多对二硫键修饰的多肽:二硫键在蛋白质的结构稳定中起到重要作用,目前我们已经能够为客户提供四对二硫键修饰的多肽。5.含有同位素C13,N15修饰的多肽:同位素标记的多肽主要应用于医学和生物学领域,通常价格较高,为了满足客户需要,我们接受微克级的同位素多肽定制。6.含有特殊氨基酸修饰的多肽:例如,D型氨基酸,氨基酸衍生物,脂肪族羧酸等等,都在我们接受的定制范围内。

[font=宋体][size=10.5000pt]摘要:关于多肽的一个常见的误解是多肽像蛋白质一样是不稳定的。事实上,多肽比蛋白质稳定得多,由于两个影响蛋白质稳定性的要素不存在多肽合成中。这两个要素是第三次折叠和蛋白酶的污染。【详情请咨询国肽生物】[/size][/font][font=宋体][size=10.5000pt][font=宋体]([/font]1[font=宋体])多肽稳定性[/font][/size][/font][font=宋体][size=10.5000pt]关于多肽的一个常见的误解是多肽像蛋白质一样是不稳定的。事实上,多肽比蛋白质稳定得多,由于两个影响蛋白质稳定性的要素不存在多肽合成中。这两个要素是第三次折叠和蛋白酶的污染。[/size][/font][font=宋体][size=10.5000pt]蛋白质很容易变性,由于它的三级构造是由非共价键联合的,例如静电互相作用和疏水互相作用。由于长度短,大多数肽没有足够量的这种互相作用使每个分子折叠到规则的三级构造。结果多肽不能像蛋白质一样变性。在这种假定下,多肽只能经过共价修饰或者肽键断裂被毁坏。不像蛋白质是从充溢各种蛋白酶的细胞里被纯化,合成的多肽被蛋白酶污染的时机是极端小的。[/size][/font][font=宋体][size=10.5000pt][font=宋体]反响有可能会毁坏例如氧化需求极端[/font]pH[font=宋体]值的多肽。在中性[/font][font=Calibri]pH[/font][font=宋体]条件下,大多数生物实验的停止速度很慢。细菌污染可能是一个比那些反响更严重的要挟,由于多肽是细菌的一种良好的营养源。因而,溶剂过滤比多肽的稳定更重要。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]普通状况下,在正常条件下,多肽溶液在室温下能保管几天,在[/font]4[font=宋体]度保管几个星期和在[/font][font=Calibri]-20[/font][font=宋体]度保管若干个月或更多;冻干的多肽粉末在室温下能保管几个月,在[/font][font=Calibri]-20[/font][font=宋体]度下保管几年。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]([/font]2[font=宋体])多肽浓度[/font][/size][/font][font=宋体][size=10.5000pt]准确测定多肽浓度比许多人预期的更复杂。事实上,没有一个简单的通用办法能用。称重和紫外线吸收力是两个最常用的办法。[/size][/font][font=宋体][size=10.5000pt]a. [font=宋体]称重 它只能提供粗略估量的多肽含量。首先,多肽粉末是不容易处置的。准确称量少量([/font][font=Calibri] 40[/font][font=宋体]%。实践含量取决于多肽序列。反离子的类型和数量取决于用于多肽纯化的溶剂和多肽序列。由这些水分子产生的不肯定性不能被疏忽。[/font][/size][/font][font=宋体][size=10.5000pt]b. [font=宋体]紫外线吸收性 假如您的多肽含有一个酪氨酸或色氨酸残基,多肽的定量剖析就变得愈加简单。色氨酸在[/font][font=Calibri]282 nm[/font][font=宋体]处的摩尔吸光度[/font][font=Calibri][1 /[/font][font=宋体]([/font][font=Calibri]M *[/font][font=宋体]厘米)[/font][font=Calibri]][/font][font=宋体]是[/font][font=Calibri]5700[/font][font=宋体],酪氨酸在在[/font][font=Calibri]275 nm[/font][font=宋体]处的摩尔吸光度是[/font][font=Calibri]1400[/font][font=宋体]。在[/font][font=Calibri]0.1N[/font][font=宋体]的[/font][font=Calibri]NaOH[/font][font=宋体]中,酪氨酸的[/font][font=Calibri]-OH[/font][font=宋体]基团充沛去质子化。这就使酪氨酸的吸收峰为[/font][font=Calibri]293[/font][font=宋体]纳米。在此条件下,它的摩尔吸光度增加到[/font][font=Calibri]2400[/font][font=宋体]。值得关注的是,假如肽的侧链之间有互相作用,紫外线吸收率能够不同。关于小的亲水性肽,这不是问题。在水溶液中,这些肽通常采用伸展构象,一切的侧链是完整暴露于溶剂中的。但关于长的疏水性多肽,这种假定是不完整正确的。有时可察看到低水平聚合和折叠。出于这个缘由,我们以为,酪氨酸在[/font][font=Calibri]0.1N NaOH[/font][font=宋体]中,在[/font][font=Calibri]293 nm[/font][font=宋体]处的吸光度是最好的,由于在此条件下,肽是完整变性的。它独一的缺陷是,用于浓度测定的样品不能被恢复。 [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]假如您的肽不含有色氨酸或酪氨酸,精确理解肽的浓度是至关重要的,独一合理的选择是氨基酸定量剖析。当然,这超出大多数实验室的日常操作。[/font] [/size][/font][font=宋体][size=10.5000pt][font=宋体]基于上面的讨论,为了多肽的浓度的准确测定,我们激烈倡议在你的多肽的[/font]N-[font=宋体]或[/font][font=Calibri]C-[/font][font=宋体]末端添加一个酪氨酸残基。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]([/font]3[font=宋体])[/font][font=Calibri]N-[/font][font=宋体]末端乙酰化和的[/font][font=Calibri]C-[/font][font=宋体]末端酰胺化[/font][/size][/font][font=宋体][size=10.5000pt]人们经常以为用乙酰基和酰胺基分别阻断肽的两端能增加肽的稳定性,实践上这是不正确的。[/size][/font][font=宋体][size=10.5000pt][font=宋体]大多数合成肽的序列都来源于蛋白质片段。在一个蛋白质中,多肽序列的[/font]N[font=宋体]末端和[/font][font=Calibri]C[/font][font=宋体]末端构成肽键。这不同于合成肽含有不带电荷的两端。带电荷和不带电荷的多肽的物理化学性质是完整不同的,反过来这些性质又影响多肽的功用。经过乙酰基和酰胺基分别封锁[/font][font=Calibri]N[/font][font=宋体]端和[/font][font=Calibri]C[/font][font=宋体]端,这些问题能够被处理,并且能够使合成肽的两端更像肽键。由于这个缘由,我们用于抗体消费的多肽是末端封锁的,除非抗原位于蛋白的末端。由于同样的缘由,我们倡议顾客在停止其它功用性研讨时封锁合成肽的两端。没有理论根底支持有自在端的多肽是不稳定的。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]([/font]4[font=宋体])多肽溶解度[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]当试图将多肽溶解在执行多肽生物功用的水溶液中时,溶解度成为关注的焦点。关于有机溶剂,溶解度基本就不是问题[/font]—简直一切的多肽都能溶解在有机溶剂中。但是这并没有多大的协助,由于大多数肽的研讨不能再有机溶剂中停止。[/size][/font][font=宋体][size=10.5000pt][font=宋体]肽的溶解度最终取决于它的序列。假如您的肽含有高比例的疏水残基,您就交好运了。不幸的是,大多数研讨人员不得不以他们现有的肽停止工作,除非他们想改动他们的研讨项目。在能够操作的条件,[/font]pH[font=宋体]值可能是最重要的。我们发现,在许多状况下,改动[/font][font=Calibri]1-3[/font][font=宋体]个[/font][font=Calibri]pH[/font][font=宋体]值单位能够使十分稳定的多肽完整溶解。过渡曲线通常是很峻峭的。在一个很窄的[/font][font=Calibri]pH[/font][font=宋体]范围内,溶液从混浊变得明澈。这可能是由于某些残基电离状态的改动,比方组氨酸。 [/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]还有另一个缘由使[/font]pH[font=宋体]值调整变得重要。由于用于肽纯化的[/font][font=Calibri]HPLC[/font][font=宋体]溶剂含有[/font][font=Calibri]0.1%[/font][font=宋体]的不能经过冻干彻底除去的[/font][font=Calibri]TFA[/font][font=宋体],收到的多肽通常含有少量的[/font][font=Calibri]TFA[/font][font=宋体]。从而使得肽溶液比你预期的更具有酸性。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]关于难以溶解的肽,你能够在有机溶剂中制备更高浓度的原液,例如[/font]DMS[font=宋体],并且在生物功用检测期间稀释肽。大多数的检测能包容[/font][font=Calibri]1-2%[/font][font=宋体]的[/font][font=Calibri]DSMO[/font][font=宋体],一些以至是[/font][font=Calibri]5%[/font][font=宋体]。但是这并不是总是起作用的。一些肽当从[/font][font=Calibri]DMSO[/font][font=宋体]中稀释时以至在更低浓度时汇集和沉淀。[/font][/size][/font][font=宋体][size=10.5000pt][font=宋体][img=,690,177]https://ng1.17img.cn/bbsfiles/images/2020/07/202007021619442576_4938_3531468_3.jpg!w690x177.jpg[/img][/font][/size][/font][font=宋体][size=10.5000pt][font=宋体]国肽生物主要提供:多肽合成、多肽定制、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、美容肽、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。详情请咨询国肽生物[/font][/size][/font]
第一种:呼吸进入,75%进入人体的汞是通过呼吸进入的。发生频率,每时每刻;第二种:饮食侵入,食品中的汞以此侵入人体。第二种:经皮侵入,大气中的汞、化妆品和服饰等以此侵入人体。汞的危害因人群而异,妇女、孩子最易受到伤害!
请教多肽高手,D、L型多肽药物的液相分析方法,目前正在做一个多肽药物,其中多肽药物的编号最后一个氨基酸的L型的是我们需要的东西,它的D型是杂质(其他的氨基酸都一样),编号最后一个氨基酸是His,在液相分析有关物质时,这两个物质的分离度一直都不是很好,用过一些柱子,也用过三氟乙酸体系和缓冲盐体系,都不是很理想,不知道有没那位高手做过类似的分离,请不吝赐教。
国肽生物是一家专业从事多肽产品的研发、生产和销售以及多肽技术转让的高新技术企业。BP公司成立之初,便成功收购了国内几家多肽、抗体公司,是目前国内的专业多肽合成、抗体制备、蛋白表达的规模型生产企业。【详情请咨询合肥国肽生物】定制多肽种类一、特殊类别多肽:订书肽、同位素标记多肽、磷酸肽、环肽、二硫键多肽、糖肽、药物肽、化妆品肽等二、修饰肽:磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC、CMK、FMK等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、RGD环肽等三、特殊氨基酸多肽:可以将种类繁多的非天然氨基酸合成到多肽上。四、合成方法:多肽固相合成、多肽液相合成、点击化学、一锅法合成等服务内容标准肽:链长至 150个氨基酸,毫克至克级,纯度最高可达99%。不同纯度范围:粗肽、脱盐、75% 、 85% 、90%、95%、98%、99%。常规修饰肽:乙酰化,酰胺化,生物素标记肽,磷酸化肽,D型氨基酸修饰肽等。特殊修饰肽:磺酸化肽(Sulfated-tyrosine),环肽(二硫键环化,首尾环化),荧光标记肽(FITC,Dabcyl/Edans,Dansyl,FAM,Abz/Dnp,Rhodamine等),甲基化多肽(Lys(Me2),Lys(Me),Lys(Me3),Arg(Me),Arg(Me2) -Symetrical,Arg(Me2) -Asymetrical),同位素标记肽(Heavy Isotope Labeled Peptides)、拟肽(peptoid)和点击化学用多肽(Peptides for Click Chemistry)。药用肽,大批量肽。协助客户建立科研肽库。抗原多肽及其与蛋白的交联:KLH,BSA, OVA服务流程确定合成序列,我们将在12小时内容提供准确报价。我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:0551-62626599
铁是人体造血合成血红蛋白最重要的元素,它是构成血肌红蛋白、红蛋白、细胞色素的主要成分,也是人体必须的微量元素。铁对人体是相当重要的,那么具体有那些作用呢? 铁是血红蛋白的组成成份,参与氧的运输和存储。铁是血红蛋白的重要组成部分,铁元素血红蛋白、肌红蛋白、细胞色素、细胞色素氧化酶及触酶的合成,红细胞的功能是输送氧,每个红细胞含2.8亿个血红蛋白,每个血红蛋白分子又含四个铁离子,而这些铁离子正是一种运输体,有它们,还能真正携带和输送氧。 铁对人体免疫系统有影响。铁元素在人体内参与着造血,并形成血红蛋白、肌红蛋白,参与氧的携带和运输的整个过程,多种酶的活性中心也是铁。有实验证明,缺铁会让中性白细胞的杀菌能力降低,使得淋巴细胞功能受损,而这些补充铁质之后都会得到改善,特别是免疫系统。 铁还直接参与人体能量代谢。铁在人体内以很多种形式存在,生理功能也很大,如肌红蛋白可贮存氧,血红蛋白可输送氧,细胞色素可转运电子,此外,铁还结合多种酶分解氧化物,解毒抑制细菌,释放能量,而释放能量的多少又与细胞中的铁有关,铁质越多,能量代谢就越好。而且铁还影响蛋白质以及去氧核糖核酸的造血及合成、维生素代谢。 可见,微量元素铁对人体的作用是很大的,但是,人体内的铁质要把握好,缺铁对身体的健康会造成危害,但是补铁过量对人体也是不好的,要保持正常含量的铁才能保证人体的健康。缺铁的话,红细胞就不能正常的生成,就会导致缺铁性贫血。但是补铁过量的话,就有可能会诱发肿瘤的发生和发展,因为铁可能是肿瘤细胞生长和复制的限制性营养素。体内铁水平高可增加某种肿瘤细胞的生存和生长,成为临床上可检测到的肿瘤。人体内的病原菌的生长和繁殖也是一种限制性营养素。而铁过多诱导的脂质过氧化反应的增强,机体氧化和抗氧化平衡就会失调,直接让DNA受损伤,从而诱发突变。 小编在这里要特别介绍一下缺铁对小孩的危害。缺铁对孩子的伤害是很大的,会影响孩子的智力,缺铁会阻碍脑组织和神经组织髓鞘的快速结合,缺铁严重的小孩,后期就算有铁质的补充,也很难恢复神经递质的传导神经冲动的动力,因此缺铁对智力造成的危害是很大的。此外缺铁还会影响孩子的情绪,甚至影响孩子的社会适应能力,对于孩子和容易缺铁的女性来说,补铁很重要,建议选用体恒健牌铁之缘片,含乳酸亚铁以及阿胶,双重补铁补血。 可见,铁过少或过量都是对身体有害的,保持体内的铁质平衡,才能最大限度的发挥铁对人体的作用。