我在用磷酸苯二钠测定土壤碱性磷酸酶时,配制的磷酸苯二钠(用硼酸缓冲液配制)溶液,在暗处放置了将近五天后出现了一些絮状物,请问下,磷酸苯二钠是不是现配现用啊?万分感谢!
请问新购买的碱性磷酸酶怎么稀释? 需要特殊的缓冲吗?
我在用磷酸苯二钠测定土壤碱性磷酸酶时,配制的磷酸苯二钠(用硼酸缓冲液配制)溶液,在暗处放置了将近五天后出现了一些絮状物,请问下,磷酸苯二钠是不是现配现用啊?万分感谢!
[b][font='微软雅黑','sans-serif'][color=#FF6600]实验原理[/color][/font][/b][font='微软雅黑','sans-serif']碱性磷酸酶(alkaline phosphatase EC 3.1.3.1简称为ALPase)广泛存于微生物界和动物界。ALPase能催化几乎所有的磷酸单酯的水解反应,产生无机磷酸和相应的醇、酚或糖。它也可以催化磷酸基团的转移反应,磷酸基团从磷酸酯转移到醇、酚或糖等磷酸受体上。在磷的生物和化学循环过程中,ALPase起了及其重要的作用。在生物体内ALPase与磷的代谢直接相关,参与磷与钙物质的消化、吸收、分泌以及骨骼的形成等生理生化过程。ALPase的作用最适PH在碱性区域,一般在PH9.0~10.5范围内。Mg[sup]2+[/sup]对该酶的活力有显著的激活使用。[/font][font='微软雅黑','sans-serif']为了获得好的提取效果,在酶的制备过程,特别应注意以下几点:[/font][font='微软雅黑','sans-serif'](1)[/font][font='微软雅黑','sans-serif']选取来源丰富、酶含量高的新鲜材料。提取工作应在获得材料后立刻开始,否则应在低温下保存。[/font][font='微软雅黑','sans-serif'](2)[/font][font='微软雅黑','sans-serif']用盐分级沉淀是一种应用非常广泛的方法。碳酸铵是最常用的盐。操作时,要注意保持缓冲液的合适PH值和温度。在加碳酸铵时需事先将其研细,需缓慢加入并及时搅拌溶解,尽量防止泡沫形成,以免酶蛋白在溶液中表面变性。盐析生成的沉淀,要静置20min以上,以使沉淀完全,然后方可时行离心分离。[/font][font='微软雅黑','sans-serif'](3)[/font][font='微软雅黑','sans-serif']有机溶剂沉淀法也常用于蛋白质的分离提纯。丙酮和乙醇是使用最为广泛的两种有机溶剂。应注意在低温下操作,缓慢加入,充分搅拌,避免局部浓度过高放出大量热量而使酶蛋白变性。离心收集沉淀后,最好立即将其溶于适量缓冲液中,以避免酶活力的丧失。[/font][font='微软雅黑','sans-serif'](4)[/font][font='微软雅黑','sans-serif']在酶的制备过程中,每经一步处理,都需测定酶的活力和比活力。唯有比活力提高较大,提纯步聚才有效。[/font][align=left][font='微软雅黑','sans-serif'] [/font][font='微软雅黑','sans-serif']酶活力的分析:通常是以对—硝基苯磷酸二纳(pNPP)为底物,在PH10.1的碳酸盐缓冲液(含2mmol/L Mg[sup]2+[/sup])的测活体系中检测酶催化pNPP水解产生黄色的对硝基苯( pNP)在405 nm处有最大的吸收峰,可以根据OD[sub]4[/sub][sub]〇5[/sub]值的增加计算酶活力的大小。酶活力定义为在37℃下,以5mmol/L pNPP为底物,在pH 10.1的碳酸盐缓冲液含2 mmol/L Mg[sup]2+[/sup]的测活体系中每分钟催化产生1 mol/L pNP的酶量定为1个酶活力单位。酶的比活力定义为每mg蛋白所具有的酶活力单位数。 [/font][/align]
开发方法时,在什么情况下需要考虑添加磷酸二氢钠和磷酸氢二钠,浓度如何选择
测定三聚磷酸钠的树脂(强碱性阴离子型,氯型,粒度0.07~0.16mm)在哪能买到?用粒度大10倍的树脂经粉碎后能不能使用?这样会不会破坏树脂的结构?
磷酸液(40%)中的钙、镁、铁、钾、钠、氯、铅,其中铁含量是百分级的,这样的样可以用ICP-MS法,将样品稀释1000倍后可以直接进样分析吗
我厂得汽包炉加入磷酸三钠后,联排的PH和电导率都会相应升高,而磷酸根却几乎无变化,一直是零点几毫克。化验后,证明磷酸三钠失效,不能正常显色,请问磷酸三钠什么情况下会失效,失效过程中的物理或化学反应是什么?谢谢了。。
土壤中存在着各种化学和生物化学反应,表现出不同的酸性或碱性。划分为9等级。 9.5极强碱性。 l 我国土壤pH大多在4.5~8.5范围内,由南向北pH值递增,长江(北纬33°)以南的土壤多为酸性和强酸性,如华南、西南地区广泛分布的红壤、黄壤,pH值大多在4.5~5.5之间;华中华东地区的红壤,pH值在5.5~6.5之间;长江以北的土壤多为中性或碱性,如华北、西北的土壤大多含CaCO3,PH值一般在7.5~8.5之间,少数强碱性土壤的pH值高达10.5。 [size=4][b]1.土壤酸度:[/b][/size] 根据土壤中H离子的存在方式,土壤酸度可分为两大类。 [b](1)活性酸度[/b]:土壤溶液中氢离子浓度的直接反映,又称为有效酸度,通常用pH表示。 [b]活性酸度[/b]的来源,主要是CO2溶于水形成的碳酸和有机物质分解产生的有机酸,以及土壤中矿物质氧化产生的无机酸,还有施用的无机肥料中残留的无机酸,如硝酸、硫酸和磷酸等。此外,由于大气污染形成的大气酸沉降,也会使土壤酸化,所以它也是土壤活性酸度的一个重要来源。 [b](2)潜性酸度[/b]:土壤潜性酸度是土壤胶体吸附的可代换性H和Al的反映。当这些离子处于吸附状态时,是不显酸性的,但当它们通过离子交换作用进入土壤溶液之后,即可增加土壤溶液的H浓度,使土壤pH值降低。只有盐基不饱和土壤才有潜性酸度,其大小与土壤代换量和盐基饱和度有关。 潜性酸度分为代换性酸度和水解酸度。 Ø [b]代换性酸度[/b]:用过量中性盐(如NaCl或KCl)溶液淋洗土壤,溶液中金属离子与土壤中H和Al发生离子交换作用,而表现出的酸度,称为代换性酸度。代换性Al是矿物质土壤中潜性酸度的主要来源。例如,红壤的潜性酸度95%以上是由代换性Al产生的。由于土壤酸度过高,造成铝硅酸盐晶格内铝氢氧八面体的破裂,使晶格中的Al释放出来,变成代换性Al。 Ø [b]水解性酸度[/b]:用弱酸强碱盐(如醋酸钠)淋洗土壤,溶液中金属离子可以将土壤胶体吸附的H、Al代换出来,同时生成某弱酸(醋酸)。此时,所测定出的该弱酸的酸度称为水解性酸度。由于生成的醋酸分子离解度很小,而氢氧化钠可以完全离解。氢氧化钠离解后,所生成的钠离子浓度很高,可以代换出绝大部分吸附的H和Al。 [b](3)活性酸度与潜性酸度的关系[/b]:活性酸度与潜性酸度是同一个平衡体系的两种酸度。二者可以互相转化,在一定条件下处于暂时平衡状态。土壤活性酸度是土壤酸度的根本起点和现实表现。土壤胶体是H和Al的贮存库,潜性酸度则是活性酸度的贮备,土壤的潜性酸度往往比活性酸度大得多,二者的比例,在砂土中约为1000;在[url=http://baike.baidu.com/view/1053488.htm]有机质[/url]丰富的粘土中则可高达5×10—1×10。 [size=4][b]2.土壤碱度[/b][/size] l 土壤溶液中OH离子的主要来源,是CO3和HCO3的碱金属(Na、K)及碱土金属(Ca、Mg)的盐类。[b]碳酸盐碱度和重碳酸盐度的总和称为总碱度[/b]。可用中和滴定法测定。 l 不同溶解度的碳酸盐和重碳酸盐对土壤碱性的贡献不同,CaCO3和MgCO3的溶解度很小,在正常的CO2分压下,它们在土壤溶液中的浓度很低,故富含CaCO3和MgCO3的石灰性土壤呈弱碱性(pH7.5~8.5);Na2CO3、NaHCO3及Ca(HCO3)2等都是水溶性盐类,可以大量出现在土壤溶液中,使土壤溶液中的总碱度很高,从土壤pH来看,含Na2CO3的土壤,其pH值一般较高,可达10以上,而含NaHCO3及Ca(HCO3)2的土壤,其pH值常在7.5~8.5,碱性软弱。 l 当土壤胶体上吸附的Na、K、Mg(主要是Na)等离子的饱和度增加到一定程度时,会引起交换性阳离子的水解作用: 土壤胶体(x Na)+yH2O=土壤胶体((x –y)Na、yH)+yNaOH 在土壤溶液中产生NaOH,使土壤呈碱性。此时Na离子饱和度称为土壤碱化度。 [size=4][b]3.土壤的缓冲性能[/b][/size] 土壤缓冲性能是指土壤具有缓和其酸碱度发生激烈变化的能力,它可以保持土壤反应的相对稳定,为植物生长和土壤生物的活动创造比较稳定的生活环境,所以土壤的缓冲性能是土壤的重要性质之一。 [b](1)土壤溶液的缓冲作用[/b]:土壤溶液中含有碳酸、硅酸、磷酸、腐殖酸和其他有机酸等弱酸及其盐类,构成一个良好的缓冲体系,对酸碱具有缓冲作用。 Ø 碳酸及其钠盐。 当加入盐酸时,碳酸钠与它作用,生成中性盐和碳酸,大大抑制了土壤酸度的提高。 Na2CO3+2HCL=2NaCL+ H2CO3 当加大Ca(OH)2时,碳酸与它作用,生成溶解度较小的碳酸钙,限制了土壤碱度。 H2CO3+Ca(OH)2= CaCO3+ 2H2O Ø 土壤中的某些有机酸(如氨基酸、胡敏酸等)是两性物质,具有缓冲作用,如氨基酸含氨基和羧基可分别中和酸和碱,从而对酸和碱都具有缓冲能力。 R-CH(NH2)(COOH)+HCL= R-CH(NH3CL)(COOH) R-CH(NH2)(COOH)+NaOH= R-CH(NH2)(COONa)+ H2O [b](2)土壤胶体的缓冲作用[/b]:土壤胶体吸附有各种阳离子,其中盐基离子和氢离子能分别对酸和碱起缓冲作用。 Ø 对酸的缓冲作用 (以M代表盐基离子) 土壤胶体-M+ HCL=土壤胶体-H+ MCL Ø 对碱的缓冲作用 土壤胶体-H+ MOH=土壤胶体-M+ H2O 土壤胶体的数量和盐基代换量越大,土壤的缓冲性能就越强。因此,砂土掺粘土及施用各种有机肥料,都是提高土壤缓冲性能的有效措施。在代换量相等的条件下,盐基饱和度愈高,土壤对酸的缓冲能力愈大;反之,盐基饱和度愈低,土壤对碱的缓冲能力愈大。 Ø 铝离子对碱的缓冲作用:在PH5.5,铝离子开始形成Al(OH)3沉淀,失去缓冲能力。 土壤酸碱性对植物的影响 1、大多数植物在pH9.0或2.5的情况下都难以生长。植物可在很宽的范围内正常生长,但各种植物有自己适宜的pH。 喜酸植物:杜鹃属、越桔属、茶花属、杉木、松树、橡胶树、帚石兰; 喜钙植物:紫花苜蓿、草木犀、南天竺、柏属、椴树、榆树等; 喜盐碱植物:柽柳、沙枣、枸杞等。 2、植物病虫害与土壤酸碱性直接相关: 1)地下害虫往往要求一定范围的pH环境条件如竹蝗喜酸而金龟子喜碱; 2)有些病害只在一定的pH值范围内发作,如悴倒病往往在碱性和中性土壤上发生。 3、土壤活性铝:土壤胶体上吸附的交换性铝和土壤溶液中的铝离子,它是一个重要的生态因子,对自然植被的分布、生长和演替有重大影响; 在强酸性土壤中含铝多,生活在这类土壤上的植物往往耐铝甚至喜铝(帚石兰、茶树);但对于一些植物来说,如三叶草、紫花苜蓿,铝是有毒性的,土壤中富铝时生长受抑制;研究表明铝中毒是人工林地力衰退的一个重要原因。 二、土壤酸碱性对养分有效性的影响 1、在正常范围内,植物对土壤酸碱性敏感的原因,是由于土壤pH值影响土壤溶液中各种离子的浓度,影响各种元素对植物的有效性; 2、土壤酸碱性对营养元素有效性的影响: (1)氮在6~8时有效性较高,是由于在小于6时,固氮菌活动降低,而大于8时,硝化作用受到抑制; (2)磷在6.5~7.5时有效性较高,由于在小于6.5时,易形成磷酸铁、磷酸铝,有效性降低,在高于7.5时,则易形成磷酸二氢钙; 无机磷的固定 (3)酸性土壤的淋溶作用强烈,钾、钙、镁容易流失,导致这些元素缺乏。在pH高于8.5时,土壤钠离子增加,钙、镁离子被取代形成碳酸盐沉淀,因此钙、镁的有效性在pH6-8时最好; (4)铁、锰、铜、锌、钴五种微量元素在酸性土壤中因可溶而有效性高;钼酸盐不溶于酸而溶于碱,在酸性土壤中易缺乏;硼酸盐在pH5-7.5时有效性较好。 三、土壤酸碱性的改良 1、土壤酸性土改良 经常使用石灰。达到中和活性酸、潜性酸、改良土壤结构的目的。 沿海地区使用含钙的贝壳灰。也可用紫色页岩粉、粉煤灰、草木灰等。 石灰施用量 生石灰需要量(g/m2 )=阳离子代换量*(1—盐基饱和度)*土壤重量*28*1/1000 2、中性和石灰性土壤的人工酸化 露地花卉可用硫磺粉(50g/平方米)或硫酸亚铁(150克/平方米),可降低0.5——1个pH单位。也可用矾肥水浇制。 3、碱性土壤 施用石膏,还可用磷石膏、硫酸亚铁、硫磺粉、酸性风化煤。
首先,大量增施有机肥的同时,掺拌绿肥或松针土。有机肥能有效补充土壤中的有机质,建议菜农大量使用,亩施25-30方(之前多次报道,在此不再赘述)。而拌绿肥和松针土,是改良碱性土壤的快捷有效方法。绿肥和松针叶土是由杂草、腐烂的松柏针叶、残枝等枯落物堆沤而成,呈较强酸性。一般在碱性土中掺入1/5-1/6的绿肥或松针土,即可改善土壤的理化性状。 其次,配施的磷肥改用磷酸二铵或过磷酸钙。碱性土壤施用磷酸二铵和过磷酸钙使用效果很好。而在追施肥料过程中,尽量施用生理酸性肥料,如硫酸铵、硫酸钾等,这些肥料可中和土壤。 再次,应用碱性土壤改良剂。研究表明,石膏或磷石膏为主的土壤改良剂应用到碱性土壤效果明显。这种碱性土壤改良剂,其组成主要包括石膏、尿素等。这种利用作物秸秆混合石膏等,把化学改良和物理改良结合起来的方法,能从根本上改善土壤板结,效果显著。 另外,在实施以上三项措施时,需注意施用深度。一般底肥应施到整个耕层之内,即15-20厘米的深度。对于有机肥、氮肥、钾肥、微肥,可以混合后均匀地撒在地表,随即耕翻入土,做到肥料与全耕层土壤均匀混合,以利于作物不同根系层对养分的吸收利用。磷肥由于移动性差,且施入土壤后易被固定而失去有效性,所以在底施时应分上下两层施用,即下层施至15-20厘米的深度,上层施至5厘米左右的深度。上层主要满足作物苗期对磷的需求,下层供应作物生长中、后期的磷素营养。
酸性食品与碱性食品在营养学上﹐一般将食品分成酸性食品和碱性食品两大类。食品的酸碱性与其本身的PH值无关(味道是酸的食品不一定是酸性食品)﹐主要是食品经过消化﹑吸收﹑代谢后﹐最后在人体内变成酸性或碱性的物质来界定。产生酸性物质的称为酸性食品﹐如动物的内脏﹑肌肉﹑植物种子(五谷类)。产生碱性物质的称为碱性食品﹐如蔬菜瓜豆类﹐茶类等。 动物的内脏﹑肌肉﹑脂肪﹑蛋白质﹑五谷类﹐因含硫(S)﹑磷(P)﹑氯(Cl)元素较多﹐在人体内代谢后产生硫酸﹑盐酸﹑磷酸和乳酸等﹐他们是人体内酸性物质的来源﹔而大多数菜蔬水果﹑海带﹑豆类﹑乳制品等含钙(Ca)﹑钾(K)﹑钠(Na)﹑镁(Mg)元素较多﹐在体内代谢后可变成碱性物质。 碱性食品进入人体后与二氧化碳反应而成碳酸盐﹐由尿中排泄﹐酸性食品则在肾脏中与亚蒙尼亚生成铵盐而排泄﹐从而得以维持血液的正常PH(酸碱值)﹐正常人的血液PH为7.35﹐呈弱碱性。PH值由1至14﹐水的PH值是7(中性)。低于7就是酸性﹐高于7就是碱性。 如果过多食用酸性食品﹐以至不能中和而导致酸性﹐消耗钙﹑钾﹑镁﹑钠等碱性元素﹐会导致血液色泽加深﹐粘度﹑血压升高﹑从而发生酸毒症(Acidosis)﹐年幼者会诱发皮肤病﹑神经衰弱﹑胃酸过多﹑便秘﹑蛀牙等﹐中老年者易患高血压﹑动脉硬化﹑脑出血﹑胃溃疡等症。酸毒症是由于过多食用酸性食品引起的﹐所以不能偏食﹐应多吃蔬菜和水果保持体内酸碱的平衡。 水果虽然含有各种有机酸﹐吃起来有酸味﹐但消化后大多氧化成碱性食物。但草莓有不能氧化代谢的有机酸(苯甲酸﹑草酸)﹐会使体液的酸度增加﹐属于酸性食品﹐是个例外。存在于蔬菜中的有机酸主要是苹果酸﹑柠檬酸﹑酒石酸和草酸。这里特别要注意的是草酸﹐它的有机体不易氧化﹐与钙盐形成的草酸钙不溶于水而累积于肾脏中﹐影响了钙的吸收。在菜蔬中﹐西红柿﹑马铃薯﹑菠菜等都含有草酸。理论上碱性中毒(alkalosis)亦会发生﹐但人类碱性中毒现象不常见﹐因为人类有大量的胃酸可以中和。
十二水合磷酸氢二钠好像比较容易风化,那怎么直观的证明十二水合磷酸氢二钠没有变质?大家实验室的十二水合磷酸氢二钠是不是直接使用,或是可以105摄氏度烘成无水磷酸氢二钠??
请教一下各位:用什么方法能够准确测定焦磷酸二氢二钠中磷酸二氢钠含量?
磷酸氢二钠为什么那么难溶解呢?上次配磷酸盐缓冲试剂(磷酸氢二钠,氯化铵,磷酸氢二钾,磷酸二氢钾)的时候,几种称好,倒上水都结块了。跟石头一样。把玻璃杯都捣坏了都没溶解完。
氧化铝国标中测钠需取0.25g氧化铝加5毫升磷酸和1毫升浓硫酸加热溶解,如何加1毫升浓硫酸又安全又方便?怎样加1毫升浓硫酸更方便,加磷酸可以存于滴瓶里用滴管加,浓硫酸会和橡胶反应,该怎样加哇?
定总磷的方法测定磷酸根如何转化成磷酸三钠的纯度?这样检测磷酸三钠是否正确?
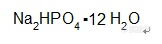
【中文名称】磷酸氢二钠【英文名称】sodium hydrogen phosphate;disodium monohydricphosphate【结构或分子式】 http://ng1.17img.cn/bbsfiles/images/2012/05/201205072109_365442_1855403_3.jpg【相对分子量或原子量】358.14【密度】1.52【熔点(℃)】34.6【折射率】1.432(20℃)【性状】 无色透明单斜晶系棱形晶体。【溶解情况】 溶于水,不溶于乙醇。【用途】 用作织物、木材和纸张的防火剂,釉药,焊药,并用于电镀等。可在食品工业中用作品质改良剂,作青霉素、链霉素的培养基、生产焙粉以及用作饲料添加剂。【制备或来源】 由碳酸钠和磷酸作用而制得。【其他】 在空气中迅速风化,在100℃失去结晶水而成无水物。在250℃分解成焦磷酸钠。在高于30℃的温度下由水溶液中结晶为7水物。【生产单位】 略
最近在做纺织品中芳香胺检测,国标《GBT 17592-2011 纺织品 禁用偶氮染料的测定》给的HPLC条件是:称取0.575g磷酸二氢铵+0.7g磷酸氢二钠,溶于1000ml水中,pH=6.9(也就是说各0.05mol/L),,如果按照方法中的重量称,配好的溶液pH是6.68,按照摩尔数称的话,pH是7,怎么和6.9也对不上。 我查了一下,我们使用的磷酸氢二钠试剂是含结晶水的,上面标的是Na2HPO4·12H2O,按照重量称的话,磷酸氢二钠的含量就不足0.05mo/l,所以pH低于6.9,我又按照摩尔数称的,pH又超过6.9,查到十二水合磷酸氢二钠很容易失去5个结晶水,我想是不是这个原因 那么你们在使用磷酸氢二钠的时候,所买试剂是否含有结晶水?如果是十二水合磷酸氢二钠,质量怎样计算呢?
十二水合磷酸氢二钠pH值为9.1-9.4(50g/L),但是60g/L时为何pH无明显变化?磷酸氢二钠溶液可能pH达到10.5么?若可能,是否风化、潮解、分解? 因目前发现磷酸氢二钠pH=10.5,暂未找到原因。
根据农业部标准NY 5029-2009 方法测定磺胺类药物,其中要用到Sep-Pak氧化铝B柱,在制备的时候遇到了困难,标准里面说:称取高温下加热3h的氧化铝粉,加水搅拌均匀,振荡3h后填充入玻璃柱中,用95%乙腈5ml前处理后备用。请问加入多少水呀!为什么要振荡呀!有碱性氧化铝卖吗?
各位好,今天做了土壤酸性和碱性磷酸酶的标准曲线,采用的苯磷酸二钠的方法。结果反应液的颜色没什么变化,而且吸光度值没有趋势。请问这是什么情况。请大家帮助分析一下!救命的啊
准备进行饲料中磺胺类药物的测定,要求使用碱性氧化铝小柱:1000mg/12mL, 120A,能否使用碱性氧化铝自己填充使用?所使用的碱性氧化铝粉末资料见http://www.reagent.com.cn/productsinfo.asp?id=20001860可是用途中说明其用于薄层色谱制板用,可以用于填充么?
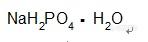
【中文名称】磷酸二氢钠;磷酸一钠;一代磷酸钠【英文名称】sodium dihydrogen phosphate;primary sodiumphosphate;monosodium phosphate【结构或分子式】 http://ng1.17img.cn/bbsfiles/images/2012/05/201205032059_364779_1855403_3.jpg 【相对分子量或原子量】137.99【密度】2.040【性状】 无色斜方晶体。【溶解情况】 易溶于水。不溶于乙醇。【用途】 是制造六偏磷酸钠和焦磷酸钠的原料,主要用于制革、处理锅炉水,作为品质改良剂和制焙粉,及在食品工业、发酵工业中作缓冲剂和发酵粉原料,还用作饲料添加剂、洗涤剂及染助剂等。【制备或来源】 由磷酸与碳酸钠在控制pH值下作用而制得。【其他】 在100℃失去结晶水,继续加热时分解而成酸性焦磷酸钠。【生产单位】 略
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=60980]湿法磷酸制磷酸三钠新工艺的研究[/url][img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=60981]湿法磷酸制磷酸三钠新工艺的研究[/url]
质量标准:WS-10001-(HD-0787)-2002释放度:取本品,照释放度测定法,采用溶出度测定法(中国药典2000年版二部附录X C第一法)装置试验,以0.1mol/L盐酸溶液750ml为溶剂,转速为每分钟100转,依法操作,经2小时,取溶液10ml,滤过,作为供试品溶液(1)。加入0.2mol/L磷酸钠溶液250ml,继续运转60分钟,取溶液10ml,滤过,作为供试品溶液(2)。取供试品溶液(1)以0.1mol/L盐酸溶液为空白,在259nm波长处测定吸收度,吸收值不得大于0.08。取供试品溶液(2),以0.1mol/L盐酸溶液75ml与0.2mol/L磷酸盐缓冲液25ml混合液为空白,按C10H14N5Na2O13P3的吸收系数(E)为279计算出每片的释放量。应符合规定。问题来了:0.2mol/L磷酸钠溶液与0.2mol/L磷酸盐缓冲液,到底用哪个?一般来说,溶出介质采用磷酸盐缓冲液,没有用磷酸钠溶液的吧?请教!!!
另外问下 有人用十二水磷酸氢二钠制取过磷酸氢二钠吗?
样品中有酸中不易消解的Cr2O3,考虑用碱性试剂(Na2CO3)铂金坩埚熔融消解,但查了一些资料有说 可以陶瓷坩埚消解 但是要加入MgO,C粉等与陶瓷部反映的试剂才可以 陶瓷坩埚的碱性熔融理论上是不可行的 不知道有没有朋友做过 如果有想请教一下经验 先谢谢了另外我做无机分析的目前主要使用微波消解仪,[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url],有同行朋友请加我QQ:490868976 [em01]
以十八烷基硅烷键合硅胶为填充剂;以乙腈-O.05mol/L磷酸二氢钠溶液(50:50)为流动相;检测波长为440 nm;柱温40℃。磷酸二氢钠刚好用完了,可以用磷酸二氢钾替代吗?不知道两者的PH是不是一样?
磷酸溶液中(磷酸含量1%-7%)含有铝离子,想用滴定方法检测磷酸含量,请问有什么比较好的方法吗?
求助各位大侠,我在做磷酸氢二钠的测定时其含量超过了100%,方法是严格按照国标做的,我想问一下这是什么原因造成的,用什么方法可以解决这个问题?感谢各位相助!小弟急用!!!