请教各位亲们,在做土壤中铅和镉 石墨炉方法时,里面加的掩蔽剂是磷酸氢二铵(优级纯)。做镉时,空白吸光度值是正常的,0.010-0.019.但是做铅的时候,同样是按照标准要求加了磷酸氢二铵,但是空白吸光度值却是0.2-0.3。怀疑可能是磷酸氢二铵过期了,现买来不及。样品催的急,呢么可不可以用磷酸二氢铵或者硝酸镧代替呢?

鲁索替尼是一种蛋白激酶的小分子抑制剂,其主要适用于治疗中间或高危骨髓纤维化,包括原发性骨髓纤维化,真性红细胞增多症后骨髓纤维化和原发性血小板增多症后骨髓纤维化患者。本试验中共有三个不同的鲁索替尼药片的产地,分别为 1 印度产; 2 香港产;3 土耳其产。三个不同来源的鲁索替尼片由于存在巨大的价格差,用仪器分析的方法判断,三者之间有什么区别。都是真的吗?提取方法:固体称重及溶解方法:采用电子分析天平,分别称取药物0.1g左右于5ml离心管中,并搅碎后,移取2ml乙腈于离心管中,溶解固体,并超声半小时,后静置2小时。将上清液过滤后,取出装进进样小瓶中用液相色谱分析。分析方法:色谱仪器:Agilent 1260 SL检测器:DAD色谱柱:phenomenex SYNERG1 4u POLAR-RP 80A 150*4.6mm色谱条件:乙腈:水=70 :30柱温:30度检测波长:227nm、254nm[align=center]检测结果[/align]1. 在227nm下各药片的液相分析图谱从保留时间看,三者一致![img=图1 印度,597,349]http://ng1.17img.cn/bbsfiles/images/2017/09/201709302026_01_1617661_3.jpg[/img]图1 印度产[img=图2 香港,602,363]http://ng1.17img.cn/bbsfiles/images/2017/09/201709302027_01_1617661_3.jpg[/img]图2 香港产[img=图3 土耳其,537,302]http://ng1.17img.cn/bbsfiles/images/2017/09/201709302027_02_1617661_3.jpg[/img]图3 土耳其产2 三种药片液相3D图[img=,557,349]http://ng1.17img.cn/bbsfiles/images/2017/09/201709302028_01_1617661_3.jpg[/img]4 印度产[img=,557,349]http://ng1.17img.cn/bbsfiles/images/2017/09/201709302028_02_1617661_3.jpg[/img]5 香港产[img=,537,335]http://ng1.17img.cn/bbsfiles/images/2017/09/201709302029_01_1617661_3.jpg[/img]6 土耳其产3 结果分析:1、从色谱分析图可以看出,三种药片的主要组分在相同液相色谱条件下出峰时间均为2.27左右,同时根据色谱3D图可以看出,在三个图在2.77左右的3D图是一样的,因此可以推断,此三种药片的组要组分是同一物质。4 数据分析以香港含量为100%计:[table][tr][td]产地[/td][td]印度[/td][td]香港[/td][td]土耳其[/td][/tr][tr][td]称重质量/g[/td][td]0.1026[/td][td]0.1184[/td][td]0.1016[/td][/tr][tr][td]峰面积%[/td][td]94.615[/td][td]96.182[/td][td]99.394[/td][/tr][tr][td]峰面积[/td][td]10229.7[/td][td]13077.5[/td][td]11064.9[/td][/tr][tr][td]相对含量[/td][td]90.2[/td][td]100[/td][td]98.6[/td][/tr][/table] 从含量结果看,香港与土耳其差别不大,印度含量低,同时感觉其杂质比较多。并且,无论是从色谱图的杂质出峰时间还是从3D图,可以看出,每个产地的药片中的杂质无论是含量还是组成,各不相同。 由于是药片,不好判断, 这些杂质来自辅料还是主药,但山寨的药物价格低廉跟药品的纯度和工艺有关,或许这检测可以提供参考。
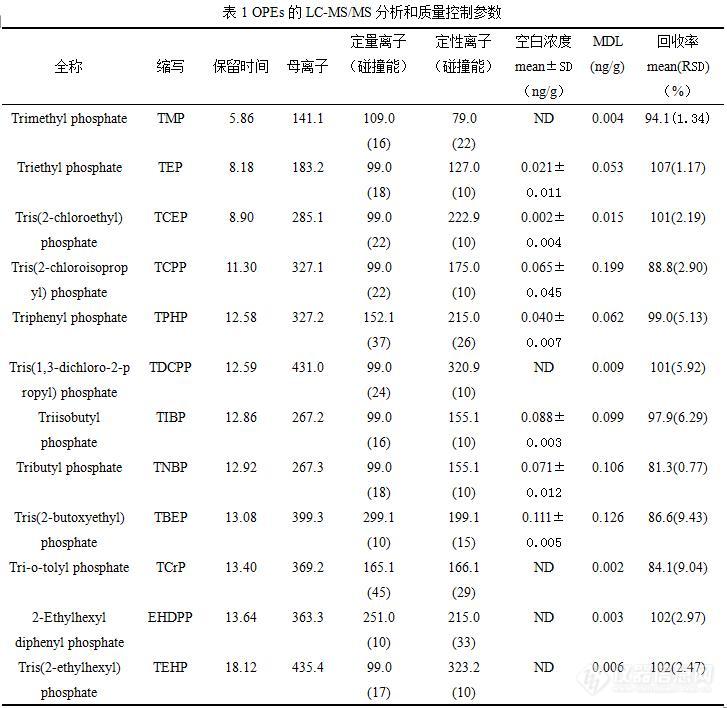
[align=center][b]方便面中有机磷酸酯的赋存及人体暴露风险[/b][/align][b]摘要:[/b]有机磷酸酯(Organophosphate esters, OPEs)在全球环境中被广泛检出,近年来受到了环境科学家的关注。目前已有一些关于食品中OPEs污染的研究,表明食品可能被其污染并成为人类暴露的重要来源。然而,作为深受消费者喜爱的快消食品方便面中的有机磷酸酯赋存研究极为缺乏。本研究对采集于中国北京市8种市售方便面(TY, KSF, NJC, JML, NX, XHX, CDK, HF)中12种OPEs的残留水平进行了分析。12种OPEs单体中,有8种单体在方便面中检出,∑8OPEs 浓度范围为1.28-99.3ng/g dw。TY中总OPEs残留水平最高。成人和青少年通过摄入方便面所致∑8OPEs的每日预计摄入量分别为2.67和7.53 ng/kg bw/day。TY是不同方便面中总OPEs暴露量的主要贡献者。初步暴露评估表明,目前通过方便面摄入的OPEs所致的慢性疾病危险商数在10-6-10-3范围内,处于低风险水平。此外,OPEs的危险指数表明,青少年(3.04×10-3)的风险高于成人(1.08×10-3)。[b]关键词:[/b]有机磷酸酯;方便面;每日预计摄入量;危险商数;危害指数有机磷酸酯(OPEs)是一组人工合成的磷酸衍生物,其作为阻燃剂、增塑剂、消泡剂、液压油、油漆和地板抛光剂等中的添加剂已使用了几十年。近年来,传统型溴代阻燃剂多溴二苯醚和六溴环十二烷因为具有持久性、生物富集性和生物毒性而相继禁用,OPEs的产量和使用量逐年增加。OPEs作为添加剂掺合到使用的材料中,其与材料之间没有稳定的化学键合作用,因此会通过磨损、泄露和挥发等方式缓慢的释放到周边环境中。目前,OPEs在空气、灰尘、水和沉积物等环境介质,水生动物,陆生动物甚至是人体血液、母乳和尿液中均有检出,表明OPEs的污染已经无处不在。许多毒理学研究表明OPEs,如三(2-正丁氧乙基)磷酸酯(Tris(2-butoxyethyl) phosphate,TBEP),三(1-氯-2丙基)磷酸酯(Tris(2-chloroisopropyl) phosphate,TCPP),三(1,3-二氯-2丙基)磷酸酯(Tris(1,3-dichloro-2-propyl) phosphate,TDCPP),三乙基磷酸酯(TEP)和三甲苯基磷酸酯(Tri-cresyl Phosphate, TCrP)对鱼类,鸟类,啮齿动物和人类的胚胎发育,mRNA表达,甲状腺激素分泌,循环胆汁酸分泌以及神经系统具有毒副作用。此外,三(2-氯乙基)磷酸酯(Tris(2-chloroethyl) phosphate,TCEP)、TCPP、TDCPP、TBEP、三正丁基磷酸酯(Tributyl phosphate, TNBP)、三苯基磷酸酯(Triphenyl phosphate, TPHP)具有潜在的致癌性。因此,了解OPEs的人体暴露水平对于制定策略用以管控其潜在危害十分重要。空气吸入,皮肤接触灰尘和饮食摄入是OPEs暴露于人体的主要途径。 目前,已有一些研究报道了皮肤接触灰尘和吸入是OPEs暴露于人体的两个重要途径,然而OPEs的膳食暴露研究却十分有限。食品在生产、储存和加工期间可能被环境中无处不在的OPEs和存在于涉及食品加工的若干材料中的OPEs污染,从而成为人类暴露的重要来源。方便面是深受消费者喜爱的快消食品。我国作为方便面的生产及消费大国,2015年总消费量为404.3亿份,占全球41.4%,远高于其他国家。然而,关于方便面中有机磷酸酯的残留水平及暴露风险的研究仍未见报道。本研究对采集于北京市8种市售方便面(TY, KSF, NJC, JML, NX, XHX, CDK, HF)中12种OPEs的残留水平进行了分析,对OPEs的暴露水平和风险进行了评估。该结果可以初步了解居民通过方便面摄入OPEs的暴露状况。[b]1 实验部分1.1 仪器、试剂与材料[/b]高效液相色谱仪(Ultimate 3000, 美国Thermo公司),三重四级杆质谱仪(TSQ Quantiva, 美国Thermo公司),高速离心机(美国Sigma-Aldrich公司),低速离心机,氮吹浓缩仪(REACTI-THERM III#TS-18824, 美国Thermo公司),分析天平(CP224S, 德国Sartorius公司)。[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]级别溶剂甲醇和乙腈均购自于美国Fisher Scientific。HPLC级甲酸(Formic acid)购自中国DiKMA公司。分散固相萃取填料氨丙基硅胶(PSA)和十八烷基硅烷(C18)均购自美国Sigma-Aldrich公司。无水MgSO4和NaCl分别购自美国Sigma-Aldrich公司和中国医药集团有限公司,二者使用前置于马弗炉中450℃烘烤8h以去除可能残留的有机物。OPEs标准品,三甲基磷酸酯(Trimethyl phosphate, TMP, 纯度95%)和三异丁基磷酸酯(Triisobutyl phosphate, TiBP, 纯度95%)分别购自美国AccuStandard公司和中国J&K Scientific公司。 纯度为98%的标准品TEP、TCEP、TCPP、TPHP、TDCPP和TNBP均购自美国Cambridge Isotope Laboratories。TBEP、TCrP、2-乙基己基二苯基磷酸酯(2-Ethylhexyl diphenyl phosphate, EHDPP)和磷酸三辛酯(Tris(2-ethylhexyl) phosphate, TEHP)标准品纯度大于98%,均购自于美国Wellington Laboratories。OPEs同位素标准品,包括TEP-d15、TCEP-d12、TCPP-d18、TDCPP-d18、TPHP-d15和TNBP-d27 均购自于美国Cambridge Isotope Laboratories。TEHP-d51(纯度100%)购自于加拿大Toronto Research Chemicals公司。[b]1.2 样品及前处理[/b]8种不同品牌的方便面样品采集自北京市区超市。使用粉碎机将面饼充分粉碎后,准确称取1g样品加入到15mL Corning离心管中,然后加入7种氘代OPE作为内标(1ng)并老化过夜。之后,加入5 mL含0.5%甲酸的乙腈溶液并涡旋1-2min至其完全混合。使用超声萃取10min,之后在4000 r/min下离心并收集上清液。提取步骤以上述相同步骤重复两次,并将提取溶液合并。合并提取液使用高纯氮气在柔和气流下浓缩至2mL。然后加入400 mg MgSO4和100 mg NaCl并涡旋1min,在4000 r/min下离心5min。将上清液小心转移至干净的Corning 离心管中,加入300 mg MgSO4和100 mg PSA以进一步去除杂质。同上,涡旋、离心、收集上清液。然后用高纯氮气以柔和气流下吹干,然后复溶至1 mL甲醇,保存于冰箱中(4℃)。进样前,在12000 r/min下离心5min,取上清液上机分析,进样量为10μL。[b]1.3 仪器分析[/b]OPEs的分析使用HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS系统。液相分离色谱柱为SunFire C18柱(4.6mm×150mm×3.5μm, Waters),柱温为40℃。采用二元流动相(A:超纯水,B:甲醇,二者均含0.1%的甲酸)进行梯度洗脱,流速为1mL/min,梯度洗脱程序为:0min (10%B),2min (10%B),5.5min (65%B),9.5min(80%B),11.5min(100%B),15min(100%B),16min(10%B),20min(10%B)。OPEs的保留时间见表1。三重四级杆质谱使用电喷雾离子源并以正离子模式运行。电喷雾电压为3.5千伏,喷雾锥和离子传输管温度均为350℃。氩气和氮气分别充当碰撞气和脱溶剂气。质谱数据采集模式为选择反应离子监测(selected reaction monitoring, SRM),每种OPEs分析物的SRM参数,包括定量/定性离子对、碰撞能等列于表1。[b]1.4 质量控制[/b]每批实际样品处理中均加入程序空白,以监测实验过程中可能存在的污染,详细数据列于表1。对于程序空白中检出的OPEs单体,以其平均浓度加上3倍标准偏差计算化合物的方法检出限(MDL)。对于程序空白中未检出的OPEs单体,以仪器检出限(IDL,3倍信噪比计算而得)代替方法检出限。本文中OPEs的方法检出限范围为:0.002-0.19ng/g,详细数据见表1。本文使用7种OPEs氘代同位素标准品作为内标,配制了内标标准曲线,线性范围为:0.1-100ng/mL,0.998 JML(2.59 ng/g dw) CDK(2.31 ng/g dw) XHX(1.43 ng/g dw) NX(1.39 ng/g dw) HF(1.28 ng/g dw)。JML、XHX、NX和HF中均以TEP和TCPP为主要单体,二者对于∑8OPEs的贡献率范围为67.6%-86.7%(77.9%,均值)。NJC中主要的OPE单体为TCrP、TPHP、TCPP和TDCPP,总贡献为89.4%,而CDK中主要的OPE单体为EHDPP、TCEP和TCPP,总贡献为73.6%。不同方便面中OPEs浓度和单体组成差异性可能与其使用的原材料、生产工艺以及包装材料差异有关。尽管不同方便面中每种OPE单体对于∑8OPEs的相对贡献率不同,但8种方便面总体上以TEP, TCEP和TCPP为主要单体,其贡献总和为78.4%(见图3),表明这三种OPE单体在方便面的生产加工或者包装中有相似的来源。[align=center][img=,690,391]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312016446825_2789_2823651_3.jpg!w690x391.jpg[/img][/align][align=center][img=,592,384]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312018367142_8877_2823651_3.jpg!w592x384.jpg[/img][/align][align=center][img=,562,380]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312021278938_1636_2823651_3.jpg!w562x380.jpg[/img][/align][align=center][img=,549,389]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312021462572_4041_2823651_3.jpg!w549x389.jpg[/img][/align][align=left][b]2.2 OPEs暴露量及其风险评估[/b][/align]表2给出了成人和青少年的OPEs膳食摄入量。成人总OPEs的平均EDIs值为2.67 ng/kg bw/day,低于青少年总OPEs的平均EDIs值(7.53 ng/kg bw/day)。TCEP和TEP是OPEs中暴露剂量最高的两种单体,二者暴露剂量之和约占总OPEs暴露剂量的93%。成人TCEP和TEP的平均EDIs值分别为2.13和0.35 ng/kg bw/day,低于青少年中TCEP和TEP的平均EDIs值(6.01和0.99)。方便面中赋存的OPEs通过膳食暴露于人体可能对健康产生危害,因此对每种OPEs单体暴露风险(HQ)及∑[sub]8[/sub]OPEs的暴露风险(HI)进行了评估,结果见表2。成人因方便面膳食摄入所致∑[sub]8[/sub]OPEs的暴露风险(HI)值为1.08×10[sup]-3[/sup]小于儿童HI 值3.04×10[sup]-3[/sup],二者因膳食方便面暴露于OPEs所致的暴露风险较低(HI1)。就每种OPEs单体而言,成人和儿童因方便面膳食摄入所致TCEP的暴露风险(HQ)值最高,分别为9.68×10[sup]-4[/sup]和2.73×10[sup]-3[/sup]。值得注意的是,本文仅评估了居民通过摄入方便面暴露于OPEs的健康风险,没有进行广泛的食品调查,因此居民通过饮食摄入暴露于OPEs的健康风险可能被低估;并且儿童和青少年作为易感人群,在未来OPEs的膳食暴露研究中更值得关注。[align=center][img=,690,391]https://ng1.17img.cn/bbsfiles/images/2019/08/201908312026331842_336_2823651_3.jpg!w690x391.jpg[/img][/align][align=left][b]3 结语[/b]在本研究中,12种OPEs单体中有8种单体在方便面中检出,∑8OPEs 浓度范围为1.28-99.3ng/g dw。TY中总OPEs残留水平最高。本研究的结果表明,通过摄入方便面是OPEs暴露于我国人体的一种重要途径;青少年作为易感人群,可能具有更高的暴露风险。此外,某些品牌中OPEs含量较高,为降低因长期摄入该品牌方便面带来的潜在健康风险,建议经常更换品牌进行消费。[/align][b]参考文献[/b]1. Wei, G. L. Li, D. Q. Zhuo, M. N. Liao, Y. S. Xie, Z. Y. Guo, T. L. Li, J. J. Zhang, S. Y. Liang, Z. Q. Organophosphorus flame retardants and plasticizers: sources, occurrence, toxicity and human exposure. Environ Pollut. 2015, 196, 29-46.2. Greaves, A. K. Letcher, R. J. A Review of Organophosphate Esters in the Environment from Biological Effects to Distribution and Fate. Bulletin of environmental contamination and toxicology. 2017, 98(1), 2-7.3. Greaves, A. K. Letcher, R. J. Comparative body compartment composition and in ovo transfer of organophosphate flame retardants in North American Great Lakes herring gulls. Environmental science & technology. 2014, 48(14), 7942-7950.4. Li, J. Xie, Z. Mi, W. Lai, S. Tian, C. Emeis, K. C. Ebinghaus, R. Organophosphate Esters in Air, Snow, and Seawater in the North Atlantic and the Arctic. Environmental science & technology. 2017, 51(12), 6887-6896.5. Salamova, A. Hermanson, M. H. Hites, R. A. Organophosphate and halogenated flame retardants in atmospheric particles from a European Arctic site. Environmental science & technology. 2014, 48(11), 6133-6140.6. He, C. Wang, X. Tang, S. Thai, P. Li, Z. Baduel, C. Mueller, J. F. Concentrations of Organophosphate Esters and Their Specific Metabolites in Food in Southeast Queensland, Australia: Is Dietary Exposure an Important Pathway of Organophosphate Esters and Their Metabolites? Environmental science & technology. 2018, 52(21), 12765-12773.7. 郭齐雅, 于冬梅, 赵丽云, 等. 2010-2012年中国6岁及以上居民方便面消费状况.卫生研究, 2018, 47(5), 700-704.8. Zhang, X. Zou, W. Mu, L. Chen, Y. Ren, C. Hu, X. Zhou, Q. Rice ingestion is a major pathway for human exposure to organophosphate flame retardants (OPFRs) in China. Journal of hazardous materials. 2016, 318, 686-693.9. Guo, X. Mu, T. Xian, Y. Luo, D. Wang, C. Ultraperformance liquid chromatography tandem mass spectrometry for the rapid simultaneous analysis of nine organophosphate esters in milk powder. Food chemistry. 2016, 196, 673-681.
按照中国药典,石墨炉法,标准曲线法测定磷酸氢钙中铅元素,样品加标回收率不合格,单独测铅标准回收率合格,表明是样品的基体干扰导致的,高盐样品如何测定其中痕量元素?谢谢
在[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原吸[/color][/url]石墨炉分析中经常使用基体改进剂,这是大家共所周知的;其中磷酸二氢铵和磷酸氢二铵因价格便宜(相对硝酸钯而言)目前仍有一些行业在用,对于上述两种改进剂的性质区别、应用效果、如何选用等问题我询问了许多业内人士均未给出明确的答复,在此版面中期待哪位有此经验的高手奉献出答案为盼!谢谢!
目前有很多客户的无卤要求已经不仅仅只是要求控制氯和溴的使用,同时还要求了三氧化二锑、红磷和磷酸三苯酯等物质。针对这三种物质:1,这三种物质的简单介绍;2,各自的用途(也就是那些材料需要我们重点关注);3,检测方法以及所选用之检测方法是否适应客户管控要求?由于我自己的分也不多,所以悬赏也只能聊表心意了,哈哈,重要的是大家踊跃参与就可以获得5个经验和2个声望。。[em0803]
请问哪位朋友对这一方面比较熟悉,最近我们公司的锅炉水送检,发现磷酸根浓度偏高,请问有什么方法能更好地控制其浓度?还有就是有没有用过磷酸根检测试纸的,好不好用?谢谢了
磷酸二氢铵和磷酸氢二铵做基体改进剂那个更好,不知道大家做个测试没有啊,我个人经验是磷酸氢二铵效果较好,是不是多了一个氨基的缘故呢?欢迎各位同仁专家做个分析哦?
高盐类的样品分析一直是个难题,近日也有版友在论坛中求助相关背景高等等问题。近日有机会做了酱油实验,对高盐样品也有了一些认识,现将实验中使用不同基体改进剂的数据与大家分享,欢迎大家讨论。1.仪器设备日立ZA3000原子吸收光谱仪铅元素空心阴极灯:北京曙光明(国产灯)Barnstead超纯水装置(美国)容量瓶:100mL、50mL、1000mL移液管:1mL、5mL、10mL2.试剂铅单元素标准溶液:1000mg/L(国家标准物质中心)实验用水均为去离子水硝酸(优级纯):北京试剂厂钯粉(优级纯):国药集团硝酸铵(分析纯):天津试剂厂磷酸二氢铵(优级纯):国药集团3.溶液配置硝酸溶液:c(HNO3)1%:取8mL硝酸溶液用去离子水稀释至500 mL,备用;1000mg/L 硝酸钯:准确称取0.1g钯粉置于烧杯中,用5mL浓硝酸加热溶解,待钯粉溶解后,转移定容至100mL锥形瓶中,得1000mg/L硝酸钯溶液1%硝酸铵:准确称取1g硝酸铵,用去离子水定容至100mL2%磷酸二氢铵:准确称取2g硝酸铵,用去离子水定容至100mL4.标准曲线的配制用移液管移取铅单元素标准溶液1mL于100 mL容量瓶中,以1%硝酸稀至刻度,混匀,既得10 mg/L铅储备液。以同样方法,逐级稀释得20μg/L铅标准储备液,备用。5.测试实验(石墨炉法)5.1仪器工作条件 Pb 仪器条件仪器 ZA3000 原子化方式 GA 检测波长(nm) 283.3 灯电流(mA) 7.5 狭缝宽度(nm) 0.4 石墨管 C型热解石墨管 测定参数测定模式 工作曲线法 信号模式 BKG校正 信号采集 峰高 时间常数(s) 0.1 温控 ON GA自动进样器进样体积(μL) 20 进样速度 4 测定阶段开始温度 结束温度 升温时间 保持时间 气体流量 气体种类 干燥 50 100 40 0 200 常规 干燥 100 140 20 5 200 常规 灰化 500 500 20 0 200 常规 原子化 2000 2000 0 5 30 常规 清除 2400 2400 0 4 200 常规 冷却 0 0 0 10 200 常规 使用C型热解石墨管,光温度控制,石墨炉升温条件5.2基体改进剂种类对实验影响的摸索5.2.1 5μL 2%磷酸二氢铵做基改http://ng1.17img.cn/bbsfiles/images/2015/08/201508261118_562953_2846602_3.bmp背景值高达1Abs,该情况下数据可信度大大下降,因为没有消除高盐背景的干扰,所以数据重现性也很差,且容易形成严重的记忆效应,指示数据不稳定。5.2.2 5μL 1%磷酸铵做基改http://ng1.17img.cn/bbsfiles/images/2015/08/201508261122_562955_2846602_3.bmphttp://ng1.17img.cn/bbsfiles/images/2015/08/201508261124_562956_2846602_3.bmp背景值高大大降低,达到与样品吸光度接近,背景在原子化之前基本清除。但是从谱图可见,出现双峰现象,该情况可以考虑使用硝酸钯基改,改善峰形。5.2.3 5μL 1000mg/L硝酸钯+5μL 2%
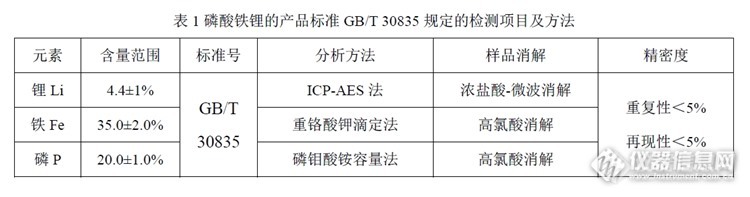
[align=center][b]磷酸铁锂中锂、铁、磷的测定方法改进[/b][/align][align=center]中国船舶重工集团公司第七二五研究所 试验测试与计量技术研究中心 张斌彬[/align][align=left] 随着移动电子设备的迅速发展, 电池要求具有高比能量、长寿命、低成本、环境兼容等特点, 这就促使锂离子电池正极材料研究不断开拓新的方向。磷酸铁锂是一种新型的锂电子电池正极材料,和传统的钴酸锂相比,具有毒性小,成本低、循环寿命长和安全性好等优点,自20世纪90年代进入产业化阶段以来,已广泛应用于手机、数码产品、电动工具和电动汽车等领域,是目前国内外锂电行业主要的产业化产品。磷酸铁锂中锂、铁、磷三种主元素的准确定量对于合成工艺调整、产物性能研究和产品质量控制有重要意义。[/align] 2015年,某厂商采购了一批磷酸铁锂材料,并慕名咨询到我们中船重工725所检测中心进行入厂复验。受客户委托,我们对磷酸铁锂材料的现有分析方法进行了详细的调研,并结合工作实际建立了准确可靠的分析方法用于试验,得到客户的一致好评!现将方法建立过程摘要如下,望各位大神多多指导![b]一、现有方法调研[/b] 经调研,磷酸铁锂的产品标准GB/T 30835中仅规定了主成分磷、铁、锂的含量范围及仲裁分析方法,详见下表:[align=center]表1磷酸铁锂的产品标准GB/T 30835规定的检测项目及方法[/align][align=center][img=,690,181]http://ng1.17img.cn/bbsfiles/images/2017/07/201707302147_01_2401507_3.jpg[/img][/align]已有报道的文献分析方法见下表:[align=center]表2 已公开报道的文献分析方法[/align][align=center][img=,601,729]http://ng1.17img.cn/bbsfiles/images/2017/07/201707302148_01_2401507_3.jpg[/img][/align][b] 二、方法改进与确认[/b] 尝试对磷酸铁锂中锂、铁、磷含量的分析方法进行改进,拟建立能够同时分析锂、铁、磷含量的ICP-OES分析方法,具体试验过程如下:[b]1. 样品溶解[/b] 磷酸铁锂的生产大多采用固相高温合成方法, 溶解比较困难,比较几种溶样用酸后,采用下述方法可使样品溶解完全:称取0.1 g磷酸铁锂样品,加入5 mL高氯酸,缓慢加热至高氯酸冒烟,继续加热至样品完全溶解,溶液澄清,冷却至室温,定容到200 mL容量瓶中。随样品配制空白溶液。[b]2. 配制标准溶液[/b] 用高纯铁,磷(1 mg/L)标准溶液,锂(1 mg/L)标准溶液,按基体匹配法配制系列标准溶液。[b]3. 谱线选择[/b] 样品中锂、铁、磷含量均在1 %以上,对样品进行谱线干扰扫描试验,锂、铁、磷的分析谱线间无元素干扰,实验室使用Leeman Prodigy XP型ICP-OES,选择分析谱线如下:[align=center]表3 分析谱线[/align][align=center][img=,690,98]http://ng1.17img.cn/bbsfiles/images/2017/07/201707302148_02_2401507_3.jpg[/img][/align][b]4. 仪器参数[/b] 仪器参数设置列于下表。[align=center]表4 仪器参数[/align][align=center][img=,690,101]http://ng1.17img.cn/bbsfiles/images/2017/07/201707302148_03_2401507_3.jpg[/img] [/align] 按上述仪器参数和分析谱线,建立校准曲线,各元素线性相关系数均大于0.999。测定样品后,选取和样品含量接近的标准样品溶液作为控样,对分析准确性进行验证,测定值与标准值误差均小于0.05 %,能够实现锂、铁、磷的快速准确测定。后续对检出限、定量范围高低标精密度、样品测定重复性试验精密度和加标回收率也做了相关验证,RSD<5 %,回收率在90 %~105 %,达到ISO 17025对非标试验的验证准则要求,能够满足日常分析检测和科研的要求。[b]三、心得与体会[/b] 测定方法改进实验过程中的几点心得和总结,还望各位大神多多指正:1.磷酸铁锂中含有一定量的石墨,在选择样品消解用酸时发现,与文献和标准一致,只有高氯酸可使样品消解完全,且不能加蒸馏水,否则样品极难快速消解完全。2.样品中的磷在消解过程中会转化为磷酸,使样品溶液黏度变大,不利于样品溶液雾化,对分析方法的稳定性有一定影响,即使增大雾化器流量,也无明显改善。但是加入少许醋酸后,可以显著提高光谱强度,降低RSD值。3.样品消解完全可以避免出现由于消解不完全或石墨粉包裹样品造成测定值偏低的情况出现,有利于提高分析准确度。4.改进后的方法可以同时测定磷酸铁锂中的锂、铁、磷。如果同时测定样品中的杂质,由于含量差别较大,为保证准确度,杂质元素的测定可尝试标准加入法或增大称样质量等方式,具体的方法还在摸索之中,欢迎有相关检测经验的达人不吝赐教。
氯化钠、硫酸钠、磷酸盐等固体试剂有有效期吗?一般是多久呢?一般是多久呢?如果过期了 还没有用完,该怎么处理呢?
最近在做纺织品中芳香胺检测,国标《GBT 17592-2011 纺织品 禁用偶氮染料的测定》给的HPLC条件是:称取0.575g磷酸二氢铵+0.7g磷酸氢二钠,溶于1000ml水中,pH=6.9(也就是说各0.05mol/L),,如果按照方法中的重量称,配好的溶液pH是6.68,按照摩尔数称的话,pH是7,怎么和6.9也对不上。 我查了一下,我们使用的磷酸氢二钠试剂是含结晶水的,上面标的是Na2HPO4·12H2O,按照重量称的话,磷酸氢二钠的含量就不足0.05mo/l,所以pH低于6.9,我又按照摩尔数称的,pH又超过6.9,查到十二水合磷酸氢二钠很容易失去5个结晶水,我想是不是这个原因 那么你们在使用磷酸氢二钠的时候,所买试剂是否含有结晶水?如果是十二水合磷酸氢二钠,质量怎样计算呢?
有关物质检查方法参照USP-34:有关物质 取装量差异项下的细粉适量(相当于头孢地尼75mg),置50ml量瓶中,加0.1mol/L磷酸缓冲液30ml溶解,并用0.1%四甲基氢氧化铵溶液稀释至刻度,制成每1ml约含头孢地尼1.5mg的溶液,滤过,取续滤液作为供试品溶液。精密称取头孢地尼对照品适量,加0.1mol/L磷酸缓冲液溶解并定量稀释制成每1ml中约含头孢地尼0.75mg的溶液,精密量取适量,加0.1%四甲基氢氧化铵溶液并定量稀释至每1ml约含头孢地尼15μg的对照品溶液。照高效液相色谱法(中国药典2010版二部附录V D)测定,用十八烷基硅烷键合硅胶为填充剂(粒径:5um,规格:4.6mm×250mm);流动相A为0.1%四甲基氢氧化铵溶液(用磷酸调节pH值至5.5)1000ml,加入0.1mol/L乙二胺四醋酸二钠溶液0.4ml,流动相B为0.1%四甲基氢氧化铵溶液(用磷酸调节pH值至5.5)-乙腈-甲醇(500:300:200),加入0.1mol/L乙二胺四醋酸二钠溶液0.4ml;按表Ⅰ进行线性梯度洗脱。柱温为40℃,检测波长为254nm。精密称取头孢地尼对照品约37.5mg,置25ml量瓶中,加0.1mol/L磷酸缓冲液10ml溶解,并加入头孢地尼杂质A对照品溶液(取头孢地尼杂质A对照品适量,加0.1%四甲基氢氧化铵溶液溶解并稀释制成每1ml含0.04mg的溶液)5.0ml、头孢地尼杂质B对照品溶液(取头孢地尼杂质B对照品适量,加0.1%四甲基氢氧化铵溶液溶解并稀释制成每1ml含0.04mg的溶液)5.0ml,用0.1%四甲基氢氧化铵溶液稀释至刻度,摇匀,作为系统适应性溶液,取10μl注入液相色谱仪,记录色谱图;头孢地尼峰保留时间约为20分钟,头孢地尼杂质A有四个峰,相对头孢地尼主峰保留时间分别约为0.85、0.94、1.11和1.14;头孢地尼杂质B峰相对头孢地尼主峰保留时间约为1.28;头孢地尼峰与头孢地尼杂质A第三个峰之间的分离度应不小于1.5;头孢地尼杂质B峰的拖尾因子不大于1.5。取对照品溶液10μl注入液相色谱仪,调节检测灵敏度,使主成分色谱峰的峰高约为满量程的20%,精密量取对照品溶液和供试品溶液各10μl,注入液相色谱仪中,记录色谱图。供试品溶液色谱图中如有杂质峰,均采用以下公式按外标法以峰面积计算,杂质的限度见表Ⅱ。(供试品溶液中任何小于头孢地尼对照品溶液主峰面积0.05倍的峰可忽略不计)。表Ⅰ时间(分钟)流动相A(%)流动相B(%)095529552275253250503750503895548955杂质的含量采用以下公式计算:(rU/rS)×(Cs/CU)×(100/F)Cs为头孢地尼对照品溶液中头孢地尼的浓度(mg/ml);CU为供试溶液中头孢地尼的浓度(mg/ml);rU为供试溶液中杂质峰面积;rS为头孢地尼对照品溶液中头孢地尼峰面积;F为表Ⅱ中各杂质的相对响应因子;表Ⅱ 有关物质相对保留时间相对响应因子限值(%)杂质Ⅷ[/siz
近日用石墨炉法做食品中铅的测试,为了消除背景干扰和减少铅在灰化阶段的损失,使用了磷酸氢二铵做基体改进剂(浓度2g/100ml,进样量5微升),由于测试结果高于考核样给定的浓度(事后已知考核样的真值浓度),故怀疑是改进剂被铅污染,于是单做改进剂的吸光值来判定其中是否有铅的成分(进样量20微升,使用热解石墨管):(1)当灰化温度为450度,原子化温度为1800度时,样品吸光度为0.0577Abs,背景吸光度为0.0114Abs;(2)当灰化温度提高到700度(在前面食品分析中,灰化温度也是700度),原子化温度仍为1800度,样品吸光度为0.0002Abs,背景吸光度为0.0044Abs;问 题:(1)通过结果2可以判定基体改进剂中没有铅的成分;因为后来对铅标液中分别测定加与不加基体改进剂的两次测定结果一致性也可以判断出。(2)如果改进剂中没有铅为何在结果1中会得到那样高的铅的吸光值呢?为何灰化温度不同,而结果却不尽相同呢?上述问题困惑我许久,无奈将此问题发在网上,希望高人不吝赐教,谢谢!
液相测试0.1%磷酸溶液一般指的是质量分数还是体积分数药典上流动相是乙腈-0.1%的磷酸溶液,请问,0.1%指的是质量分数还是体积分数?我要配1000ml的0.1%磷酸溶液,加1ml的磷酸,可以这样配吗?为什么很多流动相中都会加一些磷酸呢?谢谢

磷钼蓝分光光度法测定锅炉水中磷酸盐含量试验平行误差的确定1.实验部分根据“磷钼蓝分光光度法测定锅水中磷酸盐含量”的规定,取5mL水样(当水样中PO43-≥50mg/L时,取2mL水样)于50mL容量瓶中,加入2.5mL钼酸铵-硫酸液,混匀,加入0.15mL氯化亚锡-甘油液,定容、混匀。放置2分钟后,放入1cm比色皿中,于706nm波长下比色。2.数学模型的建立 磷酸盐含量标准系列回归方程y=a+b×x,由此可得到样品制备液的吸光度所对应的磷酸根含量: y=0.0011+0.1916×x;水中磷酸根浓度为C=y×1000/V (mg/L)式中:C为水样中磷酸盐的浓度(mg/L) ;y为制备液中磷酸根的含量(mg);V为取样量(mL)。x为吸光度3不确定度的评定A)对PO43-=0~10 mg/L含量范围的误差计算3.1重复性测定引入的相对不确定度μrel(A类)采用A类方法评定,与重复性有关的合成标准不确定度均包含在其中。对某锅炉水样品进行了8次重复性测定,取5mL水样,所得的数据如下:http://ng1.17img.cn/bbsfiles/images/2013/09/201309050647_462392_2166779_3.pnghttp://ng1.17img.cn/bbsfiles/images/2013/09/201309050648_462393_2166779_3.png
按照中国药典四部测定磷酸氢钙中铅元素含量,石墨炉标准曲线法,做准确度时,样品加标回收率为40%左右,单独测标准铅溶液的回收率为100%,考虑是高盐样品干扰,请问各位老师,如何解决?加入磷酸二氢铵~硝酸镁基体改进剂5微升,回收率为50%,标准是70%-150%。基体改进剂有没有能改进钙离子的?让它不发生原子化?
今天做实验,遇到有趣的事情,看看大家怎么看流动相:甲醇+水、甲醇+0.1%磷酸、甲醇+0.2%磷酸、甲醇+0.5%磷酸同一比例下,对物质的保留时间差异很大,如何选择,有诀窍吗?谈谈你的观点和认识http://simg.instrument.com.cn/bbs/images/default/em09511.gif
石墨炉测铅加的基体改良剂磷酸二氢铵盒子上写的不是GR而是for HPLC可以用吗?[img]https://ng1.17img.cn/bbsfiles/images/2019/12/201912131212028791_3671_4008317_3.png[/img]
按GB5750-2006每100ml去离子水中加入10ml的120g/L的磷酸二氢铵溶液,进样20ul入石墨炉。。。 125度干燥30秒 600度灰化30秒 无异常 原子化1800度。。。哇 好大的一个烟圈从石墨炉的进样口喷出 [em0904][em0904][em0904] 各位DX碰到过这种情况吗?? 是不是我的磷酸二氢铵配的有问题??该如何处理??
耸人听闻的标题是为了加速吸引人群围观,不过也不全是为空穴来风。使用磷酸氢二铵作为基改早已普遍应用,然而在PE800的随机资料“WinLab 32 for AA”中关于“如何准备基体改进剂”一节里,要求配制1%磷酸二氢铵和0.06%硝酸镁,却不让用磷酸氢二铵,它在上面写道:“Caution:do not use (NH4)2HPO4”(不要用磷酸二氢铵)。这是为何呢?
以十八烷基硅烷键合硅胶为填充剂;以乙腈-O.05mol/L磷酸二氢钠溶液(50:50)为流动相;检测波长为440 nm;柱温40℃。磷酸二氢钠刚好用完了,可以用磷酸二氢钾替代吗?不知道两者的PH是不是一样?
磷酸有较低的蒸气压,在0.8MPa时温度可达240 ℃。热HP04 适用于消解那些用HCl消解时会使某些特定痕量组分挥发损失的铁基合金,磷酸还可溶解铬矿、氧化铁矿、铝炉渣等。你是否在微波消解中使用过磷酸?当你在使用磷酸消解样品的时候一般是与其它酸组合使用的吧?具体用于哪类样品的消解?
锅炉水的磷酸根保持在多少比较好?
请问TCPP三磷酸酯和CTPB端羧聚丁二烯这两个阻燃剂用什么仪器检测,GC-MS可以吗?液相是否也可以?在线求达人回答
生命活动与蛋白质的动态变化密切相关, 很多情况下某些蛋白质是通过各种翻译后修饰来完成或改变其功能。在数量众多的蛋白质翻译后修饰中,蛋白质磷酸化修饰无疑是最重要的一类,它是指通过蛋白激酶(Protein kinase,PK)介导的酶促反应把磷酸基团从一个化合物转移到另一个化合物上的过程(Figure 1所示),是生物体内存在的一种普遍的调节方式。现今发现的所有人类蛋白质中超过30%可被磷酸化修饰,这一修饰在细胞信号的传递过程中占有极其重要的地位,与生命活动的许多过程都密切相关,对此的研究已经成为蛋白质科学的热点之一。 http://img.dxycdn.com/trademd/upload/userfiles/image/2012/09/1346918444_small.jpg磷酸化多肽(主要指肽链中的酪氨酸、丝氨酸和苏氨酸残基的侧链羟基被磷酸化生成酸式磷酸酯的修饰多肽)是研究蛋白质磷酸化过程的必不可少的工具,它可作为磷酸酶模型底物,或作为可产生抗磷酸化蛋白抗体的抗原,也可以在确定磷酸化蛋白的物理参数时作为参考化合物等。因此磷酸化多肽的合成在过去的几年中吸引了相当大的兴趣,目前已确定了较为成熟的合成路线,使磷酸化多肽的合成趋于常规。目前磷酸化多肽的合成主要有两个策略:后磷酸化法(Global phosphorylation)和单体法(Building block approach),如Figure 2所示。前者是在多肽序列合成结束后再在固相载体上对丝氨酸、苏氨酸或酪氨酸的侧链羟基进行磷酸化,可以在同一次合成中同时得到带有和不带有磷酸化位点的多肽;而后者则将适当保护的磷酸化氨基酸直接引入到多肽序列中,操作较前者更为简单,现已成为磷酸化多肽合成的首选策略。在采用单体法构建磷酸化多肽时,目前广泛采用的原料为侧链单苄基保护的氨基酸:Fmoc-AA(PO(OBzl)OH)-OH (AA = Ser, Thr or Tyr)。这类保护的磷酸化位点由于侧链磷酸化基团的离子化而产生较大的位阻效应,并且磷酸化位点的引入往往能促进肽链二级结构的形成,故而磷酸化位点及其后的氨基酸的引入会比较困难。这些问题在合成含有多个磷酸化位点的多肽时将会变得尤为严重,往往会使最终产物的组成非常复杂,难以进行纯化,甚至直接导致合成的失败。http://img.dxycdn.com/trademd/upload/userfiles/image/2012/09/1346918477_small.jpg一般来讲,增加投料量和延长反应时间都能促使连接反应趋于完全,但增加投料量无疑会提高合成成本,对于较昂贵的带有保护的磷酸化氨基酸更是这样,而延长反应时间则可能增加其它副反应发生的风险,故而在合成磷酸化多肽时,需要对氨基酸投料量、反应方法以及反应时长等进行优化调整以期达到更理想、更经济的合成效果。我们有针对性地对磷酸化多肽合成条件进行了探索和调整,采用最终的优化条件成功合成了含有多达六个磷酸化丝氨酸残基的多肽:FAM-Ahx-X(pS)XX(pS)X(pS)X(pS)XX(pS)X(pS)-NH2(客户肽,详细序列未给出;其氨基端标记FAM以进行荧光检测),经过RP-HPLC纯化后最终纯品的纯度高达95%(见Figure 3)。http://img.dxycdn.com/trademd/upload/userfiles/image/2012/09/1346918493_small.jpg参考文献:1. P. Cohen, “The Role of Protein Phosphorylation in Neural and Hormonal Control of Cellular Activity”, Nature, 1982, 296 (5858): 613-620.2. From: http://en.wikipedia.org/wiki/Protein_kinase.3. L. A. Pinna, A. Donella-Deana, “Phosphorylated Synthetic Peptides as Tools for Studying Protein Phosphatases”, Biochim. Biophys. Acta., 1994, 1222 (3): 415-431.4. W. C. Chan, P. D. White, “Fmoc Solid Phase Peptide Synthesis-A Practical Approach” (2000), Oxford University Press.
各位大侠,请问石墨炉测定Ca元素时,磷酸根与火焰法是一样的干扰吗?也会形成磷酸钙吗?谢谢啦![em0815]
如题:基体改进剂:氯化钯和磷酸二氢铵哪个比较好一点?磷酸二氢铵是生成铵盐,氯化钯基改原理是什么呢?有哪位高人知道能告知一下?
[font=SimSun, STSong, &]单体磷酸盐特性,复合磷酸盐如何用[/font]
锅炉水中的磷酸三钠怎么检测,请高手提供标准方法!谢谢