RT、硫酸鱼精蛋白注射液告急什么原因造成的???有知道的吗?
硫酸沉血样中的蛋白,浓度多大,加多少量?
“不同饱和度硫酸铵沉淀中的蛋白浓度测定结果表明血红蛋白主要集中于50%和60%饱和度的硫酸铵沉淀中,杂蛋白主要集中在10%~40%饱和度的硫酸铵沉淀中。”这是文献中的原话,我想知道怎么知道哪部分是杂蛋白呢?怎么分辨哪部分的沉淀是自己的目标蛋白,哪部分的沉淀是杂蛋白呀[img]https://simg.instrument.com.cn/bbs/images/default/em09509.gif[/img]
测定粗蛋白为什么要乘以硫酸铵的系数?
心血管手术的必用药-鱼精蛋白,其无机酸盐具有抗凝血作用。现在国内只有上海第一生化药业有限公司在生产,虽说海洋污染严重,捕捞量不够,但价格低,生产成本高很可能是重要原因。鱼精蛋白是一种碱性蛋白,主要在鱼类(如蛙鱼、蹲鱼、鲱鱼等)成熟精子细胞核中作为和DNA结合的核精蛋白存在。鱼精蛋白发现于1870年,到1940~1960年间,正式用作抗菌剂的研究才盛行起来。现在普遍用作心血管手术的抗凝血药。全国争抢鱼精蛋白 山东仅得30盒无奈暂停手术http://news.e23.cn/content/2011-09-11/2011091100220.html
各位老师,有没有试过大豆蛋白复合纤维在70%硫酸中能溶解吗?
测蛋白时,用盐酸标准溶液滴定好,还是选择硫酸标准溶液合理?
做粗蛋白的时候,做样品得出的含量突然均低于理论正常值四个点。采取过的处理方法是: 首先虽然所用的药品试剂都是曾经使用过的,但是仍然更换各类药品试剂, 其二怀疑是管路老化,所用更换了与加碱,蒸馏的管路 其三怀疑蒸汽不足,经过处理,蒸汽压力达到6个左右,同时压力有轻微的波动,原来正常情况下也有。 其四,仪器运行时观察,并无明显泄露,出蒸汽的管道高度离消化管的底部没有变化。经过这么处理以后,检测出的硫酸铵(消化和未消化)得出的值也低于(21.19±0.2)%。 所用请教各位大侠,指导指导,鄙人不胜感激!
奶粉蛋白质中乳清蛋白含量的测定 十二烷基硫酸钠-毛细管凝胶电泳法该标准还未正式发布
【中文名称】腐殖酸蛋白饲料【英文名称】humic acid-protein fodder【性状】 黑色固体。【用途】 用作饲料添加剂,促进禽畜生长,提高繁殖能力,减少疾病,助消化。【制备或来源】 将风化的煤粉碎后,用氢氧化钠综合提取,加尿素、硫酸铵等经混合、灭菌,然后,接种发酵、浓缩、干燥即得成品。【其他】 除含动物所需的蛋白质(≥48%)外,还含有动物生长激素。【生产单位】 黑龙江鹤岗市蛋白饲料厂
GB 5009.169-2016中,用乙酸锌和亚铁氰化钾沉淀蛋白,对于添加的量,会不会影响到牛磺酸的检测,同样,硫酸锌加入的量会不会影响泛酸
[font=宋体]中国食品药品检定研究院(以下简称“中检院”)对纤维蛋白原和硫酸氨基葡萄糖氯化钠标准物质原料项目进行公告,现诚邀符合项目要求的供应商报名参加。[/font][b][font=宋体]一、项目基本情况[/font][/b][font=宋体]项目名称:中检院纤维蛋白原和硫酸氨基葡萄糖氯化钠标准物质原料项目[/font][font=宋体]项目编号:ZFCG202300023[/font][font=宋体]采购需求:[/font][table][tr][td=1,1,30][b][font=宋体]序号[/font][/b][/td][td=1,1,79][b][font=宋体]品种名称[/font][/b][/td][td=1,1,64][b][font=宋体]采购数量[/font][/b][/td][td=1,1,95][b][font=宋体]预算金额(万元)[/font][/b][/td][td=1,1,221][b][font=宋体]技术要求[/font][/b][/td][td=1,1,108][b][font=宋体]供应商特殊资质要求[/font][/b][/td][/tr][tr][td=1,1,30][font=宋体]1[/font][/td][td=1,1,79][font=宋体]纤维蛋白原[/font][/td][td=1,1,64][font=宋体]8000[/font][font=宋体]支[/font][/td][td=1,1,95][font=宋体]52.8[/font][/td][td=1,1,221][align=left][font=宋体]标准试剂,应为牛血来源,应为白色安瓿冻干分装,凝固物含量应不低于50%。[/font][/align][/td][td=1,1,108][font=宋体]/[/font][/td][/tr][tr][td=1,1,30][font=宋体]2[/font][/td][td=1,1,79][font=宋体]硫酸氨基葡萄糖氯化钠[/font][/td][td=1,1,64][font=宋体]1000g[/font][/td][td=1,1,95][font=宋体]2.2[/font][/td][td=1,1,221][align=left][font=宋体]应符合硫酸氨基葡萄糖氯化钠质量标准规定,氯化钠为19.0%-22.0%,乙醇应不得超过0.5%,硫酸根应为16.3%-17.3%,干燥失重应小于0.5%,炽灼残渣应为23.5%-26.0%,纯度应大于99.0%,含量应不低于99.0%。[/font][/align][/td][td=1,1,108][font=宋体] [/font][font=宋体]应具有硫酸氨基葡萄糖氯化钠原料药生产许可或口服制剂批准文号[/font][/td][/tr][/table][font=宋体]提供技术资料要求:[/font][font=宋体]1[/font][font=宋体]、根据采购需求中“技术要求”提供品种检验报告,报告应包括要求所列明内容;[/font][font=宋体]2[/font][font=宋体]、具有特殊资质要求的品种,按要求提供相关资质证明文件;[/font][font=宋体]3[/font][font=宋体]、货期要求[b]:[/b]纤维蛋白原3个月[b];[/b]硫酸氨基葡萄糖氯化钠:现货。[/font][font=宋体]4[/font][font=宋体]、质保期要求标化合格后1年。[/font][b][font=宋体]二、供应商资格要求[/font][/b][font=宋体]1.[/font][font=宋体]具有独立承担民事责任的能力;[/font][font=宋体]2.[/font][font=宋体]具有良好的商业信誉和健全的财务会计制度;[/font][font=宋体]3.[/font][font=宋体]具有履行合同所必需的专业技术能力;[/font][font=宋体]4.[/font][font=宋体]有依法缴纳税收和社会保障资金的良好记录;[/font][font=宋体]5.[/font][font=宋体]参加政府采购活动前三年内,在经营活动中没有重大违法记录;[/font][font=宋体]6.[/font][font=宋体]资格审查时,通过“信用中国”网站、中国政府采购网、国家企业信用信息公示系统、天眼查、企查查网站等渠道查询供应商信用记录,经查询列入失信被执行人、重大税收违法案件当事人名单、政府采购严重违法失信行为记录名单、经营异常名录信息、严重违法失信企业名单(黑名单)信息的,经查询在经营活动中有重大违法记录的,截至本项目采购活动开始前三年内因违法经营受到刑事处罚或者责令停产停业、吊销许可证或者执照、较大数额罚款等行政处罚的,不得参加本项目;[/font][font=宋体]7.[/font][font=宋体]单位负责人为同一人或者存在控股、管理关系的不同单位,不得参加同一项目响应;[/font][font=宋体]8.[/font][font=宋体]本项目不接受联合体参加,禁止转包或分包;[/font][font=宋体]9.[/font][font=宋体]法律、行政法规规定的其他条件。[/font][b][font=宋体]三、报名及提交响应文件方式[/font][/b][font=宋体]1.[/font][font=宋体]本项目采取网上报名的方式,不设现场报名及其他形式的报名。[/font][font=宋体]符合项目要求的潜在供应商需填写完整报名表(附件1)发送至邮箱hqzc@nifdc.org.cn。(邮件命名:项目名称+报名单位名称)[/font][font=宋体]2.[/font][font=宋体]潜在供应商需提交真实有效的响应文件(具体内容见附件2)并盖章密封邮寄至中检院联系人处。[/font][font=宋体]3.[/font][font=宋体]报名和邮寄时间截止至2023年3月10日(北京时间)。[/font][b][font=宋体]四、供应商确定原则[/font][/b][font=宋体]本项目以单品种有效报价最低原则确定供应商。[/font][b][font=宋体]五、联系方式[/font][/b][font=宋体]采购单位:中国食品药品检定研究院[/font][font=宋体]地址:北京市大兴区生物医药产业基地华佗路31号院后勤政采部[/font][font=宋体]联系人: 王晓雅[/font][font=宋体]联系电话:010-53852853[/font][font=宋体]电子邮箱:hqzc@nifdc.org.cn [/font][font=宋体]附件:[/font][font=宋体]1.[/font][font=宋体]标准物质原料项目报名表[/font][font=宋体]2.[/font][font=宋体]供应商报名响应文件[/font][font=宋体][/font]
检测蛋白回收率为啥要用硫酸铵?因其含氮量接近乳粉含氮量?做空白时是用水代替样品还是其它物质?网上有说用对氨基苯磺酸或者蔗糖,能否解释原因?还有硫酸铵用分析纯的是否可以?干燥时温度有要求吗?问题比较多,感谢各位高手帮忙解答!
请问大家做蛋白时用什么做催化剂硒片还是用硫酸铜硫酸钾,还有用其他的吗用不同的催化剂消化时间和结果有差异吗还有硒片在哪买的到啊
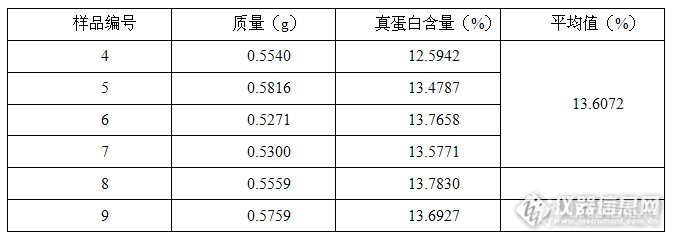
ps:在论坛上找了半天没找到适合这篇文章的地,暂且先放这吧。饲料中真蛋白的测定方法1.前言饲料作为畜牧养殖生产中的重要生产资料,其营养价值的高低直接影响到畜牧养殖的效益,而饲料中蛋白质的含量是一项重要的指标,饲料中粗蛋白质包括真蛋白质和非蛋白质两部分含氮物质,后者主要包括游离氨基酸、硝酸盐、铵盐等,故不能反映出饲料蛋白质对动物的真正营养价值。有些不法生产商故意添加硫酸铵、尿素等非蛋白质来提高产品的粗蛋白含量,导致部分养殖场户存在一个误区,认为标签上标注的粗蛋白质高,营养价值就高,从而造成养殖效益的低下。本文在凯氏定氮方法的基础上进行相应的前处理从而达到测定真蛋白的目的。蛋白质经沸水提取并在一定碱性条件下,能与硫酸铜发生盐析作用而析出沉淀,此沉淀物不溶于热水,而非蛋白氮则易溶于水,用热水洗沉淀,将水溶性含氮物洗去,剩下的沉淀物再用凯氏定氮法测定,得出真蛋白质的含量。2.实验部分2.1 仪器与试剂粉碎机、40目分样筛、分析天平(感量0.1mg)、烧杯250ml、玻璃棒、漏斗(直径10cm)、定性滤纸(中速,12.5cm,15cm)、可控温干燥箱、K1100F全自动凯氏定氮仪、SH420石墨消解炉、可控温电炉浓硫酸(98%)、硫酸铜(分析纯)、硫酸铜溶液(10%)、硫酸钾、氢氧化钠溶液(40%)、氢氧化钠溶液(2.5%)、硼酸(20g/L,按混合指示剂:硼酸=1:100加入指示剂)、甲基红-溴甲酚绿混合指示剂[font=Times New Roman
什么是粗蛋白, 粗蛋白跟蛋白质又有什么区别,如何测量饲料中粗蛋白的含量,粗蛋白的含量高是不是一定代表着蛋白质的含量高。我想,当你看到这个题目时,肯定会联想到这一连串的问题中的其中几个。那么接下来,我就来详细介绍下粗蛋白的概念、粗蛋白测量和其他关于饲料中粗蛋白含量的问题。粗蛋白概念:粗蛋白不仅包括蛋白质这一物质,它涵盖的范围更广,包括含氮的全部物质。粗蛋白含量:下面我介绍几种常见物质的粗蛋白含量,仅供大家参考。薏苡仁 粗蛋白含量:13%-14%棉粕 粗蛋白含量:可达40%以上农大白早糯玉米 粗蛋白含量:3.41%蠡玉168 粗蛋白含量:9.63%台湾大青枣 粗蛋白含量:0.86%上文介绍了几种农产品或水果的粗蛋白含量情况,如果需要更多的资料,大家可自己查阅。粗蛋白测定:方法一:最简便也是最快键的方法,就是用蛋白质测定仪(参见www.top17.net/product/993.html)来测量。本标准参照采用ISO 5983—1979 《动物饲料──氮含量的测定和粗蛋白含量计算》。 1 主题内容与适用范围 本标准规定了饲料中粗蛋白含量的测定方法。 本标准适用于配合饲料、浓缩饲料和单一饲料。2 引用标准 GB 601 化学试剂 滴定分析(容量分析)用标准溶液的制备3 原理 凯氏法测定试样中的含氮量,即在催化剂作用下,用硫酸破坏有机物,使含氮物转化成硫酸铵。加入强碱进行蒸馏使氨逸出,用硼酸吸收后,再用酸滴定,测出氮含量,将结果乘以换算系数6.25,计算出粗蛋白含量。4 试剂4.1 硫酸(GB 625):化学纯,含量为98%,无氮。4.2 混合催化剂:0.4g硫酸铜,5个结晶水(GB 665),6g硫酸钾(HG 3—920)或硫酸钠(HG 3—908),均为化学纯,磨碎混匀。4.3 氢氧化钠(GB 629):化学纯,40%水溶液(m/V)。4.4 硼酸(GB 628):化学纯,2%水溶液(m/V)。4.5 混合指示剂:甲基红(HG 3—958)0.1%乙醇溶液,溴甲酚绿(HG 3—1220)0.5%乙醇溶液,两溶液等体积混合,在阴凉处保存期为三个月。4.6 盐酸标准溶液:邻苯二甲酸氢钾法标定,按GB 601制备。4.6.1 盐酸标准溶液:c(HCl)=0.1mol/L。8.3mL盐酸(GB 622,分析纯),注入 1 000mL蒸馏水中。4.6.2 盐酸标准溶液:c(HCl)=0.02mol/L。1.67mL盐酸(GB 622,分析纯),注入1 000mL蒸馏水中。4.7 蔗糖(HG 3—1001):分析纯。4.8 硫酸铵(GB 1396):分析纯,干燥。4.9 硼酸吸收液:1%硼酸水溶液1 000mL,加入0.1%溴甲酚绿乙醇溶液10mL,0.1%甲基红乙醇溶液7mL,4%氢氧化钠水溶液0.5mL,混合,置阴凉处保存期为一个月(全自动程序用)。5 仪器设备5.1 实验室用样品粉碎机或研钵。5.2 分样筛:孔径0.45mm(40目)。5.3 分析天平:感量0.0001g。5.4 消煮炉或电炉。5.5 滴定管:酸式,10、25mL。5.6 凯氏烧瓶:250mL。5.7 凯氏蒸馏装置:常量直接蒸馏式或半微量水蒸气蒸馏式。5.8 锥形瓶:150、250mL。5.9 容量瓶:100mL。5.10 消煮管:250mL。5.11 定氮仪:以凯氏原理制造的各类型半自动,全自动蛋白质测定仪。6 试样的选取和制备 选取具有代表性的试样用四分法缩减至200g,粉碎后全部通过40目筛,装于密封容器中,防止试样成分的变化。7 分析步骤7.1 仲裁法7.1.1 试样的消煮 称取试样0.5~1g(含氮量5~80mg)准确至0.0002g,放入凯氏烧瓶(5.6)中,加入6.4g混合催化剂(4.2),与试样混合均匀,再加入12mL硫酸(4.1)和2粒玻璃珠,将 凯氏烧瓶(5.6)置于电炉(5.4)上加热,开始小火,待样品焦化,泡沫消失后,再加强火力 (360~410℃)直至呈透明的蓝绿色,然后再继续加热,至少2h。7.1.2 氨的蒸馏(蒸馏步骤的检验见附录A)7.1.2.1 常量蒸馏法 将试样消煮液(7.1.1)冷却,加入60~100mL蒸馏水,摇匀,冷却。将蒸馏装置(5.7)的冷凝管末端浸入装有25mL硼酸(4.4)吸收液和2滴混合指示剂(4.5)的锥形瓶内。然后小心地向凯氏烧瓶(5.6)中加入50mL氢氧化钠溶液(4.3),轻轻摇动凯氏烧瓶(5.6),使溶液混匀后再加热蒸馏,直至流出液体积为100mL。降下锥形瓶,使冷凝管末端离开液面,继续蒸馏1~2min,并用蒸馏水冲洗冷凝管末端,洗液均需流入锥形瓶内,然后停止蒸馏。7.1.2.2 半微量蒸馏法 将试样消煮液(7.1.1)冷却,加入20mL蒸馏水,转入100mL容量瓶中,冷却后用水稀释至刻度,摇匀,做为试样分解液。将半微量蒸馏装置(5.7)的冷凝管末端浸入装有20mL硼酸(4.4)吸收液和2滴混合指示剂(4.5)的锥形瓶(5.8)内。蒸汽发生器 (5.7)的水中应加入甲基红指示剂数滴,硫酸数滴,在蒸馏过程中保持此液为橙红色,否则需补加硫酸。准确移取试样分解液10~20mL注入蒸馏装置(5.7)的反应室中,用少量蒸馏水冲洗进样入口,塞好入口玻璃塞,再加10mL氢氧化钠溶液(4.3),小心提起玻璃塞使之流入反应室,将玻璃塞塞好,且在入口处加水密封,防止漏气。蒸馏4min降下锥形瓶(5.8)使冷凝管末端离开吸收液面,再蒸馏1min,用蒸馏水冲洗冷凝管末端,洗液均流入锥形瓶内,然后停止蒸馏。 注:7.1.2.1和7.1.2.2蒸馏法测定结果相近,可任选一种。7.1.2.3 蒸馏步骤的检验 精确称取0.2g硫酸铵(4.8),代替试样,按7.1.2或7.2.2步骤进行操作,测得硫酸铵含氮量为21.19±0.2%,否则应检查加碱、蒸馏和滴定各步骤是否正确。 7.1.3 滴定 用7.1.2.1或7.1.2.2法蒸馏后的吸收液立即用0.1mol/L(4.6.1)或0.02mol/L(4.6.2)盐酸标准溶液滴定,溶液由蓝绿色变成灰红色为终点。7.2 推荐法7.2.1 试样的消煮 称取0.5~1g试样(含氮量5~80mg)准确至0.0002g,放入消化管中,加2片消化片(仪器自备)或6.4g混合催化剂(4.2),12mL硫酸(4.1),于420 ℃下在消煮炉上消化1h。取出放凉后加入30mL蒸馏水。7.2.2 氨的蒸馏 采用全自动定氮仪(5.11)时,按仪器本身常量程序进行测定。 采用半自动定氮仪(5.11)时,将带消化液的管子插在蒸馏装置上,以25mL硼酸(4.4)为吸收液,加入2滴混合指示剂(4.5),蒸馏装置(5.7)的冷凝管末端要浸入装有吸收液的锥形瓶内,然后向消煮管中加入50mL氢氧化钠溶液(4.3)进行蒸馏。蒸馏时间以吸收液体积达到100mL时为宜。降下锥形瓶,用蒸馏水冲洗冷凝管末端,洗液均需流入锥形瓶内。7.2.3 滴定 用0.1mol/L的标准盐酸溶液(4.6.1)滴定吸收液,溶液由蓝绿色变成灰红色为终点。8 空白测定 称取蔗糖0.5g,代替试样,按第7章进行空白测定,消耗0.1mol/L盐酸标准溶液(4.6.1)的体积不得超过0.2mL。消耗0.02mol/L盐酸标准溶液(4.6.2)体积不得超过0.3mL。9 分析结果的表述9.1 计算见下式:粗蛋白质(%)=(V2-V1)• c×0.0140×6.25/(m×V'/V) ×100 式中:V2── 滴定试样时所需标准酸溶液体积,mL; V1── 滴定空白时所需标准酸溶液体积,mL; c── 盐酸标准溶液浓度,mol/L; m── 试样质量,g; V── 试样分解液总体积,mL; V── 试样分解液蒸馏用体积,mL; 0.0140── 与1.00mL盐酸标准溶液〔c(HCl)=1.000mol/L〕相当的、以克表示的氮的质量。 6.25── 氮换算成蛋白质的平均系数。 9.2 重复性 每个试样取两个平行样进行测定,以其算术平均值为结果。 当粗蛋白质含量在25%以上时,允许相对偏差为1%。 当粗蛋白含量在10%~25%之间时,允许相对偏差为2%。 当粗蛋白质含量在10%以下时,允许相对偏差为3%。
本文引用自cheney《蛋白胨和胰蛋白胨简介》蛋白胨是将肉、酪素或明胶用酸或蛋白酶水解后干燥而成的外观呈淡黄色的粉剂,具有肉香的特殊气息。蛋白质经酸、碱或蛋白酶分解后也可形成蛋白胨。蛋白胨富含有机氮化合物,也含有一些维生素和糖类。它可以作为微生物培养基的主要原料,在抗生素、医药工业、发酵工业、生化制品及微生物学科研等领域中的用量均很大。不同的生物体需要特定的氨基酸和多肽,因此存在着各种蛋白胨,一般来说,用于蛋白胨生产的蛋白包括动物蛋白(酪蛋白、肉类)和植物蛋白(豆类)等两种。能为微生物提供C源、N源、生长因子等营养物质。因此,蛋白胨从来源上可分为动物性蛋白胨和植物性蛋白胨。胰胨、肉胨、骨胨等都是动物性蛋白胨,而大豆蛋白胨等则是植物性蛋白胨。动物性来源的蛋白胨还有:蚕蛹蛋白胨、血液蛋白胨等。 不同来源的蛋白质和不同的水解条件,其水解物中组成可千差万别。所以胨往往是一个复杂的多肽混合物。可溶于水,过热不凝固,在饱和硫酸铵中不发生沉淀但可为蛋白质沉淀剂所沉淀。可用作微生物和动物细胞培养基、特种功能性食品和化妆品的配料,也有用作啤酒等产品的稳定剂。胰蛋白胨,又称胰酪蛋白胨(Casein Tryptone)、胰酶消化酪蛋白胨(Pancreatic digest of casein),是一种优质蛋白胨,是以新鲜牛肉和牛骨经胰酶消化,浓缩干燥而成的浅黄色粉末。具有色浅、易溶、透明、无沉淀等良好的物理性状。含有丰富的氮源、氨基酸等,可配制各种微生物培养基,用于细菌的培养、分离、增殖、鉴定,以及无菌试验培养基、厌氧菌培养基等细菌生化特性试验用培养基的配置。胰蛋白胨还广泛应用于高品质的抗生素、维生素、医药工业,氨基酸、有机酸、酶制剂、黄原胶等发酵工业,生化制品及微生物学科研等领域中的用量均很大,临床用于抗炎消肿,工业上用于皮革制造,生丝处理,食品加工。在国际市场上,胰蛋白胨也属于货紧价昂的短线品种之一。 胰酪蛋白胨质量标准及其检验标准: 常规各项理化指标: 1. 澄清度(磷酸盐、碱性沉淀):无沉淀、澄清 2. 2%水溶液:透明 3. 酸碱度:6-7 4. 氨基氮:≥3% 5. 色氨酸:≥0.8% 6. 胨含量:≥80% 7. 总氮:≥13% 8. 水份:≤5% 9. 灰份:≤6% 10. 氯化钠:≤0.2%胰蛋白胨特指用胰蛋白酶酶解酪蛋白生成的蛋白胨产物,与一般蛋白胨的区别在于酶解工艺处理上,属于水解度更高、胨分子量更小更均衡的蛋白胨。
蛋白沉淀剂的选用有什么资料可看吗?我最近在选择沉淀血清的物质:硫酸锌还是高氯酸?使用的是反相。10%硫酸锌会不会产生堵柱的可能?高氯酸会不会因为它的酸度过高也对柱子有影响?谢谢!
蛋白多肽多肽:多肽是α-氨基酸以肽键连接在一起而形成的化合物,是蛋白质水解的中间产物。由两个氨基酸分子脱水缩合而成的化合物叫做二肽,同理类推还有三肽、四肽、五肽等。通常由10~100氨基酸分子脱水缩合而成的化合物叫多肽,它们的分子量低于10,000Da(Dalton,道尔顿),能透过半透膜,不被三氯乙酸及硫酸铵所沉淀。也有文献把由2~10个氨基酸组成的肽称为寡肽(小分子肽);10~50个氨基酸组成的肽称为多肽;由50个以上的氨基酸组成的肽就称为蛋白质。蛋白质:生物体中广泛存在的一类生物大分子,由核酸编码的α氨基酸之间通过α氨基和α羧基形成的肽键连接而成的肽链,经翻译后加工而生成的具有特定立体结构的、有活性的大分子。是α—氨基酸按一定顺序结合形成一条多肽链,再由一条或一条以上的多肽链按照其特定方式结合合而成的高分子化合物。蛋白偶联KLH/BSA/Ovalbumin etc 偶联小肽/半抗原必须耦合到载体蛋白(KLH,BSA,Ova),才可以获得高效的抗体。一般来说,多肽可以与蛋白偶联的条件如下:1 有一个自由的氨基或羧基2 半胱氨酸上的-SH也可以与载体蛋白偶联目前我公司提供高质量的偶联载体蛋白(KLH,BSA,OVA)[img=,690,300]https://ng1.17img.cn/bbsfiles/images/2019/02/201902191022256586_4193_3531468_3.jpg!w690x300.jpg[/img]我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。请移步百度搜“[b]合肥国肽生物[/b]”即可
[color=#555555]各位好,请教各位一个问题,希望得到指点哈!最近做手工蛋白结果总是偏低,不知道为啥?[/color][color=#555555]方法:称取0.2g 硫酸铜和6.0g硫酸钾,加入5.0g含乳蛋白饮料。先消化3.5h,然后冷却,加一级水冲洗,看有无黑色颗粒,一般也没有,然后再消化0.5到1.0h,消化好后,再次用一级水冲洗,冷却后蒸馏。蒸馏前会用纯水将蒸馏系统清洗两次,样品蒸馏5分钟后滴定,滴定用0.1的硫酸标准溶液,最后滴成灰红色,结果连续做几次,我做的结果都比别人的低,不知道是哪里操作错误。[/color]
维纶基牛奶蛋白纤维和维纶基大豆蛋白纤维定性分析的研究维纶基大豆蛋白纤维是迄今为止我国获得的唯一完全知识产权的纤维发明,在纺织行业得到了快递的发展,广泛的应用,但与维纶基大豆蛋白纤维一样由我国企业自主研发的维纶基牛奶蛋白纤维也申请到专利好几年了,但迟迟没有相关标准的出台,使这一我国自主研发的新型纤维得不到有效利用新型纤维的不断推出,为我们提供了更多的纤维原料,但同时由于国家标准的相对滞后,给检测工作者带来了很大的难题,下面就目前市场上两种新型蛋白复合纤维给予试验,进行定性分析。主要原理是在观察了维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维显微结构和燃烧性状后,研究两者在常用化学试剂中的溶解性。试验结果表明,维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维在88%甲酸和浓硝酸中都能够部分溶解;在沸腾水浴中,维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维能够完全溶解于75%硫酸和98%硫酸牛奶蛋白纤维是再生蛋白质纤维,是以牛奶为原料经脱水、脱脂、分离、纯化、浓缩制成牛奶酪蛋白,与高分子化合物共混、共聚制成纺丝液,再经湿法纺丝而成;牛奶酪蛋白与聚乙烯醇制得的纤维称为维纶基牛奶蛋白纤维;牛奶酪蛋白与纤维素共聚制得粘胶基牛奶蛋白纤维。牛奶蛋白纤维含有多种氨基酸,具有良好的亲肤性和吸湿导湿性,抗菌防蛀,服用性强,受到消费者的青睐。维纶基牛奶蛋白纤维呈浅黄色,是由牛奶酪蛋白和聚乙烯醇大分子共混、共聚、醛化、揉和、脱泡,湿法纺成的纤维,克服了合成纤维吸湿性差和天然纤维强度低的不足,其比电阻介于天然纤维和合成纤维之间,吸湿性也优于聚乙烯醇纤维,在直接染料、弱酸性染料、活性染料和中性染料中都有良好的上染能力。本文在观察维纶基牛奶蛋白纤维和维纶基大豆蛋白纤维显微结构和燃烧性状后,研究两者在常用化学试剂中的溶解性,为纤维检测提供参数。大豆蛋白纤维属于再生植物蛋白纤维类,是以榨过油的大豆豆粕为原料,利用生物工程技术,提取出豆粕中的球蛋白,通过添加功能性助剂,与腈基、羟基等高聚物接枝、共聚、共混,制成一定浓度的蛋白质纺丝液,改变蛋白质空间结构,经湿法纺丝而成. 其有着羊绒般的柔软手感,蚕丝般的柔和光泽,棉的保暖性和良好的亲肤性等优良性能,还有明显的抑菌功能,被誉为“新世纪的健康舒适纤维”。大豆纤维是以脱去油脂的大豆豆粕作原料,提取植物球蛋白经合成后制成的新型再生植物蛋白纤维,是由我国纺织科技工作者自主开发,并在国际上率先实现了工业化生产的高新技术,也是迄今为止我国获得的唯一完全知识产权的纤维发明。1 试验1. 1试验材料、仪器和试剂纤维细度成分显微分析仪,万分之一电子天平;SHA-C水浴振荡器;鼓风恒温烘箱; 索氏萃取器;酒精灯;具塞三角瓶若干。甲酸(88%);硫酸(75%);浓硫酸(98%);浓硝酸;1MOL/L次氯酸钠溶液;石油醚(馏程为40℃~60℃)。1.2试验方法显微结构试验:用纤维细度成分显微分析仪观察纤维的显微结构。 以下试验维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维同一方法分别做一次燃烧性状试验:点燃酒精灯,用镊子夹取10mg左右纤维束,徐徐靠近火焰,观察试样对热的反应情况。将纤维移入火焰,观察纤维的燃烧情况;然后离开火焰,观察纤维的燃烧情况,并用鼻子闻试样燃烧刚熄灭的气味。最后,待试样熄灭冷却,观察残留物灰分的状态。预处理:取纤维5g左右,用定量滤纸包好,置于索氏萃取器中,用石油醚萃取1h,每小时至少循环6次,待试样中的石油醚挥发后,把试样浸入冷水中浸泡1h,再在(65±5)℃的水中浸泡1h,浸泡过程中时时搅拌。水(mL)与试样(g)之比为100:1。然后抽吸脱水,晾干。溶解性试验:准确称取试样1g置于具塞三角瓶中,加入100mL化学试剂,在搅拌条件下观察不同温度下纤维和试剂随时间的变化情况。待一定时间后,洗涤,抽吸排液,烘干。2 试验结果2.1显微结构在显微镜下观察维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维的横截面呈腰圆形或哑铃形,纵向有沟槽,两种纤维在显微镜下几乎无差别,无法区分这两种纤维。2.2燃烧性状维纶基牛奶蛋白纤维与维纶基大豆蛋白纤维靠近火焰时现象都是熔融并卷曲;进入火焰,熔融、卷曲并燃烧;离开火焰,燃烧,有时会自然熄灭。燃烧过程中散发出蛋白质燃烧时所特有的臭味。纤维燃烧的一端形成黑褐色硬块。两种纤维在燃烧情况下,火焰颜色,气味几乎无差别,无法区分这两种纤维。2.3溶解性取维纶基牛奶蛋白纤维与和维纶基大豆蛋白纤维分别置于88%甲酸、75%硫酸、浓硫酸、浓硝酸和1MOL/L次氯酸钠溶液中进行溶解性试验, 品名/溶液88%甲酸[/ali
以水解液中氨基态氮、可溶性蛋白及可溶性固形物含量为指标,研究13 种常用食品添加剂对罗非鱼蛋白自溶作用的影响。结果表明:在葡萄糖≤ 2.00%、苯甲酸钠≤ 0.02%、亚硫酸钠≤ 0.03%、氯化钠≤ 10%、柠檬酸≤ 0.10% 的添加量范围内,对罗非鱼蛋白自溶有一定的促进作用,超过该范围则显示抑制作用;氯化钙、抗坏血酸则对蛋白自溶具有较好的促进作用;乳酸≥ 1.00%、酒石酸≥ 0.10% 、乙二胺四乙酸二钠(EDTA-2Na)≥ 0.02%的添加量对罗非鱼蛋白自溶有一定的抑制作用;氯化钾、硫酸镁、氯化镁对罗非鱼蛋白自溶无明显作用。添加苯甲酸钠、柠檬酸、乳酸及酒石酸可使罗非鱼蛋白水解液腥味减少,并减缓其腐败变质。
牛奶中蛋白检验本方法适用于公司所有原辅料、半成品及成品蛋白质的检验1. 仪器:分析天平,消煮炉,FOSS公司-凯氏定氮仪。2. 试剂:硫酸(化学纯),混合催化剂,NaOH(化学纯),硼酸(化学纯),混合指示剂,盐酸标准溶液。3. 操作步骤:3.1试样的消煮:称取试样3g(准确至0.0002g),放入消化管中,加两片消化片、12mL硫酸于250℃的消化炉上消化1小时,420℃再消化1小时,取出放凉后加入30mL蒸馏水,放入凯氏定氮仪中。设定加入硼酸吸收液25mL,NaOH50mL,在吸收液中加5滴混合指示剂(先作两个空白样以清洗)开始蒸馏,蒸馏时间4分钟为宜,用0.1mol∕L的盐酸标准溶液滴定吸收液,溶液由蓝绿色变为灰红色为滴定终点。3.2空白样测定:除不加试样外,其他操作步骤同上。3.3计算: 蛋白质(%)=v×c×0.0140×6.25×100mV——滴定试样时所需标准盐酸溶液体积(mL)C——盐酸溶液浓度(mol∕L)M——试样质量(g)0.0140——每毫克当量氮的克数(g)6.25—氮换算成蛋白质的平均系数
饲料粗蛋白的快速测定1 实验意义 饲料是畜牧养殖生产中的重要生产资料,饲料中蛋白质含量是判定饲料营养价值的一项重要指标,对饲料质量进行监管检测十分必要。本文开发了饲料粗蛋白的快速测定方法,比常用的国标法、凯氏定氮法以及强碱蒸馏法更加方便、快捷。采用双氧水—硫酸法是消解饲料样品,减少了消化时间。在我公司饲料快速检测仪特定波长下进行比色测定,根据溶液吸光度(颜色深度)与浓度呈正比关系,转换出粗蛋白含量,,无需滴定,适合实际检测使用。2 测定原理 浓硫酸和30%浓度的双氧水都是强氧化剂。饲料中的有机物接触到浓硫酸便会被脱水炭化,但是在高温条件下,往未被硫酸氧化完全的饲料中加入30%的双氧水,会使饲料中的有机物彻底氧化、分解,放出CO2、SO2,而释放出的氨气则和硫酸结合生成硫酸铵。NH-4+-N在碱性条件下与纳氏试剂络合生成黄色络合物,在特定波长下进行比色测定,氮含量和溶液吸光度(颜色深度)呈线性关系。3 操作步骤 取样品0.2±0.0002g于100ml三角瓶中,后各加入2ml浓硫酸摇匀,管口放一只弯颈小漏斗,三角瓶内放3-4颗玻璃珠,放在电炉上加热,使瓶内液体保持微沸,硫酸大量冒烟,消化液呈酱油色时,将三角瓶取下冷却至不烫手,向管内加入30%双氧水30-40滴,加热消化。反复多次,直至管内溶液澄清透明为止。消化结束后冷却,分别过滤转移至100ml容量瓶中,加水定容至刻度。再各从中吸取2ml定容至另一100ml容量瓶,为待测液。显色后测定吸光度。4 回收率试验 用该方法进行了添加实验和测试结果与常规的比对试验,结果表明,方法回收率在90%—110%之间,与常规测试结果绝对差值符合《GB/T18823-2002饲料检测结果判定的允许误差》标准要求,有关的数据如下:4.1 样品添加实验数据: 样品量mg添加量mg添加后mg回收率%4.4510.4615.76108.134.3310.8015.68105.097.5511.4418.9699.747.21 11.1918.1797.9411.83 11.4423.2599.9111.6311.4423.0699.914.2 速测结果与常规测试结果比对数据: 测试方法样品1样品2样品3速测法蛋白含量41.2%40.5%47.3%常规法蛋白含量40%41%46%绝对误差(%)1.20.51.35 结论 [size=
如何避免粗蛋白平行样误差大问题。硫酸铵回收正常
含有一对或多对二硫键修饰的多肽:二硫键在蛋白质的结构稳定中起到重要作用,目前我们国肽生物已经能够为客户提供四对二硫键修饰的多肽。多对二硫键成环技术蛋白质和多肽类药物具有作用位点专一,疗效明确等优点,近年来,蛋白质和多肽类药物的研究和发展已经成为生物医药领域研究的一个热点。二硫键在维持多肽和蛋白质的空间立体结构及由此决定的生物活性中发挥着重要的作用。二硫键即为蛋白质或多肽分子中两个不同位点Cys的巯基(-SH)被氧化形成的S-S共价键。一条肽链上不同位置的氨基酸之间形成的二硫键,可以将肽链折叠成特定的空间结构。[align=center][img=,526,200]https://ng1.17img.cn/bbsfiles/images/2019/04/201904300953261874_7512_3531468_3.jpg!w526x200.jpg[/img][/align]多肽分子通常分子量较大,空间结构复杂,结构中形成二硫键时要求两个半胱氨酸在空间距离上接近。此外,多肽结构中还原态的巯基化学性质活泼,容易发生其他的副反应,而且肽链上其他侧链也可能会发生一系列修饰,因此,肽链进行修饰所选取的氧化剂和氧化条件是反应的关键因素,反应机理也比较复杂,既可能是自由基反应,也可能是离子反应。多肽的二硫键修饰中,分子内或者分子间一对二硫键的合成通常比较容易,反应条件有多种选择,比如空气氧化,DMSO氧化等温和的氧化过程,也可以采用H2O2,I2,汞盐等激烈的反应条件,反应产物也比较容易纯化分离,得到较高的纯度和产率。空气氧化法形成二硫键是多肽合成中最经典的方法,并且在早期的研究中取得了较好的结果。采用空气氧化法通常是将巯基处于还原态的多肽溶于水中,在近中性或弱碱性条件下(PH值6.5~10),反应24小时以上。为了降低分子之间二硫键形成的可能,该方法通常需要在低浓度条件下进行。碘氧化法在多肽合成中应用同样广泛,一般将多肽溶于25%的甲醇水溶液或30%的醋酸水溶液中,逐滴滴加10~15mol/L的碘进行氧化,反应15~40min。当肽链中含有对碘比较敏感的Tyr、Trp、Met和His的残基时,氧化条件要控制的更精确,氧化完后,立即加入维生素C或硫代硫酸钠除去过量的碘。当一条肽链上需要形成两对或两对以上的二硫键时,反应过程就变得相对复杂。在固相合成多肽之前,需要提前设计几对二硫键形成的顺序和方法路线,选择不同的侧链巯基保护基,利用其性质差异,分步氧化形成两对或多对二硫键。通常采用的巯基保护基有trt,Acm,Mmt,tBu,Bzl,Mob,Tmob等多种基团。我们分别列出两种以2-Cl树脂和Rink树脂为载体合成的多肽上多对二硫键形成路线:[align=center][img=,666,432]https://ng1.17img.cn/bbsfiles/images/2019/04/201904300953443844_9290_3531468_3.jpg!w666x432.jpg[/img][/align]二硫键的形成一直是多肽合成中的一个难点,经过不懈的研究和累积,我们公司已经具备相当成熟的多对二硫键成环技术,目前我们已经能够高成功率的合成三对和四对二硫键的多肽。不断克服实验困难,不停提高产品质量,不懈努力达到客户要求是我们国肽生物的不变宗旨。成功案例:固相合成序列DC*TSHNGAC*NHHSHC*C*SNVC*NTWAHLC*T,并对其成功进行3对二硫键修饰。HPLC分析:[align=center][img=,562,246]https://ng1.17img.cn/bbsfiles/images/2019/04/201904300954000045_2353_3531468_3.jpg!w562x246.jpg[/img][/align]MS分析:[align=center][img=,562,224]https://ng1.17img.cn/bbsfiles/images/2019/04/201904300954145791_912_3531468_3.jpg!w562x224.jpg[/img][/align][align=left]我们主要提供:多肽合成、定制多肽、同位素标记肽、人工胰岛素、磷酸肽、生物素标记肽、荧光标记肽(Cy3、Cy5、Fitc、AMC等)、目录肽、偶联蛋白(KLH、BSA、OVA等)、化妆品肽、多肽文库构建、抗体服务、糖肽、订书肽、药物肽、RGD环肽等。合肥国肽生物官网:http://www.bankpeptide.com欢迎咨询服务热线:17718122172;17718122684;17730030476;17718122397[/align]
正在做麸皮的蛋白测定,称样约0.2g,消化时硫酸用量是20ml,用的是半自动凯氏定氮仪,加的蒸馏水为50ml, 但不知道要加多少碱,和蒸馏时间设定多少呢?做了一个加碱70ml的,但蒸馏没有生成大量沉淀,溶液的颜色依然是蓝色的。还有就是硼酸的用量10ml可以吗?正在做麸皮的蛋白测定,称样约0.2g,消化时硫酸用量是20ml,用的是半自动凯氏定氮仪,加的蒸馏水为50ml, 但不知道要加多少碱,和蒸馏时间设定多少呢?做了一个加碱70ml的,但蒸馏没有生成大量沉淀,溶液的颜色依然是蓝色的。还有就是硼酸的用量10ml可以吗?
常用蛋白质沉淀剂的蛋白质沉淀效率 上清液PH 沉淀0。5ml血浆95%以上蛋白时所需沉淀剂体积/ml 三氯醋酸(0.1g/ml) 1.4~2.0 0.2 高氯酸 (0.06g/ml) 1.5 0.4 钨酸 2.2~3.9 0.6 焦磷酸(0.05g/ml) 1.6~2.7 0.4 硫酸铜-钨酸钠 5.7~7.3 1.0 氢氧化锌 6.5~7.5 1.5 硫酸铵 7.0~7.7 2.0 乙腈 8.5~9.5 1.0 丙酮 9~10 1.0 乙醇 9~10 1.5 甲醇 8.5~9.5 1.5
采用Agilent的zobrax SAX (强阴离子柱)4.6*150。蛋白样品:BSA 分子量约60kDa,pI=4.8。上样浓度1mg/ml,进样50ul,流速:0.8ml/min,280nm紫外检测。流动相 A 20mM,pH7磷酸钠buffer,B:A+1M NaCl。程序0~15min:100%A;15~45min:梯度B至100%;45~50min:100%B没有蛋白样品峰我尝试过pH6.5,6.0的buffer,也尝试过pH8.0的Tris-HClbuffer,B的洗脱盐尝试过1M硫酸铵。以上条件均无法洗脱出蛋白峰。直接0.5M NaOH再生柱子可以从柱子上洗脱出峰。离子交换一般用NaCl或者硫酸铵即可。很奇怪,BSA上样后没有洗脱峰,不知诸位版友有和建议?
1.蒸馏步骤的回收率,我们这里用硫酸铵做。请问:硫酸铵需要105度烘后干燥塔冷却,再称重吗?烘干结果能达到98.6%,不烘的结果能达到99.9%2.消化蒸馏全过程的回收率,我们开始用乙酰替苯胺+蔗糖做,方法上说是真空中80度烘干,可我们没有这种设备,在普通环境下烘干,结果偏差很大,只有91.2%。我们后来用甘氨酸(不经过烘干处理)+蔗糖做,能达到99.8%,但问题是和其他公司对标样品总是偏低。请问:我们后边的方法,甘氨酸是否需要烘干处理?有别的测蛋白回收率的方法吗?======================注:经验证,盐酸标准溶液浓度没有问题。