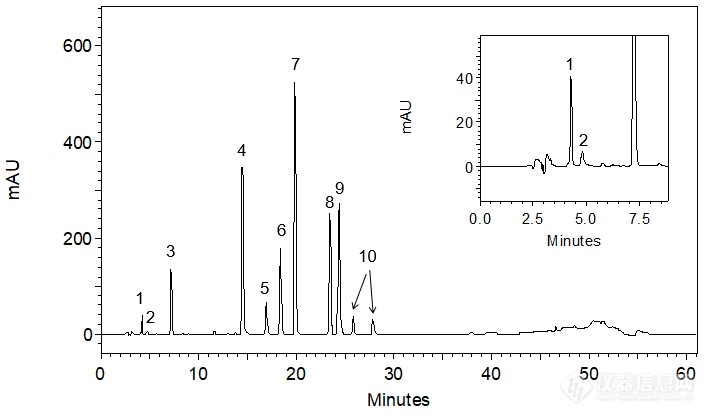
[align=center][b]头孢克洛有关物质——与9种杂质的共同分析[/b][/align]头孢克洛(cefaclor)为白色至微黄色粉末或结晶性粉末的化学品,微臭,本品在水中微溶,在甲醇、乙醇、三氯甲烷或二氯甲烷中几乎不溶,分子式:C15H14ClN3O4S。头孢克洛是β-内酰胺类抗生素,头孢菌素类药,是第二代头孢菌素,主要适用于敏感菌所致的急性咽炎、急性扁桃体炎、中耳炎、支气管炎、肺炎等呼吸道感染、皮肤软组织感染和尿路感染等。[align=center][img=,144,171]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140859582934_5220_2222981_3.gif!w144x171.jpg[/img][/align][align=center]头孢克洛[/align][align=center]M.W.: 367.81[/align]本实验对客户提供的头孢克洛原料药以及9种杂质(杂质A、B、C、D、E,7-ACCA,头孢克洛δ-3异构体,α-苯甘氨酸,苯甘氨酸甲酯盐酸盐)进行分析,希望得到杂质混合对照溶液及供试品溶液中各杂质的良好分离。客户反馈,将流动相磷酸盐体系的pH值由4.0提高到4.5可得到杂质混合对照溶液中7-ACCA和α-苯甘氨酸之间的良好分离,但头孢克洛与其相邻杂质E峰之间分离较难。客户前期使用了CAPCELL PAK C[sub]18 [/sub]MGII S3 4.6 mm i.d. × 250 mm色谱柱进行分析,在此基础上,我们尝试了其他填料的几款色谱柱进行分离尝试,分别为CAPCELL PAK C[sub]18[/sub] AQ(S3& S5)、CAPCELL PAK ADME(金刚烷基)、SUPERIOREX ODS、CAPCELL PAK PFP(五氟苯基)、CAPCELL PAK CN(氰基)。首先,参考客户提供的液相条件,使用高极性色谱柱[b]CAPCELL PAK C[sub]18 [/sub]AQ[/b]对杂质混合对照溶液进行分析尝试;为了得到杂质间的更好分离,粒径选择3 μm,如图1,[color=#2F5496]各杂质间均能得到良好的分离结果,头孢克洛与杂质[/color][color=#2F5496]E[/color][color=#2F5496]的分离度为[/color][color=#2F5496]2.70[/color][color=#2F5496],达到基线分离。[/color][color=#2F5496][/color][align=center][img=,690,405]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140902184290_9307_2222981_3.png!w690x405.jpg[/img][/align][align=center]图1 AQ S3 分析杂质混合对照溶液结果[/align][align=center] [/align][align=center]1.α-苯甘氨酸 2. 7-ACCA 3. 杂质A 4. 杂质B 5. 苯甘氨酸甲酯盐酸盐 6.杂质C[/align][align=center]7. 头孢克洛δ-3异构体 [color=#ff0000]8. 头孢克洛 9. 杂质E [/color]10.杂质D[/align][color=#2F5496][img=,555,311]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140902187828_2715_2222981_3.png!w555x311.jpg[/img][/color]进一步分析供试品溶液,如图2,由于样品浓度较高,导致头孢克洛主峰向后展宽,进而将杂质E包于其中。[color=#2F5496][/color][align=center][color=#2F5496][img=,659,441]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140915544228_5404_2222981_3.png!w659x441.jpg[/img][/color][/align][align=center]图2 AQ S3 分析供试品溶液结果[/align][align=center][/align][align=left]为使头孢克洛和杂质E之间得到更好的分离,我们尝试对色谱条件进行调整。[/align][align=left][/align][align=left][b]1.调整柱温[/b][/align][align=left][b][/b]首先对温度进行调整:实验过程中发现柱温对头孢克洛与杂质E的出峰行为有较大影响——当柱温设置为20 ℃时,头孢克洛和杂质E之间能够得到良好分离;将温度提高到30℃时,杂质E向前移动趋势较大。为使杂质E峰出在头孢克洛峰前,避免由于供试品中头孢克洛峰的展宽而使杂质E被包于其内,进一步将柱温提高到40℃,发现头孢克洛与杂质E峰重合;最终,将柱温提高到45℃,此时杂质E峰移至头孢克洛峰前,但未能得到理想的分离结果。[/align][align=left][/align][align=center][img=,659,430]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140916597550_373_2222981_3.png!w659x430.jpg[/img][/align][align=center]图3 不同柱温条件下AQ S3分析杂质混合对照溶液结果[/align][align=center][/align][align=left][b]2.调整流动相[/b][/align][align=left][b][/b][/align][align=left]考虑到提高柱温对色谱柱寿命的影响,仍选择初始使用的20℃,对流动相梯度条件进行调整。在增强整体保留时间的同时,发现[color=#538135]头孢克洛和杂质[/color][color=#538135]E[/color][color=#538135]的出峰顺序发生了颠倒[/color],且[color=#538135]分离良好[/color],进而有效避免了杂质E被包于头孢克洛主峰中的问题;而在主峰后出峰的杂质D与头孢克洛之间分离度亦较高,即使供试品溶液中的头孢克洛峰展宽,也不会出现将杂质D包于其中的问题。[/align][align=left]因此我们在此梯度条件下进一步对供试品溶液进行分析,如图4,头孢克洛与各杂质峰之间均能得到良好的分离结果。[/align][align=left][/align][align=center][img=,679,417]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140917450308_6331_2222981_3.png!w679x417.jpg[/img][/align][align=center]图4 AQ S3分析杂质混合对照溶液及供试品溶液结果(调整梯度)[/align][align=center] [/align][align=center]1.α-苯甘氨酸 2. 7-ACCA 3. 杂质A 4. 杂质B 5. 苯甘氨酸甲酯盐酸盐 6.杂质C[/align][align=center]7. 头孢克洛δ-3异构体 [color=#ff0000]8. 杂质E 9. 头孢克洛[/color] 10.杂质D[/align][align=left][img=,587,335]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140918136074_9375_2222981_3.png!w587x335.jpg[/img][/align][align=left][/align][align=left]为使客户有更多的色谱柱选择,本实验室也尝试使用键合金刚烷基的高极性色谱柱CAPCELL PAK ADME分析杂质混合对照溶液和供试品溶液,如图5,在分析杂质混合对照溶液时,能够得到各组分的良好分离,同时发现杂质E和头孢克洛出峰顺序发生颠倒,但同时也发现头孢克洛峰与其后相邻杂质D峰之间分离度较低(Rs=1.71);因此,如图6,在分析供试品溶液时,由于色谱峰向后展宽,使得杂质D被包于头孢克洛主峰中,未能得到理想分离结果。[/align][align=left][/align][align=center][img=,690,426]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140918484278_6616_2222981_3.png!w690x426.jpg[/img][/align][align=center]图5 ADME 分析杂质混合对照溶液结果[/align][align=center] [/align][align=center]1.α-苯甘氨酸 2. 7-ACCA 3. 杂质A 4. 杂质B 5. 苯甘氨酸甲酯盐酸盐 6.杂质C[/align][align=center]7. 头孢克洛δ-3异构体 [color=#ff0000]8. 杂质E 9. 头孢克洛[/color] 10.杂质D[/align][align=left][/align][align=center][img=,689,417]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140918485898_9906_2222981_3.png!w689x417.jpg[/img][/align][align=center]图6 ADME 分析杂质混合对照溶液结果[/align][align=left][img=,585,336]http://ng1.17img.cn/bbsfiles/images/2018/06/201806140919331328_5070_2222981_3.png!w585x336.jpg[/img][/align][align=left][/align][align=left][/align][align=left]之后,我们也尝试使用了CN(氰基柱)和PFP(五氟苯基)以及高碳载量的SUPERIOREX ODS色谱柱,在客户提供的色谱条件下对杂质混合对照溶液进行分析,均未能得到更理想的分离结果。[/align]
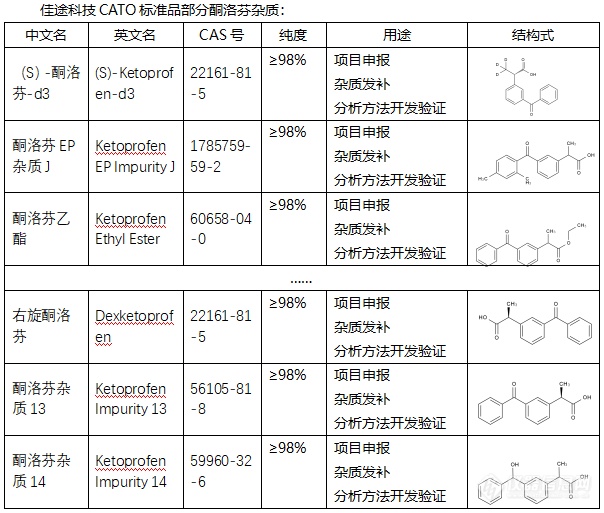
[font=宋体]◇关于酮洛芬杂质[/font][font=微软雅黑]酮洛芬杂质[/font][font=微软雅黑][color=#666666]是一种非甾体类抗炎[/color][/font][font=微软雅黑][color=#666666]杂质[/color][/font][font=微软雅黑][color=#666666],[/color][/font][font=微软雅黑][color=#666666]它的两个[/color][/font][font=微软雅黑][color=#666666]主要成分为对乙酰氨基酚、阿司匹林。[/color][/font][font=微软雅黑]酮洛芬杂质[/font][font=Helvetica][color=#333333]具有镇痛、消炎及解热作用[/color][/font][font=宋体][color=#333333],[/color][/font][font=微软雅黑][color=#666666]临床上主要用于缓解轻至中度疼痛以及发热等症[/color][/font][font=微软雅黑][color=#666666],[/color][/font][font=微软雅黑]酮洛芬杂质[/font][font=微软雅黑]的原理机制是[/font][font=微软雅黑][color=#666666]通过与体内前列腺素合成途径中的环氧合酶结合而起[/color][/font][font=微软雅黑][color=#666666]效果[/color][/font][font=微软雅黑][color=#666666],并且可以减少细胞内花生四烯酸转化为前列腺素的过程[/color][/font][font=微软雅黑][color=#666666]。[/color][/font][font=宋体][color=#333333]相比其他抗炎杂质,其不良反应更小[/color][/font][font=Helvetica][color=#333333]30%一90%[/color][/font][font=宋体][color=#333333]是以尿液[/color][/font][url=https://baike.baidu.com/item/%E8%91%A1%E8%90%84/0?fromModule=lemma_inlink][font=Helvetica][color=#136ec2]葡萄[/color][/font][/url][font=Helvetica][color=#333333]糖醛酸结合物形式[/color][/font][font=宋体][color=#333333][font=宋体]在[/font][font=Helvetica]24[/font][font=宋体]小时内排[/font][/color][/font][font=宋体][color=#333333]出。[/color][/font][font=宋体][font=Calibri]CATO[/font][font=宋体]标准品提供的酮洛芬杂质[/font][/font][font=宋体],[/font][font=宋体]对[/font][font=宋体][color=#333333]各种关节炎以及痛风有十分显著的效果。[/color][/font][img=,604,513]https://ng1.17img.cn/bbsfiles/images/2024/02/202402042137581297_3118_6381607_3.png!w604x513.jpg[/img]
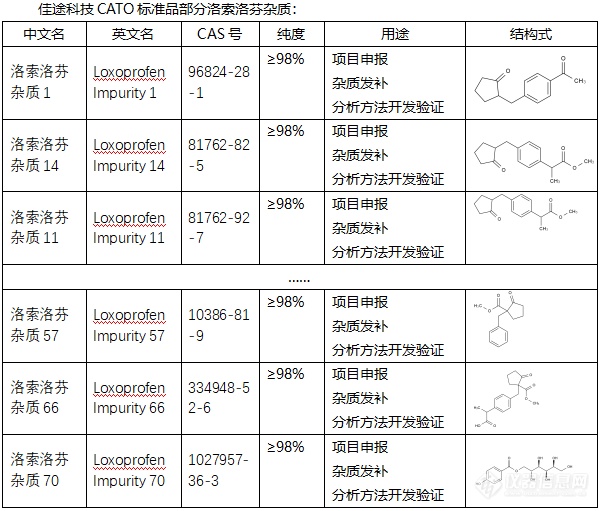
◇关于洛索洛芬杂质 洛索洛芬杂质是一种[font=Arial][color=#333333][font=宋体]非甾体抗炎[/font][/color][/font]杂质,具有镇痛、抗炎症以及解热作用。索洛芬钠杂质主要通过以下机制发挥药效:一、抑制环氧化酶:这种酶在炎症过程中起着重要作用,通过抑制它能够减少前列腺素的生成。二、[font=.pingfang sc]阻断前列腺素合成:洛索洛芬钠片通过作用于环氧合酶([/font]COX)的特定位置,阻止了前列腺素的合成,从而起到了抗炎和镇痛的效果。[font=UICTFontTextStyleBody] [/font][font=UICTFontTextStyleBody]CATO[/font]标准品提供的[font=宋体]洛索洛芬杂质[/font][font=宋体],有着广泛的作用,其中它的镇痛效果十分显著。[img=,601,511]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041058193581_5312_6381607_3.png!w601x511.jpg[/img][/font]
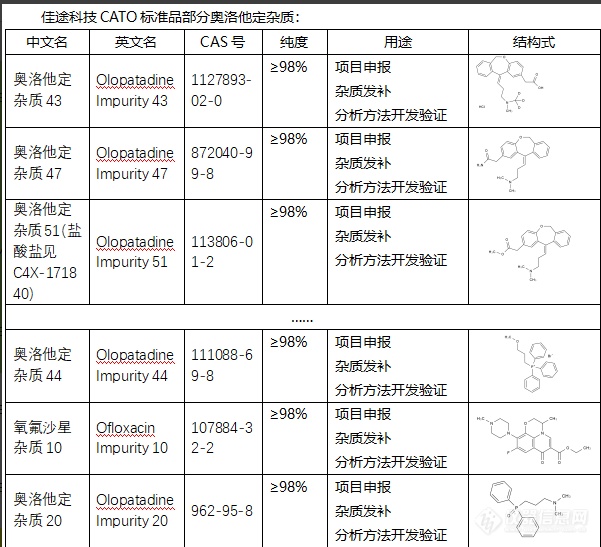
奥洛他定是一种用于治疗孤独症、精神分裂症和双相情感障碍的药物。在其生产过程中可能产生一些杂质。这些杂质可能源于原料、废弃的生产物或制造过程中的化学反应。过多的杂质可能会干扰药物的效力,引起不良反应,甚至影响患者的安全性。因此,对奥洛他定药品的杂质进行严格的检测和控制是非常重要的。制药公司必须遵循严格的质量控制程序,以保证药品的质量和安全性。CATO标准品对奥洛他定杂质进行研究和分析,可以为改善和优化制造过程,以及提高药品质量提供有价值的信息。通过了解含有哪些杂质,及其如何形成,制药厂商可以改进其生产过程,以减少杂质的产生,并提高药物的纯度和效力[img=,601,547]https://ng1.17img.cn/bbsfiles/images/2024/02/202402052109512474_2064_6381668_3.png!w601x547.jpg[/img]
工业生产中,采用甲醛与液氨反应,生成乌洛托品。再经结晶、离心机分离、干燥得到乌洛托品成品。已知甲醛会带入微量的甲酸及少量的甲醇,液氨中也有0.2%左右的油性杂质。成品中除了有小于0.5%的水份外,还含有什么杂质啊?
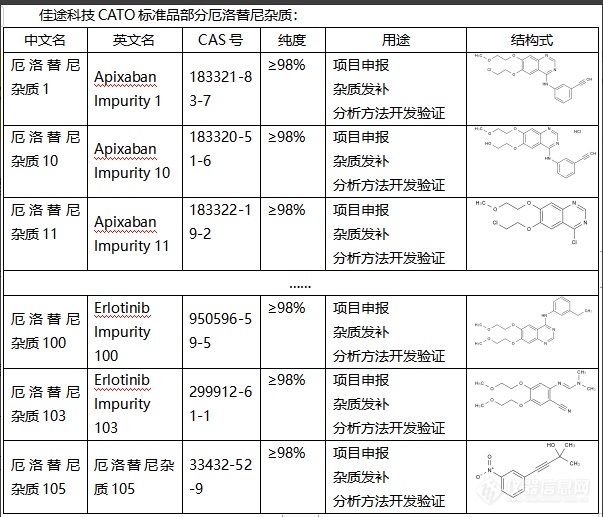
厄洛替尼杂质是药物制备过程中的副产品或污染物,可能会影响药物的安全性和有效性。常见的杂质有重金属、溶剂残留、有毒化合物等。对于厄洛替尼来说,杂质可能会影响其药效和安全性。一方面,杂质可能降低药物的纯度,从而降低其抑制肿瘤生长的效果。另一方面,某些杂质可能具有毒性或致敏性,可能导致患者出现不良反应。因此,对厄洛替尼的杂质进行检测和控制是药品质量控制的重要环节。这需要使用一种或多种分析方法,如高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法、[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法、质谱法等,以检测并定量药物中的杂质。CATO标准品针对可能的杂质源(如起始材料、反应条件、催化剂、溶剂等)进行控制,可以有效地减少杂质的生成。[img=,603,517]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021655361773_9862_6381668_3.png!w603x517.jpg[/img]
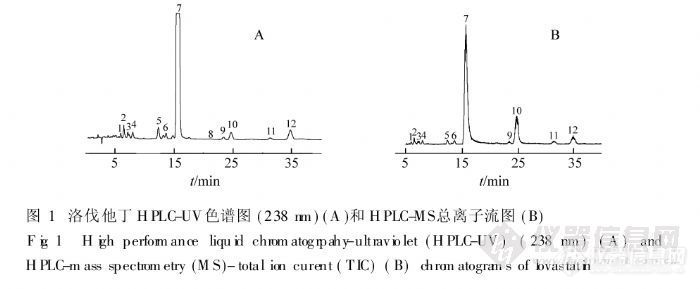
【作者】 吴永江; 朱炜; 邵青; 程翼宇;【Author】 Wu Yongjiang,Zhu Wei,Shao Qin,Cheng Yiyu~*(College of Pharmaceutical Sciences,Zhejiang University,Hangzhou 310031)【机构】 浙江大学药学院; 浙江大学药学院 杭州310031; 杭州310031;【摘要】 利用高效液相色谱-二极管阵列检测器-质谱联用方法对洛伐他丁及其杂质成分进行分离分析和结构鉴定。实验采用D iamonsil C18(5μm,4.6 mm×250 mm)为分离柱,乙腈-水(含0.1%乙酸)(65∶35)为流动相,分离并检测了洛伐他丁及其杂质;通过与DAD检测器和离子阱质谱联用,获得了它们的紫外光谱和质谱数据;紫外光谱表明除氢化洛伐他丁外其余杂质与洛伐他丁基本结构相同,利用MS和MS2数据确定了杂质的分子量和侧链结构,由此鉴定了其中10个杂质的结构。实验结果表明,高效液相色谱-二极管阵列检测器-质谱联用技术可以快速鉴定洛伐他丁中的杂质化学成分。 http://ng1.17img.cn/bbsfiles/images/2012/07/201207301723_380642_2379123_3.jpg
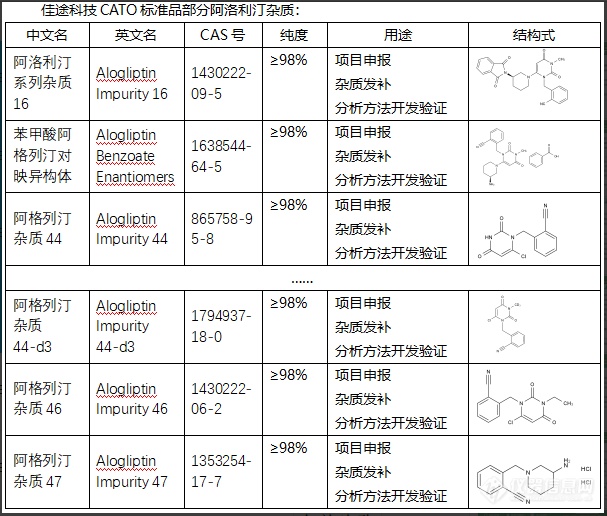
阿洛利汀杂质可以作为标准物质,用于评价阿洛利汀的质量和纯度。通过测量此类杂质的含量,可以对阿洛利汀的生产过程进行控制和优化,以制造出更优质的药物。此外,某些类型的杂质还可能被用作药物的标记物,以跟踪药物在体内的分布和代谢。CATO标准品目前的药品生产技术已经可以有效地降低杂质的含量,保证药品的质量和安全性。任何药物在上市之前,都需要经过严格的质量控制检测,以确保其杂质含量符合规定的标准。此外,药品在上市后也会进行定期的质量监控,以确保其安全性和效力。[img=,607,516]https://ng1.17img.cn/bbsfiles/images/2024/02/202402041447097355_1644_6381668_3.png!w607x516.jpg[/img]
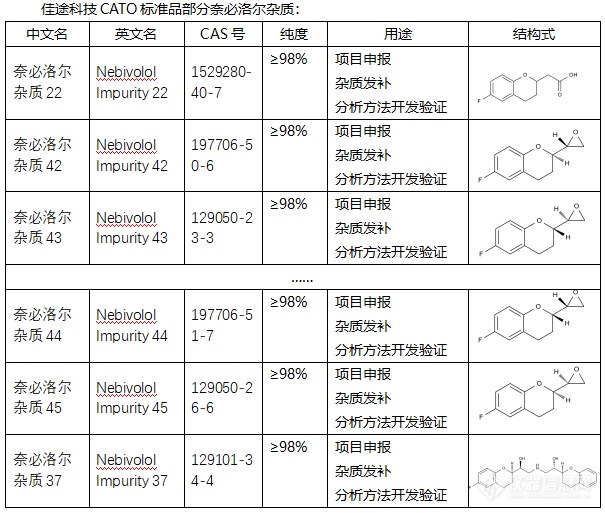
[font=宋体]◇[/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]杂质[/font][font=宋体][font=宋体] 奈必洛尔杂质是指在奈必洛尔([/font][font=Calibri]Nebivolol[/font][font=宋体])的生产或保存过程中产生的非目标化合物。奈必洛尔杂质有多种,包括但不限于以下几种:奈比洛尔杂质([/font][font=Calibri]L-[/font][font=宋体]奈必洛尔),英文名称为[/font][font=Calibri](-)-Nebivolol[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]118457-16-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]9[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]920275-23-6[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]C[/font][font=宋体](非对映体混合物),英文名为[/font][font=Calibri]Nebivolol Impurity C (Mixture of Diastereomers)[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]B[/font][font=宋体],英文名为[/font][font=Calibri]Nebivolol impurity B[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]119365-25-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]去氟奈必洛尔,英文名为[/font][font=Calibri]Desfluoro Nebivolol[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=宋体]Ⅰ和奈必洛尔杂质Ⅱ等。[/font][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套的杂质[/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[/font][img=,605,513]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182153192686_9605_6381607_3.png!w605x513.jpg[/img][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套[/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=75567]乙丙昔罗中杂质限量检查方法的研究[/url]
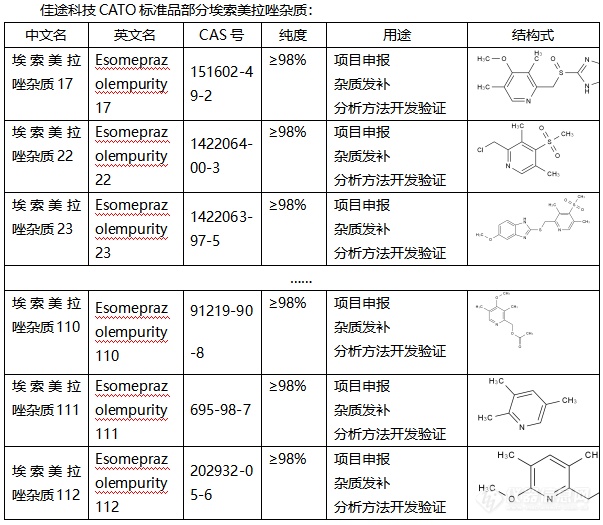
◇关于埃索美拉唑杂质 埃索美拉唑杂质是一种质子泵抑制剂,它不仅是[font=UICTFontTextStyleBody]治疗胃食管反流性杂质,还可以防止胃酸形成,[/font]它的原理主要是通过抑制胃壁细胞中[font=.pingfang sc]的[/font]H+/K+-ATP酶来达到减少胃酸分泌。埃索美拉唑杂质是一种高效且广泛应用于胃酸相关疾病治疗的质子泵抑制剂,通过抑制质子泵的活性,它不仅可以减少胃酸的分泌,还可以帮助溃疡的愈合。其作用机理是通过与胃腺细胞内的质子泵结合,形成稳定的复合物来发挥作用。[font=UICTFontTextStyleBody] [/font][font=UICTFontTextStyleBody]CATO[/font]标准品提供的[font=宋体]埃索美拉唑杂质[/font][font=宋体],在治疗肠胃道疾病中发挥着重要的作用,并且有针对性的抗菌作用。[img=,603,525]https://ng1.17img.cn/bbsfiles/images/2024/02/202402040930531289_1324_6381607_3.png!w603x525.jpg[/img] [/font]
请问大家布洛芬中杂质4-异丁基苯基乙酮是用什么方法测定的,我按欧洲药典中的梯度洗脱怎么测出来只有一个主峰呢,其他的峰都是很小很小,几乎看不出来,具体方法:流动相A是乙腈:水:磷酸=340:660:0.5,流动相B是乙腈,梯度洗脱,柱温=30,流速=2,波长=214,你们都是用什么方法测这个杂质的呀,求指教!
我们在方法考察的时候发现有未知峰产生,对主成分和未知峰进行质谱分析,主成分分子量为369,未知杂质为355,后面对两个成分进行碎裂,主成分的碎片分子量分别为124,130,158,170,295,未知杂质的碎片分子量有124,144,170,172,295,麻烦帮忙分析下这个碎片有可能是什么结构,主要是未知杂质的。[img]https://ng1.17img.cn/bbsfiles/images/2020/07/202007090700013804_321_3860760_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2020/07/202007090700016398_2033_3860760_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2020/07/202007090700021177_6207_3860760_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2020/07/202007090700024981_9266_3860760_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2020/07/202007090700030956_1648_3860760_3.png[/img]
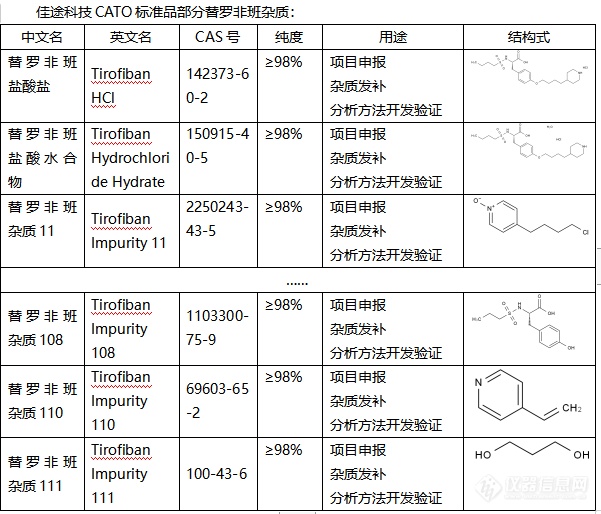
在当今的医疗领域,药物的质量控制至关重要,直接关系到患者的生命健康。替罗非班是一种广泛应用于心血管疾病治疗的药品,其质量控制尤为重要。而杂质分析作为药物质量控制的关键环节,能够准确评估药物的安全性和有效性。本文将重点探讨替罗非班杂质分析与CATO标准品应用研究的重要性。首先,杂质分析是确保药物质量的重要手段。在替罗非班的制备过程中,可能会产生一系列杂质,这些杂质的存在可能对药物的疗效和安全性产生不良影响。CATO标准品作为一种有效的分析工具,能够准确鉴定和量化替罗非班中的杂质,为药物的质量控制提供科学依据。其次,CATO标准品的应用有助于深入了解杂质的来源和性质。通过与标准品的比对分析,研究人员可以追溯杂质的产生途径,从而优化生产工艺,降低杂质的产生。此外,CATO标准品还可以用于评估杂质的毒性和风险,为药物的安全性评价提供有力支持。此外,CATO标准品在指导药物生产和改进方面也具有重要意义。通过对替罗非班中杂质的准确分析,生产商可以针对性地优化生产工艺、加强质量控制,从而提高药物的纯度和安全性。这不仅有助于保障患者的用药安全,还有助于提升企业的生产效益和市场竞争力。综上所述,替罗非班杂质分析与CATO标准品应用研究在药物质量控制中发挥着关键作用。通过深入研究替罗非班中的杂质,并借助CATO标准品这一强大工具,我们能够更好地了解杂质的来源、性质和影响,从而优化药物的生产工艺、提升药物的安全性和有效性。[img=,601,514]https://ng1.17img.cn/bbsfiles/images/2024/02/202402021849065001_3752_6381568_3.png!w601x514.jpg[/img]欢迎有需要的各位联系
弗罗里硅土小柱在有机氯净化步骤里是吸附杂质还是吸附目标物??

喝奶的时候你可能喝出过凝结的团块,但是如果里面有很多的细小杂质,除非经过过滤你才可以看到的。这些杂质大家在平时几乎不会去关注。杂质出现的原因分析:1) 原料奶里面就可能含有,按工艺流程来说,在过均质机的时候会有过滤的过程,如果机器出现故障,那么就出现了隐患。2) 管道的清洗,液奶前期处理的CIP,或者是后端出粉的干燥塔,都要定期做清洗。尤其是在对干燥塔清洗时,必须要将糊粉冲洗干净。3) 清洗剂造成的污染,清洗过程中,清洗剂本身的污染4) 机械杂质,工艺上的每一个螺丝铁钉都要有编号,随时进行保养防止机械杂质的脱落。运气不好的出现过铁钉螺丝。再说说杂质的危害:机械性的螺丝铁钉就不用说了,很容易喝道肚子里面的。其他的细小杂质很容易造成微生物的污染。用于巴氏杀菌乳、灭菌乳、生乳、炼乳及乳粉杂质度的测定,不适用于含非乳蛋白质、淀粉类成分、不溶性有色物质及影响过滤的添加物质。原理试样经过滤板过滤、冲洗,根据残留于过滤板上的可见带色杂质的数量确定杂质量。仪器和设备1.过滤设备:杂质度过滤机或配有可安放过滤板漏斗的2000 mL~2500 mL抽滤瓶。2.过滤板:直径32 mm,单位面积质量为135g/m,过滤时通过面积的直径为28.6 mm。3.杂质度标准板(附带图片)。http://ng1.17img.cn/bbsfiles/images/2014/05/201405231325_500242_2227357_3.jpg实验过程:液体乳样量取500 mL;乳粉样称取62.5 g(精确至0.1 g),用8倍水充分调和溶解,加热至60 ℃;炼乳样称取125 g(精确至0.1 g),用4倍水溶解,加热至60 ℃,于过滤板上过滤,为使过滤迅速,http://ng1.17img.cn/bbsfiles/images/2014/05/201405231325_500243_2227357_3.jpg可用真空泵抽滤,用水冲洗过滤板,取下过滤板,置烘箱中烘干,将其上杂质与标准杂质板比较即得杂质度。http://ng1.17img.cn/bbsfiles/images/2014/05/201405231326_500244_2227357_3.jpg当过滤板上杂质的含量介于两个级别之间时,判定为杂质含量较多的级别。异常的杂质版:http://ng1.17img.cn/bbsfiles/images/2014/05/201405231326_500245_2227357_3.jpg合格的杂质版:http://ng1.17img.cn/bbsfiles/images/2014/05/201405231327_500246_2227357_3.jpg
在EP药典中的有关物质检测中,有用液相归一法的,用相对保留时间来确定杂质是什么,在药典中会给出相对保留时间的一个值,可是每台机器都有差别不会符合的那么好,结果都会有一定的差别,那么对于相对保留时间的这个值在多大范围内变动算是可以接受的正常范围呢?

药物杂质即影响药物纯度的物质。药品在临床使用中产生的不良反应除了与药品本身的药理活性有关外,有时与药品中存在的杂质也有很大关系[b][color=#ff0000]。杂质直接关系到药品的质量可控性与安全性[/color][/b],在药物的研究、生产、供应和临床使用等方面,规范地进行杂质的研究,并将其控制在一个安全、合理的限度范围之内,才能保证药物的有效性和安全性。[color=#ff0000][b]因此杂质的研究及检测技术是药品研发的一项重要内容[/b][/color]。 [color=#3366ff][b]2018年8月30日[/b][/color],仪器信息网网络讲堂栏目将为您呈现“化学药物杂质研究及检测技术”主题网络研讨会。届时将邀请业内专家及技术人员为大家介绍化学药物杂质研究的最新进展及检测技术。 [b]如果你是一个对知识渴望的化学药物研究者或从业人员,想了解药物杂质的最新研究进展;又或者是不安于现状的检验检测机构工作者,想要提高检测技术水平,那就千万不要错过这个难得的沟通交流机会,保证会让你有意想不到的收获哦~欢迎大家踊跃报名[/b]([b][url=https://www.instrument.com.cn/webinar/meetings/icd/]点击即可传送至免费报名处[/url],[color=#ff0000]报名截止日期8月29日[/color][/b])![url=https://www.instrument.com.cn/webinar/meetings/icd/][img=,690,636]https://ng1.17img.cn/bbsfiles/images/2018/08/201808281042237666_6386_3429861_3.jpg!w690x636.jpg[/img][/url][url=https://www.instrument.com.cn/webinar/meetings/icd/][img=,690,724]https://ng1.17img.cn/bbsfiles/images/2018/08/201808281042363056_2579_3429861_3.png!w690x724.jpg[/img][/url]
基体为钨(或钼),粉末样品及金属样品,杂质要做20个元素左右甚至更多,包括常见元素Si、Al、Fe等等,也包括一些其它的杂质元素,如As、Pb、Sb、Bi等等,杂质的含量(未稀释)变化范围大,从0.1ppm~几千ppm不等。不知道有什么仪器能够能做?这事让我头痛很久了,也许根本不可能用一台仪器解决所有的问题,但是我也是被逼的,企业的状况似乎不太可能同时添置几台仪器。[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url]能做吗?Si是不是不好做?
兄弟们做微量杂质(溶液浓度为0.xppm)时,有没有杂质吸附到容量瓶的现象。我最近做试验发现,定容后放一个小时进行测量,发现测量比较低(但是精密度很好),然后我摇容量瓶,再次测量发现测量值增加很高。这是否可以理解杂质吸附到容量瓶上呢? 敬请解答。[em0814]

最近在生产线出现废品率很高,经过调查,发现根本原因可能是最新用的一批焊料(锡球)(下面是锡球的电镜图)出了问题。通过显微镜检查,发现新锡球中混入了一些绿色杂质。http://ng1.17img.cn/bbsfiles/images/2014/10/201410301509_520885_2942222_3.jpg1.杂质分析经显微镜放大,发现混入的绿色杂质有点像晶体或者无机物,而且是多种颜色。http://ng1.17img.cn/bbsfiles/images/2014/10/201410301510_520886_2942222_3.jpg为了分析这个杂质,首先把这杂质挑出出来放在碳胶布,进行SEM/EDX分析,确定它的成分从而找到它的来源。SEM观察http://ng1.17img.cn/bbsfiles/images/2014/10/201410301510_520887_2942222_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/10/201410301511_520888_2942222_3.jpg EDX分析http://ng1.17img.cn/bbsfiles/images/2014/10/201410301534_520904_2942222_3.jpgSEM观察显示这个杂质的外观不太像常见的脏污;而EDX的分析显示这个杂质主要含有元素C,O,Al,Si,Cl;很奇怪。2. 存放锡球的瓶子分析这些杂质是哪里来的呢?首先考虑到是杂质存在的地方:存放锡球的瓶子。因为这个瓶http://ng1.17img.cn/bbsfiles/images/2014/10/201410301514_520891_2942222_3.jpg子肉眼看起来也是绿色的,特别是瓶盖和瓶子内部,如果这两个地方表面不平或者很粗糙,就可能会导致一些本身材料的颗粒掉到瓶子里,跟里面的锡球混在一起。下面是对瓶子分析:首先,用手术刀在瓶子内壁刮下一些碎片放在硅片上,然后进行显微镜观察和SEM/EDX分析。显微镜观察显示瓶子材料跟杂质明显不同,也不像杂质那样有多种颜色。http://ng1.17img.cn/bbsfiles/images/2014/10/201410301519_520892_2942222_3.jpgSEM观察也发现瓶子材料跟杂质明显不同;瓶子材料的表面也非常光滑,所以表面材料脱落的可能性也很小。http://ng1.17img.cn/bbsfiles/images/2014/10/201410301520_520893_2942222_3.jpghttp://ng1.17img.cn/bbsfiles/images/2014/10/201410301521_520894_2942222_3.jpgEDX[font=
索非布韦杂质是一种化学物质,它是索非布韦的同分异构体或相关化合物。索非布韦是一种直接作用在肝脏的抗病毒药物,用于治疗丙型肝炎。COTO标准品是一种高纯度的标准物质,用于测定索非布韦及其杂质的纯度、含量和化学性质。通过与COTO标准品进行对比和分析,可以确定索非布韦及其杂质的结构、组成和含量,从而保证索非布韦的质量和安全性。在药物研发和生产过程中,COTO标准品的使用非常重要。它可以提供可靠的参照物,用于质量控制、药物分析和化学计量学研究。通过使用COTO标准品,可以确保索非布韦及其杂质的准确性和可靠性,为药物的安全性和有效性提供保障。总的来说,COTO标准品在索非布韦杂质的研究和控制中具有重要作用。通过使用COTO标准品,可以更好地了解索非布韦及其杂质的性质和含量,从而确保药物的安全和有效性。同时,也需要加强生产过程中的管理和监督,加强质量标准和监管措施的执行力度,确保药物质量和安全。
替诺福韦杂质是一种化学物质,它是替诺福韦的同分异构体或相关化合物。替诺福韦是一种核苷酸逆转录酶抑制剂,用于治疗HIV和乙型肝炎。COTO标准品是一种高纯度的标准物质,用于测定替诺福韦及其杂质的纯度、含量和化学性质。通过与COTO标准品进行对比和分析,可以确定替诺福韦及其杂质的结构、组成和含量,从而保证替诺福韦的质量和安全性。在药物研发和生产过程中,COTO标准品的使用非常重要。它可以提供可靠的参照物,用于质量控制、药物分析和化学计量学研究。通过使用COTO标准品,可以确保替诺福韦及其杂质的准确性和可靠性,为药物的安全性和有效性提供保障。总的来说,COTO标准品在替诺福韦杂质的研究和控制中具有重要作用。通过使用COTO标准品,可以更好地了解替诺福韦及其杂质的性质和含量,从而确保药物的安全和有效性。同时,也需要加强生产过程中的管理和监督,加强质量标准和监管措施的执行力度,确保药物质量和安全。
有没有做过维生素A杂质的液相色谱分析?维生素A及其杂质维生素A环氧化物、维生素A醛、维生素A酸没有杂质对照品,以上物质在甲醇-水(90:10)流动相,C18*250mm柱能不能分的开?
[B][center]药物中杂质的来源及杂质限量检查[/center] [/B]药物只有合格品与不合格品;一般化学试剂分为4个等级(基准试剂、优级纯、分析纯、化学纯) [B]药物中一般杂质检查 [/B][B]氯化物为一指示性杂质。[/B] 通过对氯化物的控制,可同时控制与氯化物结合的一些阳离子以及某些同时生成的副产物。可从氯化物检查结果显示药物的纯度,间接考核生产、贮藏过程是否正常。 1. 原理 药物中微量的氯化物在硝酸酸性条件下与硝酸银反应,生成氯化银的胶体微粒而显白色浑浊,与一定量的标准氯化钠溶液在相同条件下产生的氯化银浑浊程度比较,判定供试品中氯化物是否符合限量规定。 Ag+ + Cl- → AgCl ↓ [B]硫酸盐检查法 [/B] 1. 原理 药物中微量的硫酸盐在稀盐酸酸性条件下与氯化钡反应,生成硫酸钡的微粒而显白色浑浊,与一定量的标准硫酸钾溶液在相同条件下产生的硫酸钡浑浊程度比较,判定供试品中硫酸盐是否符合限量规定。 [B]铁盐检查法 [/B]硫氰酸盐法 巯基醋酸法 砷盐检查法 1. 古蔡氏法 1. 原理 金属锌与酸作用产生新生态的氢,与药物中微量砷盐反应生成具挥发性的砷化氢,遇溴化汞试纸产生黄色至棕色的砷斑,与同条件下一定量标准砷溶液所生成的砷比较斑,判断砷盐的含量。 [B]硒、氟及硫化物检查法 [/B]1. 氧瓶燃烧法 适用于以共价键结合的卤素、硫、硒的有机药物。 本法系将有机药物防入充满氧气的密闭燃烧瓶中进行燃烧,将燃烧所产生的欲测组分吸收于适当的吸收液中,然后根据欲测组分的性质,选用合适的分析方法进行鉴别、检查或含量测定。 [B]注意事项及讨论 [/B]1. 根据被燃烧分解的样品量选用适宜大小的燃烧瓶。 2. 测定氟化物时应改用石英燃烧瓶。 1. 硒检查法 (1). 操作方法 样品与对照品液,调节Ph2.0±0.2,加盐酸羟胺,二氨基萘,比色。 [B]硫化物检查法 [/B] 方法同砷盐检查第一法,不装醋酸铅棉花,以醋酸铅试纸代替溴化汞试纸。 标准液取1ml 5/ml [B]澄清度检查法 [/B]将一定浓度的供试品溶液与浊度标准液分别置于配对的比浊用玻璃管,同置黑色背景上,在漫射光下观察。浊度标准液 硫酸肼与乌洛托品溶液混合分五个等级,未超过0.5等级即为澄清。BP98规定未超过1等级即为澄清。 [B]溶液颜色检查法 [/B]CHP2000 [B]1. 比色法[/B] 色调标准贮备液 黄色液 重铬酸钾液(BP98用氯化铁) 红色液 氯化钴液 蓝色液 硫酸铜液 配成各种色调色号标准比色液共50种。 [B]2. 分光光度法 [/B] [B]易碳化物检查法 [/B]检查药物中含有的遇硫酸易碳化或易氧化而呈色的有机杂质。 对照品液 样品液 加硫酸5后,加供试品。 [B]炽灼残渣检查法[/B] 取供试品1.0~2.0g或个药品项下规定的重量,置已炽灼至恒重的坩埚中,精密称定,缓缓炽灼至完全碳化,放冷至室温;除另有规定外,加硫酸使湿润,低温加热至硫酸蒸气除尽后,在700~800炽灼使完全灰化,移至干燥器内,放冷至室温,精密称定,再在700~800炽灼至恒重,即得。残渣限量一般为0.1~0.2% 一般应使炽灼残渣量为1~2mg 若需将炽灼残渣留作重金属检查时,炽灼温度必须控制在500~600。 [B]干燥失重测定 [/B]1. 常压恒温干燥法 2. 干燥剂干燥法 3. 减压干燥法 [B]水分测定法 [/B][B]费休氏法 [/B] 本法是根据碘和二氧化硫在吡啶和甲醇溶液中能与水起定量反应的原理以测定水分。 [B]甲苯法[/B] 在加热状态下,甲苯夹带着水分蒸出,收集蒸出的水分测定。 [B]药物中特殊杂质检查 [/B] [B]一、物理法 [/B] [B]二、化学反应法 [/B](一)容量分析法 (二)重量分析法 (三)比色法和比浊法 [B]三、色谱法 [/B]1.纸色谱法 薄层色谱法 TLC是药典中最常用的特殊杂质限量检查方法。 1.在一定供试品及检查条件下,不允许有杂质斑点存在 2.以待测杂质对照品检测 3.将供试品稀释到适当浓度作为杂质对照品溶液 4.选用质量符合规定的与供试品相同的药物作为杂质对照品 [B]高效液相色谱法 [/B] [B][url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法 [/B] 1.面积归一化法 2.主成分自身对照法 3.内标法测定 4.内标法加校正因子法 5.外标法 有机溶剂残留量测定法 [B]分光光度法 紫外分光光度法 比色法 [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法[/B]
化药质量控制CTD申报资料中杂质研究的几个问题张哲峰成海平宁黎丽田洁化药药学二部 摘要:杂质研究与控制是把控药品质量风险的重要内容之一,基于杂质谱分析的杂质控制是“质量源于设计”基本理念在杂质研究与控制中的具体实践,需要与CMC各项研究乃至药理毒理及临床安全性研究等环节关联思考、综合考虑,而不仅仅拘泥于提供准确的分析数据。本文针对当前CTD申报资料中杂质研究方面存在的问题与不足,结合CTD过程控制和终点控制相结合、研究和验证相结合、全面系统的药品质量控制理念,探讨仿制药杂质研究与控制的基本逻辑思路,提出CTD申报资料中杂质研究与控制方面几个需要关注的问题。 关键词:杂质研究与控制 杂质谱 CTD格式 杂质研究与控制是一项系统工程,需要以杂质谱分析为主线,安全性为核心,按照风险控制的策略,将杂质研究与CMC各项研究,乃至药理毒理及临床安全性研究等环节关联思考、综合考虑,而不仅仅拘泥于提供准确分析数据的传统思维,不是一项孤立的分析工作。CTD(Common Technical Document)申报格式体现了过程控制和终点控制相结合、研究和验证相结合、全面系统的药品质量控制理念,更加符合杂质研究与控制的基本规律和逻辑思路。自2011年4月起,药审中心陆续发布了多项有关CTD格式及技术审评的相关要求及电子刊物,对于国内研发单位正确理解CTD格式内含的基本精神起到了一定的促进作用,但就目前阶段的申报情况看,有些申报资料在杂质研究方面仍存在一些不足,仅仅是形式上的CTD格式,尚未实质性贯彻CTD的基本逻辑思路。以下是针对目前CTD申报资料中杂质研究相关问题的一些考虑。 1、CTD格式中杂质控制的考虑要体现在CMC的各个环节,而不是仅仅局限在“质量控制”模块。如制剂的原辅料控制中,原辅料的选择与控制要考虑以符合制剂质量要求(杂质等)为核心,必要时进行精制处理并制定内控标准;关键工艺步骤及参数的确立、工艺开发过程等要考虑以杂质是否得到有效控制为重点关注之一;制剂相关特性中要体现与原研产品杂质谱等的对比情况;包材、贮藏条件以及有效期的确立等也要以杂质是否处于安全合理的可控范围内为核心等等。实际上这正是源头控制、过程控制与终点控制相结合的杂质控制理念的体现,在研发工作及申报资料的整理中都需要针对性的贯彻实施。 问题与案例:有些申报资料在某种程度上未能充分体现杂质研究的整体性,对杂质控制措施仅强调了终点控制措施,尚未充分体现源头控制与过程控制的基本思路,具体表现在如下方面: (1)制剂杂质控制受制于原料药质控水平的约束,以目前国内批准的原料药杂质水平现状为由,未能根据该品当前杂质控制的水平与趋势,对原料药提出较为严格的针对性的杂质控制要求,并进行质量内控,因而难以确保制剂杂质控制水平与目前国际水平相适应; (2)在论述说明制剂相关特性时,未提供与原研产品杂质谱的对比分析情况; (3)关键工艺步骤及参数的确立、工艺开发过程相关内容中未详细说明杂质谱的变化情况,缺失关键质量数据的支持。 2、CTD格式的特点之一是研究内容模块化呈现,但需关注杂质分析与控制的系统性与整体性,不能割裂各项内容的必然联系和有机统一。比如对原料药而言,杂质分析与控制的相关内容会分布在分析方法(3.2.S.4.2)、方法学验证(3.2.S.4.3)、杂质对比研究与杂质谱分析(3.2.S.4.5)、杂质情况分析总结(3.2.S.3.2)、样品检测与数据积累(3.2.S.4.4)、控制限度(2.3.S.4.1)等各模块中,但杂质研究又是一项系统工程,具有统一的整体性,因此,不要因为申报资料格式的模块化而人为割裂各项研究内容的相互联系,甚至遗漏相关研究内容,要高度关注杂质分析与控制的系统性与整体性,将杂质研究与控制的全部内容和信息体现在相应模块中。如详细的杂质研究报告可以体现在3.2.S.4.5中;3.2.S.3.2要报告杂质研究的结果;杂质分析方法的筛选、研究与验证内容要在3.2.S.4.3中体现;对仿制药而言,杂质限度确定的论证与依据需要在与原研产品进行全面的杂质谱对比研究基础上进行论证说明,因此,与原研产品的对比研究及结论要在3.2.S.4.5中体现。 问题与案例:有些申报资料忽视了各项研究间的关联性,未能充分突出仿制药研发的特点,具体体现如下: (1)对分析方法的来源没有足够明确的说明,在分析方法的筛选、优化等方面做了哪些研究等信息缺失,只有方法学验证内容,缺失方法学筛选研究的相关信息; (2)没有比较说明采用的杂质分析方法与USP、BP/EP、JP等药典同品种分析方法相比有哪些区别和优势,未能从分析方法、杂质控制种类及限度要求等方面的比较情况评估拟定质量标准的杂质控制水平; (3)缺失放行标准质控限度确定的依据进行论述,3.2.S.4.5中只对货架期标准限度的确定进行了相关说明,未从杂质来源与特点、数据积累、稳定性考察等角度论述放行标准中相关限度确定的依据。 3、从杂质谱分析入手确立科学的杂质研究基本思路。杂质谱包括药物中所有杂质的种类、来源及特性等信息,通过杂质谱分析较为全面地掌握产品中杂质概貌(种类、含量、来源和结构等);有针对性地选择合适的杂质分析方法,以确保杂质的有效检出和确认;通过与原研产品杂质谱的对比研究,根据各相应杂质的一致性求证,或跟踪杂质谱对安全性试验或临床试验结果产生的影响,评估各杂质的安全性风险和可接受水平;结合规模化生产时杂质谱的变化情况,确立安全合理的杂质控制水平。 基于杂质谱分析的杂质研究是一种“以源为始”的主动思维模式,以“质量源于设计”的观点,从杂质来源入手,从制备工艺、化学结构、处方组成的分析出发,评估、预测产品中可能存在的及潜在的副产物、中间体、降解物以及试剂、催化剂残留等大体的杂质概况,辅以适当的强制降解、对照物质的加入等验证的手段,考证建立的分析方法是否能够将它们逐一检出,并进行相应的方法学验证工作;相比之下,传统的杂质研究是一种“以终为始”的被动行为和逆向思维模式,从杂质分析的结果出发,仅从建立的某种检测方法所检出的有关物质中归属其来源情况,而未充分分析与验证可能存在的潜在杂质情况,建立的分析方法能否全面检出这些杂质,故容易出现杂质漏检的情况,难以全面掌握产品的杂质谱。 问题与案例:杂质谱分析表明某原料药所采用的合成路线会产生具有遗传毒性的双叠氮杂质ROX,但最初建立的分析方法未检出该杂质,但不能确定是产品中的确不存在该杂质,还是建立的分析方法不能有效检出该杂质,经定向制备该杂质,采用标准加入法有针对性的分析考查,采用改进后分析方法在正常产品中检测到该物质,尽管其含量极低,考虑到其较强的毒性情况,质量标准中仍作为特定杂质予以严格控制,保证了其临床应用的安全性。因此,基于杂质谱分析的杂质研究是一种相对科学的思维模式,对于有效掌控杂质安全性风险具有重要意义。 4、分析方法的验证应具备针对性和全面性。杂质的微量性和复杂性,使得检测方法的专属性、灵敏度和准确度十分关键。杂质分析方法的对象是各个潜在的杂质,因此,其分析方法的验证需要根据不同杂质的特点综合设计验证方案,进行有针对性的规范验证。 问题与案例:一些申报资料中对杂质分析方法的灵敏度、准确度等仅仅针对主药化合物进行验证,仍无法说明是否适用于相关杂质的检出和定量。如下是某药物有关物质测定方法学验证总结,基本体现了方法学验证的针对性与全面性,建议参考。 项目验证结果专属性①统适用性良好,峰形、峰纯度、柱效参数等符合要求。②在酸、碱、高温、氧化各破坏条件下的主峰峰纯度角均小于纯度阈值,主峰峰纯度良好,破坏后的主峰与各杂质峰均能有效分离,分离度均大于1.5。③供试液加入起始原料、反应试剂、副产物及中间体等,均可有效检出,并良好分离。线性和范围①质A浓度在0.036μg/ml~1.204μg/ml范围内,线性关系良好(n=8);y=13703x-174.83;R2=0.9991。②杂质B浓度在0.089μg/ml~1.192μg/ml范围内,线性关系良好(n=7);y=10941x-517;R2=0.9995。③杂质C浓度在0.299μg/ml~4.784μg/ml范围内,线性关系良好(n=7);y=13257x-492.44;R2=0.9999。④主药浓度在0.3μg/ml~4.8μg/ml范围内,线性关系良好(n=6);y=15008x+565.48;R2=0.9999。灵敏度杂质A、B、C及主药最低检出限分别为0.012ng、0.0
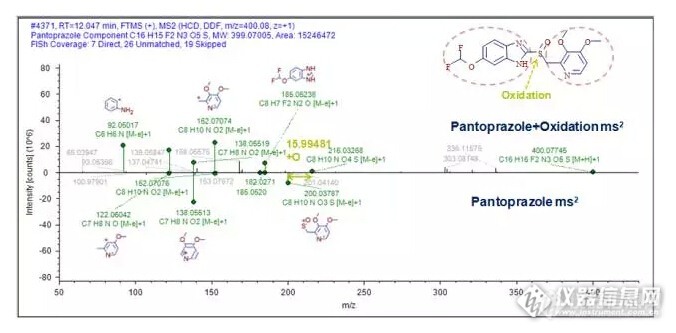
药物杂质是药物活性成分(原料药)或药物制剂中不希望存在的化学成分,会对用药的安全性和有效性带来隐患,因此杂质的检测是保证药物质量至关重要的部分,FDA、EMEA、PMDA、CFDA等各国药品监管部门制定了相应的指导原则对其进行严格管控。http://ng1.17img.cn/bbsfiles/images/2015/12/201512141737_577892_3005330_3.jpg 独有的四极杆静电场轨道阱Q Exactive™ Focus高分辨液质联用技术,凭其高灵敏度、高专属性和高准确性的分析能力,可对样品中药物杂质进行全面的信息采集。结合新一代的智能小分子化合物鉴定软件Compound Discoverer™,以高度灵活的自定义方式制定分析工作流程,对数据中的目标和非目标杂质进行提取、比对及鉴定,工作流程如下:http://ng1.17img.cn/bbsfiles/images/2015/12/201512141737_577893_3005330_3.jpg 通过软件对样品数据的分析和提取,在Compound Discoverer中可以直观、便捷的查看和筛选预期和未知的杂质分析结果,从结果界面中可获得不同条件下样品杂质的变化情况,获得所有杂质保留时间、一级质谱、同位素和二级质谱等丰富信息:http://ng1.17img.cn/bbsfiles/images/2015/12/201512141738_577894_3005330_3.jpg 在获得母药和杂质的一级和二级质谱信息后,软件将调用碎裂数据库(Fragmentation Library)快速的对泮托拉唑的碎片结构进行归属,该数据库几乎涵盖了所有已发表的文献,保证了碎片解析的准确性。在此研究结果之上,通过软件对杂质与母药二级质谱信息之间的比对,可进一步对杂质变化位点进行推测。在本例中,通过152、185等共有碎片和200、216等特征差异碎片的比对,推测出该杂质为泮托拉唑砜:http://ng1.17img.cn/bbsfiles/images/2015/12/201512141738_577895_3005330_3.jpg 基于新一代四极杆-静电场轨道阱质谱Q Exactive Focus和新一代小分子化合物分析软件Compound Discoverer,建立了药物杂质鉴定的新流程。无论是优质数据的有效获取,还是获取后对已知和未知杂质的分析鉴定,该工作流程都可以完美的实现。在本例中,共鉴定到泮托拉唑杂质15个,其中可能的降解杂质9个,可能的工艺杂质6个,为药物杂质的质量控制、安全性评估提供了富有价值的信息。(分享)
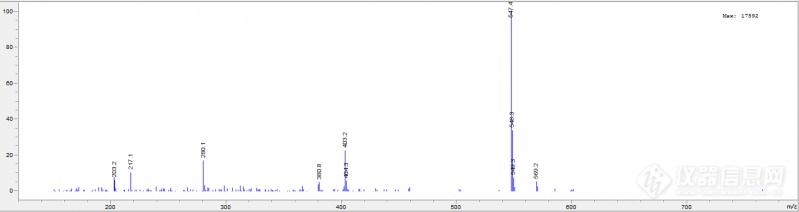
[color=#444444]我在做乙霉威(农药)的杂质分析,用的安捷伦[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url],ESI正离子模式,有一个杂质的质谱图如下,丰度最大的m/z为547.4,其次为403.2和280.1,缺乏[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]谱图解析的知识,还请帮忙,谢谢[/color][color=#444444][img=,690,183]https://ng1.17img.cn/bbsfiles/images/2019/08/201908081445310576_6431_1676638_3.png!w690x183.jpg[/img][/color]
喹硫平杂质主要在制药工艺中扮演质量控制的角色。在药物制备过程中,有时会产生一些不希望的化合物,这些化合物被称为杂质。它们可能来自原料、副反应、分解产物等。喹硫平是一种用于治疗精神障碍的药物,如精神分裂症。在其制备过程中可能会产生杂质。这些杂质如果未被充分去除,可能会影响药物的安全性和有效性。例如,一些杂质可能会引发过敏反应,降低药物的效力,或增加潜在的毒性效应。因此,对喹硫平的纯度要求非常高,其杂质的含量必须控制在严格的范围内。在药品的质量控制过程中,CATO标准品对杂质的检测和分析非常重要。它可以确保药品在整个生产和储存过程中保持一致的质量和安全性。此外,对喹硫平杂质的研究也有助于优化其制药流程,从而提高其生产效率和产品质量。[img=,610,528]https://ng1.17img.cn/bbsfiles/images/2024/02/202402052054525835_779_6381668_3.png!w610x528.jpg[/img]
请问有版友做过Te9999、Bi99.997、Se-1、Sb-4N等的杂质分析吗?一个ICP-OES可以完成这些杂质分析吗?测试的标准方法是什么? 杂质有Cu,Pb,Al,Bi,Fe,Na,Si,S,Se,As,Mg,Zn,Ag,Te,Sb,Cl,Sn,Cd,Hg,Ni,Mn,B,C等。 现在正计划购买这些杂质标准溶液,如果都买单标的话,实在是太多了。您是怎么做的呢?杂质标准溶液哪里有混标卖?谢谢!