【CEM】Fmoc-His(Boc)-OH在基于Fmoc的固相肽合成中的应用
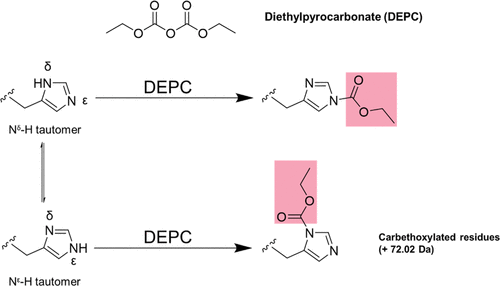
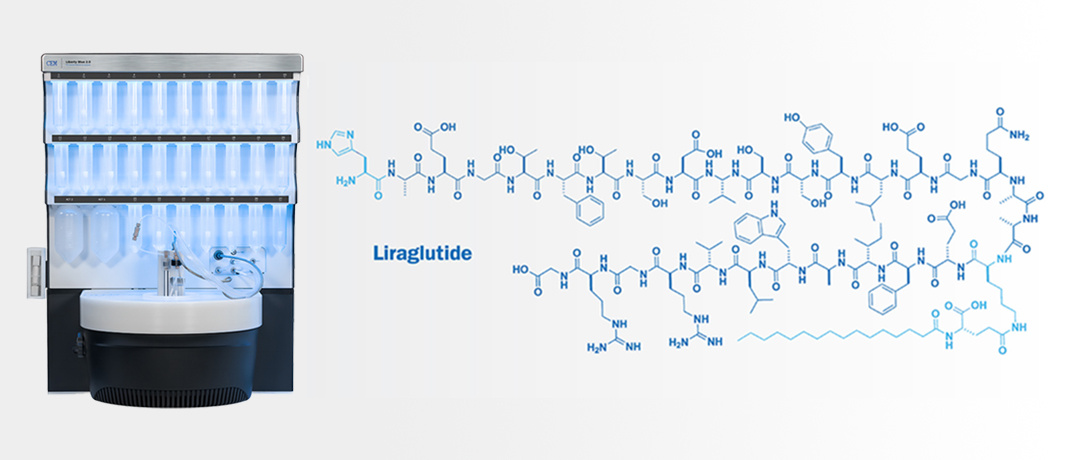
一、组氨酸的差向异构化对映体纯度极大地影响肽的生物活性;因此,避免D-异构体含量的增加至关重要。1在固相肽合成(SPPS)的偶联过程激活阶段,组氨酸特别容易发生差向异构化。组氨酸倾向于差向异构化(图1)是一种分子内的副反应,这是由于咪唑Nπ上的孤对电子与酸性α碳氢的接近性所导致。当氨基酸被激活时,1号位的孤对电子具有足够的碱性以进行去质子化,从而形成一个无立体选择性的酯烯醇盐22。此时,转化为L-或D-异构体3并没有热力学上的优先途径。当反应位点聚集,且组氨酸在激活状态保持较长时间的期间,差向异构化的可能性增加。图1:Fmoc-His(PG)-OH在激活过程中高差向异构化水平的机制解释二、组氨酸侧链保护对咪唑环的保护(图2)通常采用在Nτ位置使用三苯甲基(Trt)基团的方式实现4。Trt基团因其体积大和具有吸电子性,能够有效抑制诸如环上N-酰化等副反应,然而在控制差向异构化方面效果有限。其他侧链保护基团,尤其是那些提供Nπ保护的,例如Fmoc-His(π-Mbom)-OH(5),通过阻断α-氢的接触途径来减少差向异构化。但这些衍生物的缺点在于它们本身的高成本和因多步骤合成策略导致的低批量供应,这种策略需要在连接Mbom基团时对Nα位置进行互斥保护。3,4,5,6此外,在肽切割过程中还需添加额外的清除剂,以防止新暴露的氨基功能团上发生羟甲基化。 本文中,Fmoc-His(Boc)-OH(6)被证实是Fmoc SPPS中组氨酸并入的宝贵替代物,因为它在高温下对差向异构化具有较高的稳定性,成本低,且比其他任何市场上可购买的衍生物具有更好的批量供应能力。 图2:Fmoc-SPPS用的组氨酸衍生物:Fmoc-His(Trt)-OH(4),Fmoc-His(π-Mbom)-OH(5)和Fmoc-His(Boc)-OH(6)三、Fmoc-His(Boc)-OH的优势Fmoc-His(Boc)-OH 能够以游离酸和环己胺(CHA)盐的形式大量购买。对于盐形式,需要通过提取过程来移除CHA基团。鉴于这一过程相对繁琐,我们的研究便专注于游离酸的应用。根据先前的报告,与His(Trt) 相比,His(Boc)在差向异构化方面的倾向性更低。7这一现象可以归因于氨基甲酸酯基团较强的吸电子效应,它有效地从π子中抽取电子云密度,从而降低了其碱性。四、讨论一项采用利拉鲁肽和1-42Beta淀粉样蛋白的可行性研究评估了-Boc基团在微波(MW)辅助固相肽合成(SPPS)过程中对差向异构化的抑制效果及侧链的稳定性。肽段是在HE-SPPS条件下制备的,具体操作包括1分钟90°C的去保护和2分钟90°C使用DIC和Oxyma Pure进行的偶联。8与基于尿嘧啶的激活策略相比,DIC/Oxyma Pure激活在偶联效率和抑制差向异构化方面提供了更优的结果。后者的表现归因于碳二亚胺活化所固有的酸性环境。9,10在室温或稍高的条件(例如50°C)下并入组氨酸能进一步降低D-异构体的形成,但这样的条件对于His(Trt)仍然不够理想。我们比较了His(Trt)和His(Boc)在使用两种常见协议时的偶联条件:(1)10分钟50°C和(2)2分钟90°C。最后,我们研究了溶液中的稳定性,以确定其在Liberty BlueTM HT12上的高通量自动化应用的可行性。利拉鲁肽的合成利拉鲁肽具有一个N端的组氨酸,这在与肽链的偶联中存在一定难度,因此,通过微波加热来增强酰化作用是有益的。使用三苯甲基保护在50°C下偶联组氨酸10分钟,结果显示D-异构体的形成增加到了6.8%(如表1所示)。在相同条件下,Fmoc-His(Boc)-OH显著减少了差向异构化,仅为0.18%。 Fmoc-His(Boc)-OH在90°C时的表现也相当出色,观察到的差向异构化水平为0.81%,相比之下His(Trt)则大于16%。Fmoc-His(Trt)-OH和Fmoc-His(Boc)-OH都以相当的粗纯度获得了目标肽(图3)。Fmoc-His(π-Mbom)-OH在纯度和D-His方面提供了与Fmoc-His(Boc)-OH相似的结果。 图3:使用(a) Fmoc-His(Trt)-OH或(b) Fmoc-His(Boc)-OH的利拉鲁肽UPLC色谱图。组氨酸偶联条件 = 50°C,10分钟。总合成时间 = 2小时55分钟 表1:利拉鲁肽中组氨酸在不同偶联条件下的D-异构体形成情况1-42Beta淀粉样的合成之前的研究表明,在长时间的哌啶处理过程中,Nτ-Boc侧链基团显示出不稳定性。11为了测试高温去保护过程中–Boc的稳定性,我们合成了包含三个组氨酸残基的1-42Beta淀粉样蛋白。1-42Beta淀粉样蛋白的合成序列是出了名的困难,需要使用特殊的偶联试剂,即使在严苛条件下,产物纯度通常也过低,无法进行分析和纯化。12与常规合成方法不同,HE-SPPS即便在未优化的条件下也能获得木及高的粗纯度。我们比较了His(Trt)和His(Boc)在50°C下偶联10分钟以及90°C下偶联2分钟的情况。His(Boc)将总合成时间从4小时24分钟缩短到3小时58分钟,并且将差向异构化的比例从2.88%降低至1.29% D-异构体(表2)。UPLC分析表明,这两种合成方法得到的目标产物在粗纯度上具有可比性(图4)。 表2:BA中His(Trt)和His(Boc)的差向异构化情况图4:使用(a) His(Trt)和(b) His(Boc)的1-42 Beta淀粉样蛋白的UPLC色谱图溶液中的稳定性在自动化高通量SPPS应用中,要求底物能在溶液中保持溶解状态长达10天。通常,像组氨酸这样的反应物由于保护基团的降解/丢失而导致变色和沉淀,其溶液寿命仅限于5天。在这项研究中,我们测试了组氨酸溶液(DMF,0.2 M)在大气条件下存放10天的稳定性(图5)。所有样品都迅速溶解,得到无色溶液。Fmoc-His(Trt)-OH的变色在短短24小时内就开始出现,并在10天的时间里加剧。10天后,Fmoc-His(π-Mbom)-OH溶液略呈黄色,而Fmoc-His(Boc)-OH溶液在研究期间保持无色。UPLC分析表明,Fmoc-His(Boc)-OH和Fmoc-His(π-Mbom)-OH保持了99%的纯度。基于强烈的变色,预计在10天的研究期间Fmoc-His(Trt)-OH样品中形成了几种杂质(图6)。然而,使用质谱对这些杂质进行定性未能成功。 图5:不同组氨酸衍生物溶液中的稳定性颜色测试 图6. 10天后DMF中组氨酸衍生物(0.2 M)的UPLC分析;(a) = Fmoc-His(Trt)-OH (b) = Fmoc-His(π-Mbom)-OH (c) = Fmoc-His(Boc)-OH五、结论上述数据表明,His(Boc)是一种强大的组氨酸衍生物,可以在90°C下高效偶联,提供优良的粗纯度,同时缩短偶联时间并显著降低差向异构化。与其他抑制差向异构化的N保护衍生物相比,Fmoc-His(Boc)-OH更易获得,同时保持相当的合成性能。总之,Fmoc-His(Boc)-OH的核心优势包括: &bull 商业批量可用性强,价格相对于Fmoc-His(Trt)-OH更具竞争力&bull 在高温下具有低水平的差向异构化;50°C及以下的偶联温度使得Fmoc-His(Boc)-OH适用于活性药物成分的合成,无需复杂的偶联试剂和条件13 &bull 优异的溶液稳定性;与Fmoc-His(π-Mbom)-OH相当,且优于Fmoc-His(Trt)-OH六、材料与方法试剂以下Fmoc氨基酸和树脂购自位于Matthews,NC的CEM公司,包含所示的侧链保护基团:Ala, Arg(Pbf), Asn(Trt), Asp(OMpe), Gln(Trt), Gly, His(Boc), His(Trt), Ile, Leu, Lys(Boc), Lys(palmitoyl-Glu-OtBu), Phe, Pro, Ser(tBu), Tyr(tBu), Val。Rink Amide ProTideTM LL, Cl-MPA ProTideTM LL, 以及Fmoc-Gly Wang PS LL树脂也购自CEM公司。二异丙基碳二亚胺(DIC),哌啶,三氟乙酉夋(TFA),3,6-二氧杂-1,8-辛二硫醇(DODT)和三异丙基硅烷(TIS)购自Sigma-Aldrich(St. Louis, MO)。二氯甲烷(DCM),N,N-二甲基甲酰胺(DMF),无水二乙酉迷(Et2O),乙酸,高效液相色谱级水,以及乙腈购自VWR(West Chester, PA)。液相色谱-质谱级水(H2O)和液相色谱-质谱级乙腈(MeCN)购自Fisher Scientific(Waltham, MA)。D-异构体通过手性GC-MS(C.A.T. GmbH)进行测定。肽合成:利拉鲁肽在CEM Liberty Blue自动化微波肽合成器上,以0.10 mmol的规模合成了该肽。使用了0.313克Fmoc Gly Wang PS LL树脂(0.32 meq/g置换)。去保护作用采用20%哌啶和0.1 M Oxyma Pure在DMF中执行。偶联反应使用5倍过量的0.2 M Fmoc-AA、1.0 M DIC和1.0 M Oxyma Pure在DMF(CarboMAX)中进行。切割则应用CEM Razor&trade 高通量肽切割系统,配比为92.5:2.5:2.5 TFA/H2O/TIS/DODT。切割后,肽通过Et2O沉淀并过夜冻干。肽合成:1-42Beta淀粉样蛋白采用CEM Liberty Blue自动化微波肽合成器,以0.10 mmol的规模在0.512g Cl-MPA ProTide树脂(0.19 meq/g置换)上合成了该肽。去保护作用使用20%哌啶和0.1 M Oxyma Pure在DMF中进行。偶联反应用5倍过量的0.2 M Fmoc-AA、1.0 M DIC和1.0 M Oxyma Pure在DMF(CarboMAX)中进行。切割采用CEM Razor&trade 高通量肽切割系统,配比为92.5:2.5:2.5 TFA/H2O/TIS/DODT。切割后,肽通过Et2O沉淀并过夜冻干。稳定性研究在50毫升离心管中,制备了0.2摩尔浓度的组氨酸溶液(总共5毫升DMF),并对管进行了密封。这些溶液在实验室环境下保持在室温,持续10天。为了准备用于超高效液相色谱-质谱分析的样品,将10微升的组氨酸溶液稀释到5毫升的50/50(体积比)乙腈和水的混合溶剂中。调整进样量,直至吸光度达到35 – 55单位。七、参考文献(1) Kusumoto, S. Matsukura, M. Shiba, T. Biopolymers, 1981, 20,1869 --1875.(2) Kates, S. A. Albericio, F. Solid-Phase Synthesis – A Practical Approach Kates, S. A Albericio, F. Eds. Marcel Dekker Inc: New York, New York, 2000 Chapter 4. Van Den Nest, W. Yuval, S. Albericio, F. J. Pept. Sci. 2001, 7, 115.(3) Colombo, R. Colombo, F. J. Chem. Soc., Chem. Commun. 1984, 0, 292 – 293. Mergler, M. Dick, F. Sax, B. Schwindling, J. Vorherr, Th. J. Pept. Sci. 2001, 7, 502 – 510.(4) Okada, Y. Wang, J. Yamatot, T. Mu, Y. Yokoi, T. J. Chem. Soc., Perkin Trans. 1 1996, 17, 2139 – 2143.(5) Hibino, H. Nishiuchi, Y. Tetrahedron Lett. 2011, 52, 4947 – 4949.Hibino, H. Miki, Y. Nishiuchi, Y. J. Pept Sci. 2012, 18, 763 – 769.(6) Suppliers: EMD/Sigma-Aldrich = $1338 per 5g bottle Peptide Institute = $400.5 per 5gbottle.(7) Clouet. A Darbre, T. Reymond, J. L. Biopolymers, 2006, 84, 114.(8) Collins, J. M. Porter, K. A. Singh, S. K. Vanier, G. S. Org. Lett. 2014, 16, 940 – 943.(9) Patent: US20160176918(10) CEM Application Note (AP0124). “CarboMAX – Enhanced Peptide Coupling at Elevated Temperature.”(11) Sieber, P. Riniker, B. Tetrehedron Lett. 1987, 28, 6031 –6034.(12) Tickler, A. K Clippingdale, A. B Wade, J. D. Protein Peptide Lett. 2004, 11, 377 – 384.(13) Bacem Application Note. Mergler, M. Dick, F. Vorherr, Th. Methods for Fmoc-His(Trt)-OH Resulting in Minimal Racemization.(14) CEM Technical Note (P/N: 600837) - “Cl-MPA ProTide and Cl-TCP(Cl) ProTide Resin Loading and Protected Cleavage Procedures.