我们原来采用的吡啶-巴比土酸测定水中氰化物,但是由于《生活饮用水卫生规范》已经作废,新的GB/T 5750-2006中已经没有对应的检测方法,所以转换为异烟酸-巴比土酸法测定氰化物。但是在试验过程中碰到了问题,按照标准方法进行校准曲线的绘制中,在最后一步加完异烟酸-巴比土酸后放置15分钟时,必然会发生浑浊,导致无法比色,经多方查找原因也无法解决问题,在此求教各位了。
异烟酸-巴比妥酸(硫代巴比妥酸)显色体系分析应用研究[align=center]十月[/align]巴比妥酸([color=#333333]barbituric acid,[/color]BA)和硫代紫尿酸(thivioluric acid,TVA)是两种应用广泛的[color=#222222]化学分析试剂或生化试剂,在氯胺T存在下,BA和TBA分别与异烟酸联用,可[/color]应用于尿液中硫氰酸盐和水中氰化物的测定。本文就异烟酸-巴比妥酸和异烟酸-硫代巴比妥酸显色体系分析应用情况总结分析于下。异烟酸-巴比妥酸显色体系光度测定尿液中硫氰酸盐[sup][1][/sup]。[color=#666666]在弱酸性介质中及氯胺T存在条件下,SCN[/color][sup][color=#666666]-[/color][/sup][color=#666666]可与异烟酸-巴比妥酸形成一紫蓝色染料,该染料最大吸收波长位于598 nm,表观摩尔吸光系数ε=1.19×10[/color][sup][color=#666666]5[/color][/sup][color=#666666]Lmol[/color][sup][color=#666666]-1[/color][/sup][color=#666666]cm[/color][sup][color=#666666]-1[/color][/sup][color=#666666],且其吸光度A与SCN[/color][sup][color=#666666]-[/color][/sup][color=#666666]含量在0~2.50μg/5.0 mL范围内呈良好的线性关系,建立了测定人尿中微量SCN[/color][sup][color=#666666]-[/color][/sup][color=#666666]的异烟酸-巴比妥酸分光光度法。方法用于生人尿中微量SCN[/color][sup][color=#666666]-[/color][/sup][color=#666666]的测定,其结果与国家标准方法(吡啶-巴比妥酸分光光度法)[/color][sup][2][/sup][color=#666666]相吻合,加标回收率在90~104%,方法最低检出浓度为0.50mg/L。[/color]2、[color=#222222]异烟酸-硫代巴比妥酸[/color]显色体系光度测定水中氰化物[sup][3][/sup]。在弱酸性介质中及氯胺T存在条件下,CN[sup]-[/sup]可与异烟酸-硫代巴比妥酸形成一红-蓝色染料,该染料分别在525 nm和642nm各有一个吸收峰,且其吸光度A[sub]525[/sub]和A[sub]642[/sub]及其二者之和A[sub]525+642[/sub]均与CN[sup]-[/sup]含量在一定的范围内呈良好的线性关系,建立了测定生活饮用水中微量CN[sup]-[/sup]的异烟酸-硫代巴比妥酸分光光度法,本法CN[sup]-[/sup]含量均在0~4.0ug/10.0ml范围内符合比耳定律,方法用于生活饮用水中微量CN[sup]-[/sup]的测定,加标回收率在94%~106%。3、[color=#333333]异烟酸-硫代巴比妥酸-CTMAB显色体系[/color]光度测定水中氰化物[sup][4][/sup]。[color=#666666]在弱酸性介质中,有溴化十六烷基三甲铵(CTMAB)存在条件 下,CN-与异烟酸-硫代巴比妥酸形成一蓝色化合物,其最大吸收波长(λmax)位于646 nm,表观摩尔吸光系数ε[/color][sub][color=#666666]646[/color][/sub][color=#666666]=4.67×10[/color][sup][color=#666666]4[/color][/sup][color=#666666]Lmol[/color][sup][color=#666666]-1[/color][/sup][color=#666666]cm[/color][sup][color=#666666]-1[/color][/sup][color=#666666],灵敏度比二元体系提高了39%,且其吸光度A与氰化物含量在一定的范围内呈良好的线性关系。建立了测定生活饮用水中微量氰化物的CTMAB-异烟酸-硫代巴比妥酸显色光度法。本法氰化物含量在0~4.0μg/10.0 mL范围内符合比耳定律,用于生活饮用水中微量氰化物的测定,其结果与国家标准方法(异烟酸-巴比妥酸分光光度法)[/color][sup][5][/sup][color=#666666]相吻合,[/color]方法的选择性、稳定性和灵敏度均令人满意。4、[color=#333333]异烟酸-硫代巴比妥酸-CTMAB显色体系[/color]光度测定尿液中的硫氰酸盐[sup][6][/sup]。[color=#666666]在弱酸性介质中及溴化十六烷基三甲铵(CTMAB)和氯胺T存在条件下,硫氰酸盐(SCN[/color][sup][color=#666666]-[/color][/sup][color=#666666])与异烟酸-硫代巴比妥酸形成一蓝绿色染料,其最大吸收波长位于648 nm,ε=4.30×10[/color][sup][color=#666666]4[/color][/sup][color=#666666] Lmol[/color][sup][color=#666666]-1[/color][/sup][color=#666666]cm[/color][sup][color=#666666]-1[/color][/sup][color=#666666],且其吸光度A与SCN[/color][sup][color=#666666]-[/color][/sup][color=#666666]含量在一定的范围内呈良好的线性关系,建立了测定人尿中微量SCN-的异烟酸-硫代巴比妥酸-CTMAB显色光度法,本法SCN[/color][sup][color=#666666]-[/color][/sup][color=#666666]含量在0~6.0μg/5.0 mL范围内符合比耳定律,方法用于人尿中微量SCN[/color][sup][color=#666666]-[/color][/sup][color=#666666]的测定,结果令人满意。[/color]参考文献黄选忠,汪,波,舒开继,等. 异烟酸-巴比妥酸分光光度法测定尿硫氰酸盐[J]. 山东化工,2019,48(20):106-107,112中华人民共和国卫生部.中华人民共和国卫生行业标准 尿中硫氰酸盐的吡啶-巴比妥酸分光光度测定方法 WS/T 39-1996[s].北京:中国标准出版社,1996黄选忠,甘发清,徐留森.[color=#222222]CN[/color][sup][color=#222222]-[/color][/sup][color=#222222]-异烟酸-硫代巴比妥酸显色反应的研究及应用[/color][J].分析科学学报, 2007, 23(3):361-363中华人民共和国卫生部,国家标准化管理委员会. 中华人民共和国国家标准 生活饮用水标准检验方法.无机非金属GB5750.5-2006[s].北京:中国标准出版社,20065)黄选忠,汪 波,郑 凌.[color=#333333]CN[/color][sup][color=#333333]-[/color][/sup][color=#333333]-异烟酸-硫代巴比妥酸-CTMAB显色体系的研究及应用[/color][J].分析科学学报,2008,24(3):370-3726)舒开继,黄选忠,杜宏山.在CTMAB存在下,异烟酸-硫代巴比妥酸显色光度法测定尿液中硫氰酸盐[J].山东化工, 2021,50(16):137-138.[/s][/s]
做标准曲线 加入异烟酸-巴比妥酸显色剂出现絮状物 干扰显色。 个人觉得可能是巴比妥酸的问题,因为我之前做的时候用的的 无结晶水的巴比妥酸,显色正常。那瓶用完后重新购置一瓶含两个结晶水的巴比妥酸,换算后加入标系显色就出现絮状物了。联系本地试剂供应商说没有无水的巴比妥酸,现在郁闷了。 请问各位大虾,你们做的时候有没有出现这个问题? 你们怀疑是什么地方出问题了? 怎么解决的 ? 顺便请问哪里有 无水的巴比妥酸可买 ,谢谢各位了
国标HJ484-2009异烟酸巴比妥酸法测氰化物,异烟酸巴比妥酸显色剂和氯胺T用时现配,配完没用完第二天能继续用吗?磷酸二氢钾缓冲溶液,并没有用无水磷酸二氢钾配,用的磷酸二氢钾,有影响吗?
大家好,我在实验室用异烟酸-巴比妥酸这个方法做总氰化物的测定,现在很多厂家都不出售无水巴比妥酸了,很多都是二水的,请问各位知道哪里有的买啊?谢谢,
氰化物测定时 按附件第四篇吡啶巴比妥酸比色时 发现结果没颜色 而按异烟酸巴比妥酸显色的话 结果颜色就很好 吡啶巴比妥酸比色流程是 :氰化钠+0.1%氢氧化钠到10ml,加1滴酚酞,用盐酸调到无色,加缓冲剂5ml,摇匀,迅速加氯胺T0.2ml,摇匀,等3min,加吡啶巴比妥酸溶液5ml,定容,40度水浴20min,然后上机。异烟酸巴比妥酸比色流程是 :氰化钠+0.1%氢氧化钠到10ml,加缓冲剂5ml,摇匀,迅速加氯胺T0.2ml,摇匀,加异烟酸巴比妥酸溶液5ml,定容。这个立马有颜色出来。各位大侠帮忙分析下,这里哪个环节出问题了
请高手指点 做氰化物时1、异烟酸-巴比妥酸溶液如何配制?我先把异烟酸和巴比妥酸称好,混在一起,加氢氧化钠溶液,结果成糊状,水浴溶解长了,溶液变成黄褐色,不知如何解决?2、蒸馏加硝酸锌产生沉淀,这现象对不对?蒸馏结束后溶液颜色变白,不是红色,对结果有什么影响?多谢!
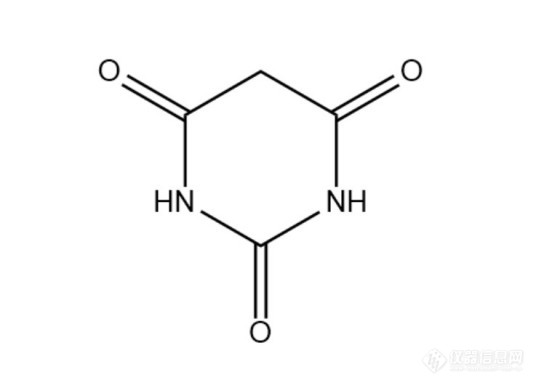
巴比妥酸-亚硝酸盐显色体系分析应用研究[align=center]十月[/align]巴比妥酸([color=#333333]barbituric acid,[/color]BA)又称丙二酰脲或2,4,6-嘧啶三酮,[font=arial][color=#333333]化学式为C?H?N?O?,[/color][/font]其结构式见图1,BA可用作[color=#222222]化学分析或生化试剂在实验室被广泛应用,[/color]曾应用于尿液中硫氰酸[align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/08/202308011034128631_7790_3127170_3.jpg[/img][/align][align=center]图1 巴比妥酸的结构式[/align]盐(吡啶-巴比妥酸分光光度法和异烟酸-巴比妥酸分光光度法)[sup][1-2][/sup]、车间空气中吡啶[sup][3][/sup]和水中氰化物(异烟酸-巴比妥酸分光光度法和流动注射法)[sup][4][/sup]测定。BA也可与亚硝酸盐(NO[sub]2[/sub][sup]-[/sup])发生反应生成紫红色的紫尿酸(violuric acid,VA),VA进而与铁(Ⅱ)、钴(Ⅱ)反应形成蓝色和黄色配阴离子而应用于铁、钴和巴比妥酸的测定。本文就巴比妥酸—亚硝酸盐(NO[sub]2[/sub][sup]-[/sup])显色体系分析应用情况总结分析于下。1、铁(Ⅱ)-巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色体系分光光度法测定铁[sup][5][/sup]。在碱性介质中,铁(Ⅱ)与巴比妥酸-NO[sub]2[/sub][sup]-[/sup]体系发生显色反应形成一种蓝色配阴离子,该配阴离子的最大吸收波长(λmax)位于630nm,其摩尔吸光系数(ε)为1.86×104 L/(molcm),且其吸光度与铁(Ⅱ)的质量浓度在0~50μg/25mL范围内符合比尔定律,方法检测限为30μg/L,方法应用于水样中微量铁的测定获得了满意的结果。2、铁(Ⅱ)-巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色体系树脂相分光光度法测定水中微量铁[sup][6][/sup]。在碱性介质中,铁(Ⅱ)与巴比妥酸( BA )-NO[sub]2[/sub][sup]-[/sup]体系反应形成一种稳定的兰色配阴离子,其最大吸收波长位于635 nm处,该配阴离子能被阴离子交换树脂完全吸附,且树脂相在635 nm处的吸光度与铁含量在0~25μg/25 mL的范围内呈良好的线性关系,方法应用于水样中微量铁的测定,其结果与[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法相吻合,加标回收率为96%~102%,相对标准偏差(RSD)小于5.0%(n=5)。3、铁(Ⅱ)、钴(Ⅱ)-巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色体系分光光度法同时测定微量铁和钴[sup][7][/sup]。[align=center]在碱性介质中,铁(Ⅱ)和钴(Ⅱ)可与巴比妥酸(BA)-NO[sub]2[/sub][sup]-[/sup]体系反应,分别形成一种稳定的兰色和黄色配合物,铁(Ⅱ)配合物分别在波长630 nm和350 nm具有吸收峰,钴(Ⅱ)配合物只有一个吸收峰位于365 nm波长处(见图2),体系的吸光度AFe630,AFe365和ACo365与铁、钴[/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/08/202308011034130370_236_3127170_3.png[/img][/align][size=12px]波长[/size][font=times new roman][size=12px] λ/nm[/size][/font] [font=仿宋_gb2312] [/font][font=仿宋_gb2312] [/font][font=宋体][size=12px]图2 吸收光谱[/size][/font][align=center] 1:试剂空白(水参比) [/align][align=center] 2: Fe(Ⅱ)-BA-NO[sub]2[/sub][sup]-[/sup]体系(试剂空白参比)[/align][align=center] 3:Co(Ⅱ)-BA-NO[sub]2[/sub][sup]-[/sup]体系(试剂空白参比)[/align]含量在一定的范围内呈良好的线性关系,且铁(Ⅱ)和钴(Ⅱ)配合物在365 nm波长处的吸光度具有良好的加和性,建立了一种同时测定微量铁和钴的分析方法。方法的线性范围均为0~50μg/25mL,应用于水样中微量铁和钴的同时测定,其结果分别与[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法和亚硝基R盐光度法相吻合,加标回收率分别为98%~102%和96%~104%,相对标准偏差(RSD)分别为1.8%~3.9%和2.1%~4.3%(n=5)。4、巴比妥酸-NO[sub]2[/sub][sup]-[/sup]-铁(Ⅱ)-CPB显色体系光度测定巴比妥酸[sup][8][/sup]。对巴比妥酸-NO[sub]2[/sub][sup]-[/sup]-铁(Ⅱ)-CPB显色体系进行了研究,建立了一种测定巴比妥酸的分光光度法,该方法巴比妥酸含量在1.0×10[sup]-6[/sup]~2.0×10[sup]-5[/sup]g/mL范围内符合比尔定律。方法简便,快速且具有良好的选择性及重现性,用于巴比妥类药物合成样中巴比妥酸的测定,回收率在90.2%~102.1%。参考文献中华人民共和国卫生部.中华人民共和国卫生行业标准 尿中硫氰酸盐的吡啶-巴比妥酸分光光度测定方法 WS/T 39-1996[s].北京:中国标准出版社,1996黄选忠,汪,波,舒开继,等. 异烟酸-巴比妥酸分光光度法测定尿硫氰酸盐[J]. 山东化工,2019,48(20):106-107,1123)国家技术监督局,中华人民共和国卫生部.中华人民共和国国家标准 [color=#333333]车间空气中吡啶的巴比妥酸分光光度测定方法 GB/T 16116-1995[/color][s].北京:中国标准出版社,19954)国家市场监督管理总局,国家标准化管理委员会. 中华人民共和国国家标准 生活饮用水卫生标准检验方法:第5部分:无机非金属指标GB/T5750.5-2023[s].北京:中国标准出版社,20235)黄选忠.铁(Ⅱ)-巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色反应的研究及应用[J].化学分析计量, 1996, 5(2):31-32,486)彭兰,黄维红,鄢丽华,等. 树脂相分光光度法测定水中微量铁[J]. 化学分析计量,2011, 20(6):80-827)黄选忠,吕全勇,杜宏山,等.铁(Ⅱ)和钴(Ⅱ)与巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色反应的研究及应用[J].分析科学学报, 2011, 27(1):93-968)黄选忠,郑林.巴比妥酸-NO[sub]2[/sub][sup]-[/sup]-铁(Ⅱ)-CPB显色体系光度测定巴比妥酸的研究[J].分析科学学报, 1999, 15(3):238-241[/s][/s][/s]
按照GB/T 5750.10-2006异烟酸-巴比妥酸法测氯化氰曲线不显色。所有试剂加完后水样不显色,无色透明,无浑浊。氰化物标液是中国计量院的,50mg/L,巴比妥酸国药的,进口的都试过。pH值也调过,还是不显色。是pH的问题,氯胺T的问题,还是显色剂的问题?流动注射用的测氰化物的曲线、试剂也试过,也不显色。和流动注射唯一的区别就是蒸馏了。弄不明白究竟哪里出了问题。
求助,加入标液后,加入2ml磷酸盐缓冲溶液,再加0.25ml氯胺T,过2分钟后加入4ml异烟酸巴比妥酸(1.2g氢氧化钠 1g异烟酸 1g巴比妥酸 用纯水定容100ml) 之后定容至25ml刻度线 问题是溶液由红变篮紫 不久就慢慢颜色淡了。
正在准备考核氰化物 新购入异烟酸和巴比妥酸 在60度NAOH中溶解 但是还是出现沉淀 ~~~冷却后 在标准和样品中加入该显色剂 尽然出现絮状沉淀......这可如何是好啊!!!???
求助各位:为何做水中氰化物,方法是异烟酸-巴比妥酸分光光度法,标准会出现混浊?而且样品管也出现了浑浊,试剂差不多都是新买的,那个巴比妥酸是二水的,应该不会影响结果吧!
按照“工作场所无机含氮化合物的测定”标准,用异烟酸-巴比妥酸法测定氰化物,为什么加入显色剂后标曲全部都不显色?已经做了2次还是这样的结果,每次也都是严格按照标准来做的,不知到底是哪里出了问题?求高手指点,谢谢!
异烟酸-巴比妥酸分光光度法测氰化物的质量控制 实验中有什么干扰?怎样去除?http://simg.instrument.com.cn/bbs/images/brow/em09511.gif
我按照吡啶-巴比妥酸分光光度法测试,严格按照标准操作,每次加完试剂及时盖好盖子摇匀而且很迅速。各浓度点及吸光值分别如下:线性方 程:吸光度=2.78987XC-0.00175。线性:0.98352。本人第一次操作,请各位大侠指点需要注意哪些点?浓度 (PPM) 吸光度0 0.00020.008 0.02030.020 0.05170.040 0.10420.080 0.20630.120 0.34060.160 0.50000.200 0.5148
求助!请问国标异烟酸巴比妥酸法里的酚酞是要全部用95%乙醇稀释,还是用一半95%乙醇一半纯水一起稀释定容?最后一步需要用纯水定容至25ml吗?还有最后一步需要水浴25°显色15分钟吗?谢谢!
我在做氰化物曲线时,所有试剂加完是有颜色显示的,开始时加深的,等过了10分钟之后颜色越变越浅,测定时吸光值也是一直在下降,最后颜色都褪为无色了。之前做的即使放很久颜色还是不会褪的,而且褪色本身就不合逻辑。巴比妥酸是新买的,其他均与之前所用试剂相同。请各位大侠帮我分析一下到底是哪里出了问题??是试剂的问题吗?

[align=center][b]异烟酸-巴比妥酸分光光度法测定尿硫氰酸盐[/b][/align][align=center][b]黄选忠[sup]*[/sup] [/b][/align][align=center][b](湖北兴山县疾病预防控制中心,443711)[/b][/align][b]摘要 [/b] 在弱酸性介质中及氯胺T存在条件下,SCN[sup]-[/sup]可与异烟酸-巴比妥酸形成一紫蓝色染料,该染料最大吸收波长位于598nm,且其吸光度A与SCN[sup]-[/sup]含量在一定的范围内呈良好的线性关系,据此我们建立了测定人尿中微量SCN[sup]-[/sup]的异烟酸-巴比妥酸分光光度法,本法SCN[sup]-[/sup]含量均在0~2.50μg/5.0mL范围内符合比耳定律,方法用于人尿中微量SCN[sup]-[/sup]的测定,结果令人满意。[b]关键词[/b] 硫氰酸盐 分光光度法 异烟酸 巴比妥酸[b]中图分类号[/b]:O657.3硫氰酸盐(SCN[sup]-[/sup])是致甲状腺肿物质,可阻滞甲状腺激素合成,引起甲状腺肿,因此监测人血、尿等标本中的SCN[sup]-[/sup]含量具有重要意义。同时尿中SCN[sup]-[/sup]含量也是接触氰化物的一项生物接触指标[sup][/sup],目前,测定尿中微量SCN[sup]-[/sup]的方法主要有分光光度法、[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[sup][/sup]、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[sup][/sup]等,其中[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法均需要专门仪器,且耗时较长。分光光度法以其简便灵敏、设备简单而被广泛采用。已报道的分光光度法主要有异烟酸-吡唑啉酮光度法[sup][/sup]、吡啶-巴比妥酸光度法[sup][/sup](为国家卫生行业标准方法)、三氯化铁显色光度法等[sup][/sup],其中吡啶-巴比妥酸法和三氯化铁法的灵敏度较低,且所用吡啶有恶臭,有损于分析人员的健康,使其应用受到影响。异烟酸-巴比妥酸光度法已应用于生活饮用水微量氰化物的测定[sup][/sup],但应用于人尿中微量SCN[sup]-[/sup]的测定似未见报道。我们对异烟酸-巴比妥酸光度法比妥酸光度法测定人尿中微量SCN[sup]-[/sup]进行了研究,结果表明,在弱酸性介[u] [/u]*黄选忠,男,1962-10,主任技师,主要研究方向:卫生化学检验技术。工作单位:兴山县疾病预防控制中心,联系电话:13872688318,E-mail:xscdchxz@sina.com)质中,氯胺T可将SCN[sup]-[/sup]转化成氯化氰(CNCl),CNCl再与异烟酸-巴比妥酸形成一紫蓝色染料,该染料的最大吸收波长(λ[sub]max[/sub])位于598nm,其表观摩尔吸光系数ε达1.19×10[sup]5[/sup]Lmol[sup]-1[/sup]cm[sup]-1[/sup],且其吸光度与SCN[sup]-[/sup]含量在一定的范围内呈良好的线性关系(r0.9996),据此建立了测定人尿中微量SCN[sup]-[/sup]的异烟酸-巴比妥酸分光光度法,该法SCN[sup]-[/sup]含量在0~2.50μg/5.0mL范围内符合比耳定律,方法用于人尿中微量SCN[sup]-[/sup]的测定,其结果与国家行业标准方法相吻合,加标回收率在90%~104%,方法的选择性、稳定性和灵敏度均令人满意。[b]1 实验部分 1.1主要仪器及试剂[/b]TU-1810SPC紫外可见分光光度计(北京普析通用仪器有限公司);SCN[sup]-[/sup]标准溶液:1.0mg/mL的标准储备液,按文献的方法配制。临用时稀释成1.0μg/mL(A液)和5.0μg/mL(B液)的标准应用液;1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]缓冲溶液:pH≈4.67[sup][/sup];异烟酸-巴比妥酸(含二个水分子)溶液:称取0.615g异烟酸和1.025g巴比妥酸(含二个水分子)加入1.0mol/L的NaOH溶液12~13mL,搅拌使其溶解后补充纯水至100 mL(此溶液pH为近中性,其浓度分别为0.05mol/L和0.063mol/L);0.044 mol/L的氯胺T溶液(临用时配制);以上试剂为AR级,实验用水为超纯水(18.25ΜΩcm)。[b]1.2实验方法[/b]1.2.1标准曲线的绘制:取SCN[sup]-[/sup]标准应用A液(1.0μg/mL )0、0.20、0.50mL和B液0.20、0.30、0.40和0.50mL于10 mL比色管中,补充纯水至0.80mL,加入1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]缓冲溶液2.0 mL、氯胺T溶液0.25 mL混匀,放置3min,加入异烟酸-巴比妥酸溶液2.0mL混匀,放置20-25min,以试剂空白为参比用1cm比色皿于598nm处测定各管吸光度A,以SCN[sup]-[/sup]含量对A绘制标准曲线。1.2.2尿样分析:取新鲜尿液0.10mL(SCN[sup]-[/sup]≤2.5μg)按实验方法1.2.1操作测定吸光度,以标准曲线法进行SCN[sup]-[/sup]定量,同时进行标准方法[sup][/sup]对照分析及加标回收实验。[b]2 结果与讨论2.1吸收光谱[/b]在本试验条件下,SCN[sup]-[/sup]与异烟酸-巴比妥酸形成一紫蓝色染料, 该染料的λ[sub]max[/sub]位于598 nm,而相应试剂空白在500-700nm基本无吸收,见图1。[b]2.2pH值的影响、缓冲溶液的选择及用量[/b][align=center][img=,384,268]https://ng1.17img.cn/bbsfiles/images/2019/09/201909161110577563_8288_3237657_3.png!w384x268.jpg[/img][/align][align=center]图1 吸收光谱[/align][align=center] 曲线1、2:分别为0.4和0.8μgSCN[sup]-[/sup]显色液(对试剂空白)[/align]试验结果表明,pH值对该显色体系的影响主要在SCN[sup]-[/sup]转化成CNCl的这一阶段,对后续显色阶段的影响相对较小,且溶液pH值在4.5~5.7的KH[sub]2[/sub]PO[sub]4[/sub]/Na[sub]2[/sub]HPO[sub]4[/sub](1/15mol/L)[sup][/sup]缓冲介质中体系有最大稳定的吸光度,同时对柠檬酸钠/盐酸(pH=5.25)、醋酸钠/盐酸(pH=4.58)、1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液(pH≈4.67)和KH[sub]2[/sub]PO[sub]4[/sub]/Na[sub]2[/sub]HPO[sub]4[/sub](1/15mol/L ,pH=5.29)等缓冲体系的进行了试验,结果表明,用柠檬酸钠/盐酸、醋酸钠/盐酸两种缓冲体系不仅吸光度偏低,且尿样加标回收率也偏低,用KH[sub]2[/sub]PO[sub]4[/sub]/Na[sub]2[/sub]HPO[sub]4[/sub]缓冲体系虽然体系可达最大吸光度,但尿样加标回收率偏低,而用1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液时,体系可达最大吸光度且尿样加标回收率较高这可能与尿样的基体干扰有关,当1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液的加入抵消了尿样的基体干扰,试验选用1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液控制显色体系酸度及离子强度,其用量在1.5-2.5 mL时体系有最大稳定的吸光度,试验选用2.0 mL[b]2.3氯化氰转化时间及氯胺T溶液用量的影响[/b]本试验条件下,SCN[sup]-[/sup]转化成CNCl的时间在2~5min ,0.044mol/L的氯胺T溶液用量在0.20~0.30 mL体系有最大稳定的吸光度,试验分别选用3min 和0.25mL。[b]2.4异烟酸和硫代巴比妥酸溶液用量的影响[/b]试验表明,0.10 mol/L的异烟酸和巴比妥酸溶液用量分别在0.50~1.50mL和 1.0~1.50 mL体系有最大稳定的吸光度,试验分别选用1.0 mL和1.25mL。[b]2.5异烟酸和巴比妥酸溶液混合加入实验[/b]试验表明,将异烟酸和巴比妥酸分别以0.05mol/L和0.063mol/L的浓度配成混合溶液一次加入2.0mL,可使体系吸光度提高20%以上,且提高了工作效率。[b]2.6共存物质的影响[/b]在本试验条件下,CN[sup]-[/sup]与SCN[sup]-[/sup]可发生相同显色反应而产生正干扰,但正常尿液中CN[sup]-[/sup]的含量较低,其影响可忽略。但考虑到尿液的成分较复杂,其中含量较大的物质(主要有尿素、氯化物、硫酸盐、磷酸氢盐、肌酐和铵离子等)可能因基体效应(较大的离子强度)对体系的显色反应产生影响,这在结果与讨论部分2.2结果中得到印证。为考察基体效应对体系显色反应的影响,按照尿液正常成分[sup][/sup]配制成含尿素(20g/L)、Cl[sup]-[/sup](13g/L)、Na[sup]+[/sup](9g/L),HPO[sub]4[/sub][sup]2-[/sup]、SO[sub]4[/sub][sup]2-[/sup](2.0g/L)、肌酐(1.4g/L)、NH[sub]4[/sub][sup]+[/sup](0.93 g/L)的尿液对照液,取0.10-0.30 mL尿液对照液加入1.0μg SCN[sup]-[/sup]测定吸光度,结果表明,至少三倍于尿样中的上述成分对1.0μg SCN[sup]-[/sup]的测定结果基本无影响(吸光度误差在±5%范围内),可见方法的选择性良好。[b]2.7标准曲线[/b]本法SCN[sup]-[/sup]含量在0~2.50μg/5.0mL范围内符合比耳定律(标准色阶见图2),标准曲线的回归方程及由曲线斜率法求得的表观摩尔吸光系数为:A=0.4118C[sub](SCN-,[/sub][sub]μ[/sub][sub]g[/sub][sub])[/sub]-0.0086,r=0.9996,ε=1.19×10[sup]5[/sup]Lmol[sup]-1[/sup]cm[sup]-1[/sup]若以吸光度为0.01、取样量为0.10mL计,方法最低检出浓度为0.5mg/L。[b][/b][align=center][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2019/09/201909161111153203_545_3237657_3.jpg!w690x517.jpg[/img][/align][align=center]图2 0~2.50μg SCN[sup]-[/sup]/5.0mL的标准色阶[/align][b]2.8呈色稳定性[/b]在本试验条件下,SCN[sup]-[/sup]与异烟酸-巴比妥酸形成蓝色染料,其吸光度在20-25min达稳定最大值且至少再1h内基本稳定(吸光度变化值小于5%)。[b]2.9 重复性实验[/b]分别对0.20、0.50和2.00 μg SCN[sup]-[/sup]标准液平行测定5次,测定结果见表1,从表1可见,三水平测定结果的相对标准偏差(RSD)分别为2.98%、1.97%和1.06%,表明方法的重复性良好。[align=center][b]表1 重复性试验结果[/b][/align] [table=469][tr][td] [align=center]SCN[sup]-[/sup][/align] [/td][td] [align=center]测定值/[/align] [/td][td] [align=center]平均值/[/align] [/td][td] [align=center]RSD/[/align] [/td][/tr][tr][td] [align=center](μg )[/align] [/td][td] [align=center](A)[/align] [/td][td] [align=center](A)[/align] [/td][td] [align=center]%[/align] [/td][/tr][tr][td] [align=center]0.20[/align] [/td][td] [align=center]0.072,0.074,0.075,0.076,0.078[/align] [/td][td] [align=center]0.075[/align] [/td][td] [align=center]2.98[/align] [/td][/tr][tr][td] [align=center]0.50[/align] [/td][td] [align=center]0.178,0.182,0.183,0.184,0.188[/align] [/td][td] [align=center]0.183[/align] [/td][td] [align=center]1.97[/align] [/td][/tr][tr][td] [align=center]2.00[/align] [/td][td] [align=center]0.807,0.815,0.819,0.824,0.830[/align] [/td][td] [align=center]0.819[/align] [/td][td] [align=center]1.06[/align] [/td][/tr][/table][b]2.10尿样分析及回收试验结果[/b]取8份尿样按实验方法1.2.2操作测定SCN[sup]-[/sup]含量,同时用国家行业标准方法(吡啶-巴比妥酸光度法[sup][/sup])作对照分析,并进行加标回收实验,本法结果与标准方法结果相吻合,加标回收率在90%~104%,见表2。[align=center][b]表2 尿样分析结果[/b][/align] [table=592][tr][td=1,3] [align=left]样品编号[/align] [/td][td=5,1] [align=center]本法结果[/align] [/td][td] [align=center]标准方法结果/[/align] [/td][/tr][tr][td] [align=left]测定结果/[/align] [/td][td] [align=left]本底值/[/align] [/td][td] [align=left]加入量/[/align] [/td][td] [align=left]测定量/[/align] [/td][td] [align=left]回收率/[/align] [/td][td=1,2] [align=center]μg/mL[/align] [/td][/tr][tr][td] [align=center]μg/mL[/align] [/td][td] [align=center]μg[/align] [/td][td] [align=center]μg[/align] [/td][td] [align=center]μg[/align] [/td][td] [align=center]%[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]4.41 [/align] [/td][td] [align=center]0.44[/align] [/td][td] [align=center]1.00[/align] [/td][td] [align=center]1.45[/align] [/td][td] [align=center]101[/align] [/td][td] [align=center]4.19[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]3.56 [/align] [/td][td] [align=center]0.36[/align] [/td][td] [align=center]1.50[/align] [/td][td] [align=center]1.92[/align] [/td][td] [align=center]104[/align] [/td][td] [align=center]3.35[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]8.20 [/align] [/td][td] [align=center]0.82[/align] [/td][td] [align=center]0.50[/align] [/td][td] [align=center]1.30[/align] [/td][td] [align=center]96[/align] [/td][td] [align=center]8.53[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]10.72 [/align] [/td][td] [align=center]1.07[/align] [/td][td] [align=center]0.20[/align] [/td][td] [align=center]1.25[/align] [/td][td] [align=center]90[/align] [/td][td] [align=center]10.56[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]6.72 [/align] [/td][td] [align=center]0.67[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]6.74[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]7.57 [/align] [/td][td] [align=center]0.76[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]7.72[/align] [/td][/tr][tr][td] [align=center]7[/align] [/td][td] [align=center]6.55 [/align] [/td][td] [align=center]0.66[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]6.55[/align] [/td][/tr][tr][td] [align=center]8[/align] [/td][td] [align=center]9.66 [/align] [/td][td] [align=center]0.97[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]9.53[/align] [/td][/tr][/table][b]3结语[/b] 以异烟酸-巴比妥酸为显色剂分光光度法测定微量SCN[sup]-[/sup],方法灵敏度高,选择性及重复性良好,方法操作简便,测定结果准确,所用试剂无毒无害,可用于人尿中微量SCN[sup]-[/sup]的定量分析。[b]参考文献[/b]1 中华人民共和国卫生部.GBZ209-2008职业性急性氰化物中毒诊断标准[s].北京:人民卫生出版社,2008[/s][align=left]2[color=#333333]邵国建,郭和光,余娟.[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定尿中硫氰酸盐含量研究[/color][color=#333333],浙江预防医学,2011,23(4):95-96[/color][/align][align=left][url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E9%92%9F%E8%89%AF%E5%BA%B7&option=101][color=windowtext]3[/color][color=windowtext]钟良康[/color][/url],方波.超短柱顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定尿中硫氰酸盐,[url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E4%B8%AD%E5%9B%BD%E5%8D%AB%E7%94%9F%E6%A3%80%E9%AA%8C%E6%9D%82%E5%BF%97&option=110][color=windowtext]中国卫生检验杂志[/color][/url],2005,15(5):568,628[/align][align=left]4刘晓宇,云自厚.衍生[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定人尿和唾液中微量硫氰酸根,环境与健康杂志,1994,11(3):130-131[/align]5 冯翠霞,[url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E6%9E%97%E4%B8%BD%E7%8E%B2&option=101][color=windowtext]林丽玲[/color][/url],[url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E9%BB%84%E8%BE%89%E6%B6%9B&option=101][color=windowtext]黄辉涛[/color][/url].分光光度法测定尿中硫氰酸盐的异烟酸-吡唑酮,中国职业医学,2009,36(6):501,5046 WS/T39-1996.尿中硫氰酸盐的吡啶-巴比妥酸分光光度测定方法[s].北京:中国标准出版社,19977 蔡秀丽,施逸岚,陈建忠.人尿中硫氰酸盐的快速测定方法,中国卫生检验杂志,2015,25(11):1703-1704,17078 GB/T5750.5-2006.生活饮用水标准检验方法 无机非金属指标[s].北京:中国标准出版社,2007:18-199 全国高等医学院校检验专业专科教材.无机化学.北京:中国医药科技出版社,1990:31-3310 张孙玮,汤福隆,张 泰.现代化学试剂手册第二分册化学分析试剂.北京:化学工业出版社,1987:391-39211 全国中等卫生学校试用教材.临床检验.成都:四川人民出版社,1980:162[/s][/s][align=center][b][color=#333333]Determination of UrineThiocyanate by[/color][/b][/align][align=center][b][color=#333333]Isonicotinic acid [/color][color=#333333]-[/color] barbituric acid[color=#333333]Spectrophotometry[/color][/b][/align][b] [/b][align=center][b]HUANGXuan-zhong WANG Bo SHU Kai-ji ZOU Shao-xian[/b][/align][b] [/b]([b][i]Prevention andHealth Protection Centre of Xingshan County,Hubei,[/i]443711[/b],[b]china)Abstract: [/b]In a weakly acidic solution,and in the presence of chloramine T,[color=#333333]thiocyanate[/color] reacts with iso nicotinicacid -barbituric acid to form purple blue dye.The absorption peck of dye lies 598nm,andits apparent absorptivity is 1.19×10[sup]5[/sup]L· mol[sup]-1[/sup]· cm[sup]-1[/sup],a newspectrophotometry for determination of [color=#333333]thiocyanate[/color]was established.Beer's law is obeyed for[color=#333333]thiocyanate[/color] in the range of 0~2.50μg /5.0mL.The method shows satisfactory selectivity and precisionand has been applied to determine [color=#333333]thiocyanate[/color]in human urine with satisfactory results.[b]Keywords:[/b] [color=#333333]Thiocyanate[/color];Spectrophotometry[b];[/b]Iso Nicotinic Acid;Barbituric Acid

[align=center][b]SCN[sup]-[/sup]-异烟酸-硫代巴比妥酸- CTMAB显色体系的研究及应用[/b][/align][align=center]黄选忠 [/align][align=center](湖北兴山县疾病预防控制中心,443711)[/align][b]摘要 [/b] 在弱酸性介质中及溴化十六烷基三甲铵(CTMAB)和氯胺T存在条件下,硫氰酸盐(SCN[sup]-[/sup])与异烟酸-硫代巴比妥酸形成一蓝绿色染料,其最大吸收波长位于648nm,ε=4.30×10[sup]4[/sup]Lmol[sup]-1[/sup]cm[sup]-1[/sup],且其吸光度A与SCN[sup]-[/sup]含量在一定的范围内呈良好的线性关系,建立了测定人尿中微量SCN[sup]-[/sup]的异烟酸-硫代巴比妥酸- CTMAB显色光度法,本法SCN[sup]-[/sup]含量在0~6.0μg/5.0mL范围内符合比耳定律,方法用于人尿中微量SCN[sup]-[/sup]的测定,结果令人满意。[b]关键词[/b] 硫氰酸盐 CTMAB 分光光度法 异烟酸 硫代巴比妥酸[b]中图分类号[/b]:O657.3硫氰酸盐(SCN[sup]-[/sup])是致甲状腺肿物质,可阻滞甲状腺激素合成,引起甲状腺肿,因此监测人血、尿等标本中的SCN[sup]-[/sup]含量具有重要意义。同时尿中SCN[sup]-[/sup]含量也是接触氰化物的一项生物接触指标[sup][/sup],目前,测定尿中微量SCN[sup]-[/sup]的方法主要有分光光度法、[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[sup][/sup]、顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[sup][/sup]、衍生[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法[sup][/sup]等,其中[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法和[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法均需要专门仪器,且耗时较长。分光光度法以其简便灵敏、设备简单而被广泛采用。已报道的分光光度法主要有异烟酸-吡唑啉酮光度法[sup][/sup]、吡啶-巴比妥酸光度法[sup][/sup]、三氯化铁显色光度法[sup][/sup]等,其中后两种方法的灵敏度较低,且所用吡啶[color=#333333]有强烈刺激性及[/color]恶臭,[color=#333333]能麻醉[/color][url=https://baike.so.com/doc/433193-458687.html]中枢神经系统[/url],有损分析人员的健康,使其应用受到影响。异烟酸-硫代巴比妥酸-CTMAB显色光度法曾成功测定了饮用水中微量氰化物[sup][/sup],但应用于人尿中微量SCN[sup]-[/sup]的测定似未见报道。我们对异烟酸-硫代巴比妥酸-CTMAB显色体系光度测定人尿中微量SCN[sup]-[/sup]进行了研究,结果表明,在弱酸性介质中,氯胺T将SCN[sup]-[/sup]转化成氯化氰(CNCl),CNCl再与异烟酸-硫代巴比妥酸形成一蓝绿色染料,该染料的最大吸收波长(λ[sub]max[/sub])位于643nm,当有CTMAB存在时,该染料的λ[sub]max[/sub]红移至648nm,其表观摩尔吸光系数(ε)也从3.26×10[sup]4[/sup]Lmol[sup]-1[/sup]cm[sup]-1[/sup]提高到4.30×10[sup]4[/sup]Lmol[sup]-1[/sup]cm[sup]-1[/sup],增幅达30%以上,且其吸光度与SCN[sup]-[/sup]含量在一定的范围内呈良好的线性关系(r0.9997),建立了测定人尿中微量SCN[sup]-[/sup]的异烟酸-硫代巴比妥酸-CTMAB显色光度法,该法SCN[sup]-[/sup]含量在0~6.0μg/5.0mL范围内符合比耳定律,方法用于人尿中微量SCN[sup]-[/sup]的测定,其结果与国家行业标准方法相吻合,加标回收率在96%~102.5%,方法的选择性、稳定性和灵敏度均令人满意。[b]1 实验部分1.1主要仪器及试剂[/b]TU-1810SPC紫外可见分光光度计(北京普析通用仪器有限公司);SCN[sup]-[/sup]标准溶液:1.0mg/mL的标准储备液,按文献的方法配制。临用时稀释成1.0μg/mL(A液)和10.0μg/mL(B液)的标准应用液;1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]缓冲溶液:pH≈4.67[sup][/sup];异烟酸-硫代巴比妥酸溶液:称取1.23异烟酸和1.08g硫代巴比妥酸加入少量纯水和1.0mol/L的NaOH溶液16~17mL,搅拌使其溶解后补充纯水至100 mL(此溶液pH为近中性,异烟酸和硫代巴比妥酸浓度分别为0.10mol/L、0.075mol/L);0.044 mol/L的氯胺T溶液(临用时配制):CTMAB溶液(含20%乙醇):0.20 mol/L。以上试剂为AR级,试验用水为超纯水(18.25ΜΩ· cm)。[b]1.2实验方法[/b]取SCN[sup]-[/sup]标准应用A液0、0.20、0.50mL和B液0.10、0.20、0.40、0.60mL及新鲜尿样0.20mL((SCN[sup]-[/sup]≤6μg))于10 mL比色管中,补充纯水至约0.5mL,加入1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]缓冲溶液2.0 mL、氯胺T溶液0.25 mL混匀,放置4min,加入异烟酸-硫代巴比妥酸溶液2.0mL混匀,加入CTMAB溶液0.20并补充纯水至5mL刻度混匀,放置28min,以试剂空白为参比用1cm比色皿于648nm处测定各管吸光度A,以SCN[sup]-[/sup]含量对A绘制标准曲线,以标准曲线法进行尿SCN[sup]-[/sup]定量。[b]2 结果与讨论2.1吸收光谱[/b]在弱酸性介质中,SCN[sup]-[/sup]与异烟酸-硫代巴比妥酸形成蓝绿色染料,其λ[sub]max[/sub]位于643nm,当加入CTMAB后,其吸光度提高30%以上,且吸收峰红移至648nm,而相应的试剂空白在500~700nm范围内无吸收峰,见图1。[align=center][img=,404,272]https://ng1.17img.cn/bbsfiles/images/2019/09/201909161057189333_5216_3237657_3.png!w404x272.jpg[/img][/align][align=center]图1 吸收光谱[/align][align=center]1. SCN[sup]-[/sup]-异烟酸-硫代巴比妥酸体系(对试剂空白)[/align][align=center]2 SCN[sup]-[/sup](1.5μg)-异烟酸-硫代巴比妥酸-CTMAB体系(对试剂空白)[/align][align=center]3 SCN[sup]-[/sup](2μg)-异烟酸-硫代巴比妥酸-CTMAB体系(对试剂空白)[/align][b]2.2酸度的影响及缓冲溶液的用量[/b]试验结果表明,pH值对该显色体系的影响主要在SCN[sup]-[/sup]转化成CNCl的这一阶段,对后续显色阶段的影响相对较小,且溶液pH值在4.49~5.29的KH[sub]2[/sub]PO[sub]4[/sub]/Na[sub]2[/sub]HPO[sub]4[/sub](0.25mol/L)[sup][/sup]缓冲介质中体系有最大稳定的吸光度,但尿样加标回收率偏低,而用1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液(pH≈4.67)时体系可达最大吸光度且尿样加标回收率较高,这可能与尿样的成分复杂产生的基体干扰有关,使用1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液可能抵消了尿样的基体干扰,试验选用1.0mol/L的KH[sub]2[/sub]PO[sub]4[/sub]溶液控制显色体系酸度,其用量在1.5-2.5 mL时体系有最大稳定的吸光度,试验选用2.0 mL。[b]2.3 SCN[sup]-[/sup]转化时间及氯胺T溶液用量的影响[/b]本试验条件下,SCN[sup]-[/sup]转化成氯化氰的时间在3~5min ,0.044 mol/L的氯胺T溶液用量在0.20~0.35 mL体系有最大稳定的吸光度,试验分别选用4min 和0.25mL。[b]2.4异烟酸和硫代巴比妥酸溶液用量的影响[/b]试验表明,异烟酸(0.20mol/L)和硫代巴比妥酸(0.15mol/L)溶液用量均在0.75~1.25mL体系有最大稳定的吸光度,试验均选用1.0mL。[b]2.5异烟酸和硫代巴比妥酸溶液混合加入试验[/b]试验表明,异烟酸和硫代巴比妥酸分别以0.10mol/L和0.075mol/L的浓度配成混合溶液一次加入2.0mL,可使体系吸光度提高20%以上,且提高了工作效率。[b]2.6 CTMAB溶液的影响及用量[/b]试验表明,适量的CTMAB可使SCN[sup]-[/sup]-异烟酸-硫代巴比妥酸显色体系的吸光度提高30%以上、体系的λ[sub]max[/sub]从643 nm红移至648nm,证明形成了新的物质。0.20mol/L的CTMAB溶液用量在0.20~0.30 mL范围内体系有最大且稳定的吸光度,实验选用0.25mL。[b]2.7呈色稳定性[/b]试验表明,SCN[sup]-[/sup]与异烟酸-硫代巴比妥酸-CTMAB显色体系的吸光度在28-30min可达最大值且至少可稳定10min。[b]2.8共存物质的影响[/b]根据本法显色机理,CN[sup]-[/sup]因与SCN[sup]-[/sup]一样,可与异烟酸-硫代巴比妥酸-CTMAB体系发生相同显色反应而产生正干扰,但正常尿液中CN[sup]-[/sup]的含量甚微,其影响可忽略。但考虑到尿液的成分较复杂,其中含量较大的物质(主要有尿素、氯化钠、硫酸盐、磷酸氢盐、肌酐和氯化铵等)可能因基体效应对体系的显色反应产生影响,这在前述2.2结果中得到印证。为考察基体效应对体系显色反应的影响,按照尿液正常成分[sup][/sup]配制成含尿素(20g/L)、Cl[sup]-[/sup](13g/L)、Na[sup]+[/sup](9g/L),HPO[sub]4[/sub][sup]2-[/sup]、SO[sub]4[/sub][sup]2-[/sup](2.0g/L)、肌酐(1.4g/L)、NH[sub]4[/sub][sup]+[/sup](0.93 g/L)的尿液对照液, 取0.20-0.40 mL尿液对照液加入2.0μg SCN[sup]-[/sup]测定吸光度,结果表明,至少二倍于尿样中的上述成分对2.0μg SCN[sup]-[/sup]的测定结果基本无影响(吸光度误差在±5%范围内),可见方法的选择性良好。[b]2.9标准曲线[/b]本法SCN[sup]-[/sup]含量在0~6.0μg/5.0ml范围内符合比耳定律(标准色阶见图2),标准曲线的回归方程及由曲线斜率法求得的ε为:A=0.1484C[sub](SCN-,[/sub][sub]μ[/sub][sub]g[/sub][sub])[/sub]-0.0029,r=0.9997,ε=4.30×10[sup]4[/sup]L· mol[sup]-1[/sup]· cm[sup]-1[/sup]本法最低检出量为0.2μg、当取样量为0.20mL时,方法最低检出浓度为1.0mg/L。[align=center][img=,690,517]https://ng1.17img.cn/bbsfiles/images/2019/09/201909161057344493_9830_3237657_3.jpg!w690x517.jpg[/img][/align][align=center]图2 0~6.0μg SCN[sup]-[/sup]/5.0ml的标准色阶[/align][b]2.10精密度实验[/b]对0.20、0.50、2.00和4.00μg SCN[sup]-[/sup]标准液平行测定5次,测定结果见表1,从表1可见,四水平测定结果的相对标准偏差(RSD)分别为4.54%、3.15%、2.46%和1.66%,表明方法的重复性良好。[align=center][b]表1 重复性试验结果[/b][/align] [table=455][tr][td] [align=center]SCN[sup]-[/sup][/align] [/td][td] [align=left] 测定值/[/align] [/td][td] [align=left]平均值/[/align] [/td][td] [align=left] RSD/[/align] [/td][/tr][tr][td] [align=center](μg )[/align] [/td][td] [align=left] (A)[/align] [/td][td] [align=left](A)[/align] [/td][td] [align=left] %[/align] [/td][/tr][tr][td] [align=center]0.20 [/align] [/td][td] [align=left]0.025,0.026,0.027,0.029,0.027[/align] [/td][td] [align=center]0.027[/align] [/td][td] [align=center]4.54[/align] [/td][/tr][tr][td] [align=center]0.50 [/align] [/td][td] [align=left]0.068,0.070,0.071,0.072,0.074[/align] [/td][td] [align=center]0.071[/align] [/td][td] [align=center]3.15[/align] [/td][/tr][tr][td] [align=center]2.00 [/align] [/td][td] [align=left]0.292,0.308,0.289,0.299,0.297[/align] [/td][td] [align=center]0.297[/align] [/td][td] [align=center]2.46[/align] [/td][/tr][tr][td] [align=center]4.00 [/align] [/td][td] [align=left]0.577,0.589,0.592,0.585,0.602[/align] [/td][td] [align=center]0.589[/align] [/td][td] [align=center]1.56[/align] [/td][/tr][/table][b]2.11尿样分析结果[/b]取6份尿样按试验方法1.2操作测定SCN[sup]-[/sup]含量,同时用吡啶-巴比妥酸分光光度法[sup] [/sup]作对照分析,并进行加标回收试验,本法结果与行业推荐标准方法相吻合,加标回收率在96.0%~102.5%,见表2。[align=center][b]表2 尿样分析结果[/b][/align] [table=523][tr][td=1,3] [align=left]样品编号[/align] [/td][td=4,1] [align=center]本法结果[/align] [/td][td=1,3] [align=center]标准方法结果/[/align] [align=center]mg/L[/align] [/td][/tr][tr][td] [align=left]结果均值/[/align] [/td][td] [align=left]加入量/[/align] [/td][td] [align=left]回收率/[/align] [/td][td] [align=center] RSD/[/align] [/td][/tr][tr][td] [align=center]mg/L[/align] [/td][td] [align=center]μg[/align] [/td][td] [align=center]%[/align] [/td][td] [align=center] % (n=5) [/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]12.8 [/align] [/td][td] [align=center]2.00[/align] [/td][td] [align=center]102.5 [/align] [/td][td] [align=center]1.99[/align] [/td][td] [align=center]12.5[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]6.9 [/align] [/td][td] [align=center]5.00[/align] [/td][td] [align=center]100.8 [/align] [/td][td] [align=center]2.29[/align] [/td][td] [align=center]6.8[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]7.3 [/align] [/td][td] [align=center]4.00[/align] [/td][td] [align=center]100.5 [/align] [/td][td] [align=center]2.17 [/align] [/td][td] [align=center]7.4 [/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]15.2 [/align] [/td][td] [align=center]0.50[/align] [/td][td] [align=center]96.0 [/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]15.8[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]8.9 [/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]8.8[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]4.6 [/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]/[/align] [/td][td] [align=center]4.4[/align] [/td][/tr][/table][align=center][b] [/b][/align][b]参考文献 [/b]1 中华人民共和国卫生部.GBZ209-2008职业性急性氰化物中毒诊断标准[s].北京:人民卫生出版社,2008[/s][align=left]2[color=#333333]邵国建,郭和光,余娟.[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定尿中硫氰酸盐含量研究[/color][color=#333333],浙江预防医学,2011,23(4):95-96[/color][/align][align=left][url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E9%92%9F%E8%89%AF%E5%BA%B7&option=101][color=windowtext]3[/color]钟良康[/url],方波.超短柱顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定尿中硫氰酸盐[color=#333333],[/color][url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E4%B8%AD%E5%9B%BD%E5%8D%AB%E7%94%9F%E6%A3%80%E9%AA%8C%E6%9D%82%E5%BF%97&option=110]中国卫生检验杂志[/url],2005,15(5):568,628[/align][align=left]4刘晓宇,云自厚.衍生[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定人尿和唾液中微量硫氰酸根,环境与健康杂志,1994,11(3):130-131[/align]5 冯翠霞,[url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E6%9E%97%E4%B8%BD%E7%8E%B2&option=101]林丽玲[/url],[url=http://www.istic.ac.cn/suoguan/searchList.htm?indexname=101&text=%E9%BB%84%E8%BE%89%E6%B6%9B&option=101]黄辉涛[/url].分光光度法测定尿中硫氰酸盐的异烟酸-吡唑酮,中国职业医学,2009,36(6):501,5046 WS/T39-1996.尿中硫氰酸盐的吡啶-巴比妥酸分光光度测定方法[s].北京:中国标准出版社,19977 蔡秀丽,施逸岚,陈建忠.人尿中硫氰酸盐的快速测定方法,中国卫生检验杂志,2015,25(11):1703-1704,1707[color=#333333]8 [/color]黄选忠,汪 波,郑 凌.CN[sup]-[/sup]与异烟酸-硫代巴比妥酸-CTMAB显色体系的研究及应用,分析科学学报,2008,24(3):370-3729 全国高等医学院校检验专业专科教材.无机化学.北京:中国医药科技出版社,1990:31-3310 张孙玮,汤福隆,张 泰.现代化学试剂手册第二分册化学分析试剂.北京:化学工业出版社,1987:391-39211 全国中等卫生学校试用教材.临床检验.成都:四川人民出版社,1980:162(黄选忠,主任技师,研究方向:卫生化学检验技术。工作单位:兴山县疾病预防控制中心,联系电话:13872688318,E-mail:xscdchxz@sina.com)[/s]
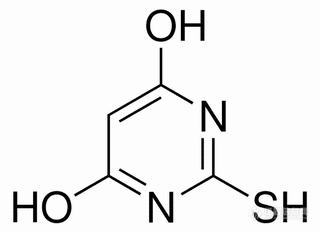
硫代巴比妥酸-亚硝酸盐显色体系分析应用研究[align=center]十月[/align]硫代巴比妥酸([color=#333333]thiobarbituric acid,[/color]TBA)又称为[color=#222222]4,6-二羟基-2-巯基嘧啶或[/color]丙二酰缩硫脲,化学式为[url=https://www.chembk.com/cn/search/C4H4N2O2S][color=black]C[/color][sub][color=black]4[/color][/sub][color=black]H[/color][sub][color=black]4[/color][/sub][color=black]N[/color][sub][color=black]2[/color][/sub][color=black]O[/color][sub][color=black]2[/color][/sub][color=black]S[/color][/url],其结构式见图1,TBA[color=#222222]在实验室应用广泛,曾作为化学分析或生化试剂用于食品和水中氰化物[/color][sup][1-3][/sup][color=#222222]、山梨酸[/color][sup][4][/sup]、[color=#222222]丙二醛、糠醛、香草醛[/color]及戊二醛等[color=#222222]醛类物质[/color][sup][5-9][/sup][color=#222222]、热老化物质[/color][sup][10][/sup]、[color=#222222]血清脂质过氧化物[/color][sup][11-12][/sup]、[color=#222222]唾液酸[/color][sup][13][/sup]和尿液中硫氰酸盐[sup][14][/sup]的测定,也用于修饰金纳米探针[align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/09/202309011020085866_2731_3127170_3.jpg[/img][/align][align=center]图1 硫代巴比妥酸的结构式[/align]高灵敏检测三聚氰胺[sup][15][/sup]。TBA与BA有相同(似)的化学性质(结构),也能与亚硝酸盐(NO[sub]2[/sub][sup]-[/sup])发生反应生成紫红色的硫代紫尿酸(thivioluric acid,TVA)。TVA进而与铁(Ⅱ)、钴(Ⅱ)反应形成蓝绿色和黄色配阴离子而应用于铁、钴的测定。本文就硫代巴比妥酸—亚硝酸盐(NO[sub]2[/sub][sup]-[/sup])显色体系分析应用情况总结分析于下。1)铁(Ⅱ)-硫代巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色体系分光光度法测定铁[sup][16][/sup]。研究了铁(Ⅱ)-硫代巴比妥酸-NO[sub]2[/sub][sup]-[/sup]体系显色反应的适宜条件及配合物的存在形式和光度特性,并对体系的显色机理进行了探讨,建立了一种测定微量铁的新分光光度法。2)铁(Ⅱ)-硫代巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色体系树脂相光度法测定微量铁[sup][17][/sup]。在碱性介质中,铁(Ⅱ)可与硫代巴比妥酸(TBA) - NO[sub]2[/sub][sup]-[/sup]体系反应形成一种稳定的蓝色配阴离子,其最大吸收波长位于671 nm处,该配阴离子能被阴离子交换树脂完全吸附,且树脂相在671 nm处的吸光度与铁含量在0~15μg/25 mL的范围内呈良好的线性关系,将该法应用于水样中微量铁的测定,测定结果与[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法测定结果相吻合,加标回收率为94%~102%,测定结果的相对标准偏差为3.4%~4.8%(n=5)。3)Fe(Ⅱ)-TAB-NO[sub]2[/sub][sup]-[/sup]显色体系双波长光度法测定水中的微量铁[sup][18][/sup]。在碱性介质中,铁(Ⅱ)与硫代巴比妥酸-NO[sub]2[/sub][sup]-[/sup]体系发生显色反应形成一种蓝色配阴离子,该配阴离子具有两个吸收峰分别位于658 nm和384 nm,且体系的吸光度A658、A384及其二者之和A均与铁(Ⅱ)含量在0~30μg/25 mL范围内具有良好的线性关系,方法的加标回收率为94%~104%,测定结果的相对标准偏差为3.4%~4.8%(n=5)。4)铁(Ⅱ)、钴(Ⅱ)-硫代巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色体系分光光度法同时测定微量铁和钴[sup][19][/sup]。在碱性介质中,铁(Ⅱ)和钴(Ⅱ)可与硫代巴比妥酸-NO[sub]2[/sub][sup]-[/sup]体系反应分别形成一种稳定的兰色和黄色配合物,铁(Ⅱ)配合物在656nm和386nm具有吸收峰,钴(Ⅱ)配合物只有一个吸收峰位于423nm,体系的吸光度AFe656、AFe423、ACo423与铁和钴含量在一定的范围内呈良好的线性关系,且铁(Ⅱ)、钴(Ⅱ)配合物在423nm波长处的吸光度具有良好的加和性,建立了一种同时测定微量铁和钴的新的分光光度法。方法的线性范围分别为铁0~50μg/25mL、钴0~25μg/25mL。将该法应用于水样中微量铁和钴的同时测定,其结果分别与[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]法和紫尿酸光度法相吻合,加标回收率分别为98%~102%和94%~106% ,相对标准偏差(RSD)分别为1.0%~1.8%和3.1%~4.7%(n=5)。参考文献张娅, 李春江, 王茜.异烟酸-硫代巴比妥酸显色反应测定酒中氰化物的研究[J].中国酿造,2013,32(12):138-1402)黄选忠,甘发清,徐留森.[color=#222222]CN[/color][sup][color=#222222]-[/color][/sup][color=#222222]-异烟酸-硫代巴比妥酸显色反应的研究及应用[/color][J].分析科学学报, 2007, 23(3):361-3633)黄选忠,汪 波,郑 凌.[color=#333333]CN[/color][sup][color=#333333]-[/color][/sup][color=#333333]-异烟酸-硫代巴比妥酸-CTMAB显色体系的研究及应用[/color][J].分析科学学报,2008,24(3):370-3724)[color=#666666] [/color][url=https://netl.istic.ac.cn/site/s?f=1&mid=466496091303411EB27FB4298C9BA46C&fieldid=C6ADB01393364592A3C34A78BFC163F3&q=%E6%9D%8E%E7%AB%B9%E4%BA%91%22 \o %22%E6%9D%8E%E7%AB%B9%E4%BA%91]李竹云[/url],[url=https://netl.istic.ac.cn/site/s?f=1&mid=466496091303411EB27FB4298C9BA46C&fieldid=C6ADB01393364592A3C34A78BFC163F3&q= %E7%8E%8B%E4%B8%BD%E5%8D%8E%22 \o %22 %E7%8E%8B%E4%B8%BD%E5%8D%8E]王丽华[/url],[url=https://netl.istic.ac.cn/site/s?f=1&mid=466496091303411EB27FB4298C9BA46C&fieldid=C6ADB01393364592A3C34A78BFC163F3&q= %E7%8E%8B%E9%B2%81%E6%95%8F%22 \o %22 %E7%8E%8B%E9%B2%81%E6%95%8F]王鲁敏[/url],等.[url=https://netl.istic.ac.cn/site/link?cdoi=0120100312760687&mid=466496091303411EB27FB4298C9BA46C%22 \o %22%E5%85%89%E5%BA%A6%E6%B3%95%E6%B5%8B%E5%AE%9A%E9%A3%9F%E5%93%81%E6%B7%BB%E5%8A%A0%E5%89%82%E5%B1%B1%E6%A2%A8%E9%85%B8%E7%9A%84%E7%A0%94%E7%A9%B6%22 \t %22https://netl.istic.ac.cn/site/_blank]光度法测定食品添加剂山梨酸的研究[/url][J].[url=https://netl.istic.ac.cn/site/link?cdoi=spkx&mid=2F54B3A514A34193AB662FE41DEAE1D1%22 \o %22食品科学,[/url]2008,15(3):429-4325)中华人民共和国国家卫生和计划生育委员会.中华人民共和国国家标准 食品安全国家标准: 食品中丙二醛的测定GB5009.181-2016[s].北京:中国标准出版社,20166)周琦,梁运祥.动物肝组织中丙二醛含量测定方法的改进[color=black][J][/color].时珍国医国药,2010,21(1):224-2257)[url=https://netl.istic.ac.cn/site/s?f=1&mid=466496091303411EB27FB4298C9BA46C&fieldid=C6ADB01393364592A3C34A78BFC163F3&q=%E6%AC%A7%E9%83%81%E5%BC%BA%22 \o %22%E6%AC%A7%E9%83%81%E5%BC%BA][color=black]欧郁强[/color][/url][color=black],[/color][url=https://netl.istic.ac.cn/site/s?f=1&mid=466496091303411EB27FB4298C9BA46C&fieldid=C6ADB01393364592A3C34A78BFC163F3&q= %E6%9D%8E%E8%83%9C%E5%88%A9%22 \o %22 %E6%9D%8E%E8%83%9C%E5%88%A9][color=black]李胜利[/color][/url][color=black],[/color][url=https://netl.istic.ac.cn/site/s?f=1&mid=466496091303411EB27FB4298C9BA46C&fieldid=C6ADB01393364592A3C34A78BFC163F3&q= %E5%90%B4%E5%9E%82%E6%98%8E%22 \o %22 %E5%90%B4%E5%9E%82%E6%98%8E][color=black]吴垂明[/color][/url][color=black],[/color]等.[url=https://netl.istic.ac.cn/site/link?cdoi=0120160105147895&mid=466496091303411EB27FB4298C9BA46C%22 \o %222-%E7%A1%AB%E4%BB%A3%E5%B7%B4%E6%AF%94%E5%A6%A5%E9%85%B8%E6%98%BE%E8%89%B2%E6%B3%95%E6%A3%80%E6%B5%8B%E5%8F%98%E5%8E%8B%E5%99%A8%E6%B2%B9%E4%B8%AD%E7%B3%A0%E9%86%9B%E7%9A%84%E7%A0%94%E7%A9%B6%22 \t %22https://netl.istic.ac.cn/site/_blank][color=black]2-硫代巴比妥酸显色法检测变压器油中糠醛的研究[/color][/url][color=black][J].[/color][url=https://netl.istic.ac.cn/site/link?cdoi=jycltx&mid=2F54B3A514A34193AB662FE41DEAE1D1%22 \o %22[color=black]绝缘材料,[/color][/url][color=black]2015,50(10):67-71[/color][color=black]8)[/color]何新亚,刘金霞,曹晓红,等.硫代巴比妥酸光度法测定香草醛[J].分析试验室,1999,18(5):58-60[color=black]9)[/color]何新亚,叶英植.硫代巴比妥酸分光光度法测定消毒液中戊二醛[J].分析化学,1998,26(11):1358-1361[color=#333333]10)张文会[/color].[url=https://netl.istic.ac.cn/site/link?cdoi=0120121101161287&mid=466496091303411EB27FB4298C9BA46C][color=#333333]利用2-硫代巴比妥酸TBA方法测定啤酒和饮料中的热老化物质[/color][/url][color=black][J][/color].啤酒科技,2012,17(7):58-62,5711)杨李,唐瑛,左娟,等.硫代巴比妥酸法测定血清脂质过氧化物方法的改进[color=black][J][/color].华南国防医学杂志,2004,18(1):)30-3212)赖泽仁.TBARS显色法测定血清过氧化脂质及其实验研究[color=black][J][/color].医药论坛杂志,2006,27(22):38-3913)何岳文,黄覆成,张爱宏.硫代巴比妥酸比色法测定尿液中唾液酸[color=black][J][/color].铁道医学,1994,22(6):357-35814)舒开继,黄选忠,杜宏山.在CTMAB存在下,异烟酸-硫代巴比妥酸显色光度法测定尿液中硫氰酸盐[J].山东化工, 2021,50(16):137-138.15)[color=black]费瑶,郭涵,奚焕祥[/color],等.[url=https://netl.istic.ac.cn/site/link?cdoi=0120140500523702&mid=466496091303411EB27FB4298C9BA46C][color=black]2-硫代巴比妥酸修饰金纳米探针高灵敏比色检测三聚氰胺[/color][/url][color=black][J][/color].应用化学,[color=black]2014,31(4):496-501[/color]16)黄选忠.铁(Ⅱ)硫代巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色反应[J]. 光谱学与光谱分析,1998,18(6):759-76117)王仁兴,张文学,黄良柱.铁(Ⅱ)-硫代巴比妥酸-NO[sub]2[/sub][sup]-[/sup]显色体系树脂相光度法测定微量铁[J].化学分析计量, 2011, 20(4):65-6618)黄伟,黄选忠.双波长光度法测定水中的微量铁[J].化学分析计量, 2008, 17(6):52-5419)夏世平.分光光度法同时测定微量铁和钴[J].化学分析计量, 2010, 19(1):43-45[/s]
[align=center][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[/font][font=宋体]同时[/font][font=宋体]测定[/font][font=宋体]药品中巴比妥酸和硝酸盐[/font][font=宋体]的研究[/font][/align][align=center][font=宋体]黄选忠[/font][/align][align=center][font=宋体](湖北[/font][font=宋体]兴山县[/font][font=宋体]疾病预防控制中心,湖北[/font][font=宋体]兴山[/font][font=宋体]443[/font][font=宋体]711[/font][font=宋体])[/font][/align][b][font=宋体]摘要 [/font][/b][font=宋体]建立[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url][/font][font=宋体][font=Times New Roman]-[/font][/font][font=宋体]抑制电导检测法[/font][font=宋体]同时[/font][font=宋体]测定[/font][font=宋体]巴比妥酸和硝酸盐[/font][font=宋体][font=宋体]的新方法。以[/font]SH-AC-3型阴离子交换柱为分离柱,以[/font][font=宋体]5[/font][font=宋体].0 mmol/L Na[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体][font=宋体]溶液为淋洗液,流量为[/font]1.0 mL/min,采用等度洗脱的方式可将[/font][font=宋体]巴比妥酸和硝酸盐[/font][font=宋体]与[/font][font=宋体]氟化物、[/font][font=宋体]氯化物、[/font][font=宋体]磷酸盐[/font][font=宋体]和硫酸盐等常见阴离子完全分离,通过抑制电导检测[/font][font=宋体],巴比妥酸[/font][font=宋体]的峰面积与其[/font][font=宋体]质量[/font][font=宋体][font=宋体]浓度在[/font]0.[/font][font=宋体]1[/font][font=宋体]0~50.0mg/L范围内呈良好的线性关系,相关系数[/font][i][font=宋体]r[/font][/i][font=宋体]分别[/font][font=宋体]为[/font][font=宋体]0.9999[/font][font=宋体],硝酸盐[/font][font=宋体]的峰面积与其[/font][font=宋体]质量[/font][font=宋体]浓度[/font][font=宋体]分别[/font][font=宋体][font=宋体]在[/font]0.[/font][font=宋体]1[/font][font=宋体]0~[/font][font=宋体]3[/font][font=宋体]0.0mg/L[/font][font=宋体]和[/font][font=宋体]30.0[/font][font=宋体]~[/font][font=宋体]5[/font][font=宋体]0.0mg/L范围内呈良好的线性关系,相关系数[/font][i][font=宋体]r[/font][/i][font=宋体]分别[/font][font=宋体]为[/font][font=宋体]0.9994和[/font][font=宋体]0.999[/font][font=宋体]9[/font][font=宋体],该方法应用[/font][font=宋体]巴比妥、苯巴比妥和维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]等药品中[/font][font=宋体]巴比妥酸和硝酸盐同时[/font][font=宋体]的测定,[/font][font=宋体]加标回收率分别为[/font][font=宋体]90.4%[/font][font=宋体]~[/font][font=宋体]101.4%和98.0%[/font][font=宋体]~[/font][font=宋体]101.3%,5次平行测定结果的相对标准偏差[/font][font=宋体][font=宋体]([/font]RSD)[/font][font=宋体][font=宋体]分别为[/font]1.71%[/font][font=宋体]~[/font][font=宋体]2.39%和1.21%[/font][font=宋体]~[/font][font=宋体]2.66%,巴比妥酸和硝酸盐的[/font][font=宋体][font=宋体]最低检出限分别为[/font]0.10mg/L和[/font][font=宋体]0.03[/font][font=宋体]mg/L[/font][font=宋体],[/font][font=宋体]方法回收率较高、重现性良好,操作简便快速,可用于巴比妥、苯巴比妥和维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]等样品中[/font][font=宋体]巴比妥酸和硝酸盐[/font][font=宋体]的定量分析。[/font][b][font=宋体]关键词 [/font][/b][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法;[/font][font=宋体]巴比妥酸[/font][font=宋体];[/font][font=宋体]硝酸盐;巴比妥;苯巴比妥;维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][b][font=宋体]中图分类号:[/font][/b][font=宋体]O652.63[/font][b][font=宋体] [font=宋体]文献标识码:[/font] 文章编号:[/font][/b][align=center][font=宋体]Simultaneous determination of barbituric acid and nitrate in pharmaceuticals by ion chromatography[/font][/align][align=center][font=宋体](Prevention and Health Protection Centre of Hubei [/font][font=宋体]Xingshan[/font][font=宋体] [font=宋体]C[/font][/font][font=宋体]ounty[/font][font=宋体][font=宋体],[/font] [/font][font=宋体]Xingshan[/font][font=宋体]443[/font][font=宋体]711[/font][font=宋体][font=宋体],[/font] China)[/font][/align][font=宋体] [font=宋体]Abstract A new method for simultaneous determination of barbituric acid and nitrate by ion chromatography with suppressed conductivity detection was developed. SH-AC-3 anion exchange column was used as separation column, 5.0 mmol/L Na[/font][/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体] [font=宋体]solution was used as eluent and the flow rate was 1.0 ml/min, barbituric acid and nitrates can be completely separated from common anions such as fluoride, chloride, phosphate and sulfate by isometric elution, and can be detected by inhibiting conductance, there is a good linear relationship between the peak area and the concentration of barbituric acid in the range of 0.10[/font][/font][font=宋体]~[/font][font=宋体]50.0 mg/l, and the Correlation Coefficient R is 0.9999, the peak area of nitrate has a good linear relationship with its concentration in the range of 0.10[/font][font=宋体]~[/font][font=宋体]30.0 mg/l and 30.0[/font][font=宋体]~[/font][font=宋体]50.0 mg/l, respectively. The Correlation Coefficients R are 0.9994 and 0.9999, respectively, the method was applied to the simultaneous determination of barbituric acid and nitrate in barbiturate, phenobarbital and vitamin B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]. The recoveries were 90.4% [/font][font=宋体]~[/font][font=宋体]101.4% and 98.0% [/font][font=宋体]~[/font][font=宋体]101.3% , respectively, the relative standard deviation (RSD) was 1.71% [/font][font=宋体]~[/font][font=宋体]2.39% and 1.21% [/font][font=宋体]~[/font][font=宋体] [font=宋体]2.66% , respectively. The minimum detection limits of barbituric acid and nitrate were 0.10 mg/l and 0.03 mg/l, respectively, the method is simple and fast, and can be used for the barbituric acid and nitrate Quantitative analysis of barbiturate, phenobarbital and vitamin B[/font][/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体].[/font][font=宋体] [/font][b][font=宋体]Key words[/font][font=宋体] [/font][/b][font=宋体]i[/font][font=宋体]on chromatography[/font][font=宋体];[/font][font=宋体]barbituric acid;[/font][font=宋体]n[/font][font=宋体]itrate;Barbiturates;[/font][font=宋体]phenobarbital[/font][font=宋体];[/font][font=宋体]vitamin B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体] [/font][font=宋体]巴比妥酸是合成巴比妥、苯巴比妥等镇静催眠药和维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]等药品的中间体[/font][sup][font=宋体][font=宋体][1][/font][/font][/sup][font=宋体],但由于巴比妥酸[/font][font=宋体][font=宋体]在生理条件下[/font]99%以上是离子状态而无疗效[/font][sup][font=宋体][font=宋体][2][/font][/font][/sup][font=宋体],[/font][font=宋体]因此监测[/font][font=宋体]巴比妥、苯巴比妥和维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]等药品中的巴比妥酸具有重要意义。[/font][font=宋体]硝酸盐对人体有害,过量摄入可能导致高铁血红蛋白血症,并在体内转化成致癌性的亚硝胺[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体][font=宋体]3[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体],持续少量摄入也会引起消化不良、精神抑郁和头痛[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体][font=宋体]4[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体],[/font][font=宋体]中国药典对相关药品中[/font][font=宋体]硝酸盐的含量都有明确的限量要求如[/font][font=宋体]维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]1[/font][/font][/sub][font=宋体]原料药中[/font][font=宋体]硝酸盐含量不得大于[/font][font=宋体][font=Times New Roman]0.25%[/font][/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体][font=宋体]5[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体],[/font][font=宋体]因此监测[/font][font=宋体]药品中[/font][font=宋体]硝酸盐含量对保障用药安全[/font][font=宋体]具有重要[/font][font=宋体]意义。[/font][font=宋体]目前[/font][font=宋体]测定药品中微量[/font][font=宋体]巴比妥酸[/font][font=宋体]的方法已报道的仅有化学发光法[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体][font=宋体]6[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体]和分光光度法[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体][font=宋体]7[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体],其中,[/font][font=宋体]化学发光法需要专用仪器[/font][font=宋体],而[/font][font=宋体]分光光度法则灵敏度偏低。[/font][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[/font][font=宋体]目前[/font][font=宋体]已成为测定无机阴离子和有机酸的首选方法,[/font][font=宋体]已[/font][font=宋体]应用于[/font][font=宋体]维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]1[/font][/font][/sub][font=宋体][font=宋体]注射液中的[/font]EDTA及硝酸根离子的同时测定[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体][font=宋体]4[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体]和[/font][font=宋体]水、尿液、[/font][font=宋体]食品等样品中[/font][font=宋体]邻苯二甲酸[/font][font=宋体]([/font][font=宋体]根[/font][font=宋体])、[/font][font=宋体]草酸、枸橼酸、琥珀酸、柠檬酸、酒石酸、乙醇酸、[/font][font=宋体]甲酸、乙酸、酒石酸、氨基磺酸[/font][font=宋体][font=宋体]等有机酸[/font][/font][font=宋体]的[/font][font=宋体]定量分析[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体][font=宋体]8-14[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体],[/font][font=宋体]但[/font][font=宋体]测定[/font][font=宋体]药品[/font][font=宋体]中[/font][font=宋体]巴比妥酸[/font][font=宋体][font=宋体]尚未见报道。本实验研究用[/font]SH-AC-3型阴离子交换柱和CIC-100型色谱仪[/font][font=宋体]同时[/font][font=宋体]测定[/font][font=宋体]巴比妥、苯巴比妥和维生素[/font][font=宋体]B12等药品中的巴比妥酸和硝酸盐[/font][font=宋体][font=宋体]的色谱条件和可行性,结果表明,以[/font]SH-AC-3型阴离子交换柱为分离柱、[/font][font=宋体]5[/font][font=宋体].0mmol/LNa[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体][font=宋体]溶液作淋洗液,流量为[/font]1.0ml/min,采用等度洗脱的方式可使[/font][font=宋体]巴比妥酸和硝酸盐[/font][font=宋体]与氟化物、氯化物、亚硝酸盐、溴化物[/font][font=宋体]、[/font][font=宋体]磷酸盐、硫酸盐等常见阴离子完全分离,且[/font][font=宋体]巴比妥酸[/font][font=宋体]的峰面积与其[/font][font=宋体]质量[/font][font=宋体][font=宋体]浓度在[/font]0.[/font][font=宋体]1[/font][font=宋体]0~50.0mg/L范围内呈良好的线性关系,相关系数r[/font][font=宋体]分别[/font][font=宋体]为[/font][font=宋体]0.9999[/font][font=宋体],硝酸盐[/font][font=宋体]的峰面积与其[/font][font=宋体]质量[/font][font=宋体]浓度[/font][font=宋体]分别[/font][font=宋体][font=宋体]在[/font]0.[/font][font=宋体]1[/font][font=宋体]0~[/font][font=宋体]3[/font][font=宋体]0.0mg/L[/font][font=宋体]和[/font][font=宋体]30.0[/font][font=宋体]~[/font][font=宋体]5[/font][font=宋体]0.0mg/L范围内呈良好的线性关系,相关系数r[/font][font=宋体]分别[/font][font=宋体]为[/font][font=宋体]0.9994和[/font][font=宋体]0.999[/font][font=宋体]9[/font][font=宋体],方法应用于[/font][font=宋体]巴比妥、维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]和[/font][font=宋体]苯巴比妥[/font][font=宋体]等样品中巴比妥酸和硝酸盐[/font][font=宋体]的[/font][font=宋体]同时[/font][font=宋体]测定,[/font][font=宋体]并在[/font][font=宋体]3种样中分别添加1.0、5.0、10.0[/font][font=宋体]mg/L[/font][font=宋体]的[/font][font=宋体]巴比妥酸和硝酸盐[/font][font=宋体],分别[/font][font=宋体][font=宋体]平行测定[/font]5次,[/font][font=宋体]加标回收率分别为[/font][font=宋体]90.4%[/font][font=宋体]~[/font][font=宋体]101.4%和98.0%[/font][font=宋体]~[/font][font=宋体]101.3%,测定结果的相对标准偏差[/font][font=宋体][font=宋体]([/font]RSD)[/font][font=宋体][font=宋体]分别为[/font]1.71%[/font][font=宋体]~[/font][font=宋体]2.39%和1.21%[/font][font=宋体]~[/font][font=宋体]2.66%,[/font][font=宋体]按[/font][font=宋体]3倍信噪比[/font][font=宋体]([/font][i][font=宋体]3N[/font][font=宋体]/[/font][font=宋体]b[/font][/i][font=宋体])计[/font][font=宋体],[/font][font=宋体]巴比妥酸和硝酸盐的[/font][font=宋体]最低检出限[/font][font=宋体]分别[/font][font=宋体][font=宋体]为[/font]0.10mg/L[/font][font=宋体]和[/font][font=宋体]0.03[/font][font=宋体]mg/L[/font][font=宋体],方法适用于[/font][font=宋体]巴比妥、苯巴比妥和维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]等样品中的巴比妥酸和硝酸盐的同时测定[/font][font=宋体]。[/font][b][font=宋体]1 实验部分[/font][font=宋体]1.1 [/font][/b][font=宋体]主要仪器与试剂[/font][font=宋体][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]:[/font]CIC-100,青岛盛瀚色谱公司。[/font][font=宋体]抑制器:[/font][font=宋体]SHY-2型[/font][font=宋体]自再生抑制器[/font][font=宋体],[/font][font=宋体]青岛盛瀚色谱公司。[/font][font=宋体][font=宋体]定量环体积:[/font]25μL;[/font][font=宋体][font=宋体]自动进样器:[/font]SHA[/font][font=宋体]—[/font][font=宋体]15型,青岛盛瀚色谱公司。[/font][font=宋体]0.[/font][font=宋体]45[/font][font=宋体]μm[/font][font=宋体][font=宋体]滤膜过滤器:[/font]13 mm,青岛盛瀚色谱公司。[/font][font=宋体][font=宋体]巴比妥酸([/font]C[/font][sub][font=宋体][font=宋体]4[/font][/font][/sub][font=宋体]H[/font][sub][font=宋体][font=宋体]4[/font][/font][/sub][font=宋体]N[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]O[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]2H[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]O[/font][font=宋体])[/font][font=宋体]:分析纯,[/font][font=宋体]国药集团化学试剂有限公司。[/font][font=宋体] [/font][font=宋体]巴比妥酸[/font][font=宋体][font=宋体]标准溶液:[/font]1000mg/L,称取[/font][font=宋体]1.2942[/font][font=宋体]g[/font][font=宋体]巴比妥酸[/font][font=宋体][font=宋体],溶解于高纯水[/font],定容至1000ml容量瓶。[/font][font=宋体] [/font][font=宋体]磷酸二氢钾[/font][font=宋体]、[/font][font=宋体]溴化钾[/font][font=宋体]:分析纯,[/font][font=宋体]国药集团化学试剂有限公司。[/font][font=宋体] [/font][font=宋体]H[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]PO[/font][sub][font=宋体][font=宋体]4[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体][font=宋体]标准溶液:[/font]1000 mg/L,称取磷酸二氢钾0.1402g用[/font][font=宋体]高[/font][font=宋体][font=宋体]纯水溶解,定容至[/font]100mL容量瓶。[/font][font=宋体] [/font][font=宋体]Br[/font][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体][font=宋体]标准溶液:[/font]1000 mg/L,准确称取[/font][font=宋体]0.1[/font][font=宋体]489g在105℃烘烤2h的溴化钾,[/font][font=宋体]高[/font][font=宋体][font=宋体]纯水溶解定容至[/font]100ml容量瓶。[/font][font=宋体] [/font][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]、[/font][font=宋体]F[/font][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]、[/font][font=宋体]Cl[/font][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]、[/font][font=宋体]SO[/font][sub][font=宋体][font=宋体]4[/font][/font][/sub][sup][font=宋体][font=宋体]2-[/font][/font][/sup][font=宋体]、[/font][font=宋体]NO[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]标准溶液:[/font][font=宋体]均为[/font][font=宋体]1000 mg/L[/font][font=宋体],编号分别为[/font][font=宋体]GBW(E)080223[/font][font=宋体]、[/font][font=宋体]GBW(E)080549[/font][font=宋体]、[/font][font=宋体]GBW(E)080268[/font][font=宋体]、[/font][font=宋体]GBW(E)080266[/font][font=宋体]、[/font][font=宋体]GBW(E)080264,[/font][font=宋体]中国计量科学研究院。[/font][font=宋体]无水碳酸钠、碳酸氢钠:分析纯,国药集团化学试剂有限公司。[/font][font=宋体][font=宋体]实验所用其它试剂均为[/font]AR级。[/font][font=宋体][font=宋体]实验用水为高纯水(电阻率为[/font]18.2ΜΩcm)。[/font][b][font=宋体]1.2[/font][/b][font=宋体] 仪器工作条件[/font][font=宋体][font=宋体]色谱分离柱:[/font]SH-AC-3型阴离子交换柱(250 mm×4.0 mm,青岛盛瀚色谱公司);保护柱:SH-AC-3型(50 [/font][font=宋体]mm×4.0 mm,青岛盛瀚色谱公司);淋洗液[/font][font=宋体]:5[/font][font=宋体].0mmol/LNa[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体][font=宋体]溶液,流量为[/font]1.0ml/min;柱箱温度:35℃;电流:75mA;检测器:电导检测器;自动进样器:全定量环取样,取样后清洗(每针之[/font][font=宋体][font=宋体]间),置换量[/font]70μL,取样量25μL,扎针深度4mm。[/font][b][font=宋体]1.[/font][font=宋体]3[/font][/b][font=宋体] 实验方法[/font][b][font=宋体]1.[/font][font=宋体]3[/font][font=宋体].1[/font][/b][font=宋体] 标准溶液配制[/font][font=宋体] [/font][font=宋体]巴比妥酸和[/font][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]混合[/font][font=宋体]标准[/font][font=宋体]应用液[/font][font=宋体]:临用前将[/font][font=宋体]巴比妥酸和[/font][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]标准溶液[/font][font=宋体]稀释成含[/font][font=宋体]巴比妥酸和[/font][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]均为[/font][font=宋体]10.0[/font][font=宋体]mg/L[/font][font=宋体]([/font][font=宋体]A[/font][font=宋体]液)[/font][font=宋体]和[/font][font=宋体]100.0[/font][font=宋体]mg/L[/font][font=宋体]([/font][font=宋体]B液)。[/font][font=宋体]取[/font][font=宋体]巴比妥酸和[/font][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]混合[/font][font=宋体]标准[/font][font=宋体][font=宋体]应用液([/font]A液)0.[/font][font=宋体]1[/font][font=宋体]0、[/font][font=宋体]0.25、[/font][font=宋体]0.50、1.00mL及B液0.50、1.0、2.0、3.0、4.0、5.0mL于[/font][font=宋体]10只[/font][font=宋体]10mL容量瓶中加纯水至刻度,混匀,配制成含[/font][font=宋体]巴比妥酸和[/font][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]均为[/font][font=宋体]0.[/font][font=宋体]1[/font][font=宋体]0、0.[/font][font=宋体]2[/font][font=宋体]5、[/font][font=宋体]0.50、[/font][font=宋体]1.00、[/font][font=宋体]5[/font][font=宋体].0[/font][font=宋体]0[/font][font=宋体]、[/font][font=宋体]10[/font][font=宋体].[/font][font=宋体]0[/font][font=宋体]0、[/font][font=宋体]20.0[/font][font=宋体]0、[/font][font=宋体]30[/font][font=宋体].0[/font][font=宋体]0[/font][font=宋体]、[/font][font=宋体]40[/font][font=宋体].0[/font][font=宋体]0[/font][font=宋体]和[/font][font=宋体]50.0mg/L的系列标准工作溶液[/font][font=宋体]。[/font][b][font=宋体]1.3.2[/font][/b][font=宋体]标准曲线绘制[/font][font=宋体] [/font][font=宋体]取[/font][font=宋体]1.3.1制备的[/font][font=宋体]系列标准工作溶液[/font][font=宋体],[/font][font=宋体][font=宋体]各管取[/font]1.5mL于样品瓶中,启动自动进样器进样[/font][font=宋体],[/font][font=宋体]分别测定[/font][font=宋体],以巴比妥酸和[/font][font=宋体]硝酸盐[/font][font=宋体]的峰面积[/font][font=宋体]([/font][i][font=宋体]y[/font][/i][font=宋体])[/font][font=宋体]为纵坐标,以[/font][font=宋体]色谱峰面积[/font][font=宋体]对[/font][font=宋体]应的[/font][font=宋体]巴比妥酸和[/font][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]的质量[/font][font=宋体]浓度[/font][font=宋体]([/font][i][font=宋体]x[/font][/i][font=宋体])[/font][font=宋体]为横坐标[/font][font=宋体],[/font][font=宋体]绘制工作曲线。[/font][b][font=宋体]1.[/font][font=宋体]3[/font][font=宋体].[/font][font=宋体]3[/font][font=宋体] [/font][/b][font=宋体]样品处理[/font][font=宋体][font=宋体]称取巴比妥[/font]0.250[/font][font=宋体]g[/font][font=宋体]加[/font][font=宋体]5[/font][font=宋体]mL[/font][font=宋体]无水乙醇溶解后[/font][font=宋体],用高纯水[/font][font=宋体]定容至[/font][font=宋体]100[/font][font=宋体]ml[/font][font=宋体],取该样液[/font][font=宋体][font=宋体]用高纯水稀释[/font]1倍并[/font][font=宋体][font=宋体]经[/font]0.45μm滤膜过滤后[/font][font=宋体]供测试[/font][font=宋体],样品测试液中[/font][font=宋体][font=宋体]巴比妥的质量浓度为[/font]1250[/font][font=宋体]mg/L[/font][font=宋体]。[/font][font=宋体][font=宋体]将苯巴比妥片研磨均匀称取[/font]0.420[/font][font=宋体]g[/font][font=宋体](含[/font][font=宋体][font=宋体]苯巴比妥[/font]200[/font][font=宋体]mg[/font][font=宋体])[/font][font=宋体]加[/font][font=宋体]10[/font][font=宋体]mL[/font][font=宋体]无水乙醇充分搅拌溶解后[/font][font=宋体],用高纯水[/font][font=宋体]定容至[/font][font=宋体]100[/font][font=宋体]ml[/font][font=宋体],滤去不溶物,滤液[/font][font=宋体][font=宋体]用高纯水稀释[/font]1倍并[/font][font=宋体][font=宋体]经[/font]0.45μm滤膜过滤后[/font][font=宋体]供测试[/font][font=宋体],样品测试液中苯[/font][font=宋体][font=宋体]巴比妥的质量浓度为[/font]1000[/font][font=宋体]mg/L[/font][font=宋体]。[/font][font=宋体]取[/font][font=宋体]维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体][font=宋体]片[/font]40片(含[/font][font=宋体]维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体][font=宋体]约[/font]1000[/font][font=仿宋_GB2312][font=Times New Roman]μ[/font][/font][font=仿宋_GB2312]g[/font][font=宋体])用[/font][font=宋体]高纯水洗去表面糖衣后,加高纯水充分[/font][font=宋体]研磨溶解并[/font][font=宋体]定容至[/font][font=宋体]100[/font][font=宋体]ml[/font][font=宋体],滤去不溶物,滤液[/font][font=宋体]用[/font][font=宋体]0.45μm滤膜过滤后[/font][font=宋体]供测试[/font][font=宋体],样品测试液中[/font][font=宋体]维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体][font=宋体]的质量浓度为[/font]10[/font][font=宋体]mg/L[/font][font=宋体]。[/font][b][font=宋体]1.3.4[/font][/b][font=宋体]样品测定[/font][font=宋体]取[/font][font=宋体]1.3.3[/font][font=宋体]的样品测试液[/font][font=宋体]1.5[/font][font=宋体]ml于样品瓶中,启动自动进样器进样测定[/font][font=宋体]巴比妥酸和[/font][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]的[/font][font=宋体]峰面积,以标准曲线法定量,同时进行加标回收试验。[/font][b][font=宋体]2 结果与讨论[/font][font=宋体]2.1[/font][/b][font=宋体] 色谱条件的选择[/font][b][font=宋体]2.1.1[/font][/b][font=宋体] 淋洗液的选择[/font][font=宋体]试验考察了[/font][font=宋体]淋洗液[/font][font=宋体]中[/font][font=宋体] [font=宋体]Na[/font][/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]与[/font][font=宋体]NaHCO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]溶液[/font][font=宋体]浓度配比分别[/font][font=宋体]为[/font][font=宋体]5+0、5+0.5、5+0.75、5+1[/font][font=宋体]mmol/L、流量为1.0mL/min[/font][font=宋体]时[/font][font=宋体][font=宋体],[/font]SH-AC-3型柱[/font][font=宋体]对巴比妥酸和硝酸盐与[/font][font=宋体]H[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]PO[/font][sub][font=宋体][font=宋体]4[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]、[/font][font=宋体]硫酸盐常见阴离子[/font][font=宋体]的分离情况,结果见表[/font][font=宋体]1,从表[/font][align=center][font=宋体]表[/font][font=宋体]1 [/font][font=宋体]淋洗液[/font][font=宋体]中[/font][font=宋体]Na[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]与[/font][font=宋体]NaHCO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]不同配比对各组分[/font][font=宋体]峰分离度([/font][font=宋体]R)的影响[/font][/align][table][tr][td=1,2][align=center][font=宋体]组分[/font][/align][/td][td=4,1][align=center][font=宋体]Na[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]+NaHCO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体](mmol/L)[/font][/align][/td][/tr][tr][td][align=center][font=宋体]5[/font][font=宋体]+[/font][font=宋体]0[/font][/align][/td][td][align=center][font=宋体]5[/font][font=宋体]+[/font][font=宋体]0.5[/font][/align][/td][td][align=center][font=宋体]5[/font][font=宋体]+[/font][font=宋体]0.75[/font][/align][/td][td][align=center][font=宋体]5+1[/font][/align][/td][/tr][tr][td][align=center][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][/align][/td][td][align=center][font=宋体]1.94[/font][/align][/td][td][align=center][font=宋体]1.62[/font][/align][/td][td][align=center][font=宋体]1.25[/font][/align][/td][td][align=center][font=宋体]1.30[/font][/align][/td][/tr][tr][td][align=center][font=宋体]巴比妥酸[/font][/align][/td][td][align=center][font=宋体]3.59[/font][/align][/td][td][align=center][font=宋体]3.94[/font][/align][/td][td][align=center][font=宋体]3.58[/font][/align][/td][td][align=center][font=宋体]3.55[/font][/align][/td][/tr][tr][td][align=center][font=宋体]H[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]PO[/font][sub][font=宋体][font=宋体]4[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][/align][/td][td][font=宋体] [font=宋体]0.61[/font][/font][/td][td][align=center][font=宋体]1.29[/font][/align][/td][td][align=center][font=宋体]2.20[/font][/align][/td][td][align=center][font=宋体]2.05[/font][/align][/td][/tr][tr][td][align=center][font=宋体]SO[/font][sub][font=宋体][font=宋体]4[/font][/font][/sub][sup][font=宋体][font=宋体]2-[/font][/font][/sup][/align][/td][td][align=center][font=宋体]/[/font][/align][/td][td][align=center][font=宋体]/[/font][/align][/td][td][align=center][font=宋体]/[/font][/align][/td][td][align=center][font=宋体]/[/font][/align][/td][/tr][/table][font=宋体]1可见,随着[/font][font=宋体]淋洗液[/font][font=宋体]中[/font][font=宋体]NaHCO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]浓度的增加[/font][font=宋体],[/font][font=宋体]硝酸盐的峰分离度([/font][font=宋体]R)[/font][font=宋体]逐渐降低[/font][font=宋体],[/font][font=宋体]巴比妥酸的峰分离度则无明显的改变[/font][font=宋体],而H[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]PO[/font][sub][font=宋体][font=宋体]4[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]的峰分离度逐渐增加[/font][font=宋体],为使[/font][font=宋体]巴比妥酸和硝酸盐均有较高的峰分离度[/font][font=宋体],本试验以单纯的[/font][font=宋体]Na[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]溶液[/font][font=宋体]为[/font][font=宋体]淋洗液[/font][font=宋体]。[/font][font=宋体]Na[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]溶液浓度[/font][font=宋体]选择试验结果表明[/font][font=宋体],[/font][font=宋体]当[/font][font=宋体]Na[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]溶液浓度分别为[/font][font=宋体]4[/font][font=宋体].0、[/font][font=宋体]5[/font][font=宋体].0和[/font][font=宋体]6[/font][font=宋体].0 mmol/L时[/font][font=宋体],[/font][font=宋体]巴比妥酸的峰分离度分别为[/font][font=宋体]4.97、3.60[/font][font=宋体]和[/font][font=宋体]3.10,[/font][font=宋体]硝酸盐的峰分离度分别为[/font][font=宋体]2.04、1.96[/font][font=宋体]和[/font][font=宋体]1.77,完全[/font][font=宋体]满足[/font][font=宋体]相邻[/font][font=宋体]组分完全分离的要求[/font][font=宋体]([/font][font=宋体]R[/font][font=宋体]≥1.5[/font][font=宋体])[/font][sup][font=宋体][font=宋体][1[/font][/font][/sup][sup][font=宋体][font=宋体]5[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体],故[/font][font=宋体]本实验选择[/font][font=宋体]5[/font][font=宋体].0mmol/L[/font][font=宋体]的[/font][font=宋体]Na[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]溶液为淋洗液[/font][font=宋体],在[/font][font=宋体]此淋洗条件下[/font][font=宋体]巴比妥酸和硝酸盐[/font][font=宋体]与常见阴离子的分离[/font][font=宋体]色谱[/font][font=宋体][font=宋体]图见图[/font]1。[/font][b][font=宋体]2.1.2[/font][/b][font=宋体] 色谱柱的选择[/font][font=宋体]以[/font][font=宋体]5[/font][font=宋体].0 mmol/L Na[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体][font=宋体]溶液为淋洗液、流量[/font]1.0 mL/min等度洗脱,考察了SH-AC-1型和SH-AC-3型阴离子交换柱对[/font][font=宋体]巴比妥酸和硝酸盐与其他常见[/font][font=宋体]阴离子[/font][font=宋体][font=宋体]的分离效果。结果表明,[/font]SH-AC-1型阴离子交换柱[/font][font=宋体]虽然能将[/font][font=宋体]氯化物[/font][font=宋体]、[/font][font=宋体]硝酸盐和[/font][font=宋体]硫酸盐[/font][font=宋体]完全分离,但[/font][font=宋体]不能将[/font][font=宋体]氯化物[/font][font=宋体]与巴比妥酸完全分离且巴比妥酸严重拖尾、峰形较差[/font][font=宋体][font=宋体],[/font]SH-AC-3型阴离子交换柱[/font][font=宋体]不仅能将[/font][font=宋体]氯化物[/font][font=宋体]与巴比妥酸完全分离且巴比妥酸的峰形良好[/font][font=宋体],[/font][font=宋体]试[/font][font=宋体][font=宋体]验选择[/font]SH-AC-3型阴离子交换柱为分离柱。[/font][b][font=宋体]2.1.3 [/font][/b][font=宋体]淋洗液流量的[/font][font=宋体]影响[/font][font=宋体]考察了[/font][font=宋体]淋洗液流量[/font][font=宋体]分别[/font][font=宋体][font=宋体]为[/font]0.8、1.0、1.2 mL/min[/font][font=宋体]时各组分的分离情况,试验结果见表[/font][font=宋体]2[/font][font=宋体],从表[/font][font=宋体]2可见:[/font][font=宋体]随着[/font][font=宋体]淋洗液流量[/font][font=宋体]的升高,[/font][font=宋体]各组分[/font][font=宋体]的保留时间[/font][font=宋体]([/font][font=宋体]T)[/font][font=宋体]逐渐缩短[/font][font=宋体],[/font][font=宋体]峰分离度([/font][font=宋体]R)和峰面积[/font][font=宋体]逐渐降低[/font][font=宋体],[/font][font=宋体]对于[/font][font=宋体]硝酸盐,[/font][font=宋体]当[/font][font=宋体]淋洗液流量[/font][font=宋体]从[/font][font=宋体]0.8[/font][font=宋体]mL/min[/font][font=宋体]上升至[/font][font=宋体]1.0[/font][font=宋体]mL/min[/font][font=宋体]时,[/font][font=宋体]保留时间[/font][font=宋体]缩短[/font][font=宋体]2.0min,[/font][font=宋体]峰分离度变化较小,[/font][font=宋体]当[/font][font=宋体]淋洗液流量[/font][font=宋体]从[/font][align=center][font=宋体] [/font][/align][align=center][font=宋体][font=宋体]表[/font]2 淋洗液流量[/font][font=宋体]的影响[/font][font=宋体]([/font][font=宋体]5[/font][font=宋体].0mmol/LNa[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]CO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][font=宋体]溶液[/font][font=宋体])[/font][/align][table][tr][td=1,2][align=center][font=宋体]组分[/font][/align][/td][td=2,1][align=center][font=宋体]0.8ml/min[/font][/align][/td][td=2,1][align=center][font=宋体]1.0ml/min[/font][/align][/td][td=2,1][align=center][font=宋体]1.2ml/min[/font][/align][/td][/tr][tr][td][align=center][font=宋体]T[/font][font=宋体]/min[/font][/align][/td][td][align=center][font=宋体]R[/font][/align][/td][td][align=center][font=宋体]T[/font][font=宋体]/min[/font][/align][/td][td][align=center][font=宋体]R[/font][/align][/td][td][align=center][font=宋体]T[/font][font=宋体]/min[/font][/align][/td][td][align=center][font=宋体]R[/font][/align][/td][/tr][tr][td][align=center][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][/align][/td][td][align=center][font=宋体]10.741[/font][/align][/td][td][align=center][font=宋体]1.94[/font][/align][/td][td][align=center][font=宋体]8.678[/font][/align][/td][td][align=center][font=宋体]1.98[/font][/align][/td][td][align=center][font=宋体]7.359[/font][font=宋体] [/font][/align][/td][td][align=center][font=宋体]1.77[/font][/align][/td][/tr][tr][td][align=center][font=宋体]巴比妥[/font][font=宋体]酸[/font][/align][/td][td][align=center][font=宋体]12.319[/font][/align][/td][td][align=center][font=宋体]4.0[/font][font=宋体]4[/font][/align][/td][td][align=center][font=宋体]10.025[/font][/align][/td][td][align=center][font=宋体]3.90[/font][font=宋体] [/font][/align][/td][td][align=center][font=宋体]8.391[/font][font=宋体] [/font][/align][/td][td][align=center][font=宋体]3.7[/font][font=宋体]5 [/font][/align][/td][/tr][tr][td][align=center][font=宋体]H[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][font=宋体]PO[/font][sub][font=宋体][font=宋体]4[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][/align][/td][td][align=center][font=宋体]16.565[/font][/align][/td][td][align=center][font=宋体]/[/font][/align][/td][td][align=center][font=宋体]13.430[/font][/align][/td][td][align=center][font=宋体]/[/font][/align][/td][td][align=center][font=宋体]11.206[/font][font=宋体] [/font][/align][/td][td][align=center][font=宋体]/[/font][/align][/td][/tr][/table][font=宋体]1.0[/font][font=宋体]mL/min[/font][font=宋体]上升至[/font][font=宋体]1.2[/font][font=宋体]mL/min[/font][font=宋体]时,[/font][font=宋体]保留时间[/font][font=宋体]缩短[/font][font=宋体]1.3min,[/font][font=宋体]峰分离度从[/font][font=宋体]1.98下降至1.77[/font][font=宋体];对于巴比妥酸,[/font][font=宋体]当[/font][font=宋体]淋洗液流量[/font][font=宋体]从[/font][font=宋体]0.8[/font][font=宋体]mL/min[/font][font=宋体]上升至[/font][font=宋体]1.0[/font][font=宋体]mL/min[/font][font=宋体]时,[/font][font=宋体]保留时间[/font][font=宋体]缩短[/font][font=宋体]2.3min,[/font][font=宋体]峰分离度从[/font][font=宋体]4.04下降至3.90[/font][font=宋体],[/font][font=宋体]当[/font][font=宋体]淋洗液流量[/font][font=宋体]从[/font][font=宋体]1.0[/font][font=宋体]mL/min[/font][font=宋体]上升至[/font][font=宋体]1.2[/font][font=宋体]mL/min[/font][font=宋体]时,[/font][font=宋体]保留时间[/font][font=宋体]缩短[/font][font=宋体]1.6min,[/font][font=宋体]峰分离度从[/font][font=宋体]3.90下降至3.75。同时,[/font][font=宋体]淋洗液流量[/font][font=宋体]每增加[/font][font=宋体]0.20[/font][font=宋体]mL/min[/font][font=宋体]巴比妥酸和硝酸盐的[/font][font=宋体][font=宋体]峰面积约下降[/font]18%-20%。[/font][font=宋体]在保证目标分析物与其他离子良好分离的前提下,以使组分有较短的保留时间[/font][font=宋体]、较高的[/font][font=宋体]峰分离度和检测灵敏度、[/font][font=宋体]系统有较低的压力,[/font][font=宋体]综合考虑,确定[/font][font=宋体]淋洗液[/font][font=宋体]流量为[/font][font=宋体]1.0mL/min。[/font][b][font=宋体]2.1.4[/font][/b][font=宋体] 柱箱温度的选择[/font][font=宋体]试验了柱箱温度[/font][font=宋体]为[/font][font=宋体]30℃、35℃、40℃时各组分的分离效果,结果显示,随着柱温的升高,[/font][font=宋体]巴比妥酸和硝酸盐[/font][font=宋体]的[/font][font=宋体]保留时间稍微[/font][font=宋体]缩短[/font][font=宋体],峰面积逐渐增加,[/font][font=宋体]对于[/font][font=宋体]硝酸盐,当[/font][font=宋体][font=宋体]柱温从[/font]30℃上升到35℃时峰面积增加6[/font][font=宋体].7[/font][font=宋体]%,[/font][font=宋体][font=宋体]从[/font]35℃上升到40℃时,[/font][font=宋体]峰面积增加[/font][font=宋体]5.6[/font][font=宋体]%,[/font][font=宋体]对于[/font][font=宋体]巴比妥酸,当[/font][font=宋体][font=宋体]柱温从[/font]30℃上升到35℃时峰面积增加[/font][font=宋体]4.4[/font][font=宋体]%,[/font][font=宋体][font=宋体]但从[/font]35℃上升到40℃时,峰面积[/font][font=宋体]仅[/font][font=宋体]增加[/font][font=宋体]1.6%[/font][font=宋体],[/font][font=宋体]这与[/font][font=宋体]邻苯二甲酸根[/font][font=宋体]的试验结果[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体][font=宋体]8[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体]类似[/font][font=宋体],同时硝酸盐的的峰分离度逐渐降低[/font][font=宋体],分别为1.94、1.78和1.65,[/font][font=宋体]巴比妥酸的峰分离度则逐渐增加,分别为[/font][font=宋体]3.62、3.80和4.54,[/font][font=宋体]综合考虑待测组分[/font][font=宋体]的检测灵敏度[/font][font=宋体]和峰分离度[/font][font=宋体],[/font][font=宋体]本试验[/font][font=宋体]选择[/font][font=宋体]的[/font][font=宋体][font=宋体]柱箱温度为[/font]35℃。[/font][b][font=宋体]2.2[/font][/b][font=宋体]共存物质的影响[/font][font=宋体] [font=宋体]分别取[/font]1.1所列各种[/font][font=宋体]标准溶液配制成含巴比妥酸[/font][font=宋体]20[/font][font=宋体]mg/L[/font][font=宋体]、[/font][font=宋体]硝酸盐[/font][font=宋体]、[/font][font=宋体]磷酸盐[/font][font=宋体]各[/font][font=宋体]10[/font][font=宋体]mg/L[/font][font=宋体]、[/font][font=宋体]氯化物、溴化物、硫酸盐[/font][font=宋体]、亚[/font][font=宋体]硝酸盐[/font][font=宋体]各[/font][font=宋体]5[/font][font=宋体]mg/L、氟化物[/font][font=宋体]3[/font][font=宋体]mg/L[/font][font=宋体]的混合标准溶液,[/font][font=宋体][font=宋体]取[/font]1.5mL于样品瓶中,启动自动进样器进样[/font][font=宋体]测定,以[/font][font=宋体]考察[/font][font=宋体]巴比妥酸和[/font][font=宋体]硝酸盐与[/font][font=宋体]前述[/font][font=宋体]6种常见阴离子的[/font][font=宋体]分离效果[/font][font=宋体],[/font][font=宋体]结果见图[/font][font=宋体]1[/font][font=宋体],[/font][font=宋体]从图[/font][font=宋体]1可知,[/font][font=宋体]在本试验条件下,[/font][font=宋体]巴比妥酸和[/font][font=宋体]硝酸盐与[/font][font=宋体]前述[/font][font=宋体]6种常见[/font][font=宋体]阴离子可以完全分离,[/font][font=宋体]其中[/font][font=宋体]磷酸盐[/font][font=宋体]与[/font][font=宋体]硫酸盐[/font][font=宋体]不能完全分离[/font][font=宋体],[/font][font=宋体]除[/font][font=宋体]磷酸盐[/font][font=宋体]与[/font][font=宋体]硫酸盐外,其余[/font][font=宋体]组分[/font][font=宋体]的出峰顺序均在待测物之前,均不影响[/font][font=宋体]巴比妥酸和[/font][font=宋体]硝酸盐[/font][font=宋体]的测定。[/font][align=center][img=,484,358]https://ng1.17img.cn/bbsfiles/images/2021/10/202110251215077925_9467_3389662_3.jpg!w484x358.jpg[/img][font=宋体] [/font][/align][align=center][font=宋体]图[/font][font=宋体]1[/font][font=宋体]巴比妥酸和[/font][font=宋体]硝酸盐[/font][font=宋体]与[/font][font=宋体]常见阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]图[/font][/align][b][font=宋体]2.3 [/font][/b][font=宋体]线性方程、线性范围与检出限[/font][font=宋体][font=宋体]按照[/font]1.[/font][font=宋体]3[/font][font=宋体].1配制标准系列,测定[/font][font=宋体]巴比妥酸和[/font][font=宋体]硝酸盐[/font][font=宋体]的峰面积[/font][font=宋体],以[/font][font=宋体]峰面积[/font][font=宋体]([/font][i][font=宋体]y[/font][/i][font=宋体])[/font][font=宋体]为纵坐标[/font][font=宋体],[/font][font=宋体]以[/font][font=宋体]其质量[/font][font=宋体]浓度[/font][font=宋体]([/font][i][font=宋体]x[/font][/i][font=宋体])[/font][font=宋体]为横坐标绘制标准曲线,进行线性回归。测定[/font][font=宋体][font=宋体]仪器[/font]30min的基线噪声[/font][sup][font=宋体][font=宋体][[/font][/font][/sup][sup][font=宋体][font=宋体]16[/font][/font][/sup][sup][font=宋体][font=宋体]][/font][/font][/sup][font=宋体],[/font][font=宋体]以[/font][font=宋体]3倍[/font][font=宋体]基线噪声[/font][font=宋体]除以标准曲线的斜率[/font][font=宋体]([/font][i][font=宋体]3N[/font][font=宋体]/[/font][font=宋体]b[/font][/i][font=宋体])计算[/font][font=宋体]巴比妥酸和[/font][font=宋体]硝酸盐[/font][font=宋体]的最低检出限。其标准曲线的线性范围、回归方程、相关系数[/font][i][font=宋体]r[/font][/i][font=宋体](回归方程的截距、斜率和[/font][i][font=宋体]r[/font][/i][font=宋体]均由仪器软件自动生成)[/font][font=宋体]、检出限[/font][font=宋体]列于表[/font][font=宋体]3[/font][font=宋体][font=宋体]。从表[/font]1可见,[/font][font=宋体]巴比妥酸[/font][font=宋体]的峰面积与其[/font][font=宋体]质量[/font][font=宋体][font=宋体]浓度在[/font]0.[/font][font=宋体]1[/font][font=宋体]0~50.0mg/L范围内呈良好的线性关系,相关系数r[/font][font=宋体]分别[/font][font=宋体]为[/font][font=宋体]0.9999[/font][font=宋体],硝酸盐[/font][font=宋体]的峰面积与其[/font][font=宋体]质量[/font][font=宋体]浓度[/font][font=宋体]分别[/font][font=宋体][font=宋体]在[/font]0.[/font][font=宋体]1[/font][font=宋体]0~[/font][font=宋体]3[/font][font=宋体]0.0mg/L[/font][font=宋体]和[/font][font=宋体]30.0[/font][font=宋体]~[/font][font=宋体]5[/font][font=宋体]0.0mg/L范围内呈良好的线性关系,相关系数r[/font][font=宋体]分别[/font][font=宋体]为[/font][font=宋体]0.9994和[/font][font=宋体]0.999[/font][font=宋体]9[/font][font=宋体],[/font][font=宋体]检出限分别[/font][font=宋体][font=宋体]为[/font]0.10mg/L[/font][font=宋体]和[/font][font=宋体]0.03[/font][font=宋体]mg/L。其中,10mg/L的[/font][font=宋体]巴比妥酸和[/font][font=宋体]硝酸盐[/font][font=宋体]的标准色谱图见图[/font][font=宋体]2[/font][font=宋体]。[/font][align=center][font=宋体]表[/font][font=宋体]3[/font][font=宋体]巴比妥酸和[/font][font=宋体]硝酸盐[/font][font=宋体]的[/font][font=宋体]线性范围、回归方程、相关系数[/font][font=宋体]和检出限[/font][/align][table][tr][td][align=center][font=宋体]组分[/font][/align][/td][td][align=center][font=宋体][font=宋体]线性范围[/font]/[/font][font=宋体]mgL[/font][sup][font=宋体][font=宋体]-1[/font][/font][/sup][/align][/td][td][align=center][font=宋体]线性方程[/font][/align][/td][td][align=center][font=宋体]相关系数[/font][/align][/td][td][align=center][font=宋体][font=宋体]检出限[/font]/mgL[/font][sup][font=宋体][font=宋体]-1[/font][/font][/sup][/align][/td][/tr][tr][td][align=center][font=宋体]巴比妥酸[/font][/align][/td][td][align=center][font=宋体]0.10~50.0[/font][/align][/td][td][align=center][i][font=宋体]y[/font][/i][font=宋体]=4081+39810[/font][i][font=宋体]x[/font][/i][/align][/td][td][align=center][font=宋体]0.9999[/font][/align][/td][td][align=center][font=宋体]0.10 [/font][/align][/td][/tr][tr][td][align=center][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][/align][/td][td][align=center][font=宋体]0.10~30.0[/font][/align][/td][td][align=center][i][font=宋体]y[/font][/i][font=宋体]=207000[/font][i][font=宋体]x-[/font][/i][font=宋体]25020[/font][/align][/td][td][align=center][font=宋体]0.9994[/font][/align][/td][td][align=center][font=宋体]0.03[/font][/align][/td][/tr][tr][td][align=center][font=宋体] [/font][/align][/td][td][align=center][font=宋体]30.0~50.0[/font][/align][/td][td][align=center][i][font=宋体]y[/font][/i][font=宋体]=1160000+171000[/font][i][font=宋体]x[/font][/i][/align][/td][td][align=center][font=宋体]0.9999[/font][/align][/td][td][align=center][font=宋体] [/font][/align][/td][/tr][tr][td][align=center][font=宋体] [/font][/align][/td][td][align=center][font=宋体]0.10~50.0[/font][/align][/td][td][align=center][i][font=宋体]y[/font][/i][font=宋体]=24740+198300[/font][i][font=宋体]x[/font][/i][/align][/td][td][align=center][font=宋体]0.9993[/font][/align][/td][td][align=center][font=宋体] [/font][/align][/td][/tr][/table][align=center][img=,481,346]https://ng1.17img.cn/bbsfiles/images/2021/10/202110251215449342_2235_3389662_3.jpg!w481x346.jpg[/img][font=宋体] [/font][/align][align=center][font=宋体]图[/font][font=宋体]2[/font][font=宋体]巴比妥酸和[/font][font=宋体]硝酸盐[/font][font=宋体]的标准色谱图[/font][/align][b][font=宋体]2.[/font][font=宋体]4[/font][/b][font=宋体]样品测定及加标[/font][font=宋体]回收试验[/font][font=宋体]按[/font][font=宋体]1.3.3、1.3.4的步骤操作,[/font][font=宋体]测定[/font][font=宋体]巴比妥、维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]和[/font][font=宋体]苯巴比妥[/font][font=宋体]等样品中的巴比妥酸和硝酸盐[/font][font=宋体]的含量[/font][font=宋体]。并在[/font][font=宋体]3种样中分别添加1.0、5.0、10.0[/font][font=宋体]mg/L[/font][font=宋体]的[/font][font=宋体]巴比妥酸和硝酸盐[/font][font=宋体],平行测定[/font][font=宋体]5次,计算加标回收率及测定结果的相对标准偏差[/font][font=宋体][font=宋体]([/font]RSD)[/font][font=宋体],[/font][font=宋体]结果见表[/font][font=宋体]4[/font][font=宋体]。[/font][font=宋体]由表[/font][font=宋体]4可知,[/font][font=宋体]巴比妥、苯巴比妥和维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]等[/font][font=宋体]3种样品中[/font][font=宋体]硝酸盐[/font][font=宋体]的测定结果在[/font][font=宋体]0.15[/font][font=宋体]~[/font][font=宋体]0.22[/font][font=宋体]mg/L[/font][font=宋体],加标回收率在[/font][font=宋体]98.0%[/font][font=宋体]~[/font][font=宋体]101.3%,测定结果的相对标准偏差为1.21%[/font][font=宋体]~[/font][font=宋体]2.66%,[/font][font=宋体]巴比妥酸含量均[/font][font=宋体]0.10[/font][font=宋体]mg/L[/font][font=宋体],加标回收率在[/font][font=宋体]90.4%[/font][font=宋体]~[/font][font=宋体]101.4%,测定结果的相对标准偏差为1.71%[/font][font=宋体]~[/font][font=宋体]2.39%,方法的回收率较高、重现性良好。其中苯[/font][font=宋体]巴比妥[/font][font=宋体]加标[/font][font=宋体]样品[/font][font=宋体]色谱图见图[/font][font=宋体]3[/font][font=宋体]。[/font][align=center][img=,455,345]https://ng1.17img.cn/bbsfiles/images/2021/10/202110251216039913_5283_3389662_3.jpg!w455x345.jpg[/img][font=宋体] [/font][/align][align=center][font=宋体]图[/font][font=宋体]3[/font][font=宋体] 苯巴比妥[/font][font=宋体]加标[/font][font=宋体]样品色谱图[/font][/align][align=center][font=宋体]表[/font][font=宋体]4[/font][font=宋体] [/font][font=宋体]巴比妥、苯巴比妥和维生素[/font][font=宋体]B12样品[/font][font=宋体]测定及加标回收试验结果[/font][/align][table][tr][td][align=center][font=宋体]样品名称[/font][/align][/td][td][align=center][font=宋体]组分[/font][/align][/td][td][align=center][font=宋体][font=宋体]本底值/([/font]mgL[/font][sup][font=宋体][font=宋体]-1[/font][/font][/sup][font=宋体])[/font][/align][/td][td][align=center][font=宋体][font=宋体]加入量/([/font]mgL[/font][sup][font=宋体][font=宋体]-1[/font][/font][/sup][font=宋体])[/font][/align][/td][td][align=center][font=宋体]测得量/[/font][/align][align=center][font=宋体][font=宋体]([/font]mgL[/font][sup][font=宋体][font=宋体]-1[/font][/font][/sup][font=宋体])[/font][/align][/td][td][align=center][font=宋体][font=宋体]回收率[/font]/%[/font][/align][/td][td][align=center][font=宋体]RSD/%[/font][/align][/td][/tr][tr][td][align=center][font=宋体]1250[/font][font=宋体]mg/[/font][font=宋体]L[/font][font=宋体]巴比妥[/font][/align][/td][td][align=center][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][/align][align=center][font=宋体]巴比妥酸[/font][/align][/td][td][align=center][font=宋体]0.21[/font][/align][align=center][font=宋体]0.10mg/L[/font][/align][/td][td][align=center][font=宋体]1.0[/font][/align][/td][td][align=center][font=宋体]1.14,1.20,1.18,1.21,1.22[/font][/align][align=center][font=宋体]0.893,0.901,0.904,886,0.937[/font][/align][/td][td][align=center][font=宋体]98.0[/font][/align][align=center][font=宋体]90.4[/font][/align][/td][td][align=center][font=宋体]2.66[/font][/align][align=center][font=宋体]2.17[/font][/align][/td][/tr][tr][td][align=center][font=宋体]1000[/font][font=宋体]mg/[/font][font=宋体]L[/font][font=宋体]苯巴比妥[/font][/align][/td][td][align=center][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][/align][align=center][font=宋体]巴比妥酸[/font][/align][/td][td][align=center][font=宋体]0.15[/font][/align][align=center][font=宋体]0.10mg/L[/font][/align][/td][td][align=center][font=宋体]10[/font][font=宋体].0[/font][/align][/td][td][align=center][font=宋体]9.94,10.13,10.16,10.21,10.26[/font][/align][align=center][font=宋体]9.95,10.01,10.39,10.17,10.20[/font][/align][/td][td][align=center][font=宋体]99.0[/font][/align][align=center][font=宋体]101.4[/font][/align][/td][td][align=center][font=宋体]1.21[/font][/align][align=center][font=宋体]1.71[/font][/align][/td][/tr][tr][td][align=center][font=宋体]20[/font][font=宋体]mg/[/font][font=宋体]L[/font][font=宋体]维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][/align][/td][td][align=center][font=宋体]NO[/font][sub][font=宋体][font=宋体]3[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][/align][align=center][font=宋体]巴比妥酸[/font][/align][/td][td][align=center][font=宋体]0.22[/font][/align][align=center][font=宋体]0.10mg/L[/font][/align][/td][td][align=center][font=宋体]5[/font][font=宋体].0[/font][/align][/td][td][align=center][font=宋体]5.30,5.16,5.35,5.38,5.23[/font][/align][align=center][font=宋体]5.10,4.98,4.85,4.87,4.81[/font][/align][/td][td][align=center][font=宋体]101.3[/font][/align][align=center][font=宋体]98.4[/font][/align][/td][td][align=center][font=宋体]1.70[/font][/align][align=center][font=宋体]2.39[/font][/align][/td][/tr][/table][b][font=宋体]3 结语[/font][/b][font=宋体]1)[/font][font=宋体][font=宋体]建立了以[/font]SH-AC-3型阴离子交换柱为分离柱,以[/font][font=宋体]5[/font][font=宋体].0 mmol/L Na2CO3溶液为淋洗液,流量为1.0 mL/min等度洗脱,[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]-抑制电导检测法同时测定巴比妥酸和硝酸盐的新方法。方法应用于巴比妥、苯巴比妥和维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]等样品中[/font][font=宋体]巴比妥酸和硝酸盐同时的测定,加标回收率分别为[/font][font=宋体]90.4%[/font][font=宋体]~[/font][font=宋体]101.4%和98.0%[/font][font=宋体]~[/font][font=宋体]101.3%,5次平行测定结果的相对标准偏差[/font][font=宋体][font=宋体]([/font]RSD)小于[/font][font=宋体]3%,巴比妥酸和硝酸盐的[/font][font=宋体][font=宋体]最低检出限分别为[/font]0.10mg/L和[/font][font=宋体]0.03[/font][font=宋体]mg/L[/font][font=宋体],[/font][font=宋体]方法回收率较高、重现性良好,操作简便快速,可用于巴比妥、苯巴比妥和维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]12[/font][/font][/sub][font=宋体]等样品中微量[/font][font=宋体]巴比妥酸和硝酸盐的定量分析。[/font][font=宋体]参考文献[/font][font=宋体]2)[/font][font=宋体]刘琪,梅洪波,刘野,等[/font][font=宋体].[/font][font=宋体]镇静催眠药巴比妥酸的合成研究[/font][font=宋体][J],[/font][font=宋体]辽宁化工[/font][font=宋体][font=宋体],[/font]201[/font][font=宋体]9[/font][font=宋体],[/font][font=宋体]48[/font][font=宋体]([/font][font=宋体]1[/font][font=宋体]):[/font][font=宋体]33[/font][font=宋体]3)[/font][font=宋体]李正化[/font][font=宋体].[/font][font=宋体]药物化学[/font][font=宋体][[/font][font=宋体]M[/font][font=宋体]][/font][font=宋体].[/font][font=宋体]北京:人民卫生出版社,[/font][font=宋体]1979:33[/font][font=宋体]4)[/font][font=宋体][font=宋体]钟莺莺[/font],陈平,俞雪钧,[/font][font=宋体]等[/font][font=宋体].[/font][font=宋体]改进的离子色普法测定乳制品中亚硝酸盐和硝酸盐[/font][font=宋体][J],[/font][font=宋体]色谱[/font][font=宋体][font=宋体],[/font]201[/font][font=宋体]2[/font][font=宋体],[/font][font=宋体]30[/font][font=宋体]([/font][font=宋体]6[/font][font=宋体]):[/font][font=宋体] [font=宋体]636[/font][/font][font=宋体]5)[/font][font=宋体][font=宋体]陈柳生[/font],蔡自由,周伟明[/font][font=宋体].[/font][font=宋体]离子色普法测定维生素[/font][font=宋体]B[/font][sub][font=宋体][font=宋体]1[/font][/font][/sub][font=宋体][font=宋体]注射液中的[/font]EDTA及硝酸根离子[/font][font=宋体][J],[/font][font=宋体]中国实验方剂学杂志[/font][font=宋体][font=宋体],[/font]201[/font][font=宋体]4[/font][font=宋体],[/font][font=宋体]20[/font][font=宋体]([/font][font=宋体]14[/font][font=宋体]):[/font][font=宋体]61[/font][font=宋体]6)[/font][font=宋体]国家药典委员会[/font][font=宋体].[/font][font=宋体]中华人民共和国药典[/font][font=宋体] [/font][font=宋体]二部[/font][font=宋体][[/font][font=宋体]S[/font][font=宋体]][/font][font=宋体].[/font][font=宋体]北京:中国医药科技出版社,[/font][font=宋体]2010:896[/font][font=宋体]7)[/font][font=宋体]罗挽兰,高华,何治柯,等[/font][font=宋体].[/font][font=宋体]钌[/font][font=宋体]([/font][font=宋体]Ⅱ)-联吡啶-巴比妥酸-Ce(Ⅳ)化学发光体系测定巴比妥酸的[/font][font=宋体]研究[/font][font=宋体][J],[/font][font=宋体]分析科学学报[/font][font=宋体],[/font][font=宋体]1996[/font][font=宋体],[/font][font=宋体]12[/font][font=宋体]([/font][font=宋体]2[/font][font=宋体]):[/font][font=宋体]142[/font][font=宋体]8)[/font][font=宋体]黄选忠,郑林[/font][font=宋体].[/font][font=宋体][font=宋体]巴比妥酸[/font]-NO[/font][sub][font=宋体][font=宋体]2[/font][/font][/sub][sup][font=宋体][font=宋体]-[/font][/font][/sup][font=宋体]-Fe[/font][font=宋体]([/font][font=宋体]Ⅱ)-CPB显色体系光度测定巴比妥酸的[/font][font=宋体]研究[/font][font=宋体][J],[/font][font=宋体]分析科学学报[/font][font=宋体],[/font][font=宋体]1999[/font][font=宋体],[/font][font=宋体]15[/font][font=宋体]([/font][font=宋体]3[/font][font=宋体]):[/font][font=宋体]238[/font][font=宋体]9)[/font][font=宋体]李红江[/font][font=宋体].[/font][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定[/font][font=宋体]实验室废水中[/font][font=宋体]邻苯二甲酸根[/font][font=宋体][J],[/font][font=宋体]化学[/font][font=宋体]分析[/font][font=宋体]计量[/font][font=宋体][font=宋体],[/font]20[/font][font=宋体]21[/font][font=宋体][font=宋体],[/font]3[/font][font=宋体]0[/font][font=宋体]([/font][font=宋体]6[/font][font=宋体]):[/font][font=宋体]31[/font][font=宋体]9)[/font][font=宋体]张丽,黄选忠,杜宏山[/font][font=宋体].[/font][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[/font][font=宋体]同时[/font][font=宋体]测定尿液中草酸[/font][font=宋体]和硫氰酸盐[/font][font=宋体][J],[/font][font=宋体]化学[/font][font=宋体]分析[/font][font=宋体]计量[/font][font=宋体][font=宋体],[/font]20[/font][font=宋体]21[/font][font=宋体][font=宋体],[/font]3[/font][font=宋体]0[/font][font=宋体]([/font][font=宋体]2[/font][font=宋体]):[/font][font=宋体] [font=宋体]46[/font][/font][font=宋体]10)[/font][font=宋体][font=宋体]蒋越华,陈永森,金刚,等[/font].[/font][font=宋体]离子交换色谱法测定西番莲中有机酸[/font][font=宋体][J],化学分析计量,20[/font][font=宋体]18[/font][font=宋体],[/font][font=宋体]27[/font][font=宋体]([/font][font=宋体]6[/font][font=宋体]):[/font][font=宋体]47[/font][font=宋体]11)华丰[/font][font=宋体].[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定灵芝超声水提取物中4种代表有机酸的含量[J],生物加工过程,20[/font][font=宋体]21[/font][font=宋体],[/font][font=宋体]19[/font][font=宋体]([/font][font=宋体]1[/font][font=宋体]):[/font][font=宋体]74[/font][font=宋体]12)郭柏坤,周垚[/font][font=宋体].[/font][url=https://netl.istic.ac.cn/site/link?cdoi=0120191200702074&mid=466496091303411EB27FB4298C9BA46C][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定水果中的有机酸[/font][/url][font=宋体][J],发酵科技通讯,20[/font][font=宋体]18[/font][font=宋体],[/font][font=宋体]38[/font][font=宋体]([/font][font=宋体]3[/font][font=宋体]):[/font][font=宋体]170[/font][font=宋体]13)[/font][url=https://netl.istic.ac.cn/site/s?f=1&mid=466496091303411EB27FB4298C9BA46C&fieldid=C6ADB01393364592A3C34A78BFC163F3&q=%E7%BA%AA%E5%87%A4%E5%A8%A3][font=宋体]纪凤娣[/font][/url][font=宋体],[/font][url=https://netl.istic.ac.cn/site/s?f=1&mid=466496091303411EB27FB4298C9BA46C&fieldid=C6ADB01393364592A3C34A78BFC163F3&q= %E5%A4%8F%E8%93%89][font=宋体]夏蓉[/font][/url][font=宋体],[/font][url=https://netl.istic.ac.cn/site/s?f=1&mid=466496091303411EB27FB4298C9BA46C&fieldid=C6ADB01393364592A3C34A78BFC163F3&q= %E9%99%B6%E6%B1%87%E6%BA%90][font=宋体]陶汇源[/font][/url][font=宋体],[/font][font=宋体][font=宋体]等[/font].[/font][font=宋体] [/font][url=https://netl.istic.ac.cn/site/link?cdoi=0120201001064937&mid=466496091303411EB27FB4298C9BA46C][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法测定食醋及其制品中有机酸的分析方法[/font][/url][font=宋体][J],食品科学,2020,41(18):239[/font][font=宋体]14)宋卫得,李兆杰,刘冰,[/font][font=宋体][font=宋体]等[/font].[/font][font=宋体][font=宋体][url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法同时测定葡萄酒中[/font]26种有机酸和阴离子[J],酿酒科技,2018,41(4):106[/font][font=宋体]15)[/font][font=宋体][font=宋体]许春向,邹学贤[/font].现代卫生化学[M].北京:人民卫生出版社,2000:491[/font][font=宋体]16)[/font][font=宋体]JJG823-2014 中华人民共和国国家计量检定规程 [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url][/font][font=宋体][s][/s][/font][s][font=宋体] [/font][/s]
各位坛友大家好,我用异烟酸巴比妥酸法做了一条氰化物曲线,用57.9微克每升的质控按证书上的方法稀释蒸馏以后按照标准分析步骤操作后扣除空白吸光度是0.114,代入曲线后乘上V1除以V*V2后数值很小,我想请问一般是是蒸馏步骤出了问题浓度偏低还是计算方法不对。我曲线是y=0.1507x+0.0047
摘 要:目的探讨饮用水中氯化氰的检验方法。方法采用吡啶一巴比妥酸光度法测定饮用水中氯化氰,对溶液的pH值、显色剂的配比、样品稳定性、氯胺T的加入量、显色反应时间和最大吸收波长等进行优化。结果该方法的线性范围为0~0.1μg/ml,相关系数为0.9994,回归方程为y=0.194x一0.033,检出限为0.003 μg/ml,测定下限为0.0l mg/L,相对标准偏差在1.5%-6.2%之间,回收率为92.9%一107.1%。结论该方法准确、灵敏、简便、快速,满足《生活饮用水卫生规范)(2001)的要求。[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=102566]饮用水中氯化氰的吡啶一巴比妥酸分光光度测定法[/url]
作者单位:北京市机电研究院环境保护技术研究所母体文献:第一届环境保护学术年会论文集会议名称:第一届环境保护学术年会 会议时间:1989年6月1日会议地点:北京主办单位:中国机械工程学会,中国环境保护学会【题名】:吡啶-巴比妥酸分光光度法测定氰化物方法的改进这里有个链接 http://d.wanfangdata.com.cn/Conference_89384.aspx
The approach to the Garden sloped like a hillside and the several parts of the structure rose from one another tier on tier...On all this, the earth had been piled...and was thickly planted with trees of every kind that, by their great size and other charm, gave pleasure to the beholder...The water machines(raised) the water in great abundance from the river, although no one outside could see it. ——Diodorus Siculus ruits and flowers... Waterfalls... Gardens hanging from the palace terraces... Exotic animals...This is the picture of the Hanging Gardens of Babylon in most people's minds.It may be surprising to know that they might have never existed except in the minds of Greek poets and historians! Location On the east bank of the River Euphrates, about 50 km south of Baghdad, Iraq. History The Babylonian kingdom flourished under the rule of the famous King, Hammurabi[2] (1792-1750 BC[3]).It was not until[4] the reign of the Neo-Babylonian dynasty that the Mesopotamian [5] civilization reached its ultimate glory.Nebuchadnezzar II[6] (604-562 BC) is credited for building the legendary Hanging Gardens.It is said that the Gardens were built by Nebuchadnezzar to please his wife or concubinewho had been "brought up in Media[7] and had a passion for mountain surroundings".While the most descriptive accounts of the Gardens come from Greek historians such as Berossus and Diodorus Siculus,Babylonian records stay silent on the matter.Tablets from the time of Nebuchadnezzar do not have a single reference to the Hanging Gardens,although descriptions of his palace, the city of Babylon, and the walls are found.Even the historians who give detailed descriptions of the Hanging Gardens never saw them.Modern historians argue that when Alexander[8] 's soldiers reached the fertile land of Mesopotamia and saw Babylon, they were impressed.When they later returned to their rugged homeland, they had stories to tell about the amazing gardens and palm trees at Mesopotamia...About the palace of Nebuchadnezzar... About the Tower of Babel[9] and the ziggurats.And it was the imagination of poets and ancient historians that blended all these elements together to produce one of the World Wonders.It wasn't until the twentieth century that some of the mysteries surrounding the Hanging Gardens were revealed.Archaeologists are still struggling to gather enough evidence before reaching the final conclusions about the location of the Gardens, their irrigation system, and their true appearance.注释: 1.Babylon:古代西亚两河流域的最大城市,古巴比伦王国与新巴比伦王国的首都。位于幼发拉底河中游,距今巴格达南约89公里。“空中花园”位于新巴比伦王国的都城中。 2.Hammurabi:汉谟拉比(公元前1792~1750)古巴比伦王国第六代国王。他在位其间,重新统一了两河流域。实行中央集权统治,兴修水利,发展经济。颁布有名的《汉谟拉比法典》。 3.BC:BC是“公元前”、AD是“公元后”。你知道为什么有公元前和公元后之分吗?其实公元记年是由后来的一位知识渊博的大主教发明的,以基督(Christ)的出生为分界线来划分。BC 就是Before Christ;而AD来自拉丁文anno Domini(=Since Christ was born)。 4.It was not until...:这个句子看起来挺让人迷惑,其实这是...not ...unitil...(直到……才……)的强调句型。It is ...that...是英语的情调句型。比如:It's man that counts.(出自《实用英语语法》)起作用的是人。强调...not ...unitil...时,是把not和 until引导的从句放在that 前。 5.Mesopotamian:美索不达米亚,西亚一古地区,地处幼发拉底河和底格里斯河之间,是世界文明发祥地之一。公元前4000年苏美尔人在南美索不达尼亚建立起世界最早的文明,约公元前2340年,阿卡帝国首次兴起,此后巴比伦和亚述两帝国相继崛起。 6.NebuPage: 1 chadnezzar II:尼布甲尼撒二世(前605~前562),新巴比伦王国国王。即位后,大举进攻腓尼基和巴勒斯坦,与埃及争夺势力范围。公元前586年攻陷耶路撒冷,灭犹太王国,俘虏大批犹太居民。前567年远征埃及,并掠夺大量财富,是为新巴比伦王国鼎盛时期。 7.Media:米底,西亚古国,在今伊朗西部和阿塞拜疆东部地区。 8.lexander the Great:亚历山大大帝(前356~前323)马其顿国王。前334年以无敌之师大举东进,入小亚细亚,转埃及,建立亚历山大城,挺进两河流域,入侵中亚细亚,南下印度。后因气候不适,士兵厌战而退兵巴比伦。前324年,建立了以亚历山大城为中心的东起印度河、西至尼罗河与巴尔干半岛领域的古代大帝国——亚历山大帝国。 9.the Tower of Babel:巴别塔,据《圣经旧约》,诺亚在巴比伦的子孙想建造一座“塔顶通天”的塔以扬名,同时反抗上帝。上帝便变乱他们原来统一的语言,使之互不相通,结果塔未能建成,而人类分散到世界各地。 巴比伦的空中花园 通往花园的道路象山坡一样倾斜着,建筑物的几个部分一层一层地向上交错排列着……泥土在这些上面堆积着……并且浓密地种植着各种各样的树木,它们以其巨大的身躯和其他一些魅力,令观赏者赏心悦目……抽水的机器把大量的水从河中(提升到)上面,尽管没有人从外面能看到它。 ——Diodorus Siculus 水果与鲜花……、瀑布……、花园高悬在宫殿的阳台上……、奇异的动物……,这是大多数人想象中的巴比伦空中花园。让人吃惊的是空中花园除了在希腊的诗人和历史学家的头脑中出现过外,可能从来就没有存在过。 位置: 位于幼发拉底河的东岸,距伊拉克的首都巴格达南约50公里。 历史: 古巴比伦王国在著名的国王汉谟拉比(公元前1792~1750)的统治下曾经繁荣一时。但是直到新巴比伦王朝,美索不达米亚文明才达到了它的鼎盛时期。人们相信传说中的空中花园是由尼布甲尼撒二世(公元前604年~562年)建造的。据传,尼布甲尼撒为了取悦于其在米底亚长大并对山景怀有深厚感情的王后或者是妃子而建造了空中花园。 虽然对花园最详尽的记述是出自Berossus 和 Diodorus Siculus等希腊历史学家笔下, 但巴比伦的历史记录却对此事只字未提。尽管在尼布甲尼撒时期存留下的各种书写板上发现了对他的宫殿、巴比伦城以及巴比伦的城墙的种种描述,但这些书写板上却没有一处提到过空中花园。甚至那些对空中花园进行过详细描述的历史学家们也从没有亲眼目睹过它们。现代历史学家争论说:当亚力山大的士兵们到达了富饶的美索不达米亚地区并看到了巴比伦时,他们深为(眼前的美景)所震撼。当他们后来回到崎岖不平的家乡时,带回了有关美索不达米亚的令人惊叹的花园和椰子树……、有关尼布甲尼撒的宫殿……以及有关巴别塔和金字型神塔的各种故事。是诗人和古代历史学家的想象力把这所有的元素混合在一起制造出了世界奇观之一。 直到二十世纪,围绕着空中花园的一些不解之迷才被揭示出来。在得到关于花园的地理位置、灌溉系统,和真正面目的最终结论之前,考古学家们仍在努力地收集足够的证据。
为什么用反相高效液相色谱分离巴比妥与苯巴比妥时,是巴比妥先出峰?
丙二醛/TBARs/硫代巴比妥酸/MDA (这些名字都可以描述为同一个东西)。作为水产品重要氧化指标之一,按照国标方法进行实验,90℃,水浴1h后溶液不显示粉红色,显示微微黄色。在酶标仪的吸光值也极其微弱。请问这是什么原因?
总氰化物分析用滴定法测为3.5毫克/升,用吡啶巴比妥酸不显色,请专家指点
巴比妥酸和硫代巴比妥酸[align=center]在SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱上色谱特性总结分析[/align][align=center]十月[/align]巴比妥酸(BA)又称丙二酰脲或2,4,6-嘧啶三酮,硫代巴比妥酸(TBA)又称为[color=#222222]4,6-二羟基-2-巯基嘧啶或[/color]丙二酰缩硫脲[color=#222222],[/color]二者均可用作[color=#222222]化学分析或生化试剂[/color]、塑料和染料及巴比妥类药物、维生素B[sub]12[/sub]等药品的的中间体,[color=#222222]在实验室和制药企业应用广泛,均[/color]溶于热水,在水溶液中BA和TBA均离解成阴离子状态。SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱是[color=black]青岛盛瀚色谱技术公司开发生产的一款疏水型、碳酸盐分离体系阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱。[/color]曾成功应用于[color=black]BrO[/color][sub][color=black]3[/color][/sub][sup][color=black]-[/color][/sup][color=black]、ClO[/color][sub][color=black]3[/color][/sub][sup][color=black]-[/color][/sup][color=black]、ClO[/color][sub][color=black]2[/color][/sub][sup][color=black]-[/color][/sup]、[color=black]ClO[/color][sub][color=black]4[/color][/sub][sup][color=black]-[/color][/sup][color=black]、[/color]BA、TBA、[color=black]三氯乙酸等成分的测定。[/color]现将BA和TBA在SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱上色谱特性总结分析如下:1、BA在不同淋洗条件下的峰分离度及其与各组分的分离情况:试验结果见表1,从表1可见,随着淋洗液中NaHCO[sub]3[/sub]浓度的增加,BA的峰分离度(R)从3.97缓慢下降至3.16,但仍在1.5以上,当以[color=black]6.0mmol/LNa[/color][sub][color=black]2[/color][/sub][color=black]CO[/color][sub][color=black]3[/color][/sub][color=black]-1.0mmol/L[/color]NaHCO[sub]3[/sub][color=black]溶液为[/color]淋洗液,流量为0.80ml/min等度洗脱,BA的保留时间在12min以内(在此条件下,TBA在120min内没出峰),色谱峰介于NO[sub]3[/sub][sup]-[/sup]与H[sub]2[/sub]PO[sub]4[/sub]之间,属于弱保留组[align=center]表1 淋洗液配比对BA等组分峰分离度(R)的影响(流量0.80 ml/min,[color=black]柱箱温度35[/color]℃)[/align][table][tr][td=1,2][align=center][color=black]组分[/color][/align][/td][td=6,1][align=center][color=black]Na[/color][sub][color=black]2[/color][/sub][color=black]CO[/color][sub][color=black]3[/color][/sub][color=black]+NaHCO[/color][sub][color=black]3[/color][/sub][color=black](mmol/L)[/color][/align][/td][/tr][tr][td][align=center][color=black]6.0+0[/color][/align][/td][td][align=center][color=black]6.0+0.9[/color][/align][/td][td][align=center][color=black]6.0+1.0[/color][/align][/td][td][align=center][color=black]6.0+1.1[/color][/align][/td][td][align=center][color=black]6.0+2[/color][/align][/td][td][align=center][color=black]6.0+3.0[/color][/align][/td][/tr][tr][td][align=center][color=black]NO[/color][sub][color=black]3[/color][/sub][sup][color=black]-[/color][/sup][/align][/td][td][align=center][color=black]2.02[/color][/align][/td][td][align=center][color=black]1.61 [/color][/align][/td][td][align=center][color=black]1.53[/color][/align][/td][td][align=center][color=black]1.54[/color][/align][/td][td][align=center][color=black]1.27[/color][/align][/td][td][align=center][color=black]1.08 [/color][/align][/td][/tr][tr][td][align=center][color=black]BA[/color][/align][/td][td][align=center][color=black]3.97[/color][/align][/td][td][align=center][color=black]3.75[/color][/align][/td][td][align=center][color=black]3.57[/color][/align][/td][td][align=center][color=black]3.48 [/color][/align][/td][td][align=center][color=black]3.55[/color][/align][/td][td][align=center][color=black]3.16[/color][/align][/td][/tr][tr][td][align=center][color=black]H[/color][sub][color=black]2[/color][/sub][color=black]PO[/color][sub][color=black]4[/color][/sub][/align][/td][td=1,2][align=center][color=black]二者合并为一个峰[/color][/align][/td][td][align=center][color=black]1.47[/color][/align][/td][td][align=center][color=black]1.63[/color][/align][/td][td][align=center][color=black]1.62[/color][/align][/td][td][align=center][color=black]2.27 [/color][/align][/td][td][align=center][color=black]2.88[/color][/align][/td][/tr][tr][td][align=center][color=black]SO[/color][sub][color=black]4[/color][/sub][sup][color=black]2-[/color][/sup][color=black] [/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][/tr][/table][align=center]图1 [color=black]BA[/color]与常见阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]图[/align][align=center][color=black](6.0mmol/LNa[/color][sub][color=black]2[/color][/sub][color=black]CO[/color][sub][color=black]3[/color][/sub][color=black]-1.0mmol/L[/color]NaHCO[sub]3[/sub],流量0.80 ml/min,[color=black]柱温35[/color]℃)[/align]分,并能与F[sup]-[/sup]、Cl[sup]-[/sup]、NO[sub]2[/sub][sup]-[/sup]、Br[sup]-[/sup]、NO[sub]3[/sub][sup]-[/sup]、H[sub]2[/sub]PO[sub]4[/sub][sup]-[/sup]和SO[sub]4[/sub][sup]2-[/sup][color=black]等7种无机阴离子[/color]完全分离,且峰形良好,见图1。2、TBA在SH-AP-2型色谱柱上的色谱特性:当以15.0、20.0、25.0和30.0 mmol/L的Na[sub]2[/sub]CO[sub]3[/sub]溶液为淋洗液时,TBA的保留时间(T)分别为49、39、31和28min多钟(可见在SH-AP-2型色谱柱上TBA属强保留组分),峰面积及半峰宽逐渐降低,峰高基本保持不变,试验结果见表2。[align=center]表2 TBA在SH-AP-2型色谱柱上洗脱试验结果(流量0.80 ml/min,柱温35℃)[/align][table][tr][td][align=center]Na[sub]2[/sub]CO[sub]3[/sub]溶液浓度[/align][align=center]( mmol/L)[/align][/td][td][align=center][color=black]T/min[/color][/align][/td][td][align=center][color=black]S[/color][/align][/td][td][align=center][color=black]H[/color][/align][/td][td][align=center][color=black]半峰宽[/color][/align][/td][/tr][tr][td][align=center]15.0[/align][/td][td][align=center][color=black]49.633[/color][/align][/td][td][align=center][color=black]907129[/color][/align][/td][td][align=center][color=black]8175[/color][/align][/td][td][align=center][color=black]104.207[/color][/align][/td][/tr][tr][td][align=center]20.0[/align][/td][td][align=center][color=black]39.179[/color][/align][/td][td][align=center][color=black]570446[/color][/align][/td][td][align=center][color=black]8085[/color][/align][/td][td][align=center][color=black]73.155[/color][/align][/td][/tr][tr][td][align=center]25.0[/align][/td][td][align=center][color=black]31.414[/color][/align][/td][td][align=center][color=black]531245[/color][/align][/td][td][align=center][color=black]8074[/color][/align][/td][td][align=center][color=black]61.719[/color][/align][/td][/tr][tr][td][align=center]30.0[/align][/td][td][align=center][color=black]28.207[/color][/align][/td][td][align=center][color=black]479141[/color][/align][/td][td][align=center][color=black]8070[/color][/align][/td][td][align=center][color=black]55.758[/color][/align][/td][/tr][/table]有机改性剂丙酮对TBA色谱特性的影响:当在25.0mmol/L的Na[sub]2[/sub]CO[sub]3[/sub]溶液中加入20%的丙酮时,TBA的保留时间明显缩短,从[color=black]31.414min缩短为18.762min,[/color]峰高及峰面积明显增加,分别增加了213%和96%,半峰宽显著降低,从[color=black]61.791下降至38.799,[/color]峰型明显改善,试验结果见表3。[align=center]表3丙酮对TBA色谱峰参数的影响(流量0.80 ml/min,柱温35℃)[/align][table][tr][td][align=center]25.0mmol/LNa[sub]2[/sub]CO[sub]3[/sub]溶液[color=black]中丙酮浓度(V/V)[/color][/align][/td][td][align=center][color=black]T/min[/color][/align][/td][td][align=center][color=black]峰面积比[/color][/align][/td][td][align=center][color=black]峰高比[/color][/align][/td][td][align=center][color=black]半峰宽[/color][/align][/td][/tr][tr][td][align=center][color=black]0[/color][/align][/td][td][align=center][color=black]31.414[/color][/align][/td][td][align=center][color=black]1.000[/color][/align][/td][td][align=center][color=black]1.000[/color][/align][/td][td][align=center][color=black]61.791[/color][/align][/td][/tr][tr][td][align=center]20.0[/align][/td][td][align=center][color=black]18.762[/color][/align][/td][td][align=center][color=black]1.968[/color][/align][/td][td][align=center][color=black]3.135[/color][/align][/td][td][align=center][color=black]38.799[/color][/align][/td][/tr][/table]4、TBA与常见阴离子及BA的分离情况:当以25.0mmol/L的Na[sub]2[/sub]CO[sub]3[/sub]-20%丙酮溶液为淋洗液时,柱温35℃,流量0.80 ml/min等度洗脱,TBA可与F[sup]-[/sup]、Cl[sup]-[/sup]、NO[sub]3[/sub][sup]-[/sup]、H[sub]2[/sub]PO[sub]4[/sub][sup]-[/sup]、SO[sub]4[/sub][sup]2-[/sup]、BA完全分离(NO[sub]3[/sub][sup]-[/sup]、H[sub]2[/sub]PO[sub]4[/sub][sup]-[/sup]、SO[sub]4[/sub][sup]2-[/sup]和BA四者合并为一个峰),[align=center]图2 T[color=black]BA[/color]与常见阴离子及BA分离色谱图[/align][align=center](25.0mmol/LNa[sub]2[/sub]CO[sub]3[/sub]-20%丙酮溶液,流量0.80 ml/min,柱温35℃)[/align]TBA的色谱峰在SO[sub]4[/sub][sup]2-[/sup]之后,属强保留组分,见图2。[color=black]5、线性方程、线性范围与检出限[/color]:在上述相应最佳条件下,BA和TBA色谱峰面积(y)与其质量浓度(x)分别在[color=black]0.10~20.0mg/L和0.05~40.0mg/L范围内呈良好的线性关系,[/color]相关系数r均为0.9999,检出限(3N/b)分别为0.06mg/L[color=black]和[/color]0.025mg/L,结果见表4。[align=center]表4 BA[color=black]和TBA[/color]的线性范围、回归方程、相关系数和检出限[/align][table][tr][td][align=center][color=black]组分[/color][/align][/td][td][align=center][color=black]线性范围/mg/L[/color][/align][/td][td][align=center][color=black]回归方程[/color][/align][/td][td][align=center][color=black]相关系数/[/color][color=black]r[/color][/align][/td][td][align=center][color=black]检出限/mg/L[/color][/align][/td][/tr][tr][td][align=center][color=black]BA[/color][/align][/td][td][align=center][color=black]0.10~20.0[/color][/align][/td][td][align=center]y[color=black]=34990[/color]x[color=black]-2426[/color][/align][/td][td][align=center][color=black]0.9999[/color][/align][/td][td][align=center][color=black]0.06[/color][/align][/td][/tr][tr][td][align=center]TBA[/align][/td][td][align=center]0.05~40.0[/align][/td][td][align=center]y[color=black]=58660[/color]x[color=black]-2647[/color][/align][/td][td][align=center][color=black]0.9999[/color][/align][/td][td][align=center][color=black]0.025[/color][/align][/td][/tr][/table]小结:(1)BA和TBA是结构、性质相似的两种化合物,一般化学方法难以将二者区分,但在适宜的淋洗条件下SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱能将二者与其他阴离子完全分离,且BA属于弱保留组分而TBA属于强保留组分,为BA和TBA这类结构性质相似化合物的定性、定量分析提供了依据,也为其他相似化合物的[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]分离提供了参考。(2)TBA的电导响应灵敏度高于BA。(3)SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱可用于BA和TBA的定量分析。
巴比妥酸和硫代巴比妥酸[align=center]在SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱上色谱特性总结分析[/align][align=center]十月[/align]巴比妥酸(BA)又称丙二酰脲或2,4,6-嘧啶三酮,硫代巴比妥酸(TBA)又称为[color=#222222]4,6-二羟基-2-巯基嘧啶或[/color]丙二酰缩硫脲[color=#222222],[/color]二者均可用作[color=#222222]化学分析或生化试剂[/color]、塑料和染料及巴比妥类药物、维生素B[sub]12[/sub]等药品的的中间体,[color=#222222]在实验室和制药企业应用广泛,均[/color]溶于热水,在水溶液中BA和TBA均离解成阴离子状态。SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱是[color=black]青岛盛瀚色谱技术公司开发生产的一款疏水型、碳酸盐分离体系阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱。[/color]曾成功应用于[color=black]BrO[/color][sub][color=black]3[/color][/sub][sup][color=black]-[/color][/sup][color=black]、ClO[/color][sub][color=black]3[/color][/sub][sup][color=black]-[/color][/sup][color=black]、ClO[/color][sub][color=black]2[/color][/sub][sup][color=black]-[/color][/sup]、[color=black]ClO[/color][sub][color=black]4[/color][/sub][sup][color=black]-[/color][/sup][color=black]、[/color]BA、TBA、[color=black]三氯乙酸等成分的测定。[/color]现将BA和TBA在SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱上色谱特性总结分析如下:1、BA在不同淋洗条件下的峰分离度及其与各组分的分离情况:试验结果见表1,从表1可见,随着淋洗液中NaHCO[sub]3[/sub]浓度的增加,BA的峰分离度(R)从3.97缓慢下降至3.16,但仍在1.5以上,当以[color=black]6.0mmol/LNa[/color][sub][color=black]2[/color][/sub][color=black]CO[/color][sub][color=black]3[/color][/sub][color=black]-1.0mmol/L[/color]NaHCO[sub]3[/sub][color=black]溶液为[/color]淋洗液,流量为0.80ml/min等度洗脱,BA的保留时间在12min以内(在此条件下,TBA在120min内没出峰),色谱峰介于NO[sub]3[/sub][sup]-[/sup]与H[sub]2[/sub]PO[sub]4[/sub]之间,属于弱保留组[align=center]表1 淋洗液配比对BA等组分峰分离度(R)的影响(流量0.80 ml/min,[color=black]柱箱温度35[/color]℃)[/align][table][tr][td=1,2][align=center][color=black]组分[/color][/align][/td][td=6,1][align=center][color=black]Na[/color][sub][color=black]2[/color][/sub][color=black]CO[/color][sub][color=black]3[/color][/sub][color=black]+NaHCO[/color][sub][color=black]3[/color][/sub][color=black](mmol/L)[/color][/align][/td][/tr][tr][td][align=center][color=black]6.0+0[/color][/align][/td][td][align=center][color=black]6.0+0.9[/color][/align][/td][td][align=center][color=black]6.0+1.0[/color][/align][/td][td][align=center][color=black]6.0+1.1[/color][/align][/td][td][align=center][color=black]6.0+2[/color][/align][/td][td][align=center][color=black]6.0+3.0[/color][/align][/td][/tr][tr][td][align=center][color=black]NO[/color][sub][color=black]3[/color][/sub][sup][color=black]-[/color][/sup][/align][/td][td][align=center][color=black]2.02[/color][/align][/td][td][align=center][color=black]1.61 [/color][/align][/td][td][align=center][color=black]1.53[/color][/align][/td][td][align=center][color=black]1.54[/color][/align][/td][td][align=center][color=black]1.27[/color][/align][/td][td][align=center][color=black]1.08 [/color][/align][/td][/tr][tr][td][align=center][color=black]BA[/color][/align][/td][td][align=center][color=black]3.97[/color][/align][/td][td][align=center][color=black]3.75[/color][/align][/td][td][align=center][color=black]3.57[/color][/align][/td][td][align=center][color=black]3.48 [/color][/align][/td][td][align=center][color=black]3.55[/color][/align][/td][td][align=center][color=black]3.16[/color][/align][/td][/tr][tr][td][align=center][color=black]H[/color][sub][color=black]2[/color][/sub][color=black]PO[/color][sub][color=black]4[/color][/sub][/align][/td][td=1,2][align=center][color=black]二者合并为一个峰[/color][/align][/td][td][align=center][color=black]1.47[/color][/align][/td][td][align=center][color=black]1.63[/color][/align][/td][td][align=center][color=black]1.62[/color][/align][/td][td][align=center][color=black]2.27 [/color][/align][/td][td][align=center][color=black]2.88[/color][/align][/td][/tr][tr][td][align=center][color=black]SO[/color][sub][color=black]4[/color][/sub][sup][color=black]2-[/color][/sup][color=black] [/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][td][align=center][color=black]/[/color][/align][/td][/tr][/table][align=center]图1 [color=black]BA[/color]与常见阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]图[/align][align=center][color=black](6.0mmol/LNa[/color][sub][color=black]2[/color][/sub][color=black]CO[/color][sub][color=black]3[/color][/sub][color=black]-1.0mmol/L[/color]NaHCO[sub]3[/sub],流量0.80 ml/min,[color=black]柱温35[/color]℃)[/align]分,并能与F[sup]-[/sup]、Cl[sup]-[/sup]、NO[sub]2[/sub][sup]-[/sup]、Br[sup]-[/sup]、NO[sub]3[/sub][sup]-[/sup]、H[sub]2[/sub]PO[sub]4[/sub][sup]-[/sup]和SO[sub]4[/sub][sup]2-[/sup][color=black]等7种无机阴离子[/color]完全分离,且峰形良好,见图1。2、TBA在SH-AP-2型色谱柱上的色谱特性:当以15.0、20.0、25.0和30.0 mmol/L的Na[sub]2[/sub]CO[sub]3[/sub]溶液为淋洗液时,TBA的保留时间(T)分别为49、39、31和28min多钟(可见在SH-AP-2型色谱柱上TBA属强保留组分),峰面积及半峰宽逐渐降低,峰高基本保持不变,试验结果见表2。[align=center]表2 TBA在SH-AP-2型色谱柱上洗脱试验结果(流量0.80 ml/min,柱温35℃)[/align][table][tr][td][align=center]Na[sub]2[/sub]CO[sub]3[/sub]溶液浓度[/align][align=center]( mmol/L)[/align][/td][td][align=center][color=black]T/min[/color][/align][/td][td][align=center][color=black]S[/color][/align][/td][td][align=center][color=black]H[/color][/align][/td][td][align=center][color=black]半峰宽[/color][/align][/td][/tr][tr][td][align=center]15.0[/align][/td][td][align=center][color=black]49.633[/color][/align][/td][td][align=center][color=black]907129[/color][/align][/td][td][align=center][color=black]8175[/color][/align][/td][td][align=center][color=black]104.207[/color][/align][/td][/tr][tr][td][align=center]20.0[/align][/td][td][align=center][color=black]39.179[/color][/align][/td][td][align=center][color=black]570446[/color][/align][/td][td][align=center][color=black]8085[/color][/align][/td][td][align=center][color=black]73.155[/color][/align][/td][/tr][tr][td][align=center]25.0[/align][/td][td][align=center][color=black]31.414[/color][/align][/td][td][align=center][color=black]531245[/color][/align][/td][td][align=center][color=black]8074[/color][/align][/td][td][align=center][color=black]61.719[/color][/align][/td][/tr][tr][td][align=center]30.0[/align][/td][td][align=center][color=black]28.207[/color][/align][/td][td][align=center][color=black]479141[/color][/align][/td][td][align=center][color=black]8070[/color][/align][/td][td][align=center][color=black]55.758[/color][/align][/td][/tr][/table]有机改性剂丙酮对TBA色谱特性的影响:当在25.0mmol/L的Na[sub]2[/sub]CO[sub]3[/sub]溶液中加入20%的丙酮时,TBA的保留时间明显缩短,从[color=black]31.414min缩短为18.762min,[/color]峰高及峰面积明显增加,分别增加了213%和96%,半峰宽显著降低,从[color=black]61.791下降至38.799,[/color]峰型明显改善,试验结果见表3。[align=center]表3丙酮对TBA色谱峰参数的影响(流量0.80 ml/min,柱温35℃)[/align][table][tr][td][align=center]25.0mmol/LNa[sub]2[/sub]CO[sub]3[/sub]溶液[color=black]中丙酮浓度(V/V)[/color][/align][/td][td][align=center][color=black]T/min[/color][/align][/td][td][align=center][color=black]峰面积比[/color][/align][/td][td][align=center][color=black]峰高比[/color][/align][/td][td][align=center][color=black]半峰宽[/color][/align][/td][/tr][tr][td][align=center][color=black]0[/color][/align][/td][td][align=center][color=black]31.414[/color][/align][/td][td][align=center][color=black]1.000[/color][/align][/td][td][align=center][color=black]1.000[/color][/align][/td][td][align=center][color=black]61.791[/color][/align][/td][/tr][tr][td][align=center]20.0[/align][/td][td][align=center][color=black]18.762[/color][/align][/td][td][align=center][color=black]1.968[/color][/align][/td][td][align=center][color=black]3.135[/color][/align][/td][td][align=center][color=black]38.799[/color][/align][/td][/tr][/table]4、TBA与常见阴离子及BA的分离情况:当以25.0mmol/L的Na[sub]2[/sub]CO[sub]3[/sub]-20%丙酮溶液为淋洗液时,柱温35℃,流量0.80 ml/min等度洗脱,TBA可与F[sup]-[/sup]、Cl[sup]-[/sup]、NO[sub]3[/sub][sup]-[/sup]、H[sub]2[/sub]PO[sub]4[/sub][sup]-[/sup]、SO[sub]4[/sub][sup]2-[/sup]、BA完全分离(NO[sub]3[/sub][sup]-[/sup]、H[sub]2[/sub]PO[sub]4[/sub][sup]-[/sup]、SO[sub]4[/sub][sup]2-[/sup]和BA四者合并为一个峰),[align=center]图2 T[color=black]BA[/color]与常见阴离子及BA分离色谱图[/align][align=center](25.0mmol/LNa[sub]2[/sub]CO[sub]3[/sub]-20%丙酮溶液,流量0.80 ml/min,柱温35℃)[/align]TBA的色谱峰在SO[sub]4[/sub][sup]2-[/sup]之后,属强保留组分,见图2。[color=black]5、线性方程、线性范围与检出限[/color]:在上述相应最佳条件下,BA和TBA色谱峰面积(y)与其质量浓度(x)分别在[color=black]0.10~20.0mg/L和0.05~40.0mg/L范围内呈良好的线性关系,[/color]相关系数r均为0.9999,检出限(3N/b)分别为0.06mg/L[color=black]和[/color]0.025mg/L,结果见表4。[align=center]表4 BA[color=black]和TBA[/color]的线性范围、回归方程、相关系数和检出限[/align][table][tr][td][align=center][color=black]组分[/color][/align][/td][td][align=center][color=black]线性范围/mg/L[/color][/align][/td][td][align=center][color=black]回归方程[/color][/align][/td][td][align=center][color=black]相关系数/[/color][color=black]r[/color][/align][/td][td][align=center][color=black]检出限/mg/L[/color][/align][/td][/tr][tr][td][align=center][color=black]BA[/color][/align][/td][td][align=center][color=black]0.10~20.0[/color][/align][/td][td][align=center]y[color=black]=34990[/color]x[color=black]-2426[/color][/align][/td][td][align=center][color=black]0.9999[/color][/align][/td][td][align=center][color=black]0.06[/color][/align][/td][/tr][tr][td][align=center]TBA[/align][/td][td][align=center]0.05~40.0[/align][/td][td][align=center]y[color=black]=58660[/color]x[color=black]-2647[/color][/align][/td][td][align=center][color=black]0.9999[/color][/align][/td][td][align=center][color=black]0.025[/color][/align][/td][/tr][/table]小结:(1)BA和TBA是结构、性质相似的两种化合物,一般化学方法难以将二者区分,但在适宜的淋洗条件下SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱能将二者与其他阴离子完全分离,且BA属于弱保留组分而TBA属于强保留组分,为BA和TBA这类结构性质相似化合物的定性、定量分析提供了依据,也为其他相似化合物的[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]分离提供了参考。(2)TBA的电导响应灵敏度高于BA。(3)SH-AP-2型阴[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]柱可用于BA和TBA的定量分析。