液相色谱中怎样设置梯度洗脱?我分析的是双氧水中2-乙基蒽醌和四氢中2-乙基蒽醌的含量,用的溶剂是水和甲醇。
百眼藤【英文名】Littleleaf Indianmulberry, Littleleaf Indianmulberry Herb, Root or stem of Littleleaf Indianmulberry【别名】爬山虎、五眼子、泥藤草、鸡眼藤、猪糠藤、爬山虎、咸鱼头、大甘草、小叶羊角藤【来源】药材基源:为双子叶植物药茜草科植物细叶巴戟天的全株。拉丁植物动物矿物名:Morinda parvifolia Bartl.ex DC.采收和储藏:夏、秋季采收,洗净,晒干。【原形态】攀援灌木。小枝顶部被短粗毛。叶对生;叶柄长4-8mm;托叶膜质,长2-3mm;叶片倒卵状椭圆形,稀椭圆形,衡椭圆状长圆形,长2-6cm,宽1-2(-3)cm,先端急尖或钝而具小凸尖,基部楔形,上面无毛,下面脉腋内有短束毛和有时沿主脉上被短粗毛,纸质。花序由2-6个小头状花序组成伞形花序式顶生,小头状花序直径5-8mm,有花4-8朵,着生于长5-10mm的总花梗上;萼简半球形,长约1mm;花冠白色或绿白色,长约5mm,裂片4,几达基部,长圆状披针形,近中部以下密被卷绒毛,顶端内弯。聚合果扁球形,直径8-10mm,熟时红色。花期夏季。【生境分布】生态环境:生于山野灌丛中。资源分布:分布我国南部。【化学成份】全株含蒽醌类成分:百眼藤醌(morindaparvin)A、B,茜草素-1-甲醚(alizarin-1-methyl ether),光泽定-w-乙醚(luicdin-w-ethyl ether),光泽定-w-甲醚(lucidin-w-methyl ether),锈色洋地黄醌醇(digiferruginol),1-羟基-6-或7-羟甲基蒽醌(1-hy-droxy-6-or 7-hydroxymethyl anthraquinone)和2-羟甲基蒽醌(2-hy-droxymethyl anthraquinone)。【药理作用】本品所含成分百契藤醌A对BDF;小鼠体内P388淋巴细胞白血病具有较强的抑制作用。在10mg/(dg·d)剂量下,百眼藤醌A抗小鼠P388淋巴细胞白血病的T/C(治疗动物生存/对照动物生存率)为129%。体外细胞培养试验表明,百眼藤醌A和从百眼藤中新分离出的百眼藤醌B抑制P388淋巴细胞白敌国病组织细胞生长的ED50分别为1.85μg/ml和10.5μg/ml,抑制鼻咽癌(KB)细胞生长的ED50分别为10μg/ml和4.0μg/ml。【性味】甘;凉【归经】肺经【功能主治】清热解毒;散瘀止痛;和胃化湿。主感冒咳嗽;百日咳;消化不良;湿疹;跌打损伤,腰肌劳损【用法用量】内服:煎汤,15-60g。
【英文名】Littleleaf Indianmulberry, Littleleaf Indianmulberry Herb, Root or stem of Littleleaf Indianmulberry【别名】爬山虎、五眼子、泥藤草、鸡眼藤、猪糠藤、爬山虎、咸鱼头、大甘草、小叶羊角藤【来源】药材基源:为双子叶植物药茜草科植物细叶巴戟天的全株。拉丁植物动物矿物名:Morinda parvifolia Bartl.ex DC.采收和储藏:夏、秋季采收,洗净,晒干。【原形态】攀援灌木。小枝顶部被短粗毛。叶对生;叶柄长4-8mm;托叶膜质,长2-3mm;叶片倒卵状椭圆形,稀椭圆形,衡椭圆状长圆形,长2-6cm,宽1-2(-3)cm,先端急尖或钝而具小凸尖,基部楔形,上面无毛,下面脉腋内有短束毛和有时沿主脉上被短粗毛,纸质。花序由2-6个小头状花序组成伞形花序式顶生,小头状花序直径5-8mm,有花4-8朵,着生于长5-10mm的总花梗上;萼简半球形,长约1mm;花冠白色或绿白色,长约5mm,裂片4,几达基部,长圆状披针形,近中部以下密被卷绒毛,顶端内弯。聚合果扁球形,直径8-10mm,熟时红色。花期夏季。【生境分布】生态环境:生于山野灌丛中。资源分布:分布我国南部。【化学成份】全株含蒽醌类成分:百眼藤醌(morindaparvin)A、B,茜草素-1-甲醚(alizarin-1-methyl ether),光泽定-w-乙醚(luicdin-w-ethyl ether),光泽定-w-甲醚(lucidin-w-methyl ether),锈色洋地黄醌醇(digiferruginol),1-羟基-6-或7-羟甲基蒽醌(1-hy-droxy-6-or 7-hydroxymethyl anthraquinone)和2-羟甲基蒽醌(2-hy-droxymethyl anthraquinone)。【药理作用】本品所含成分百契藤醌A对BDF;小鼠体内P388淋巴细胞白血病具有较强的抑制作用。在10mg/(dg·d)剂量下,百眼藤醌A抗小鼠P388淋巴细胞白血病的T/C(治疗动物生存/对照动物生存率)为129%。体外细胞培养试验表明,百眼藤醌A和从百眼藤中新分离出的百眼藤醌B抑制P388淋巴细胞白敌国病组织细胞生长的ED50分别为1.85μg/ml和10.5μg/ml,抑制鼻咽癌(KB)细胞生长的ED50分别为10μg/ml和4.0μg/ml。【性味】甘;凉【归经】肺经【功能主治】清热解毒;散瘀止痛;和胃化湿。主感冒咳嗽;百日咳;消化不良;湿疹;跌打损伤,腰肌劳损【用法用量】内服:煎汤,15-60g。
我的课题是有关雷公藤内酯甲的,内酯甲的分子式C30H22O3,现在要进行含量的测定,我选择的方法是高效液相,我选用C18柱,购买标准品的时候的条件我是严格执行的,但是结果却大相径庭........流动相:乙腈比水=78比22,加上我是初次接触液相,现在出现的问题是: 1 基线跑好后进溶剂——乙腈,就会出现10min处的一个小峰,15min附近的一个较大的负峰。 2 每次进完样后用甲醇对柱子进行洗脱时都会出现一个很大的峰(约15min),峰形不好。我试着尝试用甲醇做流动相(与水比是3比1),结果在15min后又出现一个很大的峰,峰形也不好,且直到30min我检测时间结束该峰也没下来。 3 我用的色谱工作站的纵坐标单位是AU,见好多文献上是mV,这是不是和仪器的灵敏度有关,怎么修改呀? 以上是我遇到的几个问题,请各位老师和前辈尽快给予建议和帮助,谢谢!!!
[align=center][font='times new roman'][size=20px]藤青泡[/size][/font][font='times new roman'][size=20px]腾片[/size][/font][font='times new roman'][size=20px]纯化[/size][/font][font='times new roman'][size=20px]工艺研究[/size][/font][/align][size=16px]由于提取工艺中采用水为溶剂,其极性大,浸出范围广,选择性较差,药材中的有机酸盐、多糖、蛋白质、[/size][size=16px]苷[/size][size=16px]类、黄酮等均能被浸出,所含与疗效无关的成份较多,使浸膏得率偏高,患者每天所需服用量大,顺应性差,因此采用适当的方法进行纯化。[/size][size=16px]本实验采用醇沉的方法对药液进行[/size][size=16px]纯化,沉淀除去[/size][size=16px]药[/size][size=16px]液中的[/size][size=16px]多糖、蛋白质[/size][size=16px]等杂质,[/size][size=16px]以提高有效成分纯度[/size][size=16px]。[/size][size=16px]采[/size][size=16px]用正交试验的方法考察各因素对醇[/size][size=16px]沉结果[/size][size=16px]的影响,筛选最佳醇沉条件。[/size][font='times new roman'][size=20px]仪器与试药[/size][/font][size=16px]([/size][size=16px]1[/size][size=16px])[/size][size=16px]实验仪器[/size][table][tr][td][size=16px]低温冷却液循环泵[/size][size=16px]DLSB-5/20[/size][/td][td][size=16px]郑州长城科技工贸有限公司[/size][/td][/tr][tr][td][size=16px]循环水式多用真空泵[/size][size=16px]SHB -[/size][size=16px]Ⅲ[/size][/td][td][size=16px]郑州长城科技工贸有限公司[/size][/td][/tr][tr][td][size=16px]旋转蒸发仪[/size][size=16px]RE-2000[/size][/td][td][size=16px]上海亚荣生化[/size][size=16px]仪器厂[/size][/td][/tr][tr][td][size=16px]低速多管离心机[/size][size=16px]LXJ-[/size][size=16px]Ⅱ[/size][size=16px]B[/size][/td][td][size=16px]上海飞鸽电器厂[/size][/td][/tr][/table][size=16px]([/size][size=16px]2[/size][size=16px])[/size][size=16px]实验试药[/size][table][tr][td][size=16px]无水乙醇[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][/table][font='times new roman'][size=20px]泡腾片醇沉工艺条件的研究[/size][/font][font='times new roman'][size=18px]醇沉正交试验筛选[/size][/font][size=16px]称取药材藤茶、葛花、青果、甘草各[/size][size=16px]0.5[/size][size=16px]倍处方量,共[/size][size=16px]1[/size][size=16px]份,按[/size][size=16px]“[/size][size=16px]1.2.1[/size][size=16px]”[/size][size=16px]项所筛选的最佳提取工艺[/size][size=16px]A3B1C3[/size][size=16px],即[/size][size=16px]20[/size][size=16px]倍量水、提取[/size][size=16px]0.5h[/size][size=16px]、提取[/size][size=16px]3[/size][size=16px]次,合并[/size][size=16px]3[/size][size=16px]次提取液,分成[/size][size=16px]9[/size][size=16px]份,每份[/size][size=16px]350 ml[/size][size=16px],以提取液浓度([/size][size=16px]A[/size][size=16px]),含醇量([/size][size=16px]B[/size][size=16px]),醇沉时间([/size][size=16px]C[/size][size=16px])为考察因素,按表[/size][size=16px]5[/size][size=16px]的因素水平进行[/size][size=16px]L9[/size][size=21px]([/size][size=16px]3[/size][font='times new roman'][size=16px]4[/size][/font][size=21px])[/size][size=16px]正交试验,并以总黄酮提取量、干浸膏得率为评价指标,考察最佳醇沉工艺条件。[/size][size=16px]醇沉浸膏得率的测定[/size][size=16px]精密量取上述醇沉后药液[/size][size=16px]5 ml[/size][size=16px],参照[/size][size=16px]“[/size][size=16px]1.2.1[/size][size=16px].1”[/size][size=16px]项下的方法测定浸膏得率,结果见表[/size][size=16px]6[/size][size=16px]。[/size][size=16px]醇沉后总黄酮的含量测定[/size][size=16px]对照品溶液的制备:对照品溶液的制备:[/size][size=16px]称[/size][size=16px]芦丁对照品适量,精密称定,加甲醇溶解[/size][size=16px]并定量稀释至每[/size][size=16px]1 ml[/size][size=16px]含[/size][size=16px]0.2 mg[/size][size=16px]的[/size][size=16px]芦丁溶液,[/size][size=16px]制得对照品溶液[/size][size=16px]。[/size][size=16px]供试品溶液[/size][size=16px]的制备:取上述[/size][size=16px]9[/size][size=16px]份醇沉后药液各[/size][size=16px]1 ml[/size][size=16px],置[/size][size=16px]50 ml[/size][size=16px]容量瓶中,并用水稀释至刻度。[/size][size=16px]芦丁对照品标准曲线制备:芦丁对照品标准曲线制备:精密吸取芦丁对照品溶液[/size][size=16px]0.0[/size][size=16px],[/size][size=16px]1.0[/size][size=16px],[/size][size=16px]2.0[/size][size=16px],[/size][size=16px]3.0[/size][size=16px],[/size][size=16px]4.0[/size][size=16px],[/size][size=16px]5.0[/size][size=16px],[/size][size=16px]6.0[/size][size=16px] [/size][size=16px]ml[/size][size=16px],分别置[/size][size=16px]25 ml[/size][size=16px]([/size][size=16px]V[/size][font='times new roman'][size=16px]3[/size][/font][size=16px])量瓶中,加水至[/size][size=16px]6 ml[/size][size=16px],[/size][size=16px]加入[/size][size=16px]1 ml[/size][size=16px]的[/size][size=16px]5%[/size][size=16px][back=#ffffff] NaNO[/back][/size][font='times new roman'][size=16px][back=#ffffff]2[/back][/size][/font][size=16px],[/size][size=16px]混匀,放置[/size][size=16px]6min[/size][size=16px],[/size][size=16px]往容量瓶里加入[/size][size=16px]1 ml[/size][size=16px]的[/size][size=16px]10%A[/size][size=16px]l[/size][size=16px](NO[/size][font='times new roman'][size=16px]3[/size][/font][size=16px])[/size][font='times new roman'][size=16px]3[/size][/font][size=16px],[/size][size=16px]混匀后静置[/size][size=16px]6min[/size][size=16px],加[/size][size=16px]入[/size][size=16px]10[/size][size=16px] ml [/size][size=16px]NaOH[/size][size=16px]试液,[/size][size=16px]混匀,[/size][size=16px]加[/size][size=16px]蒸馏[/size][size=16px]水至刻度,[/size][size=16px]混匀[/size][size=16px],[/size][size=16px]静置[/size][size=16px]15[/size][size=16px]分钟,以[/size][size=16px]0.0 ml[/size][size=16px]对照品溶液制[/size][size=16px]备[/size][size=16px]的溶剂为空白[/size][size=16px]对照[/size][size=16px],[/size][size=16px]在[/size][size=16px]510nm[/size][size=16px]波长下[/size][size=16px]测定[/size][size=16px]各组的[/size][size=16px]吸[/size][size=16px]光[/size][size=16px]度值。[/size][size=16px]以吸光度为纵坐标[/size][size=16px]([/size][size=16px]A[/size][size=16px])[/size][size=16px],浓度为横坐标([/size][size=16px]mg/ml[/size][size=16px]),绘制标准曲线[/size][size=16px], [/size][size=16px]结果见图[/size][size=16px]2.[/size][size=16px]样品测定:[/size][size=16px]精密吸取精密吸取[/size][size=16px]供试溶液[/size][size=16px]8 ml[/size][size=16px]([/size][size=16px]V[/size][font='times new roman'][size=16px]2[/size][/font][size=16px]),至[/size][size=16px]25 ml[/size][size=16px]量瓶中,照[/size][size=16px]“[/size][size=16px]1.2.1[/size][size=16px].2”[/size][size=16px]自[/size][size=16px]“[/size][size=16px]加入[/size][size=16px]5%[/size][size=16px]亚硝酸钠溶液[/size][size=16px]1 ml”[/size][size=16px]起,在波长[/size][size=16px]510nm[/size][size=16px]处分别测定吸收度值,[/size][size=16px][color=#000000]从标准曲线上读出[/color][/size][size=16px][color=#000000]供试品溶液中含总黄酮[/color][/size][size=16px][color=#000000]的浓度[/color][/size][size=16px][color=#000000]([/color][/size][size=16px][color=#000000]C[/color][/size][size=16px][color=#000000])[/color][/size][size=16px][color=#000000],计算样品中总黄酮的含量([/color][/size][size=16px][color=#000000]X[/color][/size][size=16px][color=#000000])。[/color][/size][size=16px]计算方法:[/size][size=16px]参照[/size][size=16px]“[/size][size=16px]1.2.1[/size][size=16px].2”[/size][size=16px]项下的[/size][size=16px]计算方法进行计算。结果见表[/size][size=16px]6[/size][size=16px],表[/size][size=16px]7.[/size][size=16px][color=#000000]图[/color][/size][size=16px][color=#000000]2 [/color][/size][size=16px][color=#000000]芦丁标准品标准曲线[/color][/size][align=center][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009241153149717_1330_2166779_3.jpeg[/img][/align][align=center][size=16px]表[/size][size=16px]5[/size][size=16px]醇沉正交试验因素水平表[/size][/align][table][tr][td=1,2][align=center][size=16px]水平[/size][/align][/td][td=3,1][align=center][size=16px]因素[/size][/align][/td][/tr][tr][td][align=center][size=16px]A[/size][size=16px]药液相对密度[/size][/align][/td][td][align=center][size=16px]B[/size][size=16px]含醇量[/size][size=16px](%)[/size][/align][/td][td][align=center][size=16px]C[/size][size=16px]醇[/size][size=16px]沉时间[/size][size=16px](h)[/size][/align][/td][/tr][tr][td][align=center][size=16px]1[/size][/align][/td][td][align=center][size=16px]1.0035-1.0039[/size][/align][/td][td][align=center][size=16px]60[/size][/align][/td][td][align=center][size=16px]16[/size][/align][/td][/tr][tr][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]1.0009-1.0016[/size][/align][/td][td][align=center][size=16px]70[/size][/align][/td][td][align=center][size=16px]20[/size][/align][/td][/tr][tr][td][align=center][size=16px]3[/size][/align][/td][td][align=center][size=16px]0.9959-0.9965[/size][/align][/td][td][align=center][size=16px]80[/size][/align][/td][td][align=center][size=16px]24[/size][/align][/td][/tr][/table][size=16px]注:以[/size][size=16px]D[/size][size=16px]因素为误差项[/size][size=16px]采用[/size][size=16px][back=#ffffff]加权平均法对浸膏得率、总黄酮含量进行综合评分,由于[/back][/size][size=16px][back=#ffffff]含量对泡腾[/back][/size][size=16px][back=#ffffff]片疗效的影响较大,因此,分别给予浸膏得率、总黄酮含量[/back][/size][size=16px][back=#ffffff]40%[/back][/size][size=16px][back=#ffffff]、[/back][/size][size=16px][back=#ffffff]60%[/back][/size][size=16px][back=#ffffff]的权重进行分配。浸膏的率越高,患者最终单次的给[/back][/size][size=16px][back=#ffffff]药量越[/back][/size][size=16px][back=#ffffff]多,宜越低越好,故以最低得率[/back][/size][size=16px]18.68[/size][size=16px][back=#ffffff]%[/back][/size][size=16px][back=#ffffff]为最高得分,而总黄酮为主要有效成份,宜越高越好,故以[/back][/size][size=16px]1.625[/size][size=16px][back=#ffffff]为最高得分。以序号[/back][/size][size=16px][back=#ffffff]1[/back][/size][size=16px][back=#ffffff]为例计算综合评分:[/back][/size][size=16px][back=#ffffff]([/back][/size][size=16px]18.680[/size][size=16px][back=#ffffff]/[/back][/size][size=16px]28.002[/size][size=16px][back=#ffffff])*0.4+(1.190/1.625)*0.6=0.706[/back][/size][size=16px][back=#ffffff],同理,可求得其余各综合评分,结果见表[/back][/size][size=16px][back=#ffffff]6[/back][/size][size=16px][back=#ffffff].[/back][/size][align=center][size=16px]表[/size][size=16px]6[/size][size=16px]醇沉正交试验结果([/size][size=16px]n[/size][size=16px]=9[/size][size=16px])[/size][/align][table][tr][td][align=center][font='宋体'][size=16px]序号[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]A[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]B[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]C[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]D[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]浸膏得率[/size][/font][size=16px](%)[/size][/align][/td][td][align=center][font='宋体'][size=16px]总黄酮含量[/size][/font][size=16px](g)[/size][/align][/td][td][align=center][font='宋体'][size=16px]综合评分[/size][/font][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][size=16px]28.002 [/size][/align][/td][td][align=center][size=16px]1.190 [/size][/align][/td][td][align=center][size=16px]0.706 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][size=16px]18.680 [/size][/align][/td][td][align=center][size=16px]0.863 [/size][/align][/td][td][align=center][size=16px]0.719 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][size=16px]27.900 [/size][/align][/td][td][align=center][size=16px]1.143 [/size][/align][/td][td][align=center][size=16px]0.690 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]4[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][size=16px]30.799 [/size][/align][/td][td][align=center][size=16px]1.405 [/size][/align][/td][td][align=center][size=16px]0.761 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]5[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][size=16px]30.447 [/size][/align][/td][td][align=center][size=16px]1.370 [/size][/align][/td][td][align=center][size=16px]0.751 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]6[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][size=16px]28.441 [/size][/align][/td][td][align=center][size=16px]1.313 [/size][/align][/td][td][align=center][size=16px]0.747 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]7[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][size=16px]32.887 [/size][/align][/td][td][align=center][size=16px]1.592 [/size][/align][/td][td][align=center][size=16px]0.815 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]8[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][size=16px]31.601 [/size][/align][/td][td][align=center][size=16px]1.582 [/size][/align][/td][td][align=center][size=16px]0.820 [/size][/align][/td][/tr][tr][td][align=center][font='宋体'][size=16px]9[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]3[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]2[/size][/font][/align][/td][td][align=center][font='宋体'][size=16px]1[/size][/font][/align][/td][td][align=center][size=16px]31.258 [/size][/align][/td][td][align=center][size=16px]1.625 [/size][/align][/td][td][align=center][size=16px]0.839 [/size][/align][/td][/tr][tr][td][align=center][size=16px]K1[/size][/align][/td][td][align=center][size=16px]2.11 [/size][/align][/td][td][align=center][size=16px]2.28 [/size][/align][/td][td][align=center][size=16px]2.27 [/size][/align][/td][td][align=center][size=16px]2.30 [/size][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][align=center][size=16px]K2[/size][size=16px] [/size][/align][/td][td][align=center][size=16px]2.26 [/size][/align][/td][td][align=center][size=16px]2.29 [/size][/align][/td][td][align=center][size=16px]2.32 [/size][/align][/td][td][align=center][size=16px]2.28 [/size][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][align=center][size=16px]K3[/size][/align][/td][td][align=center][size=16px]2.47 [/size][/align][/td][td][align=center][size=16px]2.28 [/size][/align][/td][td][align=center][size=16px]2.26 [/size][/align][/td][td][align=center][size=16px]2.27 [/size][/align][/td][td][/td][td][/td][td][/td][/tr][tr][td][align=center][size=16px]R[/size][/align][/td][td][align=center][size=16px]0.12 [/size][/align][/td][td][align=center][size=16px]0.00 [/size][/align][/td][td][align=center][size=16px]0.02 [/size][/align][/td][td][align=center][size=16px]0.01 [/size][/align][/td][td][align=center][font='宋体'][size=16px] [/size][/font][/align][/td][td][align=center][font='宋体'][size=16px] [/size][/font][/align][/td][td][align=center][font='宋体'][size=16px] [/size][/font][/align][/td][/tr][/table][align=center][size=16px]表[/size][size=16px]7 [/size][size=16px]醇沉正交试验方差分析[/size][/align][table][tr][td][align=center][size=16px]方差来源[/size][/align][/td][td][align=center][size=16px]离差平方和[/size][/align][/td][td][align=center][size=16px]自由度[/size][/align][/td][td][align=center][size=16px]F[/size][size=16px]值[/size][/align][/td][td][align=center][size=16px]均方[/size][/align][/td][td][align=center][size=16px]显著性[/size][/align][/td][/tr][tr][td][align=center][size=16px]相对密度[/size][/align][/td][td][align=center][size=16px]0.02185[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]205.2415[/size][/align][/td][td][align=center][size=16px]0.01093[/size][/align][/td][td][align=center][size=16px]**[/size][/align][/td][/tr][tr][td][align=center][size=16px]含醇量[/size][/align][/td][td][align=center][size=16px]0.00003302[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]0.3101[/size][/align][/td][td][align=center][size=16px]0.00001651[/size][/align][/td][td][/td][/tr][tr][td][align=center][size=16px]醇[/size][size=16px]沉时间[/size][size=16px] [/size][/align][/td][td][align=center][size=16px]0.0007093[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]6.6615[/size][/align][/td][td][align=center][size=16px]0.0003547[/size][/align][/td][td][/td][/tr][tr][td][align=center][size=16px]误差[/size][/align][/td][td][align=center][size=16px]0.0001065[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]1.0000 [/size][/align][/td][td][align=center][size=16px]0.00005324[/size][/align][/td][td][/td][/tr][/table][size=16px]由表[/size][size=16px]7[/size][size=16px]可知,以总黄酮含量与水提取液浸膏得率为[/size][size=16px]评价[/size][size=16px]指标,[/size][size=16px]各因素对结果的影响大小为:[/size][size=16px]药液相对密度[/size][size=16px][/size][size=16px]醇[/size][size=16px]沉时间[/size][size=16px][/size][size=16px]含醇量,即主要影响因素是药液相对密度,其次是醇沉时间,[/size][size=16px]含醇量[/size][size=16px]影响[/size][size=16px]最小[/size][size=16px]。[/size][size=16px]以实验[/size][size=16px]结果[/size][size=16px]为参考[/size][size=16px],结合实际[/size][size=16px]生产情况,最终[/size][size=16px]确定[/size][size=16px]醇沉[/size][size=16px]工艺为[/size][size=16px]:药液[/size][size=16px]相对密度为[/size][size=16px]0.9959-0.9965[/size][size=16px],[/size][size=16px]含醇量[/size][size=16px]70%[/size][size=16px],醇[/size][size=16px]沉时间[/size][size=16px]20h[/size][size=16px]。[/size][font='times new roman'][size=18px]醇沉正交验证实验[/size][/font][size=16px]根据以上所选最佳醇沉工艺条件,相对密度为[/size][size=16px]0.9959-0.9965[/size][size=16px],[/size][size=16px]含醇量[/size][size=16px]70%[/size][size=16px],醇[/size][size=16px]沉时间[/size][size=16px]20h[/size][size=16px],平行[/size][size=16px]3[/size][size=16px]份,对醇沉后药液的浸膏得率与总黄酮含量进行测定,按[/size][size=16px]2.2.1[/size][size=16px].2[/size][size=16px]项下的方法计算综合评分后,[/size][size=16px]求平均[/size][size=16px]得分,结果见表[/size][size=16px]8.[/size][align=center][size=16px]表[/size][size=16px]8[/size][size=16px]醇沉正交实验验证结果([/size][size=16px]n[/size][size=16px]=3[/size][size=16px])[/size][/align][table][tr][td][align=center][size=16px]编号[/size][/align][/td][td][align=center][size=16px]浸膏得率[/size][size=16px](%)[/size][/align][/td][td][align=center][size=16px]总黄酮含量[/size][size=16px](g)[/size][/align][/td][td][align=center][size=16px]综合评分[/size][/align][/td][td][align=center][size=16px]平均得分[/size][/align][/td][/tr][tr][td][align=center][size=16px]1[/size][/align][/td][td][align=center][size=16px]27.9[/size][/align][/td][td][align=center][size=16px]1.780[/size][/align][/td][td][align=center][size=16px]0.925[/size][/align][/td][td=1,3][align=center][size=16px]0.918[/size][/align][/td][/tr][tr][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]28.4[/size][/align][/td][td][align=center][size=16px]1.757[/size][/align][/td][td][align=center][size=16px]0.911[/size][/align][/td][/tr][tr][td][align=center][size=16px]3[/size][/align][/td][td][align=center][size=16px]28.4[/size][/align][/td][td][align=center][size=16px]1.776[/size][/align][/td][td][align=center][size=16px]0.918[/size][/align][/td][/tr][/table][size=16px]由表[/size][size=16px]8[/size][size=16px]可知,最佳醇沉工艺的平均得分[/size][size=16px]0.918[/size][size=16px],大于正交设计中的各项综合评分,且评分最高,有较高的准确率,所筛选的醇沉工艺条件基本稳定,可作为[/size][size=16px]藤青泡[/size][size=16px]腾片的醇沉方法。[/size][font='times new roman'][size=20px]小结与讨论[/size][/font][size=16px]通过正交实验,确定最佳醇沉工艺为:将药液浓缩至相对密度为[/size][size=16px]0.9959-0.9965[/size][size=16px],[/size][size=16px]含醇量[/size][size=16px]70%[/size][size=16px],醇[/size][size=16px]沉时间[/size][size=16px]20h[/size][size=16px]。醇沉正交试验过程中,各实验组尽可能采用同一批次的提取液,以排除提取因素对结果的影响,且提取液放置过程会有少许沉淀,取样时应先混匀;测定相对密度时,要待浓缩的药液冷却至室温后再测,因高温会是玻璃比重瓶体积变大,导致结果不准确;加入乙醇的过程中,乙醇的滴加速度以及搅拌速度应当一致,到醇[/size][size=16px]沉时间[/size][size=16px]后,及时分离出沉淀物并用旋转蒸发仪回收乙醇。[/size]
[align=center][size=24px]千金藤素的提取和纯化[/size][/align][align=center][/align][align=left]摘要:本研究从中药山乌龟中提取得到含千金藤素的提取液;该提取液用键合硅胶层析柱进行纯化,得到含量大于99%的千金藤素,该方法简单、环保、经济且具备工业放大可行性。[/align][align=left][/align][table][tr][td][align=left][font='calibri'][size=13px]样品名称[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]别名[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]结构式[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]分子量[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]CAS号[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]药物功效[/size][/font][/align][/td][/tr][tr][td][align=left][font='calibri'][size=13px]千金藤素[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]千金藤碱[/size][/font][/align][/td][td][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115068700_8263_3120214_3.png[/img][/align][/td][td][align=left][font='calibri'][size=13px]606.71[/size][/font][/align][/td][td][align=left][font='calibri'][size=13px]481-49-2[/size][/font][/align][/td][td][align=left]抗炎,抗肿瘤;抑制冠状病毒复制的倍数为15393倍*[/align][/td][/tr][/table][align=left]*:[font='helvetica'][size=9px][color=#333333]2022年5月10日,中国科学家发现的新冠治疗新药获得国家发明专利授权。专利说明书显示,10μM(微摩尔/升)的千金藤素抑制冠状病毒复制的倍数为15393倍。美国学者之后也在《科学》发表论文证实,千金藤素的数据在其研究的26种药物中数据亮眼,而且优于已经获批上市的瑞德西韦和帕罗韦德。[/color][/size][/font][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115069773_3887_3120214_3.jpeg[/img][/align][align=left][font='helvetica'][size=13px][color=#333333]实验部分[/color][/size][/font][/align][align=left]1. [font='helvetica'][size=13px][color=#333333]样品提取:取中药材山乌龟片,用研钵捣碎至粉末,称取5g于具塞锥形瓶中,加入200ml甲醇,超声提取20min,静置冷却。[/color][/size][/font][/align][align=left]2. [font='helvetica'][size=13px][color=#333333]色谱分析:将提取液用甲醇稀释2倍后,过0.45um膜,进[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用仪[/color][/url]进行色谱分析,色谱条件如下:[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]色谱柱:Bioseps AQ C18, 2.1*100mm, 3um, 100[/color][/size][/font][font='calibri'][size=13px][color=#333333]?[/color][/size][/font][font='helvetica'][size=13px][color=#333333] [/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]流动相:甲醇:0.1%TEA=80:20(V/V)[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]检测波长:282nm[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]流速:0.3ml/min;[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]柱温:35℃[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]进样量:1ul[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]质谱电压:3000V, 扫描范围150~1500m/z, Pos-TIC模式[/color][/size][/font][/align][align=left][font='helvetica'][size=13px][color=#333333]提取液检测[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]检测图:[/color][/size][/font][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115073934_9473_3120214_3.png[/img][/align][align=left]3. 层析纯化:将提取液过0.45μm的膜,进制备[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]进行纯化。制备色谱工艺参数如下:[/align][align=left]层析填料:Bioseps-Flash C18, 20-45μm,100[font='calibri']?[/font];[/align][align=left]填装规格:20×250mm;[/align][align=left]进样体积:10ml (折合样品500mg)[/align][align=left]洗脱液:甲醇:水=85:15(V/V)[/align][align=left]洗脱流速:18mL/min [/align][align=left]收集方式:紫外检测282nm, 35-39.5min [/align][align=left]4. 后处理:馏分35℃下减压旋蒸除去甲醇,冷冻干燥,得白色固体,称重为1.23mg.[/align][align=left]5. 纯化检测,经[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LCMS[/color][/url]检测,样品纯度为97.2%, 检测[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LCMS[/color][/url]图如下:[/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115077303_9982_3120214_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206071115078485_5049_3120214_3.png[/img][/align][align=left]小结:[/align][align=left]1. 由纯品质量折算山乌龟中千金藤素的含量约为0.246%;[/align][align=left]2. 该工艺使用的层析填料为大粒径键合硅胶,有利于放大至规模化生产,建议的生产设备配置如下:[/align][align=left]DAC 800, 系统耐压2MPa,配置集成化层析控制柜,符合GMP生产要求,产能估算,每日分离提取液160L,折合中药样品8kg,可得千金藤素纯品20g.[/align][align=left][/align]
[align=center][font='times new roman'][size=20px] [/size][/font][font='times new roman'][size=20px]藤青泡[/size][/font][font='times new roman'][size=20px]腾片成型工艺研究[/size][/font][/align][size=16px]为了提高产品疗效,质量的稳定性,将复方提取液制成泡腾片,通过摸索性试验,用崩解速度、发泡数量、[/size][size=16px]pH[/size][size=16px]值以及口感为评价标准[/size][size=16px],[/size][size=16px]筛选稀释剂、崩解剂、粘合剂、[/size][size=16px]矫[/size][size=16px]味剂的种类,确定各自用量,[/size][size=16px]探索[/size][size=16px]藤青泡[/size][size=16px]腾片[/size][size=16px]最佳组[/size][size=16px]方及配比[/size][size=16px]。[/size][font='times new roman'][size=20px]仪器与试药[/size][/font][size=16px]([/size][size=16px]1[/size][size=16px])[/size][size=16px]实验仪器[/size][table][tr][td][size=16px]常压恒温干燥箱[/size][size=16px] XMTD-822[/size][/td][td][size=16px]上海精宏实验设备有限公司[/size][/td][/tr][tr][td][size=16px]单冲压片机[/size][size=16px] TDP-1.5[/size][/td][td][size=16px]上海超亿制药机械设备有限公司[/size][/td][/tr][/table][size=16px]([/size][size=16px]2[/size][size=16px])[/size][size=16px]实验试[/size][size=16px]药[/size][size=16px] [/size][table][tr][td][size=16px]柠檬酸[/size][size=16px] (AR) [/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]无水乙醇[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]酒石酸[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]碳酸氢钠[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]碳酸钠[/size][size=16px] (AR)[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]无水乳糖[/size][size=16px] [/size][/td][td][size=16px]Aladdin Industrial [/size][size=16px]Inc[/size][/td][/tr][tr][td][size=16px]聚乙烯吡咯烷酮[/size][size=16px]K30[/size][/td][td][size=16px]上海展云化工有限公司[/size][/td][/tr][tr][td][size=16px]甘草甜素(食用级)[/size][/td][td][size=16px]陕西帕尼尔生物科技有限公司[/size][/td][/tr][tr][td][size=16px]甜菊糖苷(食用级)[/size][/td][td][size=16px]南通华康甜菊糖有限公司[/size][/td][/tr][tr][td][size=16px]阿斯巴甜(食用级)[/size][/td][td][size=16px]Aladdin Industrial [/size][size=16px]Inc[/size][/td][/tr][tr][td][size=16px]硬脂酸镁[/size][size=16px] [/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][tr][td][size=16px]PEG6000[/size][/td][td][size=16px]国药集团化学试剂有限公司[/size][/td][/tr][/table][font='times new roman'][size=20px]成型工艺处方的筛选[/size][/font][font='times new roman'][size=18px]崩解剂的筛选与优化[/size][/font][size=16px]([/size][size=16px]1[/size][size=16px])崩解剂的种类筛选[/size][size=16px]按表[/size][size=16px]9[/size][size=16px]中的组份进行制软材,压片,崩解实验,以筛选崩解剂种类。[/size][align=center][/align][align=center][size=16px]表[/size][size=16px]9[/size][size=16px]不同种类崩解剂的制剂考察[/size][/align][table][tr][td][align=center][size=16px]样品[/size][/align][/td][td][align=center][size=16px]稠[/size][size=16px]浸膏[/size][size=16px](g) [/size][/align][/td][td][align=center][size=16px]酸材[/size][size=16px](g) [/size][/align][/td][td][align=center][size=16px]碱材[/size][size=16px](g)[/size][/align][/td][td][align=center][size=16px]结果[/size][/align][/td][/tr][tr][td][align=center][size=16px]1[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]柠檬酸[/size][size=16px]1.1[/size][/align][/td][td][align=center][size=16px]碳酸钠[/size][size=16px]0.9[/size][/align][/td][td][align=center][size=16px]易吸湿,气泡多,崩解快[/size][/align][/td][/tr][tr][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]柠檬酸[/size][size=16px]1.1[/size][/align][/td][td][align=center][size=16px]碳酸氢钠[/size][size=16px]0.9[/size][/align][/td][td][align=center][size=16px]易吸湿,气泡量适中,崩解快[/size][/align][/td][/tr][tr][td][align=center][size=16px]3[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]酒石酸[/size][size=16px]1.1[/size][/align][/td][td][align=center][size=16px]碳酸钠[/size][size=16px]0.9[/size][/align][/td][td][align=center][size=16px]较不吸湿,气泡多,崩解快[/size][/align][/td][/tr][tr][td][align=center][size=16px]4[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]酒石酸[/size][size=16px]1.1[/size][/align][/td][td][align=center][size=16px]碳酸氢钠[/size][size=16px]0.9[/size][/align][/td][td][align=center][size=16px]较不吸湿,气泡量适中,崩解快[/size][/align][/td][/tr][/table][size=16px]结果表明,样品[/size][size=16px]4[/size][size=16px]的效果较好。[/size][size=16px]([/size][size=16px]2[/size][size=16px])崩解剂的用量优化[/size][size=16px]为了获得崩解剂的最佳用量,以表[/size][size=16px]9[/size][size=16px]中样品[/size][size=16px]4[/size][size=16px]为基础,查阅相应文献崩解剂的用量大多在[/size][size=16px]20%-40%[/size][size=16px],酸碱比例在[/size][size=16px]1:1-1.2:1[/size][size=16px]之间,[/size][size=16px]故设计[/size][size=16px]表[/size][size=16px]10[/size][size=16px],不同崩解剂的用量及酸碱比例,根据片剂的崩解速度,得到最佳用量及酸碱比例。[/size][align=center][size=18px]表[/size][size=18px]10[/size][size=16px]崩解剂的用量及酸碱比例优化[/size][/align][table][tr][td][align=center][size=16px]样品[/size][/align][/td][td][align=center][size=16px]崩解剂占片[/size][/align][align=center][size=16px]重比例[/size][size=16px](%)[/size][/align][/td][td][align=center][size=16px]酸碱比例[/size][/align][/td][td][align=center][size=16px]崩解时间([/size][size=16px]s[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]结果[/size][/align][/td][/tr][tr][td][align=center][size=16px]5[/size][/align][/td][td][align=center][size=16px]20[/size][/align][/td][td][align=center][size=16px]1:1[/size][/align][/td][td][align=center][size=16px]55[/size][/align][/td][td][align=center][size=16px]泡量适中[/size][size=16px],部分颗粒[/size][size=16px]不[/size][size=16px]崩解[/size][/align][/td][/tr][tr][td][align=center][size=16px]6[/size][/align][/td][td][align=center][size=16px]20[/size][/align][/td][td][align=center][size=16px]1.2:1[/size][/align][/td][td][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]泡量适中[/size][size=16px],崩解较完全[/size][/align][/td][/tr][tr][td][align=center][size=16px]7[/size][/align][/td][td][align=center][size=16px]30[/size][/align][/td][td][align=center][size=16px]1:1[/size][/align][/td][td][align=center][size=16px]49[/size][/align][/td][td][align=center][size=16px]气泡较多,部分颗粒[/size][size=16px]不[/size][size=16px]崩解[/size][/align][/td][/tr][tr][td][align=center][size=16px]8[/size][/align][/td][td][align=center][size=16px]30[/size][/align][/td][td][align=center][size=16px]1.2:1[/size][/align][/td][td][align=center][size=16px]47[/size][/align][/td][td][align=center][size=16px]气泡较多,崩解较完全[/size][/align][/td][/tr][tr][td][align=center][size=16px]9[/size][/align][/td][td][align=center][size=16px]40[/size][/align][/td][td][align=center][size=16px]1:1[/size][/align][/td][td][align=center][size=16px]47[/size][/align][/td][td][align=center][size=16px]气泡多,部分颗粒[/size][size=16px]不[/size][size=16px]崩解[/size][/align][/td][/tr][tr][td][align=center][size=16px]10[/size][/align][/td][td][align=center][size=16px]40[/size][/align][/td][td][align=center][size=16px]1.2:1[/size][/align][/td][td][align=center][size=16px]45[/size][/align][/td][td][align=center][size=16px]气泡多,崩解较完全[/size][/align][/td][/tr][/table][size=16px]由上表可知,崩解剂中酸微过量时崩解完全,比例为[/size][size=16px]1.2:1[/size][size=16px]时较好;当崩解剂在片重中的比例增加时,崩解时间减小,但变化幅度较小,且崩解剂比例增加时,溶液的[/size][size=16px]p[/size][size=16px]H[/size][size=16px]值减小,对胃伤害较大,故选用[/size][size=16px]崩解剂占片重[/size][size=16px]比例[/size][size=16px]20%[/size][size=16px],酸碱比例为[/size][size=16px]1.2:1[/size][size=16px]为[/size][size=16px]最[/size][size=16px]宜。[/size][font='times new roman'][size=18px]稀释剂的选择[/size][/font][size=16px]由于泡腾片溶解以后溶液[/size][size=16px]应该[/size][size=16px]澄清,因此稀释剂应[/size][size=16px]能溶于水[/size][size=16px]的,[/size][size=16px]本实验[/size][size=16px]主要考虑可溶性淀粉、乳糖、糖粉,由于[/size][size=16px]藤青泡[/size][size=16px]腾片的提取液味较苦,加入糖粉后,挤压制[/size][size=16px]粒比较[/size][size=16px]困难,乳糖[/size][size=16px]易过筛[/size][size=16px]制粒,可压性强,故选用乳糖作为稀释剂。[/size][font='times new roman'][size=18px]粘合剂的选择[/size][/font][size=16px]常用的粘合剂有乙醇、淀粉浆、[/size][size=16px]PVP[/size][size=16px]。本实验分别用无水乙醇、[/size][size=16px]10%[/size][size=16px]淀粉浆、[/size][size=16px]5%[/size][size=16px]聚乙烯吡咯烷酮[/size][size=16px]K30[/size][size=16px]乙醇溶液作为粘合剂,分别与酸材、[/size][size=16px]碱材混匀[/size][size=16px],过[/size][size=16px]20[/size][size=16px]目筛挤压制粒,[/size][size=16px]6[/size][size=16px]0[/size][size=16px]℃[/size][size=16px]干燥[/size][size=16px]30min[/size][size=16px],压片。乙醇作为粘合剂,干燥以后颗粒较散,[/size][size=16px]细分较多[/size][size=16px],流动性较差,片重差异较大,淀粉[/size][size=16px]浆[/size][size=16px]粘合性较差,压片时容易出现松片,聚乙烯吡咯烷酮[/size][size=16px]K30[/size][size=16px]颗粒不易结块,崩解良好,故选聚乙烯吡咯烷酮[/size][size=16px]K30[/size][size=16px]作粘合剂。[/size][font='times new roman'][size=18px]润滑剂的选择[/size][/font][size=16px] [/size][size=16px]湿法制粒时,在压片前通常需要加入适当的润滑剂,以改善颗粒的流动性,[/size][size=16px]使[/size][size=16px]片重[/size][size=16px]均匀[/size][size=16px],片剂[/size][size=16px]外表[/size][size=16px]光滑。本实验[/size][size=16px]对[/size][size=16px]硬脂酸镁、[/size][size=16px]聚乙二醇[/size][size=16px]6000[/size][size=16px]进行对比试验[/size][size=16px],[/size][size=16px]根据[/size][size=16px]休止角与堆积密度[/size][size=16px]的大小[/size][size=16px],[/size][size=16px]比较两者[/size][size=16px]对颗粒流动性的影响[/size][size=16px]。[/size][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009241643187478_4227_2166779_3.jpeg[/img][size=16px]3.2.4[/size][size=16px].1[/size][size=16px]休止角的测定[/size][size=16px]用固定[/size][size=16px]圆锥底法[/size][size=16px]进行[/size][size=16px]测量[/size][size=16px],把漏斗固定[/size][size=16px]于[/size][size=16px]铁架台上,下方放置一张滤纸,[/size][size=16px]漏斗下端出口垂直于滤纸表面且对准圆心,调节[/size][size=16px]高度约[/size][size=16px]4cm[/size][size=16px],把加入润滑剂的药物颗粒[/size][size=16px]从上口[/size][size=16px]倒入漏斗中,直到铺满[/size][size=16px]整张[/size][size=16px]滤纸为止,测[/size][size=16px]量[/size][size=16px]圆锥的高度,如图[/size][size=16px]3[/size][size=16px],计算休止角:[/size][size=16px]atgθ[/size][size=16px]= h/r[/size][size=16px],平行测定[/size][size=16px]3[/size][size=16px]次,结果见表[/size][size=16px]11.[/size][size=16px]图[/size][size=16px]3 [/size][size=16px]流动角测定装置[/size][size=16px] [/size][size=16px]堆积密度的测定[/size][size=16px] [/size][size=16px]取一只[/size][size=16px]20 ml[/size][size=16px]量筒,洗净,干燥,称重,将颗粒从距[/size][size=16px]瓶口正[/size][size=16px]上方约[/size][size=16px]5cm[/size][size=16px]处流下,直至量筒内颗粒堆积至[/size][size=16px]20 ml[/size][size=16px]刻度处,称量[/size][size=16px]出量筒[/size][size=16px]总重量,求得颗粒重量,平行测[/size][size=16px]3[/size][size=16px]次,取平均值,根据重量与体积计算堆积密度,结果见表[/size][size=16px]11.[/size][align=center][size=16px]表[/size][size=16px]11[/size][size=16px]润滑剂对颗粒流动性影响考察[/size][/align][table][tr][td][align=center][size=16px]样品[/size][/align][/td][td][align=center][size=16px]药物颗粒量[/size][size=16px](g)[/size][/align][/td][td][align=center][size=16px]硬脂酸镁([/size][size=16px]g[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]PEG6000(g)[/size][/align][/td][td][align=center][size=16px]休止角[/size][size=16px]([/size][size=16px]℃[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]堆积密度[/size][size=16px](g/cm[/size][font='times new roman'][size=16px]3[/size][/font][size=16px])[/size][/align][/td][/tr][tr][td][align=center][size=16px]11[/size][/align][/td][td][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]0[/size][/align][/td][td][align=center][size=16px]0[/size][/align][/td][td][align=center][size=16px]37.6[/size][/align][/td][td][align=center][size=16px]0.53[/size][/align][/td][/tr][tr][td][align=center][size=16px]12[/size][/align][/td][td][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]0[/size][/align][/td][td][align=center][size=16px]27.9[/size][/align][/td][td][align=center][size=16px]0.60 [/size][/align][/td][/tr][tr][td][align=center][size=16px]13[/size][/align][/td][td][align=center][size=16px]50[/size][/align][/td][td][align=center][size=16px]0[/size][/align][/td][td][align=center][size=16px]2[/size][/align][/td][td][align=center][size=16px]28.1[/size][/align][/td][td][align=center][size=16px]0.59[/size][/align][/td][/tr][/table][size=16px]由[/size][size=16px]上表堆积密度可知,加入润滑剂以后,粉体的堆积度明显增大,即粉体的流动性、填充性得到改善,压片过程中可减小片重差异,同时减小粉体间的孔隙率,增强可压性;而休止角方面,[/size][size=16px]在没有加[/size][size=16px]任何润滑剂的时候,休止角大,流动性[/size][size=16px]不好[/size][size=16px],且压片后表面粗糙无光泽,不符合生产要求,加入硬脂酸镁、[/size][size=16px]PEG6000[/size][size=16px]后,流动性[/size][size=16px]得到提高[/size][size=16px],片重差异减小,片剂表面光滑,但硬脂酸镁崩解后在溶液表面形成一层薄膜,有浑浊感,故[/size][size=16px]以[/size][font='arial'][size=16px][color=#333333]聚乙二醇[/color][/size][/font][size=16px]6000[/size][size=16px]作为润滑剂。在实验过程中发现,在相同重量的颗粒中,随着加入润滑剂的增加,片剂表面变光滑,但崩解时间也相应延长,实验表明,当用量为[/size][size=16px]2%[/size][size=16px]时,表面光滑,崩解性能良好。[/size][font='times new roman'][size=18px]矫[/size][/font][font='times new roman'][size=18px]味剂的选择[/size][/font][size=16px]矫[/size][size=16px]味剂种类选择[/size][size=16px] [/size][size=16px]由于[/size][size=16px]藤青泡[/size][size=16px]腾片提取液的苦味较强,需[/size][size=16px]采用[/size][size=16px]合适的[/size][size=16px]矫[/size][size=16px]味剂[/size][size=16px]进行矫正[/size][size=16px]。本实验中,主要考察了蔗糖、阿斯巴甜、甜菊糖苷以及甘草甜素对苦味的改善情况,结果表明,蔗糖由于甜度小,制剂过程中加入量大,不符合生产要求;阿斯巴甜甜度较大,但加入后[/size][size=16px]药物[/size][size=16px]变硬结块,难以挤压制粒;甜菊糖苷,甜度大,服用后涩味明显,不宜作为[/size][size=16px]矫[/size][size=16px]味剂,甘草甜素甜度大,服用后喉间有回甘,[/size][size=16px]且藤青泡[/size][size=16px]腾片原料药中含有甘草,故选用甘草甜素作为[/size][size=16px]矫[/size][size=16px]味剂。[/size][size=16px]矫[/size][size=16px]味剂用量优化[/size][size=16px]甘草甜素甜度较大,且个人口感差异较大,因此在[/size][size=16px]矫[/size][size=16px]味剂限量范围内,设计添加量为[/size][size=16px]0.45%[/size][size=16px],[/size][size=16px]0.90%[/size][size=16px],[/size][size=16px]1.8[/size][size=16px]0[/size][size=16px]%[/size][size=16px]三个梯度甜度的[/size][size=16px]藤青泡[/size][size=16px]腾片,在人群中进行口感调查,以[/size][size=16px]0-10[/size][size=16px]分进行评价,口感满意度越好,分值越高,最后[/size][size=16px]求平均[/size][size=16px]得分,获得最受大众接受甜度。结果见表[/size][size=16px]12.[/size][align=center][size=16px]表[/size][size=16px]12[/size][size=16px]不同甜度口感满意度调查结果[/size][size=16px]([/size][size=16px]n[/size][size=16px]=16[/size][size=16px])[/size][/align][table][tr][td][align=center][size=16px]样品[/size][/align][/td][td][align=center][size=16px]矫[/size][size=16px]味剂添加量[/size][/align][/td][td][align=center][size=16px]总得分[/size][/align][/td][td][align=center][size=16px] [/size][size=16px]平均得分[/size][/align][/td][td][align=center][size=16px]备注[/size][/align][/td][/tr][tr][td][align=center][size=16px]14[/size][/align][/td][td][align=center][size=16px]0.45%[/size][/align][/td][td][align=center][size=16px]87[/size][/align][/td][td][align=center][size=16px]5.44[/size][/align][/td][td][align=center][size=16px]苦味强烈[/size][/align][/td][/tr][tr][td][align=center][size=16px]15[/size][/align][/td][td][align=center][size=16px]0.90%[/size][/align][/td][td][align=center][size=16px]107[/size][/align][/td][td][align=center][size=16px]6.69[/size][/align][/td][td][align=center][size=16px] [/size][size=16px]酸味较明显[/size][/align][/td][/tr][tr][td][align=center][size=16px]16[/size][/align][/td][td][align=center][size=16px]1.80%[/size][/align][/td][td][align=center][size=16px]115[/size][/align][/td][td][align=center][size=16px]7.19[/size][/align][/td][td][align=center][size=16px] [/size][size=16px]酸度适宜,无苦涩感[/size][/align][/td][/tr][/table][size=16px]由[/size][size=16px]上表可知,在甘草甜[/size][size=16px]素加入[/size][size=16px]量较少时,药物提取液的苦味较明显,随添加量增加,苦味被覆盖,酒石酸的味道明显,当加入量为[/size][size=16px]1.8%[/size][size=16px]时,口感满意。[/size][font='times new roman'][size=20px]藤青泡[/size][/font][font='times new roman'][size=20px]腾片成型工艺路线[/size][/font][font='times new roman'][size=20px][color=#ff0000] [/color][/size][/font][align=center][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009241643189568_2916_2166779_3.jpeg[/img][/align][font='times new roman'][size=20px]藤青泡[/size][/font][font='times new roman'][size=20px]腾片处方工艺[/size][/font][size=16px](1)[/size][size=16px]处方:[/size][size=16px] [/size][size=16px] [/size][size=16px][color=#ff0000] [/color][/size][table][tr][td][align=center][size=16px]藤茶[/size][/align][/td][td][align=center][size=16px]60[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]葛花[/size][/align][/td][td][align=center][size=16px]30[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]青果[/size][/align][/td][td][align=center][size=16px]2[/size][size=16px]0[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]甘草[/size][/align][/td][td][align=center][size=16px]12[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]酒石酸[/size][/align][/td][td][align=center][size=16px]42.5g[/size][/align][/td][/tr][tr][td][align=center][size=16px]碳酸氢钠[/size][size=16px]([/size][size=16px]外加[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]30.6g[/size][/align][/td][/tr][tr][td][align=center][size=16px]乳糖[/size][/align][/td][td][align=center][size=16px]247[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]甘草甜素[/size][/align][/td][td][align=center][size=16px]8.5g[/size][/align][/td][/tr][tr][td][align=center][size=16px]PEG6000([/size][size=16px]外加[/size][size=16px])[/size][/align][/td][td][align=center][size=16px]9[/size][size=16px].0[/size][size=16px]g[/size][/align][/td][/tr][tr][td][align=center][size=16px]5%PVP[/size][/align][/td][td][align=center][size=16px]适量[/size][/align][/td][/tr][/table][size=16px]共制成泡腾片([/size][size=16px]0.45g/[/size][size=16px]片)[/size][size=16px] [/size][size=16px] [/size][size=16px] 1000[/size][size=16px]片[/size][size=16px](2)[/size][size=16px]制备工艺[/size][size=16px]:[/size][size=16px]将藤茶、葛花、青果、甘草加水煎煮三次,每次[/size][size=16px]30[/size][size=16px]分钟,分次滤过,合并滤液,浓缩成流浸膏,放冷,加乙醇适量,静置,取上清液,回收乙醇,浓缩成稠膏,备用。加入酒石酸、乳糖、甘草甜素,混匀,以[/size][size=16px]5%PVP[/size][size=16px]乙醇溶液为粘合剂,制粒,干燥,整粒,加入[/size][size=16px]PEG6000[/size][size=16px]和碳酸氢钠,混匀,压制成[/size][size=16px]1000[/size][size=16px]片,即得。[/size][font='times new roman'][size=20px]小结与讨论[/size][/font][size=16px]通过[/size][size=16px]对泡腾片[/size][size=16px]组[/size][size=16px]方及配比的探讨[/size][size=16px],最终[/size][size=16px]得到[/size][size=16px]最[/size][size=16px]适[/size][size=16px]配方为:崩解剂[/size][size=16px]15.7%[/size][size=16px],酒石酸与碳酸氢钠比例[/size][size=16px]1.2:1[/size][size=16px],[/size][size=16px] [/size][size=16px]稀释剂乳糖[/size][size=16px]53.2%[/size][size=16px],粘合剂[/size][size=16px]PEG6000 1.9%[/size][size=16px],[/size][size=16px]矫[/size][size=16px]味剂甘草甜素[/size][size=16px]1.8%[/size][size=16px],[/size][size=16px]PVP[/size][size=16px]适量,按[/size][size=16px]3.4[/size][size=16px]项下的制备工艺进行制备。实验过程中发现,由于黄酮会与碱性崩解剂碳酸氢钠发生化学反应,所制的颗粒颜色变深,导致酸碱软材颜色不一致,压片后出现花斑,因此碳酸氢钠采用外加法,即在压片前加[/size][size=16px]入、混合后压片;由于浸膏中含有部分多糖,解热条件下粘度增加,干燥过程中温度不宜过高;润滑剂的用量需适量,过少表面粗糙,片重差异较大,过多会导致崩解迟缓;本实验过程中,用单冲压片机进行压片,使前需进行试压,调整好进样量、压力后在进行压片,以免出现顶车现象,损坏电机,手动压片时尽量转动速度均匀;由于空气湿度、[/size][size=16px]温度对泡腾[/size][size=16px]片的影响较大,整个生产过程,相对湿度[/size][size=16px]不宜超过[/size][size=16px]45%[/size][size=16px],温度在[/size][size=16px]15℃-25℃[/size][size=16px]为宜。[/size]
化妆品工业高速发展,大大小小的化妆品生产企业遍布各地,近年来,化妆品损害消费者健康的事件时有发生,因此加强对化妆品的监测尤为重要。氢醌和苯酚具有一定的美白作用,但其毒性和刺激性大,故我国卫生标准规定:祛斑类化妆品中禁用氢醌和苯酚。由于此类物质易获得且价格低廉,常被一些化妆品生产厂家用于祛斑类漂白化妆品中,长期使用含量高的氢醌类化妆品会引起皮肤刺激,色素加深甚至出现白斑。苯酚在医疗上常用于消毒,3%~5%水溶液可消毒皮肤,但苯酚对皮肤刺激性很大,可引起刺激损伤。 由于目前只有《化妆品卫生规范》中规定化妆品中苯酚和氢醌的检测,但由于化妆品种类繁多,基体复杂,只通过甲醇、乙醇提取后,上机分析,净化效果不佳,易造成假阳性;迪马科技根据目标物的性质特征,建立了SPE固相萃取柱-ProElut PSA进行前处理净化,高效液相色谱检测化妆品中苯酚和氢醌的解决方案,具有前处理简单,回收率损失少,固相萃取柱净化效果明显、重现性好等优点。 详细解决方案如下:
如题,用岛津[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]质8045scan扫氢醌母离子,负离子模式,1ppm10ppm都扫不出母离子,甲醇,乙腈,水,5mM乙酸铵,0.1%甲酸都扫不出来
如题,液相对苯二醌的分析测试方法哪里能找到,摸条件怎么摸呀,配个甲醇与水的流动相,然后跑跑就行么
想做一个熔点标准物,现在手里有蒽醌粗品,如何把它纯化?请指教!!!
目前国内一些不良化妆品生产企业,为了使化妆品达到较好的祛斑效果,往往会添加氢醌和苯酚, 氢醌和苯酚具有一定的美白作用,但其毒性和刺激性大,故我国卫生标准规定:祛斑类化妆品中禁用氢醌和苯酚。 不过,由于此类物质易获得且价格低廉,常被一些化妆品生产厂家用于祛斑类漂白化妆品中,长期使用含量高的氢醌类化妆品会引起皮肤刺激,色素加深甚至出现白斑。苯酚在医疗上常用于消毒,3%~5%水溶液可消毒皮肤,但苯酚对皮肤刺激性很大,可引起刺激损伤。 目前只有《化妆品卫生规范》中规定化妆品中苯酚和氢醌的检测,但由于化妆品种类繁多而且基体复杂,规定中前处理,只通过甲醇、乙醇提取后,上机分析,净化效果不佳,易造成假阳性; 针对以上问题,迪马科技根据目标物的性质特征,建立了SPE固相萃取柱-ProElut PSA进行前处理净化,高效液相色谱检测化妆品中苯酚和氢醌的解决方案,具有前处理简单,回收率损失少,固相萃取柱净化效果明显、重现性好等优点。详细解决方案如下:1 适用范围该方法适用于祛斑类化妆品和香波中氢醌、苯酚含量的测定。2 样品准备2.1 香波类化妆品(1) 取1 g样品,加入3mL饱和氯化钠溶液,5 mL提取液*,涡旋1 min,6000 rpm下离心2 min,收集上清液;(2) 将下层残留物再用5 mL提取液*重复提取一次,合并两次提取上清液;(3) 将上清液用提取液*定容至10 mL,混匀,供HPLC测定。2.2 乳液、面霜等化妆品(1) 取1 g样品,加入3mL饱和氯化钠溶液,5 mL提取液*,涡旋1 min,6000 rpm下离心2 min,收集上清液;(2) 将下层残留物再用5 mL提取液*重复提取一次,合并两次提取上清液;(3) 将上清液用提取液*定容至10 mL,混匀,取5 mL上清液并加入2.5 mL正己烷,混匀待净化。提取液*:甲基叔丁基醚:正己烷=3:13乳液、面霜等化妆品的SPE柱净化——ProElut PSA 1 g/6 mL (Cat.#:63206)(1)活 化:向柱中加入5 mL甲基叔丁基醚:正己烷=1:1,弃去流出液;(2)上 样:将待净化液加入柱中,弃去流出液;(3)淋 洗:向柱中加入5 mL正己烷,弃去流出液;(4)洗 脱:向柱中加入5 mL甲醇,收集流出液;(5)重新溶解:将洗脱液在40 ℃缓慢通入氮气吹至1 mL,再用二氯甲烷定容至1 mL,供HPLC分析。4 分析条件色谱柱:Diamonsil C18(2),250 mm×4.6 mm,5μm(Cat# 99603)流 速:1.0mL/min检测器:*UV 280nm柱 温:30℃ 进样量: 20 μL流动相:A:水B:甲醇梯度时间(min)010151625A(%)8050308080B(%)2050702020*本方法中,目标化合物是由[color=b
[color=#231815]大黄提取物中5种蒽醌化合物的分离纯化[/color][color=#231815][color=#333333]为研究大孔树脂对大黄5种蒽醌的分离效果,本文采用静态吸附实验,比较6种大孔树脂(HPD-100、XDA-6、AB-8、LX-38、ADS-7和ADS-17)对5种游离蒽醌(芦荟大黄素、大黄酸、大黄素、大黄酚、大黄素甲醚)的吸附及解吸附性能,筛选出对大黄5种蒽醌吸附率和吸附率最高的大孔树脂。然后以筛选的大孔树脂作为载体,对其动态吸附特性进行了初步研究。结果显示,HPD-100大孔树脂对大黄5种蒽醌吸附率和吸附率最高 在层析柱径高比1∶8,上样溶液5种蒽醌总浓度为3.64 mg/mL,上样体积2.0 BV,流速1.0 BV/h,85%的乙醇洗脱,洗脱体积为3.0 BV的优化条件下,HPD-100对5种蒽醌的动态吸附率为86.3%,洗脱率为85.9%,5种蒽醌总含量增加了2.88倍,由原来的7.13%增加到20.5%,总回收率98.7%,提取物中残留的离子液体Br也同时被除去,表明本实验选择的优化条件具有可行性。[/color][/color]
分析方法 金的测定期 容量法-氢醌滴定法中氢醌正常的滴定度是多少
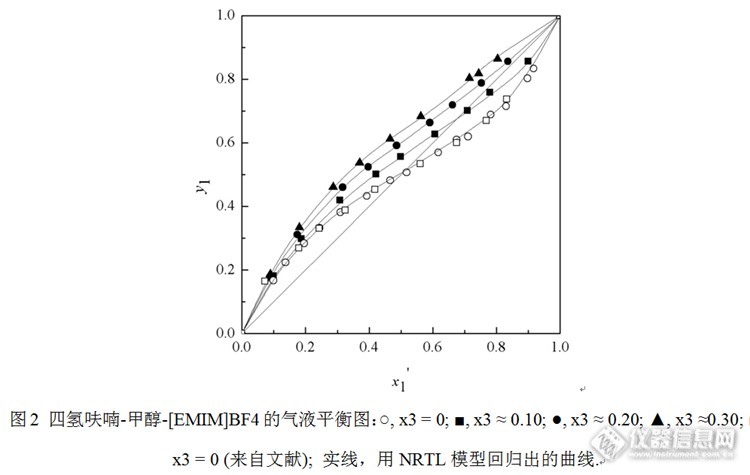
前言 本阶段进行了1-乙基-3-甲基咪唑四氟硼酸盐(4])、1-丁基-3-甲基咪唑四氟硼酸盐(4])、1-丁基-3-甲基咪唑六氟磷酸盐([PF[sub]6])、1-辛基-3-甲基咪唑六氟磷酸盐([PF[sub]6])对四氢呋喃-甲醇二元体系的气液平衡的影响,并对实验结果运用了NRTL模型进行了关联,关联结果良好。最后将关联的结果导入aspen plus模拟软件模拟了整个萃取精馏过程,为今后的工业应用提供基础的理论数据。1.1 气液平衡试验的流程1.1.1 试验设备及试剂试验所采用的主要试验仪器如下:[align=center]表1-1主要实验仪器[/align] [table=606][tr][td] [align=center]编号[/align] [/td][td] [align=center]仪器名称[/align] [/td][td] [align=center]生产厂家[/align] [/td][td] [align=center]量程及精度[/align] [/td][/tr][tr][td] [align=center]1[/align] [/td][td] [align=center]Bs120s型 电子天平[/align] [/td][td] [align=center]德国sartorius公司[/align] [/td][td] [align=center]0.0001g[/align] [/td][/tr][tr][td] [align=center]2[/align] [/td][td] [align=center]CE-2型汽液平衡数据测定仪[/align] [/td][td] [align=center]天津大学北洋化工实验设备有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][tr][td] [align=center]3[/align] [/td][td] [align=center]旋转蒸发仪[/align] [/td][td] [align=center]上海申顺生物科技有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][tr][td] [align=center]4[/align] [/td][td] [align=center]Sp6890型气相色谱仪[/align] [/td][td] [align=center]北京精科瑞达有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][tr][td] [align=center]5[/align] [/td][td] [align=center]N2000型 色谱工作站[/align] [/td][td] [align=center]浙江大学智达信息工程有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][tr][td] [align=center]6[/align] [/td][td] [align=center]真空干燥箱DZF-6020型[/align] [/td][td] [align=center]上海一恒科技有限公司[/align] [/td][td] [align=center]N/A[/align] [/td][/tr][/table]另外还有烧杯、容量瓶、移液管、磁力搅拌器、微样进样针(1μL)等。试验中所采用的主要试验试剂如下:甲醇,四氢呋喃:北京化工厂,分析纯,质量分数≥99.8 %;本文共用到五种不同的离子液体,分别为:1-乙基-3-甲基咪唑四氟硼酸盐(BF[sub]4);1-丁基-3-甲基咪唑四氟硼酸盐(BF[sub]4);1-丁基-3-甲基咪唑六氟磷酸盐([PF[sub]6]);1-辛基-3-甲基咪唑六氟磷酸盐([PF[sub]6])。离子液体从上海成捷化学有限公司购买,产品的质量分数≥98%。1.1.2 试验流程 本文测定了四氢呋喃-甲醇共沸物系分别加入不同浓度的离子液体(BF[sub]4、BF[sub]4、[PF[sub]6]、[PF[sub]6])后的汽液相平衡数据。每个摩尔分数下的离子液体做10个浓度点,每个点取样5次,每个样品在色谱仪中出峰时间约为6分钟,然后根据色谱分析对应浓度,对五次平行试验结果进行平均得出最终浓度。整个操作的实验流程如图1.实验测定步骤如下:(1) 依据实验所要求的摩尔比将各个组分所需要的体积量和质量计算列表,然后以体积量为估计值,利用移液管在容量瓶中加入比体积量稍少体积的试剂,最后用分析天平通过滴管准确滴至所需质量。同样的方法加入其它组分。在全部组分加入完成后,摇匀,密封,静止以观察是否分层。容量瓶如装有含离子液体的溶液,需要用溶剂清洗回收离子液体。容量瓶用洗涤剂清洗,最后用去离子水润洗。配液过程用所用的烧杯,滴定管,移液管等如果用过不同的液体需要清洗烘干。(2) 用甘油作为导热剂,在测温套管中加入适量甘油,标准温度计插入套管中;(3) 对系统的气密性进行检查,保证试验装置的气密性不会有样品损失而影响平衡数据的测定,再加样进行实验;(4) 沸腾室内加入配制好的四氢呋喃-甲醇-离子液体混合溶液约70ml,打开冷却水,打开电源进行加热。采用逐步升温加热,开始时调节小电流(0.1A)控制加热温度,等到整个仪器预热完毕调大电流到0.2A稳定十分钟,继续调到0.3A左右持续稳定加热,以沸腾室内液体能沸腾为准适当调节电流。冷凝回流液控制在每秒1-3滴,待温度计度数不变,稳定回流30分钟左右以建立平衡状态;(5) 达到平衡后,读取温度计的温度并记录;(6) 应用1μL微量进样器直接从汽相取样口取出0.4μL试样,取液前应先进行5次以上的洗针操作,以保证针管内润湿同时减少误差。取液时应注意每次取液时尽量取同样的位置,取样量保持一致。每次取样后应尽快打入色谱仪中,打针时遵循快进快出原则,以免液体被气化。待将样品打入仪器中,尽快点采集数据进行分析。待所有的峰积分完成以后,稳定一分钟进行数据的记录和保存。重复上述过程,每个样品汽液相各测3-5个点取平均。同样的再次使用微量进样器从液相取样口取出0.4μL试样,也是进行色谱分析浓度,同样操作,记录数据;(7) 重复以上第六步的操作,进行下一数据点的测定,对每个点的汽液相至少分别测试五次,取相近的较为稳定的四针样品浓度进行平均,得出最后浓度;(8) 当样品的数据测试完成后,将电流调至零点,关闭加热电源,静置平衡釜至温度较低时,拆卸装置。平衡釜中的液体从液相口倒出,用低沸点的溶剂将平衡釜清洗1至2次。如果平衡釜内为二元样品,可直接将样品及洗液倒入废液瓶,若果为加入离子液体的三元样品,需将样品和洗液收集起来以回收里面的离子液体。清洗完平衡釜后,用电吹风开加热档吹10分钟以上,将平衡釜里面残留的溶剂吹干为止。(9) 将含有离子液体的废液加入蒸发瓶,安置到旋转蒸发仪上,固定。加热器应逐级升温,以防蒸发液暴沸,减压旋转蒸发维持3个小时以上,保证离子液体纯度。(10)每天实验结束后,首先关闭色谱加热,冷却色谱降温,待色谱中热导温度降至80度以下时,关闭仪器,关闭色谱工作站,最后关闭氢气。如检测含离子液体的三元组分物系,需注意色谱工作站的谱线是否出现峰值和面积减小,某些峰的检测能力下降等的异常,这是由于离子液体积存在仪器中衬管的棉花上,导致样品通过量减少。这时,需按照上述步骤完全关闭仪器,更换衬管的石棉并且对衬管进行清洗。注意在安装衬管时,衬管安装松紧要合适,过紧会顶碎衬管,过松会导致设备漏气。安装完成后,检查压力表示数与安装前是否一致,以确定是否漏气。[img=,512,436]http://ng1.17img.cn/bbsfiles/images/2015/09/201509281522_568298_2984502_3.jpg[/img]1.2 二元体系的气液相平衡 为了验证整个实验过程的可靠性,我们首先对四氢呋喃-甲醇体系的二元气液平衡数据进行了测定,测定的结果如下,实验结果与文献吻合度较高,说明我们的实验仪器可以用于含离子液体的三元体系的测定。[img=,547,623]http://ng1.17img.cn/bbsfiles/images/2015/09/201509281523_568299_2984502_3.jpg[/img] 由图三可以看出,在四氢呋喃-甲醇二元体系当中,101.3kPa下共沸点存在于四氢呋喃的含量为x1=0.512时,平衡温度为T=332.4K。实验结果表明此二元体系存在共沸现象,要分离需要采用特殊精馏的方法。而本文的目的就是为分离这个体系选取绿色有效的萃取剂。1.3带有四氟硼酸根的离子液体对四氢呋喃甲醇体系的气液平衡的影
雷公藤内酯醇是中药雷公藤的主要生物活性成分,具有包括抗肿瘤在内的多重生物学作用。中科院上海药物研究所缪泽鸿课题组、李援朝课题组、丁健课题组与意大利博洛尼亚大学Giovanni Capranico实验室合作,在雷公藤内酯醇及其衍生物的抗肿瘤作用和机制研究中取得阶段性进展。 在阐明C14β位羟基取代的雷公藤内酯醇衍生物具有选择性体内抗肿瘤作用 (J Med Chem. 2009; 52: 5115–5123) 的基础上,研究发现雷公藤内酯醇可升高细胞内低氧诱导因子1α(HIF-1α)水平却降低其转录活性,与其抗肿瘤作用相关 (Mol Cancer. 2010; 9:268)。已有研究显示,雷公藤内酯醇可以与通用转录因子TFIIH大亚基XPB直接结合,并引起RNA聚合酶II(RNAPII)大亚基Rpb1降解。 该合作研究深入揭示了雷公藤内酯醇作用于这一核心靶点的分子基础和意义。雷公藤内酯醇降低Rpb1水平与其细胞毒活性紧密相关,即阻滞RNAPII于基因的启动子处,减少基因启动子和外显子处染色质结合的RNAPII,增加Rpb1羧基末端结构域的磷酸化 (5位丝氨酸) 和泛素化。蛋白酶体抑制剂或CDK7抑制剂可减低雷公藤内酯醇降解Rpb1的能力。研究人员由此发现雷公藤内酯醇触发CDK7介导RNAPII降解的新模式,提出了雷公藤内酯醇结合XPB、降解RNAPII的通用机制。该机制可以很好地解释雷公藤内酯醇包括其强效抗肿瘤在内的多重治疗学特性 (Cancer Res.2012; doi:10.1158/0008-5472.CAN-12-1006)。 研究人员还受邀撰写雷公藤内酯醇专题综述,系统总结了雷公藤内酯醇的结构修饰、构效关系、作用与机制以及临床开发的研究进展 (Nat Prod Rep. 2012; 29: 457-475)。 相关论文: 1.Li Z, Zhou ZL, Miao ZH, Lin LP, Feng HJ, Tong LJ, Ding J, Li YC. Design and synthesis of novel C14-hydroxyl substituted triptolide derivatives as potential selective antitumor agents. J Med Chem. 2009; 52:5115-23. 2.Zhou ZL, Luo ZG, Yu B, Jiang Y, Chen Y, Feng JM, Dai M, Tong LJ, Li Z, Li YC, Ding J, Miao ZH. Increased accumulation of hypoxia-inducible factor-1a with reduced transcriptional activity mediates the antitumor effect of triptolide. Mol Cancer. 2010; 9:268. 3.Manzo SG, Zhou ZL, Wang YQ, Marinello J, He JX, Li YC, Ding J, Capranico J, Miao ZH. Natural product triptolide mediates cancer cell death by triggering CDK7-dependent degradation of RNA polymerase II. Cancer Res. 2012; doi:10.1158/0008-5472.CAN-12-1006. 4.Zhou ZL, Yang YX, Ding J, Li YC, Miao ZH. Triptolide: structural modifications, structure-activity relationships, bioactivities, clinical development and mechanisms. Nat Prod Rep. 2012; 29:457-75.http://www.cas.cn/ky/kyjz/201208/W020120829347054661848.jpghttp://www.cas.cn/ky/kyjz/201208/W020120829347054676369.jpg雷公藤内酯醇及其衍生物抗肿瘤研究取得阶段性进展
压力0.1MPa都不到,流量300ml/min属于正常范围。测量的是纯氢中的氧气,氢气由天然气裂解制备。分析仪刚开机使用正常,1个月之后发现数据超量程,氧电池漏液了,更换一个全新的,没到一个月又漏液,第三次更换之后没多久还是漏液。旁边一台测量氮中氧的一直工作正常。氢气氧气中未发现杂质,预处理系统上的前级过滤器很干净,为什么总是漏液???很头疼啊http://simg.instrument.com.cn/bbs/images/default/em09509.gif
不知道大家有没有看到新闻报道里的关于扬州大学设立的“贫困楼”一事 ,以下是一位网友的一些看法。我想,教育是当前我们颇为关注的一件大事,而且,我也身处高校,对于高校好多的事情很是无赖!我想转帖他的一些看法,希望大家茶余饭后,仁者见仁,智者见智,当我看到扬州大学专门设立“贫困生楼”让贫困大学生居住的消息(见9月9日《江南时报》)时,我产生的第一个反应是,再没有什么方式能比这种刻薄寡恩的作法更有效地撕裂我们的社会了。这不是教育家在办大学,这是浑身散发着铜臭气的市侩在办大学。 在中国的贫富差距已经到了一个非常危险的水平,社会上“不要仇富”的呼吁和对“为富不仁”的控诉交替上升的大背景下,大学几乎成了惟一一个能够敉平贫富对立的地方了,说它是防止社会断裂的焊接点也不为过。因为只有在大学,财富才不会成为衡量一个人价值高低主要标志,一个人的才华、能力、道德水平和奋斗精神才是他能不能受到尊重的主要原因。也只有在这样的氛围中,穷人的子弟和富家子弟才能够平等的交流,加深对对方的理解,在互相尊重的基础上建立起真挚的友谊,为他们日后走上社会后在不同阶层间进行沟通与合作奠定基础。 但“贫困生楼”的出现将无情地击碎这个焊接点,因为它把原来仅仅是背景的不平等显性化、仪式化、固定化了。你受到不同的对待,和你的品质无关,仅仅和你父母的财富有关。原本应该是统一的大学生群体,被极为清晰地分割成了“贫困生楼的居民”和“公寓楼的居民”。大学生的“我们”分裂了,分裂成了“我们”和“你们”。同在一所大学,却不在同一个世界生活,有的被蔑视,有的被仇恨。这种强烈的反差势必留下巨大的心理阴影,“蔑视”和“仇恨”也将被他们从校园带进社会。 当然,我相信扬大能够找到充分的理由为自己辩解,他们会说设立贫困生楼正是为贫困生着想,扬大的一位工作人员不是对记者说,“贫困生楼”很受贫困生欢迎吗?他这里所依据的逻辑是市场的逻辑而不是教育的逻辑。贫富差距以及由贫富差距带来的不平等在目前来讲的确是一个让人感到很无奈的现实,但作为大学,应该努力抗拒这种不平等带来的负面影响,树立起对知识、能力和品格的尊重,而不推波助澜地张扬对金钱的崇拜。贫困生选择住“贫困生楼”是对现实无奈的妥协,并不代表他们没有受到伤害。因此,扬大应该通过其他方式消化学生公寓装修的成本,而不应该简单把它转嫁到学生身上。 大学校长应该比其他人更为敏感地意识到社会断裂严重后果,也应该比其他人有更多的社会责任来未雨绸缪!一切从“成本—收益”的考虑出发,只重视短期效益,那是商人的思维方式,不是大学校长的思维方式;一切从有利于社会的和谐和长远发展的考虑出发,才能说是真正有眼光的大学校长。作为一个契机,扬大的“贫困生楼”事件,应该引发我们对整个教育理念的再反思。
中文通用名称:鱼藤酮 英文通用名称:rotenone 化学名称:[2R-(2α,6aα,12aα)]-1,2,12,12a-四氢-8,9-二甲氧基-2-(1-甲基乙烯基)[1]苯并吡喃[3,4-b]糠酰[2,3-h][1]苯并吡喃-6(6aH)-酮 化学结构式 理化性质:鱼藤酮可从鱼藤根的萃取液中结晶得到。纯品为无色六角板状晶体,熔点163℃(同质二晶型的熔点181℃)。几乎不溶于水(100℃水中溶解度15毫克/升),微溶于矿油和四氯化碳,易溶于极性有机溶剂,在氯仿中溶解度最大(472克/升)。遇碱消旋,易氧化,尤其在光或碱存在下氧化快,而失去杀虫活性。在干燥情况下比较稳定。 毒性:按我国农药毒性分级标准,鱼藤酮属中等毒。原药大鼠急性经口LD5124.4毫克/公斤,急性经皮LD50≥2050毫克/公斤。 作用特点:鱼藤酮是一种历史比较久的植物性杀虫剂,具选择性,无内吸性,见光易分解,在空气中易氧化,在作物上残留时间短,对环境无污染,对天敌安全。该药剂杀虫谱广,对害虫有触杀和胃毒作用。本品能抑C-谷氨酸脱氢酶的活性,而使害虫死亡。该药剂能有效地防治蔬菜等多种作物上的蚜虫,安全间隔期为3天。 制剂:2.5%鱼藤酮乳油 2.5%鱼藤酮乳油 理化性质及规格:2.5%鱼藤酮乳油含有效成分鱼藤酮2.5%,外观为淡黄至棕黄色液体,比重0.91,pH≤8.5,闪点29℃,低温易析出结晶,高于80℃易变质。 毒性:大鼠急性经口LD50176.6毫克/公斤,大鼠急性经皮≥2086毫克/公斤。 登记情况及厂家:2.5%鱼藤酮乳油已在我国获得老品种登记,登记号为PD91105,登记厂家为广东省云浮县云城农药厂、广东省广州农药厂,登记号为PD91105-2,批准登记作物和防治对象为叶菜类蔬菜的蚜虫。 (记者 佚名)
概叙:岛津04年购进的LC-10Avp液相,严重漏液,停用1年了。领导要求重整起来用于新手学习。http://ng1.17img.cn/bbsfiles/images/2014/08/201408281138_511952_1635352_3.jpg上面是“重灾区的特写”,已经开始生锈了,惨不忍睹http://ng1.17img.cn/bbsfiles/images/2014/08/201408281138_511954_1635352_3.jpg放大一点,台面上也还看得到痕迹。http://ng1.17img.cn/bbsfiles/images/2014/08/201408281138_511955_1635352_3.jpg再来一张全图。仪器是有些老了,04年买的,老的是单泵,手动进样。08年三聚氰胺事件那会儿它可是个“功臣”。之后样品量大了,领导狠心加了个泵,配了个自动进样器用起来还是很稳的,多次比对做得都很好,一次性通过再之后,实验室又买了几台更高级的HPLC,它就很少上场了,只做三聚氰胺12年,走样时间一长(比如半天)就漏得特别厉害。13年计量检定不合格,连续进6针,到了第5针明显峰高就小了,到第6针又好了算算到现在停用进1年了,之前排查过,泵、检测器、柱子都没问题。怀疑是自动进样器出了问题,但按网友们的建议也一直也没发现哪里漏液。就算不进样单走流动相一样也会湿一大片。最近闲下来又排查了一次,意外发现泵旁边一大扎的管路上有液体渗出(如下图标记处)。http://ng1.17img.cn/bbsfiles/images/2014/08/201408281138_511956_1635352_3.jpg顺藤摸瓜,发现液体居然是从A泵的废液管里面流出来的,A泵可是后来新配的泵呀,一直都是走甲醇的。而且这个泵还换过一次柱塞杆密封圈。之前一直怀疑B泵会漏液的。打开看如下图,打记号的白色管子就是泵的废液管。http://ng1.17img.cn/bbsfiles/images/2014/08/201408281138_511957_1635352_3.jpg因为之前碰到过这种情况,可以确定是A泵的柱塞杆密封圈又坏了。下面是岛津说明书上的http://ng1.17img.cn/bbsfiles/images/2014/08/201408281138_511958_1635352_3.jpg如正常运行仪器,流动相从泵的废液管出的话,极大可能是泵内起密封作用的柱塞杆密封圈磨损了,导致泵里面漏液。但因长时间没用也没备耗材了,只等申购、、、 到这里,还有个问题一直令我很困惑:难道走有机试剂如甲醇比走缓冲盐对泵的损耗更大?按理说甲醇的粘度应该比反冲盐的粘度要小呀。还是后来买的泵先天不足本身质量就差些呢?小结:也许换上新的柱塞杆密封圈后,开机检查还会有漏液。但这次的排查提醒我们再“不可能”都是会“有可能的”,不能放过任何一个细节。
目的 建立超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]串联质谱法(UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS)同时测定昆明山海棠片中15种活性成分的含量。方法 采用Waters Cortecs T[size=12px]3[/size]色谱柱(2.1 mm×100 mm,1.6 μm),以体积分数0.1%甲酸乙腈溶液(A)-体积分数0.1%甲酸水溶液(B)为流动相,梯度洗脱,流速0.3 mLmin[size=12px]-1[/size],柱温35 ℃,通过正负离子切换扫描,在多反应监测模式下建立昆明山海棠片中15种活性成分的含量测定方法,包括2种黄酮(儿茶素和表儿茶素)、9种二萜(雷公藤内酯三醇、雷醇内酯、雷公藤内酯二醇、雷公藤甲素、雷公藤氯内酯醇、雷公藤内酯酮、雷酚内酯、雷公藤对醌A和雷公藤对醌B)和4种三萜(去甲泽拉木醛、雷公藤红素、雷公藤内酯甲和扁塑藤素)。结果 15种待测成分分别在各自范围内线性关系良好([i]r[/i][size=12px]2 [/size]≥ 0.999 1),加样回收率在88.36%~115.91%范围内(RSD ≤ 4.94%),含量测定结果显示,不同企业生产的昆明山海棠片中活性成分的含量存在较大差异,可能会给制剂的临床药效和安全性带来影响。结论 可用于昆明山海棠片中活性成分的含量测定,同时测定结果可为该制剂的质量评价提供参考和依据。
仪器用的是安捷伦1260系列。发生漏液之前是用了十几个小时的磷酸二氢钾作为流动相来进行检测。仪器用完之后本来打算用10%的甲醇水冲洗柱子和仪器的,结果不小心用成了90%的甲醇水,后面用水或者低浓度的甲醇水冲洗仪器和柱子就发现会漏液(图中标注位置)。换成二通也会漏液。流速一上0.3一上就漏。请问各种大佬这该怎么解决啊[img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206060947132833_7570_5312205_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206060947133058_3028_5312205_3.png[/img][img]https://ng1.17img.cn/bbsfiles/images/2022/06/202206060947131794_9571_5312205_3.png[/img]
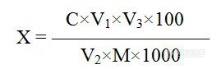
[color=black][b]藤青泡腾片提取工艺研究[/b][/color]藤青泡腾片是以闽产药食资源为基础制成的复方制剂,处方由藤茶、青果、葛花、甘草[font=times new roman]4[/font]味药材组成,具有调节血脂,保护化学性肝损伤的作用。传统中药煎煮繁琐,携带不便,气味较苦,将其制成泡腾片,携带、服用方便,崩解速度快,提高其生物利用度、临床疗效。本处方中各味药的主要有效成份为黄酮,水溶性较好,且二氢杨梅素等在热水中的溶解度大,因此采用水为提取溶液进行加热提取,成本低、实验条件简单。采用正交试验的方法考察各因素对总黄酮、浸膏得率的影响,获得最佳提取工艺。1.1[font=宋体][b]仪器与试药[/b][/font](1)实验仪器[font=times new roman] [/font][table][tr][td]电子分析天平[font=times new roman]XS105[/font][/td][td]METTLER TOLEDO[/td][/tr][tr][td]电子调温电热套[font=times new roman]98-1-B[/font]型[/td][td]天津市泰斯特仪器有限公司[/td][/tr][tr][td]电热恒温水浴锅[font=times new roman]HWS24[/font][/td][td]上海一恒科学仪器有限公司[/td][/tr][tr][td]常压恒温干燥箱[font=times new roman]XMTD-822[/font][/td][td]上海精宏实验设备有限公司[/td][/tr][tr][td]紫外分光光度计[font=times new roman]UV9100[/font][/td][td]北京瑞利分析仪器公司[/td][/tr][tr][td][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff][url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url][/color][/url]([font=times new roman]200 μL[/font]、[font=times new roman]1000 μL[/font])[/td][td]GILSON[/td][/tr][/table](2)实验试药葛花[font=times new roman] [/font]产地:安徽[font=times new roman] [/font]北京三和药业有限公司[font=times new roman] [/font]藤茶(产地:广西)、青果(产地:广东)、甘草(产地:甘肃)[table][tr][td]芦丁对照品[/td][td]批号:[font=times new roman]100080-20708[/font]中国[font=宋体]食品[/font]药品[font=宋体]检[/font]定[font=宋体]研究院[/font][/td][/tr][tr][td]甲醇[font=times new roman] (AR)[/font][/td][td]国药集团化学试剂有限公司[/td][/tr][tr][td]亚硝酸钠[font=times new roman](AR)[/font][/td][td]上海联试化工试剂有限公司[/td][/tr][tr][td]硝酸铝[font=times new roman](AR)[/font][/td][td]上海展云化工有限公司[/td][/tr][tr][td]氢氧化钠[font=times new roman](AR)[/font][/td][td]上海联试化工试剂有限公司[/td][/tr][/table] [font=times new roman][size=13px]1.2 [/size][/font][size=13px]泡腾片提取工艺条件的研究[/size]1.2.1[font=宋体][b]正交试验筛选[/b][/font]称取藤茶、葛花、青果、甘草各[font=times new roman]0.5[/font]倍处方量为[font=times new roman]1[/font]份,共[font=times new roman]9[/font]份,以加水量([font=times new roman]A[/font]),提取时间([font=times new roman]B[/font]),提取次数([font=times new roman]C[/font])为考察因素,按表[font=times new roman]1[/font]的因素水平进行[font=times new roman]L9[/font][font=times new roman][size=21px]([/size][/font][font=times new roman]3[/font][font=times new roman]4[/font][font=times new roman][size=21px])[/size][/font]正交试验,根据总黄酮含量、浸膏得率进行评价,考察最佳提取工艺条件。1.2.1.1[font=宋体][b]水提取液浸膏得率的测定[/b][/font]吸取1.2.1项下提取的每份药液[font=times new roman]15 ml[/font],转移到干燥蒸发皿内,置于水浴锅内蒸发水份至流浸膏后,放入烘箱于[font=times new roman]100[/font]℃烘干到恒重,称重,记录结果并计算,结果见表[font=times new roman]2[/font]1.2.1.2[font=宋体][b]水提取液总黄酮的含量测定[/b][/font]对照品溶液的制备:称芦丁对照品适量,精密称定,加甲醇溶解并定量稀释至每1 ml含[font=times new roman]0.2 mg[/font]的芦丁溶液,制得对照品溶液。供试品溶液的制备:取上述[font=times new roman]9[/font]份提取物各[font=times new roman]1[/font] [font=times new roman]ml[/font],于[font=times new roman]50[/font] [font=times new roman]ml[/font]容量瓶中,并用水稀释至刻度。芦丁对照品标准曲线制备:精密吸取芦丁对照品溶液[font=times new roman]0.0[/font],[font=times new roman]1.0[/font],[font=times new roman]2.0[/font],[font=times new roman]3.0[/font],[font=times new roman]4.0[/font],[font=times new roman]5.0[/font],[font=times new roman]6.0[/font] [font=times new roman]ml[/font],分别置[font=times new roman]25 ml[/font]([font=times new roman]V[/font][font=times new roman]3[/font])量瓶中,加水至[font=times new roman]6 ml[/font],加入1 ml的[font=times new roman]5%[/font] NaNO2,混匀,放置[font=times new roman]6min[/font],往容量瓶里加入1 ml的[font=times new roman]10%A[/font]l[font=times new roman](NO[/font][font=times new roman]3[/font][font=times new roman])[/font][font=times new roman]3[/font],混匀后静置[font=times new roman]6min[/font],加入[font=times new roman]10[/font] ml NaOH试液,混匀,加蒸馏水至刻度,混匀,静置[font=times new roman]15[/font]分钟,以[font=times new roman]0.0 ml[/font]对照品溶液制备的溶剂为空白对照,在[font=times new roman]510nm[/font]波长下测定各组的吸光度值。以吸光度为纵坐标[font=times new roman]([/font][font=times new roman][i]A[/i][/font][font=times new roman])[/font],浓度为横坐标([font=times new roman]mg/ml[/font]),绘制标准曲线,结果见图[font=times new roman]1[/font]。样品测定:吸取待测溶液[font=times new roman]10 ml[/font]([font=times new roman]V[/font][font=times new roman]2[/font])于[font=times new roman]25 ml[/font]容量瓶中,照芦丁对照品标准曲线制备自“加入[font=times new roman]1 ml[/font]的[font=times new roman]5%[/font] NaNO2”起,在波长[font=times new roman]510nm[/font]下测定样品的吸光度,([font=times new roman][i]X[/i][/font])。根据标准曲线求出样品中总黄酮的含量[img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009212136303003_5694_2166779_3.png[/img][color=black]结果计算:[/color][color=black] [/color][color=black] [/color][color=black]X—[/color][font=宋体][color=black]试样中总黄酮百分含量,以芦丁[/color][/font][color=black](C[/color][color=black]27[/color][color=black]H[/color][color=black]30[/color][color=black]O[/color][color=black]16[/color][color=black])[/color][font=宋体][color=black]计, [/color][/font][color=black]g/100g[/color][font=宋体][color=black]([/color][/font][color=black]ml[/color][font=宋体][color=black]);[/color][/font][color=black]C—[/color][font=宋体][color=black]标准曲线上读出供试品溶液中总黄酮的浓度,[/color][/font][color=black]mg/ml[/color][font=宋体][color=black];[/color][/font][color=black]V[/color][color=black]1[/color][color=black]—[/color][font=宋体][color=black]试样定容体积,[/color][/font][color=black]ml[/color][font=宋体][color=black];[/color][/font][color=black]V[/color][color=black]2[/color][color=black]—[/color][font=宋体][color=black]吸取供试液体积,[/color][/font][color=black]ml[/color][font=宋体][color=black];[/color][/font][color=black]V[/color][color=black]3[/color][color=black]—[/color][font=宋体][color=black]显色定容体积,[/color][/font][color=black]ml[/color][font=宋体][color=black];[/color][/font][color=black]M—[/color][font=宋体][color=black]试样取样量,[/color][/font][color=black]g(ml)[/color][font=宋体][color=black]。[/color][/font][color=black]结果见表[/color][font=times new roman][color=black]2[/color][/font][color=black],表[/color][font=times new roman][color=black]3. [/color][/font][font=times new roman][color=red] [/color][/font][align=center]表[font=times new roman]1 [/font]提取正交试验因素水平表[/align][table][tr][td=1,2][align=center]水平[/align][/td][td=3,1][align=center]因素[/align][/td][/tr][tr][td][align=center]A[font=宋体]加水量[/font]([font=宋体]倍[/font])[/align][/td][td][align=center]B[font=宋体]提取时间[/font](h)[/align][/td][td][align=center]C[font=宋体]提取次数[/font][/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]10[/align][/td][td][align=center]0.5[/align][/td][td][align=center]1[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]15[/align][/td][td][align=center]1.0[/align][/td][td][align=center]2[/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]20[/align][/td][td][align=center]1.5[/align][/td][td][align=center]3[/align][/td][/tr][/table]注:以[font=times new roman]D[/font]因素为误差项[color=black]图[/color][font=times new roman][color=black]1[/color][/font][color=black]芦丁标准品标准曲线 [/color][align=center][img]https://ng1.17img.cn/bbsfiles/images/2020/09/202009212136306476_9524_2166779_3.png[/img][size=16px] [/size][/align]采用加权平均法对浸膏得率、总黄酮含量进行综合评估,由于含量对泡腾片疗效的影响较大,因此,分别给予浸膏得率、总黄酮含量[font=times new roman]40%[/font]、[font=times new roman]60%[/font]的权重进行分配。浸膏的率越高,患者最终单次的给药量越多,较低较好,以最低得率[font=times new roman]19.808%[/font]为最高得分,而总黄酮为主要有效成份,宜越高越好,故以[font=times new roman]1.969[/font]为最高得分。以序号[font=times new roman]1[/font]为例计算综合评分:[font=times new roman](19.808/19.808)*0.4+(0.796/1.969)*0.6=0.643[/font],同理,可求得其余各综合评分,结果见表[font=times new roman]2.[/font] 表[font=times new roman]2[/font]提取正交试验结果([font=times new roman][i]n[/i][/font][font=times new roman]=9[/font])[table][tr][td][align=center]序号[/align][/td][td][align=center]A[/align][/td][td][align=center]B[/align][/td][td][align=center]C[/align][/td][td][align=center]D[/align][/td][td][align=center]浸膏得率[font=times new roman](%)[/font][/align][/td][td][align=center]总黄酮含量[font=times new roman](g)[/font][/align][/td][td][align=center]综合评分[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]1[/align][/td][td][align=center]19.808 [/align][/td][td][align=center]0.796 [/align][/td][td][align=center]0.643 [/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]2[/align][/td][td][align=center]2[/align][/td][td][align=center]29.159 [/align][/td][td][align=center]1.109 [/align][/td][td][align=center]0.610 [/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]3[/align][/td][td][align=center]3[/align][/td][td][align=center]3[/align][/td][td][align=center]34.835 [/align][/td][td][align=center]1.499 [/align][/td][td][align=center]0.684 [/align][/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]33.656 [/align][/td][td][align=center]1.490 [/align][/td][td][align=center]0.689 [/align][/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]2[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]37.467 [/align][/td][td][align=center]1.854 [/align][/td][td][align=center]0.776 [/align][/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]23.851 [/align][/td][td][align=center]0.978 [/align][/td][td][align=center]0.630 [/align][/td][/tr][tr][td][align=center]7[/align][/td][td][align=center]3[/align][/td][td][align=center]1[/align][/td][td][align=center]3[/align][/td][td][align=center]2[/align][/td][td][align=center]40.161 [/align][/td][td][align=center]1.969 [/align][/td][td][align=center]0.797 [/align][/td][/tr][tr][td][align=center]8[/align][/td][td][align=center]3[/align][/td][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]3[/align][/td][td][align=center]26.402 [/align][/td][td][align=center]1.099 [/align][/td][td][align=center]0.635 [/align][/td][/tr][tr][td][align=center]9[/align][/td][td][align=center]3[/align][/td][td][align=center]3[/align][/td][td][align=center]2[/align][/td][td][align=center]1[/align][/td][td][align=center]34.196 [/align][/td][td][align=center]1.544 [/align][/td][td][align=center]0.702 [/align][/td][/tr][tr][td][align=center]K1[/align][/td][td][align=center]1.94 [/align][/td][td][align=center]2.13 [/align][/td][td][align=center]1.91 [/align][/td][td][align=center]2.12 [/align][/td][td] [/td][td] [/td][td] [/td][/tr][tr][td][align=center]K2 [/align][/td][td][align=center]2.10 [/align][/td][td][align=center]2.02 [/align][/td][td][align=center]2.00 [/align][/td][td][align=center]2.04 [/align][/td][td] [/td][td] [/td][td] [/td][/tr][tr][td][align=center]K3[/align][/td][td][align=center]2.13 [/align][/td][td][align=center]2.02 [/align][/td][td][align=center]2.26 [/align][/td][td][align=center]2.01 [/align][/td][td] [/td][td] [/td][td] [/td][/tr][tr][td][align=center]R[/align][/td][td][align=center]0.07 [/align][/td][td][align=center]0.04 [/align][/td][td][align=center]0.12 [/align][/td][td][align=center]0.04 [/align][/td][td][align=center] [/align][/td][td][align=center] [/align][/td][td][align=center] [/align][/td][/tr][/table][align=center]表[font=times new roman]3[/font]提取正交试验方差分析[/align][table][tr][td][align=center]方差来源[/align][/td][td][align=center]离差平方和[/align][/td][td][align=center]自由度[/align][/td][td][align=center]F[font=宋体]值[/font][/align][/td][td][align=center]均方[/align][/td][td][align=center]显著性[/align][/td][/tr][tr][td][align=center]加水量[/align][/td][td][align=center]0.007349[/align][/td][td][align=center]2[/align][/td][td][align=center]3.2139[/align][/td][td][align=center]0.003675[/align][/td][td] [/td][/tr][tr][td][align=center]提取时间[/align][/td][td][align=center]0.002731[/align][/td][td][align=center]2[/align][/td][td][align=center]1.1945[/align][/td][td][align=center]0.001366[/align][/td][td] [/td][/tr][tr][td][align=center]提取次数[/align][/td][td][align=center]0.02189[/align][/td][td][align=center]2[/align][/td][td][align=center]9.5733[/align][/td][td][align=center]0.01095[/align][/td][td][align=center]**[/align][/td][/tr][tr][td][align=center]误差[/align][/td][td][align=center]0.002287[/align][/td][td][align=center]2[/align][/td][td][align=center]1.0000 [/align][/td][td][align=center]0.001143[/align][/td][td] [/td][/tr][/table]由表[font=times new roman]3[/font]可知,根据水提取液中总黄酮含量与浸膏得率进行评估,各因素对结果的影响大小:提取次数[font=times new roman][/font]加水量[font=times new roman][/font]提取时间,即主要影响因素是提取次数,其次是加水量,提取时间影响最小。以实验结果为参考,结合实际生产情况,最终确定提取工艺为:加水[font=times new roman]20[/font]倍量,每次提取[font=times new roman]0.5h[/font],提取[font=times new roman]3[/font]次。1.2.2[font=宋体][b]提取正交验证实验[/b][/font]根据以上所选最佳提取工艺条件,加水[font=times new roman]20[/font]倍量,每次提取[font=times new roman]0.5h[/font],提取[font=times new roman]3[/font]次,平行[font=times new roman]3[/font]份,对水提取液的浸膏得率与总黄酮含量进行测定,按[font=times new roman]1.2.1.2[/font]项下的方法计算综合评分后,求平均得分,结果见表[font=times new roman]4.[/font][align=center]表[font=times new roman]4[/font]提取正交实验验证结果([font=times new roman][i]n[/i][/font][font=times new roman]=3[/font])[/align][table][tr][td][align=center]编号[/align][/td][td][align=center]浸膏得率(%)[/align][/td][td][align=center]总黄酮含量(g)[/align][/td][td][align=center]综合评分[/align][/td][td][align=center]平均得分[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]37.3[/align][/td][td][align=center]2.036[/align][/td][td][align=center]0.833[/align][/td][td=1,3][align=center]0.830[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]38.1[/align][/td][td][align=center]2.038[/align][/td][td][align=center]0.829[/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]37.4[/align][/td][td][align=center]2.021[/align][/td][td][align=center]0.828[/align][/td][/tr][/table]由表[font=times new roman]4[/font]可知,[font=times new roman]3[/font]份平行实验最终的平均得分为[font=times new roman]0.830[/font],接近于正交设计中的[font=times new roman]A3B1C3[/font]综合评分,且评分最高,有良好的重复性和较高的准确率,所筛选的提取工艺条件基本稳定,可作为藤青泡腾片的提取方法。小结与讨论在提取工艺的探讨过程中,用正交试验的方法研究加水量、提取时间、提取次数对药液浸膏得率和总黄酮含量的影响,获得最适提取条件为:[font=times new roman]20[/font]倍量水,提取[font=times new roman]3[/font]次,每次提取[font=times new roman]0.5h[/font]。试验中发现,青果为橄榄的干燥果实,本处方中用量较少,为方便称取,同时提高没食子酸等有效成份的提取率,宜先将其进行粉碎;藤茶、葛花密度小,提取过程中浮于水面,应将其充分润湿,使其浸没于水中,以免影响各成份的提取率;若直接加热煎煮,提取过程中水分蒸发严重,实验结果重现性差,宜采用冷凝回流的方法进行提取。
[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]六联采样器,最近堵住了,开始抽气取样阀开始漏液,有人说样品没有用甲醇清洗和堵塞后,我想知道是否有必要进几针甲醇清洗完每次样品走完,是什么原因造成漏液?
今天突然看见醌氢醌,虽然是个简单的对苯二酚,但不知用什么用途,是说在PH的缓冲溶液中加入过量的醌氢醌,不知是什么用途,不知哪位版友能给与解答,先行谢过!!!在PH的缓冲溶液中加入过量的醌氢醌,是在PH4和7的缓冲溶液中加入过量的醌氢醌,说是这样此缓冲溶液可以延长保质期至一周,不知是什么原理?
纯度分析操作看似容易,要注意的问题不少,其实做起来并不简单。 主要问题是线形范围问题。 热导线形范围窄,做高纯物体分析有困难。电子俘获类似。 氢焰检测器要注意进样量,否则主峰容易超限,小峰容易漏检。
单纯用液相如何判断哪种品牌的甲醇或乙腈更好?市面上用于HPLC的甲醇和乙腈品牌很多,有国产的也有进口的,当我们用的一个牌子的试剂不爽的时候,我们会想着找一个替代的品牌,但如何保证新品牌的质量比原来好至少不亚于原来的品牌呢?这经常会让我们感到头疼。说来也很讽刺,液相是通常是用于检测有机物含量的,但是我们有液相却没有办法用它来检测甲醇或乙腈的纯度和含量,甲醇和乙腈的纯度含量分析通常是用气相来做的,可我们只有液相(当然同时拥有气相的朋友就方便多了),怎么办?
[b][font=宋体]藤三七[/font][font=宋体]总[/font][font=宋体]多糖的制备、鉴别与纯度检查[/font][font=宋体]及提取[/font][font=宋体]条件优化[/font][/b][font=宋体]1.[/font][font=宋体]样品预处理[/font][font=宋体]干燥样品经粉碎机粉碎,过[/font]40[font=宋体]目筛,置密封袋中,干燥、避光条件下密封保存[/font][b][font=宋体]2.[/font][font=宋体]可见分光光度法测定条件[/font][/b][font=宋体]精密吸取葡萄糖对照品溶液和供试品溶液适量,置[/font][font=宋体]10 mL[/font][font=宋体]具塞磨口试管中,[/font][font=宋体]加入[/font]5[font=宋体] [/font]%[font=宋体]苯酚溶液[/font]1 mL[font=宋体],充分混匀后,加入浓硫酸[/font]6 mL[font=宋体],[/font]40[font=宋体] [/font][font=宋体]℃反应[/font]20 min[font=宋体],放置室温,在[/font]490 nm[font=宋体]处测得吸光度。[/font][b][font=宋体]藤三七[/font][font=宋体]总[/font][font=宋体]多糖的制备、鉴别与纯度检查[/font][font=宋体]与提取[/font][font=宋体]3.[/font][font=宋体]藤三七[/font][font=宋体]纯化[/font][font=宋体]多糖的制备[/font][/b][font=宋体]取藤三七药材干粉约[/font]10 g[font=宋体],精密称定,[/font][font=宋体]加入石油醚[/font](60[font=宋体]~[/font]90 [font=宋体]℃[/font])100 mL[font=宋体]回流提取两次,每次[/font]2 h[font=宋体],弃去[/font][font=宋体]提取液[/font][font=宋体]([/font][font=宋体]除去[/font][font=宋体]脂溶性成分[/font][font=宋体])[/font][font=宋体],药渣烘干,用[/font]80[font=宋体] [/font]%[font=宋体]乙醇[/font]100 mL[font=宋体]浸泡过夜,回流提取[/font]2[font=宋体]次,每次[/font]2 h[font=宋体]。弃去提取液[/font]([font=宋体]除去单糖、低聚糖[/font][font=宋体]和苷类等小分子物质[/font])[font=宋体],药渣烘干,[/font][font=宋体]加蒸馏水[/font]100 mL[font=宋体]回流,提取三次,每次[/font]2 h[font=宋体]。合并提取液,减压浓缩至[/font]40 mL[font=宋体],[/font][font=宋体]即得粗多糖的水溶液。[/font][font=宋体]在粗多糖水溶液中加入[/font]Sevage[font=宋体]试剂[/font][font=宋体]([/font][font=宋体]氯仿:正丁醇[/font][font=宋体]=[/font]4[font=宋体]:[/font]l[font=宋体])[/font]10 mL[font=宋体],剧烈震荡[/font]20 min[font=宋体],使其充分混合,在[/font]4000 rmin[sup] -1[/sup][font=宋体]转速下离心[/font]5 min[font=宋体],弃去中间变性蛋白层和下层有机层,水相继续重复上述操作[/font]8[font=宋体]次,直至水相与有机相中间无变性蛋白出现为止,[/font][font=宋体]即得脱蛋白多糖水溶液。[/font][font=宋体]向脱蛋白多糖水溶液中加入[/font][font=宋体]无水乙醇[/font]80 mL[font=宋体],使溶液含醇量达[/font]80[font=宋体] [/font]%[font=宋体]以上,充分[/font][font=宋体]搅拌,[/font][font=宋体]静置过夜。在[/font]4000 r min[sup] -1[/sup][font=宋体]转速下离心[/font]5 min[font=宋体],弃去上清液,所得沉淀依次用无水乙醇、丙酮、无水乙醚各洗涤[/font]3[font=宋体]次,弃去有机溶剂[/font][sup][2[/sup][sup][font=宋体]2[/font][/sup][sup]-2[/sup][sup][font=宋体]5[/font][/sup][sup]][/sup][font=宋体]后挥干沉淀,并用真空干燥机抽真空,[/font]60[font=宋体] [/font][font=宋体]℃干燥[/font]30 min[font=宋体],得到灰白色颗粒状多糖样品。[/font][b][font=宋体]4.[/font][font=宋体]藤三七[/font][font=宋体]总[/font][font=宋体]多糖的鉴别与纯度检查[/font][font=宋体]([/font]1[font=宋体])[/font]Molish[font=宋体]试验[/font][/b](1)[font=宋体]供试品溶液:取藤三七多糖[/font]10 mg[font=宋体],加[/font]10 mL[font=宋体]蒸馏水,加热溶解,[/font][font=宋体]量取[/font]1 mL[font=宋体]至试管中,[/font][font=宋体]再加入[/font]α-[font=宋体]萘酚[/font][font=宋体]乙醇溶液[/font][font=宋体];[/font](2)[font=宋体]阳性对照品溶液:取淀粉[/font]10 mg[font=宋体],加[/font]10 mL[font=宋体]蒸馏水,加热溶解,[/font][font=宋体]量取[/font]1 mL[font=宋体]至试管中,[/font][font=宋体]再加入[/font]α-[font=宋体]萘酚[/font][font=宋体]乙醇溶液[/font][font=宋体];[/font](3)[font=宋体]阴性对照品溶液:[/font][font=宋体]量取[/font]1 mL[font=宋体]蒸馏水于试管中[/font][font=宋体],加入[/font]α-[font=宋体]萘酚[/font][font=宋体]乙醇溶液[/font][font=宋体]。[/font][font=宋体]分别摇匀上述溶液,将试管倾斜,沿试管壁慢慢加入浓硫酸,竖直试管观察。结果,供试品溶液与阳性对照品溶液试管中界面呈[/font][font=宋体]紫堇[/font][font=宋体]色环,阴性对照品溶液试管界面无变化,表明供试品为糖类。[/font][b][font=宋体]([/font]2[font=宋体])[/font]Feling[font=宋体]试验[/font][/b]Feling[font=宋体]试剂的配[/font][font=宋体]制[/font][font=宋体]:[/font][font=宋体]甲液[/font][font=宋体]:[/font][font=宋体]取[/font]34.6 g[font=宋体]酒石酸钾钠[/font]KNaC[sub]4[/sub]H[sub]4[/sub]O[sub]6[/sub]4H[sub]2[/sub]O[font=宋体],[/font]14.2 g NaOH[font=宋体]固体溶于[/font]80 mL[font=宋体]水中,加水稀释到[/font]100[font=宋体] [/font]mL[font=宋体];[/font][font=宋体]乙液[/font][font=宋体]:称取[/font]7.28 g CuSO[sub]4[/sub]5H[sub]2[/sub]O[font=宋体]溶于[/font]40 mL[font=宋体]水中,加水稀释到[/font]100 mL[font=宋体]待用。使用时取等体积两溶液混合即可。[/font](1)[font=宋体]供试品溶液:[/font] [font=宋体]取上述[/font][font=宋体]多糖溶液[/font]1 mL[font=宋体]于试管中;[/font](2)[font=宋体]阳性对照品溶液:取葡萄糖[/font]10 mg[font=宋体],加[/font]10 mL[font=宋体]蒸馏水,溶解,摇匀,[/font][font=宋体]量取[/font]1 mL[font=宋体]于试管中;[/font](3)[font=宋体]阴性对照品溶液:[/font] [font=宋体]量取蒸馏水[/font]1 mL[font=宋体]于试管中。[/font][font=宋体]分别加入[/font]Feling[font=宋体]试剂[/font]2 mL[font=宋体],在沸水中加热[/font]10 min[font=宋体]。结果,供试品溶液与阴性对照品溶液为蓝色,阳性对照品溶液变为砖红色。单糖多为还原性糖,可与[/font]Feling [font=宋体]试剂反应产生砖红色,而多糖为非还原性糖,不与[/font]Feling[font=宋体]试剂反应,结果表明供试品中不含有单糖。[/font][b][font=宋体]([/font]3[font=宋体])[/font][font=宋体]紫外可见光谱分析[/font] [/b][font=宋体]将上述供试品溶液在[/font]190 ~ 500 nm[font=宋体]区间进行光谱扫描,结果在[/font]260 ~ 280 nm[font=宋体]处无明显吸收峰,而未经脱蛋白处理的藤三七粗多糖水溶液,在[/font]260 ~ 280 nm[font=宋体]处有明显吸收峰,表明多糖样品中不含有蛋白质、多肽和核酸类物质。[/font][font=宋体]通过以上三种试验证明所制藤三七多糖为不含单糖、蛋白质、多[/font][font=宋体]肽[/font][font=宋体]、核酸等物质的纯化多糖。[/font][b][font=宋体]5.[/font] [font=宋体]苯酚[/font][font=宋体]-[/font][font=宋体]硫酸法测定总[/font][font=宋体]多[/font][font=宋体]糖含量的条件优化[/font][font=宋体]检测波长的选择[/font][/b][font=宋体]吸取一定浓度的葡萄糖对照品溶液[/font] 0. 2 mL[font=宋体],用蒸馏水补充至[/font]1 mL[font=宋体],加入[/font]5[font=宋体] [/font]%[font=宋体]苯酚溶液[/font]1 mL[font=宋体],充分混匀后,加入浓硫酸[/font]6 mL[font=宋体],振摇[/font]5 min[font=宋体],至[/font]40[font=宋体] [/font][font=宋体]℃水中反应[/font] 20 min[font=宋体],放置室温,同法制得空白溶液,紫外可见分光光度计在[/font]200~800 nm[font=宋体]范围内扫描,结果表明最大吸收波长为[/font]490 nm[font=宋体]。[/font][b][font=宋体]提取方法的优化[/font][/b][font=宋体]采用正交设计,选用提取溶剂用量[/font](A)[font=宋体]、提取时间[/font](B)[font=宋体]及提取温度[/font](C)3[font=宋体]个因素,每个因素选[/font]3[font=宋体]个水平,用[/font]L[sub]9[/sub](3[sup]4[/sup])[font=宋体]正交表进行实验设计的优选,见表[/font]1[font=宋体]。[/font][font=宋体]以藤三七总多糖的含量为检测指标,[/font] [font=宋体]处理组合见表[/font]2[font=宋体] ~[/font]3[font=宋体]。[/font][align=center][font=宋体]表[/font].1 The factor-level table[/align][table][tr][td]levels[/td][td][align=center]A[/align][align=center]Quant. of solvent [/align][align=center](mL)[/align][/td][td][align=center]B[/align][align=center]Time[/align][align=center](h)[/align][/td][td][align=center]C[/align][align=center]Temp[/align][align=center]([font=宋体]℃[/font])[/align][/td][/tr][tr][td]1[/td][td][align=center]10[/align][/td][td]2[/td][td]70[/td][/tr][tr][td]2[/td][td][align=center]20[/align][/td][td]3[/td][td]80[/td][/tr][tr][td]3[/td][td][align=center]30[/align][/td][td]4[/td][td]90[/td][/tr][/table][font=宋体] [/font][font=宋体]取烘干并粉碎的藤三七药材[/font]9[font=宋体]份,每份[/font]1 g[font=宋体],精密称定,用[/font]80[font=宋体] [/font]%[font=宋体]乙醇浸泡过夜,再用[/font]80[font=宋体] [/font]%[font=宋体]乙醇回流[/font]2 h[font=宋体],残渣挥去溶剂,根据正交实验设计,分别加入不同体积水、按不同提取时间、不同提取温度提取。提取液过滤,待冷却后转移于[/font]250 m[font=宋体]L[/font][font=宋体]容量瓶,用蒸馏水稀释至刻度。精密吸取[/font]l mL[font=宋体]于试管中,再分别加入[/font]5[font=宋体] [/font]%[font=宋体]苯酚溶液[/font]1 mL[font=宋体],充分混匀后,加入浓硫酸[/font] 6 mL[font=宋体],[/font]40[font=宋体] [/font][font=宋体]℃[/font][font=宋体]反应[/font]20 min[font=宋体],放至室温,[/font]490 nm[font=宋体]处测得吸光度。[/font][align=center][font=宋体]表[/font]2 Results of L[sub]9[/sub](3[sup]4[/sup]) orthogonal design[/align][table][tr][td][align=center] [/align][align=center]Test NO.[/align][/td][td][align=center]A[/align][align=center]Volume[/align][/td][td][align=center]B[/align][align=center]Time[/align][/td][td][align=center]C[/align][align=center]Temp[/align][/td][td][align=center] [/align][align=center]Content (%)[/align][/td][/tr][tr][td][align=center]1[/align][/td][td]10[/td][td][align=center]2[/align][/td][td][align=center]70[/align][/td][td][align=center]1.66[font=宋体]2[/font][/align][/td][/tr][tr][td]2[/td][td][align=center]10[/align][/td][td][align=center]3[/align][/td][td][align=center]80[/align][/td][td][align=center]2.53[font=宋体]1[/font][/align][/td][/tr][tr][td]3[/td][td][align=center]10[/align][/td][td][align=center]4[/align][/td][td][align=center]90[/align][/td][td][align=center]3.4[font=宋体]18[/font][/align][/td][/tr][tr][td]4[/td][td][align=center]20[/align][/td][td][align=center]2[/align][/td][td][align=center][font=宋体]8[/font]0[/align][/td][td][align=center]2.31[font=宋体]4[/font][/align][/td][/tr][tr][td]5[/td][td][align=center]20[/align][/td][td][align=center]3[/align][/td][td][align=center][font=宋体]9[/font]0[/align][/td][td][align=center]3.19[font=宋体]4[/font][/align][/td][/tr][tr][td]6[/td][td][align=center]20[/align][/td][td][align=center]4[/align][/td][td][align=center][font=宋体]7[/font]0[/align][/td][td][align=center]1.80[font=宋体]3[/font][/align][/td][/tr][tr][td]7[/td][td][align=center]30[/align][/td][td][align=center]2[/align][/td][td][align=center][font=宋体]9[/font]0[/align][/td][td][align=center]4.02[font=宋体]2[/font][/align][/td][/tr][tr][td]8[/td][td][align=center]30[/align][/td][td][align=center]3[/align][/td][td][align=center][font=宋体]7[/font]0[/align][/td][td][align=center]1.90[font=宋体]4[/font][/align][/td][/tr][tr][td]9[/td][td][align=center]30[/align][/td][td][align=center]4[/align][/td][td][align=center][font=宋体]8[/font]0[/align][/td][td][align=center]2.76[font=宋体]0[/font][/align][/td][/tr][tr][td]K[sub]1[/sub][/td][td][align=center]2.537[/align][/td][td][align=center]2.663[/align][/td][td][align=center]1.787[/align][/td][td][/td][/tr][tr][td]K[sub]2[/sub][/td][td][align=center]2.433[/align][/td][td][align=center]2.54[/align][/td][td][align=center]2.533[/align][/td][td][/td][/tr][tr][td]K[sub]3[/sub][/td][td][align=center]2.893[/align][/td][td][align=center]2.66[/align][/td][td][align=center]3.543[/align][/td][td][/td][/tr][tr][td][align=center] R[/align][/td][td][align=center]0.64[/align][/td][td][align=center]0.123[/align][/td][td][align=center]1.756[/align][/td][td][/td][/tr][/table][font=宋体]表[/font]3 Results of analysis of varianee[table][tr][td][align=center]Source of[/align][align=center]variation[/align][/td][td][align=center]Sum of[/align][align=center]squares[/align][/td][td]Degrees of freedom[/td][td][align=center]F[/align][/td][td][align=center]P[/align][/td][/tr][tr][td][align=center]A[/align][/td][td][align=center]0.379[/align][/td][td][align=center]2[/align][/td][td][align=center]2.958[/align][/td][td][align=center] [/align][/td][/tr][tr][td][align=center]B[/align][/td][td][align=center]0.03[/align][/td][td][align=center]2[/align][/td][td][align=center]0.254[/align][/td][td][align=center] [/align][/td][/tr][tr][td][align=center]C[/align][/td][td][align=center]4.663[/align][/td][td][align=center]2[/align][/td][td][align=center]39.517[/align][/td][td][align=center]AB[font=宋体],最佳水平组合为[/font]A[sub]3[/sub]B[sub]1[/sub] C[sub]3[/sub][font=宋体],即加入[/font]30[font=宋体]倍体积水于[/font]90[font=宋体] [/font][font=宋体]℃水浴中提取[/font]2 h[font=宋体]。[/font][font=宋体]方差分析[/font] [font=宋体]由表[/font]2-3[font=宋体]方差分析结果可见:水浴温度对测定结果有显著性影响。[/font][font=宋体]综合分析[/font] [font=宋体]综合考虑各因素对[/font]3[font=宋体]个考察指标的影响,确定藤三七总多糖的最佳提取工艺条件为[/font]A[sub]3[/sub]B[sub]1[/sub]C[sub]3[/sub][font=宋体],即加入[/font]30[font=宋体]倍量体积水于[/font]90[font=宋体] [/font][font=宋体]℃水浴中提取[/font]2 h[font=宋体]。[/font][font=宋体]多糖提取次数的考察[/font] [font=宋体]称取藤三七药材粉末约[/font]1 g[font=宋体],精密称定,按正交试验优选的最佳工艺条件分别提取[/font]3[font=宋体]次,实验结果见表[/font]4[font=宋体]。[/font][align=center][font=宋体]表[/font]-4 Results with the different times[/align][table][tr][td][align=center]time[/align][/td][td][align=center][font=宋体]extraction rate [/font](%)[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center][font=宋体]77.63[/font][/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center][font=宋体]22.37[/font][/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center][font=宋体]1.225[/font][/align][/td][/tr][/table][font=宋体]由表可以看出,第[/font]1[font=宋体]次和第[/font]2[font=宋体]次[/font][font=宋体]的[/font][font=宋体]多糖[/font][font=宋体]提取[/font][font=宋体]率较多,而第[/font]3[font=宋体]次多糖[/font][font=宋体]的提取[/font][font=宋体]率较少,多糖[/font][font=宋体]提取率[/font][font=宋体]不足[/font][font=宋体]1.3 [/font]%[font=宋体],所以提取次数可选为[/font]2[font=宋体]次。[/font][font=宋体]综上所述,本实验得到藤三七多糖最佳提取工艺条件为[/font]30[font=宋体]倍量体积的水,于[/font]90[font=宋体] [/font][font=宋体]℃水浴中提取[/font]2[font=宋体]次,每次[/font]2 h[font=宋体]。[/font]
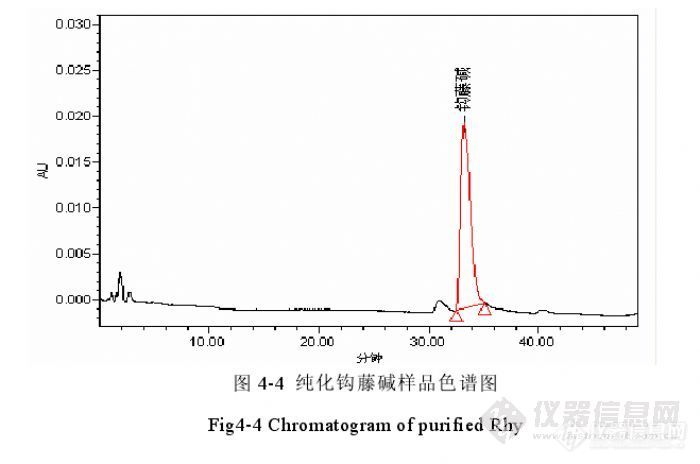
作者】 刘明; 【导师】 汤建林;【作者基本信息】 第三军医大学, 药物分析学, 2011, 硕士【摘要】 钩藤为我国传统中药,其药材中所含吲哚类生物碱为主要药效成分,现代药理研究表明,钩藤生物碱除具有降压、抗癫痫作用外,还有一定抗焦虑作用,应用价值较高。为了进一步研究钩藤活性成分,特别是钩藤生物碱的药用价值,如何从钩藤药材中获得钩藤生物碱有效成分成为进一步研究的关键。现有提取工艺主要针对钩藤粗提物及总生物碱,针对有效成分的提取研究较少。本课题对钩藤碱提取纯化工艺、质量标准及抗焦虑药效学进行研究,确定最佳提取纯化工艺,考察质量标准,并对其抗焦虑药效进行初步评价。1.定性定量方法建立建立薄层色谱定性分析钩藤碱的方法,以丙酮-石油醚-氨水(1:2:0.2)为展开剂,钩藤碱在GF254硅胶板(规格:厚度0.20.25mm,25×40mm)上能与其它生物碱及杂质有效分离,在5分钟内即可完成钩藤碱的鉴别。建立高效液相色谱外标法定量分析钩藤碱的方法,采用Platisil ODS(150 mm×4.6 mm,5μm)色谱柱,以乙腈:0.01mol/L磷酸二氢钾(KOH调pH8.0)为流动相,梯度洗脱,在40 min内乙腈与0.01mol/L磷酸二氢钾比例由30:70线性递增至60:4... http://ng1.17img.cn/bbsfiles/images/2012/07/201207311344_380867_2379123_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/07/201207311346_380868_2379123_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/07/201207311347_380869_2379123_3.jpg
文章来源:科学网 时间:2012.05.21 近日来自厦门大学药学院的研究人员在新研究中从传统中草药雷公藤分离出活性成分雷公藤甲素(triptolide),并在体内外实验中证实其可以调控tRXRα介导的癌细胞存活信号通路。相关研究论文发布在《Plos ONE》杂志上。 厦门大学的曾锦章教授和张晓坤教授为这篇文章的共同通讯作者。陆娜和刘金星两位硕士研究生是该文章的共同第一作者。 从天然产物中寻找抗肿瘤活性成分是发展抗肿瘤药物的重要策略之一,雷公藤是我国一种资源比较丰富的传统中草药,其结构多样的有效成分具有明显的抗炎、免疫抑制和抗肿瘤等作用,是开发治疗药物的一个宝藏,但雷公藤具有很大的毒性,分子靶点和作用机制不清楚,是迄今制约雷公藤发展成真正治疗药物的关键。 在这篇文章中,研究人员从中药雷公藤中分离出活性成分雷公藤甲素,并证实其调控了tRXRα介导的癌细胞存活信号通路。研究结果显示雷公藤甲素依赖于细胞内的tRXRα表达水平强有力地诱导了癌细胞凋亡,证实了tRXRα是雷公藤甲素一个重要的细胞内靶点。 tRXRα是核受体视黄醇X受体-α(RXRα)的一种在其N-端截短的突变体,普遍存在于各种肿瘤组织中,与其全长RXRα?主要定位于细胞核不同,tRXRα?通常转位于细胞质,通过与p85相互作用激活PI3K/AKT信号转导通路,是肿瘤微环境中大量表达的肿瘤坏死因子TNFα?所依赖的生存通道,tRXRα的高度表达对于肿瘤的生长有重要的促进作用。 研究人员证实雷公藤甲素选择性地诱导了tRXRα降解,并抑制了tRXRα依赖的AKT活性,但却没有影响全长的RXRα。研究人员还证实雷公藤甲素靶向tRXRα强有力地激活了TNFα死亡信号,并促进了其他化疗的抗癌活性。 新研究确定了雷公藤甲素是tRXRα依赖的存活信号通路的一个新的调控物质,从而提供了关于雷公藤甲素作用诱导癌细胞凋亡机制的新见解。雷公藤甲素代表了具有不良副效应的传统中草药天然产物最有希望的一个治疗先导物。新研究发现为开发出用于癌症治疗的改良雷公藤甲素类似物提供了分子基础和新方向。