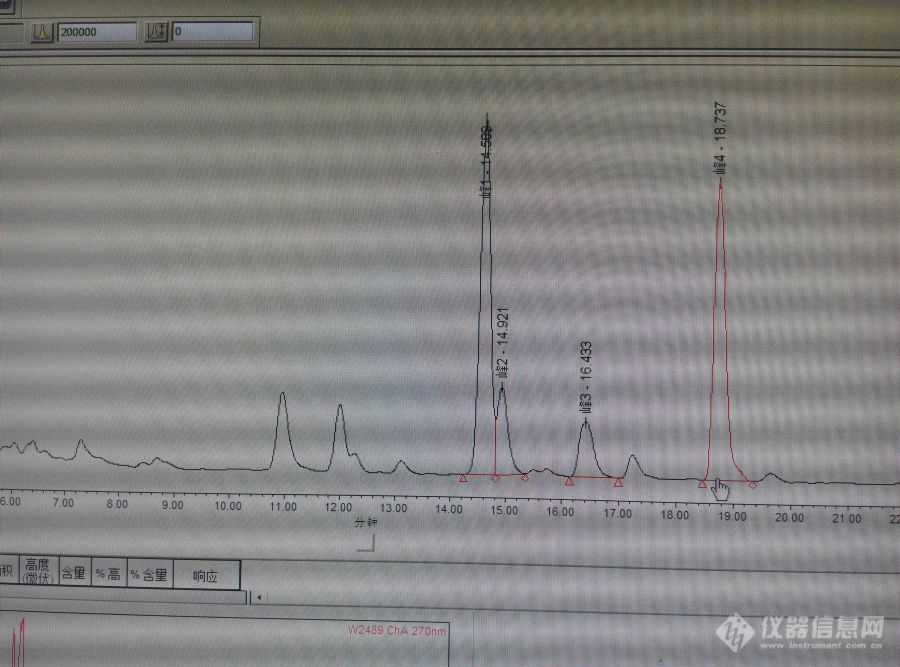
请问,增补二,丹参—丹参酮类中隐丹参酮与丹参酮1的峰就是分不开的吗?[img=,690,511]https://ng1.17img.cn/bbsfiles/images/2019/07/201907251441315687_7589_1750127_3.jpg!w690x511.jpg[/img]
提问帖(4.05)如果用丹参酮合成二氢丹参酮二乙酯需要用迪马哪些产品呢?
哪有卖丹参素钠和丹参酮?
求助:丹参中丹参酮类的行列计算方法?先要计算出隐丹参酮和丹参酮I的保留时间?还是直接用丹参酮IIA的峰面积乘以校正因子来计算3个成分的含量?
优良的遗传基因是决定优质药用植物形成的基础和内在因素[1]。DNA分子标记可以从居群及分子的水平上来阐明优质药用植物产生的生物学本质[2],已有大量报道表明基于DNA分子标记的遗传多样性分析揭示了厚朴、肉苁蓉、甘草等道地药材独特药材品质是由当地独特的环境与药材基因型相互作用所产生的[3-6]。目前,已开发出包括扩增片段长度多态性(amplified fragment length polymorphism,ALFP)、简单重复序列(simple sequence repeats,SSR)、相关序列扩增多态性(sequence related amplified polymorphism,SRAP)、简单重复序列间区(inter-simple sequence repeat,ISSR)、目标起始密码子多态性(start codon targeted polymorphism,SCoT)、单核苷酸多态性(single nucleotide polymorphisms,SNP)在内的大量分子标记可用于药用植物研究[7-9],其中,ISSR和SCoT由于具有引物通用性、随机性、设计简单、重复性好等优势而更加适用于药用植物遗传多样性及亲缘关系分析[10, 11]。 《神农本草经》中提出“土地所出,真伪新陈,并各有法”。特定的大气、水文、土壤等环境条件造就了不同的药材特性[12]。因此,为了增加药用植物中有效成分的含量,提高药材的品质,需要探索分析药用植物的品质与赖以生存的环境之间的联系[13]。例如,年平均气温、年日照时数、pH、Sr、Ca、S和交换性K等生态因子都是影响远志有效成分和生物活性的主要因素[14]。日照时数、相对湿度是影响黄芪中黄芪甲苷和黄芪多糖及黄酮类成分的关键因子[15]。除遗传因素和环境因素的影响外,药材的栽培、采收技术和产地的初加工等人文因素都会对药用植物的次生代谢产物有影响[16],近年来,随着野生资源的逐渐减少。栽培的中药材已经成为了常用中药的主要来源。大多药材栽培产区的药农在长期栽培过程中结合实践,积累了丰富的种植生产经验,有效的控制了药材的质量[17-18]。 丹参Salvia miltiorrhiza Bge.隶属唇形科(Labiatae)鼠尾草属Salvia L.,为多年生草本植物[19],以其干燥根及根茎入药,用于治疗胸痹心痛、月经不调、疮瘍肿痛等病症[20]。丹参酮Ⅰ、丹参酮ⅡA、隐丹参酮等是丹参中主要的二萜类有效成分[21-22]。迷迭香酸、丹酚酸A、丹酚酸B等则是主要的酚酸类成分[23-24]。现代药理学认为,丹参酮类和丹酚酸类化合物(尤其是丹酚酸B)均具有较强的抗肿瘤、抗菌消炎、心脏保护等多种药理作用,临床上广泛应用于心脑血管疾病的治疗[25-26]。丹参一般栽种在海拔较低的丘陵地带,野生丹参常见于草丛、林下、山坡及溪谷旁[27]。其对环境的适应性较强,广泛的分布于我国华东、华中、华北、华南等地区,西北、西南的部分省区也有分布。四川、山东、陕西、河南是丹参栽培的传统道地产区,其中,四川中江所产丹参在各产区丹参中品质较佳,一直作为中药丹参出口的优质道地药材,大量出口于中国周边东南亚国家。 近年以来,由于丹参长期的只种不选导致栽培品种退化,质量下降,使得道地性丧失。另一方面,由于过度采挖,导致野生资源遭到破坏,而临床需求量不断增大使得丹参资源日益紧缺、丹参的药材市场混杂,药材质量和数量难以保证,严重影响其疗效,制约其产业发展。因此,本研究以采自四川中江、陕西商州(镇安、山阳)、山东蒙阴(临朐、济阳、新泰、平邑)、河南伊川、山西曲沃等丹参主要栽培区的丹参样品以及栽培区土壤气候为研究对象,利用ISSR和SCoT标记对不同产区丹参进行遗传多样性评价,并结合有效成分、生态环境的分析,明确影响丹参品质的主导因子以及丹参种植的适宜环境,以期为丹参的高产稳产、优质及后续丹参扩大种植的产区选择提供理论依据。 1 仪器与材料 T100 [url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]仪(美国Bio-Rad公司)、GelDoc XR凝胶成像系统(美国Bio-Rad公司)、DYY-7C型电泳仪(北京六一生物科技有限公司)、BCD-532WDPT型超低温冰箱(青岛海尔股份有限公司)、LC-20A型高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url](日本岛津公司)、CR22N型高速冷冻离心机(德国Eppendorf公司)、Thermo Scientific? iCAP? PRO XP ICP-OES(美国Thermo Fisher公司)等。本研究共采集22个丹参S. miltiorrhiza Bge.居群,每个居群随机选取3株植株分别取适量幼嫩叶片,用于丹参遗传关系的分析。选择部分产地丹参为代表测定丹参有效成分,同时采集丹参根际土壤,材料采集信息如表1、2所示。 2 方法 2.1 ISSR和SCoT分子标记分析 使用植物DNA提取试剂盒(浙江兰博生物科技有限公司)提取四川、山东、陕西、河南、山西5个省22个居群66份材料的DNA。由擎科生物技术有限公司合成UBC加拿大哥伦比亚大学设计的ISSR引物和Collard & Mackill开发的36条SCoT引物[28-29]。2种分子标记的[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]反应体系均为10 μL 2×Taq [url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url] Master MIX Ⅱ(北京天根生物科技有限公司)、引物1 μL、模版DNA 1 μL、ddH2O补齐至总体积20 μL。ISSR标记的[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]扩增步骤为:94 ℃预变性10 min,39个循环下94 ℃变性30 s、48~59 ℃退火1 min、72 ℃延伸1 min,最后再设置72 ℃继续延伸10 min。SCoT标记的[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]扩增步骤为:94 ℃预变性5 min,36个循环下94 ℃变性30 s、52.9~59.7 ℃退火90 s、72 ℃延伸1 min,最后72 ℃继续延伸10 min。 2.2 丹酚酸和丹参酮类成分测定 按照《中国药典》2020年版[20]所规定的提取方法及色谱条件,提取不同居群丹参中的丹参酮Ⅰ、丹参酮ⅡA、隐丹参酮和丹酚酸B,并利用高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法(HPLC)进行含量测定。 2.3 气象指标调查 在中国气象数据网(http://data.cma.cn)上查询极大风速、最低气压、最高气压、最高温度、平均气温、平均最高气温、平均气压、平均水气压、平均2 min风速、平均相对湿度、日降水量≥0.1 mm日数、日照时数、最大风速、最大日降水量和最小相对湿度等15个气象指标。 2.4 土壤理化检测 参照《土壤分析技术规范》(第二版)[30]中土壤样品的采集、处理与贮存,采用五点取样法,收集丹参种植土壤,混合均匀,自然风干,过筛备用。并参照其中方法测定土壤有机质(油浴加热重铬酸钾氧化-容量法)、颗粒组成(比重计法)、阳离子交换量(乙酸钙法)、全N(凯氏蒸馏法)、全P(氢氧化钠熔融—钼锑抗比色法)、全K([url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法)、水解N(碱解扩散法)、有效P(碳酸氢钠法)、速效K(火焰光度计测定法[31])、全量铜、锰、锌、钠、钙、镁、硼、铝(电感耦合等离子体原子发射光谱法)。 2.5 数据处理与分析 利用Excel 2019、SPSS 19.0进行数据的统计和分析,本研究所有数据均保证3个生物重复和3个技术重复。对于扩增产物的电泳结果,有条带的记为“1”,无条带的记为“0”,通过Excel 2019统计扩增位点总数(total number of amplification bits,TB)和多态性位点数(number of polymorphic bits,PB)。采用非加权组算术平均法(UPGMA)进行聚类分析。使用POPGENE 1.32分析得到的存在/不存在数据矩阵,计算等位基因数(number of alleles,Na)、有效等位基因数(effective number of alleles,Ne)、Nei氏基因多样性指数(Nei’s gene diversity index,H)、香农信息指数(Shannon information index,I)、多态性百分比(percentage of polymorphic bits,PPB)等遗传参数。 3 结果与分析 3.1ISSR和SCoT标记多态性分析 本研究从42对ISSR引物中筛选出了14对扩增条带清晰,多态性好、重复性好的引物,用于后续ISSR多样性分析。共扩增出140条条带,其中有133条多态性条带,PPB达到95%,平均每对引物扩增得到10条条带。引物UBC 808、UBC 823、UBC 825、UBC 834扩增的条带数目最多,有12条,多态性条带也是12条,PPB为100%。引物UBC 841扩增得到的条带数目最少为7条,(图1-A,表3)。 利用POPGENE 1.32计算,得到Na、Ne、H和I。其中UBC 811的Ne、H、I各项指数最高,分别为1.68、0.37和0.53。UBC 825的Ne、H、I各项指数最低,分别为1.19、0.14和0.26。Na、Ne、H和I平均值分别为1.95、1.41、0.24和0.37(表3)。 从36对SCoT引物中共筛选出10个扩增条带清晰、重复性好的引物,用于扩增22个?丹参居群(66个样本)的DNA。共扩增出97条条带,其中93条为多态性条带,平均多态性率为95.88%(图1-B,表4)。SCOT 28引物的扩增条带数最低为7条,多态性条带也是7条,PPB为100%。SCOT 3引物的扩增条数最高(14条),多态性率为100%,表明SCoT引物也具有较高的多态性和信息量。SCoT 28的Ne、H、I各项指数最高,分别为1.70、0.40和0.58。SCoT 14的Ne、H、I各项指数最低,分别为1.33、0.19和0.31。Na、Ne、H和I平均值分别为1.96、1.51、0.30和0.45(表4)。 3.2 不同居群丹参遗传多样性分析 结合ISSR和SCoT标记计算不同居群丹参的遗传多样性参数,Na范围1.64~1.79,平均值为1.71,Ne为1.34~1.43,平均值为1.38。H为0.21~0.26,平均值为0.23,I为0.31~0.37,平均值为0.35。其中,山东产区各居群的杂合度较高,遗传多样性较为丰富,四川中江产区杂合度较低,遗传多样性较低,稳定性较强(表5)。 3.3 不同丹参居群间遗传距离、PCA及聚类分析 遗传距离是用来衡量居群之间亲缘关系的重要参数,遗传距离越小,代表居群间的亲缘关系越近。结合ISSR和SCoT标记,计算了居群间的遗传距离,如图2-A所示,方格颜色越蓝代表2个居群间的遗传距离越近,越红则越远。来自四川中江的5个居群(SCZJ-1、SCZJ-2、SCZJ-3、SCZJ-4、SCZJ-5)互相之间表现出较近的遗传距离,而其他居群间的遗传距离较远。PCA分析和UPGMA聚类分析均表明SCZJ-1、SCZJ-2、SCZJ-3、SCZJ-4、SCZJ-5聚到了一类,而山东产区的丹参居群混杂的聚到了河南、陕西产区的类群中(图2-B、C)。总体说明四川中江各居群间的遗传稳定性较强,亲缘关系较近,而山东各居群的遗传变异性较大,亲缘关系混杂。 3.4 不同居群丹参有效成分含量测定 测定了不同产区丹参中丹酚酸B、隐丹参酮、丹参酮Ⅰ、丹参酮ⅡA和总丹参酮的含量。色谱图见图3。各产地丹参的丹酚酸B含量均达到《中国药典》2020年版要求,其中,四川中江(SCZJ)的丹酚酸B含量远高于药典规定的3%,并且显著高于其他产区栽培丹参。陕西野生丹参(SXZA-Y、SXSY-Y)也具有较高的丹酚酸B含量,具体结果见图4。除了山西曲沃(SXQW)丹参酮总量未达到《中国药典》要求外,其他产地均达到《中国药典》的0.25%。此外,2个陕西野生丹参(SXZA-Y、SXSY-Y)的总丹参酮含量均未达到《中国药典》要求,且明显低于各产区栽培丹参。 山东蒙阴(SDMY)的隐丹参酮、丹参酮Ⅰ以及总丹参酮含量均显著高于其他产区,并且,SDMY和山东济南(SDJN)的丹参酮ⅡA含量显著高于其他产区。此外,SCZJ、山东临朐(SDLQ)、山东新泰(SDXT)和河南伊川(HNYC)等产区也具有较高的丹参酮ⅡA含量。总体而言,SCZJ富含丹酚酸B,山东产区丹参的丹参酮含量普遍较高,而SXQW的丹参酮类化合物和丹酚酸B均显著低于其他产区。 3.5 丹参产地气候资料收集与分析 丹参各产地间的多个气象因子均有明显差异,其中,平均相对湿度在51.02%~80.91%,日降水量≥0.1 mm的天数在66~123 d,这2个气候因子均以四川中江最高,陕西商州次之,山西曲沃最低。最大日降水量32.0~151.8 mm,年日照时数在1 084.4~2 363.4 h,其中,四川中江和陕西商州的日照时数明显低于其他几个产地。平均气温在13.37~17.77 ℃,陕西商州最低,四川中江最高。平均最高气温(19.68~22.33 ℃)也是四川中江为最高,陕西商州为最低。山东产区最高气压、最低气压、平均气压、日照时数均高于其他产区,但其日降水量≥0.1 mm日数低于其他产区。山西曲沃产区的降水量最少,相对湿度最低(表6)。 3.6 丹参种植土壤理化性质分析 11个不同的产地中有6个产地为壤质黏土,2个产地为砂质壤土,2个产地为黏壤土,1个产地为砂质黏壤土。丹参种植土壤多为壤质黏土,没有过砂和过黏的土壤(表7)。进一步对不同产地丹参种植土壤的pH、有机质含量、阳离子交换量进行测定,结果显示SXQW丹参种植土壤pH最高(8.37),SDMY丹参种植土壤pH最小(6.75),不同产区土壤pH值介于6.75~8.37栽培产区丹参种植土壤pH值呈中性和弱碱性,由此可见,丹参在中性和微碱性的土壤中都可生长(图5-A)。丹参种植土壤中有机质含量以SDXT最高,为28.17 g/kg;以SXZA-Y最低,为7.15 g/kg,除了SDMY和SXZA-Y偏低外,有机质含量大多为10~20 g/kg(图5-B)。土壤阳离子交换量是衡量土壤肥力的指标和合理施肥的重要依据,本次研究结果表明不同采集地丹参种植土壤阳离子交换量均有显著性差异(P<0.05)。其中SXSY-Y土壤阳离子交换量最高,为20.482 cmol(+)/kg。除SDXT和SDPY 2个产地含量较低外,其他几个产地丹参种植土壤阳离子交换量均在10~20 cmol(+)/kg(图5-C)。 3.7 不同产地丹参土壤中矿质元素分析 通过对丹参种植土壤速效N、P、K的研究发现,不同产地丹参种植土壤碱解N含量差别较大,含量在3.80~66.85 mg/kg,其中,SXQW土壤碱解N含量最低(3.80 mg/kg),SCZJ和SDMY 2个产地土壤碱解N含量较其他产地丰富。土壤速效P质量分数处于27.61~63.29 mg/kg,11份土壤样品速效P含量均较丰富。土壤速效K研究结果表明,SXQW土壤速效K量极高,达到420.95 mg/kg。不同产地全N量在1.00~4.97 g/kg不等,全P量在0.19~0.67 g/kg,全K量在9.27~25.46 g/kg(表8)。进一步对不同采集地丹参种植土壤中的微量元素进行测定,8种无机元素中Ca的含量最高,Cu的含量最低。各产地中Na、Ca、B和Mg元素的变化范围很大,这不仅与土壤的理化性质有关,而且与植物自生营养的吸收以及代谢产物的合成有关。道地产区SCZJ产地的丹参种植土壤中Al、Mn、Ca、Mg等无机元素含量明显低于其他大部分产地,B含量高于其他产地(表9)。 3.8 环境因子与丹参有效成分相关性 丹参药材中的有效成分与气象因子之间呈现出不同程度的相关性,风速、气压等与丹参酮ⅡA、丹参酮Ⅰ、隐丹参酮呈显著(P<0.05)或极显著正相关(P<0.01)。日降水量≥0.1 mm日数与丹参酮Ⅰ含量呈显著负相关(P<0.05)。平均水气压、平均相对湿度、日降水量≥0.1 mm日数与丹酚酸B含量成显著(P<0.05)或极显著(P<0.01)正相关,日照时数与丹酚酸B含量成显著负相关(P<0.05)(图6-A)。同时,将土壤理化指标及矿质元素含量与丹参有效成分进行相关性分析,发现隐丹参酮含量与土壤质地中<0.002 mm粒径含量显著性负相关(P<0.05),丹酚酸B含量与土壤有机质呈显著性负相关(P<0.05)(图6-B)。隐丹参酮含量与丹参种植土壤中的Cu、Mg元素含量呈极显著(P<0.01)正相关,丹酚酸类化合物中的丹酚酸B含量与碱解N(HN)含量呈极显著性正相关(P<0.01),与K、速效K(AK)含量呈显著(P<0.05)或极显著负相关(P<0.01)(图6-C)。 综上所述,风速、气压以及土壤中Cu、Mg元素含量是促进丹参酮类成分积累的主要环境因子,气压、湿度、降水量、以及土壤中碱解N含量主要促进了丹酚酸B含量的积累。同样的,过多的降水,土壤粒径过小也会抑制丹参酮的积累。日照过长、土壤中有机质含量或是钾离子含量过高则阻碍了丹酚酸B的积累。 3.9 遗传因子与环境因子、有效成分之间的相关性 平均水气压与Na、I之间呈显著负相关,平均相对湿度与Na显著负相关,与Ne和I极显著负相关。平均最高气温与H呈显著负相关,日降水量≥0.1 mm日数与Na和H显著负相关,与Ne和I极显著负相关。日照时数与Na、Ne和I极显著正相关,与H显著正相关(图7-A)。pH、阳离子交换量、有机质含量以及土壤粒径含量等指标与遗传因子之间均不具有显著相关性(图7-B)。土壤中的N与H呈显著正相关,而碱解氮(HN)与H呈显著负相关。Al与H显著正相关,Ca与Ne显著正相关,与H极显著正相关(图7-C)。I与丹参酮ⅡA含量显著正相关,丹参酮I与Na呈显著正相关,与Ne、H和I呈极显著正相关,I与隐丹参酮含量显著正相关,而丹酚酸B含量与H和I显著负相关(图7-D)。综上所述,水气压、湿度、气温、降水、日照等气候因子以及土壤中N、Al和Ca影响了丹参的遗传变异。不同居群丹参的遗传多样性越强可以促进丹参酮类成分的积累,而遗传稳定性越强则有助于丹酚酸B含量的积累。 4 讨论 ISSR和SCoT标记由于引物设计具有随机性和通用性的特点,在以往多种药用植物的研究中均表现出高的多态性[32-34]。本研究利用这2种标记对不同居群丹参遗传多样性进行分析,基于PPB、Na、Ne、H、I、Ht、Hs等指标发现ISSR和SCoT都具有丰富的多态性,说明了它们都是鉴别丹参亲缘关系的有力标记。结合ISSR和SCoT标记分析的不同居群丹参之间的遗传距离指数进行聚类分析,四川中江所有居群(SCZJ1~SCZJ5)单独聚到一类,在DNA水平和其他群体产生了较大的差异,是由于四川丹参花发育异常导致不结实,长期采取无性繁殖[35-36]。这种繁殖方式加速了四川丹参的地理隔离进程,阻碍了与其他产区丹参之间的基因交流。而四川丹参表现出的色朱味浓、皮细而肥壮、丹酚酸B含量高等独特的性状,与其在基因型上与其他产区丹参的差异密切相关。但是,长期单一的无性繁殖方式会导致其种性退化,因此,想要促进四川丹参产业的可持续性发展,应加强对四川丹参的品种选育和资源保护。 温春秀等利用AFLP对几个丹参居群的遗传分化情况进行了研究,结果显示山东居群丹参的遗传多样性最丰富[37]。本研究得到的分析结果与其一致,山东产区丹参居群分布在不同聚类组中,并且其遗传距离和地理分布没有直接的相关性,显示山东丹参遗传变异较大,这可能是由于山东丹参栽培主要靠种子繁殖,同时丹参在山东种植区域分布很广,人工选育和引种的手段也是导致其遗传变异大,种质资源混杂的原因之一[38]。所以后续应加强山东丹参种植过程中的种子种苗选育过程,从而来保证其种质的稳定。 药材道地性的形成往往是生态环境与基因型相互作用的结果,不同产地之间的气候类型存在一定差异,或许是造就不同产区丹参遗传变异以及质量差异的重要原因。在本研究中,风速、气压与丹参酮类成分含量呈显著正相关,降水量≥0.1 mm日数与丹参酮I含量呈显著负相关。可能是由于降水较少,植物易受到干旱胁迫,轻度的干旱胁迫能够促进丹参酮类成分的积累[39],且降水量≥0.1 mm日数与Na、Ne、H、I等遗传因子均显著负相关,而这些遗传因子与丹参酮类有效成分呈显著正相关,说明降水过多会制约丹参的遗传多样性,将不利于丹参酮类成分积累。但相对湿度不足的情况下,降水量过低则导致重度干旱,同时也会抑制有效成分的积累,这可能是山西产区有效成分偏低的原因。本研究还发现,水气压、相对湿度和日降水量≥0.1 mm日数与丹酚酸B含量呈显著正相关,日照时数与丹酚酸B含量呈显著负相关。已有研究表明,轻度的水分涝胁迫能显著提高丹酚酸B的含量,降低丹参酮的含量[40]。丹参是喜光植物,一定的日照时数有利于有机物的合成积累,但过长的日照时数则会引起土壤水分的蒸发,抑制丹参根系生长,因此日照时数保证的情况下,较少的日照时数和充足的降水量有利于植物根系的生长,从而导致分布在整个根的丹酚酸B含量的积累[41]。并且,水气压、相对湿度和日降水量≥0.1 mm日数与Na、Ne、H、I等遗传因子呈显著负相关,而这些遗传因子与丹酚酸B含量具有显著负相关关系。说明了这些气候因子可以增强丹参居群的遗传稳定性,从而促进丹酚酸B含量积累。总体而言,降水量、湿度和日照时数是影响丹参遗传变异和有效成分的主要气候因子,这与此前余彦鸽对野生丹参生态因子分析研究的结果相似[31]。其中,降水量介导了丹酚酸B和丹参酮含量积累的分流。因此,后期可根据当地的降水量、湿度和日照时数等条件判断是否适宜丹参种植。 除气候因素外,由于不同的土壤类型中土壤质地及理化性质差异会引起土壤水、热、养分、通透性的不同,从而影响到植物根系水分及养分吸收,最终也会对药用植物的生长发育和产量、质量造成一定影响[42-43]。本研究中,土壤粒径<0.002 mm以后将不利于隐丹参酮的积累。这可能与植物成分在根系的分布类型有一定关系,水溶性成分相对于脂溶性成分的分布在全根中比较均匀,脂溶性丹参酮主要都集中在表皮上,所以更易受到土壤质地的影响。土壤中矿质元素是影响药用植物生长发育及次生代谢物积累的生态因子[44-46],中药材生长所需要的矿质元素主要有N、P、K等10多种[47]。本研究发现,隐丹参酮含量与无机元素Cu和Mg含量呈显著正相关,Cu和Mg是植物所需的微量元素,适量的Cu和Mg积累能促进药用植物中有效成分合成。丹酚酸B含量与碱解N呈显著性正相关,与K、速效K呈显著负相关,碱解N含量与H遗传因子显著负相关,而H与丹酚酸B含量显著负相关,说明碱解N能促进丹参遗
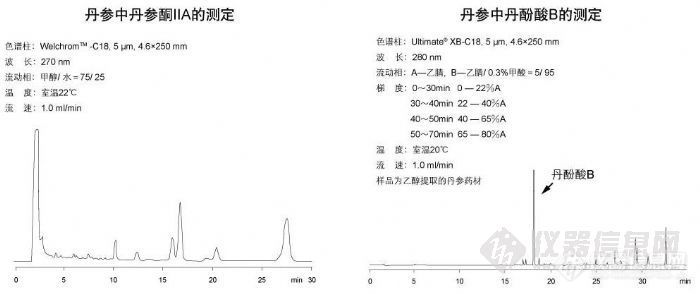
丹参中丹参酮IIA的测定和丹参中丹酚酸B的测定http://ng1.17img.cn/bbsfiles/images/2009/10/200910311036_179302_1896702_3.jpg

[align=center][b][/b][/align][align=center][b][/b][/align][align=center][b]液相色谱泵及色谱柱对丹参酮类化合物分离度影响[/b][/align]1. [b]色谱条件与系统适用性试验[/b] 以十八烷基硅烷键合硅胶为填充剂;以乙腈为流动相A,以0.02% 磷酸溶液为流动相B ,按下表中的规定进行梯度洗脱;柱温为20°C 检测波长为270 nm。理论板数按丹参酮II A峰计算应不低于60000。表1 梯度洗脱程序表[img=,598,240]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041605406100_5206_2613952_3.jpg!w598x240.jpg[/img]2. [b]对照品溶液的制备[/b] 取丹参酮II A对照品适量,精密称定,置棕色量瓶中,加甲醇制成25.2 μg/mL溶液,即得。3. [b]供试品溶液的制备 [/b] 取本品粉末(过三号筛)约0.3g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,密塞,称定重量,超声处理(功率140W,频率42kHz) 30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。4. [b]测定法 [/b] 分别精密吸取对照品溶液与供试品溶液各10 μL, 注入液相色谱仪测定。以丹参酮IIA对照品为参照, 以其相应的峰为S 峰,计算隐丹参酮、丹参酮I的相对保留时间,其相对保留时间应在规定值的± 5 %范围之内。相对保留时间及校正因子见下表:表2 药典丹参酮类化合物相对保留时间及校正因子[align=left][img=,523,200]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041606235938_8876_2613952_3.png!w523x200.jpg[/img][/align]5. [b]结果与讨论[/b]5.1 二元高压泵色谱峰定位 依次将隐丹参酮、丹参酮I、丹参酮IIA对照品溶液在配置有二元高压泵的液相色谱仪上机分析,在依据保留时间对隐丹参酮、丹参酮I、丹参酮IIA进行色谱峰定位。隐丹参酮、丹参酮I、丹参酮IIA色谱图及保留时间见下图。[img=,690,308]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041641467848_7200_2613952_3.jpg!w690x308.jpg[/img] 图1 丹参酮I色谱图[img=,690,308]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041642177002_7482_2613952_3.jpg!w690x308.jpg[/img] 图2 隐丹参酮色谱图[img=,690,308]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041642305674_9673_2613952_3.jpg!w690x308.jpg[/img] 图3 丹参酮IIA色谱图5.2 四元泵色谱峰定位 依次将隐丹参酮、丹参酮I、丹参酮IIA对照品溶液在配置有四元泵的液相色谱仪上机分析,在依据保留时间对隐丹参酮、丹参酮I、丹参酮IIA进行色谱峰定位。隐丹参酮、丹参酮I、丹参酮IIA色谱图及保留时间见下图。[img=,690,219]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041646050499_4164_2613952_3.png!w690x219.jpg[/img] 图4 四元泵隐丹参酮色谱图[img=,690,232]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041646211305_4912_2613952_3.png!w690x232.jpg[/img] 图5 四元泵丹参酮I色谱图[img=,690,220]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041646454301_6774_2613952_3.png!w690x220.jpg[/img] 图6 四元泵丹参酮IIA色谱图5.3不同色谱柱对丹参酮类化合物分离度影响(二元高压泵) 在配置有二元高压泵的液相色谱仪上,分别以XDB C18、SB C18色谱柱分析同一丹参药材供试品溶液,色谱图见图7、图8。[img=,690,308]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041647134017_3086_2613952_3.jpg!w690x308.jpg[/img] 图7 XDB C18色谱柱药材色谱图[img=,690,307]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041647453361_5976_2613952_3.jpg!w690x307.jpg[/img] 图8 SB C18色谱柱丹参药材色谱图5.4 不同泵对丹参酮类化合物分离度影响 分别在在配置有二元高压泵、四元泵的液相色谱仪上,SB C18色谱柱分析同一丹参药材供试品溶液,色谱图见图9、图10。[align=left][img=,690,307]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041649350009_4280_2613952_3.jpg!w690x307.jpg[/img][/align][align=left] 图9 SB C18色谱柱丹参药材色谱图(二元高压泵)[/align][align=left][img=,690,220]https://ng1.17img.cn/bbsfiles/images/2019/07/201907041650042149_4182_2613952_3.png!w690x220.jpg[/img][/align][align=left] 图10 SB C18色谱柱丹参药材色谱图(四元泵)[/align][b]6 讨论[/b]6.1 丹参中丹参酮类化合物含量测定时不同色谱柱、不同类型的泵对隐丹参酮、丹参酮I、丹参酮IIA分离度影响较大。6.2 丹参酮类化合物在同一厂家二元泵的分离度优于四元泵,二元泵仪器上隐丹参酮、丹参酮I分开,隐丹参酮、丹参酮I在四元泵仪器采集色谱图上是一个对称性良好的一个色谱峰,未见分开趋势。6.3 不同类型的C18色谱柱对于丹参酮类化合物分离度也有影响,本实验中二元泵仪器上XDB色谱柱分离丹参酮类化合物效果优于SB色谱柱。 综上,建议测定丹参中丹参酮类化合物时选择合适的仪器、色谱柱,丹参酮类化合物才能更好分离,进而准确定位及含量计算。
骨性关节炎是以软骨细胞去分化、软骨退化和软骨缺损为特征的致残性疾病,目前尚缺乏有效的药物来促进骨性关节炎患者软骨缺损的修复,临床治疗以延缓病情为主[1]。骨性关节炎涉及髌下脂肪垫和滑膜、关节周围肌肉、韧带、软骨下骨,尤其是关节软骨周围的各种组织学病变[2]。关节软骨主要由软骨细胞及其产生的大量细胞外基质组成,软骨细胞负责维持细胞外基质合成代谢和分解代谢之间的平衡,然而炎性细胞因子、异常机械刺激、软骨细胞凋亡和氧化应激等多种因素会破坏软骨细胞生理学和基质转换的平衡,进而导致基质丢失和组织变性,从而导致骨性关节炎的发生[3]。丹参属于传统的活血祛瘀中药,丹参酮ⅡA是丹参中脂溶性成分,具有抗炎、抗氧化、抗血小板聚集、抗肿瘤、雌激素样活性等多种药理作用,临床广泛用于心脑血管疾病、糖尿病、肝病、肿瘤等多种疾病的治疗[4]。丹参酮ⅡA可降低炎症反应、保护软骨组织以防治骨性关节炎。本文综述了丹参酮ⅡA防治骨性关节炎的研究进展,总结其作用机制,为丹参酮ⅡA临床治疗骨性关节炎提供参考。 1 降低炎症反应 1.1 阻止Tol样受体4/髓分化因子88/核因子-κB(TLR4/Myd88/NF-κB)信号通路激活 TLR4/Myd88/NF-κB信号通路通过促进多种炎症因子的表达参与骨性关节炎的炎症反应进程,可造成软骨组织炎症损伤,加快软骨退变进程[5]。张金锋等[6]使用丹参酮ⅡA治疗前交叉韧带切断术建立膝骨性关节炎大鼠模型,结果显示,10、20、50 mg/kg丹参酮ⅡA能显著提高大鼠步态行为和热刺激缩足反应潜伏期,降低机械刺激缩足反应阈值,显著改善大鼠软骨厚度、滑膜厚度和Mankin评分,显著减轻软骨表明粗糙、断裂、溃疡等病理损伤,显著降低外周血清和关节组织中肿瘤坏死因子-α(TNF-α)、白细胞介素(IL)-1β、IL-6、胶原羧基端交联肽(CTX)-I、CTX-II的水平,显著降低NF-κB p65蛋白的表达,表明丹参酮ⅡA可通过阻止TLR4/Myd88/NF-κB信号通路激活以降低骨性关节炎的炎症反应。洪瑛等[7]使用丹参酮ⅡA干预小鼠原代软骨细胞,30、60、90、120、150、180、210、240、270、300、400 μmol/L丹参酮ⅡA呈浓度和时间相关性降低IL-1β引起的原代细胞的增殖抑制率,显著阻止NF-κB p65、TRAF6蛋白和基因的表达,结果证实丹参酮ⅡA通过阻止NF-κB信号通路激活以减轻软骨细胞的炎症损伤。 1.2 抑制磷脂酰肌醇3激酶/蛋白激酶B/核因子-κB(PI3K/Akt/NF-κB)信号通路激活 PI3K/Akt/NF-κB是介导骨性关节炎的重要信号通路,激活后可诱导IL-6、基质金属蛋白酶(MMP)、TNF-α等多种下游炎症因子的分泌,参与骨性关节炎的病理进程,可诱导软骨组织降解,降低软骨的抗应能力[8]。孟如丹等[9]研究使用丹参酮ⅡA干预大鼠原代软骨细胞,发现6.25、12.5、25、50 μmol/L丹参酮ⅡA能促进软骨细胞增殖,12.5、25、50 μmol/L丹参酮ⅡA对IL-1β的干预能促使软骨细胞增殖,还能抑制软骨细胞中前列腺素E2(PGE2)、IL-6、TNF-α、一氧化氮(NO)的分泌,以及MMP-13、环氧化酶-2(COX-2)、诱导型一氧化氮合酶(iNOS)、ADAMTS-5基因和蛋白表达,结果证实丹参酮ⅡA可通过抑制PI3K/Akt/NF-κB的激活以阻止软骨细胞的炎症反应,降低软骨组织的降解,对软骨组织发挥保护作用。 1.3 调节微小RNA(miR)-155/叉头框蛋白O3(FOXO3)轴的表达 miR是一类进化上保守的单链非编码小RNA分子,在转录后水平调控基因表达,miR-155在骨性关节炎软骨细胞中显著上调,参与骨性关节炎的发病机制,可靶向促使FOXO3的3′UTR的表达下调,进而加剧骨性关节炎组织间的炎症反应,促进软骨细胞凋亡[10]。Zhou等[11]使用丹参酮ⅡA干预乙酰半胱氨酸处理的人原代软骨细胞,发现5、10 μmol/L丹参酮IIA能显著降低软骨细胞中IL-1β、IL-6、TNF-α蛋白和基因的表达,显著降低miR-155-5p的表达和提高FOXO3的表达,通过下调caspase-3-9的表达以抑制软骨细胞凋亡,通过miR-155抑制剂反向验证丹参酮ⅡA对miR-155的靶向抑制作用,表明丹参酮ⅡA可靶向调节miR-155/FOXO3轴的表达显著降低骨关节炎的炎症反应。 1.4 上调β-arrestin2的表达 β-arrestin2是NF-κB信号通路的上游因子,过表达能阻止TLR4/NF-κB信号通路激活,继而介导多种炎症因子的分泌,诱导并加剧软骨组织的炎症损伤[12]。张建业等[13]使用IL-1β诱导软骨细胞炎症反应并使用Hulth法建立膝骨性关节炎大鼠模型,结果100 μmol/L丹参酮ⅡA能逆转IL-1β引起的软骨细胞活力下降,降低IL-1β引起的软骨细胞中COX-2、iNOS、PGE2、NO、MMP、p65表达的升高,呈浓度相关性促进β-arrestin2、聚集蛋白聚糖、II型胶原蛋白的表达,经0.5 mg/kg丹参酮ⅡA治疗后,大鼠的软骨骨质变薄、粗糙、软骨细胞排列紊乱的病理获得明显改善,还能降低Mankin评分,结果证实丹参酮ⅡA可通过上调β-arrestin2的表达来降低软骨组织的炎症反应,进而控制骨性关节炎的病情发展。 1.5 抑制炎症因子的表达 炎性细胞因子引发炎症反应,参与骨性关节炎的发生、发展,其中多种促炎细胞因子(IL-1β、TNF-α和iNOS)的水平显著升高,进而诱导软骨细胞凋亡和增加软骨组织降解[14]。Jia等[15]使用前交叉韧带横断术和内侧半月板切除术建立骨性关节炎大鼠模型,使用0.5 mg/kg丹参酮ⅡA进行治疗,结果发现丹参酮ⅡA能有效抑制大鼠软骨降解和软化,降低大鼠的Mankin评分,有助于降低半月板切除引起的滑膜内膜崩解和炎症细胞积累,抑制软骨细胞凋亡,促进基质金属蛋白酶组织抑制因子1(TIMP-1)的表达和降低MMP-13的表达,降低大鼠血清中TNF-α、IL-1β和iNOS的水平,促进软骨细胞中骨形态发生蛋白2(BMP-2)和人转化生长因子β1(TGF-β1)蛋白的表达,证实丹参酮ⅡA可通过降低炎症因子的表达以阻止软骨细胞的降解,用于骨性关节炎的治疗。 2 保护软骨组织 2.1 调节Wnt/β-连环蛋白(Wnt/β-catenin)信号通路表达 Wnt/β-catenin参与关节软骨形成和分化的调节,β-catenin可促使多种降解酶的表达,加快细胞外基质的降解和软骨组织损伤,Wnt的过表达可增加关节内蛋白酶的活性,促进胶原蛋白的分泌和细胞外基质的形成[16]。宋奕等[17]使用丹参酮ⅡA干预大鼠原代软骨细胞,发现6.25、12.5、25、50 μmol/L丹参酮ⅡA可呈浓度相关性提高软骨细胞的II型胶原蛋白和II型胶原的分泌,并降低β-catenin蛋白的表达,表明丹参酮ⅡA通过调节Wnt/β-catenin信号通路以促进软骨细胞II型胶原蛋白的表达,对关节软骨发挥保护作用。 2.2 上调长链非编码RNA(lncRNA)的表达 lncRNA在骨性关节炎中起着重要作用,与富核丰度转录本1(NEAT1)相互作用,影响软骨细胞增殖、迁移和凋亡以及细胞外基质分泌,NEAT1_2在软骨细胞对炎症因子和去分化引起的应激的反应中起着关键作用[18]。Sun将[19]丹参酮IIA用于IL-1β干预兔软骨细胞,发现2 μg/mL丹参酮IIA能提高兔软骨细胞中NEAT1_2的表达,显著提高细胞中SOX9、ACAN mRNA水平和COL II/COL I比率,继而增强软骨细胞表型基因的转录,有效减轻IL-1β和TNF-α诱导的软骨细胞凋亡,阻断细胞应激的加重,与软骨细胞共同培养能促进软骨组织再生,证实丹参酮IIA通过上调lncRNA NEAT1_2有效促进软骨再生,可望成为治疗骨性关节炎的新策略。 2.3 抑制铁死亡 铁死亡是一种细胞死亡形式,由铁依赖性脂质过氧化引发,活性氧(ROS)过度分泌会破坏氧化还原稳态,增加促死亡元素(如Bax、Bid),并降低促生存因子(如Bcl-2)的表达,谷胱甘肽(GSH)耗竭或谷胱甘肽过氧化物酶4(GPX4)失活引起的脂质过氧化是细胞铁死亡的典型特征,铁死亡可加重软骨细胞损伤,加剧骨性关节炎的病情发展[20]。Xu等[21]使用丹参酮IIA干预小鼠软骨细胞系ATDC5,发现40、100 μmol/L丹参酮IIA能显著降低脂多糖诱导的ATDC5细胞凋亡,逆转脂多糖引起的Bax蛋白增加和Bcl-2蛋白降低,降低MMP13、ADAMTS5 mRNA的水平,提高Col II mRNA和蛋白的水平,通过提高ATDC5细胞中GSH、GPX-4的水平,降低ROS水平,缓解脂多糖诱导的炎症反应,降低软骨细胞铁死亡,结果证实丹参酮IIA通过抑制铁死亡来改善软骨细胞凋亡和软骨变性,并可能成为骨性关节炎的潜在治疗剂。 2.4 促进软骨组织形成 关节软骨覆盖了人体滑膜关节的所有关节表面,由细胞外基质和极少数位于该组织内的软骨细胞组成,由于软骨内缺乏血管,极大地限制了关节软骨的自我修复能力,软骨组织工程技术生产的支架是目前临床促进软骨修复的主要治疗手段[22]。Chen等[23]通过冷冻干燥法制备丹参酮IIA递送丝素蛋白支架,通过5、10、20、40 μg/mL丹参酮IIA制作成不同质量浓度的支架,发现10 μg/mL丹参酮IIA组成的支架(SF/T10)促使软骨细胞中COL Ⅱ/COL Ⅰ的表达升高,程度优于其他质量浓度,还能显著促进软骨样细胞外基质的生成和软骨形成,将SF/T10用于裸鼠的皮下区域后发现移植区域均生长出软骨样组织,将SF/T10用于兔软骨缺损修复的实验发现可促使缺损部位完全修复,再生组织与周围软骨相似,结果证实丹参酮IIA递送丝素蛋白支架能促进软骨组织形成。 2.5 阻止软骨细胞去分化 软骨细胞在骨性关节炎病理进程中可发生去分化,失去其软骨生成特征,并显示成纤维细胞样形态,通常从多边形变为纺锤形,软骨细胞去分化程度与骨性关节炎的骨损伤程度呈正相关[24]。Zhang等[25]将100 μg/mL丹参酮IIA与软骨细胞进行体外培养,结果丹参酮IIA能促使软骨细胞早期迅速增殖,促使糖胺聚糖的表达,上调Col II、SOX6 mRNA的表达,基于网络药理学发现丹参酮IIA发挥作用机制的5 020个潜在靶基因,COL2A1、COL10A1、ADAMTS5、MMP13、COMP、GDF5、SOX6 7个枢纽基因是关键靶点,结果证实丹参酮IIA可阻止软骨细胞去分化,可能成为骨性关节炎的候选药物。 3 结语 丹参酮ⅡA可通过阻止TLR4/Myd88/NF-κB信号通路激活,抑制PI3K/Akt/NF-κB信号通路激活,调节miR-155/FOXO3轴的表达,调节Wnt/β-catenin信号通路表达,上调β-arrestin2的表达,上调lncRNA的表达,抑制炎症因子的表达,抑制铁死亡,促进软骨组织形成,阻止软骨细胞去分化等多种途径发挥降低炎症反应和软骨组织保护作用,以防治骨性关节炎。目前丹参酮ⅡA用于骨性关节炎多以基础研究或动物研究为主,在人体的药理作用尚需试验验证,并且丹参酮ⅡA的量效关系、药物安全性还需进一步确认,但是丹参酮ⅡA用于骨性关节炎具有较好前景,值得深入探讨。

10,抽取5个版友);中奖名单:ZHAOGUANGXI(注册ID:ZHAOGUANGXI)yifan1117(注册ID:yifan1117)dahua1981(注册ID:dahua1981)牛一牛(注册ID:v2700892)翠湖园(注册ID:hhx050)http://ng1.17img.cn/bbsfiles/images/2017/02/201702221529_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2017/02/201702221529_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================筋骨痛消丸中丹参酮ⅡA的测定方法:HPLC基质:药品应用编号:102869化合物:丹参酮ⅡA固定相:Diamonsil C18色谱柱/前处理小柱:Diamonsil C18, 150 x 4.6mm样品前处理:对照品溶液的制备:取丹参酮ⅡA对照品适量,精密称定,加甲醇制成每1 ml含10 μg的溶液,即得。 供试品溶液的制备:取装量差异项下的本品,研细,取约0.4 g,精密称定,至具塞锥形瓶中,精密加入甲醇30ml,超声处理45min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。色谱条件:色谱柱:Diamonsil C18,150×4.6 mm,5 μm (Cat#:99901) 流动相:甲醇:水=75:25 流速: 1.0 mL/min 柱温: 30 ℃ 检测器:UV 268 nm 进样量:10 μL文章出处:迪马科技关键字:丹参酮ⅡA,hplc,diamonsil C18,钻石一代,筋骨痛消丸摘要:Diamonsil C18检测筋骨痛消丸中丹参酮ⅡA。谱图:http://www.dikma.com.cn/u/image/2015/03/19/1426742973115325.pnghttp://www.dikma.com.cn/u/image/2015/03/19/1426742977113113.png
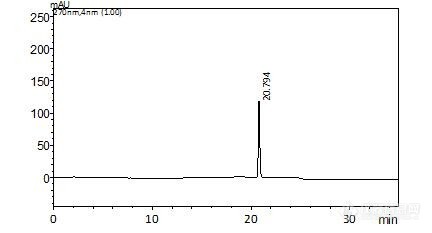
[align=center][b][font=宋体][color=#333333]近期测外样发现丹参对色谱柱的柱效及柱温要求很高,现对实验中注意的问题做一下讨论:[/color][/font][/b][/align][font='Times New Roman', serif]1[/font][font=宋体]材料[/font][font=宋体]丹参药材(送检样);乙腈(色谱级),甲醇、磷酸(分析纯);丹参酮Ⅱ[/font][font='Times New Roman', serif]A[/font][font=宋体]对照品(购自中检院)。[/font][font='Times New Roman', serif]2 [/font][font=宋体]仪器与设备[/font][font=宋体]岛津[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url][/font][font='Times New Roman', serif]LC-20AT[/font][font=宋体]配制[/font][font='Times New Roman', serif]UV/DAD[/font][font=宋体]检测器,安家[/font][font='Times New Roman', serif]Eclipse XDB C18[/font][font=宋体]色谱柱[/font][font='Times New Roman', serif](250mm*4.6μm*5μm)[/font][font=宋体],超声波清洗器。[/font][font='Times New Roman', serif]3 [/font][font=宋体]实验方法[/font][font='Times New Roman', serif]3.1 [/font][font=宋体]色谱条件[/font][font=宋体]流动相(参照中国药典[/font][font='Times New Roman', serif]2020[/font][font=宋体]年第一部):乙腈[/font][font='Times New Roman', serif]-0.02%[/font][font=宋体]磷酸水[/font][font=宋体][color=#333333]为流动相,进行梯度洗脱;检测波长[/color][/font][font='Times New Roman', serif][color=#333333]270nm[/color][/font][font=宋体][color=#333333];柱温:[/color][/font][font='Times New Roman', serif][color=#333333]20 [/color][/font][font=宋体][color=#333333]℃[/color][/font][font=宋体][color=#333333];流速:[/color][/font][font='Times New Roman', serif][color=#333333]1.0mL/min[/color][/font][font=宋体][color=#333333],进样量:[/color][/font][font='Times New Roman', serif][color=#333333]10μL[/color][/font][font=宋体][color=#333333]。[/color][/font][font='Times New Roman', serif][color=#333333]3.2[/color][/font][font=宋体][color=#333333]对照品溶液制备[/color][/font][font=宋体][color=#333333]取丹参酮[/color][/font][font=宋体][color=#333333]Ⅱ[/color][/font][font='Times New Roman', serif][color=#333333]A[/color][/font][font=宋体][color=#333333]对照品适量,精密称定,加甲醇制成每[/color][/font][font='Times New Roman', serif][color=#333333]1mL[/color][/font][font=宋体][color=#333333]含[/color][/font][font='Times New Roman', serif][color=#333333]20 μg[/color][/font][font=宋体][color=#333333]的溶液,即得。色谱图如下:[/color][/font][align=center][img=,432,233]https://ng1.17img.cn/bbsfiles/images/2022/09/202209010920076504_5804_1858223_3.jpg!w432x233.jpg[/img][/align][align=center][/align][font=宋体][/font][align=center][font=宋体][color=#333333]图[/color][/font][font='Times New Roman', serif][color=#333333]1[/color][/font][font=宋体]丹参酮Ⅱ[/font][font='Times New Roman', serif]A[/font][font=宋体][color=#333333]标准品([/color][/font][font='Times New Roman', serif][color=#333333]Eclipse XDB C18 [/color][/font][font=宋体][color=#333333])[/color][/font][/align][font='Times New Roman', serif][color=#333333]3.3 [/color][/font][font=宋体][color=#333333]供试品溶液的制备[/color][/font][font='Times New Roman', serif][color=#333333] [/color][/font][font=宋体][color=#333333](参照中国药典[/color][/font][font='Times New Roman', serif][color=#333333]2020[/color][/font][font=宋体][color=#333333]年版第一部)[/color][/font][font=宋体][color=#333333]供试品溶液的制备[/color][/font][font=宋体][color=#333333]取本品粉末(过三号筛)约[/color][/font][font='Times New Roman', serif][color=#333333]0.3 g[/color][/font][font=宋体][color=#333333],精密称定,置具塞锥形瓶中,精密加入甲醇[/color][/font][font='Times New Roman', serif][color=#333333]50 mL[/color][/font][font=宋体][color=#333333],密塞,称定重量,超声处理[/color][/font][font='Times New Roman', serif][color=#333333]30[/color][/font][font=宋体][color=#333333]分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。测定法[/color][/font][font=宋体][color=#333333]分别精密吸取对照品溶液与供试品溶液各[/color][/font][font='Times New Roman', serif][color=#333333]10[/color][/font][font=宋体][color=#333333]μ[/color][/font][font='Times New Roman', serif][color=#333333]L[/color][/font][font=宋体][color=#333333],注入[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],测定。以丹参酮Ⅱ[/color][/font][font='Times New Roman', serif][color=#333333]A[/color][/font][font=宋体][color=#333333]对照品为参照,以其相应的峰为[/color][/font][font='Times New Roman', serif][color=#333333]S[/color][/font][font=宋体][color=#333333]峰,计算隐丹参酮、丹参酮Ⅰ的相对保留时间[/color][/font][font=宋体][color=#333333]。色谱图如下:[/color][/font][align=center][img=,533,590]https://ng1.17img.cn/bbsfiles/images/2022/09/202209010921297596_689_1858223_3.jpg!w533x590.jpg[/img][/align][align=left][font='Times New Roman', serif]4 [/font][font=宋体]结果与讨论[/font][color=#333333][url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url]使用中关键因素是流动相和色谱柱,根据待测物质的化学性质,选择合适的色谱柱,但是测定丹参的过程中发现柱温对其影响也比较大,使得待测物质不能能够有效分离,从而不能准确定性定量。丹参药材注意的就是柱温一定要在20[font=宋体]±2[/font][font=宋体][color=#333333]℃左右,进样才能达到有效分离。[/color][/font][/color][font=宋体][color=#333333] [/color][/font][/align]
如题,求丹参酮IIA测定的高效液相色谱法
[b]Q:[b][b][b][/b][/b]宁神补心片中丹参酮ⅡA的检测,色谱条件是?[/b]A:色谱柱: Diamonsil C18 250*4.6 mm, 5 μm (Cat#:99903)流动相: 甲醇 -水=78:22流速: 1.0 mL/min柱温: 30 ℃检测器: UV 270 nm进样量: 10 μL===============================================================【活动内容】1、每个工作日上午10:00左右发布一个关于应用数据库的应用问答题,版友根据题目给出自己理解的答案。2、每个工作日下午15:10公布参考答案。【活动奖励】幸运奖:抽奖软件,当天随机抽取3个或5个回答正确的版友ID号(最后一个ID号,截止至下午15:00),每人奖励[color=#ff0000]2钻石币[/color](抽奖人数≤10,抽取3个版友;抽奖人数>10,抽取5个版友);中奖名单:莫名其妙(注册ID:moyueqiu)PAEs(注册ID:v2911392)捌道巴拉巴巴巴(注册ID:v3082413)[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/10/201810261502264899_878_1610895_3.png!w690x388.jpg[/img][img=,690,388]https://ng1.17img.cn/bbsfiles/images/2018/10/201810261502287949_4850_1610895_3.png!w690x388.jpg[/img]积分奖励:所有回答正确的版友奖励[color=#ff0000]10个积分[/color](幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次[/b][align=left][color=#ff0000][b]PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。[/b][/color][/align][align=left][color=#ff0000][b] 下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。[/b][/color][/align][align=center]=======================================================================[/align]方法:HPLC基质:药品应用编号:103658化合物:丹参酮ⅡA色谱柱:[url=http://www.dikma.com.cn/product/details-229.html]Diamonsil C18 5μm 250 x 4.6mm[/url]样品前处理:1.对照品溶液:取丹参酮ⅡA对照品 适量, 精密称定, 加甲醇 制成每 1ml 含 16 μg的溶液,即得。2.供试品溶液:取本品10 片,除去包衣,精密称定,取约1.0g,精密称定,置具塞锥形瓶中,精密加入甲醇25ml,密塞,称定重量,超声处理(功率250W,频率33kHz)30 分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。色谱条件:色谱柱: Diamonsil C18 250*4.6 mm, 5 μm (Cat#:99903)流动相: 甲醇 -水=78:22流速: 1.0 mL/min柱温: 30 ℃检测器: UV 270 nm进样量: 10 μL文章出处:天津应用实验室关键字:宁神补心片、丹参酮ⅡA、HPLC、2015药典、Diamonsil C18摘要:Diamonsil C18检测宁神补心片中丹参酮ⅡA。图谱:[img]http://www.dikma.com.cn/u/image/2015/07/22/1437545772408543.png[/img][img]http://www.dikma.com.cn/u/image/2015/07/22/1437545776938092.png[/img]

问题:精制冠心软胶囊中丹参酮IIA的检测药典要求理论板数按丹参酮ⅡA峰计算应?答案:药典要求理论板数按丹参酮ⅡA峰计算应不低于18000【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币大川之子,纵横四海(注册ID:chuangu120)zgx3025(ID:v2844608)WUYUWUQIU(注册ID:wulin321)http://ng1.17img.cn/bbsfiles/images/2016/01/201601281519_583857_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/01/201601281519_583858_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。======================================================================= 精制冠心软胶囊中丹参酮IIA的检测样品制备 制备方法1. 对照品:取丹参酮ⅡA对照品适量,精密称定,加甲醇制成每1 mL含7 μg的溶液,即得。2. 供试品:取装量差异项下的本品内容物,混匀,取0.3 g,精密称定,精密加入甲醇50 mL,称定重量,超声处理(功率400 W,频率40 kHz)20分钟,轻摇使分散,70 ℃加热回流1小时,取出,趁热摇匀,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。分析条件 色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相A:乙腈 B:0.1%磷酸 梯度流速1.0 mL/min柱温30 ℃检测器UV 270nm进样量10 μL色谱图对照品 http://ng1.17img.cn/bbsfiles/images/2016/01/201601280958_583751_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 22.638 530257 43763 77157.275 0.969 -- *药典要求理论板数按丹参酮ⅡA峰计算应不低于18000供试品http://ng1.17img.cn/bbsfiles/images/2016/01/201601280959_583752_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 22.602 475768 39344 77352.888 0.975 -- *药典要求理论板数按丹参酮ⅡA峰计算应不低于18000本品种同时使用了DiamonsilC18、DiamonsilC18(2)两款色谱柱,在药典规定条件下进行丹参酮IIA的检测,均满足药典要求。

问题:精制冠心片中芍药苷、丹酚酸B、丹参酮ⅡA的检测使用了哪几款液相色谱柱?答案:Platisil ODS 、Diamonsil C18、Leapsil C18 【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币吕梁山(ID:shih20j07)mengzhaocheng(ID:mengzhaocheng)梧桐(ID:mengzhou)http://ng1.17img.cn/bbsfiles/images/2016/01/201601251513_583448_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/01/201601251514_583449_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================精制冠心片中芍药苷、丹酚酸B、丹参酮ⅡA的检测样品制备制备方法1. 对照品:取芍药苷对照品、丹酚酸B对照品、丹参酮ⅡA对照品适量,精密称定,加甲醇制成每1 mL各含芍药苷80 μg、丹酚酸B 0.16 mg、丹参酮ⅡA10 μg的混合溶液,即得。2. 供试品:取本品10片,除去包衣,精密称定,研细,取约0.5 g,精密称定,精密加入75%甲醇25 mL,密塞,称定重量,超声处理(功率400 W,频率40 kHz)40分钟,放冷,再称定重量,用75%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。分析条件色谱柱Platisil ODS 150 x 4.6 mm,5 μm (Cat#:99501)流动相A:乙腈 B:0.1%磷酸溶液 梯度流速1.0 mL/min柱温30 ℃检测器芍药苷、丹酚酸B:UV 230 nm,丹参酮ⅡA:UV 270 nm 进样量5 μL 色谱图对照品http://ng1.17img.cn/bbsfiles/images/2016/01/201601251002_583419_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 12.068 1598880 89096 10350.125 0.958 -- 2 59.100 863860 30575 99529.191 0.971 76.864 *药典要求理论板数按芍药苷峰计算应不低于8000 http://ng1.17img.cn/bbsfiles/images/2016/01/201601251002_583420_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数 N USP拖尾因子 分离度 1 92.337 372136 25387 865104.545 0.974 -- 供试品http://ng1.17img.cn/bbsfiles/images/2016/01/201601251003_583421_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 [a

商品名称:精制冠心软胶囊成分:丹参、川芎、赤勺、红花、降香。功能主治:活血化瘀;用于心血瘀阻之冠心病,心绞痛。http://ng1.17img.cn/bbsfiles/images/2016/11/201611281133_01_1610895_3.jpg样品制备:1、对照品溶液:取芍药苷对照品、丹酚酸B对照品适量,精密称定加 75%甲醇制成每 1ml 各含15 μg的混合溶液, 即得。2、供试品溶液:取装量差异项下的本品适量,研细,取约0.5g,精密称定,精密加入75%甲醇50ml,密塞,称定重量,超声处理(功率400W, 频率40kHz)40分钟,放冷,再称定重量,用75%甲醇补足减失的重量,摇匀,离心,取上清液,即得。色谱条件:色谱柱: Platisil ODS 250*4.6 mm,5 μm(Cat#:99503) 流动相: A:乙腈 B:0.1%磷酸 流速: 1.0 mL/min 柱温: 30 ℃ 检测器: UV 265 nm 进样量: 5 μLhttp://www.dikma.com.cn/u/image/2015/08/03/1438573476130902.pnghttp://www.dikma.com.cn/u/image/2015/08/03/1438573490326137.pnghttp://www.dikma.com.cn/u/image/2015/08/03/1438573503569482.png2015药典要求理论板数按丹参酮IIA峰计算应不低于18000,而Platisil ODS检测的理论塔板数为77157.275,远远高出药典要求。
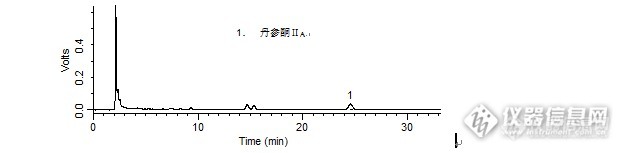
问题:宁神补心片中丹参酮ⅡA的检测:用了迪马哪几款色谱柱?答案:Diamonsil C18(2)、PlatisilODS、Diamonsil C18获奖名单:吕梁山(ID:shih20j07)999youran(ID:999youran)梧桐(ID:mengzhou)http://ng1.17img.cn/bbsfiles/images/2016/01/201601221610_583213_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/01/201601221610_583214_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/01/201601221610_583215_708_3.jpghttp://ng1.17img.cn/bbsfiles/images/2016/01/201601221611_583216_708_3.jpg【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。宁神补心片中丹参酮ⅡA的检测样品制备 制备方法1. 对照品:取丹参酮ⅡA对照品适量,精密称定,加甲醇制成每1 mL含16 μg的溶液,即得。2. 供试品:取本品10片,除去包衣,精密称定,取约1.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,密塞,称定重量,超声处理(功率250 W,频率33 kHz)30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。分析条件 色谱柱Diamonsil C18(2) 250 x 4.6 mm,5 μm (Cat#:99603)流动相甲醇:水=78:22流速1.0 mL/min柱温30 ℃检测器UV 270 nm进样量10 μL色谱图对照品http://ng1.17img.cn/bbsfiles/images/2016/01/201601221051_583177_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 24.663 1158959 40545 16962.300 0.964 -- *药典要求理论板数按丹参酮ⅡA峰计算应不低于2000供试品http://ng1.17img.cn/bbsfiles/images/2016/01/201601221051_583178_708_3.png 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 24.591 1022036 36288 17183.645 0.969 -- *药典要求理论板数按丹参酮ⅡA峰计算应不低于2000本品种同时使用了PlatisilODS、Diamonsil C18两款色谱柱,在药典规定条件下进行丹参酮ⅡA的检测,均满足药典要求。
药典中丹参的含量测定是用的一测多评法,要求如下,我测得丹参酮IIA在14.027,隐丹参酮在10.573,溶剂峰时间在2.123(我是看的第一个出峰的时间,不知道对不对),请问1.相对保留时间应该是10.573/14.027=0.7537606045,还是(14.027-2.123)/(10.573-2.123)或者有其他算法。2.如果是算法二,相对保留时间就不符合药典规定,我进了一针对照品,隐丹参酮对照品出峰时间在10.363,对照品也不在规定的相对保留时间内,我想问相对保留时间不符合药典,但是我通过对照品能确定是该物质,能用药典规定的校正因子计算含量吗?3.丹参酮IIA理论踏板数不低于60000,是指在供试品中的丹参酮IIA,还是指对照品,我的理论踏板数只有49000,这样计算出的含量能算正确吗?4.药典规定的测定温度为20度,流速为1.2,我能改动的范围怎么计算?恳请各位不吝赐教!
[size=14px] [/size] [size=14px]丹参酮是中药丹参的功效物质,丹参酮I(Tanshinone I,Tan I)是丹参酮的一个亚类,具有芳香二萜醌的结构,具有抗菌和抗炎活性。然而,其过高的亲脂性,效价较弱,溶解度低、不稳定等特质,极大地限制了丹参酮I的应用。因此,建立有效的化学演化机制,开发更有效的丹参酮Ⅰ衍生物具有重要意义。哌啶是一种重要的饱和杂环支架,是美国FDA批准的药物中最常用的氮杂环,具有良好的药理特性。该团队将丹参酮Ⅰ和哌啶的骨架杂交,得到了一类新型有效的NLRP3炎症小体抑制剂。2023年2月14日,浙江大学药学院的崔孙良和王毅团队在J Med Chem(IF=7.3)上发表题为“Scaffold Hybrid of the Natural Product Tanshinone I with Piperidine for the Discovery of a Potent NLRP3 Inflammasome Inhibitor”的文章,通过骨架杂交策略得到了一系列具有NLRP3抑制活性的丹参酮Ⅰ-哌啶杂化物,相较于丹参酮Ⅰ,这些化合物在活性、选择性和类药性具有显著改善。其中化合物5j、12a和12d对IL-1β的分泌有较强的抑制作用,在脓毒症小鼠模型中也具有较好的治疗效果。机制研究表明,这些化合物可以阻断ASC的寡聚化,抑制NLRP3炎症小体的激活,且化合物5j可与NLRP3蛋白直接结合,对NLRP3蛋白具有显著亲和力。本研究发现了一种全新结构的丹参酮Ⅰ衍生物,为NLRP3炎性体抑制剂的开发提供了新的思路。[/size] [size=14px] [/size] [size=14px] [/size] [size=14px]1、设计合成了36种Tan Ⅰ-哌啶杂化物前期研究发现Tan Ⅰ中的醌结构是其主要药效团,不宜进行结构修饰。因此研究团队从呋喃结构入手,通过支架杂交的策略,利用哌啶合成出了5个系列 36个Tan Ⅰ的衍生物。为了提升反应活性,在引入哌啶骨架前,研究团队将Tan Ⅰ中的醌并呋喃部分活化为富电子的苯并呋喃。[/size] [size=14px] [/size] [size=14px] [/size] [size=14px]2、体外生物学评价Tan Ⅰ-哌啶杂化物抗炎活性前期研究发现Tan Ⅰ具有抗炎活性,而NLRP3炎症小体作为炎症反应的核心,被证明与多种炎症性疾病相关。因此,作者选用小鼠腹膜巨噬细胞(PMs)开展了一系列体外生物学评价,首先通过MTT法发现36种Tan Ⅰ-哌啶杂化物在4 μΜ浓度无明显细胞毒性,随后发现与Tan-I相比,化合物5d、5j、10c、10f、10g、12a、12d在2 μΜ浓度下更能抑制IL-1β分泌,其中化合物12d与经典的NLRP3抑制剂MCC950活性相当。综合构效关系结果发现引入氢键受体或亲水基团可提升抑制活性(5j、12a、12d),于是作者选用化合物5j、12a、12d作为进一步的研究对象。[/size] [size=14px] [/size] [size=14px] [/size] [size=14px]3、化合物5j、12a和12d阻断NLRP3炎症小体激活,是广谱抑制剂NLRP3炎症小体通路包含准备和激活两个阶段,准备阶段pro-IL-1β和pro-caspase-1的表达升高,而激活阶段IL-1β和caspase-1分泌增加。作者发现化合物5j、12a、12d可抑制IL-1β和caspase-1的分泌,而对pro-IL-1β和pro-caspase-1的表达没有显著影响,表明它们通过阻断激活阶段而不是准备阶段来抑制NLRP3炎症小体活化。此外,5j、12a、12d也可以抑制尿酸钠晶体(MSU)、尼日利亚菌素(Nig)刺激的NLRP3炎症小体激活,表明5j、12a和12d是针对NLRP3炎症小体激活的广谱抑制剂。[/size] [size=14px] [/size] [size=14px] [/size] [size=14px]4、Tan Ⅰ-哌啶杂化物5j/12a/12d可抑制ASC寡聚化,5j可直接结合NLRP3蛋白ASC寡聚化可促进caspase-1的活化,是NLRP3炎症小体活化的标志之一。作者进一步研究化合物5j、12a、12d抑制NLRP3炎症小体的作用机制,通过免疫荧光实验发现在添加化合物5j、12a、12d和阳性药MCC950时,ASC寡聚化形成的斑点显著减少,表明它们均可抑制ASC寡聚化。接着利用表面等离子体共振分析(SPR)和细胞热位移测定(CETSA)实验证明化合物5j和NLRP3存在直接互作。[/size] [size=14px] [/size] [size=14px]5、Tan Ⅰ-哌啶杂化物在脓毒症小鼠模型的体内抗炎评价接着作者对Tan Ⅰ-哌啶杂化物5j、12a、12d进行了成药性评价,发现它们相较于Tan Ⅰ有极大的改善。进一步开展体内抗炎效果评价,发现在LPS诱导的炎症性脓毒症小鼠模型中,化合物5j、12a和12d预处理可以显著降低IL-1β的释放,显著改善肺组织病理损伤,如肺泡壁增厚明显减轻,粒细胞数量和炎症浸润显著减少。[/size] [size=14px] [/size] [size=14px] [/size] [size=14px]总结该研究通过骨架杂交策略得到了一系列具有NLRP3抑制活性的丹参酮Ⅰ-哌啶杂化物,与原型丹参酮Ⅰ相比,这些新的结构化合物在效力、选择性和类药性方面有显著改善,其中化合物5j、12a和12d对IL-1β的分泌具有高抑制活性。机制研究表明,这些化合物可以阻断ASC的寡聚化,抑制NLRP3炎症小体的激活,同时SPR和CETSA显示化合物5j可与NLRP3蛋白直接结合。体内研究表明它们对脓毒症小鼠模型具有较好的治疗效果,研究开发出了一种丹参酮I的简单结构修饰策略并提供了一类新的有效的NLRP3炎症小体抑制剂。[/size] [size=14px] [/size] [size=14px] [/size] [size=14px] [/size] [size=14px] [/size] [size=14px] [/size] [size=14px] [/size] [size=14px] [/size] [size=14px] [/size]
丹参中药材第二增补本丹参酮类含量测定色谱图,求图谱,还有保留时间对不上怎么处理,求计算方法
[font=宋体]丹参是鼠尾草属植物丹参[/font][i]Salvia miltiorrhiza [/i]Bunge[font=宋体]的根以及根茎经过干燥炮制后而成。别名郄蝉草、奔马草等,最早被[color=var(--weui-LINK)]《神农本草经》[i][/i][/color]列为上品[/font][font=宋体],丹参整体作用平和,具有活血祛瘀而不伤正气之效[/font][font=宋体],[/font][font=宋体]常有“一味丹参饮,功同四物汤”之说。中医认为,丹参具有活血祛瘀、通经止痛等功效,适用于血瘀诸证。高血压慢性病程导致的肾损害,病机虚实夹杂,病势缓慢而持久,正如古人云:“久病必瘀”,故高血压肾病以肾络血瘀为基本病机,贯穿疾病始终,临床治疗上多以活血通络为主要治法[/font][font=宋体]。《神农本草经》中认为:“(丹参)破癥除瘕,止顿满,益气”。《日华子本草》记载丹参能“通利关脉”“破宿血,补新生血”。[color=var(--weui-LINK)]《本草正义》[i][/i][/color]中认为:“《本经》所谓益气,《名医别录》所谓养血,皆言其积滞既去,而正气自伸之意,亦以通为补耳。”故丹参古往今来被广泛应用于肾络血瘀为主要病机的各种肾系病证。[/font][font=宋体]现代研究发现,丹参具有抗氧化应激、抗炎、抗肿瘤、抗纤维化、抗动脉粥样硬化、降血压、调节血脂等功效,广泛应用于心脑血管疾病、癌症、肾脏疾病以及肝脏疾病中[/font][font=宋体]。 随着现代药理研究的不断深入,提取出的丹参的主要化学成分为二萜类、三萜类、酚酸类、黄酮类以及含氮类化合物、内酯类化合物、多糖等共百余种物质,其中活性成分主要以二萜类与酚酸类化合物为主。二萜类主要包括丹参酮[/font][color=black]I[/color][font=宋体]、丹参醇[/font]A[font=宋体]、丹参酮[/font]II[sub]A[/sub][font=宋体]、丹参酮[/font]II[sub]B[/sub][font=宋体]等含有醌类结构母核及二萜类结构特征的化合物。三萜类以齐墩果酸和熊果酸的衍生物居多。酚酸类成分有以丹参素([/font]danshensu[font=宋体],[/font]DSS[font=宋体])、丹酚酸[/font]A[font=宋体]([/font]salvianolic acid A[font=宋体],[/font]Sal A[font=宋体])、丹酚酸[/font]B[font=宋体]([/font]salvianolic acid B[font=宋体],[/font]Sal B[font=宋体])、原儿茶醛([/font]protocatechuic aldehyde[font=宋体],[/font]PAL[font=宋体])等为主。其中丹参酮[/font]II[sub]A[/sub][font=宋体]、丹参多酚酸和丹参素是保护肾功能的主要成分。通过以丹参为主要成分的中药组方(如大黄丹参汤)、丹参提取液(如丹参注射液)及生物活性成分的临床和基础实验证实,丹参能够通过抑制氧化应激、抗炎、抗纤维化及对血压调节等作用,广泛应用于抑制肾脏纤维化中,同时对包括高血压肾病和糖尿病肾病在内的慢性肾脏病具有较好的治疗作用。[/font]

[align=center][img=,600,254]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201412140213_28_932_3.jpg!w690x293.jpg[/img][/align]近期有不少客户来向我们反馈,在按照药典条件进行丹参中丹参酮类含量测定的过程中,分离度经常达不到要求。月旭科技今天就通过对丹参的测定,一起来寻找分离度达不到要求的原因,并且解决它![b]中国药典的色谱条件:[/b]色谱柱:月旭Ultimate Plus-C18,4.6×250mm,5μm。流动相:[table=378][tr][td=1,1,88]时间min[/td][td=1,1,178]A:0.02%磷酸溶液(%)[/td][td=1,1,112]B:乙腈(%)[/td][/tr][tr][td=1,1,88]0[/td][td=1,1,178]39[/td][td=1,1,112]61[/td][/tr][tr][td=1,1,88]6[/td][td=1,1,178]39[/td][td=1,1,112]61[/td][/tr][tr][td=1,1,88]20[/td][td=1,1,178]10[/td][td=1,1,112]90[/td][/tr][tr][td=1,1,88]20.5[/td][td=1,1,178]39[/td][td=1,1,112]61[/td][/tr][tr][td=1,1,88]25[/td][td=1,1,178]39[/td][td=1,1,112]61[/td][/tr][/table]检测波长:270nm;柱温:20℃;流速:1.0mL/min;进样量:10μL。在与客户交流的过程中发现,客户的所有测定参数都一样,只有柱温有所区别,客户使用的柱温是35℃。那么问题究竟是不是出在了柱温上呢?我们今天就用35℃以及20℃两种柱温进行测试,来一探问题究竟![align=center][b]柱温20℃测试效果[/b][/align][align=center][img=,600,255]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201413018211_3604_932_3.png!w690x294.jpg[/img][/align][align=center][color=#333333]丹参酮IIA对照溶液[/color][/align][align=center][img=,600,48]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201413055825_8536_932_3.png!w690x56.jpg[/img][/align][align=center][img=,600,260]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201413084428_255_932_3.png!w690x300.jpg[/img][/align][align=center][color=#333333]供试品溶液[/color][/align][align=center][img=,600,92]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201413111660_9521_932_3.png!w690x106.jpg[/img][/align][align=center][b][/b][/align][align=center][b]柱温35℃测试效果[/b][/align][align=center][img=,600,260]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201413140383_8150_932_3.png!w690x300.jpg[/img][/align][align=center][img=,600,61]https://ng1.17img.cn/bbsfiles/images/2019/09/201909201413170926_4920_932_3.png!w690x71.jpg[/img][/align][align=center][/align]怎么样?!是不是发现目标物合并掉了,并没有分开呢?所以我们得到的结论就是:在按照药典条件进丹参中丹参酮类含量测定的过程中,影响分离度的主要因素是柱温。在按照药典中要求的20℃进行测试时,分离度就可以达到要求。如果您在日常的实验中也会遇到类似的问题,包括色谱柱的使用问题,色谱柱的筛选,项目优化等等一系列的问题,均可以联系我们!我们将全心全意解决您的问题![align=center][color=#f96e57][b]垂询热线[/b][/color][/align][align=center][color=#f96e57][b]400-810-6969[/b][/color][/align][color=#f96e57][b][/b][/color]
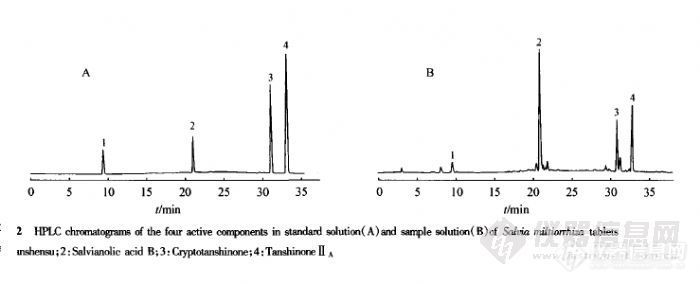
【作者】 孙棣; 刘文英; 梁彩;【Author】 SUN Di,LIU Wen-ying,LIANG Cai Department of Pharmaceutical Analysis,China Pharmaceutical University,Nanjing 210009,China【机构】 中国药科大学药物分析教研室; 中国药科大学药物分析教研室 南京210009; 南京210009;【摘要】 目的:建立一种快速准确同时测定丹参片中脂溶性及水溶性有效成分的方法。方法:建立PR-HPLC法,以甲醇-0.5%甲酸水溶液为流动相进行梯度洗脱,丹参素、丹酚酸B、隐丹参酮、丹参酮ⅡA在Diamonsil C18(250mm×4.6mmID,5μm)柱上得到完全分离。结果:4种物质线性良好,回收率在96.63%~100.3%之间且RSD小于2%。结论:该法能在35min 测定丹参片中脂溶性及水溶性有效成分。http://ng1.17img.cn/bbsfiles/images/2012/07/201207181219_378454_1761902_3.jpg
中国中医科学院首席研究员黄璐琦与中国科学院大连化学物理研究所赵宗保研究员联手,在中药活性成分合成生物学研究方面取得重要进展,所取得的成果证实了中药药用活性成分单一化合物异源生产的可行性,具有重要科学意义和应用价值,相关论文近期发表在国际顶级化学杂志《美国化学会志》上。丹参酮类化合物是丹参中一类松香烷型去甲二萜醌类化合物的活性成分,是丹参治疗心脑血管疾病、感染性疾病、抗肿瘤和糖尿病等的物质基础。这类活性成分目前主要通过从丹参根茎中提取得到,产量低,需要消耗大量药材。由于提取物成分复杂,不利于阐明药效机制和进行新药研发。
丹参总酮上硅胶柱分得色带,继续用硅胶薄层板分离,经过层层分离(约有5-6次),应该算是成分比较单一了,可继续分离每次都会有一条像杂质沉积似的色带在下方,请问为什么?而且经层层分离的认为比较单一的成分上MS检测总离子流图仍有许多许多的峰.我快疯了.

10,抽取5个版友);中奖名单:玲儿响叮当(注册ID:jshbhh)zengzhengce163(注册ID:zengzhengce163)dahua1981(注册ID:dahua1981)mengzhaocheng(注册ID:mengzhaocheng)捌道巴拉巴巴巴(注册ID:v3082413)http://ng1.17img.cn/bbsfiles/images/2017/01/201701201542_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2017/01/201701201542_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================复方丹参软胶囊质量标准的研究方法:HPLC基质:药品应用编号:102722化合物:丹参酮亚ⅡA固定相:Diamonsil C18色谱柱/前处理小柱:Diamonsil C18, 250 x 4.6mm色谱条件:色谱柱:Diamonsil C18 250 mm× 4.6 mm, 5μm(Cat#:99903) 流动相: 甲醇-水(73 : 2 7 ) 流速: 1.5 mL/min 柱温: 30℃ 进样量: 10 μL 检测器: UV 270 nm文章出处:中国药品标准 2002,3(6):365-368关键字:复方丹参软胶囊, 丹参, 三七, 冰片, 质量标准, 丹参酮亚ⅡA, Diamonsil C18, 钻石一代, 高效液相色谱法, HPLC谱图:摘要:目的:改进复方丹参软胶囊质量标准。方法:采用TLC鉴别处方中丹参、三七;采用RP-HPLC法测定复方丹参软胶囊中丹参酮ⅡA的含量,色谱条件:Diamonsil C18;流动相:甲醇-水(73:27);流速:1.5ml/min;检测波长:270nm。 结果:含量测定线性范围8~80μg/ml,r=0.9999。加样回收率99.60%,RSD=1.10%。结论:建立了专属性较强的薄层色谱鉴别并解决了辅料(PEG)对薄层展开的干扰;采用高效液相色谱法测定复方丹参软胶囊中丹参酮ⅡA的含量,方法简便,准确,灵敏度高,重现性好,其他组分对测定无干扰,可用于该制剂的质量控制。http://www.dikma.com.cn/Public/Uploads/images/91-9.JPG
1. 丹参煮田鸡【组方】 丹参15克,田鸡250克,调味品适量。 【制法】 将诸药择净,将田鸡去皮洗净,放入药罐中,加清水适量与丹参同时浸泡片刻,煮熟后调味,饮汤食田鸡。每日1剂,10~15日为1个疗程,连续1~2个疗程。 【功用】 活血化瘀,理气和胃。适用于上腹部刺痛或痛如刀割,固定不移而拒按,疼痛剧烈时可见肢凉,汗出,痛彻胸背,或见反复吐血,便黑,舌质黯紫或有瘀斑点,脉弦或细涩。 2. 山丹桃仁粥【组方】 丹参15克,山楂30克,桃仁6克,大米50克。 【制法】 将丹参择净,放入药罐中,加清水适量,浸泡片刻,煎煮15~20分钟,去渣取汁,再放山楂、桃仁及大米,加清水适量,武火煮沸,文火熬成粥即成。每日1剂,7~10日为1个疗程,连续2~3个疗程。 【功用】 活血化瘀,通络止痛。适用于气滞血瘀型颈椎病。 3. 丹参红枣粥【组方】 丹参30克,糯米100克,大枣30克,红糖20克。 【制法】 将丹参、大枣洗净,放入药罐中,加清水适量,浸泡片刻,煮沸一3. 丹参红枣粥【组方】 丹参30克,糯米100克,大枣30克,红糖20克。 【制法】 将丹参、大枣洗净,放入药罐中,加清水适量,浸泡片刻,煮沸一刻钟,去渣取汁与糯米一同煮粥,待熟后调入红糖后食用。每日1剂,每日2次分食,7~10日为1个疗程,连续2~3个疗程。 【功用】 理气行滞,活血化瘀。适用于风湿性心脏病气滞血瘀,症见面色晦黯或两颧紫红,唇甲青灰,头晕乏力,心悸怔忡,咳嗽甚则咯血,胸闷气喘,或见心痛,胁下痞块,肢体浮肿,舌质紫黯,或有瘀点,脉细数。 4. 丹参牛蛙汤【组方】 丹参10克,牛蛙200克,调味品适量。 【制法】 将诸药择净,将牛蛙去皮、内脏,洗净,与丹参一同放入药罐中,加清水适量,浸泡片刻,煮汤,调味食用。每日1剂,7~10日为1个疗程,连续2~3个疗程。 【功用】 疏肝健脾,活血化瘀。适用于病毒性肝炎所致的气滞血瘀型,症见胁肋胀痛,面色晦黯,食欲缺乏,脘腹胀满,嗳气,肝脾大,舌质黯淡或有瘀斑,苔薄,脉弦涩等。 5. 猪心丹参山楂汤【组方】 丹参20克,山楂25克,猪心1个。 【制法】 将诸药择净,猪心洗净切片,同丹参、山楂共同放入沙锅内,加清水适量,浸泡片刻,小火炖至猪心熟烂离火。吃肉喝汤,每日1剂,7~10日为1个疗程,连续2~3个疗程。 【功用】 养血安神宁心。适用于血虚心悸,乏力,怔忡,自汗,失眠等症。对防治动脉粥样硬化、心绞痛和血管栓死有很好效果。 6. 黄豆炖猪骨【组方】 紫丹参15克,猪长干骨250克,黄豆50克,调味品适量。 【制法】 将诸药择净。猪长干骨洗净,剁段,与黄豆、紫丹参一起放入沙锅中,加清水适量,浸泡片刻,炖煮半小时,加入调味品,再煮一、二沸即可食用。每日1剂,7~10日为1个疗程,连续2~3个疗程。 【功用】 补骨生髓,活血止痛。适用于骨折恢复期。 7. 川芎丹参蟹骨酒【组方】 丹参30克,川芎20克,红花10克,蟹骨30克,白酒1 000毫升。 【制法】 将诸药择净。蟹骨洗净晒干,与丹参、川芎、红花一起放于酒瓶内,密封浸泡半个月,即可服用。每次服50毫升,每日1次,7~10日为1个疗程,连续1~2个疗程。 【功用】 活血消肿,化瘀止痛,续筋接骨。适用于骨折初期,血瘀疼痛,肿胀等症。 8. 丹参灵芝酒【组方】 丹参、三七、茯苓、灵芝各30克,冬虫夏草10克,白酒2 000毫升。 【制法】 将诸药择净,同放入白酒瓶中,密封浸泡1周后饮用。每日2次,每次30毫升,7~10日为1个疗程,连续2~3个疗程。 【功用】 补虚弱,益精神。适用于神经衰弱,失眠头昏,冠心病等症。 9. 丹参鲫鱼汤【组方】 丹参、灵芝、墨旱莲、太子参、黄芪、白术各15克,女贞子18克,白花蛇舌草20克,鲫鱼1条,食盐适量。 【制法】 将诸药择净,放入药罐中,加清水适量,浸泡片刻,煎煮20分钟,去渣取汁。将鲫鱼去磷、杂,洗净,切块,入药汁中煮熟,加食盐调味服食,每日1剂,7~10日为1个疗程,连续2~3个疗程。[size=16
[b][size=15px][color=#595959]丹参酮IIA[/color][/size][/b][size=15px][color=#595959] (TIIA)[/color][/size][size=15px][color=#595959]是中药丹参的主要脂溶性活性成分,具有延缓[/color][/size][b][size=15px][color=#595959]动脉粥样硬化[/color][/size][/b][size=15px][color=#595959](AS)[/color][/size][size=15px][color=#595959]的作用。[/color][/size][size=15px][color=#595959]TIIA还可以通过发挥抗炎和抗氧化作用来治疗帕金森病等神经系统疾病。[/color][/size][size=15px][color=#595959]然而,目前尚不清楚TIIA是否[/color][/size][size=15px][color=#595959]可以通过调节[/color][/size][b][size=15px][color=#595959]胞葬作用(e[/color][/size][size=15px][color=#595959]fferocytosis)[/color][/size][/b][size=15px][color=#595959]从而改善动脉粥样硬化。[/color][/size] [align=center] [/align] [size=15px][color=#595959][/color][/size][size=15px][color=#595959]该研究旨在[b]确定TIIA是否可以通过增强胞葬作用来减少脂质积累和治疗AS[/b]。[/color][/size] [size=15px][color=#595959]首先,对LDLR敲除(LDLR-/-)小鼠进行为期24周的体内实验,分别采用组织病理学染色、[/color][/size][size=15px][color=#595959]免疫[/color][/size][size=15px][color=#595959]荧光和Western blot实验从疗效和机制两部分进行验证;此外,利用细胞在体外再次验证。具体实验设计方案如下:在体内,以西方饮食(高脂肪饮食)喂养12周的LDLR-/-小鼠为AS模型,以正常饮食喂养的LDLR-/-小鼠为空白对照组。TIIA组和阳性对照组(阿托伐他汀,ATO)分别通过腹腔注射(15 mg/kg/d)和灌胃(1.3 mg/kg/d)干预12周。体外分别用ox-LDL (50 ug/mL)或ox-LDL (50 ug/mL) + TIIA (20 uM/L或40 uM/L)培养RAW264.7细胞。[/color][/size] [size=15px][color=#595959]采用Masson染色和油红O染色分别评价[/color][/size][size=15px][color=#595959]主动脉[/color][/size][size=15px][color=#595959]斑块和RAW264.7细胞泡沫细胞形成的病理变化。采用生化方法检测小鼠血脂水平。采用免疫荧光法检测斑块中凋亡细胞和胞葬作用相关信号的表达。采用RT-q[url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url]和Western blot方法观察小鼠主动脉和RAW264.7细胞中胞葬作用相关分子的变化趋势。还使用中性红法评估RAW264.7细胞的吞噬能力。[/color][/size] [align=center] [/align] [size=15px][color=#595959]与模型组比较,TIIA降低了血清TC、TG、LDL-C水平(p 0.01),减少了小鼠主动脉富含脂质斑块的相对管腔面积(p 0.01),增强了小鼠主动脉斑块的稳定性(p 0.01),减少了ox-LDL诱导的RAW264.7细胞脂质堆积(p 0.01),上调了ox-LDL诱导的RAW264.7细胞的胞葬作用相关分子表达,提高了胞葬作用率。[/color][/size] [align=center] [/align] [size=15px][color=#595959]TIIA可能[b]通过增强巨噬细胞的胞葬作用功能来减少脂质积累[/b],从而治疗AS。继续深入研究TIIA使巨噬细胞在AS中保持[b]强吞噬和[/b][/color][/size][b][size=15px][color=#595959]消化[/color][/size][size=15px][color=#595959]吸收[/color][/size][/b][size=15px][color=#595959]的具体机制,可能会推动TIIA作为巨噬细胞胞浆作用的靶向治疗剂的进展。[/color][/size]
[align=left][font=Times New Roman][color=#f10b00][size=3]维权声明:本文为qinjianping原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现的,均属侵权违法行为,我们将追究法律责任。[/size][/color][b] HPLC[/b][/font][b][font=宋体]法同时测定益心舒片中五味子醇甲、五味子酯甲、五味子甲素、五味子乙素和丹参酮[/font][font=宋体]Ⅱ[/font][font=Times New Roman]A[/font][font=宋体]的含量[/font][/b][/align][size=3][font=Times New Roman] [/font][/size][size=3][b][font=宋体]摘要:[/font][font=Times New Roman] [/font][font=宋体]目的[/font][font=Times New Roman] [/font][/b][font=Times New Roman][/font][font=宋体]建立[/font][font=Times New Roman]HPLC[/font][color=black][font=宋体]法同时测定益心舒[/font][/color][font=宋体]片中五味子醇甲、五味子酯甲、五味子甲素、五味子乙素和丹参酮Ⅱ[/font][font=Times New Roman]A[/font][font=宋体]的含量。[b][color=black]方法[/color][/b][/font][b][color=black][font=Times New Roman] [/font][/color][/b][color=black][font=宋体]采用[/font][/color][font=Times New Roman][color=black]Phenomenex Kinetex [/color]C[sub]18[/sub][/font][font=宋体]柱,以[/font][font=宋体]乙腈-水[color=black]梯度洗脱[/color][/font][color=black][font=宋体],[/font][/color][font=宋体]流速[/font][font=Times New Roman]1ml/min[/font][font=宋体],柱温[/font][font=Times New Roman]30[/font][font=宋体]℃[/font][font=宋体],检测波长[/font][font=宋体]250nm[/font][font=宋体]。[/font][b][font=宋体]结果[/font][font=Times New Roman] [/font][/b][font=宋体]五味子醇甲在[/font][font=宋体]0.2156[/font][font=宋体]~2.1560μg(r=0.9999),五味子酯甲在[/font][color=black][font=宋体]0.0650[/font][/color][color=black][font=宋体]~0.6500[/font][/color][font=宋体]μg(r=0.9999),五味子甲素在[/font][color=black][font=宋体]0.0346[/font][/color][color=black][font=宋体]~0.3460[/font][/color][font=宋体]μg(r=0.9999),五味子乙素在[/font][color=black][font=宋体]0.0692[/font][/color][color=black][font=宋体]~0.6920[/font][/color][font=宋体]μg(r=0.9999),[/font][font=宋体]丹参酮Ⅱ[/font][font=Times New Roman]A[/font][font=宋体]在[/font][color=black][font=宋体]0.0240[/font][/color][color=black][font=宋体]~0.2400[/font][/color][font=宋体]μg(r=0.9999)[/font][font=宋体]范围内呈良好的线性关系,[color=black]平均回收率[/color]五味子醇甲为[/font][font=宋体]97.92[/font][font=宋体]%,[/font][font=Times New Roman]RSD[/font][font=宋体]为[/font][font=宋体]2.34%[/font][font=宋体](n=6)[/font][font=宋体];五味子[/font][font=宋体]酯[/font][font=宋体]甲为[/font][font=宋体]100.28[/font][font=宋体]%,[/font][font=Times New Roman]RSD[/font][font=宋体]为[/font][font=宋体]2.57%[/font][font=宋体](n=6)[/font][font=宋体];五味子甲素为[/font][font=宋体]98.34[/font][font=宋体]%,[/font][font=Times New Roman]RSD[/font][font=宋体]为[/font][font=宋体]2.73%[/font][font=宋体](n=6)[/font][font=宋体];五味子乙素为[/font][font=宋体]98.06[/font][font=宋体]%,[/font][font=Times New Roman]RSD[/font][font=宋体]为[/font][font=宋体]1.61%[/font][font=宋体](n=6)[/font][font=宋体];丹参酮Ⅱ[/font][font=Times New Roman]A[/font][font=宋体]为[/font][font=宋体]99.13[/font][font=宋体]%,[/font][font=Times New Roman]RSD[/font][font=宋体]为[/font][font=宋体]1.42%[/font][font=宋体](n=6)[/font][font=宋体];[b]结论[/b][/font][font=Times New Roman] [/font][font=宋体]本法简便,灵敏度高,重现性好,可用于益心舒片的质量控制。[/font][color=black][font=宋体][/font][/color][/size][size=3][b][font=宋体]关键词[/font][/b][font=宋体]:益心舒片;五味子醇甲;[/font][font=宋体]五味子酯甲;五味子甲素;五味子乙素;[/font][font=宋体]丹参酮Ⅱ[/font][font=Times New Roman]A[/font][font=宋体];[/font][font=Times New Roman]HPLC[/font][font=宋体]法[/font][/size][b][color=black][font=Times New Roman]Determination of Schizandrin ,Schisantherin, Deoxyschizandrin , γ-Schishandrin and Tanshinone [/font][/color][color=black][font=宋体]Ⅱ[/font][/color][color=black][font=Times New Roman]A in Yixinshu Tablet by HPLC[/font][/color][/b][color=black][size=3][font=宋体]QIN Qian-ping[/font][/size][/color][color=black][size=3][font=宋体],WU Jian-xiong, BI Yu-an,LIN Xia,WANG Zhen-zhong,XIAO Wei [/font][/size][/color][size=3][font=Times New Roman][color=black](Jiangsu Kanion Pharmaceutical Co.Ltd, Lianyungang 222001,China )[/color][font=宋体][/font][/font][/size][b][color=black]Abstract : Objective [/color][/b][color=black]To establish a HPLC method for the determination of Schizandrin ,Schisantherin, Deoyschizandrin ,γ-Schishandrin and Tanshinone [/color]ⅡA in Yixinshu tablet. [b]Methods [/b][color=black]The Phenomenex Kinetex C[sub]18[/sub] column was used with a mobile [/color][size=3][font=宋体][color=black]phase of acetonitrile-water gradient elution[/color][color=black],the flow rate was 1ml/min,the column temperature was [/color][color=black]30[/color][color=black]℃,the detection wavelength was 250nm.[/color][color=black] [b]Results [/b][/color][color=black]The linear ranges [/color][/font][/size][size=3][font=宋体][color=black]of [/color][color=black]Schizandrin ,Schisantherin, Deoxyschizandrin ,γ-Schishandrin and Tanshinone[/color][/font][/size][size=3][font=宋体][color=black]ⅡA[/color][color=black] were [/color][color=black]0.2156[/color][color=black]~2.1560[/color][/font][color=black][font='Courier New']μ[/font][/color][font=宋体][color=black]g[/color][color=black](r=0.9999),0.0650~0.6500[/color][/font][color=black][font='Courier New']μ[/font][/color][font=宋体][color=black]g[/color][color=black] (r=0.9999)[/color][color=black],0.0346~0.3460[/color][/font][color=black][font='Courier New']μ[/font][/color][font=宋体][color=black]g[/color][color=black] (r=0.9999)[/color][color=black] ,[/color][color=black] 0.0692[/color][color=black]~0.6920[/color][/font][color=black][font='Courier New']μ[/font][/color][font=宋体][color=black]g[/color][color=black] (r=0.9999) and 0.0240[/color][color=black]~0.2400[/color][/font][color=black][font='Courier New']μ[/font][/color][font=宋体][color=black]g[/color][color=black] (r=0.9999) [/color][color=black]respectively.The average recoveries of five components were[/color][color=black] 97.92[/color][color=black]%,[/color][color=black]100.28[/color][color=black]%,[/color][color=black]98.34[/color][color=black]%,[/color][color=black]98.06[/color][color=black]% and [/color][color=black]99.13[/color][color=black]%.[/color][b][color=black]Conclusion[/color][/b][color=black] The method is simple [/color][color=black],sensitive and repeatable.It can be a method for quality control of [/color][color=black]Yixinshu tablet.[/color][color=black] [/color][/font][/size][size=3][font=宋体][b][color=black]Key words[/color][/b][color=black]:[/color][color=black]Yixinshu tablet[/color][color=black] Schizandrin Schisantherin Deoxyschizandrin [/color][/font][/size][size=3][font=宋体][color=black]γ-Schishandrin Tanshinone [/color][color=black]ⅡA [/color][color=black] HPLC[/color][color=black][/color][/font][/size][size=3][font=宋体]益心舒片处方由人参、丹参、五味子等药组成,其中五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素和五味子乙素[/font][/size][size=3][font=宋体]为五味子中的主要有效成分,丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]是丹参的主要有效成分。为了更好的控制产品质量,保证临床疗效,本文参照药典[/font][/size][sup][size=3][font=Times New Roman][1][/font][/size][/sup][size=3][font=宋体]及文献[/font][/size][sup][size=3][font=Times New Roman][2] [3][/font][/size][/sup][size=3][font=宋体],建立了[/font][/size][size=3][font=Times New Roman]HPLC[/font][/size][size=3][font=宋体]法测定益心舒片制剂中五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素、五味子乙素和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]的含量,方法可靠、灵敏、快速。[/font][/size][size=3][/size][b][size=3][font=Times New Roman]1 [/font][/size][size=3][font=宋体]仪器和试药[/font][/size][size=3][/size][/b][size=3][font=Times New Roman]Waters 2695[/font][/size][size=3][font=宋体]高效液相色谱仪;[/font][/size][size=3][font=Times New Roman]Waters 2487[/font][/size][size=3][font=宋体]检测器;五味子醇甲(批号:[/font][/size][size=3][font=Times New Roman]110857-200709[/font][/size][size=3][font=宋体]),[/font][/size][size=3][font=宋体]五味子酯甲[/font][/size][size=3][font=宋体](批号:[/font][/size][color=black][size=3][font=Times New Roman]111529-200803[/font][/size][/color][size=3][font=宋体]),[/font][/size][size=3][font=宋体]五味子甲素[/font][/size][size=3][font=宋体](批号:[/font][/size][color=black][size=3][font=Times New Roman]110764-200609[/font][/size][/color][size=3][font=宋体]),[/font][/size][size=3][font=宋体]五味子乙素[/font][/size][size=3][font=宋体](批号:[/font][/size][color=black][size=3][font=Times New Roman]110765-200508[/font][/size][/color][size=3][font=宋体]),丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体](批号:[/font][/size][color=black][size=3][font=Times New Roman]110766-200616[/font][/size][/color][size=3][font=宋体]),对照品均购自中国药品生物制品检定所;乙腈(色谱纯),水(超纯水),其余试剂均为分析纯。益心舒片(江苏康缘药业股份有限公司生产)。[/font][/size][size=3][/size][font=Times New Roman][b][size=3]2 [/size][/b][size=3][/size][/font][b][size=3][font=宋体]方法与结果[/font][/size][/b][size=3][/size][b][size=3][font=Times New Roman]2.1[/font][/size][size=3][font=宋体]色谱条件[/font][/size][size=3][/size][/b][size=3][font=宋体]色谱柱:[/font][/size][color=black][size=3][font=Times New Roman]Phenomenex Kinetex 2.6µ C18 100A(100*4.6mm)[/font][/size][/color][color=black][size=3][font=宋体];流动相:[/font][/size][/color][color=black][size=3][font=宋体]乙腈(A)-水溶液(B)梯度洗脱,线性洗脱程序为0~35min 30%→70%(A)[/font][/size][/color][color=black][size=3][font=宋体];流[/font][/size][/color][color=black][size=3][font=宋体]速:[/font][/size][/color][color=black][size=3][font=Times New Roman]1ml/min[/font][/size][/color][color=black][size=3][font=宋体];柱温:[/font][/size][/color][color=black][size=3][font=Times New Roman]30[/font][/size][/color][size=3][font=宋体]℃[/font][/size][color=black][size=3][font=宋体];测定波长:[/font][/size][/color][color=black][size=3][font=宋体]250nm[/font][/size][/color][color=black][size=3][font=宋体];进样量:10[/font][/size][/color][color=black][size=3][font=Times New Roman]μl[/font][/size][/color][color=black][size=3][font=宋体];[/font][/size][/color][color=black][size=3][font=宋体]理论塔板数以五味子醇甲峰计,不得低于4000。[/font][/size][/color][b][size=3][font=Times New Roman]2.2 [/font][/size][size=3][font=宋体]对照品溶液的制备[/font][/size][size=3][/size][/b][size=3][font=宋体]取五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素、五味子乙素和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]对照品适量,精密称定[/font][/size][size=3][font=Times New Roman],[/font][/size][size=3][font=宋体]加甲醇制成每[/font][/size][size=3][font=Times New Roman]1ml[/font][/size][size=3][font=宋体]含五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素、五味子乙素和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]分别为[/font][/size][size=3][font=Times New Roman]44[/font][/size][size=3][font=宋体]μg[/font][/size][size=3][font=宋体]、[/font][/size][size=3][font=Times New Roman]15[/font][/size][size=3][font=宋体]μg、15μg、8μg和6μg[/font][/size][size=3][font=宋体]的混合对照品溶液,即得。[/font][/size][size=3][/size][b][size=3][font=Times New Roman]2.3 [/font][/size][size=3][font=宋体]供试品溶液的制备[/font][/size][size=3][/size][/b][size=3][font=宋体] [/font][/size][size=3][font=宋体]取本品10片,除去薄膜衣,研细,取约1g,精密称定,[/font][/size][size=3][font=宋体]置锥形瓶中,精密加入甲醇10ml,超声(功率 250W,频率 40kHz) 提取40分钟,放冷,再称定重量,用甲醇补足减失的重量,滤过,取续滤液,即得。[/font][/size][b][size=3][font=Times New Roman]2.4 [/font][/size][size=3][font=宋体]线性关系的考察[/font][/size][/b][size=3][/size][size=3][font=宋体][/font][/size][size=3][font=宋体]精密称取对照品[/font][/size][size=3][font=宋体]五味子醇甲[/font][/size][size=3][font=宋体]21.56mg[/font][/size][size=3][font=宋体]、[/font][/size][size=3][font=宋体]五味子酯甲6.50mg、五味子甲素3.46mg、五味子乙素6.92mg和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体] 2.40mg[/font][/size][size=3][font=宋体],置50ml量瓶中,加甲醇溶解并稀释至刻度,摇匀,得[/font][/size][size=3][font=宋体]五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素、五味子乙素和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]浓度分别为431.20μg/ml、130.00μg/ml、69.20μg/ml、138.40μg/ml和48.00μg/ml的标准品储备液。分别精密量取上述溶液0.5ml,1.0ml,2.0ml,4.0ml,5.0ml,置10ml量瓶中,加甲醇稀释至刻度,摇匀,即得。分别精密吸取10μl,注入液相色谱仪,以峰面积为纵坐标(Y),进样量为横坐标(X),绘制标准曲线。[color=black]结果见表1。[/color][/font][/size][b][color=black][font=宋体][size=3]表1 线性范围、回归方程和相关系数[/size][/font][/color][color=black][font=宋体][size=3]Tab1 Results of linear ranges,regression equations and correlation coefficients[/size][/font][/color][/b][table][tr][td=1,1,142][color=black][font=宋体][size=3]成 分[/size][/font][/color][/td][td=1,1,142][size=3][color=black][font=宋体]线性范围([/font][/color][font=宋体]μg)[color=black][/color][/font][/size][/td][td=1,1,142][color=black][font=宋体][size=3]回归方程 [/size][/font][/color][/td][td=1,1,142][color=black][font=宋体][size=3]相关系数r[/size][/font][/color][/td][/tr][tr][td=1,1,142][size=3][font=宋体]五味子醇甲[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,142][size=3][color=black][font=宋体]0.2156[/font][/color][color=black][font=宋体]~2.1560[/font][/color][/size][/td][td=1,1,142][color=black][font=宋体][size=3]Y=33328X+19388[/size][/font][/color][/td][td=1,1,142][color=black][font=宋体][size=3]r=0.9999[/size][/font][/color][/td][/tr][tr][td=1,1,142][size=3][font=宋体]五味子酯甲[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,142][size=3][color=black][font=宋体]0.0650[/font][/color][color=black][font=宋体]~0.6500[/font][/color][/size][/td][td=1,1,142][color=black][font=宋体][size=3]Y=24524X-10302[/size][/font][/color][/td][td=1,1,142][color=black][font=宋体][size=3]r=0.9999[/size][/font][/color][/td][/tr][tr][td=1,1,142][size=3][font=宋体]五味子甲素[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,142][size=3][color=black][font=宋体]0.0346[/font][/color][color=black][font=宋体]~0.3460[/font][/color][/size][/td][td=1,1,142][color=black][font=宋体][size=3]Y=40977X-11022[/size][/font][/color][/td][td=1,1,142][color=black][font=宋体][size=3]r=0.9999[/size][/font][/color][/td][/tr][tr][td=1,1,142][size=3][font=宋体]五味子乙素[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,142][size=3][color=black][font=宋体]0.0692[/font][/color][color=black][font=宋体]~0.6920[/font][/color][/size][/td][td=1,1,142][color=black][font=宋体][size=3]Y=32190X-23084[/size][/font][/color][/td][td=1,1,142][color=black][font=宋体][size=3]r=0.9999[/size][/font][/color][/td][/tr][tr][td=1,1,142][size=3][font=宋体]丹参酮Ⅱ[/font][font=Times New Roman]A[font=宋体][/font][/font][/size][/td][td=1,1,142][size=3][color=black][font=宋体]0.0240[/font][/color][color=black][font=宋体]~0.2400[/font][/color][/size][/td][td=1,1,142][color=black][font=宋体][size=3]Y=70100X-44948[/size][/font][/color][/td][td=1,1,142][color=black][font=宋体][size=3]r=0.9999[/size][/font][/color][/td][/tr][/table][b][size=3][font=Times New Roman]2.5 [/font][/size][size=3][font=宋体]精密度试验[/font][/size][/b][size=3][font=宋体][/font][/size][size=3][font=宋体][/font][/size][size=3][font=宋体]精密吸取混合对照品溶液 ([/font][/size][size=3][font=宋体]五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素、五味子乙素和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]浓度分别为43.12μg/ml、16.60μg/ml、6.48μg/ml、14.92μg/ml和5.18μg/ml) 10μl,注入液相色谱仪,重复进样6次,测得峰面积,计算RSD。[/font][/size][size=3][font=宋体]五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素、五味子乙素和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]峰面积的[/font][/size][size=3][font=Times New Roman]RSD[/font][/size][size=3][font=宋体]分别为[/font][/size][size=3][font=Times New Roman]2.41%[/font][/size][size=3][font=宋体]、[/font][/size][size=3][font=Times New Roman]2.48%[/font][/size][size=3][font=宋体]、[/font][/size][size=3][font=Times New Roman]2.23%[/font][/size][size=3][font=宋体]、[/font][/size][size=3][font=Times New Roman]2.34%[/font][/size][size=3][font=宋体]和[/font][/size][size=3][font=Times New Roman]2.47%[/font][/size][size=3][font=宋体]。结果表明精密度良好。[/font][/size][size=3][font=宋体][/font][/size][b][size=3][font=Times New Roman]2.6 [/font][/size][size=3][font=宋体]稳定性试验[/font][/size][size=3][/size][/b][size=3][font=宋体][/font][/size][size=3][font=宋体]取本品(批号:090501)10片,除去包衣,研细,取约1g,精密称定。按供试品溶液制备项下方法制备供试品溶液,精密吸取供试品溶液10μl,分别于第0、2、4、6、9、12小时注入液相色谱仪,测得峰面积,计算RSD。[/font][/size][size=3][font=宋体]五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素、五味子乙素和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]峰面积的[/font][/size][size=3][font=Times New Roman]RSD[/font][/size][size=3][font=宋体]分别为[/font][/size][size=3][font=Times New Roman]1.10%[/font][/size][size=3][font=宋体]、[/font][/size][size=3][font=Times New Roman]1.36%[/font][/size][size=3][font=宋体]、[/font][/size][size=3][font=Times New Roman]0.99%[/font][/size][size=3][font=宋体]、[/font][/size][size=3][font=Times New Roman]1.54%[/font][/size][size=3][font=宋体]和[/font][/size][size=3][font=Times New Roman]1.24%[/font][/size][size=3][font=宋体]。[/font][/size][size=3][font=宋体]结果表明,供试品溶液在12小时内稳定。[/font][/size][b][size=3][font=Times New Roman]2.7 [/font][/size][size=3][font=宋体]重复性试验[/font][/size][size=3][/size][/b][size=3][font=宋体]取本品(批号:090501)10片,除去包衣,研细,取约1g,精密称定。按供试品溶液制备项下方法制备供试品溶液,平行制备6份,测定,计算含量,结果五味子醇甲平均含量为0.15mg/片,RSD为1.03%;五味子酯甲平均含量为0.036mg/片,RSD为2.96%;五味子甲素平均含量为0.019mg/片,RSD为2.88%;五味子乙素平均含量为0.043mg/片,RSD为2.96%;[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]平均含量为0.014mg/片,RSD为2.66%。结果表明本方法重复性良好。[/font][/size][b][size=3][font=Times New Roman]2.8 [/font][/size][size=3][font=宋体]回收率试验[/font][/size][size=3][/size][/b][size=3][font=宋体][/font][/size][size=3][font=宋体]取本品(批号:090501,含量:五味子醇甲为0.15mg/片,五味子酯甲为0.036mg/片,五味子甲素为0.019mg/片,五味子乙素为0.043mg/片,[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]为0.014mg/片。),除去包衣,研细,取6份,每份约0.5g,精密称定,分别精密加入含[/font][/size][size=3][font=宋体]五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素、五味子乙素和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]为2160μg/ml、679.0μg/ml、346.0μg/ml、662.0μg/ml和148.0μg/ml的混合对照品溶液1ml,然后精密加入甲醇9ml,按供试品溶液制备项下方法制备供试品溶液,进行含量测定,并计算回收率。结果见表2。[/font][/size][align=center][b][font=宋体][size=3]表2 回收率测定结果(n=6)[/size][/font][/b][/align][align=center][b][font=宋体][size=3]Tab 2 Results of recovery[color=black][/color][/size][/font][/b][/align][table=100%][tr][td=1,1,29%][color=black][font=宋体][size=3]成 分[/size][/font][/color][/td][td=1,1,41%][color=black][font=宋体][size=3]平均回收率(%)[/size][/font][/color][/td][td=1,1,24%][size=3][color=black][font=宋体]RSD[/font][/color][color=black][font=宋体](%)[/font][/color][/size][/td][td=1,1,5%][color=black][font=宋体][size=3][/size][/font][/color][/td][/tr][tr][td=1,1,29%][size=3][font=宋体]五味子醇甲[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,41%][size=3][font=宋体]97.93[/font][font=宋体]%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,24%][size=3][font=宋体]2.34%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,5%][color=black][font=宋体][size=3][/size][/font][/color][/td][/tr][tr][td=1,1,29%][size=3][font=宋体]五味子酯甲[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,41%][size=3][font=宋体]100.29[/font][font=宋体]%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,24%][size=3][font=宋体]2.57%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,5%][color=black][font=宋体][size=3][/size][/font][/color][/td][/tr][tr][td=1,1,29%][size=3][font=宋体]五味子甲素[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,41%][size=3][font=宋体]98.34[/font][font=宋体]%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,24%][size=3][font=宋体]2.73%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,5%][color=black][font=宋体][size=3][/size][/font][/color][/td][/tr][tr][td=1,1,29%][size=3][font=宋体]五味子乙素[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,41%][size=3][font=宋体]98.05[/font][font=宋体]%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,24%][size=3][font=宋体]1.61%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,5%][color=black][font=宋体][size=3][/size][/font][/color][/td][/tr][tr][td=1,1,29%][size=3][font=宋体]丹参酮Ⅱ[/font][font=Times New Roman]A[font=宋体][/font][/font][/size][/td][td=1,1,41%][size=3][font=宋体]99.08[/font][font=宋体]%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,24%][size=3][font=宋体]1.42[/font][font=宋体]%[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,5%][color=black][font=宋体][size=3][/size][/font][/color][/td][/tr][/table][b][size=3][font=Times New Roman]2.9 [/font][/size][size=3][font=宋体]样品含量的测定[/font][/size][size=3][font=Times New Roman] [/font][/size][/b][size=3][font=宋体]取3批益心舒片样品,制备供试品溶液。分别精密吸取供试品溶液、对照品溶液各10μl,注入高效液相色谱仪,测定,计算,结果见表3. [/font][/size][align=center][b][font=宋体][size=3]表3 样品测定结果(n=3)[/size][/font][/b][/align][align=center][size=3][b][font=宋体]Tab 3 Results of content determination of the samples[/font][font=宋体][/font][/b][/size][/align][table][tr][td=1,1,142][table=139][tr][td=1,1,139][align=center][font=宋体][size=3]成分 批号[/size][/font][/align][/td][/tr][/table][align=center][font=宋体][size=3][/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]090501[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]090502[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]090503[/size][/font][/align][/td][/tr][tr][td=1,1,142][size=3][font=宋体]五味子醇甲([/font][font=Times New Roman]mg/[/font][font=宋体]片)[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,142][font=宋体]0.15[/font][/td][td=1,1,142][font=宋体]0.16[/font][/td][td=1,1,142][align=center][font=宋体][size=3]0.16[/size][/font][/align][/td][/tr][tr][td=1,1,142][size=3][font=宋体]五味子酯甲[/font][font=宋体]([/font][font=Times New Roman]mg/[/font][font=宋体]片)[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,142][align=center][font=宋体][size=3]0.036[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]0.042[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]0.037[/size][/font][/align][/td][/tr][tr][td=1,1,142][size=3][font=宋体]五味子甲素[/font][font=宋体]([/font][font=Times New Roman]mg/[/font][font=宋体]片)[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,142][align=center][font=宋体][size=3]0.019[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]0.021[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]0.022[/size][/font][/align][/td][/tr][tr][td=1,1,142][size=3][font=宋体]五味子乙素[/font][font=宋体]([/font][font=Times New Roman]mg/[/font][font=宋体]片)[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,142][align=center][font=宋体][size=3]0.043[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]0.046[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]0.047[/size][/font][/align][/td][/tr][tr][td=1,1,142][size=3][font=宋体]丹参酮Ⅱ[/font][font=Times New Roman]A[/font][font=宋体]([/font][font=Times New Roman]mg/[/font][font=宋体]片)[/font][color=black][font=宋体][/font][/color][/size][/td][td=1,1,142][align=center][font=宋体][size=3]0.014[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]0.017[/size][/font][/align][/td][td=1,1,142][align=center][font=宋体][size=3]0.015[/size][/font][/align][/td][/tr][/table][b][size=3][font=Times New Roman]3 [/font][/size][size=3][font=宋体]讨论[/font][/size][size=3][font=Times New Roman] [/font][/size][/b][size=3][font=宋体]3.1[/font][/size][size=3][font=宋体]在供试品溶液的制备时,考虑到指标成分的提取率,以及其他成分对含量测定的影响,考察了提取溶媒乙醇、甲醇、80%甲醇、70%乙醇、50%甲醇和50%乙醇,比较了超声提取和回流提取的效果。结果表明采用甲醇超声处理提取效果较好。[/font][/size][size=3][font=宋体]3.2[/font][/size][size=3][font=宋体]本文采用HPLC法进行[/font][/size][size=3][font=宋体]五味子醇甲、[/font][/size][size=3][font=宋体]五味子酯甲、五味子甲素、五味子乙素和[/font][/size][size=3][font=宋体]丹参酮Ⅱ[/font][/size][size=3][font=Times New Roman]A[/font][/size][size=3][font=宋体]的含量测定,比较了甲醇[/font][/size][size=3][font=Times New Roman]-[/font][/size][size=3][font=宋体]水、乙腈[/font][/size][size=3][font=Times New Roman]-[/font][/size][size=3][font=宋体]水和乙腈[/font][/size][size=3][font=Times New Roman]-0.1%[/font][/size][size=3][font=宋体]磷酸溶液[/font][/size][sup][size=3][font=Times New Roman][4][/font][/size][/sup][size=3][font=宋体]三种流动相系统的分离效果,结果采用乙腈[/font][/size][size=3][font=Times New Roman]-[/font][/size][size=3][font=宋体]水溶液分离效果较好。比较了检测波长[/font][/size][sup][size=3][font=Times New Roman][4] [5] [/font][/size][/sup][size=3][font=宋体],结果表明[/font][/size][size=3][font=Times New Roman]250nm[/font][/size][size=3][font=宋体]处,各峰峰形良好,基线平稳,分离度高。比较了[/font][/size][color=black][size=3][font=Times New Roman]Phenomenex Kinetex C18[/font][/size][/color][color=black][size=3][font=宋体]柱、[/font][/size][/color][color=black][size=3][font=Times New Roman]Phenomenex Luna C18[/font][/size][/color][color=black][size=3][font=宋体]柱和[/font][/size][/color][color=black][size=3][font=Times New Roman]Kromasil C18[/font][/size][/color][color=black][size=3][font=宋体]柱,结果[/font][/size][/color][color=black][size=3][font=Times New Roman]Phenomenex Luna C18[/font][/size][/color][color=black][size=3][font=宋体]柱和[/font][/size][/color][color=black][size=3][font=Times New Roman]Kromasil C18[/font][/size][/color][color=black][size=3][font=宋体]柱未能使本文中所检测的[/font][/size][/color][color=black][size=3][font=Times New Roman]5[/font][/size][/color][color=black][size=3][font=宋体]个成分均达到基线分离,快速分离柱[/font][/size][/color][color=black][size=3][font=Times New Roman]Phenomenex Kinetex C18[/font][/size][/color][color=black][size=3][font=宋体]柱能较好的分离本品中上述[/font][/size][/color][color=black][size=3][font=Times New Roman]5[/font][/size][/color][color=black][size=3][font=宋体]个成分。[/font][/size][/color][size=3][/size]

目的:研究不同干燥方式对丹参质量的影响方法:以指标性成分进行HPLC和TLC检测一、三种干燥方法简介:减压干燥原理:湿物料进行干燥时,同时进行着二个过程:(1)热量由热空气传递给湿物料,使物料表面上的水分立即气化,并通过物料表面处的气膜,向气流主体中扩散;(2)由于湿物料表面处水分气化的结果,使物料内部与表面之间产生水分浓度差,于是水分即由内部向表面扩散。因此,在干燥过程中同时进行着传热和传质二个相反的过程。干燥过程的重要条件是必须具有传热和传质的推动力。物料表面蒸气压一定要大于干燥介质(空气)中的蒸气分压,压差越大,干燥过程进行得越快。冷冻干燥(以下简称冻干)就是将含水物质,先冻结成固态,而后使其中的水分从固态升华成气态,以除去水分而保存物质的方法。喷雾干燥是利用不同的喷雾器,将悬浮液或黏滞的液体喷成雾状,与热空气之间发生热量和质量传递而进行干燥的过程。成品以粉末状态沉陷于干燥室底部,连续或间断地从卸料器排出。二、TLC检测结果(1)取本品粉末lg,加乙醚5ml,振摇,放置1小时,滤过,滤液挥于,残渣加乙酸乙酯1ml使溶解,作为供试品溶液。取丹参酮Ⅱ对照品,加乙酸乙酯制成每1ml含2mg的溶液,作为对照品溶液。照薄层色谱法(附录ⅥB)试验,吸取上述三种溶液各5μl,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)一乙酸乙酯(4:1)为展开剂,展开,取出,晾干。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点;在与对照品色谱相应的位置上,显相同的暗红色斑点。结果如下:http://ng1.17img.cn/bbsfiles/images/2011/12/201112031621_335254_1913683_3.jpg斑点依次为:对照、喷雾干燥样品、减压干燥样品、冷冻干燥样品(2)取本品粉末0.2g,加75%甲醇25ml,超声30min,滤过,滤液浓缩至1ml,作为供试品溶液。另取丹酚酸B对照品,加75%甲醇制成每1ml含2mg的溶液,作为对照品溶液。照薄层色谱法(附录ⅥB)试验,吸取上述两种溶液各5μl,分别点于同一硅胶GF254薄层板上,以甲苯一三氯甲烷一乙酸乙酯一甲醇一甲酸(2:3:4:0.5:2)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。结果如下:http://ng1.17img.cn/bbsfiles/images/2011/12/201112031623_335255_1913683_3.jpg斑点依次为:对照、喷雾干燥样品、减压干燥样品、冷冻干燥样品三、HPLC检测结果 色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂的普通C18柱;以甲醇-乙腈-甲酸- 水(30:10:1:59)为流动相;检测波长为286nm。理论板数按丹酚酸B峰计算应不低于2000。 对照品溶液的制备 [font=宋
[align=center]板栗叶水浸液对商洛丹参幼苗酶活性的影响[/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]食品事业部:魏娜[/align][b]摘要:[/b]本实验以商洛丹参种子为材料,以板栗叶为供体,研究不用浓度板栗叶水浸液对商洛丹参幼苗酶活性的影响。采用生物测定法测定丹参幼苗酶活性的状况。关键词:丹参,板栗叶水浸液,酶活性植物化感作用(Allelopathy)是指植物(含微生物)向环境释放特殊的化学物质而对其他植物或微生物产生直接或间接的有害或有益的作用,这些特殊的化学物质叫做化感物质。化感物质一方面通过植物体释放产生,另一方面通过植物地上和地下部分的残体分解产生。化感作用广泛存在于自然界中,它涵盖了各种植物之间、包括微生物间的相生相克关系,对解释植物个体及种间的相互作用机制和构建可持续的植物群落都起着重要的作用,并对农、林业生产有重要的影响,如农作物的连作障碍、森林更新失败以及生物入侵等现象都与化感作用密切相关。 化感物质进入土壤后,植物根际微生态系统将发生复杂的变化。化感物质对土壤微生物区系及酶活性的研究,包括根系分泌物数量和成分的变化与土壤微生物类群的关系、土壤酶活性与土壤微生物种类及数量的关系等,这为研究化感作用对土壤根际微生态系统的影响,特别是为根际微生物区系的变化提供了有益的参考。目前,有关植物某一部位水浸液以及纯化感物质对土壤酶活性、土壤养分和微生物数量影响的相关研究相对较少,已有研究主要包括:黄益宗等研究发现化感物质阿魏酸对土壤硝化反应的抑制作用最强,其次是对叔丁基苯甲酸 吕可等通过用花椒叶水浸液浇灌盆栽花椒幼苗研究水浸液对土壤酶和微生物的影响,结果表明:花椒叶水浸液使根际土中的细菌、真菌和放线菌数量以及微生物总数均有不同程度的减少,使根际土蛋白酶、蔗糖酶和酸性磷酸酶活性明显低于非根际土相应的酶活性,而过氧化氢酶和多酚氧化酶活性则显著升高 印楝种子壳的酒精水浸液显著抑制了土壤中放线菌的数量,显著增加了土壤中自由固氮细菌的数量,显著抑制了土壤中反硝化细菌的数量,土壤脱氢酶活性未受到影响,而磷酸酶活性受到了严重的抑制 2,4二叔丁基苯甲酸(PEDT)和香草酸两种化感物质均在低浓度下提高而在高浓度下抑制了微生物生物量及其活力。板栗(Castanea mollissima Blume),有较高的药用价值,有健脾胃、益气、补肾、强心的功用。其中所含的丰富的不饱和脂肪酸和维生素,能防治高血压病、冠心病和动脉硬化等疾病。板栗在商洛地区大面积种植,是商洛主要经济林品种之一、五大商药之一、也是商洛的主要经济作物之一。丹参(Salvia miltiorrhiza Bge. )为唇形科鼠尾草属多年生草本植物,具有祛瘀止痛、活血通经、清心除烦等功能。 其根及根茎是常用的重要中药[sup][color=#3366cc][/color][/sup],有活血化瘀、消肿止痛、养血安神的功能[sup][color=#3366cc][/color][/sup]。丹参根中含有丹参素、丹参酮等生物活性物质[sup][color=#3366cc][/color][/sup],对治疗冠心病、心绞痛和脑血管疾病有很好的疗效,同时还具有抗菌消炎、保肝和改善肾功能的作用[sup][color=#3366cc][/color][/sup]。研究不同浓度板栗叶水浸液对商洛丹参幼苗酶活性的影响,对科学构建林药复合系统,合理选择林下中药材品种,提高土地利用率,增加农民收入,促进地方经济发展,不仅具有理论指导作用,还具有非常重要的现实意义。化感作用的研究对农林(林药)复合系统中物种的配置、耕作制度和栽培措施的优化,农田病虫害的控制、复合系统的经营管理,以及保持生物多样性和农业可持续发展有重要意义。在农林(林药)复合系统中,林木会通过淋溶、挥发、残体分解和根系分泌向林下植物释放有益或有害的化学物质,促进或抑制植物的生长和生产,那么合理选择林下作物品种直接影响整个复合系统的总产量和农民的经济收入。研究板栗和丹参之间的化感作用,对林药复合生态系统的构建、管理、经营有着十分重要的意义。[b]1.材料与方法1.1 实验材料[/b]1.1.1实验材料[b] [/b] 供体材料为板栗叶,采自商州区。受体种子为商洛地道中药材丹参。1.1.2实验仪器 人工气候培养箱、分光光度计、水浴锅、冷冻离心机、制冰机、天枰、真空干燥器1.1.3实验试剂[b] 1.2 实验方法1.2.1 板栗叶水浸液的制备[/b]。取风干的板栗叶样品,剪成1cm长的小段,按30g/600mL的比例用蒸馏水浸泡,在振荡器上震荡48h(25℃),过滤后即得浓度为0.05g/mL的水浸液(母液),用蒸馏水将水浸液分别稀释至0.01、0.02、0.03、0.04、0.05mol/L,置于4℃冰箱备用。 表 1 制作不同浓度的板栗叶水浸液[table][tr][td] 板栗叶水的浓度(mol/L)[/td][td] 母液(mL)[/td][td=1,6]分别用蒸馏水定容至500mL。[/td][/tr][tr][td] 0.01[/td][td] 10[/td][/tr][tr][td] 0.02[/td][td] 20[/td][/tr][tr][td] 0.03[/td][td] 30[/td][/tr][tr][td] 0.04[/td][td] 40[/td][/tr][tr][td] 0.05[/td][td] 50[/td][/tr][/table][b]1.2.2 丹参种子萌发及幼苗培养。 [/b]取丹参种子先用0.1%HgCL[sub]2 [/sub]消毒10min,浸泡24h。蒸馏水冲洗数次,滤干后均匀排列放至培养皿中,于人工气候培养箱(温度25℃,湿度62°)中培养。从培养的第二天起及时补充等量水浸液和蒸馏水,使滤纸始终保持湿润。[b]1.2.3 [/b]超氧化物歧化酶活性的测定 取丹参种子0.20g,加5ml的mmol/L的磷酸缓冲液,研磨成匀浆,匀浆液以5000r/min离心15min,按谁谁的比色法(愈创木酚法),测定各组丹参幼苗SOD酶活性,最后以OD470/ming表示超氧化物歧化酶的活性[align=center][b]实验一 氮蓝四唑(NBT)法测定超氧化物歧化酶(SOD)活力[][/b][/align]一、原理 超氧化物歧化酶(superoxide dismutase,SOD)普遍存在于动、植物体内,是一种清除超氧阴离子自由基的酶。本实验依据超氧化物歧化酶抑制氮蓝四唑(NBT)在光下的还原作用来确定酶活性大小。在有氧化物质存在下,核黄素可被光还原,被还原的核黄素在有氧条件下极易再氧化而产生超氧阴离子自由基,超氧阴离子自由基可将氮蓝四唑还原为蓝色的甲腙,后者在560nm处有最大吸收。而SOD可清除超氧阴离子自由基,从而抑制了甲腙的形成。于是光还原反应后,反应液蓝色愈深,说明酶活性愈低,反之酶活性愈高。据此可以计算出酶活性大小。二、材料、仪器设备及试剂(一)材料:植物叶片。(二)仪器设备:高速台式离心机,分光光度计,微量进样器,荧光灯(反应试管处照度为4000lx),试管或指形管数支,黑色硬纸套。(三)试剂(1)0.05mol/L磷酸缓冲液(pH7.8)。A母液:0.2mol/L 磷酸氢二钠溶液:取Na[sub]2[/sub]HPO[sub]4[/sub]12H[sub]2[/sub]O (分子量358.14) 71.7gB母液: 0.2mol/L 磷酸二氢钠溶液:取NaH[sub]2 [/sub]PO[sub]4[/sub]2H[sub]2[/sub]O ( 分子量156.01) 31.2g分别用蒸馏水定容至1000mL;0.05mol/L磷酸缓冲液(pH7.8)的配制:分别取A母液(Na[sub]2[/sub]HPO[sub]4[/sub])228.75mL,B母液(NaH[sub]2 [/sub]PO[sub]4[/sub])21.25mL,用蒸馏水定容至1000mL。(2)130mmol/L甲硫氨酸(Met)溶液:称1.9399gMet用磷酸缓冲液定容至100ml。(3)750μmol/L氮蓝四唑溶液(NBT):称取0.06133gNBT用磷酸缓冲液定容至100ml,避光保存。(4)100μmol/L EDTA-Na[sub]2[/sub]溶液:称取0.03721g EDTA-Na[sub]2[/sub],用磷酸缓冲液定容至1000ml。(5)20 μmol/L核黄素溶液:称取0.0753g核黄素用蒸馏水定容至1000ml,避光保存。三、实验步骤1.酶液提取 取丹参幼苗0.5g于研钵中研磨成粉末,加2ml预冷的提取介质在冰浴上研磨成浆,加入提取介质冲洗研钵,提取介质终体积为5ml。取1.5-2ml于4℃下10000r/min下离心20min,上清液即为SOD粗提液。2.显色反应 取5ml指形管或试管(要求透明度好)4支,2支为测定管,另2支为对照管,按下表加入各种溶液: 表2 制作[table][tr][td][align=center]试剂名称[/align][/td][td][align=center]用量(mL)[/align][/td][td][align=center]终浓度(比色时)[/align][/td][/tr][tr][td][align=center]0.05mol/L磷酸缓冲液[/align][/td][td][align=center]1.5[/align][/td][td][align=center] [/align][/td][/tr][tr][td][align=center]130mmol/L Met溶液[/align][/td][td][align=center]0.3[/align][/td][td][align=center]13mmol/L[/align][/td][/tr][tr][td][align=center]750μmol/L NBT溶液[/align][/td][td][align=center]0.3[/align][/td][td][align=center]75μmol/L[/align][/td][/tr][tr][td][align=center]100μmol/L EDTA-Na[sub]2[/sub]溶液[/align][/td][td][align=center]0.3[/align][/td][td][align=center]10μmol/L[/align][/td][/tr][tr][td][align=center]20 μmol/L核黄素溶液[/align][/td][td][align=center]0.3[/align][/td][td][align=center]2.0μmol/L[/align][/td][/tr][tr][td][align=center]酶液[/align][/td][td][align=center]0.05[/align][/td][td][align=center]2支对照管以缓冲液代替酶液[/align][/td][/tr][tr][td][align=center]蒸馏水[/align][/td][td][align=center]0.25[/align][/td][td][align=center] [/align][/td][/tr][tr][td][align=center]总体积[/align][/td][td][align=center]3.0[/align][/td][td][align=center] [/align][/td][/tr][/table]混匀后将1支对照管罩上比试管稍长的双层黑色硬纸套遮光或置暗处,其他各管于4000lx日光下反应20min 至反应结束后,用黑布罩盖上试管,以不照光的对照管作空白,分别测定其他各管在560nm下的吸光度。