乙酰丙酮烯醇式羟基氢的吸收峰为何不是尖峰,而是宽峰?
在做二羟基丙酮的硅烷化分析的时候,出现一个问题:当标准样品的量比较少的时候比如10mg左右的时候,气相上出来的是二羟基丙酮的硅烷化的峰,但是当标品的来那个超过20mg的时候会出来二羟基丙酮硅烷化峰以及二羟基丙酮二聚体硅烷化峰,不知哪位专家做过此物质的分析,可否指点一下。
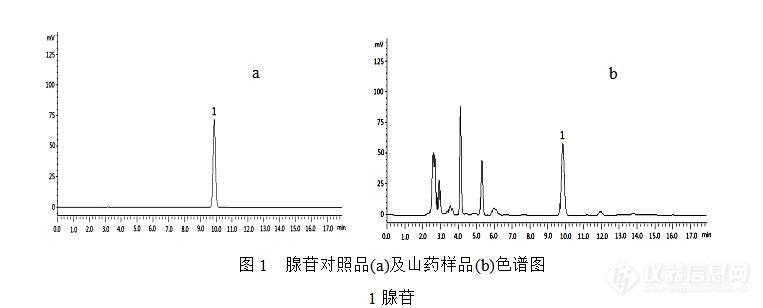
[align=center][b]HPLC测定不同来源山药中腺苷和脱氢表雄酮的含量[/b][/align] 山药(Dioscoreae Rhizoma)是薯蓣科植物薯蓣([i]Dioscorea opposita [/i]Thunb.)的干燥块茎,具有补脾养胃、生津益肺、补肾涩精的功能,是国家卫生部公布的药食两用的中药。然而在2015版《中国药典》一部中只收载了性状、鉴别、检查和浸出物等项目,缺少含量测定项指标,不足以对山药质量进行全面有效的控制。DHEA是人体肾上腺素的一种,国内外研究已经证实,DHEA对预防和治疗心血管疾病、增强免疫力、延缓衰老等均有一定效果,是山药中的重要活性成分之一。另外,腺苷具有舒张血管、降低血压、减慢心律、抑制血小板聚集、松弛血管平滑肌等生理活性。长期以来,由于对山药品种的评价和改良工作进展缓慢,目前仍然存在山药种植品种杂乱,缺乏综合性优良的品种。因此,本研究对包括野生山药在内的不同来源山药中的腺苷、DHEA含量进行测定,旨在为山药质量标准建立提供参考依据,也为山药品种驯化和选育提供一定的研究基础。[b][b]1 仪器和试药[/b][/b]LC-20AD高效液相色谱仪,配备紫外可见检测器(日本,岛津公司);ME204电子天平(德国Mettler Toledo公司),KQ-E型超声波清洗器(昆山市超声仪器有限公司)。脱氢表雄酮标准品(阿拉丁,批号为H1408213),腺苷标准品(中国食品药品检定研究院,批号为110879-200202);甲醇为色谱纯,水为娃哈哈纯净水,其他试剂均为分析纯。山药样品采自河南省温县山药种植基地。[b][b]2 方法与结果2.1标准储备溶液的制备[/b][/b]精密称取腺苷对照品6.61 mg置25 mL容量瓶中,加15 %甲醇溶解稀释至刻度,摇匀,配制成浓度为264.40 μgmL[sup]-[/sup][sup]1[/sup]的腺苷标准品储备溶液。精密称取DHEA对照品7.62 mg置50 mL容量瓶中,加甲醇溶解稀释至刻度,摇匀,配制成浓度为152.40 μgmL[sup]-[/sup][sup]1[/sup]的DHEA标准品储备溶液。[b][b]2.2样品的处理[/b][/b]2.2.1 腺苷样品的处理取本品粉末(过3号筛)约1.0 g,精密称定,置具塞锥形瓶中,精密加入15%甲醇l0 mL,密塞,摇匀,称定质量,超声处理30 min,放冷,再称定质量,用15%甲醇补足减失的重量,12000 rmin[sup]-[/sup][sup]1[/sup]离心15 min,取上清液,0.45 μm微孔滤膜滤过,取续滤液作为供试品溶液。2.2.2 DHEA样品的处理取本品粉末(过3号筛)约3.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇l5 mL,密塞,摇匀,称定质量,超声处理1 h,放冷,再称定质量,用甲醇补足减失的重量,摇匀,0.45μm微孔滤膜滤过,取续滤液作为供试品溶液。[b][b]2.3 色谱条件[/b][/b]2.3.1 腺苷色谱条件:色谱柱:Aglient Extend XDB C18柱(4.6 mm×250 mm,5 μm);流动相:磷酸盐缓冲液(pH6.5) -甲醇(94:6,[i]v/v[/i]);流速:1 mLmin[sup]-[/sup][sup]1[/sup];柱温:30 °C; 检测波长:260 nm;进样量:10 μL。HPLC图见图1。2.3.2 DHEA色谱条件:色谱柱:Welch Ultimate XB-C18柱(4.6 mm×250 mm,5 μm);流动相:甲醇-水(62:38,[i]v/v[/i]);流速:0.6 mLmin[sup]-[/sup][sup]1[/sup];柱温:30 °C; 检测波长:204 nm;进样量:10 μL。HPLC图见图2。[img=,690,278]https://ng1.17img.cn/bbsfiles/images/2019/07/201907031540228286_5423_3451954_3.jpg!w690x278.jpg[/img][img=,690,300]https://ng1.17img.cn/bbsfiles/images/2019/07/201907031540280876_3707_3451954_3.jpg!w690x300.jpg[/img][b][b]2.4标准曲线的绘制[/b][/b]精密吸取腺苷标准品储备溶液0.5,1,3,5,8,10 mL分别置于10 mL量瓶中,加甲醇定容至刻度,摇匀,按上述色谱条件进样,以峰面积值 Y为纵坐标,腺苷浓度X为横坐标绘制标准方程为:[i]Y[/i]=34197.2[i] X[/i]+25515.1,[i]r[/i]=0.9999,表明腺苷在13.22 ~ 264.40 μgmL[sup]-[/sup][sup]1[/sup]浓度内与峰面积线性关系良好。精密吸取DHEA标准品储备溶液1 mL置于10 mL量瓶中,加甲醇定容至刻度,摇匀,得15.24 μgmL[sup]-[/sup][sup]1[/sup]的DHEA使用溶液。分别精密吸取DHEA使用溶液0.5,1,3,5,8,10 mL置于10 mL量瓶中,加甲醇定容至刻度,摇匀,按上述色谱条件进样,以峰面积值 Y为纵坐标,DHEA浓度X为横坐标绘制标准方程为:[i]Y[/i]=13042.7 [i]X[/i]-1836.3,[i]r[/i]=0.9999,表明DHEA在0.76 ~ 15.24 μgmL[sup]-[/sup][sup]1[/sup]浓度内与峰面积线性关系良好。[b][b]2.5 重复性试验[/b][/b] 取同一供试品粉末6份,精密称定,按“2.2”项下方法处理,按“2.3”项下色谱条件测定峰面积。结果腺苷和DHEA峰面积的RSD分别为1.87 %和1.91 % (n=6),表明方法重复性良好。[b][b]2.6 精密度试验[/b][/b]精密吸取同一供试品溶液10 μL,按上述色谱条件连续进样6次,测定腺苷、DHEA峰面积值,其RSD分别为0.92 %和1.03 % (n=6),表明仪器及进样精密度良好。[b][b]2.7 稳定性试验[/b][/b] 精密吸取同一供试品溶液,室温放置,分别在0,2,4,8,12,24,48 h进样分析。测定腺苷、DHEA峰面积值,其RSD分别为2.07 %和1.65 % (n=6),表明供试品溶液在48 h内稳定性良好。[b][b]2.8 回收率[/b][/b]分别称取已知含量的样品6份,精密称定,分别加入相当含量的腺苷和DHEA对照品溶液,按“2.2”项下供试品溶液的制备方法制备供试品溶液,分别进行测定,计算回收率。结果腺苷、DHEA平均加样回收率为98.10 % (RSD=1.40 %)和97.72 % (RSD=1.15 %),结果见表1、2。[align=center][b]表1 山药样品中腺苷的加样回收率实验结果(n=6)[/b][/align][table][tr][td][align=center]取样量/g[/align][/td][td][align=center]样品中量/mg[/align][/td][td][align=center]添加量/mg[/align][/td][td][align=center]测得量/mg[/align][/td][td][align=center]回收率/%[/align][/td][td][align=center]平均回收率/%[/align][/td][td][align=center]RSD/%[/align][/td][/tr][tr][td][align=center]0.5014[/align][/td][td][align=center]0.1604 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3141[/align][/td][td][align=center]96.88 [/align][/td][td=1,6][align=center]98.10[/align][/td][td=1,6][align=center]1.40[/align][/td][/tr][tr][td][align=center]0.5011[/align][/td][td][align=center]0.1604 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3201[/align][/td][td][align=center]100.72 [/align][/td][/tr][tr][td][align=center]0.4989[/align][/td][td][align=center]0.1596 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3147[/align][/td][td][align=center]97.76 [/align][/td][/tr][tr][td][align=center]0.4997[/align][/td][td][align=center]0.1599 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3141[/align][/td][td][align=center]97.22 [/align][/td][/tr][tr][td][align=center]0.5001[/align][/td][td][align=center]0.1600 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3159[/align][/td][td][align=center]98.28 [/align][/td][/tr][tr][td][align=center]0.5012[/align][/td][td][align=center]0.1604 [/align][/td][td][align=center]0.1586[/align][/td][td][align=center]0.3154[/align][/td][td][align=center]97.74 [/align][/td][/tr][/table][align=center][b]表2 山药样品中DHEA的加样回收率实验结果(n=6)[/b][/align][table][tr][td][align=center]取样量/g[/align][/td][td][align=center]样品中量/mg[/align][/td][td][align=center]添加量/mg[/align][/td][td][align=center]测得量/mg[/align][/td][td][align=center]回收率/%[/align][/td][td][align=center]平均回收率/%[/align][/td][td][align=center]RSD/%[/align][/td][/tr][tr][td][align=center]1.5013[/align][/td][td][align=center]0.0293 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0589[/align][/td][td][align=center]97.13 [/align][/td][td=1,6][align=center]97.72 [/align][/td][td=1,6][align=center]1.15 [/align][/td][/tr][tr][td][align=center]1.5024[/align][/td][td][align=center]0.0293 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0591[/align][/td][td][align=center]97.72 [/align][/td][/tr][tr][td][align=center]1.4997[/align][/td][td][align=center]0.0292 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0597[/align][/td][td][align=center]99.86 [/align][/td][/tr][tr][td][align=center]1.5001[/align][/td][td][align=center]0.0293 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0589[/align][/td][td][align=center]97.21 [/align][/td][/tr][tr][td][align=center]1.4987[/align][/td][td][align=center]0.0292 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0587[/align][/td][td][align=center]96.64 [/align][/td][/tr][tr][td][align=center]1.5011[/align][/td][td][align=center]0.0293 [/align][/td][td][align=center]0.0305[/align][/td][td][align=center]0.0591[/align][/td][td][align=center]97.80 [/align][/td][/tr][/table][b][b]2.9 结果分析[/b][/b]精密称取不同来源的山药粉末,按“2.2”项下方法制备供试品溶液,分别进样,记录峰面积积分值,外标法计算腺苷及DHEA的含量。结果如下表3所示。[align=center][b]表3 不同来源山药药材中腺苷及DHEA的含量([i]n[/i]=3)[/b][/align][table][tr][td][align=center]编号[/align][/td][td][align=center]样品来源[/align][/td][td][align=center]腺苷含量/%[/align][/td][td][align=center]DHEA含量/mg/kg[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]种植铁棍山药[/align][/td][td][align=center]0.032[/align][/td][td][align=center]19.50 [/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]野生山药1[/align][/td][td][align=center]0.027[/align][/td][td][align=center]5.38 [/align][/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]野生山药2[/align][/td][td][align=center]0.024[/align][/td][td][align=center]3.29[/align][/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]驯化野生山药雌株[/align][/td][td][align=center]0.037[/align][/td][td][align=center]24.05 [/align][/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]驯化野生山药雄株[/align][/td][td][align=center]0.040[/align][/td][td][align=center]62.25 [/align][/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]紫山药[/align][/td][td][align=center]ND[/align][/td][td][align=center]ND[/align][/td][/tr][/table] 从测定结果看,不同来源山药中腺苷和DHEA含量差别较大,可能由于品种及生长环境的差异造成。研究表明,驯化野生山药雄株中腺苷和DHEA含量最高,显著高于野生山药中的含量,说明驯化过程对野生山药的改良起到了很好的积极作用。另外,驯化野生山药雄株中DHEA含量比公认的营养成分较高的铁棍山药高出3倍左右,进一步说明该山药品质的优异性。 另外,紫山药中并未检测到腺苷和DHEA两种成分的存在,这可能由于紫山药自身品种差异有关。[b][b]3 小结和讨论[/b][/b]3.1 DHEA提取条件优化 在DHEA测定前处理时,本实验曾根据李军等人的优化方法,采用甲醇-丙酮(6:4)超声提取、水浴蒸干、二氯甲烷多次萃取等主要工序对山药中DHEA进行提取,该方法提取效果较好,DHEA可以被较好的富集和检测。但是由于提取过程复杂,实验重复性和加样回收率较难控制。本实验采用甲醇、乙醇、甲醇-丙酮(1:1,[i]v/v[/i])等溶剂对山药样品进行超声1h提取,结果发现,四种溶剂提取效果没有明显差异,因此选用甲醇做为最终提取溶剂。 本实验采用的方法大大简化了山药中DHEA的提取过程,减少了有毒试剂的使用,缩短了提取时间,且提取率与李军的方法相比没有显著的差异。3.2 小结 本研究对山药中腺苷和DHEA成分的提取和测定条件进行优化,为山药质量标准建立和质量评价提供参考依据。另外,研究对包括野生、种植、驯化品种等不同来源山药中腺苷和DHEA指标含量进行测定,为山药品种的选育和驯化提供一定的研究基础。
看到这篇文章,很感兴趣,没能下载下来,下面是相关信息,欢迎有条件的上传附件,hoho:NMR技术在苯基—2’,3’,4’—三羟基苯基酮分子内活泼质子动态特性研究中的应用欧阳捷 北京师范大学分析测试中心 李敏一 北京师范大学分析测试中心 李维超 北京师范大学分析测试中心 邓志威 北京师范大学分析测试中心 摘 要:本文通过一维(ID)、二维(2D)核磁共振波谱法确定了苯基-2’,3’,4’——三羟基苯基酮分子结构,利用二维交换谱(2D EXSY)研究了该分子内活泼质子在二甲亚砜(DMSO)溶液中的动态特性,建立了活泼质子与溶液中水分子间的化学交换网络,并定量计算了化学交换的速率常数。实验结果表明:酚羟基氧形成分子内氢键使得它与自身的羟基氢的共价键被削弱,该活泼质子酸性增强,更容易发生反应。
[color=#444444]我需要用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]做羟基丙酮的外标线。但是羟基丙酮溶液是放在饱和碳酸钠里面的,而钠会对极性柱造成影响吧。想问该如何解决这个问题。[/color]
今天新建3,4-二羟基二苯甲酮的液相分析方法,试了好多流动相都没有改善峰拖尾的现象,请高手指点!用的C18柱
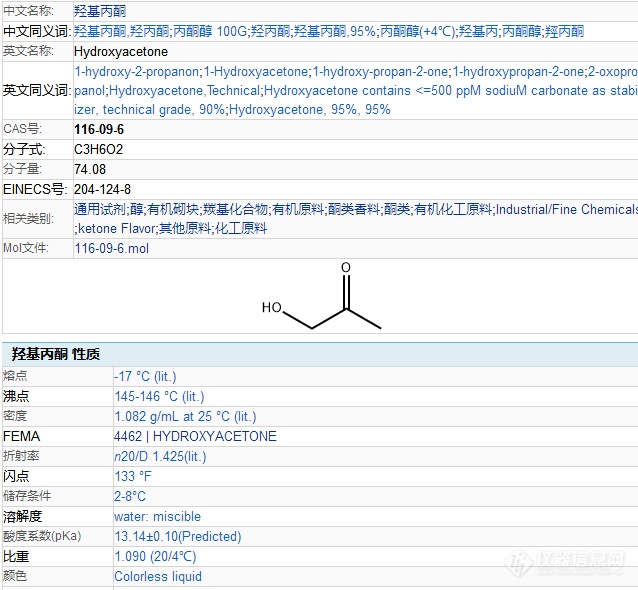
大家在分析食用香精时,是否经常看到有羟基丙酮这个物质,这不是直接加入的吧?[img=,638,590]https://ng1.17img.cn/bbsfiles/images/2021/10/202110090914118356_1121_2970225_3.png!w638x590.jpg[/img]
新手小白,刚接触GC-MS/MS,我用的是安捷伦7890A-7000B,柱子是DB-5的柱子,走的分别是羟基苯甲酸丁酯和2-氨基苯乙酮的标品,都是1ppm的,溶剂都是丙酮,升温条件50℃——220℃(15℃/min),不分流,然后不出峰。请各位大神多多指导!!!
最近在做羟基活泼氢的1H NMR实验,所用溶剂为DMSO-d6。被检测物质为二元醇,由于构型原因,结构中存在两种羟基,一个与相邻氧可形成分子内氢键,而另外一个则不能形成分子内氢键,想请教的是这样的两个羟基氢在DMSO-d6中,谁的化学位移会更大?另外,由于夏季空气湿度大,请问对于易吸水的样品所用溶剂为DMSO-6配样时,如何降低样品中的含水量。非常感谢!
本人现在在天津,要是天津有卖普通磷灰石或普通的羟基、碳基磷灰石的就最好了,如果是别处的话,也可以,但是我主要用实验室实验所用,所以用量可能不会很多,2kg应该足够了,如果有卖的请联系我,谢谢
请教在甘油氧化制备二羟基丙酮的反应中使用哪种液相色谱柱分析效果较好,我们使用了氨基柱,效果不理想,求指点。
为何核磁氢谱中的羟基和氨基活泼氢都是馒头形的峰?在所有化合物中氨基和羟基的峰都是馒头形的吗?
[color=#444444]请问4-羟基,2-丁酮的检测方法?,可以具体到用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的什么柱子,进样温度吗?[/color]
[size=3][font=宋体]请问各位大侠,怎么样在普通玻片上稳定、简单的修饰一层羟基([/font][font=Times New Roman]-OH[/font][font=宋体])。本人目前所用的方法是使用水虎鱼溶液([/font][font=Times New Roman]30%[/font][font=宋体]过氧化氢:浓硫酸[/font][font=Times New Roman]=1[/font][font=宋体]:[/font][font=Times New Roman]3[/font][font=宋体],[/font][font=Times New Roman]V:V[/font][font=宋体])浸泡[/font][font=Times New Roman]15-20min[/font][font=宋体]。但是总感觉不太好,好像没有形成羟基,或者说不够牢固。所以请教各位有没有其他其他方法代替之,万分感谢。[/font][/size]
如何对活泼氢(例如:羟基氢,氨基氢等)进行定量?
哪位同志有对羟基苯乙酮的滴定含量检测方法.我这里有一个方法,但总是滴不好,用甲醇钠溶液进行滴定,用二甲基甲酰胺进行溶解,用麝香草酚蓝作指示剂.目前存在的问题就是终点变化不明显.哪位有用到或碰到类似情况,都来说说吧.
我想求一篇文献上一个化合物的核磁数据,麻烦大家能帮帮忙,5-羟基-11-桉叶烷烯-1-酮(5-hydroxy-11-eudesmen-1-one,corymbolone)最好能把MS IR C-NMR H-NMR都给找一下,呵呵
[color=#444444]ESI 质谱条件下,M+H的二级产生含羰基的加氢峰,m/z 220,M+Na的二级碎片产生含羟基的加钠峰m/z 244,二者相差24。羰基氧和羟基氧与钠离子和氢离子的结合能力是怎样?[/color][color=#444444]难道钠离子更容易稳定含羟基离子?氢离子更容易稳定含羰基的离子?该怎么解释呢?[/color]
[color=#444444]如题[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析甲苯羟基化反应产物,内标物去什么好,用PEG柱子?谢谢[/color]
硅铝酸盐表面羟基化后,这个表面羟基的红外峰在什么位置?用透射法可能测出吗?还是用漫反射法比较好?
氢谱中羟基积分偏大,请问是怎么回事?
您好!我正在做1,3-二氯丙酮水解生成1,3-二羟基丙酮的实验,具体的方法是1,3-二氯丙酮在乙醇保护羰基的条件下加碱冰浴水解完后再加入盐酸中和,我用液相色谱分析过生成物,色谱条件为C18的的柱子,柱温25度,波段200,流动相甲醇(80%)的水溶液,检测后再2.5min有连续的峰出现,我想知道怎样能把这些峰分开,您能指导一下对于这样的物质我该用什么条件来进行分析么?我也单独分析过1,3-而羟基丙酮的纯品,在2.5min时有峰,峰面积占比96.7%。
2024年1月8日,根据《化妆品监督管理条例》,国家药监局批准发布《化妆品中非那雄胺等10种组分的测定》化妆品补充检验方法。[align=center][img=2.png,600,247]https://img1.17img.cn/17img/images/202401/uepic/e4bb2749-7324-4c9f-873e-29cc7146c224.jpg[/img][/align]非那雄胺为一种4-氮杂甾体化合物,能有效地减少血液和前列腺内的二氢睾丸酮,用于治疗前列腺增生症。但是[b]妇女、儿童和对本品过敏者禁用非那雄胺。[/b]本标准的起草单位为上海市食品药品检验研究院起草,验证单位为山东省食品药品检验研究院、广东省药品检验所和江西省药品检验检测研究院。[b]本标准规定采用高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-三重四极杆质谱联用仪测定化妆品中羟基氟他胺、非那雄胺、尼鲁米特、比卡鲁胺、氟罗地尔、氟他胺、环丙孕酮、醋酸环丙孕酮、度他雄胺、依立雄胺的含量,适用于膏霜乳类、液体类(水、油)、凝胶类、蜡基类、粉剂类化妆品中非那雄胺等10种组分的定性和定量测定。[/b]详细检测方法详见附件。附件:[img]https://img1.17img.cn/17img/images/202101/pic/3961461f-2698-4217-8a94-55eaaa9d6966.gif[/img][url=https://img1.17img.cn/17img/files/202401/attachment/55d31a89-80c2-4d2f-bcd4-c385e1eb14c0.doc]《化妆品中非那雄胺等10种组分的测定》[/url][来源:仪器信息网] 未经授权不得转载[align=right][/align]
如图化合物 文献报道酚羟基氢的位移为6.3,单峰,以氘代三氯甲烷为溶剂,而我用DMSO为溶媒 结果在靠近10的位置有一个单峰,请问可能是这个羟基峰么
有参加德国DRRR组织的护理产品中对羟基苯甲酸甲酯,对羟基苯甲酸乙酯,对羟基苯甲酸丙酯,对羟基苯甲酸丁酯,苯氧基乙醇,苯甲酸,山梨酸,甲醛,甲基异噻啉酮 能力验证的吗。可以加Q群39177650交流,或在这留言哦。测试轮编号2010206care Products-methylparaben, ethylparaben, propylparaben, butylparaben, phenoxyethanol, benzoic acid, sorbic acid , formaldehyde,methylisothiazolinone
NMR确定手性alpha-羟基酮的绝对构型[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=72023]NMR确定手性alpha-羟基酮的绝对构型[/url]
1928年C.V.拉曼实验发现,当光穿过透明介质被分子散射的光发生频率变化,这一现象称为拉曼散射。光照射到物质上发生弹性散射和非弹性散射。弹性散射的散射光是与激发光波长相同的成分。非弹性散射的散射光有比激发光波长长的和短的成分, 统称为拉曼效应。 拉曼光谱分析技术是以拉曼效应为基础建立起来的分子结构表征技术,其信号来源与分子的振动和转动。其谱线数目、位移值和谱带强度等直接反映了分子的构成及构象信息。拉曼光谱的应用范围遍及化学、物理学、生物学和医学等各个领域,对于纯定性分析、高度定量分析和测定分子结构都有很大价值。http://www.gogochina.cn/uploadPic/news/2011/8/23/201182310221232704.jpg图:大师手绘加官图陶瓷艺术花瓶 拉曼光谱技术是一种分析技术,由于它能够获得物质的分子信息而被应用于文物的分析中,特别是拉曼光谱作为无损的分析方法,可应用于文物的原位分析。 羟基是由氢和氧两种原子组成的一价离子团(-OH),即氢氧根。字中左边的羊表示氧,右边的表示氢,读音取氢(qing)之qi,取氧(yang)之韵母ang,合起来念——“抢”。 羟基在高温下不稳定,在常温、常压地表环境下是稳定的,其在陶瓷釉面中的含量与陶瓷烧造出窑时间成正比关系。羟基是鉴定古陶瓷真伪的定性、定量物质。 羟基鉴定方法原理及优点 原理(一)我们知道陶瓷在烧造过程中会发生一系列的物理和化学变化。其中比较重要的反应之一是釉料的脱水反应。反应过程如下: 1、100~110℃吸附水开始排出。 2、110~400℃其它矿物杂质所带入的水排出。 3、400~450℃结构水开始排出。 4、800~1000℃时排水结束。 由于中国古陶瓷的烧造温度均在1200℃以上(除陶器外),同样现代仿品的成瓷温度亦均在1280℃左右。因此从理论上可以得知瓷器在烧造结束后,其釉面中不存在结构水、离子水、吸附水等。我们对新烧造的陶瓷做了大量的检测,检测结果与理论推算完全相附。 (二) 新仿品和古代真品有着本质的区别,这是问题的关键。我们如果不能正确地理解仿品与真品之间的本质区别,也就无法找到正确的鉴定方法。 我们知道陶瓷的烧造过程是一个造岩过程或者成矿过程,真品的成岩过程和仿品的成岩过程有着本质的不同: 真品与仿品的烧制过程从理论上讲是相同的,但真品具有在地表条件下长期风化和水解的过程,而仿品却没有。真品在地表环境中长期变化的过程仿品是无法做到的。也就是说从理论上讲,真品的本质是无法仿制的。(地表环境指:馆藏环境,传世环境,墓葬环境,水下环境等现有古陶瓷所处的环境。) (三) 真品在地表环境下的化学反应 真品在地表环境下其釉面将会发生如下水解反应: Si-O-R + HOH → Si-OH + R+OH-Si-O-Si + OH- → Si-OH + Si-O- H+置换R+后形成硅凝胶薄膜 以上的反应生成物中既有氢氧根(羟基)、也有结构水。 上面的反应进行的很慢。 拉曼光谱——羟基古陶瓷真伪检测鉴定法的依据和原理是:现代仿品和古代真品的成岩过程有着本质区别,而时间是造成的这种区别的根本原因,造假者无法跨越时间所产生的鸿沟。时间所造成的古陶瓷的物理、化学变化是造假者无法仿制的。基于此,古陶瓷真伪拉曼光谱——羟基鉴定法的技术研发者把古陶瓷真品在地表环境下其釉面所产生的化学反应中生成的羟基作为古陶瓷鉴定的定性及定量物质。并运用世界上最先进的激光拉曼光谱测试仪( Renishaw Micro-Raman Spectroscopy System)进行相关检测,从而做出准确而科学的鉴定结论。 摘录自瓷器中国
如题,固体样品上的氢都是以羟基的形式存在的。这时候在红外上羟基特征吸收峰的个数和固体核磁氢谱上的峰的个数有对应关系么?简而言之,它俩是相同的么?
[size=4][color=#DC143C][font=黑体]同位素比质谱方法检测内源性类固醇雄烯二酮[/font][/color][/size]=========================================在所使用的禁用物质中,类固醇激素是较为普遍使用的一类药物。人体自身能合成与分泌的类固醇激素称为内源性类固醇激素,如攀酮。由于在检测方法上有一定难度,一些运动员选择使用内源性类固醇制剂以逃避兴奋剂检测。目前,兴奋剂检测实验室应用同位素比质谱分析方法检测内源性类固醇来源。13C和12C是碳元素在自然界中的天然同位素。有机化合物的来源不同,其同位素比(如13C与12C的比值)也不同。人体自身分泌的类固醇与相同化学结构的类固醇制剂的同位素比不同。应用同位素比质谱分析技术可以测定化合物13C与12C的比值,同位素比用δ(‰)值表示。根据仪器的分析流程和组成部分,本文方法称为[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]/燃烧炉/同位素比质谱([url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/C/IRMS)方法。该方法在兴奋剂检测中的应用时间较短,文献方法较为繁琐,本文建立了快速灵敏的[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/C/IRMS分析方法。-------------------------------------------------试验材料与方法1. 试剂和对照品试剂:β-葡萄糖醛酸酶,Sigma;其余均为国产分析纯试剂。对照品:睾酮(缩写T)、雄酮(缩写An)、本胆烷醇酮(缩写Etio)、5α-雄烷-3α,17β-二醇(缩写5α-diol)、5β-雄烷-3α,17β-二醇(缩写5β-diol)、孕二醇(缩写PD)购自Sigma公司。2. 样品两名健康志愿者,一名男性40岁,尿样为sample 1;一名女性38岁,尿样为sample 2,均没有服用任何药物。收集其晨尿为阴性对照尿。阳性尿样为世界反兴奋剂机构水平考试所用尿样来自兴奋剂检测中心。3. 仪器[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]/燃烧炉/同位素比值质谱仪(HP6890/DELTA PLUS,Finnigan);高效液相色谱仪(Waters2796,检测器:Waters2996 PAD,自动收集器:Waters Fraction Collector Ⅲ);Anilent 5973i[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱联用仪。4. 方法4.I [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/C/IRMS操作条件色谱柱:HP5毛细管色谱柱,25m×0.2mm i.d.×0.3μm;柱流速:1mL/min(室温);升温程序:60 ℃(2min)一50 ℃/min→255℃一2.5℃/min→280℃(6.5min);进样口温度:260℃;燃烧炉温度:960℃;质谱离子源:EI;参考气:CO2,1.8V。4.2 高效液相色谱仪操作条件色谱柱:ZQRBAX SB-C18(4.6mm×250mm,5μm);流动相:水-乙睛,梯度洗脱(0-18min:乙睛从30%→100%);流速1mL/min;柱温:室温。4.3 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MSD操作条件色谱柱:HP-1毛细管色谱柱,25 m×0.2mm i.d.×0.11μm;柱流速:1 mL/min (室温);升温程序:150 ℃(1min一5℃/min→200℃一30℃/min→310℃(10min)。4.4 样品预处理取尿样2mL,加人1Ml0.2mol pH=7.0的磷酸盐缓冲液和10μLβ-葡萄糖醛酸酶(5000 IU)混匀,在55℃恒温水浴中培养3h,取出后加pH=8.8的碳酸盐固体缓冲剂约100mg 和5mL叔丁基甲醚,振荡萃取,离心后,取出上层有机溶液,在加热的情况下,用氮气吹干,加人50μL甲醇溶解残渣,备用。将上述甲醇溶液置HPLC仪上,依前述色谱条件分离,分段收集流出液,确定收集时间程序。分别将流出组分用氮气吹干,加人50μL环己烷,备用。4.5 对照品溶液的制备分别配制对照品睾酮、雄酮、本胆烷醇酮、5α-雄烷-3α,17β-二醇、5β-雄烷-3α,17β-二醇,孕二醇的甲醇溶液,浓度为1mg/mL。4.6 样品测定4.6.1 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MSD 分析依上述[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/MSD仪器操作条件,取样品溶液及对照品溶液进行全扫描,扫描范围m/z 20~450,选择待测物的特征离子,获得SIM图。经对样品中与对照品有相同保留时间的峰进行质谱分析,及与标准品质谱图的对比,确定待测样品的组成。4.6.2 [url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/C/IRMS分析依上述CC/C/IRMS仪器操作条件,对处理后的样品进行[url=https://insevent.instrument.com.cn/t/Mp]gc[/url]/C/IRMS分析,测得内源性类固醇激素的δ值。
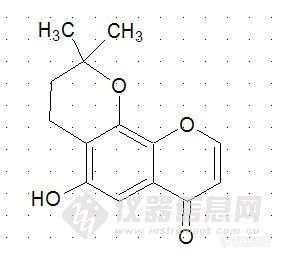
http://ng1.17img.cn/bbsfiles/images/2011/02/201102240945_279159_2238889_3.jpg这个支链 可以和8位羟基成环(图就是和8位成环后) 也可以和 6位羟基成环 但是怎么去认定具体是和那个成环呢? 环上和氧相连的碳没有氢 那么做HMBC 就不可能和母核出相关峰, 紧靠碳谱的化学位移能说明问题吗?还是有其他的什么办法?谢谢各位浏览!