【作者】 马铭研; 周丹丹; 于治国;【机构】 沈阳药科大学药学院; 沈阳药科大学药学院 辽宁沈阳110016; 辽宁沈阳110016;【摘要】 目的:比较研究大鼠尾静脉注射与局部皮肤给予酮咯酸氨丁三醇的药动学行为。方法:采用HPLC法,色谱柱:Dia-monsil C18柱(200mm×4.6mm,5μm);流动相:甲醇-水-三乙胺-冰醋酸(80∶19.9∶0.02∶0.08);流速:1.0mL.min-1;柱温:30℃;检测波长:313nm。结果:酮咯酸氨丁三醇在0.2~100mg.L-1范围内与峰面积呈良好的线性关系(r=0.999 0),日内RSD为2.3%~5.1%,日间RSD为2.2%~12.2%,萃取回收率为86.8%~96.2%,注射剂和凝胶剂的T1/2α分别为(0.4±0.3)h,(2.9±2.6)h;T1/2β分别为(2.7±2.0)h,(9.0±8.5)h。结论:本试验建立的方法操作简单,方法灵敏、特异,结果准确。酮咯酸在大鼠体内药动学行为符合二房室模型;外用给药透皮吸收良好。【谱图】 http://ng1.17img.cn/bbsfiles/images/2012/08/201208142206_383898_1609970_3.jpg
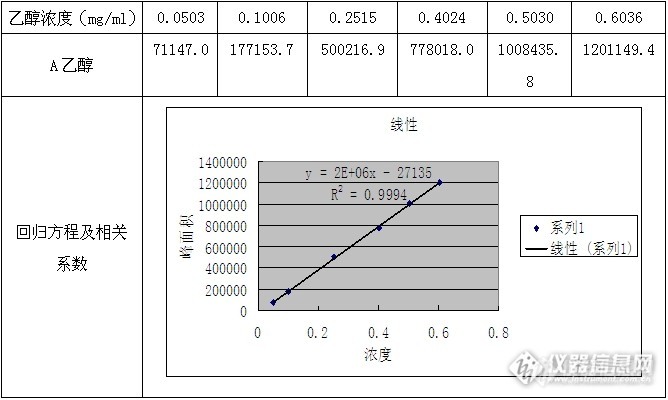
因工作需要,需要对酮咯酸氨丁三醇中的残留有机溶剂乙醇和1,2-二氯乙烷进行方法学研究,乙醇为三类溶剂,药典规定限度为0.5%,1,2-二氯乙烷为一类溶剂,药典规定限度为0.0005%,因为1,2-二氯乙烷的限度较低,在FID检测器下很难检测,故需要用到ECD检测器检测1,2-二氯乙烷。 方法学研究为,方法一,乙醇的检测;方法二,1,2-二氯乙烷的检测。1.1方法概述应用GC外标法对酮咯酸氨丁三醇中的残留有机溶剂乙醇进行定量分析。载气:氮气;检测器:FID。1.2对照品及样品名 称来源批号酮咯酸氨丁三醇样品某医药企业120201乙醇西陇化工股份有限公司11070111.3仪器和仪器参数气相色谱仪型号:岛津公司GC-2010天平型号:梅特勒公司XS105顶空进样器型号:DANI公司 HSS86.50色谱柱类型:DB-624 规格30m×0.53mm×3.0µm 载气:氮气 柱温:50 ℃检测器:FID检测器温度: 250℃;进样口温度: 200℃;流速: 3.0 ml/min;进样量: 1.0ml;分流比: 10:1样品盘平衡温度: 80℃;定量环温度: 90℃;传输线温度: 100℃;样品盘平衡时间: 30min1.4溶液配制对照溶液:准确称取乙醇50mg于100ml容量瓶中,用水稀释定容至刻度,摇匀,精密移取3ml置于20ml顶空瓶中,密封即得对照溶液。准确称取样品0.3g,置于20ml顶空瓶中,加水3.0ml,密封即得供试品溶液。1.5验证内容及结果1.5.1系统适用性试验方法:取酮咯酸氨丁三醇溶残对照溶液,依法连续进样5次,记录乙醇峰面积的相对标准偏差(RSD%)。乙醇峰面积的相对标准偏差RSD应不大于10%,乙醇的理论塔板应不小于10000,乙醇的拖尾因子应不大于1.5。结果:序号12345RSD%A乙醇[/si
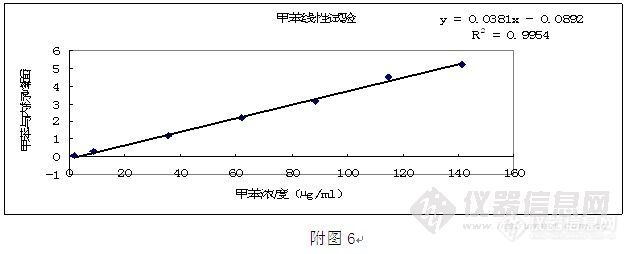
维权声明:本文为lunanjituan原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。酮咯酸氨丁三醇残留溶剂方法学验证(FID)一、方法:甲醇、乙醇、二氯甲烷、乙酸乙酯、乙酸、甲苯 称取异辛烷约20mg,精密称定,置50ml量瓶中,加DMF溶解并稀释至刻度,摇匀,作为内标贮备液;依次称取甲醇约300mg、乙醇约500mg、二氯甲烷约60mg、乙酸乙酯约500mg、乙酸约500mg、甲苯约89mg,均精密称定,置于50ml量瓶中,加DMF溶解并稀释至刻度,摇匀,精密量取溶液5ml,置50ml量瓶中,加DMF溶解并稀释至刻度,摇匀,作为对照贮备液;称取酮咯酸氨丁三醇约1.0 g,精密称定,置10ml量瓶中,加DMF适量使其溶解,加1.0 ml内标贮备液,加DMF稀释至刻度,摇匀,作为供试品溶液;精密量取对照贮备液5.0 ml,置10ml量瓶中,加1.0ml内标贮备液,用DMF稀释至刻度,摇匀,作为对照溶液。照气相色谱法(中国药典2005年版二部附录V E)和有机溶剂残留量测定法(中国药典2005年版二部附录VIII P第一法),用DB-624毛细管色谱柱(30m×0.53mm×3.0µm ),FID检测器,载气为氮气,进样口温度200ºC ,流速1.5ml/min,分流比5:1;柱温在40ºC下保留5分钟,然后以10ºC/min的速率升至200ºC,至少保留9分钟;检测器温度250ºC。分别精密量取上述两种溶液各1.0µl进样分析,记录色谱图,按内标法以峰面积计算,含甲醇、乙醇、二氯甲烷、乙酸乙酯、乙酸及甲苯分别不得过0.3%、0.5%、0.06%、0.5%、0.5%、0.089%。二、仪器与试药 岛津GC-2010气相色谱仪,FID检测器。甲醇(分析纯,国药集团化学试剂有限公司,批号:T20080109)、无水乙醇(分析纯,汕头西陇化工厂有限公司,批号: 0808141)、二氯甲烷(分析纯,汕头西陇化工厂有限公司,批号:0710311)、乙酸乙酯(沈阳瑞丰精细化学品有限公司,批号:20050626)、乙酸(上海试剂一厂,批号:20071201)、甲苯(天津瑞金特化学品有限公司,批号:20060704)、N,N-二甲基甲酰胺(分析纯,天津四友生物医学技术有限公司,批号:070914101)、异辛烷(分析纯,TEDIA company INC.USA,批号:506173)。三、色谱条件 色谱柱:DB-624毛细管气相色谱柱(30m×0.53mm×3.0µm )。FID检测器,载气为氮气,进样口温度200ºC ,流速1.5ml/min,进样量:1.0µl,分流比5:1;柱温:在40ºC下保留5分钟,然后以10ºC/min的速率升至200ºC,至少保持9分钟;检测器温度250ºC。尾吹:30ml/min。各峰的理论塔板数均应不低于10000,各峰的拖尾因子均应不大于2.0,各峰间的分离度均应不小于2.0。四、气相色谱方法学验证 照有机溶剂残留量测定法测定。根据合成路线,对甲醇、乙醇、二氯甲烷、乙酸乙酯、乙酸及甲苯等残留溶剂进行了方法学研究。1、专属性试验1.1空白基线 依柱温设定条件,得基线GC色谱图。见附图。1.2空白溶剂 精密量取DMF1.0µl 注入GC,得空白溶剂GC色谱图。见附图。1.3甲醇 称取甲醇约15mg,置于50ml量瓶中,加DMF溶解并稀释至刻度,摇匀。精密量取1.0µl 注入GC,得甲醇GC色谱图。见附图。1.4乙醇 称取乙醇约25mg,置于50ml量瓶中,加DMF溶解并稀释至刻度,摇匀。精密量取1.0µl 注入GC,得乙醇GC色谱图。见附图。1.5二氯甲烷 称取二氯甲烷约30mg,置于50ml量瓶中,加DMF溶解并稀释至刻度,摇匀,量取溶液1ml置10ml量瓶中,加DMF稀释至刻度,摇匀。精密量取1.0µl 注入GC,得二氯甲烷GC色谱图。见附图。1.6乙酸乙酯 称取乙酸乙酯约25mg,置于50ml量瓶中,加DMF溶解并稀释至刻度,摇匀。精密量取1.0µl 注入GC,得乙酸乙酯GC色谱图。见附图。1.7乙酸 称取乙酸约25mg,置于50ml量瓶中,加DMF溶解并稀释至刻度,摇匀。精密量取1.0µl 注入GC,得乙酸GC色谱图。见附图。1.8甲苯 称取甲苯约45mg,置于50ml量瓶中,加DMF溶解并稀释至刻度,摇匀,量取溶液1ml置10ml量瓶中,加DMF稀释至刻度,摇匀。精密量取1.0µl 注入GC,得甲苯GC色谱图。见附图。1.8异辛烷(内标) 称取异辛烷约20mg,置于50ml量瓶中,加DMF溶解并稀释至刻度,摇匀。精密量取1.0µl 注入GC,得异辛烷GC色谱图。见附图。1.9 对照溶液 依法配制对照溶液,精密量取1.0µl 注入GC,得对照溶液GC色谱图。见附图。由色谱图可知:待测各残留溶剂间的分离度均大于2.0,相互之间没有干扰。1.10 对照与样品混合溶液 依法配制对照溶液和样品溶液,并将二者按1:1相互混合,摇匀。精密量取1.0µl 注入GC,得对照与样品混合溶液GC色谱图。见附图。由色谱图可知:测定样品溶液中的潜在杂质对待测残留溶剂样品无干扰。2、系统适用性试验精密量取对照贮备液5.0ml,置10ml量瓶中,加1.0ml内标贮备液,加DMF稀释至刻度,摇匀,作为对照溶液。取对照溶液,依法连续进样六次,记录色谱图,记录各残留溶剂的保留时间、拖尾因子、理论塔板数、峰面积,计算各溶剂与内标峰面积的比值及RSD。结果见表1~7。http://ng1.17img.cn/bbsfiles/images/2010/12/201012091040_265708_2961690_3.jpghttp://ng1.17img.cn/bbsfiles/images/2010/12/201012091041_265709_2961690_3.jpg[img

http://ng1.17img.cn/bbsfiles/images/2015/03/201503301532_540105_1610895_3.jpg色谱条件:色谱柱: Diamonsil Plus C18-B 250*4.6 mm,5 μm(Cat#: 99409) 流动相: 0.3%(g/v)醋酸铵:甲醇=80:20 流速: 1 mL/min 柱温: 30 ℃ 检测器: UV 270 nm 进样量: 20 μL样品前处理: 精密量取本品适量,用流动相定量稀释制成每1 mL中约含氨丁三醇奥扎格雷56 μg的溶液。http://ng1.17img.cn/bbsfiles/images/2015/03/201503301551_540111_1610895_3.jpg
用[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质[/color][/url]做VOC,用的WAX柱子60米长,内径0.32mm,膜厚1um,用的是标液是甲醇溶剂,热脱附进样,分流比40:1,初温35℃,8℃/min升至80℃保持2分钟,10℃/min升至115°保持2分钟,12℃/min升至160℃保持3分钟。无论条件怎么优化,都不能将乙酸乙酯,甲醇,丁酮这三个峰完全分离开,有人能提供一下优化的方法吗?[img]https://ng1.17img.cn/bbsfiles/images/2019/04/201904032334478103_9384_3416992_3.png[/img]
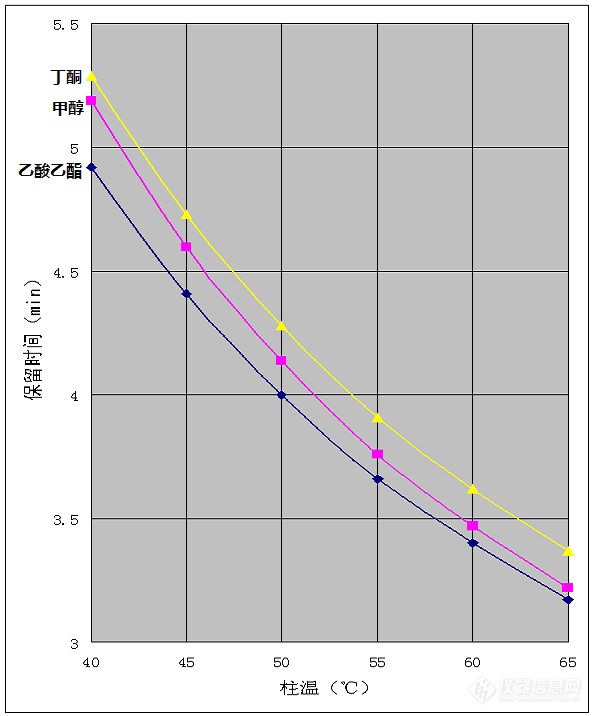
溶剂残留分析是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的重要应用之一,在药品、食品、包装等领域都是必测的项目。常见溶剂中涉及到的检测目标物经常有乙酸乙酯、甲醇、丁酮,以及二甲苯异构体这几项。最近看到 @m3091333、@p3109800、@Insm_c1196d2b 等多人发帖子讨论相关问题,我从原理上进行了一些解释,但终究纸上谈兵,于是找别的实验室要了这几种试剂,用实践检验了一下。首先,如果二甲苯异构体不要求分离,用624柱可以很容易的解决问题,这里就不讨论了。如果要求乙苯、对二甲苯、间二甲苯、邻二甲苯四种异构体分离,用624柱是无法完成的。因为二甲苯异构体色散力差异非常小,只能靠诱导力的差异分离,不同异构体在强极性柱上的极化率不同,乙苯极化率最低,其次是对二甲苯、间二甲苯,邻二甲苯极化率最大,出峰时间也随极化率的增加而延长。而624柱的极性比较弱,不能产生足够的极化作用,特别是对二甲苯与间二甲苯的极化差异非常小,无法实现分离。这个问题是由分子结构决定的,无论怎么调节色谱条件都不能解决。要想解决只能换强极性柱,常见的就是聚乙二醇柱,包括各种wax柱和FFAP柱等。三氟丙基柱也是强极性的,可以分离二甲苯异构体,但是这种柱很少使用。在聚乙二醇类的色谱柱上,乙酸乙酯、甲醇、丁酮三种目标物分离困难,各种类型的聚乙二醇柱选择性略有差异,但这三种物质都是较为接近的,想要分离是不太容易的。但是这三种物质与聚乙二醇固定相之间的作用力存在本质上的差异,因此通过调整柱温条件是可以分离的。下面三幅图是用60米*0.53mm*1um的INNOWAX柱分离乙酸乙酯、甲醇、丁酮的效果,柱温分别是40℃、50℃、60℃。[img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157168864_5041_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157170984_7926_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157172914_736_2204387_3.png!w690x796.jpg[/img]图中很明显,柱温低时甲醇与丁酮出峰时间接近分不开,高温时甲醇与乙酸乙酯出峰时间接近分不开,温度适中时三者可以实现分离。虽然未达到基线分离,但分离度都超过1,用来定量是完全可以的。这是找别人借的一根旧柱子,柱效只有4万塔板,如果是新柱子柱效应该能达到七八万塔板,分离度肯定更高,如果是0.32mm口径的柱子分离就更没问题了。要强调的是,能够实现分离的条件并不是完全靠盲目尝试获得的。我们看一看三种目标物的保留时间随柱温的变化就能发现其中的规律,见下图:[img=,594,716]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022156374904_6999_2204387_3.png!w594x716.jpg[/img]图中可以看出,三种目标物的保留时间都是随温度升高而减小的,但是减小的幅度却并不相同。甲醇的保留时间随温度升高而减小的幅度明显大一些。这是因为甲醇具有羟基,与聚乙二醇固定相的相互作用力以氢键为主,氢键的强度随温度升高而迅速减弱。而乙酸乙酯、丁酮与聚乙二醇固定相的作用力都是以诱导力和取向力为主,这种力是由分子偶极矩决定的,受温度的影响要小一些。甲醇峰位置在乙酸乙酯与丁酮之间,温度升高时保留时间都减小,但甲醇减小更多,于是甲醇与乙酸乙酯靠的更近,与丁酮的分离度提高。温度降低时保留时间都增大,但甲醇增大更多,于是甲醇与丁酮靠的更近,与乙酸乙酯的分离度提高。用其他的柱子,如DB-wax或者FFAP时,各组分之间的相对位置会有差别,甚至有时出峰顺序都会变,但是保留时间随温度变化的这种规律仍然是适用的。所以遇到分不开的情况,一定不要盲目的乱试一通,也不用盲目的换柱子,一定要把问题想明白,有针对性的优化条件。最后要强调的是,这里虽然是以溶剂检测为例讨论了如何只用一根柱子就实现分离,但实际样品很复杂,并不是每次都能通过这种优化实现全部分离目的。所以色谱实验室配备多种不同极性的色谱柱是非常重要的。特别是做复杂样品时,即使谱图上看起来分离不错,最好也能用另外一种柱子进行一次验证,以免实际样品中有干扰物共流出,造成假阳性。
[font=&][size=16px][color=#333131]可以做氨丁三醇(三羟甲基)氨基甲烷,杂质峰定性的检测机构请看过来[url=https://www.woyaoce.cn/helptest/detail-dcb6af847ef4628458ecdf6d407180cd.html]点击查看详情[/url][/color][/size][/font]
利用顶空[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法测定甲乙丙丁戊5种醇,分别测试了下正戊烷、正庚烷、丙酮、乙酸乙酯都能够与这5种醇分开,乙酸乙酯我已经选来做稀释剂,其他三种合适做内标物质吗?
热解吸做voc中丁酮和甲醇峰分不开?用的是wax柱子,请问各位老师还能怎么分离开?第一个峰是丙酮,第二峰是乙酸乙酯,第三个峰是溶剂甲醇峰覆盖目标丁酮。[img]https://ng1.17img.cn/bbsfiles/images/2018/11/201811171633448269_6611_3333718_3.png[/img]
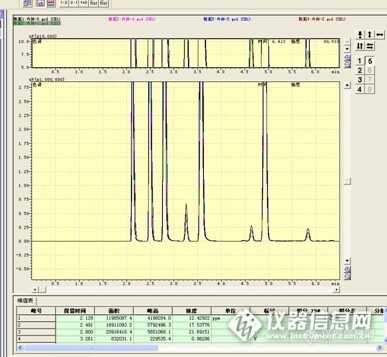
求助一下, ,我这个用程序升温法测甲醇,丙酮,正丙醇(内标) 丁醇 ,丁酯。 110℃ 2.5min 然后25℃/min升到160℃,并保持1min ,,为嘛每次都有三个小峰。如下图片
如果同时想做苯,甲苯,乙酸乙酯,乙酸丁酯,丙酮,丁酮,三氯乙烯,二氯乙烷,环己酮的话应该悬着什么样的色谱柱,什么条件.......如果实在做不到一起的话,最合适的搭配,方法,条件是什么???.
FID检测器,用水做溶剂溶解4羟基2丁酮和1,3-丁二醇时可以分开,然后用乙酸乙酯作溶剂时,只有一个峰了。条件是60℃,10℃/min升温220℃。
離子源卸調後用甲醇洗後發現全氟三丁氨質譜圖中的770和866太低,高度接近峰底,遠遠沒有背景的119高,測試10溴deca出現上面相似 問題600以上峰都很低,不知道是離子遠電壓問題還是檢測器問題,燈絲也換過還是如此,求教大俠。!!
用甲醇钠制得丁酮烯醇钠,计算收率的时候用什么方法来确定干燥品中丁酮烯醇钠的占比是多少呢?
小弟在做的溶剂标样:分别有甲醇,乙醇,异丙醇,乙酸乙酯,正丁醇,丁酮,甲苯,甲醚,甲基环乙烷,正丙酯,丁酯。。做标样的时候是这11种,但是出峰只出来9个,没有正丁醇和甲醚。。。然后单独进样的时候,正丁醇,正丙酯,甲醚的出峰时间很接近,用三种混的时候进样,却只有一个峰。不明白为什么进了三种只出了一个峰,是分离不开还是什么问题???柱温是70度。。检测器进样器都180度,毛细管柱50*25*25。。请各位大神帮忙..怎么分辨两种物质性质很相近?比如正丁醇,正丙酯,甲醚这三种为什么会那么近?
请教各位 样品是己酸乙酯 丙三醇 、2,3-丁二酮,要测定他们的重金属含量,怎样前处理 谢谢 ! 谢谢

今年扩项 HJ734-2014,从收集的资料来看乳酸乙酯是不稳定的,问了一些做过的都说乳酸乙酯不好做,论坛帖子里也有这方面的讨论。我试验发现乳酸乙酯、甲醇、组合三在热脱附过程中发生一些化学反应! 收集的一些乳酸乙酯资料:[img=,690,223]https://ng1.17img.cn/bbsfiles/images/2020/09/202009081617462892_5801_2103464_3.png!w690x223.jpg[/img] [img=,690,157]https://ng1.17img.cn/bbsfiles/images/2020/09/202009081619363949_7837_2103464_3.png!w690x157.jpg[/img] 买了24种HJ734 VOC混标,甲醇水9:1溶剂,甲醇稀释后 直接液体进样发现乳酸乙酯峰挺高的,没有发生明显的反应,下图21.6min为乳酸乙酯[img=,690,364]https://ng1.17img.cn/bbsfiles/images/2020/09/202009081622552286_9904_2103464_3.png!w690x364.jpg[/img] 然后用组合三,甲醇为溶剂配制含乳酸乙酯的24种混合HJ734标液。这里配制方式有好几种:1.用24种混标甲醇水9:1溶剂的,用甲醇稀释。2.用22种混标甲醇水9:1溶剂的,加色谱纯乳酸乙酯,苯甲醛再用甲醇稀释。3.用22种混标纯甲醇溶剂的,加色谱纯乳酸乙酯,苯甲醛再用甲醇稀释。取1μl标液进组合三,在氮气80ml/min吹扫5min取下作为标准管。 [url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]:赛默飞Trace1300-ISQ,热脱附是 PE的 ATD350色谱条件 VF-624ms柱(60m*0.25mm*1.4μm)40℃保持5min以6℃/min至100℃以15℃ /min至140℃保持5min 以15℃ /min至220℃保持2min。热脱附条件:干吹1min,一级二级脱附都是300℃,冷肼-30℃,一级脱附11min二级脱附6min,进口分流30ml/min 脱附30ml/min,出口分流9 ml/min,色谱柱流量1.3 ml/min 热脱附发现无论是哪种配制方式,也无论怎么改变条件都发现乳酸乙酯峰小,发生了反应。在最初的色谱图发现了乙醇,而且乙醇随着标液浓度增大而增大,这个乙醇是反应的副产物: [img=,690,459]https://ng1.17img.cn/bbsfiles/images/2020/09/202009081653460004_8158_2103464_3.png!w690x459.jpg[/img]在甲苯前面有两个连着的峰 17.99min是丙酮酸甲酯[img=,690,431]https://ng1.17img.cn/bbsfiles/images/2020/09/202009081654475162_4856_2103464_3.png!w690x431.jpg[/img]18.07min是乳酸甲酯:[img=,690,432]https://ng1.17img.cn/bbsfiles/images/2020/09/202009081656071579_6357_2103464_3.png!w690x432.jpg[/img] 此外乳酸乙酯旁边还发现了:20.19min是丙酮酸乙酯[img=,690,443]https://ng1.17img.cn/bbsfiles/images/2020/09/202009081656566850_3396_2103464_3.png!w690x443.jpg[/img] 20.26min才是乳酸乙酯!确实比其他峰小了好多,相对响应比液体直接进样小了好多是反应的证明![img=,690,437]https://ng1.17img.cn/bbsfiles/images/2020/09/202009081657580589_4347_2103464_3.png!w690x437.jpg[/img] 用组合三还进了一针甲醇空白,改变全扫描范围发现还有残留甲醇。 根据以上推断:甲醇中乳酸乙酯标液进组合三吹扫后,还有残留甲醇,乳酸乙酯在热脱附过程中发生酯交换反应和氧化反应,甚至还有二级反应! 部分乳酸乙酯与甲醇反应生成乳酸甲酯与乙醇!部分乳酸甲酯被氧化成丙酮酸甲酯!乳酸乙酯本身也会被部分氧化成丙酮酸乙酯! 酯交换反应式:[img=,690,163]https://ng1.17img.cn/bbsfiles/images/2020/09/202009081711230387_9047_2103464_3.png!w690x163.jpg[/img] 氧化反应可能是系统有微量氧气把乳酸乙酯或乳酸甲酯的羟基氧化成羰基! 先后试过三家不同厂家的组合三,发现了同样的反应! 此外如果采用乙腈中乳酸乙酯再用甲醇稀释,同样也会发生反应!因为乳酸乙酯又遇见了甲醇。 结论:乳酸乙酯、甲醇、组合三在热脱附过程中可能会发生酯交换反应和氧化反应,所以不稳定!
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=92808]丙酮 乙醇 氨的物理性质[/url]
请教一个问题:三异丙醇胺和盐酸反应生成水吗?如何确定?
1、现在已经试方法快试4个月了,实验室的色谱柱是Agilent XDB-C18色谱柱,检测条件试过药典规定的磷酸缓冲液:甲醇的,试过pH6.5,2.5,还试过甲醇:水的各种比例,如20:80,30:70,50:50等,试过水+三乙胺调节PH到7.5,8等。但结果一直不理想,重现性也不好,想请教下做过氨甲环酸检测的朋友们有没有试过的比较好的方法可以指点一下?2、最开始用氨甲环酸跑标曲,色谱柱检测氨甲环酸达到的信号值都很低20、30左右,而且样品在4度冰箱保存一两天后再拿出来检测就不是出单峰了,多了很多杂峰。这是因为氨甲环酸见光分解还是什么样的原理呢怎么能让样品更稳定呢?(氨甲环酸结构好像也挺稳定的)还是因为放冰箱带进去杂质?还是我冲柱子时间短了没冲平?3、前一段时间用氨甲环酸样品检测信号值能到200左右,这段时间再用那个样品现配现用,不管是跑氨甲环酸标品还是之前买的氨甲环酸样品出峰都不好,现在都是信号值到10左右的杂峰,而且有多个(3至5个)峰(感觉都没出样品峰,是不是可以尝试[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]先分辨一下每个峰是什么物质?)这会是色谱柱出问题了吗?还是我平衡时间不够?求求比较懂的各位可以指点一下,真的在努力学HPLC了,结果一直不尽人意,想请问下有没有用过同型号色谱柱跑出来的朋友们可不可以分享一下经验?或者使用过多种柱子检测的朋友们有没有推荐的柱子和方法([url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]或[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]的方法都可以)?
产品偏苯三酸三辛酯中含有微量异辛醇(浓度小于100ppm)用气质如何精确定量其中微量的异辛醇?异辛醇做标准曲线,用丙酮还是甲醇合适,谢谢
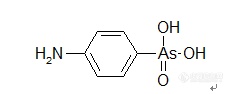
【中文名称】氨苯胂酸;对氨苯胂酸;阿散酸【英文名称】arsanilic acid【结构或分子式】 http://ng1.17img.cn/bbsfiles/images/2012/02/201202272049_351337_1855403_3.jpg【相对分子量或原子量】217.06【毒性LD50(mg/kg)】 雄小鼠经口1710,雌小鼠1330。【性状】 白色或微黄色结晶粉末,几乎无臭。【溶解情况】 在水或乙醇中微溶,在氯仿或乙醚中不溶,在氢氧化钠溶液中溶解。易溶于热水和甲醇。【用途】 抗菌剂,饲料添加剂,用于猪、鸡促进生长。【制备或来源】 由苯胺与砷酸为原料制取。【包装及贮运】 应避光、密闭,在干燥处保存。【生产单位】略
请教氨水与碱式碳酸铜会生成络氨铜吗?溶液是否是深蓝色,本人实验,加入一定量的氨水至碱式碳酸铜完全溶解,但一段时间后有沉淀产生,是氨水加入过多还是过少?还是碱式碳酸铜有杂质?(本人用的是AR)这样的反应能否完全生产络合物而不会出现氧化铜或者其他铜化合物。
我用的极性柱测甲醇丁醇乙醇异丙醇只出三个峰,50度的程序升温,这是什么原因呢
我们用的的万通 808titrando-1仪器,滴定液盐酸,测试溶液是含氨的溶液,滴定曲线有两个负的突跃,在测定有时仪器默认为第一个为终点,但我们的认为第二个是终点,现在我们要在仪器终点确认参数设置为第二个为终点(验证后实施)。现在的问题是:此滴定是否有两个突跃,其原理是什么;是否第二个突跃为终点?
关于乙醇、乙酸乙酯、甲基异丁酮、甲苯、丁酸乙酯、异戊酸乙酯、乙酸-2-甲基-1-丁醇酯、己酸乙酯、异戊酸异戊酯、异丁酸异戊酯、己酸烯丙酯、紫罗兰酮、肉桂酸异丙酯13种物质的气相方法,这13种物质能否一针全部出来,用什么柱子合适,FID对它们是不是都有响应?希望各路高手路过能留下点意见和相关资料,不胜感激!
请教一下,三乙醇氨有什么用途?是否可以用于黄金的冶炼,起什么作用?是否还是一种植物生长调节剂?先谢谢各位了。
用c18柱测氨基酸应选流动相是什么?茚三酮显色液:称取85mg 茚三酮和15mg 还原茚三酮,用10mL 乙二醇甲醚溶解。
用乙醇一步法制乙酸乙酯的时候会产生丁酮难以分离~想问一下有什么好的方法介绍一下么?[em0808]
[color=#444444]本人在做关于一株梭菌发酵产丁醇的实验,主要测乙酸丁酸乙醇丁醇,我实验室的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]是一台十分古老的仪器,型号是福立9710型,手动进样的,我用的条件是柱箱温度90℃,检测器温度180℃,进样器180℃,载气为N2,流速30 mL/min,可是并不知道程序升温如何设定,走出来的峰不是平头峰就是拖尾特别严重,而且各个组分还分不开。有没有大神指导一下各个条件该如何设置,最终走出来的样会特别好看的。。。我本人想到一个方法,就是由于我样品含有乙酸丁酸乙醇丁醇,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]分离这四个物质难度较大,我可以液相上乙酸丁酸的,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]就检测乙醇丁醇,就是这样太繁琐了,0求大神帮我解决!!~~[/color]