【序号】:8【作者】: 程珍华【题名】:壳聚糖的羟丙基化、季铵盐化修饰及其衍生物的结构与性能研究【期刊】:浙江工业大学【年、卷、期、起止页码】:2018【全文链接】:[url]https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CMFD&dbname=CMFD201801&filename=1017246430.nh&uniplatform=NZKPT&v=Sj53myVTRIHhcZwzkOJsh3h3El6tssU6oZpVOnZImBUkxEECiiP2f-I53b5DxJ2G[/url]
【序号】:5【作者】: 宓英其【题名】:不同阴离子化2-羟丙基三甲基铵类壳聚糖的制备、活性及性能研究【期刊】:中国科学院大学(中国科学院烟台海岸带研究所)【年、卷、期、起止页码】:2019【全文链接】:https://kns.cnki.net/kcms/detail/detail.aspx?dbcode=CMFD&dbname=CMFD201902&filename=1019909665.nh&uniplatform=NZKPT&v=Tb5dxN6PyXtwEP263qxVa4fkRlfspmQqPGAe_cjbNcQGjz0XyrMMcWgIhyqvAxg1
帮同学问的,根据文献操作,用紫外分光光度法测壳聚糖脱乙酰度,原本的样品测的数据是正常的,但是对壳聚糖改性之后,每次测得的吸光度都是负值,如果稀释倍数减小才能得到正值,所以脱乙酰度就不知道怎么测了。。。

[align=center][img=,600,457]https://ng1.17img.cn/bbsfiles/images/2019/09/201909251626050517_8200_932_3.jpg!w500x381.jpg[/img][/align]我们今天给大家带来的是羟丙基-β-环糊精有关物质的测定。羟丙基-β-环糊精是应用最广泛的环糊精衍生物之一。主要应用于食品、医药、化妆品行业。1、在食品、香料领域,可提高营养分子的稳定性和长效性,可掩盖或矫正食品营养分子的不良气味和口味,可改进生产工艺和产品品质。2、在化妆品原料中用作稳定剂、乳化剂、去味剂等,可降低化妆品中有机分子对皮肤粘膜组织的刺激,增强有效成分的稳定性,防止营养成分的挥发、氧化。它有一定的相对吸湿性。3、在医药工业中,由于相对表面活性和溶血活性比较低且对肌肉没有刺激性,所以它是一种理想的注射剂增溶剂和药物赋形剂。我们今天就一起来看下月旭Xtimate SEC-700(7.8×300mm,5μm)色谱柱对羟丙基-β-环糊精的测定效果如何。[b]色谱条件[/b]色谱柱:月旭Xtimate SEC-700(7.8×300mm,5μm);流动相:0.1mol/L硝酸钾/乙腈=35/65;检测波长:示差检测器;温度:40℃;柱温:40℃;流速:0.8mL/min;进样量:20μL。[b]谱图和数据[/b]1、混合溶液图[align=center][img=,600,310]https://ng1.17img.cn/bbsfiles/images/2019/09/201909251626100982_7478_932_3.jpg!w690x357.jpg[/img][/align][align=center][img=,600,94]https://ng1.17img.cn/bbsfiles/images/2019/09/201909251626155127_2008_932_3.png!w592x93.jpg[/img][/align]2、羟丙基-β-环糊精[align=center][img=,600,313]https://ng1.17img.cn/bbsfiles/images/2019/09/201909251626196371_979_932_3.jpg!w690x360.jpg[/img][/align][align=center][img=,600,80]https://ng1.17img.cn/bbsfiles/images/2019/09/201909251626247666_6386_932_3.png!w690x92.jpg[/img][/align]3、β-环糊精[align=center][img=,600,313]https://ng1.17img.cn/bbsfiles/images/2019/09/201909251626295011_5994_932_3.jpg!w690x361.jpg[/img][/align][align=center][img=,600,76]https://ng1.17img.cn/bbsfiles/images/2019/09/201909251626337665_1162_932_3.png!w690x88.jpg[/img][/align]4、空白溶液[align=center][img=,600,315]https://ng1.17img.cn/bbsfiles/images/2019/09/201909251626374979_8817_932_3.jpg!w690x363.jpg[/img][/align][align=center][b]结 论[/b][/align]使用月旭Xtimate SEC-700(7.8×300mm,5μm),在此色谱条件下检测,能满足检测需求。
中文名称: 羟丙基二淀粉磷酸酯 中文商品名称:羟丙基磷酸双淀粉 英文名称: Hydroxypropyl distarch phosphate 别名: HPDSP 详情: 理化性质:白色粉末,无臭,无味,易溶于水,不溶于有机溶剂。在醚化的基础上,适当地交联所得到的HPDSP,其膨润力、透明度仍显著高于原淀粉。糊液对温度、酸度和剪切力的稳定性高。 来源与制法: 淀粉与三偏磷酸钠或磷酰氯(≤0.1%)与环氧丙烷(≤10%)伴同酯化而成。 编辑本段毒理学依据 1、ADI:无须规定(FAO/WHO,1994)。 2、可安全用于食品(FDA,§172.892,1994)。 质量要求:质量标准(FAO/WHO,1990;CXAS,1991) 羟丙基含量/% 7.0 氯丙醇/(mg/kg)≤ 1 土豆或小麦类淀粉/% ≤ 0.14 其他类淀粉/5 ≤ 0.04 二氧化硫 谷物类/(mg/kg)≤50 其他类/(mg/kg)≤10 砷(以As计)(mg/kg) ≤ 3 重金属(以Pb计)(mg/kg) ≤ 40 铅/(mg/kg)≤ 2 编辑本段用途与注意事项 我国《食品添加剂使用卫生标准》(GB2760―2007)表A.3(可在各类食品中按生产需要适量使用的添加剂名单)第46为羟丙基二淀粉磷酸酯,功能为增稠剂。未限定最高用量,可按需添加。 FAO/WHO规定:可单独使用或与其他增稠剂合用。用于蛋黄酱,5 FAO/WHO;罐装胡萝卜(产品含有奶油或其他油脂)、发酵后经加热处理的调味酸奶及其制品,10 g/kg;冷饮制品,30 g/kg;罐装沙丁鱼和沙丁鱼类产品,20 g/kg;罐装鲐鱼和竹荚鱼,60 g/kg(仅用于填料);速冻鱼条和鱼块(仅指用面包粉和面包拖料包裹),以GMP为限。羟丙基二淀粉磷酸酯Hydroxypropyl Distarch Phosphate编码 GB 20.016;INS 1442性状 白色粉末,无臭,无味,易溶于水,不溶于有机溶剂。在醚化的基础上,适当地交联所得到的HPDSP,其膨润力、透明度仍显著高于原淀粉。制法 由淀粉在碱性条件下,与环氧丙烷进行醚化,再与磷酸交联剂进行酯化反应制得。质量标准 参见羟丙基淀粉。鉴别方法 本品呈一般食变性淀粉反应和磷酸盐反应。1.一般食用变性淀粉反应 同羟丙基淀粉鉴别方法1、2、3。2.磷酸盐反应 参见磷酸三钙。毒理学依据1.GRAS FDA-21CF
请教,羟丙基取代度测定时硫酸的加入量以及样品在处理过程中如何选择加热的时间?
羟丙基淀粉取代度的测定有什么注意点?与茚三酮络合后为何要快速测定?丙二醇的标准曲线是否每次测量都需绘制?标准曲线是大概是多少?100度的油浴能否用水浴代替?
需要买一根R,S-羟丙基-β环糊精为填充剂的色谱柱,以前没用过,大侠给推荐一下哪家的好
各位兄弟姐妹,请问羟丙基-β-环糊精在乙酸乙酯的溶解度是多少?我查了很多文献都找不到答案,打算自己去测定了!但是具体该怎么做?希望各位能指点一下小弟!
请教各位一下 有谁做过羟丙基淀粉取代度试验 那其中用到的浓硫酸是不是对其测定有很大的影响?那么所用硫酸的标准是什么?
聚羟丙基二甲基氯化铵现在只知道CAS 25988-97-0,为一种聚合物,含量一般50%-60%,现在想用HPLC测一下,安捷伦的1260,试了EXTEND/XDB C18色谱柱,都是没保留,有没有测这类物质推荐的色谱柱和流动相
新手小白,请问哪位老师做过GBT34263-2017工业用羟丙基甲基纤维素 中甲氧基、羟丙氧基含量的测定? 仪器方面该如何配置?顶空进样器?液体进样器?为什么使用顶空瓶做前处理?
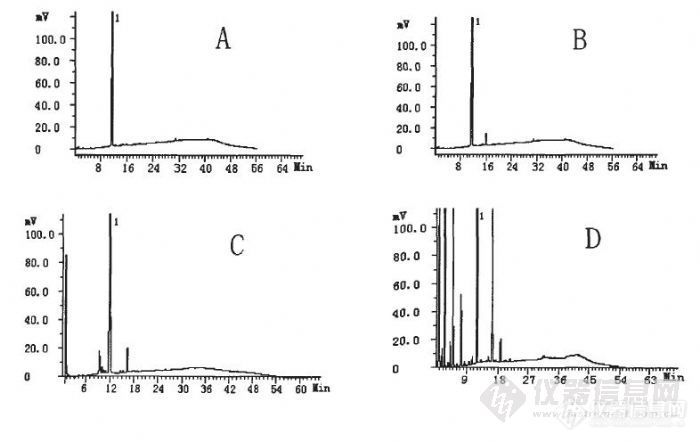
【作者】 葛文娜(东南大学)【摘要】 多烯紫杉醇(Docetaxel,商品名为Taxotere)是新一代紫杉烷类抗肿瘤药物,对乳腺癌、非小细胞肺癌、胰腺癌、头颈癌、卵巢癌以及前列腺癌等均具有良好疗效。目前,多烯紫杉醇上市剂型为注射用浓溶液,该剂型稳定性较差,临床用药不方便并时常引发严重的过敏反应。利用羟丙基-磺丁基-β-环糊精作为药物赋形剂水溶性好、溶血性小、毒性低的特点,实验室开发了多烯紫杉醇羟丙基-磺丁基-β-环糊精包合物冻干粉制剂,以期达到避免或者缓解现有制剂缺点的目的。 本文建立了多烯紫杉醇冻干粉质量的高效液相(HPLC)分析方法,以及生物样本(血浆和组织)中多烯紫杉醇的检测方法,进行了该制剂质量的评价和动物体内的药代动力学研究,为制剂的有效性和安全性评价提供方法学基础;首次提出基于电纺尼龙6纳米纤维的固相膜萃取技术,并以多烯紫杉醇为目标分子,进行了这一样品前处理的新技术在生物样本分析中的应用研究。论文主要工作如下: 一、反相高效液相色谱-紫外法测定多烯紫杉醇冻干粉含量及有关物质 采用Dikma Platisil C18柱(150mm×4.6mm,5μm),检测波长227nm,柱温:30℃。有关物质检查时以乙腈-水(40:60,v:v)为流动相A,乙腈为流动相B,进行梯度洗脱,流速1.5mL/min;含量测定时紫杉醇为内标,以乙腈-水(60:40,v/v)为流动相,进行等度洗脱,流速为1.0mL/min。结果表明:多烯紫杉醇与各有关物质分离良好。在0.05~100μg/mL的浓度范围内具有良好的线性关系(r=0.9993),检出限(LOD)为0.01μg/mL(以S/N=3计)。三个批次样品的多烯紫杉醇标示含量分别为98.79%、99.56%、100.9%,有关物质含量分别为2.8%、2.2%、2.5%。本法准确可靠,专属性强,能满足多烯紫杉醇包合物冻干粉质量控制的要求。 二、多烯紫杉醇包合物冻干粉家兔体内药代动力学的研究 本文建立了灵敏、准确的家兔血浆中多烯紫杉醇的HPLC-UV测定方法,为多烯紫杉醇包合物冻干粉家兔体内药代动力学的研究提供方法学基础。血浆中杂质不干扰样品的测定,多烯紫杉醇在0.04~10μg/mL浓度范围内线性关系良好(r=0.9996),检出限为0.02μg/mL(以S/N=3计),平均提取回收率为90.1%~93.7%,相对标准偏差(RSD)为3.2%~12%。以上方法验证结果表明,此方法满足药代动力学研究的要求。 采用血药浓度法研究了多烯紫杉醇包合物冻干粉的家兔体内药代动力学,通过测定血药浓度经时变化曲线,得出了多烯紫杉醇冻干粉(受试制剂)药代动力学参数;以上市的多烯紫杉醇注射液为参比制剂,研究了受试制剂的相对生物利用度。参比制剂的t1/2β为5.32±1.72h,AUC和CL分别为1.29±0.459μg/mL·h和5.82±1.27mL/h;受试制剂t1/2β为7.00±1.90min,AUC和CL分别为1.59±0.798μg/mL·h和4.72±2.12 mL/h。其平均相对生物利用度为123%。结果表明家兔给予受试制剂t1/2β和AUC均大于参比制剂,清除率CL小于参比制剂(P0.05),提示在相同剂量的条件下,多烯紫杉醇羟丙基-磺丁基-β-环糊精包合物冻干粉在体内可保持相对较高的血药浓度,提高了生物利用度,在一定程度上增强药物对肿瘤细胞的杀伤作用,从而产生较好的临床效果。 三、基于电纺尼龙6纳米纤维的固相膜萃取技术及其在生物样本中的应用研究 研究了基于电纺尼龙6纳米纤维的同相膜萃取技术,研制了相应的装置,在此基础上,对生物样本(家兔血浆和小鼠组织)进行前处理,全面考察了影响萃取效率的因素:蛋白酶的种类、酶解时间和温度、介质pH和离子强度、洗脱溶剂、洗脱溶剂体积,建立了基于电纺尼龙6纳米纤维的固相膜萃取富集生物样本中多烯紫杉醇的分析方法。在优化的条件下,多烯紫杉醇平均提取回收率为72.1%~78.5%(RSD8%),检出限0.015μg/mL(以S/N=3计)。与传统液-液萃取法、C18柱固相萃取法相比,此萃取方法解决了常规提取方法有机溶剂用最大、提取时间长、净化效果差的缺点,不仅使得检测灵敏度增高、干扰减少,而且提取过程快速、环保,符合“绿色化学”发展趋势。【谱图】 http://ng1.17img.cn/bbsfiles/images/2012/08/201208211806_385130_1609970_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/08/201208211803_385128_1609970_3.jpg
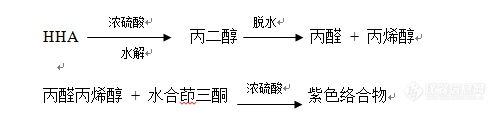
[align=center][b]羟丙基透明质酸质量标准的建立[/b][/align][align=center]杨桂兰,臧恒昌[b][/b][/align][b]摘要:[/b]透明质酸(HA)具有保湿、润滑、营养、修复和预防损伤等生理功能,在维持组织完整性方面和促进感染、损伤、胚胎发育过程中组织形成和重塑方面发挥重要作用。在化妆品、食品及医药领域的应用越来越广泛。但HA容易被体内透明质酸酶降解,体内留存时间短。研究者们期望通过对其进行修饰,得到抗酶解的HA衍生物,延长体内保留时间。修饰HA的衍生物近年来主要致力于将其修饰为两亲性衍生物,对抗酶解活性也有研究;这种亲油亲水性使其不仅能够降低降解速率,而且能够降低表面张力。其次,两亲性HA可以解决美容填充时HA分子量过大,黏度过高,注射困难的问题,修饰后的两亲性HA具有黏度降低(相同分子量相同浓度)的优点。HA两亲性衍生物也可作为生物可降解性的药物载体。 本文参考羟丙基淀粉取代度测定方法,建立了采用分光光度法测定羟丙基透明质酸(HHA)取代度的方法。同时摸索了HHA的抗酶解活性检测法、干燥失重、pH、蛋白含量及微生物等关键指标的测定方法。[b]关键词:[/b]透明质酸;羟丙基透明质酸[align=left] 本研究为确保自制羟丙基透明质酸的质量,特制定一系列产品的质量检验标准。[b]1分子量测定1.1材料[/b] NaCl(AR),NaN[sub]3[/sub] (CP) ,BSA(Roch);高效液相色谱仪,(美国Agilent);多角度激光光散射仪,DAWNEOS,美国Wyatt。[b]1.2方法[/b] 测定条件:流动相:0.2mol/L NaCl (包含0.02% NaN[sub]3[/sub]);流速:0.6ml/min,样品浓度:0.05 mg/ml;柱温:35 ℃,进样体积:500 μl。按照仪器操作规程进行操作。[b]2取代度测定2.1原理[/b][/align][align=center][b][img=,497,113]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251603456954_6718_3389662_3.png!w497x113.jpg[/img][/b][/align][align=left][b]2.2材料[/b] HHA;水合茚三酮、1,2-丙二醇、浓硫酸、亚硫酸氢钠、可见分光光度计、具塞比色管(25 ml),容量瓶(100 ml、1000 ml)[b]2.3方法 [/b] 丙二醇标准溶液的配制:准确称量1.0g丙二醇溶液于1000 ml容量瓶中,加纯化水稀释至刻度,然后分别取2、4、6、8、10 ml于100 ml容量瓶中,定容至刻度,得到丙二醇含量分别为20、40、60、80、100 mg/ml的溶液。[b]2.3.1丙二醇标准曲线的制备[/b] 分别吸取上述丙二醇溶液0.5 ml于25 ml具塞比色试管中,置于冰浴中,逐滴加入4 ml浓硫酸(不宜加入过快,并不时震荡)混合均匀后置100 ℃的水中加热3 min(秒表控制),取出后立即放入冰浴中,冷却至15℃,沿管壁加入水合茚三酮试剂0.3 ml,边加边摇匀;在25 ℃的水浴中放置80 min,再用浓硫酸稀释至12.5ml(约7.7 ml浓硫酸)。缓慢倾倒混匀后(不要用混合器震荡),静置5 min,用1 cm比色皿于590 nm波长处测定溶液的吸光度,绘制吸光度—浓度曲线,拟合丙二醇标准曲线方程。 空白:以相同条件下不加丙二醇溶液作空白。[b]2.3.2试样的测定[/b] 分别称取0.05 g~0.1 gHHA及制备该批HHA所用HA粉末于100ml的量瓶中,量取25 ml的0.5 mol/L的硫酸,缓缓加入量瓶中。置于100℃水浴中加热,缓缓摇动,至试样完全溶解,冷却,用纯水定容,量取0.5ml此溶液置25ml比色管中,其余如上述丙二醇的配制方法。羟丙基含量和取代度算法分别如公式1、2所示。[/align][align=center][img=,411,64]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251608249134_5590_3389662_3.png!w411x64.jpg[/img][/align][align=center]注: C:试样中丙二醇含量,由吸光度计算得出; m:取样量;0.7763:转换系数;[/align][align=center][img=,387,58]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251610349286_9676_3389662_3.png!w387x58.jpg[/img][/align][align=center]注:6.9190:HA分子量/环氧丙烷分子量[/align][align=left][b]3抗HAase降解特性3.1材料[/b] 注射用透明质酸酶(HAase)(上海第一生化药业有限公司、1500单位/瓶);缓冲液(磷酸二氢钠:0.0057 g、磷酸氢二钠:0.0230 g、氯化钠:9.0 g、纯化水:1.0 kg);平氏黏度计,Φ1.0 mm、Φ2.0 mm;恒温水槽,上海仪表仪器厂; DK-8D数显恒温水浴锅,金坛市医疗器械厂。[b]3.2方法[/b] 称取HHA和对照HA各 0.5 g份于150 ml肖特瓶中,加入50 ml缓冲液,震荡至完全溶解。用氢氧化钠溶液或HCl溶液调节pH值6.0~7.2,取溶解液10.0 g,纯水稀释5倍;作为起始样品测黏度。取1500单位的酶用缓冲液稀释10倍,分别吸取40单位加入上述HA和HHA溶液中,摇匀,放入37℃的水浴中降解,24 h取样:称取10.0gHA溶液于50 ml容量瓶中,加入纯化水稀释至刻度线,加热煮沸2min,冷却至室温,测其在25℃下的运动黏度,算法如公式3所示。[/align][align=center] [img=,449,41]http://ng1.17img.cn/bbsfiles/images/2018/07/201807251629104708_3045_3389662_3.png!w449x41.jpg[/img][/align] 24小时黏度下降率Δη低于75%。[align=left][b]4透光率的测定4.1材料[/b] 紫外-可见分光光度计、电子天平(精度0.01g)[b]4.2方法[/b][/align][align=left] 取本品0.50g至盛有100 ml水的锥形瓶中,在冰箱中放置过夜,溶解后,纯水作为空白,参考紫外-可见分光光度计操作规程,550 nm波长处测定溶液的透光率。[/align][align=left][b]5pH的测定5.1材料[/b][/align][align=left] 电子天平(精度0.01g)、pH计、磁力搅拌器、磁子、100 ml锥形瓶、100 ml量筒、新沸放冷的纯化水。[/align][align=left][b]5.2方法[/b][/align][align=left][b]5.2.1 溶解[/b][/align][align=left] 称取供试品0.10 g,置锥形瓶中。加新沸放冷的水100 ml和磁子,将锥形瓶用封口膜封口,将锥形瓶置磁力搅拌器上搅拌约4小时,完全溶解,目测为均一透明溶液。[b]5.2.2 测定[/b][/align][align=left] 按照所用pH计的操作规程,先对pH计进行校准,之后将电极和温度探头深入被测溶液中,缓慢搅拌,读取pH值。[b]6运动黏度的测定6.1材料[/b][/align][align=left] 电子天平(精度0.1 mg);平氏黏度计(毛细管内径为1.0 mm ± 0.05 mm);恒温水浴:控温精度±0.01 ℃;秒表:分度0.01秒;振荡器。[b]6.2方法[/b] 称量样品0.1 g(折干),置100 ml容量瓶中,加水振荡至溶解后作为供试液。取毛细管内径为1.0mm ± 0.05 mm的平氏黏度计,加入5 ml供试液,置水浴中,25 ℃下放置15分钟后,秒表测定供试液流过黏度计两条线之间的时间,取两次测定的平均值按下式计算,即为供试品的运动黏度,计算方法如公式4所示。[/align][align=left] 运动黏度ν(mm[sup]2[/sup]/s)=[i]Kt [/i]公式(4)[/align][align=center]式中 [i]K[/i]为用已知黏度的标准液测得的黏度计常数,mm[sup]2[/sup]/s[sup]2[/sup];[/align][align=center][i]t[/i]为测得的平均流出时间,s;[/align][b]7干燥失重7.1材料[/b] 卤素水份测定仪,HHA样品;[b]7.2方法[/b][align=left] 取本品约1.0g,置HG53 型卤素水分测定仪托盘内。110 ℃测定15分钟,记录测定结果。[b]8细菌、霉菌及酵母菌测定8.1供试液制备 [/b][/align][align=left] 取34ml无菌磷酸盐缓冲液1瓶,将1500U HAase加入其中,用吸量管各吸取1ml分别加入至4个平皿中,作为阴性对照。再取样品1.5 g,加入到做完阴性对照的含有HAase的30 ml磷酸盐缓冲液中,42℃下振荡溶解,制得 1﹕20的供试品溶液。[b]8.2 细菌总数测定[/b](1)阴性对照试验将温度低于45℃溶化的营养培养基分别注入上述2个含有1 ml的磷酸盐缓冲液的平皿中,每个平皿约15~20 ml左右,凝固,倒置培养。均不得有菌生长。(2)样品测定用吸量管准确吸取上述1∶20的供试液2ml加入至8 ml的磷酸盐缓冲溶液中,混匀,作为1∶100的稀释级。向平皿中分别加入1∶20、1∶100的供试液各1 ml,向每个平皿注入温度低于45℃的事先溶化的营养琼脂约15~20 ml,待凝固后倒置放入培养箱中。每个稀释级均制备2个平板。[b]8.3 霉菌及酵母菌数测定[/b](1)阴性对照试验 分别注入向2个含有1ml的上述磷酸盐缓冲液的平皿中将温度低于45℃溶化的玫瑰红钠琼脂培养基,每个平皿约15~20 ml左右,凝固,倒置培养,均不得有菌生长。(2)样品测定 用吸量管准确吸取上述1∶20供试液2ml加入至8 ml的磷酸盐缓冲溶液中,混匀,作为1∶100的稀释级。各吸取1∶20、1∶100的稀释级的供试液1 ml加入至平皿中,注入温度不超过45 ℃的溶化玫瑰红钠琼脂培养基,每个平皿约15~20 ml,待凝固后,倒置培养。每个稀释级均制备2个平板。[b]8.4 结果[/b] 将营养琼脂培养基和玫瑰红钠琼脂培养基平板分别倒置于30~35℃、23~28℃生化培养箱中,营养琼脂平板培养3天,用于细菌计数;玫瑰红钠琼脂培养平板培养5天,用于霉菌、酵母菌计数,按照稀释比例,计算出每克样品中的微生物数。[b]9 结论[/b] 采用制定的质量标准对产品检验,结果表明,HHA能保持HA的润滑性和流动性,也具有明显的抗HAase降解的特性;克服了HA衍生物抗酶解但缺少润滑性的缺点,预期用途是开发成骨关节注射液或皮下注射填充剂用于美容,期望能够延长体内保留时间起到长效治疗的作用,减少患者注射次数,减轻患者痛苦。[/align][align=center]参考文献[/align] 赵凯, 刘丽艳, 刘婧婷. 分光光度法测定羟丙基淀粉取代度. 食品科学,2011, 32(22) : 201-203.[align=center][b][/b][/align][align=center][b][/b][/align]
[size=5][b]简介[/b][/size] 苯酚-硫酸法是利用多糖在硫酸的作用下先水解成单糖,并迅速脱水生成糖醛衍生物,然后与苯酚生成橙黄色化合物。再以比色法测定。[size=5][b]原理[/b][/size] 多糖在硫酸的作用下先水解成单糖,并迅速脱水生成糖醛衍生物,然后与苯酚生成橙黄色化合物。再以比色法测定。[size=5][b]试剂[/b][/size] 1. 浓硫酸:分析纯,95.5% 2. 80%苯酚:80克苯酚(分析纯重蒸馏试剂)加20克水使之溶解,可置冰箱中避光长期储存。 3. 6%苯酚:临用前以80%苯酚配制。([b]每次测定均需现配[/b]) 4. 标准葡聚糖(Dextran,瑞典Pharmacia),或分析纯葡萄糖。 5. 15%三氯乙酸(15%TCA):15克TCA加85克水使之溶解,可置冰箱中长期储存。 6. 5%三氯乙酸(5%TCA):25克TCA加475克水使之溶解,可置冰箱中长期储存。 7. 6mol/L 氢氧化钠:120克分析纯氢氧化钠溶于500ml水。 8. 6mol/L 盐酸[size=5][b]操作[/b][/size] 1.制作标准曲线:准确称取标准葡聚糖(或葡萄糖)20mg于500ml容量瓶中,加水至刻度,分别吸取0.4、0.6、0.8、1.0、1.2、1.4、1.6及1.8ml,各以蒸馏水补至2.0ml,然后加入6%苯酚1.0ml及浓硫酸5.0ml,摇匀冷却,室温放置20分钟以后于490nm测光密度,以2.0ml水按同样显色操作为空白,横坐标为多糖微克数,纵坐标为光密度值,得标准曲线。 2.样品含量测定: ①取样品1克(湿样)加1ml 15%TCA溶液研磨,再加少许5%TCA溶液研磨,倒上清液于10毫升离心管中,再加少许5%TCA溶液研磨,倒上清液,重复3次。最后一次将残渣一起到入离心管。[b]注意:总的溶液不要超出10毫升。[/b](既不要超出离心管的容量)。 ②离心,转速3000转/分钟,共三次。第一次15分钟,取上清液。后两次各5分钟取上清液到25毫升锥形比色管中。最后滤液保持18毫升左右。([b]测肝胰腺样品时,每次取上清液时应过滤。因为其脂肪含量大容易夹带残渣。[/b]) ③水浴,在向比色管中加入2毫升6mol/L 盐酸之后摇匀,在96℃水浴锅中水浴2小时。 ④定容取样。水浴后,用流水冷却后加入2毫升6mol/L氢氧化钠摇匀。定容至25毫升的容量瓶中。吸取0.2ml的样品液,以蒸馏补至2.0ml,然后加入6%苯酚1.0ml及浓硫酸5.0ml,摇匀冷却室温放置20分钟以后于490nm测光密度。每次测定取双样对照。以标准曲线计算多糖含量。[size=5][b]注意[/b][/size][b][b](1)此法简单、快速、灵敏、重复性好,对每种糖仅制作一条标准曲线,颜色持久。 (2)制作标准线宜用相应的标准多糖,如用葡萄糖,应以校正系数0.9校正μg数。 (3)对杂多糖,分析结果可根据各单糖的组成比及主要组分单糖的标准曲线的校正系数加以校正计算。 (4)测定时根据光密度值确定取样的量。光密度值最好在0.1——0.3之间。比如:小于0.1之下可以考虑取样品时取2克,仍取0.2ml样品液,如大于0.3可以减半取0.1ml的样品液测定。[/b] [/b]
多糖的分析是一个大问题啊!和大家讨论一下吧,经综合各种文献我认为多糖结构分析内容:要搞清1. 多糖的单糖组成(种类、比例)2. 每个单糖残基的D-、L-构型,吡喃环式或呋喃环式3. 羟基被取代情况(糖苷键的位置)4. 糖苷键及构型(α、β异头异构体)5. 重复单元方法:1、单糖组成:(对照品:葡萄糖、岩藻糖、半乳糖、甘露糖、木糖、阿拉伯糖、鼠李糖)a:水解: 纸层析薄层层析气相色谱(糖氰乙酸酯衍生物、糖醇乙酸酯)液相色谱(ZORBAX-NH2、HRC-NH2、RID)首选气相,灵敏度高,液相RSD、ELSD灵敏度低b:TFA酸解:气相色谱(乙酰化物)c:甲醇解:气相色谱(三甲基硅醚)2:高碘酸钠氧化和Smith降解a:每摩尔己糖基的高碘酸消耗量、甲酸释放量。(目的:判断可氧化糖基与不可氧化糖基之比例)b:Smith降解完全水解,气相分析,如有葡萄糖(表示有1-3键糖基)、甘油(有1-6或1-2糖基)、甲酸(有1-6糖基)Smith降解部分水解,说明主干糖苷键类型。3:甲基化分析(Hakrmor法)-支链分布多糖—甲基化—水解—还原得甲基化单糖醇—乙酰化得糖醇衍生物—GC-MS检测。 对照品 2,3,4,6-四甲基葡萄糖 糖苷键类型 1—2,4,6- 三甲基葡萄糖 1—32,3,4-三甲基葡萄糖 1—62,4-二甲基葡萄糖 1—3,6 4:IR图谱解析a:吡喃环式或呋喃环式α、β异头异构体5:1HNMR及13CNMR解析(构型)6:纯度检查:a: 紫外吸收光谱(280、260)b:电泳(琼脂糖电泳、聚丙烯酰胺凝胶、醋酸纤维素薄膜)c:薄层色谱(多糖不水解)7:X射线衍射,立体构型。好多啊!想和大家讨论讨论多糖的HPLC分析,我们试验室用的液相是C18柱,紫外检测器,做多糖含量及纯度检测,这样的装备够不够用呀?是不是做前必须衍生化或有其它方法,如用示差折射仪作检测器,是不是不需衍生化?多糖的HPLC分析,用得较多用HPGPC测分子量及分子量分布。一般纯多糖紫外吸收较弱,多用RID或ELSD。至于含量测定多用硫酸蒽酮比色或苯酚硫酸法。http://img.dxycdn.com/images_new/smiles/smile_angry.gif
我想请教一下,最近在做中草药中多糖成分的提取,用到30%过氧化氢脱色,但是一直没有查到有关过氧化氢的用量,所以控制不好脱色效果,请问用30%过氧化氢脱色,一般用量是多少?
论坛里面已经有人提供了水中红外到远红外的了,但是近红外的却没有,求哪位提供一下,此外谁有羟乙级纤维素和羟丙基甲基纤维素的近红外图谱,谢谢
蘑菇中的多糖可以帮助调节免疫、降低炎症;膳食纤维有助降低餐后血糖;β葡聚糖对改善血脂有明显效果,因此,经常食用蘑菇可帮助降低慢病风险。

[align=center]保健品中粗多糖含量的测定[/align]本文研究了苯酚-硫酸法检测不同基质的保健品中粗多糖的含量,论述了不同基质的前处理方法和经验。1 前言市场上常见的保健品多种多样,胶囊、口服液、药片等等。多糖含量作为保健品中的有效成分之一,越来越引起人们的关注。从药理学上讲,多糖具有抗肿瘤、抗病毒、增强免疫力、抗氧化、抗心血管疾病等。因为具有诸多功效,许多保健品生产公司也开发越来越多的含多糖保健品,通过在保健品中添加含有多糖的中药材或者海洋生物,从而使该保健品具有较高的多糖含量,增强其功效。不仅在胶囊、口服液等常规的保健品中添加含有多糖的成分,甚至在一些咖啡、饮料、食品中也添加含有多糖的组分,使其成为功能性的产品。多糖的含量对其功效的发挥至关重要,那么怎么准确、有效地检测出保健品中多糖的含量是一个重要的环节。保健品由于种类繁多,基质复杂,找到一种简单、有效的检测方法,能够检测出各种基质的保健品中多糖的含量具有重要的意义。本实验中采用了常见的苯酚-硫酸法检测保健品中粗多糖含量,选用乙醇提取以除去单糖、低聚糖、甙类及生物碱等干扰成分,然后用去离子水提取其中所含的多糖类成分。多糖在硫酸作用下,水解成单糖,并迅速生成糖醛衍生物与苯酚综合成有色化合物,用分光光度法测定其多糖含量。2 实验部分2.1 试剂95%乙醇 葡萄糖:优级纯;葡萄糖标准液:精确称取105℃干燥恒重的葡萄糖100 mg,置100 ml容量瓶中,加蒸馏水溶液解并稀释至刻度(可加几滴甲苯或几粒苯甲酸防腐)。此标准溶液1.00 ml含葡萄糖1.00 mg,储存于冰箱冷藏;苯酚;苯酚液:称取优级纯苯酚10.0 g,加水150 g ,置棕色瓶中备用,储存于冰箱;浓硫酸。2.2 仪器分光光度计。2.3 分析步骤2.3.1 样品预处理(1) 口服液等液体样品准确移取2.00~10.00 mL液体口服液试样,置于250 mL圆底烧瓶中,加入9倍体积的95%乙醇,混匀,静置1 h,回流提取1 h,趁热过滤,残渣用95%乙醇5 ml洗涤三次。将残渣连同滤纸置于烧瓶中,加蒸馏水50 mL,在60℃水浴中加热提取30 min,趁热过滤,残渣用5 mL热水洗涤三次,洗液并入滤液,放冷后移至100 mL容量瓶中,稀释至刻度,备用。(2)内容物为膏状的胶囊样品或者膏状类样品准确称取0.50~1.00 g膏状内容物或膏状样品,倘若其中含有油脂类辅料,加入乙醚或者石油醚脱脂,离心,弃去乙醚或者石油醚层。再用一定体积的水溶解,转移至250 mL圆底烧瓶中,加入9倍体积的95%乙醇,混匀,静置1 h,回流提取1 h,趁热过滤,残渣用95%乙醇5 ml洗涤三次。将残渣连同滤纸置于烧瓶中,加蒸馏水50 mL,在60℃水浴中加热提取30 min,趁热过滤,残渣用5 mL热水洗涤三次,洗液并入滤液,放冷后移至100 mL容量瓶中,稀释至刻度,备用。(3)内容物为粉状的胶囊样品或者粉状片剂、咖啡等准确称取0.10~0.50 g均质后的粉状样品,倘若其中含有脂肪类辅料,先加入一定体积的水,溶解粉状样品,再加入乙醚或者石油醚脱脂,离心,弃去乙醚或者石油醚层。将水层转移至250 mL圆底烧瓶中,加入9倍体积的95%乙醇,混匀,静置1 h,回流提取1 h,趁热过滤,残渣用95%乙醇5 ml洗涤三次。将残渣连同滤纸置于烧瓶中,加蒸馏水50 mL,在60℃水浴中加热提取30 min,趁热过滤,残渣用5 mL热水洗涤三次,洗液并入滤液,放冷后移至100 mL容量瓶中,稀释至刻度,备用。2.3.2 标准曲线的制备吸取葡萄糖标准液0.25 mL、0.50 mL、1.00 mL、1.50 mL、2.00 mL、2.50 mL,分别置于50 mL容量瓶中,加水定容。吸取上述溶液各2.00 mL,再加苯酚液1.00 mL,涡旋混合均匀,迅速沿管壁加入浓硫酸5.00 mL,摇晃后涡旋混合,放置5 min,置沸水浴中加热15 min,取出后冷却至室温,于490 nm处以水代替样品作参比测吸光度,绘制标准曲线。2.3.3 样品中多糖含量测定吸取2.00 mL样品液,置于10 ml容量瓶中,加水定容。吸取2.00 mL上述溶液,按标准曲线制备项下方法测定吸光度。另以2.00 mL水,同上操作做空白。查标准曲线得样品液中葡萄糖含量。2.3.4 液体样品分析结果的计算计算液体样品中酸性多糖的含量按式(1)或者(2)计算,分别以mg/mL或者mg/g表示。[img=,503,114]https://ng1.17img.cn/bbsfiles/images/2024/03/202403181709449978_4859_3246897_3.png[/img][sub] [/sub] 式中: X—保健品中酸性多糖含量(以葡萄糖计), mg/g或者mg/mL表示;A—从浓度-吸光度曲线上查得样品溶液的葡萄糖浓度,μg;B—从浓度-吸光度曲线上查得空白溶液的葡萄糖浓度,μg;V[sub]1[/sub]—多糖溶液总体积,mL,如按本方法为100 mL;V[sub]2[/sub]—移取多糖溶液的初始体积,mL,如按本方法为2 mL V[sub]3[/sub]—待测多糖浓度溶液的总体积,mL,如按本方法为10 mL;V[sub]4[/sub]—待测多糖溶液的移取体积,mL,如按本方法为2 mL m—保健品的称取质量,g;V[sub]0[/sub]—保健品的测试体积,mL;如两次测定符合允许差时,取两次测定结果的算术平均值作为结果,报告结果取三位有效数字。2.3.5 允许差同一样品的两次测定值之差不得超过两次测定平均值的10%。2.3.6 结果与分析(1)含油脂类样品脱脂与否的影响含有油脂类的保健品,脱脂前后采用上述方法进行酸性多糖含量测定时,多糖含量有一定的差别,未脱脂的样品进行多糖含量测定时,过滤过程十分缓慢,耗时长,多糖含量数据经常不平行,而且数值偏高。[align=center][img=,300,307]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230846_01_3246897_3.jpg[/img][/align][align=center]图1 乙醚脱脂[/align]样品经过乙醚脱脂后有明显的油脂层。[align=center][img=,300,296]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230846_02_3246897_3.jpg[/img][/align][align=center]图2 回流后的未脱脂样品[/align][align=center][img=,300,302]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230847_01_3246897_3.jpg[/img][/align][align=center]图3 回流后的脱脂样品[/align]通过比较图2和图3,脱脂后的样品溶液更加澄清,无论是过滤还是洗涤,反应更快速,洗涤效果也更好。相反,未脱脂的样品,整个容器壁上都黏附着脂肪、油脂层,即使离心后过滤,过滤速率也很差,滤液也很浑浊,如下图4所示。[align=center][img=,300,268]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230847_02_3246897_3.jpg[/img][/align][align=center]图4 脱脂前后滤液的比较[/align][align=left]没有脱脂的样品,油脂层包裹着含有单糖或者寡糖的乙醇溶液,不容易被乙醇洗涤干净,这部分残留的单糖或者寡糖导致结果偏高。因此,对相应的含油脂保健品提前进行脱脂后再检测多糖,不仅能减少操作的时间,还能获得更为准确的结果。 [/align][align=left](2)醇沉时间的影响[/align][align=left]对以含有大豆油辅料的胶囊内容物进行脱脂后沉淀粗多糖,对比了加入9倍95%乙醇后立即回流提取多糖和加入9倍95%乙醇后室温下静置1 h再回流提取多糖,结果显示,加入乙醇后立即回流提取多糖与静置1h后再回流检测出的多糖含量分别为41.69 mg/g、48.08mg/g。可以看出,室温下醇沉时间的增加可以使更多的粗多糖醇沉完全,检测含量增高。[/align][align=left](3) 苯酚硫酸法操作方法的影响[/align][align=left]苯酚硫酸法检测粗多糖含量最为常见,操作简单,适用于常规检测。在实验过程中发现,无论苯酚和浓硫酸的加入比例是1:5还是1:10,苯酚的体积分数是5%还是6%,在进行加入时最好是一个样品加完苯酚,混匀后,立即沿管壁加入浓硫酸,混匀后,再加另一个样品的苯酚和浓硫酸,这样显色更稳定。实验中发现,倘若对所有样品全加完苯酚混匀后,再统一加浓硫酸,显色及不稳定,标准曲线甚至不成线性。苯酚易挥发,长时间与空气接触也容易被氧化,造成结果不稳定。[/align][align=center][img=,300,287]http://ng1.17img.cn/bbsfiles/images/2017/08/201708230848_01_3246897_3.jpg[/img][/align][align=center]图 5 苯酚-硫酸法检测多糖含量[/align][align=left]图5为苯酚硫酸法侧多糖含量的标准曲线和样品,采用了单个样品加完苯酚和浓硫酸后再加另一个样品的苯酚好浓硫酸,显色稳定有规律,经过分光光度计检测,线性良好,样品数据平行,能够有效避免苯酚-硫酸法重现性差这一缺点。[/align]3. 结论采用苯酚-硫酸法检测保健品中粗多糖含量时,针对各种基质进行相应的脱脂操作、增加回流前的醇沉时间、进行显色反应时加入苯酚后混匀立即加入浓硫酸,能够使检测的数据更可靠、稳定。
查找了中国药典,没有找到H-HPC的标准,如果用HPC的方法去测定其含量,对结果会产生什么影响?谁家可进行此项检测,比如什么样的机构或实验室,谢谢。[color=#00FFFF][size=4]H-HPC高取代羟丙基纤维素[/size][/color]
食品安全国家标准 食品添加剂 羟丙基甲基纤维素(HPMC)
最新发现与创新 科技日报上海6月29日电(记者左朝胜)今天,在上海浦东召开的化学糖生物学国际研讨会上,中科院上海药物研究所无限极多糖联合实验室公布了他们的最新研究成果:肠道为香菇多糖(Lentinan)等中草药多糖预留的秘密通道被发现。这些中草药多糖可以经由该通道被人体完整吸收,进而随血液达到全身各处,发挥其各种生物生理功效。 多糖是自然界中含量最丰富的物质之一,广泛存在于动物细胞膜、植物和微生物细胞壁中,对维持生命活动起着至关重要的作用。大量药理和临床研究发现,多糖、特别是中草药多糖,具有调节免疫、抗辐射、抗肿瘤、抗病毒、抗衰老、调节血糖、保护胃肠系统等作用。自1986年日本批准香菇多糖应用于临床以来,目前在中国、美国、韩国、日本及一些欧洲国家,已有几十种多糖被批准应用于疾病的治疗或辅助治疗。同时,多糖还被广泛应用于保健食品。 但由于多糖的分子量一般都很大,如果一个水分子相当面包屑那么大的话,一个高活性多糖分子起码会像一个汉堡包。水分子可以自由进出肠道壁细胞,多糖也可以吗?这个问题一直困惑着中外科学家。 2009年,中科院上海药物研究所丁侃研究员与无限极(中国)有限公司联合开展多糖吸收机制研究,经过几年努力,利用Caco-2细胞、多糖荧光标记等手段,终于找到了肠道给多糖预留的秘密通道——clathrin蛋白。 多糖可借助clathrin蛋白进入肠道细胞内,然后再进入毛细血管,随血液到达全身各处,与其受体结合发挥各种生物活性。该研究成果得到了美国功能性糖组学协会、国际糖复合物组织的赞赏和肯定,并得到世界各国多糖研究领域专家的关注。这项成果为多糖各种生理功效的活性机制研究奠定了坚实的基础,不但为口服吸收与口服有效提供了新依据,而且为多糖靶向治疗提供了可能性。 《科技日报》(2013-6-30 一版)
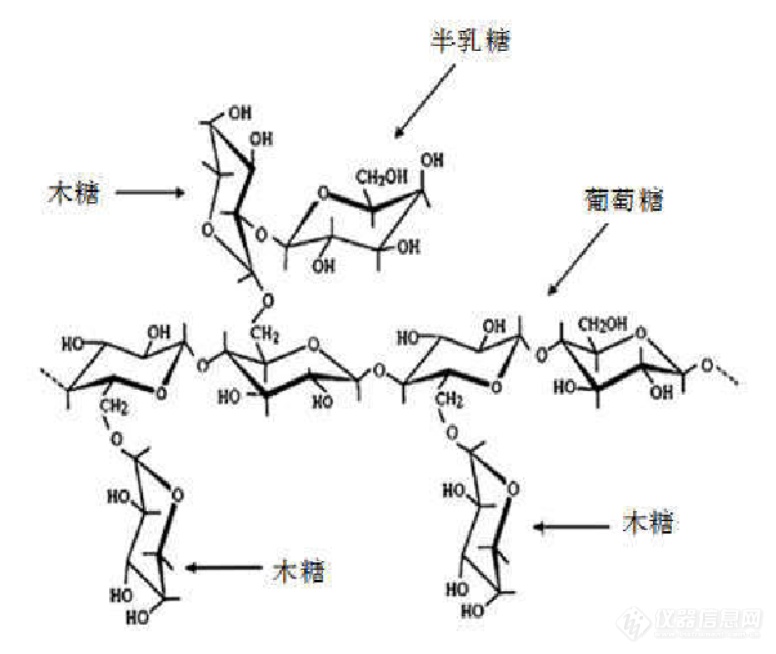
罗望子多糖胶的理化性质,应用和标准陈炳坤[align=center][/align][align=center][font='黑体'][size=20px]罗望子多糖胶的理化性质,应用和标准[/size][/font][/align][align=left][font='times new roman'][size=18px]一、引言[/size][/font][/align][align=left][font='times new roman']罗望子(Tamarindus indica L.)又称酸角、酸豆、罗晃子、酸梅(海南)、“木罕”(傣语),为苏木科(Caesalpiniaceae)酸角属(Tamarindus)的一种高大的常绿乔木植物。罗望子原产于热带非洲,经苏丹引入印度后开始繁衍种植,现广泛分布于除南、北极洲外的其他各大洲。主要分布在我国广西、广东、福建、四川等省区的南部以及海南、台湾等海拔低于 1400m 旱坡、荒地和干热河谷地区,而我国罗望子资源最丰富的地区是云南省的南部、西南部和西部地区。此外在老挝、印度、孟加拉、缅甸、斯里兰卡、马来西亚、泰国等国也有分布。[/font][/align][align=left][font='times new roman']罗望子胶又称为罗望子多糖(Tamarind[/font][font='times new roman'] [/font][font='times new roman']Seed[/font][font='times new roman'] [/font][font='times new roman']Polysaccharide,简称TSP)。它是从豆科罗望子属植物罗望子(又称酸角)的种子胚乳中提取分离出来的一种中性多糖,易分散于冷水中,加热则形成粘稠状液体。罗望子胶有良好的耐热、耐盐、耐酸、耐冷冻和解冻性,具有稳定、乳化、增稠、凝结、保水、成膜的作用,其水溶液的粘稠性较强,黏度不受酸类和盐类等的影响,是一种用途广泛的食用胶。[/font][/align][align=left][font='times new roman'][size=18px]二、[/size][/font][font='times new roman'][size=18px]罗望子多糖胶的理化性质[/size][/font][/align][align=left][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107161936326977_6875_1608728_3.png[/img][font='calibri']罗望子胶的分子主要由[/font][font='calibri']D-[/font][font='calibri']半乳糖、[/font][font='calibri']D-[/font][font='calibri']木糖、[/font][font='calibri']D-[/font][font='calibri']葡萄糖三种单糖构成,三种单糖以[/font][font='calibri']1:2:3[/font][font='calibri']的比例组成了罗望子胶的中性聚多糖。也有研究结果表示,他们三种单糖的比例是[/font][font='calibri']1:2.25:2.8[/font][font='calibri'],其分子结构图如图[/font][font='calibri']1[/font][font='calibri']所示。除中性聚多糖存在外,也有少量的[/font][font='calibri']L-[/font][font='calibri']阿拉伯糖是以游离的形式存在于罗望子胶分子内。据报道,用不同的方法测定罗望子胶的分子量,其结果差异也有所不同。据报道,用黏度法、渗透法、铜值法和3,5-二硝基水杨酸还原法测定的结果分别是523500、546000、556000和115000。[/font][/align][align=center][font='times new roman'][color=#000000]图1[/color][/font][font='times new roman'][color=#000000].[/color][/font][font='times new roman'][color=#000000]罗望子多糖胶的分子结构[/color][/font][/align][align=left][font='calibri']罗望子胶为自由流动、无臭无味、乳白色或淡米黄色的粉末,随着胶的纯度降低,制品的颜色逐渐加深,有油脂气味和手感,易结块,不溶于冷水,但是能在冷水中分散,能在热水中溶解,不溶于大多数有机溶剂和硫酸铵、硫酸钠等盐溶液。它本身不带电荷,属于中性植物性胶。但是当罗望子胶用金属氢氧化物或碱式盐溶液处理后,得到相应的金属络合物,能变成阴离子或阳离子衍生物。[/font][/align][align=left][font='calibri']望子胶是一种亲水性较强的植物胶。当罗望子胶在冷水中分散后被加热到85°C以上就会溶解,形成均匀的胶体溶液。胶液的黏度与质量浓度有关,当罗望子胶溶液的质量浓度小于158g/L左右时,溶液表现出牛顿流体性质 但当质量浓度大于158g/L左右时,罗望子胶溶液显示出非牛顿型流体的流变特性,即溶液具有剪切变稀的触变性或假塑性。加热煮沸对罗望子胶溶液的黏度影响相当大,罗望子胶溶液在煮沸20~30min时黏度首先达到最大值,然后下降,但热稳定性较高,在煮沸约5h以后其黏度只下降至最大值的一半。在97°C加热1h后的黏度残存率是瓜尔豆胶的2.5倍。而在-20°C下冷冻1h后测试,它的黏度影响很小。因此罗望子胶具有冷冻融化稳定性。罗望子胶在pH7.0~7.5时比较稳定,超过这个范围其黏度则会降低,在无机酸介质中黏度降低得特别显著,但在使用有机酸时,在pH2.0~7.0范围内溶液黏度受pH值的影响很小,黏度下降的原因是由于其高聚物的解聚引起的 而pH在7.0~7.5时黏度达到最高是由于其分子伸展的缘故。罗望子胶浆料的黏度随温度的降低而增加,但罗望子胶浆料遇冷不胶凝或变稠,且容易进行再分散,甚至贮藏几天之后也是如此。提纯的罗望子胶其溶液的黏度更高,以致很难制备质量浓度大于20g/L的流动性溶胶,其黏度也不受pH及钠盐、钙盐或铁盐的影响,反而随着盐溶液浓度的增高,其黏度有所增加。如添加蔗糖、D-葡萄糖、淀粉糖浆和其他低聚糖都可使其黏度增加,而添加过氧化氢会使其黏度大大降低。罗望子胶水溶液的稠性强,一般不溶于醇、醛、酸等有机溶剂,能与甘油、蔗糖、山梨醇及其他亲水性胶互溶,但遇乙醇会产生凝胶,与四硼酸钠溶液混合则形成半固态,而加热会变成稀凝胶。[/font][/align][align=left][font='calibri']凝胶是由微量的多糖类等物质与水作用并使之变硬的状态,也称果冻,从分子水平看,由于多糖类高分子链间的相互作用,形成立体的网状结构,他们之间的微小空间中的水处于被包围状态,在水溶液中,当高分子之间的相互作用力与高分子、水分子之间的相互作用力达到平衡时,就形成凝胶。多糖类的这种性质称为胶凝性[7]。罗望子胶溶液干燥后能形成有较高强度、较好透明度及弹性的凝胶。罗望子胶凝胶与果胶凝胶形成的模式相同,属于必须有糖存在下才能形成凝胶的氢键结合法,不同的是相同浓度的罗望子胶与果胶相比,凝胶强度要高得多。罗望子胶凝胶形成时,凝胶强度随煮沸时间的延长而极大地提高,当煮沸时间分别为5、7、10min时,凝胶强度分别为420、540、650N/cm[/font][font='calibri'][size=13px]2[/size][/font][font='calibri']。此外,罗望子胶能在很宽的pH范围内与糖形成凝胶,在中性溶液中煮沸长达2h而凝胶强度几乎不受影响,而在热的酸或碱性介质中,罗望子胶也会像果胶一样迅速降解,碱的降解作用与酸相比不太明显。[/font][/align][align=left][font='times new roman'][size=18px]二、[/size][/font][font='times new roman'][size=18px]罗望子多糖胶在食品工业中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶是一种多功能的食品添加剂,与其他动植物胶相比,罗望子多糖胶具有优良的化学性质和热稳定性。[/font][/align][align=left][font='times new roman'][size=18px]1. 在冰淇淋中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶作为稳定剂,分散于冰淇淋料液中,逐渐与水结合,使大量水分子与氢键相连,在结构上形成三维网状结构,控制了残余水相的流动性,使料液具有一定的粘稠度,这种性能有利于冰淇淋在凝冻时有效充入的空气,并且其无韧性的粘性使冰淇淋入口后融化性好,从而使冰淇淋组织细腻、致密、柔软,并使之有良好的保形性、抗融性和抗热震荡能力。此外,还能使冰淇淋形成纹理细小的冰晶。[/font][/align][align=left][font='calibri']罗望子多糖胶与其它稳定剂的兼容性好,表现在与卡拉胶、黄原胶、魔芋胶、刺槐豆胶、CMC 等胶体复配使用具有较好的效果,可弥补其它胶体冰晶粗大的缺陷。不会掩盖或吸附冰淇淋中的风味物质,有利于香味的充分释放,风味释放性明显优于其他胶体。一般情况下,罗望子多糖胶与其它胶体并用的协同增效作用不明显,但是每一种胶各自的优点不会互相抵消。[/font][/align][align=left][font='times new roman'][size=18px]2. 罗望子多糖胶在水冰中的应用[/size][/font][/align][align=left][font='calibri']在水冰类产品中,添加罗望子多糖胶对改善产品的组织结构非常明显,能够有效抑制冰晶的增长,得到组织非常细腻、表面光滑的产品。在此类产品中,罗望子多糖胶的粘结力强但不粘口,成型性好,耐酸、耐盐、抗融性好,既爽口又能增加产品的实物感。罗望子多糖胶的存在还可以使切片产品切面光滑,口感细腻润滑。[/font][/align][align=left][font='times new roman'][size=18px]3. 罗望子多糖胶在饮料中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶能在低浓度(0.05%~1.5%)下形成溶胶,粘度受酸度影响不大,在 pH 值3.2~10.5 的范围内,其粘度和色泽基本上没有变化。用作果汁饮料的增稠剂,可以增加饮用时爽滑、厚实、细腻的口感。同时,罗望子多糖胶的悬浮性还可防止果汁因长期放置而导致的小颗粒沉淀,使细小的果肉颗粒均匀地悬浮于果汁中,大大降低下沉速度。[/font][/align][align=left][font='times new roman'][size=18px]4[/size][/font][font='times new roman'][size=18px]. 用作果冻和糕点的胶凝剂[/size][/font][/align][align=left][font='calibri']罗望子多糖胶具有强保水作用,可有效地阻止温度降低时果冻和弹性糕点中的水分冷凝析出,从而形成细腻的冰晶。与其它种子胶相比,罗望子多糖胶具有优良的化学和热稳定性,使其在制作过程中加热、冷却时保持较稳定的性质。有关人员经过实验表明,制作马蹄糕时,分层现象是由于调粉浆时,有部分马蹄淀粉颗粒和其他淀粉颗粒没有充分溶胀。蒸煮过程中,未充分溶胀的淀粉颗粒因密度差而沉降使蒸出的糕体分层。当加人罗望子多糖胶后,因其对马蹄粉的增粘作用使得粉浆混合体系的粘度大大提高。因此,那些未充分溶胀的淀粉颗粒不发生沉降,形成很好的悬浮液体系,使得蒸出的糕体均匀无分层现象。制出不起丝,无黏性,耐酸性好,保形性优良,有咬劲、有弹性、润滑爽口的马蹄糕。[/font][/align][align=left][font='times new roman'][size=18px]5[/size][/font][font='times new roman'][size=18px]. 用作淀粉品质改良剂[/size][/font][/align][align=left][font='calibri']淀粉是广泛用于加工食品方面的材料,具有粘性,还可以形成食品的骨架,但是淀粉在加工各种食品的过程中,存在着许多缺点,最主要的就是已经糊化(α化)的淀粉在放置的过程中会老化(β化),致使粘度上升,甚至形成凝胶,透明的食品变成半透明或不透明,析水并生成不溶化的淀粉粒甚至沉淀等,所有这些现象都将导致食品的口感和风味受损、稳定性下降、品质变差,而加入罗望子多糖胶作为淀粉的品质改良剂能抑制淀粉老化。[/font][/align][align=left][font='calibri']罗望子多糖胶是相对分子质量 50 万以上、侧链极多的高分子多糖,添加到淀粉中时,侧链上的-OH 通过氢键与淀粉相互作用,形成一种更巨大的高分子体,这种高分子体很难定向,能够稳定地存在。另一方面,在加工过程中淀粉粒容易破裂受损,罗望子多糖胶与淀粉并用,就可以将淀粉包裹起来,防止破裂,起到保护淀粉的作用,使加工的产品在放置过程中不会出现淀粉粒的聚集和老化。此外,罗望子多糖胶还有优良的保水性,可防止析水。[/font][/align][align=left][font='calibri']罗望子多糖胶与乳化剂同时存在,抑制淀粉老化的效果比单独使用罗望子多糖胶或乳化剂大大提高。因此,罗望子多糖胶用作淀粉的品质改良剂,能稳定食品品质,改善质地和结构,提高口感和风味。[/font][/align][align=left][font='times new roman'][size=18px]6[/size][/font][font='times new roman'][size=18px]. 用于牛奶中[/size][/font][/align][align=left][font='calibri']在牛奶中添加 0.5%左右的罗望子多糖胶可增强制品的稠厚感和甜味,同时不会有黏口的感觉,用于低脂牛奶或脱脂牛奶,口感就像全脂牛奶一样;用于咖啡牛奶或果汁牛奶,可以同时增强浓厚感和甜味。[/font][/align][align=left][font='times new roman'][size=18px]7[/size][/font][font='times new roman'][size=18px]. 用于调味汁中 [/size][/font][/align][align=left][font='calibri']一些西餐用调味汁因为加入食醋使 pH 降低,这些调味汁要求有较高的粘度,若添加少量的罗望子多糖胶,由于其耐酸并有一定的增稠作用,所以可以改善调味汁的口感和稳定性。同时,罗望子多糖胶的黏附性能良好,对于烧肉、烧鸡以及蔬菜等的调味汁要求黏附在制品表面不脱落,单独使用罗望子多糖胶或将罗望子多糖胶与其它胶体并用,都能取得显著的效果。[/font][/align][align=left][font='times new roman'][size=18px]8[/size][/font][font='times new roman'][size=18px]. 用于保健食品[/size][/font][/align][align=left][font='calibri']罗望子多糖胶中的多糖是葡聚木糖,它是一种理想的膳食纤维来源。可起到防治高血症的作用,另外尚可增加小肠非扰动层的厚度,减弱糖类物质的吸收,防治糖尿病的发生发展。[/font][/align][align=left][font='calibri']总之,罗望子多糖胶在食品中的作用可以归结为以下几个方面:冰晶稳定作用,增稠稳定作用,保水作用,乳化稳定作用,悬浮稳定作用,品质改良作用,胶凝作用,保健作用。[/font][/align][align=left][font='times new roman'][size=18px]三[/size][/font][font='times new roman'][size=18px]、[/size][/font][font='times new roman'][size=18px]罗望子多糖胶在其他领域的应用[/size][/font][/align][align=left][font='times new roman'][size=18px]1.[/size][/font][font='times new roman'][size=18px] [/size][/font][font='times new roman'][size=18px]罗望子多糖胶在牙膏中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶可以作为牙膏中的粘结剂和增稠剂,其用量为0.5%~1.2%。使用罗望子多糖胶的牙膏具有较好的稳定性,牙膏在﹣2℃的低温和55℃的高温下贮存24,其膏体的硬度和挤出性均无明显改变。特别是在加酶牙膏中,其稳定性更为突出。当采用羧甲基纤维素钠(CMC)时,牙膏膏体硬度在贮存2个月后即会降低到原值的1/6,而采用罗望子多糖胶贮存4个月后,膏体的硬度基本不变。[/font][/align][align=left][font='times new roman'][size=18px]2. 罗望子多糖胶在洗涤剂中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶在液体洗涤剂中作为增稠剂和稳定剂使用时,能够确保液体洗涤剂在贮存期内粘度基本不变。从而保证液体洗涤剂在垂直的硬表面上有较好的滞留性,能够充分发挥洗涤剂的清洗效果。同时,罗望子多糖胶还有一定的乳化能力和抗再沉积能力,因为罗望子多糖胶具有耐盐、耐热、耐酸性的增稠稳定作用,其粘度不受酸类和盐类等的影响。因此,它是液体洗涤剂中良好的增稠稳定剂.[/font][/align][align=left][font='times new roman'][size=18px]3. 罗望子多糖胶在烟草工业中的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶是良好的天然粘合剂。在烟草工业中,查正根等研究发现罗望子多糖胶是生产再生烟丝(重组烟丝、膨胀烟丝)良好的粘合剂;在医药工业中,罗望子多糖胶既是药片良好的粘合剂,又是膏霜类药物的增稠剂和稳定剂。[/font][/align][align=left][font='times new roman'][size=18px]4. 罗望子多糖胶在医药行业的应用[/size][/font][/align][align=left][font='calibri']罗望子多糖胶应用于医药行业它可控制药物的释放、并具有高药物容量和高的热稳定性。例如高义霞等以罗望子多糖制备的纳米硒,可能具有硒和罗望子多糖的双重生物学功效,将在癌症的化学预防和治疗方面有光明的前景,同时可能在动物生产中将有广阔的应用前景。[/font][/align][align=left][font='times new roman'][size=18px]四[/size][/font][font='times new roman'][size=18px]、[/size][/font][font='times new roman'][size=18px]罗望子多糖胶的国家标准[/size][/font][/align][align=left][font='calibri']根据国家标准G[/font][font='calibri']B [/font][font='calibri']2760-2014的规定,罗望子多糖胶的使用标准如表1所示[/font][/align][align=center][font='times new roman'][color=#000000]表1[/color][/font][font='times new roman'][color=#000000].[/color][/font][font='times new roman'][color=#000000]罗望子多糖胶的使用标准[/color][/font][/align][table][tr][td][align=center][font='times new roman'][color=#000000]食品名称[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]最大使用量([/color][/font][font='times new roman'][color=#000000]g/kg)[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]备注[/color][/font][/align][/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]冷冻饮品(食用冰除外)[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]2[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]可可制品、巧克力和巧克力制品(包括代可可脂巧克力及制品)以及糖果[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]2[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]果冻[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]2[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]如用于果冻粉,按冲调倍数增加使用量[/color][/font][/align][/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]半固体复合调味料[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]7[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]液体复合调味料[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]3[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]果酱[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]5[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]果糕类[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]2[/color][/font][font='times new roman'][color=#000000]0.0[/color][/font][/align][/td][td] [/td][/tr][tr][td][align=center][font='times new roman'][color=#000000]果蔬汁(浆)类饮料[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]3[/color][/font][font='times new roman'][color=#000000].0[/color][/font][/align][/td][td][align=center][font='times new roman'][color=#000000]以即饮状态计,相应的固体饮料按照稀释倍数增加使用量[/color][/font][/align][/td][/tr][/table][align=left][/align][align=left][font='times new roman'][color=#000000]罗望子多糖胶没有国家检测标准,这是因为罗望子多糖胶是一种中性多糖,在检测时无法分辨罗望子多糖胶与其他多糖,因此没有专门的国家检测标准。[/color][/font][/align][align=left][font='times new roman'][size=16px][color=#000000]参考文献:[/color][/size][/font][/align]

问题来源:实验室用10版《中国药典》“玉竹”的多糖含量方法测苦荞麦中的多糖,由于前后两人测得结果差距比较大,A同学结果低、B同学结果高。然后对一系列可能影响结果的因素做了对照试验。http://ng1.17img.cn/bbsfiles/images/2015/09/201509151229_566071_3028242_3.png分析原因:两人在实验过程中“测定法”下离心时间分别为A同学:5min和B同学:25min,所以怀疑是离心时间导致结果的不一致。查找资料: 多糖的单糖基越多 所带的羟基也就越多 多糖的极性也就增大 根据相似相溶 就是 极性的有机物易容于极性的溶剂,极性小的易溶于极性小或非极性溶剂 多糖极性较大 在水中的溶解性很好不过 在醇的溶解性 很低 所以 将 醇 加到含有多糖的水溶液中 可以改变的水溶液的极性 极性大的多糖最先溶出来 极性下的最后溶出来 做到了分级纯化 其实这也是浓缩多糖的好方法。糖在浓硫酸作用下,脱水生成的糠醛或羟甲基糠醛能与苯酚缩合成一种橙红色化合物,在10-100mg范围内其颜色深浅与糖的含量成正比。对照试验:分别对两人的样品做了5min和25min的离心处理,测试结果A同学的样品离心5min的显色很低,离心25min显色深。B同学离心5min和25min显色差距不大都很深。请问这 能说明问题么?
正在做萘的异丙基化反应,因为2,6-二异丙基萘和2,7-二异丙基萘标样太贵了,请教各位大牛,这两种物质在色谱中出峰顺序哪个在前?哪个在后? 非常感谢!!
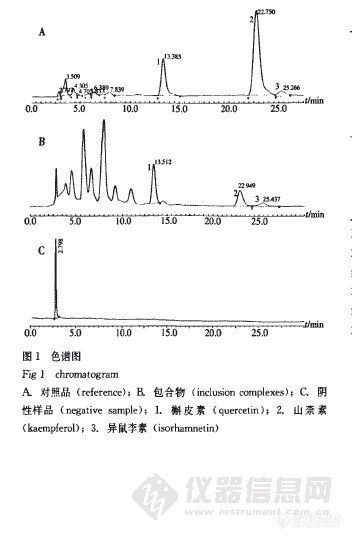
作 者:赵建彬 陈建海(南方医科大学南方医院药学部,广州,510515)摘要: 目的 建立银杏酮酯-羟丙基-β-环糊精包合物的质量标准.方法 采用高效液相色谱法测定制剂中的总黄酮苷含量,色谱柱:Diamonsil C18柱(250 mm×4.6 mm,5 μm),流动相:甲醇-0.4%磷酸(45∶55),检测波长368nm,流速:1 mL·min-1;采用红外光谱分析法鉴别包合物.结果 槲皮素在2~132 μg·mL-1与峰面积具有良好的线性关系,r=0.9995;山奈素在0.9~60 μg·mL-1与峰面积具有良好的线性关系,r=0.9998;异鼠李素在0.1~9 μg·mL-1与峰面积具有良好线性,r=0.9998.槲皮素、山奈素、异鼠李素的平均回收率分别为101.6%、100.4%、99.3%,RSD分别为1.3%,1.4%,0.63%.红外光谱法能有效鉴别包合物.结论 本法可作为该制剂的质量控制参考标准.谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208061012_381701_1606903_3.jpg
最近用HP-5MS 分析多糖的乙酰化,甲基化和单糖组成,柱流失特别严重,但是分析其他样品都没问题,只有多糖样品柱流失严重,大家遇到过这种情况吗?是什么原因呢?
多糖类手性固定相在色谱中的应用郑 芸 方积年(中国科学院上海生命科学院上海药物研究所,上海201203)摘要 手性色谱技术是最重要的手性分离方法之一,它不仅可以快速地分析对映体纯度,也可以用于大量制备光学异构体。设计和发展高效的固定相是手性色谱技术的核心。在诸多的手性固定相中,多糖类手性固定相因品种繁多、耐用而被广泛应用。本文综述了多糖类手性固定相在高效液相色谱、模拟移动床色谱、超临界流体色谱及膜分离中的应用。共引用文献52篇。关键词 多糖,手性固定相,色谱,评述1 引 言 近20年来,用色谱方法分离手性化合物取得了显著进展,已广泛应用于许多领域,如药物化学、不对称合成和生物分析等,不仅可以测定光学纯度,也可用于大量制备光学异构体。 手性色谱技术的核心是设计和制备适用范围广的手性固定相(chiral stationary phase,CSP)。至今已制备出大量用于色谱的CSP,其中120多种已商品化。CSP可分为两大类:一类是由小分子固定在硅胶载体上构成(刷型或Pirkle型),另一类是用光学聚合物固定在载体上制成,多孔胶状的聚合物也可直接用作CSP。其中Okamoto等发展的多糖类固定相是非常有用的分离工具,它们种类繁多、耐用而且负荷量大。其它广泛使用的手性固定相有衍生化的酒石酸CSP(Kromasil—TBB) ]、a1一酸性糖蛋白、Pirkle固定相、环糊精、聚丙烯酰胺和大环抗生素,如万古霉素、teicoplanin和瑞斯托菌素以及最新的用分子印记技术及仿生传感技术发展的CSP 。 多糖,如纤维素和淀粉是自然界大量存在的有光学活性的生物聚合物。它们具有良好的精细结构,能拆分异构体,包括氨基酸衍生物和联苯衍生物的阻转异构体,但它们的手性识别能力不强,适用面也很窄,只能用于毛细管电泳(CE)分析中。半合成的经过改性的多糖适用范围则大大扩展,可用于LC、CE、SFC、TLC、膜分离及萃取中,既可用于分析也可用于制备。经研究发现,多糖类衍生物的手性识别能力与单糖残基的性质、连接位置和连接形式有关。2 高效液相色谱(HPLC) 多糖类手性固定相在HPLC中的应用相当广泛,常见的商品化多糖类手性固定相及应用实例可参考相关文献。纤维素类多糖为刚性的线形结构,而淀粉类多糖具有螺旋形结构。据报道有84%的小分子外消旋化合物可用Chiralcel OJ、Chiralcel OD、Chiralpak AD、Chiralpak AS分离 。用HPLC分析对映体时,除了常用的UV或示差折光指数检测器,还可使用专门检测手性物质的旋光检测器和圆二色散检测器。这也是HPLC比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]和NMR光谱等其它分析方法的优越之处。 为提高手性分离效果以利于检测,还可以对样品进行适当的衍生化。Fukushima 用荧光试剂DBD—PZ([4.[(N,N—dimethylamino)一sulfony1]-7一piperazino-2,1,3-benzoxadiazole])和DBD—COHz(4[[(N—hydrazinoformy1)methy1]一N—methy1]amino-7一[N,N一(dimethylamino)sulfony1]-2,1,3-benzoxadiazole)对(RS)-2一芳基丙酸类化合物进行了衍生化,并发现衍生物洗脱顺序发生改变。3 动态高效液相色谱(DHPLC) 新发展的手性DHPLC方法 可用于研究高温时立体化学稳定的手性化合物,它可得到一系列受温度控制的平顶或峰形曲线,从而可以考察对映体互变的动态过程、动力学数据及对映体互变的能垒。一般在CSP上用色谱方法分离外消旋混合物,最多可以得到收率50% 的两种纯的光学异构体。而在DHPLC中,利用CSP来达到对映体互变平衡,从而使分离和平衡合二为一,理论上可以从外消旋混合物中以100%收率得到一种纯的光学异构体。它的基本原理是外消旋混合物立体化学稳定在较低温度时对映体互变过程被抑制,而较高温度发生对映体互变。实验中让外消旋混合物先通过一个低温CSP柱子,将先洗脱出来的组分(A)继续通人第二个高温CSP柱子,收集后洗脱组分(B)。(A)进入第二个柱子后停留足够长时间达到对映体互变平衡,再继续洗脱,得到(A)和(B)。如果进行多次循环平衡、过柱,则可得到纯的对映体(B)。如Lorenz等用DHPLC分离一螺环化合物,该化合物可通过螺环处的C—O 键开环和闭环进行对映体互变。将它依次通过0℃和40℃ 的两根Chiralcel OD柱,平衡2h,即可得到32% ee(enantiomerie excess,ee)的(+)一对映体。4 模拟移动床色谱(SMB) 至今批次处理色谱在应用中仍占主导地位,但大规模制备需要大量CSP。CSP价格昂贵,而且产品的浓度低,洗脱液消耗量大,难以回收。SMB可以节省90% 的流动相并得到更高的产率。在批次处理色谱中被分离组分在流动相的驱动力下移动,固定相只有一小部分起作用。在移动床色谱中,不仅流动相发生移动,固定相也要向相反方向移动,易洗脱的化合物(萃余液)随流动相移动,难洗脱的化合物(萃取液)随固定相移动。整个固定相的分离能力被持续利用,明显地提高了系统产率。但就技术而言很难移动固定相,因此采用模拟方式,SMB的环状柱子实际上是用许多小柱依次连接而成,有规律地改变进样口和出样口,可以达到和固定相移动相同的效果。SMB技术起于20世纪60年代UOP(Universal Oil Products,Des Plaines,IL,USA)从C8 中分离对二甲苯,后来该技术被广泛用于制药工业,以获得光学纯药物。其中应用于SMB的CSP约有70%是多糖类CSP。如Nagamatsu等用SMB方法替代以前的非对映体结晶的方法,用稍做改性的Chiralcel OF(cellulose 4-chlorophenyl carbamate)分离了一种制药工业的中间体喹啉甲瓦龙酸酯。Francotte等的研究还发现,SMB对于难溶的化合物,如formoterol尤为有用。而且可调节不同参数如进样率和萃取率来达到最佳纯度和产率。
维权声明:本文为huomeng520原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。本实验建立了一种以牛肉中肌肽为代表,反相分离测定亲水性物质的方法。该方法选用丙基酰胺键合硅胶亲水作用色谱柱,反相分析测定牛肉中亲水性成分—肌肽的含量。该方法操作简单,样品无需衍生处理。通过该法结合 H P L C—M S联用技术确定了保留时间为10.276~10.609min的色谱峰就是肌肽峰。将该色谱柱与常规C18色谱柱进行对比后发现,该色谱柱对L-肌肽的保留能力和分离能力均优于C18柱。此法精密度实验显示其相对标准偏差(RSD%)为1.06%,最低检测限为4.59×10-2mg/L。最后实验结果表明:亲水性色谱柱反相使用时,完全适用强极性物质含量的测定,通过实际样品分析检测,每克牛肉的肌肽含量为0.011克。引言L-肌肽(L-carnosine)是一种水溶性二肽,在1900年由Gulewitsch和Amiradzhibi在牛肉提取物中发现。L-肌肽天然存在于多种脊椎动物的骨骼肌以及新陈代谢旺盛的脑中。它具有广泛的生物活性,如抗氧化、保护膜的完整性、抗糖基化、质子缓冲、调节巨噬细胞活性等,是维持机体正常状态的一种含量很低的物质。L-肌肽的结构为β-丙氨酰—L-组氨酸。L-肌肽的结构如图1所示。从化学结构上看,肌肽由于含有较多的极性基团(-OH、-NH2、-COOH),水溶性特别强。肌肽的正辛醇—水分散系数为-2,远远小于0,理论上说明了L-肌肽的强极性,不溶于任何有机溶剂,属于亲水性成分。近年来,L-肌肽的研究一直受到人们关注。其含量测定方法一直在探索中。目前已报道的L-肌肽的分析方法主要以高效液相色谱法为主,且多采用柱前衍生化法,这种方法试剂成本高,样品预处理繁琐,且分析时间长,不利于对样品的快速检测。也曾有报道将离子色谱和毛细管电泳色谱应用于L-肌肽的测定,但两种方法较为复杂,且仪器操作较为繁琐。将氨基柱应用于反相高效液相色谱,能实现对样品中L-肌肽快速、准确地检测,但氨基柱不耐水解,长时间在反相条件下使用,会缩短氨基柱的使用寿命。所以应选择一款既耐水解,柱效又高的色谱柱对牛肉中L-肌肽进行分析。色谱柱填料通常是以硅胶为载体,在硅胶表面进行修饰。C18色谱填料是在硅胶表面键合非极性的十八烷基碳,属于非极性色谱填料。根据“相似相亲原则”,应选用极性较强的色谱柱分析极性物质,普通的C18反相色谱柱属于非极性色谱柱,对亲水性成分没有保留能力,因此不能满足对此类物质的分析要求。实验中选用丙基酰胺键合硅胶柱,该色谱柱填料以硅胶为载体,表面键合丙基酰胺基团,极性强,耐水解,适用于对极性物质的分离。马婧玮采用此柱,实现了对亲水性井冈霉素A快速准确的定量分析。本次实验从L-肌肽的性质出发,结合色谱柱的性质,将丙烯酰胺键合硅胶色谱柱与常规C18柱进行对比,并借鉴田颖刚等人已发表的L-肌肽质谱分析条件,选择分离效果最好的色谱柱与电喷雾质谱串联使用,对牛肉中肌肽进行了分析鉴定。