各位大大,小弟最近在做醇酸树脂酸值和羟值的滴定,羟值滴定的方法是用乙酸酐--4-DPMA的方法,酸值测定结果为21mg KOH/g 样品。羟值直接滴定的结果为-14mgKOH/g 样品,出现负值是不是因为羧基与滴定剂氢氧化钾反应造成的?根据方法羟值=酸值+测定的羟值,也就是21+(-14)=7mgKOH/g 样品。那这7mgKOH/g 样品就是样品羟值吗?照这样计算样品羧基中的羟基好像没有包含在结果中,现在感觉很纠结。
各位专家,大家好,我现在用GC112A分析乙酸丁酯和2,3-丁二醇,柱子用的是SE-30和SE-54,2,3-丁二醇沸点为181左右,乙酸丁酯为126.1,可是乙酸丁酯的峰在2,3-丁二醇后面,而且分离度不够,不能大于1.5,我采用了各种升温程序都不行,有谁能告诉我怎么办么??
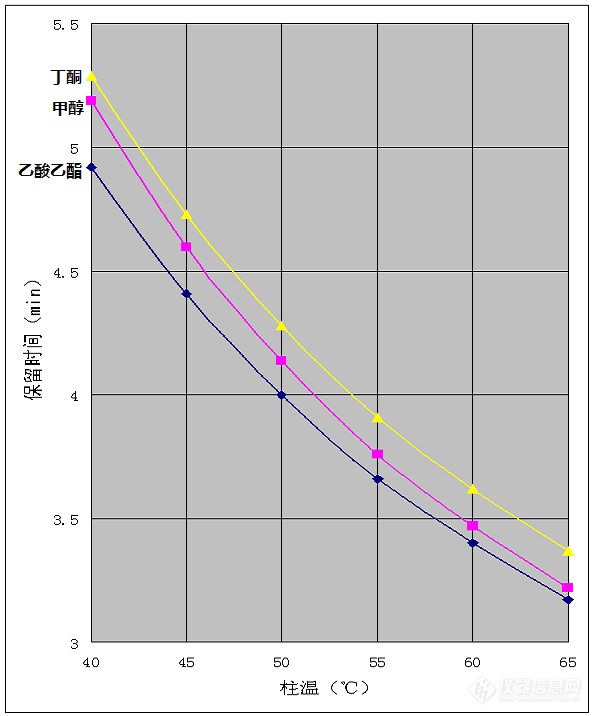
溶剂残留分析是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]的重要应用之一,在药品、食品、包装等领域都是必测的项目。常见溶剂中涉及到的检测目标物经常有乙酸乙酯、甲醇、丁酮,以及二甲苯异构体这几项。最近看到 @m3091333、@p3109800、@Insm_c1196d2b 等多人发帖子讨论相关问题,我从原理上进行了一些解释,但终究纸上谈兵,于是找别的实验室要了这几种试剂,用实践检验了一下。首先,如果二甲苯异构体不要求分离,用624柱可以很容易的解决问题,这里就不讨论了。如果要求乙苯、对二甲苯、间二甲苯、邻二甲苯四种异构体分离,用624柱是无法完成的。因为二甲苯异构体色散力差异非常小,只能靠诱导力的差异分离,不同异构体在强极性柱上的极化率不同,乙苯极化率最低,其次是对二甲苯、间二甲苯,邻二甲苯极化率最大,出峰时间也随极化率的增加而延长。而624柱的极性比较弱,不能产生足够的极化作用,特别是对二甲苯与间二甲苯的极化差异非常小,无法实现分离。这个问题是由分子结构决定的,无论怎么调节色谱条件都不能解决。要想解决只能换强极性柱,常见的就是聚乙二醇柱,包括各种wax柱和FFAP柱等。三氟丙基柱也是强极性的,可以分离二甲苯异构体,但是这种柱很少使用。在聚乙二醇类的色谱柱上,乙酸乙酯、甲醇、丁酮三种目标物分离困难,各种类型的聚乙二醇柱选择性略有差异,但这三种物质都是较为接近的,想要分离是不太容易的。但是这三种物质与聚乙二醇固定相之间的作用力存在本质上的差异,因此通过调整柱温条件是可以分离的。下面三幅图是用60米*0.53mm*1um的INNOWAX柱分离乙酸乙酯、甲醇、丁酮的效果,柱温分别是40℃、50℃、60℃。[img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157168864_5041_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157170984_7926_2204387_3.png!w690x796.jpg[/img][img=,690,796]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022157172914_736_2204387_3.png!w690x796.jpg[/img]图中很明显,柱温低时甲醇与丁酮出峰时间接近分不开,高温时甲醇与乙酸乙酯出峰时间接近分不开,温度适中时三者可以实现分离。虽然未达到基线分离,但分离度都超过1,用来定量是完全可以的。这是找别人借的一根旧柱子,柱效只有4万塔板,如果是新柱子柱效应该能达到七八万塔板,分离度肯定更高,如果是0.32mm口径的柱子分离就更没问题了。要强调的是,能够实现分离的条件并不是完全靠盲目尝试获得的。我们看一看三种目标物的保留时间随柱温的变化就能发现其中的规律,见下图:[img=,594,716]http://ng1.17img.cn/bbsfiles/images/2018/08/201808022156374904_6999_2204387_3.png!w594x716.jpg[/img]图中可以看出,三种目标物的保留时间都是随温度升高而减小的,但是减小的幅度却并不相同。甲醇的保留时间随温度升高而减小的幅度明显大一些。这是因为甲醇具有羟基,与聚乙二醇固定相的相互作用力以氢键为主,氢键的强度随温度升高而迅速减弱。而乙酸乙酯、丁酮与聚乙二醇固定相的作用力都是以诱导力和取向力为主,这种力是由分子偶极矩决定的,受温度的影响要小一些。甲醇峰位置在乙酸乙酯与丁酮之间,温度升高时保留时间都减小,但甲醇减小更多,于是甲醇与乙酸乙酯靠的更近,与丁酮的分离度提高。温度降低时保留时间都增大,但甲醇增大更多,于是甲醇与丁酮靠的更近,与乙酸乙酯的分离度提高。用其他的柱子,如DB-wax或者FFAP时,各组分之间的相对位置会有差别,甚至有时出峰顺序都会变,但是保留时间随温度变化的这种规律仍然是适用的。所以遇到分不开的情况,一定不要盲目的乱试一通,也不用盲目的换柱子,一定要把问题想明白,有针对性的优化条件。最后要强调的是,这里虽然是以溶剂检测为例讨论了如何只用一根柱子就实现分离,但实际样品很复杂,并不是每次都能通过这种优化实现全部分离目的。所以色谱实验室配备多种不同极性的色谱柱是非常重要的。特别是做复杂样品时,即使谱图上看起来分离不错,最好也能用另外一种柱子进行一次验证,以免实际样品中有干扰物共流出,造成假阳性。
关于乙醇、乙酸乙酯、甲基异丁酮、甲苯、丁酸乙酯、异戊酸乙酯、乙酸-2-甲基-1-丁醇酯、己酸乙酯、异戊酸异戊酯、异丁酸异戊酯、己酸烯丙酯、紫罗兰酮、肉桂酸异丙酯13种物质的气相方法,这13种物质能否一针全部出来,用什么柱子合适,FID对它们是不是都有响应?希望各路高手路过能留下点意见和相关资料,不胜感激!
我在GDX-102气象色谱柱(热导池法)上测混合物(含乙酸。乙醇。正丙醇。异丁醇。异戊醇。乙酸乙酯。乙酸正丙酯。乙酸异丁酯。乙酸异戊酯),请问专家:怎样控制气象色谱的操作条件能把这些混合物各自的含量测出来,而且峰形较好
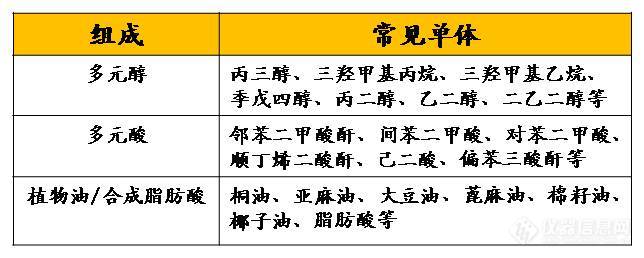
[b]一. 醇酸树脂介绍[/b] 醇酸树脂是由多元醇、多元酸和植物油/合成脂肪酸缩合聚合而成的油改性聚酯树脂,如Table 1所示。醇酸树脂的分类可依据植物油/合成脂肪酸的种类,也可依据脂肪酸或油脂在醇酸树脂中的含量(油度,OL),如Table 2所示。[align=center]Table 1 醇酸树脂的组成[/align][align=center][img=,644,258]http://ng1.17img.cn/bbsfiles/images/2018/07/201807120933417115_7822_2879355_3.jpg!w644x258.jpg[/img][/align][align=center]Table 2 醇酸树脂的分类[/align][align=center][img=,645,293]http://ng1.17img.cn/bbsfiles/images/2018/07/201807120934044045_9365_2879355_3.jpg!w645x293.jpg[/img][/align][b]二. 微谱技术在醇酸树脂结构解析方面的积累[/b] 醇酸树脂固化成膜后有光泽和韧性,附着力强,并具有良好的耐磨性、耐候性和绝缘性,通常作为木器漆、烤漆、油墨等产品的主体树脂使用。主体树脂的角色意味着醇酸树脂的性能直接影响应用产品的性能,所以对醇酸树脂的组成及单体的结构解析非常重要,而微谱胶涂油事业部已在这方面进行了一定的知识积累。 技术工程师首先利用已知单体及比例合成多组醇酸树脂标准样品,然后对这些标准样品进行GC-MS、[sup]1[/sup]H-NMR、[sup]13[/sup]C-NMR等测试,建立醇酸树脂单体谱图库,优化醇酸树脂结构解析方法,进而对醇酸树脂的合成单体(多元醇、多元酸和植物油/合成脂肪酸)进行定性定量解析。[b]三. 解析案例 解析对象:[/b]亚麻油改性的醇酸树脂 [b]解析思路:[/b]醇酸树脂中植物油/脂肪酸可以根据醇酸树脂甲酯化产物中各脂肪酸甲酯的种类与质量比来鉴定,多元醇及多元酸可以通过[sup]1[/sup]H-NMR 和[sup]13[/sup]C-NMR 中化学位移的归属进行确定。[b] 解析过程:[/b]如 Figure 1 所示,对各脂肪酸甲酯的色谱峰进行积分并作归一化计算,结果与亚麻油组分的文献值对比(Table 3),发现脂肪酸种类及含量与椰子油组分有良好的对应关系,确定醇酸树脂的植物油为亚麻油。 分析醇酸树脂的[sup]1[/sup]H-NMR(Figure 2) 和[sup]13[/sup]C-NMR(Figure3),确定多元醇为季戊四醇和二乙二醇,多元酸为邻苯二甲酸酐,并且存在羟基未反应完全的季戊四醇。单体定性确定后,通过[sup]1[/sup]H-NMR,对合成单体的特征化学位移进行积分面积计算,确定单体的定量数据。[align=center][img=,502,222]http://ng1.17img.cn/bbsfiles/images/2018/07/201807120934352578_5386_2879355_3.jpg!w502x222.jpg[/img][/align][align=center]Figure 1 醇酸树脂GCMS谱图[/align][align=center]Table 3 醇酸树脂中各脂肪酸甲酯的色谱峰面积与亚麻油组分文献值对比(%)[/align][align=center][img=,606,382]http://ng1.17img.cn/bbsfiles/images/2018/07/201807120935055605_9200_2879355_3.jpg!w606x382.jpg[/img][/align][align=center][img=,556,107]http://ng1.17img.cn/bbsfiles/images/2018/07/201807120935221815_9280_2879355_3.jpg!w556x107.jpg[/img][/align][align=center][img=,623,436]http://ng1.17img.cn/bbsfiles/images/2018/07/201807120935499435_8090_2879355_3.jpg!w623x436.jpg[/img][/align][align=center]Figure 2 醇酸树脂[sup]1[/sup]H-NMR谱图[/align][align=center][img=,623,436]http://ng1.17img.cn/bbsfiles/images/2018/07/201807120936123835_2273_2879355_3.jpg!w623x436.jpg[/img][/align][align=center]Figure 3 醇酸树脂[sup]13[/sup]C-NMR谱图[/align][b] 解析结果:[/b]对于醇酸树脂的单体结构解析,该方法准确度很高,可以将醇酸树脂中多元醇、多元酸和植物油/合成脂肪酸进行定性定量解析。该方法已为多家开发醇酸树脂的客户提供了非常大的帮助,客户按照醇酸树脂结构信息可以更快地完成产品开发,缩短研发周期。[list][*]声明:本文资料为“上海微谱化工技术服务有限公司”原创,未经允许不得私自转载。否则我司将保留追究其法律责任的权利。[/list]
测量乙酸乙酯用的柱子为填充柱,为401有机担体,固定相为己二酸乙二醇酯,老化柱子温度170度,在条件条好以后(柱温158度,TCD温度145度,载气流速54ml\min.)1h以后,柱前压有0.6kg变为0.8kg.又过2h又变为1.4kg请问高手这是何原因?该怎么解决?多谢!
我不知道我这样理解对不对,请前辈们帮我捋一捋。一般原料叫香茅醇的是不是都是右旋的?玫瑰醇照理说应该是左旋香茅醇,但是市面上卖的玫瑰醇是不是精制过的香叶油?乙酸玫瑰酯是不是乙酸左旋香茅酯?乙酸香茅酯是不是就是乙酸右旋香茅酯?
请问聚酯树脂与醇酸树脂如何区别?利用裂解色谱质谱联用是最好的方式吗。
[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]要用顶空测青霉素钾盐中的正丁醇、乙酸乙酯的残留,可样品不溶于DMS和DMSO溶剂,能溶于水,但正丁醇和乙酸乙酯不溶于水,能进样检测吗?
乙酸对叔丁基环己酯 和乙酸邻叔丁基环己酯如何区分?谢谢
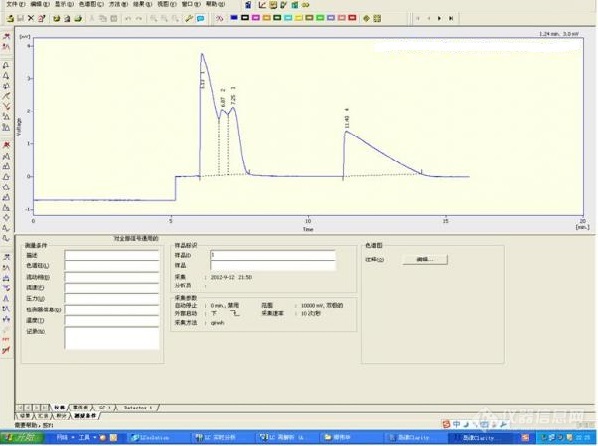
[color=#444444] 体系:[/color][color=#444444]乙酸/正丁醇/乙酸正丁酯/水;[/color][color=#444444]质量分数:均为25%[/color][color=#444444]沸点:乙酸119℃,正丁醇118℃,乙酸正丁酯126℃,水100℃。[/color][color=#444444] 分析条件:[/color][color=#444444]1. 色谱柱:DB-FFAP (30×0.25×0.25)[/color][color=#444444]2. 检测器:TCD[/color][color=#444444]载气流量:N2,0.25ml/min[/color][color=#444444]进样口温度:150℃[/color][color=#444444]柱温箱温度:120℃[/color][color=#444444]检测器温度:220℃[/color][color=#444444]图上可以看出:[/color][color=#444444]1, 基线发生瞬间跳动,一般基本上是漂移吧,为什么我这会突然发生阶跃式的跳动?分析原因是不是载气流量太低,可能载气流量发生不稳定,导致基线发生跳动?[/color][color=#444444]2, 由于有四元组分,前三个峰没有完全分开,而色谱柱分离效率跟载气流量,柱温关系最大,载气流量已经很低了,而且柱温也低于乙酸正丁酯的沸点,是不是也不能再低了。考虑能不能采用程序升温的方法,有没有可能将峰分开?如果可以的话,程序升温建议应该如何设置?[/color][color=#444444]求高手。[/color][color=#444444][img=,598,446]https://ng1.17img.cn/bbsfiles/images/2019/09/201909271014211801_6141_1752329_3.jpg!w598x446.jpg[/img][/color]
(1)原理试样经处理后,在pH6左右的溶液中,镉离子与二硫腙形成配合物,并经乙酸丁酯萃取分离,导入原子吸收仪中,原子化以后,吸收228.8nm共振线,其吸收值与镉含量成正比,与标准系列比较定量。(2)试剂 氨水、混合酸、1g/L二硫腙-乙酸丁酯溶液(称取0.1g二硫腙,加10mL三氯甲烷溶解后,再加乙酸丁酯稀释至100rnL,临用时配制)、2mo1/L柠檬酸钠缓冲液(称取226.3g柠檬酸钠及48.46g柠檬酸,加水溶解,必要时加温助溶,冷却后加水稀释至500mL,临用前用1g/L二硫腙-乙酸丁酯溶液处理以降低空白值)、镉标准储备溶液和标准使用液的配制与碘化钾-4-甲基戊酮-2法中的相同。(3)仪器原子吸收分光光度计。(4)分析步骤①试样处理对于谷类要去除其中的杂物及尘土,必要时除去外壳。对于豆类,取可食部分洗净晾干,切碎充分混匀。②样品消化称取5.00g上述试样,置于250mL高型烧杯中,加15mL混合酸,盖上表面皿,放置过夜,再于电热板或电砂浴上加热。消化过程中,注意勿使干涸,必要时可加少量硝酸,直至溶液澄明无色或微带黄色。冷后加25mL水煮沸,除去残余的硝酸至产生大量白烟为止,如此处理两次,放冷。以25mL水分数次将烧杯内容物洗入125mL分液漏斗中。取与处理样品相同量的混合酸、硝酸按同一操作方法做试剂空白试验。③萃取分离 吸取0、0.25mL、0.50mL、1.50mL、2.50mL、3.50mL、5.0mL镉标准使用液(相当于0、0.05μg、0.1μg、0.3μg、0.5μg、0.7μg、1.0μg镉)。分别置于125mL分液漏斗中,各加盐酸(1+11)至25mL。向试样品处理溶液、试剂空白液及镉标准溶液各分液漏斗中各加5mL柠檬酸钠缓冲液(2mol/L),以氨水调节pH至5~6.4,然后各加水至50mL,混匀。再各加5.0mL二硫腙-乙酸丁酯溶液(1g/L),以氨水调节pH至5~6.4,然后各加水至501mL,混匀。再各加5.0mL二硫腙-乙酸丁酯溶液(1g/L),振摇2min,静置分层,弃去下层水相,将有机层放入具塞试管中,备用。④测定测定方法与碘化钾-4-甲基戊酮-2法中的相同。⑤结果计算 样品中镉的含量按下式进行计算。X=/(m×1000)式中,X为试样中镉的含量,mg/kg;A1为测定用试样液中镉的质量,μg;A2为试剂空白液中镉的质量,μg;m为试样质量或体积,g或mL。计算结果保留两位有效数字。⑥精密度 在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的15%。
请问老师,同时分析乙酸乙酯,异丙醇,甲苯,二甲苯,丁酮用什么固定相的毛细管柱比较好?我公司用的是GC112A型色谱仪,目前用的毛细管柱对以上物质分析的分离度很不理想!请老师多指点,谢谢!
FID检测器,用水做溶剂溶解4羟基2丁酮和1,3-丁二醇时可以分开,然后用乙酸乙酯作溶剂时,只有一个峰了。条件是60℃,10℃/min升温220℃。
[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]质谱做邻苯二甲酸酯类(二丁酯、二乙基己酯),进溶剂空白(甲醇、乙腈、二氯甲烷、乙酸乙酯,均为色谱纯或农残级),空白均有很高响应,以致标准曲线都无法做,选择离子扫描,149出很大峰,希望各位专家能有解决办法,谢谢!急!
我今天按照国标GB/T5750.10-2006中的9测定二氯乙酸,进行的是加标回收。因为是用甲基叔丁基醚做的介质,质谱分析时有很多峰,我无法确定哪一个是二氯乙酸甲酯,自带的质谱库内也没有。请问哪位能帮我找一下二氯乙酸甲酯的质谱分析参数,谢谢。
我现有一产品需要做有机溶剂残留量,可能的残留有机溶剂主要为二氯甲烷,乙酸乙酯,甲醇,乙醇.请问应该用什么样的色谱条件?
请教各位专家,怎样分离 乙醇:水:乙酸异丁酯的混合物,比例约为10:5:85,目标是尽量减少乙醇和水,谢谢!
求助三氯吡氧乙酸、2,4-二氯苯氧乙酸正丁基酯(2,4-D丁酯)的检测方法
如果同时想做苯,甲苯,乙酸乙酯,乙酸丁酯,丙酮,丁酮,三氯乙烯,二氯乙烷,环己酮的话应该悬着什么样的色谱柱,什么条件.......如果实在做不到一起的话,最合适的搭配,方法,条件是什么???.
又称辣椒提取物,辣椒油,辣椒精油。是含有许多种物质的混合物,主要含有辣椒色素类物质和辣味类物质构成。其代表物为辣椒红素、辣椒玉红素、辣椒黄素、玉米黄质、堇菜黄素、辣椒红素二乙酸酯、辣椒红素软脂酸酯等 辣味物质中包括辣椒素、辣椒醇、二氢辣素、降二氢辣素等。基本信息中文名称辣椒油树脂外文名称capsicum oleoresin别称辣椒提取物,辣椒油,辣椒精油外观暗红色至橙红色粘稠油状液体目录1简介2化学成分3物性数据4辣椒油树脂的提取5用途折叠编辑本段简介辣椒油树脂,又称辣椒提取物,辣椒油,辣椒精油。是含有许多种物质的混合物,主要是由辣椒色素类物质和辣味类物质构成。其代表物为辣椒红素、辣椒玉红素、辣椒黄素、玉米黄质、堇菜黄素、辣椒红素二乙酸酯、辣椒红素软脂酸酯等 辣味物质中包括辣椒素、辣椒醇、二氢辣素、降二氢辣素等。其他的有胡萝b素、酒石酸、苹果酸等。由茄科中辣椒,尤其是牛角椒等成熟(红色)果实经粉碎后用有机溶剂(乙醚、丙酮或乙醇)提取而得。产品暗红色至橙红色,略黏。有强烈辛辣味,并有灸热感,并可及整个口腔至咽喉。在食品工业中可作调味、着色、增香剂和健身辅助剂等。也可作为制成其他复合物或单一制剂的原料。目前市场上也把辣椒提物加工成水分散性制剂以扩大应用面。辣椒油树脂为混合物,包括辣椒精油树脂和辣椒红油树脂,辣椒精油树脂是辣椒油树脂中辣味所在,辣椒红油树脂是不辣的,呈血红色。纯的辣椒红色素可以从石油醚中析出有光泽的针状结晶得到,熔点181~182℃。最大吸收光波为483nm。溶于丙酮、氯仿 也易溶于甲醇、乙醇、乙醚、苯 略溶于石油醚、二硫化碳 不溶于水和甘油而溶于大多数非挥发性油。耐热、酸、碱。遇Fe、Cu、Co等可使其褪色 遇Pb形成沉淀。如作为粗品,往往含有辣椒红素约50%、辣椒玉红素约8.3%、玉米黄质约14%、β-胡萝卜素约13.9%、隐辣椒质约5.5%等等。残留溶剂≤0.003%,重金属(以Pb计)≤0.002%。可部分溶于乙醇,但可溶于大多数非挥发油类(或食用油)。折叠编辑本段物性数据1、性状:暗红至橙红色澄明液体,用乙醇抽提者其颜色比乙醚抽提物要暗。略黏,有强烈辛辣味,并有炙热感,可及整个口腔乃至咽喉(胡椒之辣主要在舌端,姜之辣主要在舌的边缘和背部)。2、溶解性:可部分溶于乙醇,溶于大多数非挥发性油。折叠编辑本段辣椒油树脂的提取辣椒油树脂又称辣椒精,是从辣椒中提取、浓缩而得到的一种油状液体,具有辣椒固有的强烈辛辣味。它除了含有辣椒的辛辣成分外,还含有辣椒醇、蛋白、果胶、多糖、辣椒色素等化学物质。折叠工艺流程原料处理→粉碎→连续浸提→蒸馏浓缩→含水油树脂。①原料处理。选用色红、味辣、无霉变的干辣椒,经60℃恒温干燥1.5小时后粉碎,过60目筛,分别收集、待用。②连续浸提。称取原料10克,置连续浸提装置中,用30毫升食用酒精溶液浸泡一段时间后让浸液流出,缓缓加入浸出液和50毫升新鲜溶剂,放置3小时后,打开底阀,控制流速每分钟2毫升,浸提液流完后,再加入20毫升新鲜溶剂,继续连续浸提。待连续浸提完后,压出原料中余液与浸提液合并。③蒸馏浓缩。提取液在70℃,80~85兆帕减压蒸馏。回收乙醇,去除部分水分,获得含油辣椒油树脂,置于称量皿中,先在60℃恒温干燥箱中浓缩2小时,再在105℃干燥至恒重,得辣椒油树脂。成品为暗红色黏稠液体,辛辣,折射率为1.3854,相对密度1.0628,pH值为5.2,黏度0.006帕。
[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=125076]丙二醇单甲醚乙酸酯的合成[/url]
各位大侠,本部门在开展自来水106项中二氯乙酸,三氯乙酸任务时,使用甲基叔丁基醚4mL萃取酸化后(pH2)40mL水样中的二氯乙酸,三氯乙酸,后取用其中2ml甲基叔丁基醚与2mL(10%硫酸酸化的)甲醇于45℃水浴中反应降温保护卤乙酸甲酯后,使用7mL150g/L的硫酸钠水溶液对其进行萃取问题来了,硫酸钠溶液萃取前,有机溶剂剩余4mL(甲醇2mL,甲基叔丁基醚2mL),萃取之后却发现有机相大大缩水,仅剩余1mL以下萃取的目的是为了除去有机相中的甲醇,保留甲基叔丁基醚,结果发现,大量甲基叔丁基醚消失,怀疑形成甲醇-甲基叔丁基醚-水共溶,因此,做了验证试验,加入2mL甲醇,2mL甲基叔丁基醚于分液漏斗,加入7mL150g/L硫酸钠溶液,摇晃后静置15min,期间不加热,不加酸,结果留下的有机相也仅为1mL。请教诸位达人,中是否可能形成甲醇-甲基叔丁基醚-水共溶,诸位在卤乙酸的gc检测预处理过程中采用何种方法??急求,在线等
[color=#444444]本人在做关于一株梭菌发酵产丁醇的实验,主要测乙酸丁酸乙醇丁醇,我实验室的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]是一台十分古老的仪器,型号是福立9710型,手动进样的,我用的条件是柱箱温度90℃,检测器温度180℃,进样器180℃,载气为N2,流速30 mL/min,可是并不知道程序升温如何设定,走出来的峰不是平头峰就是拖尾特别严重,而且各个组分还分不开。有没有大神指导一下各个条件该如何设置,最终走出来的样会特别好看的。。。我本人想到一个方法,就是由于我样品含有乙酸丁酸乙醇丁醇,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]分离这四个物质难度较大,我可以液相上乙酸丁酸的,[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]就检测乙醇丁醇,就是这样太繁琐了,0求大神帮我解决!!~~[/color]
各位色友:利用高效液相分析醇酸树脂中的醇和酸,关键如何进行前处理,请不吝赐教,谢谢!!!!
可以从红外上区分醇酸树脂是蓖麻油、亚麻油、桐油或大豆油4者中的某一个合成的吗?谢谢!
标准配法是吸取2ml乙酸正丁酯用60%乙醇定容到100ml,怎么从安瓿瓶中吸2ml出来?移液管都比安瓿瓶粗啊?

前几天同事扩项工作场所空气中饱和脂肪酸酯类物质包括乙酸甲酯,乙酸乙酯,乙酸丙酯,乙酸丁酯,标准是GBZ/T160.63-2007。柱子是SH-Rtx5(30m*0.32mm*0.25um),同事欲恒温同时分离这四种酯类,我提示乙酸乙酯,乙酸丙酯,乙酸丁酯混一起恒温做没事,如果乙酸甲酯也混一起做那么会与溶剂二硫化碳峰难分离,于是他计划先做乙酸乙酯,乙酸丙酯,乙酸丁酯再另外单独做乙酸甲酯。 乙酸乙酯,乙酸丙酯,乙酸丁酯色谱条件:岛津气相色谱GC2010PLUS 柱温60℃ 检测器进样器均为200℃ 分流比50 恒线速度22cm/shttp://ng1.17img.cn/bbsfiles/images/2017/01/201701191702_673938_2103464_3.jpg三种乙酸酯峰型还不错。接下来他说想试试乙酸甲酯在这个条件下出峰会怎么样?因为我之前用OV101做过二硫化碳中乙酸甲酯,它是紧挨着在二硫化碳前出峰,同时也用DB-FFAP做过它是在二硫化碳之后。SH-Rtx5极性比OV101强些 比DB-FFAP弱很多,那么在二硫化碳之前还是二硫化碳之后出峰呢? 看到甲乙丙丁突然有了一想法:不是有碳数规律吗?利用碳数规律推测乙酸甲酯的保留时间:保留时间:乙酸乙酯 2.854min 乙酸丙酯 3.562min 乙酸丁酯5.162min 二硫化碳2.612min碳数规律:lnt‘=An+C t’为调整保留时间 n为同系物中碳个数 A, C均为常数首先精确计算死时间:间隔均匀同系物 精确死时间计算公式:http://ng1.17img.cn/bbsfiles/images/2017/10/2016090616020890_01_2103464_3.pngtm=(2.854*5.162-3.562*3.562)/2.854+5.162-3.562-3.562=2.292min调整保留时间代入碳数规律公式:乙酸乙酯ln0.562=4A+C 乙酸丙酯 ln1.27=5A+C 求得乙酸甲酯调整保留时间lnt’=3A+C t’=0.249min乙酸甲酯的预测保留时间0.249+2.292=2.541min.这个保留时间在二硫化碳(2.612min)之前,两者仅仅相差0.07min。于是预测同条件下乙酸甲酯在二硫化碳之前出峰并且分离度不好!同条件实验做二硫化碳中乙酸甲酯3000ug/ml来验证:http://ng1.17img.cn/bbsfiles/images/2017/10/2016090616132954_01_2103464_3.jpg实验结果乙酸甲酯保留时间是2.571min与预测的2.541min比较符合,外推是有误差的,而且本例碳数不多,碳数多些会更准确。降低柱温至40℃,线速度15cm/s 乙酸甲酯与二硫化碳分离达到定量要求!http://ng1.17img.cn/bbsfiles/images/2016/09/201609061616_608604_2103464_3.jpg 结论:碳数规律还是比较准的,可以预测出峰情况。
戴安应用文献之-AN115 多肽中三氟乙酸的测定 TFA常用于制造过程中,从固相树脂洗脱出合成肽。TFA或乙酸也被用于肽的反相高效液相色谱纯化过程。TFA由乙酸和氟化物反应合成,因此TFA中存在乙酸和氟化物的残留。残留的TFA,氟化物以及乙酸在临床使用前后的肽中多少还是存在毒性的,因此不希望在肽中存在这三种物质。测定TFA,乙酸和氟化物对于肽的形成是合适的,这样能在制造过程中查证这三种阴离子已被消除掉。下载链接:http://www.instrument.com.cn/netshow/SH100244/paperDetail.asp?ID=12193