
内标跟着文献选的L-正亮氨酸,实验室正好有L-亮氨酸请问能用吗[img=,300,400]https://ng1.17img.cn/bbsfiles/images/2022/11/202211221916333293_727_5869599_3.jpg!w690x920.jpg[/img]
大家好,我们在进行蛋白质修饰鉴定过程中,发现有异亮氨酸甲基化的修饰(采用二级CID碎裂模式),分析软件(BioPharmaView)中给定的修饰中也含有异亮氨酸,为了确定甲基化修饰的机理,我们推测,甲基化修饰在了异亮氨酸形成的肽键N上,对此我们使用etHCD碎裂模式进行二级碎裂,结果显示,甲基化并非修饰在肽键N上,我们查询文献并没有相关的报道,想问下各位大神,有知道蛋白中异亮氨酸发生甲基化是发生在哪个位置么?如果有文献支持就更好了。
我用GC MS 测20种氨基酸,MSTFA衍生,不加溶剂,HP 5-MS柱,70度,1min到5度/min,300度,得到的脯氨酸和异亮氨酸是一个峰,降低浓度也分不开,做SIM也分不开,请问谁遇到过这种情况?如何解决?
哪位老师知道L-异亮氨酸的测定,请告知。谢谢!
如题!求助亮氨酸快速检测方法!现有硅胶板层析法,速度较慢,耗时1h,不知谁有好的方法?
[color=#444444]有没有哪位大侠做过叔亮氨酸的液相检测,文献里面查到1.用手性色谱柱,以2mM硫酸铜、5%异丙醇做流动相,流速1mL/min,254nm检测;2.同样是手性柱,用硫酸铜做流动相,检测波长为220nm。3.用C18柱,以0.25%磷酸二氢铵:甲醇=100: 5,检测波长205nm。4.另外有用OPA衍生后再检测的,检测波长340nm。由于目前没有标品,不知道叔亮氨酸的最大吸收波长在什么位置,叔亮氨酸上没有共轭结构,254nm检测是不是不靠谱啊?求有相关经验的大大指条明路[/color][img=,absmiddle]http://muchongimg.xmcimg.com/data/emuch_bbs_images/smilies/wink.gif[/img][img=,absmiddle]http://muchongimg.xmcimg.com/data/emuch_bbs_images/smilies/wink.gif[/img][color=#444444]另外听说手性柱金贵的很,求指教平时使用的注意点[/color][img=,absmiddle]http://muchongimg.xmcimg.com/data/emuch_bbs_images/smilies/biggrin.gif[/img]
[color=#444444]用OPA柱前衍生反向高效液相色谱测定L-叔亮氨酸的色谱图中出现了两个面积差不多的峰是什么原因?叔亮氨酸是手性氨基酸,流动相A用的是20mmol/ L 乙酸钠缓冲液,用1 %稀乙酸调p H 至71 2 流动相B ∶乙腈和甲醇混合液(1 ∶1),洗脱程序是等度洗脱,A:B是3:2. 求解释!!![/color]
我的产物是L-叔亮氨酸,但高效用的标品是其盐酸盐,请问会有什么影响?[em0808]
很多种类的极性化合物分离条件。 UDP-葡萄糖 UDP-葡萄糖、UDP-半乳糖、磷酸半乳糖 葡萄糖 蔗糖 红细胞中的UDP-葡萄糖、UDP-半乳糖、三磷酸腺苷(ATP) ADP-葡萄糖、CDP-葡萄糖 糖核苷酸 胞嘧啶、胸腺嘧啶、尿嘧啶、鸟嘌呤、腺嘌呤 三磷酸腺苷(ATP)、一磷酸腺苷(AMP) 黄嘌呤-磷酸、鸟嘌呤-三磷酸 体液中的黄嘌呤、尿酸、次黄嘌呤 色胺、五羟色胺、多巴胺 L-天冬氨酸、L-精氨酸 L-精氨酸、L-赖氨酸、L-组氨酸 谷氨酸、赖氨酸 亮氨酸、异亮氨酸 L-甲硫氨酸、L-谷氨酸 甲基琥珀酸、戊二酸、草酸、肌酸、4-羟脯氨酸、天冬氨酸、鸟氨酸 叶酸 抗坏血酸 胆汁酸 柠檬酸、马来酸、反式乌头酸 马来酸、富马酸 3-羟基肉桂酸 矮壮素、甲哌啶 苯海拉明 4-二甲氨基吡啶 草甘膦 三聚氰胺、三聚氰酸 胍
很多种类的极性化合物分离条件。 UDP-葡萄糖 UDP-葡萄糖、UDP-半乳糖、磷酸半乳糖 葡萄糖 蔗糖 红细胞中的UDP-葡萄糖、UDP-半乳糖、三磷酸腺苷(ATP) ADP-葡萄糖、CDP-葡萄糖 糖核苷酸 胞嘧啶、胸腺嘧啶、尿嘧啶、鸟嘌呤、腺嘌呤 三磷酸腺苷(ATP)、一磷酸腺苷(AMP) 黄嘌呤-磷酸、鸟嘌呤-三磷酸 体液中的黄嘌呤、尿酸、次黄嘌呤 色胺、五羟色胺、多巴胺 L-天冬氨酸、L-精氨酸 L-精氨酸、L-赖氨酸、L-组氨酸 谷氨酸、赖氨酸 亮氨酸、异亮氨酸 L-甲硫氨酸、L-谷氨酸 甲基琥珀酸、戊二酸、草酸、肌酸、4-羟脯氨酸、天冬氨酸、鸟氨酸 叶酸 抗坏血酸 胆汁酸 柠檬酸、马来酸、反式乌头酸 马来酸、富马酸 3-羟基肉桂酸 矮壮素、甲哌啶 苯海拉明 4-二甲氨基吡啶 草甘膦 三聚氰胺、三聚氰酸 胍
培养基制备(按1000ml计)1、 营养肉汤(Nutrient broth)培养基:牛肉膏3g,蛋白胨10g,NaCl 5g,加水至1000ml,pH7.2~7.42、 营养琼脂培养基(Nutrient agar)培养基: 牛肉膏3g,蛋白胨10g,NaCl 5g,琼脂15~20g,加水至1000ml,pH7.2~7.43、 肉汁葡萄糖培养基: 牛肉膏3g,蛋白胨10g,NaCl 5g,葡萄糖20g,琼脂15~20g,,pH7.2~7.44、 察氏培养基:NaNO32g,K2HPO4 1g,KCl 0.5g,MgSO4·7H2O 0.5g,FeSO4·7H2O 0.01g,蔗糖30g, 琼脂15~20g,加水至1000ml,pH自然5、 高氏一号培养基:可溶性淀粉20g,KNO31g,NaCl 0.5g, K2HPO4 0.5g, MgSO4·7H2O 0.5g,FeSO4·7H2O 0.01g, 琼脂20g,加水至1000ml,pH7.2~7.4。此培养基适用于多数放线菌,孢子生长良好,宜保藏菌种。制法:先用少量冷水将淀粉调成糊状,再取700ml水盛于烧杯中,在电炉上加热,沸腾时边搅拌边将淀粉糊倒入,待透明后再将其他成分加入,最后补足水分至1000ml.6、 无碳基础培养基(NH4)2SO4 5g,KH2PO4 1g,NaCl 0.1g, MgSO4·7H2O 0.5g,CaCl2 0.1g,酵母膏0.2g, 加蒸馏水至1000ml,pH6.5.加2%水洗琼脂即成固体培养基.于6.86×104Pa压力下灭菌20min.此培养基适用于测定酵母菌对碳源的利用(加待测碳源2%).7、 无氮基础培养基:葡萄糖20g, K2HPO4 1g, MgSO4·7H2O 0.5g,酵母膏 0.1g或20%豆芽汁20ml,水洗琼脂20g,加无氨蒸馏水至1000ml.pH6.5. 于6.86×104Pa压力下灭菌20min.此培养基适用于测定酵母菌对氮源的利用(加待测氮源0.5%).8、 营养缺陷型筛选用培养基⑴ 普通营养肉汤培养基⑵ 加倍营养肉汤培养基: 牛肉膏3g,蛋白胨10g,NaCl 5g,加水至500ml,pH7.2⑶ Vogel 50×(即浓缩50倍): MgSO4·7H2O 10g,柠檬酸100g,NaNH4HPO4·4H2O175g,KH2PO4·2H2O599.88g,K2HPO4·3H2O656.31g,加蒸馏水至1000ml.配置时先加水500ml,加热使药品溶解后,再定容1000ml.配好后放入冰箱备用.⑷ 固体基本培养基: Vogel 50×20ml,葡萄糖20g,水洗琼脂20g,加蒸馏水至1000ml,pH7.0,⑸ 2氮液体基本培养基:K2HPO4 7g,KH2PO4 3g,柠檬酸纳·3H2O 5g,MgSO4·7H2O 0.1g,(NH4)2SO4 2g,葡萄糖20g,加蒸馏水至1000ml,pH7.0, 于4.9×104Pa压力下灭菌20~30min.⑹ 无氮液体基本培养基:在⑸的配方中除去(NH4)2SO4即可.⑺ 混合氨基酸和混合维生素的配置:将氨基酸分为七组(如下表),其中六组各有6种氨基酸,每种氨基酸等量研细,充分混匀.若所选的氨基酸为DL型,则用量加倍.第七组只有一中氨基酸.第八组为混合维生素.Ⅰ 赖氨酸 精氨酸 甲硫氨酸 半胱氨酸 胱氨酸 嘌呤Ⅱ 组氨酸 精氨酸 苏氨酸 谷氨酸 天冬氨酸 嘧啶Ⅲ 丙氨酸 甲硫氨酸 苏氨酸 羟脯氨酸 甘氨酸 丝氨酸Ⅳ 亮氨酸 半胱氨酸 谷氨酸 羟脯氨酸 异亮氨酸 缬氨酸Ⅴ 苯丙氨酸 胱氨酸 天冬氨酸 甘氨酸 异亮氨酸 Ⅵ 色氨酸 嘌呤 嘧啶 丝氨酸 缬氨酸 酪氨酸Ⅶ 脯氨酸 Ⅷ 维生素B1 维生素B2 维生素B6 泛酸 对氨基苯甲酸 烟碱酸及生物素因脯氨酸容易潮解,所以单独列为第七组.把维生素B1、B2、B6、泛酸、对氨基苯甲酸(BAPA)、烟碱酸及生物素等量研细,充分混匀,配成混合维生素为第八组。

先简单 介绍——————做氨基酸 检测想了解详细资料,请自己到迪马科技官网自行下载http://simg.instrument.com.cn/bbs/images/brow/em09510.gifPITC柱前衍生法18种天然氨基酸分析(异硫氰酸苯酯柱前衍生法)——序列号: D0241 适用范围 该方法适用于氨基酸注射液、动植物性食品和饲料中 Asp(天冬氨酸)、Glu(谷氨酸)、Ser(丝氨酸)、Gly(甘氨酸)、His(组氨酸)、Arg(精氨酸)、Thr(苏氨酸)、Ala(丙氨酸)、Pro(脯氨酸)、Tyr(酪氨酸)、Val(缬氨酸)、Met(蛋氨酸)、Cys(胱氨酸)、Ile(异亮氨酸)、Leu(亮氨酸)、Phe(苯丙氨酸)、Trp(色氨酸)、 Lys(赖氨酸)等 18种天然氨基酸的检测http://ng1.17img.cn/bbsfiles/images/2012/03/201203131711_354396_2019107_3.jpg2 溶液配制 氨基酸储备液: 称取一定量氨基酸标准品,用 0.1 mol/L HCl水溶液溶解,胱氨酸为0.01 mol/L,酪氨酸为0.02 mol/L,其他氨基酸为 0.05 mol/L 氨基酸使用液: 将储备液用0.1 mol/L HCl水溶液稀释,得到浓度为 0.002 mol/L 的氨基酸单标和混标 内标液: 以正亮氨酸作为内标物。称取一定量正亮氨酸,溶于 0.1 mol/L HCl水溶液,得到 0.02 mol/L 的正亮氨酸内标液 异硫氰酸苯酯溶液: 将 250 μl 异硫氰酸苯酯用乙腈乙腈定容至 10 ml,得到0.2 mol/L 异硫氰酸苯酯溶液 三乙胺溶液: 将1.4 ml三乙胺用乙腈定容至 10 ml,得到1.0 mol/L 三乙胺溶液 标准溶液衍生化 量取 200 µl氨基酸混合标准溶液(每种组分浓度均为 0.002 mol/L),置于 1.5 ml塑料离心管中,准确加入20 μl正亮氨酸内标溶液、100 µl 1 mol/L三乙胺乙腈溶液和100 µl 0.2 mol/L 异硫氰酸苯酯乙腈溶液,混匀,室温反应 1 小时,然后加入正己烷 400 µl,旋紧盖子后剧烈振荡5~10 s,静置分层,取 200 µl下层溶液与 800 µl水混合,0.22 µm 针式过滤器过滤,待分析。注: 通过控制原始样品质量或稀释等方法,使样品溶液中的氨基酸总量不超过0.04 mol/L 或3.0 g/L(两者中取最小值) 只有采用内标法分析时,才需要加入正亮氨酸作为内标物 衍生得到的样品溶液中含有50%的乙腈,这与流动相溶剂体系存在较大差距,因而需要加水稀释,否则会引起峰前沿或分叉迪马科技AAA氨基酸柱子 洗脱条件 http://ng1.17img.cn/bbsfiles/images/2017/01/201701191656_646181_2019107_3.gifhttp://ng1.17img.cn/bbsfiles/images/2011/04/201104221943_290383_2019107_3.gif
[em09503][em09503][em09502]人体八种必须氨基酸(第一种较为顺口)1.“一两色素本来淡些”(异亮氨酸、亮氨酸、色氨酸、苏氨酸、苯丙氨酸、赖氨酸、蛋氨酸、缬氨酸)。2.“写一本胆量色素来”(缬氨酸、异亮氨酸、苯丙氨酸、蛋氨酸、亮氨酸、色氨酸、苏氨酸、赖氨酸)。3.鸡旦酥,晾(亮)一晾(异亮),本色赖。借来一两本淡色书。生糖、生酮、生糖兼生酮氨基酸:生酮+生糖兼生酮=“一两色素本来老”(异亮氨酸、亮氨酸、色氨酸、苏氨酸、苯丙氨酸、赖氨酸、酪氨酸),其中生酮氨基酸为“亮赖”;除了这7个氨基酸外,其余均为生糖氨基酸。酸性氨基酸:天谷酸——天上的谷子很酸,(天冬氨酸、谷氨酸)碱性氨基酸:赖精组芳香族氨基酸在280nm处有最大吸收峰色老笨---只可意会不可言传. 一碳单位的来源肝胆阻塞死 (甘氨酸、蛋氨酸、组氨酸、色氨酸、丝氨酸)。(色氨酸、酪氨酸、苯丙氨酸),顺序一定要记清,色 酪 苯丙,酶的竞争性抑制作用按事物发生的条件、发展、结果分层次记忆:1.“竞争”需要双方——底物与抑制剂之间;2.为什么能发生“竞争”——二者结构相似;3.“竞争的焦点”——酶的活性中心;4.“抑制剂占据酶活性中心”——酶活性受抑。糖醛酸,合成维生素C的酶古龙唐僧(的)内子(爱)养画眉(古洛糖酸内酯氧化酶)双螺旋结构的特点:右双螺旋,反向平行碱基互补,氢键维系主链在外,碱基在内维生素A总结V.A视黄醇或醛,多种异构分顺反。萝卜蔬菜多益善,因其含有V.A原。主要影响暗视觉,缺乏夜盲看不见,还使上皮不健全,得上干眼易感染。促进发育抗氧化,氧压低时更明显。DNA双螺旋结构:DNA,双螺旋,正反向,互补链。A对T,GC连,配对时,*氢键,,十碱基,转一圈,螺距34点中间。碱基力和氢键,维持螺旋结构坚。(AT2,GC3是指之间二个氢键GC间三个.螺距34点中间即3.4)RNA和DNA的对比如下:两种核酸有异同,腺鸟胞磷能共用。RNA中为核糖, DNA中含有胸。维生素B6B6兄弟三,吡哆醛、醇、胺。他们的磷酸物,脱羧又转氨。三羧酸循环乙酰草酰成柠檬,柠檬又成α-酮琥酰琥酸延胡索,苹果落在草丛中。β-氧化β-氧化是重点,氧化对象是脂酰,脱氢加水再脱氢,硫解切掉两个碳,产物乙酰COA,最后进入三循环。酮体酮体一家兄弟三,丙酮还有乙乙酸,再加β-羟丁酸,生成部位是在肝,肝脏 生酮肝不用,体小易溶往外送,容易摄入组织中,氧化分解把能功
芴甲氧羰酰氨糖的分离,用什么展开剂啊?氨糖 我用芴甲氧羰酰氯酰化了,应该是在氮上接了酰化剂,请教高手,用什么展开剂可以 分离。两个氨糖只有2位一个羟基的区别。一个在2位上多一个羟基。
有关单位: 经国家食品药品监督管理局化妆品审评专家委员会审核,拟批准“二甲氧基甲苯基-4-丙基间苯二酚”和“聚甲基丙烯酰基赖氨酸”作为化妆品原料使用。现公开征求意见,请于2011年6月27日前将反馈意见电子版发送至chenzh@sfda.gov.cn。 附件:1.“二甲氧基甲苯基-4-丙基间苯二酚”技术要求 2.“聚甲基丙烯酰基赖氨酸”技术要求 国家食品药品监督管理局食品许可司 二〇一一年六月十五日
1. 葡萄汁粉 美国克里斯塔尔斯国际公司开发生产葡萄汁粉新产品,商品名为CrgsTalsTM,由天然成分深紫色+葡汁粉71%(固形物)组成,固形物成分中含有高抗氧化作用的Vc,该保健产品有增强心血管功能、强化营养功能及抗病防病功能。 CrgsTalsTM采用冷冻干燥法制造,在无氧条件下用非热处理法连续生产,经干燥后产品含水量仅2.5%以下,产品耐藏保质性好,在21℃以下可保存2年,广泛应用于焙烤食品、婴儿食品、冷冻食品、营养辅助食品、饮料、沙司、浸渍食品及混合乳制品中。 2. 椰浆粉 菲律宾利用椰子精汁制成椰浆粉,为天然不含防腐剂与人造着色剂的新型食品添加剂,赋予食品椰子类产品纯天然风味与更佳口感,可加到咖喱、椰饭、甜品、饼干、布丁、椰子果浆、糕点、面包、饮料、冷饮品、蛋糕、巧克力、糖果、奶茶、调味料等食品中。 椰浆粉制造是用新鲜椰果去除椰壳、椰皮后的椰肉、除去黑膜,加以破碎、榨汁,高温干燥处理加工成白色粉。椰浆粉加工要求严格,整个操作在无菌化条件下进行,采用的是先进的高压瞬间灭菌设备。使用新鲜椰果,从采摘后到加工产品时间不超过2小时。产品应用广、市场潜力大。 3. 儿茶素纯品 上海诺德生物实业有限公司开发生产天然高活性儿茶素纯品,纯度高达99%,可作医药、食品的添加剂,有抑制和抵抗病毒细菌、抑制和预防心血管病、预防和消灭癌细胞、预防和治疗锶、钴等辐射危害、延缓衰老等效用,还有除臭、防褪色、降血脂、降血压、减肥、防糖尿病、防血栓、解毒、治牙周病、防晒、防皮肤起皱纹功效,应用于饮料、糖、谷物、乳品、调味品、营养品、减肥食品等中作营养剂、保鲜剂、抗氧化剂、除臭剂等。 4. 罗汉果苷糖 美国宝洁公司以罗汉果为原料提取得到罗汉果苷糖,是一种高甜度低热量甜味剂,其甜度为蔗糖的300—350倍,热量仅为蔗糖的1/5。该苷糖在水中溶解性好,热稳定性高,在100℃水溶液中很稳定,120℃高温下也不会破坏。它不被微生物发酵,因此有利于食品的加工与储存。可直接冲饮或作医药品、保健食品、食品的甜味剂,是糖尿病人、肥胖症、高血压、心脏病患者最适用的甜味剂及保健品。 罗汉果苷糖提取法:罗汉果清洗→去皮核→用去离子水提取→酶解→酸化→匀浆→过滤→浓缩→干燥→大孔径树脂纯化→进一步精制→罗汉果甜苷提取物(成品)。 5.乳清蛋白 乳清蛋白有良好的成胶性、水中分散性及乳化稳定性、泡沫稳定性,营养价值也高,是所有天然蛋白中支链氨基酸—亮氨酸、异亮氨酸、缬氨酸含量最高的;还含有含硫氨基酸半胱氨酸、蛋氨酸,能维持人体的抗氧化剂水平;含有精氨酸、赖氨酸,能刺激生长激素生长,减少脂肪,增强肌肉;含有谷酰胺,能预防过劳造成的免疫力下降;乳清蛋白中含高生物钙,每100g中含800mg钙。乳清蛋白高营养,易消化,多功能,益健康,是饮料(乳基饮料、运动饮料、茶饮料、益生菌饮料、乳品饮料)的最适用配料,可代替部分脱脂奶粉。 6. 新型糖果脂肪 巴西圣保罗大学研究从树果Copuassu中提取出新型糖果脂肪Copuassu脂肪,具有多晶型的特性,在温度24—25℃可产生晶体,含有的甘油三酯量接近可可脂,可代替可可脂添加到巧克力中。它能使巧克力更柔软,还能提高其质量。 7. 米制糖浆系列甜味剂 美国利用精白米、糙米或有机米为原料,用酶解法制成米制糖浆系列产品。产品有(1)DE值(葡萄糖)26的糊精糖浆,黏度高,只有细微甜味,有黏着性。应用于挤压加工的膳食纤维和冷冻甜食的制作,可提高其冻结点;(2)DE42—50的高麦芽米制糖浆,含高麦芽糖,应用于挤压加工的食品及硬糖、糕点、甜食中,口感润滑、爽口、味甜;(3)DE42—60的米糖浆,作大豆饮料、糕点类、早餐谷物与焙烤类制品,有良好甜味与润滑感;(4)DE70的高葡萄糖米糖浆,黏度低,应用于早餐谷物、沙司、调味料及大豆制品中作甜味剂,又有降低冻结点效果。 8. 花生种皮提取物 日本常磐植物化学研究所开发从花生种皮中提取加工成粉末状的花生种皮提取物,并应用于食品和饮料中作功能性食品材料。 该产品含有藤黄菌素、芦丁、异鼠李醚配糖体等黄酮化合物和β-谷甾醇及其配糖体、原花青素甙等多种活性成分,有抗氧化作用、阻碍透明质酸酶作用、阻碍蛋白质糖化反应和抗艾滋病作用等。其中阻碍透明质酸酶作用可有效防治花粉症、过敏性皮炎和风疹块等过敏疾病。产品受到国际市场关注。
供 参考吧葡萄酒中总二氧化硫的测定及葡萄酒质量简介 近年来,国家统计局数据,2009年全国全年葡萄酒产量为96万吨;中国大陆地区实现进口从2000年的20万升上涨至2009年的1,370万升,共翻了68倍,2010年河北省产量增加至9,952万升。葡萄酒越来越成为重要的新兴产业,而葡萄酒的生产与销售呈现加速兴旺的发展势头,越来越成为人们喜欢的健康饮品,葡萄酒的质量对人民健康的影响也越来越大。因为葡萄酒有益健康具有较高的保健价值,越来越多地摆上人们的餐桌,成为人们享受生活的一种方式。 葡萄酒指用葡萄发酵酿制成的含有酒精的天然健康饮品。我国明朝药物学家李时珍在《本草纲目》中曾记载了葡萄酒具有“暖腰肾,驻颜色,耐寒”的功效。近代的测试已证实:约有几百种化合物存在于葡萄酒中,其中包括糖类、氨基酸(含有人体自身不能合成的8种“必需氨基酸”)(异亮氨酸、色氨酸、亮氨酸、缬氨酸、赖氨酸、苏氨酸、苯丙氨酸、蛋氨酸)矿物质(如铁、锌、铜、锰、碘、铬等)、含有抗氧化成分和丰富的酚类化合物(约有200多种)、含有较多的抗氧化剂(花色苷、前花青素、单宁等)、白藜芦醇(防止正常细胞癌变,并能抑制癌细胞的扩散),特别是唯一的碱性酒精性饮品,所以人们把葡萄酒称为“天然氨基酸食品”,并被联合国卫生食品组织批准为最健康、最卫生的食品。 一、葡萄酒的术语和定义1.1葡萄酒的分类按我国标准GB15037—2006,葡萄酒的定义为“以鲜葡萄或葡萄汁为原料,经全部或部分发酵酿制而成的,含有一定酒精的发酵酒”。可以分为:1.1.1从二氧化碳含量上:分为平静葡萄酒和起泡葡萄酒,通常饮用的是平静葡萄酒(比如香槟属于起泡葡萄酒)。1.1.2从颜色看分为3种:红葡萄酒:是用皮红肉白或皮肉皆红的葡萄带皮发酵而成,酒液中含有果皮或果肉中的有色物质,使之成为以红色调为主的葡萄酒。白葡萄酒:用白皮白肉或红皮白肉的葡萄经去皮发酵而成。桃红葡萄酒:用带色葡萄经部分浸出有色物质发酵而成,它的颜色介于红葡萄酒和白葡萄酒之间,主要有桃红色、浅红色、淡玫瑰红色等。1.1.3、从含总糖量分为4种:干葡萄酒(dry wines):含糖(以葡萄糖计)小于或等于4.0 g/L的葡萄酒。或者当总糖与总酸(以酒石酸计)的差值小于或等于2.0 g/L时,含糖最高为9.0 g/L的葡萄酒。半干葡萄酒(semi-dry wines):含糖大于干葡萄酒,最高为12.0 g/L的葡萄酒。或发总糖与总酸(以酒石酒计)的差值小于或等于2.0 g/L时,含糖最高为18.0 g/L的葡萄酒。半甜葡萄酒(semi-sweet wines):含糖大于半干葡萄酒,最高为45.0 g/L的葡萄酒。甜葡萄酒(sweet wines):含糖大于45.0 g/L的葡萄酒。 如果感兴趣大家可以查阅《GB/T 15037-2006 葡萄酒》这个标准中的详细介绍。 二、感官要求项目要求外观色泽白葡萄酒近似无色、微黄带绿、浅黄、禾杆黄、金黄色红葡萄酒紫红、深红、宝石红、红微带棕色、棕红色桃红葡萄酒桃红、淡玫瑰红、浅红色澄清程度澄清,有光泽,无明显悬浮物(使用软木塞封口的酒允许有少量软木渣,装瓶超过1年的葡萄酒允许有少量沉淀)[tr
蛋白胨水培养基( l )成分 蛋白胨 10g 水 l000ml 氯化钠 5g ( 2 )制法 取上述成分混合,微温使溶解,调pH 值使灭菌后为7.3 士0.1 ,分装于小试管,121 ℃ 灭菌15 分钟。( 3 )用途 用于鉴别细菌能否分解色氨酸而产生靛基质的生化反应。 ① 靛基质试验取可疑菌落或斜面培养物,接种于蛋白胨水培养基中,置35 ℃ 培养24~48 小时,必要时培养4~5 天,沿管壁加人靛基质试液数滴,液面呈玫瑰红色为阳性,呈试剂本色为阴性。 ② 靛基质试液 称取对二甲氨基苯甲醛5g ,加入戊醇(或异戊醇)75ml ,充分振摇,使完全溶解后,再取盐酸25ml 徐徐滴入,边加边振摇,以免骤热导致溶液色泽变深.或称取对二甲氨基苯甲醛1g ,加人95 %乙醇95ml ,充分振摇,使完全溶解后,再取盐酸20ml 徐徐滴入。
国内最大最专业的国家标准物质服务平台坛墨质检-国家标准物质中心(北京坛墨质检科技有限公司),是国家质检总局指定的国家标准物质研制单位,是国内最大最专业的食品、环境、职业卫生标准物质生产商和服务商。 产品编号 产品名称 标准值 BW4061 维生素E醋酸酯标准品,有证书 99.90% BW4060 L-天门冬氨酸标准品,有证书 99.60% BW4059 D-棉籽糖标准品,有证书 98.00% BW4058 L-谷氨酸标准品,有证书 99.90% BW4057 水杨酸钠标准品,有证书 99.30% BW4056 低聚果糖-蔗果五糖标准品,有证书 94.80% BW4055 低聚果糖-蔗果四糖标准品,有证书 99.20% BW4054 低聚果糖-蔗果三糖标准品,有证书 99.90% BW4053 D-麦芽糖标准品,有证书 98.00% BW4052 柠檬酸标准品,有证书 99.80% BW4051 L-亮氨酸标准品,有证书 98.00% BW4050 D-苹果酸标准品,有证书 99.50% BW4049 L-茶氨酸标准品,有证书 98.00% BW4048 乳糖标准品,有证书 98.00% BW4048 乳糖标准品,有证书 98.00% BW4047 木糖标准品,有证书 99.50% BW4046-1 果糖成分分析标准物质,有证书 99.50% BW4045 水合物糖精钠标准品,有证书 99.90% BW4044 乙酰苯胺标准品,有证书 99.50% BW4043-1g 蔗糖标准品,有证书 ≥98% BW4043 蔗糖标准品,有证书 99.70% BW4042 维生素D3标准品,有证书 99.00% BW4041 维生素D2标准品,有证书 98.00% BW4040 维生素B1标准品,有证书-(盐酸硫胺) 99.00% BW4039 维生素K1标准品,有证书 99.90% BW4038 甜蜜素标准品,有证书 99.50%
“格瓦斯”是以面包等为底物,经酵母菌和乳酸菌发酵而生产的饮品,具有丰富的营养,它的酒精度一般低于1%,因此不同于啤酒,不属于酒类。格瓦斯中所含的二氧化碳是自然发酵而产生的,而非充加二氧化碳,因此也不属于碳酸型饮料。 目前市场上有发酵格瓦斯产品,也有格瓦斯饮料。格瓦斯饮料是以麦芽汁、面包浸汁或果汁为原料,再配以各种添加剂(防腐剂、甜味剂、香料、色素等)并冲加碳酸水而生产,有的经发酵,有的不经发酵,没有发酵格瓦斯所具有的丰富营养和健康价值,不能称为发酵格瓦斯。 发酵格瓦斯是由酵母和乳酸菌发酵的产品,所以其香味主要源自于所用菌种发酵过程中的代谢物,如醇、醛、酸、酮等的呈味物质,这些不同性质的化合物会发生极其复杂的化学反应,最终形成复合香味,其中乙酸乙酯是主体香味;此外还有所用原料的香味。因此,发酵格瓦斯的香味非常浓郁怡人。而格瓦斯饮料的口味主要来自添加剂和原料。 格瓦斯营养成分的种类有碳水化合物、蛋白质、维生素、有机酸和微量元素等。 碳水化合物中有麦芽糖、葡萄糖、果糖、蔗糖等。格瓦斯的干物质含量按标准规定为5.6%,有的为7.3%。蛋白质含量为2克/升。氨基酸含量为202.2毫克/升,其中含量高者有缬氨酸、亮氨酸、异亮氨酸、赖氨酸、苏氨酸、蛋氨酸(26.6毫克/升)、谷氨酸(24.8毫克/升)、苯丙氨酸(22.2毫克/升)、谷氨酸(24.8毫克/升)。而格瓦斯饮料中的氨基酸含量仅为8.7毫克/升,比发酵格瓦斯少二十多倍。格瓦斯所含维生素有维生素C、维生素B1、维生素B2、维生素P和维生素D。格瓦斯所含有机酸有乳酸、醋酸、柠檬酸等,其含量为3克/升。格瓦斯所含矿物质元素有钙、磷、铁、铜、锰、钼、锌、钴等。每100毫升格瓦斯的热量约30千卡。 格瓦斯中的二氧化碳是由酵母菌和乳酸菌在发酵过程中产生的,为天然成分。当二氧化碳从体内呼出时,会将体内热量带出,赋与人以清凉感,与此同时还会将格瓦斯的香味成分带出来,使人感到怡人的香味。但现代医学中,对二氧化碳是有争议的,认为高含量二氧化碳对人的消化系统有损害,二氧化碳从胃里向上返出后,会刺激食道,导致胃炎等疾病风险,所以饮料中二氧化碳含量不宜过高。格瓦斯二氧化碳含量以0.3%—0.4%为宜,可以保证泡沫的高度和稳定性,而且口感也很好。
一、常规理化项目及营养成分测试项目检测项目项目内容理化指标干燥失重、灼烧残渣、水分、灰分、红外鉴别、旋光度、密度、净含量、比体积、膨胀率、酸价、过氧化值等宏量营养素碳水化合物总碳水化合物,单糖、二糖、低聚糖、多糖蛋白质总蛋白 必需氨基酸:赖氨酸、蛋氨酸、亮氨酸、异亮氨酸、苏氨酸、缬氨酸、色氨酸、苯丙氨酸 非必需氨基酸: 谷氨酸、丙氨酸、甘氨酸、天门冬氨酸、胱氨酸、脯氨酸、丝氨酸和酪氨酸等。脂肪甘油三脂 磷脂:卵磷脂、脑磷脂、肌醇磷脂。糖脂:脑苷脂类、神经节昔脂。脂蛋白:乳糜微粒、极低密度脂蛋白、低密度脂蛋白、高密度脂蛋白。类固醇:胆固醇、麦角因醇、皮质甾醇、胆酸、雄激素、雌激素、孕激素。膳食纤维总可溶性膳食纤维、总不可溶性膳食纤维 纤维素、半纤维素、果胶、树胶、木质素、抗性淀粉等微量营养素维生素脂溶性维生素A、D、E、K 水溶性维生素B族维生素、维生素C、维生素PP等矿物元素常量元素:钙、磷、钾、钠、镁等微量元素:铁、锌、铬、锰、钴、镍、氟、碘、硒等二、食品添加剂和非食品物质检测项目检测项目项目内容食品添加剂甜味剂糖精钠、甜蜜素、甜味素、木糖醇、山梨糖醇、甘露糖醇等防腐剂苯甲酸钠、山梨酸钾、纳他霉素、丙酸钙、雷帕霉素、富马酸单甲酯等抗氧化剂没食子酸丙酯(PG)、叔丁基羟基茴香醚(BHA)、2,6-二叔丁基对甲酚(BHT)、特丁基对苯二酚 (TBHQ)等漂白剂亚硫酸盐、二氧化硫等有机酸草酸、酒石酸、柠檬酸、苹果酸、甲酸(蚁酸)、乳酸、乙酸(醋酸)、丁二酸色素合成色素:苋菜红、胭脂红、柠檬黄、日落黄和靛蓝等天然色素:姜黄素、红花黄色素、辣椒红素、虫胶色素、红曲米、酱色、甜菜红、叶绿素铜钠盐和β—胡萝卜素等增稠剂明胶、酪蛋白酸钠、阿拉伯胶、罗望子多糖胶、田菁胶、琼脂、海藻酸钠、卡拉胶 、果胶、黄原胶、β-环状糊精、羧甲基纤维素钠、淀粉磷酸酯钠、羧甲基淀粉钠、羟丙基淀粉、藻酸丙二醇酯(PGA)乳化剂脂肪酸单甘油脂、蔗糖酯、山梨糖醇脂、大豆磷脂、月桂酸单甘油酯、丙二醇脂肪酸酯等保湿剂三聚磷酸盐、多聚磷酸盐非食用物质三聚氰胺、盐酸克伦特罗、莱克多巴胺、沙丁胺醇、己烯雌酚、解抗剂、苏丹红(1—4号)、甲醛次硫酸氢钠(吊白块)、碱性橙Ⅱ(王金黄、块黄)、硼酸、硼砂、硫氰酸钠、美术绿、孔雀石绿和结晶紫、碱性嫩黄、酸性橙、玫瑰红(罗丹明)B、工业用甲醛、工业用火碱、一氧化碳、硫化钠、工业硫磺、工业染料、罂粟壳、皮革水解物、溴酸钾、金玉兰酶制剂、富马酸二甲酯、动物水解蛋白、硫氰酸根等三、农药残留检测项目检测项目检测内容有机氯农药六六六、滴滴涕、五氯硝基苯、艾氏剂、七氯、狄氏剂、异狄氏剂等有机磷农药敌敌畏、敌百虫、克线丹、地亚农、对硫磷、甲基对硫磷、甲胺磷、乙酰甲胺磷、甲拌磷、乙硫磷、甲基异柳磷、喹硫磷、马拉硫磷、乐果、氧化乐果、二嗪磷、久效磷、倍硫磷、毒死蜱、甲基毒死蜱、甲基嘧啶磷、磷胺、杀扑磷、杀螟硫磷、亚胺硫磷、蝇毒磷等氨基甲酸甲酯类农药西维因、涕灭威、呋喃丹、抗蚜威、速灭威、残杀威、叶蝉散、异丙威等拟除虫菊酯类农药联苯菊酯、二氯苯醚菊酯、功夫菊酯、溴氰菊酯、氰戊菊酯、氟氯氰菊酯、甲氰菊酯、氯氰菊酯、顺式氯氰菊酯、高效氯氰菊酯、氰戊菊酯、顺式氰戊菊酯、溴氰菊酯等其他砜嘧磺隆、甲胺基阿维菌素苯甲酸盐、啶酰菌胺、霜脲氰、环酰菌胺、氟胺磺隆、吡蚜酮、醚苯磺隆量、八氯二苯醚量、灭虫灭死量四、兽药残留检测项目检测项目检测内容硝基呋喃类呋喃它酮、呋喃妥因、呋喃西林、呋喃唑酮沙星类依诺沙星、氧氟沙星、诺氟沙星、培氟沙星、环丙沙星、洛美沙星、丹诺沙星、恩诺沙星、沙拉沙星、双氟沙星、司帕沙星四环素族金霉素、土霉素、四环素、强力霉素磺胺类药物磺胺醋酰、磺胺甲噻二唑、磺胺二甲异噁唑、磺胺氯哒嗪、磺胺嘧啶、磺胺甲基异噁唑、磺胺噻唑、磺胺-6-甲氧嘧啶、磺胺甲基嘧啶、磺胺邻二甲氧嘧啶、磺胺吡啶、磺胺对甲氧嘧啶、磺胺甲氧哒嗪、磺胺二甲嘧啶、磺胺苯吡唑、磺胺间二甲氧嘧啶其他氯霉素、杆菌肽锌、阿维菌素、喹乙醇、孔雀石绿和结晶紫、己烯雌酚、盐酸克伦特罗和莱克多巴胺、氯羟吡啶、尼卡巴嗪、克球酚、恶喹酸、金刚烷胺、利巴韦林、地克珠利、妥曲珠利、癸氧喹酯五、食品毒害物质检测检测项目项目内容重金属镉Cd、铬Cr、铅Pb、砷As、汞Hg、重金属总量硝酸盐类硝酸盐、亚硝酸盐生物毒素黄曲霉素M1、B1、B2、G1、G2、呕吐毒素、赭曲霉毒素A、T-2毒素、玉米赤酶烯酮、微囊藻毒素-LR其他毒害物质丙烯酰胺、二甲基亚硝胺、二乙基亚硝胺其他污染物六氯苯、烷基汞六、微生物检测检验项目项目内容
蛋白质分子量肌球蛋白甲状腺球蛋白β-半乳糖苷酶副肌球蛋白磷酸化酶a血清白蛋白L-氨基酸氧化酶地氧化氢酶丙酮酸激活酶谷氨酸脱氢酶亮氨酸氨肽酶γ-球蛋白,H链延胡索酸酶(反丁烯二酸酶)卵白蛋白醇脱氢酶(肝)烯醇酶醛缩酶肌酸激酶胃蛋白酶原D-氨基酸氧化酶醇脱氢酶(酵母)甘油醛磷酸脱氢酶原肌球蛋白乳酸脱氢酶胃蛋白酶转磷酸核糖基酶天冬氨酸氨甲酰转移酶,C链羧肽酶 A碳酸酐酶枯草杆菌蛋白酶γ-球蛋白,L链γ-blobulin,L chain糜蛋白酶原(胰凝乳蛋白酶原)木瓜蛋白酶(羧甲基)β-乳球蛋白[font=Tim
南瓜的营养分析 营养分析 每100克含蛋白质0.6克,脂肪1克。碳水化合物5.7克,粗纤维1.1克,灰分6克,钙10毫克,磷32毫克,铁0.5毫克,胡萝卜素0.57毫克,核黄素0.04毫克,尼克酸0.7毫克,抗坏血酸5毫克。此外,还含有瓜氨素、精氨酸、天门冬素、葫芦巴碱、腺嘌呤、葡萄糖、甘露醇、戊聚糖、果胶。 南瓜中对人体的有益成分有:多糖、氨基酸、活性蛋白类胡萝卜素及多种微量元素等。各种成分的功用: 1. 多糖类:南瓜多糖是一种非特异性免疫增强剂,能提高机体免疫功能,促进细胞因子生成,通过活化补体等途径对免疫系统发挥多方面的调节功能。 2. 类胡罗卜素:南瓜中丰富的类胡萝卜素在机体内可转化成具有重要生理功能的维生素A,从而对上皮组织的生长分化、维持正常视觉、促进骨骼的发育具有重要生理功能。 3. 矿质元素:南瓜中高钙、高钾、低钠,特别适合中老年人和高血压患者,有利于预防骨质疏松和高血压。此外,还含有磷、镁、铁、铜、锰、铬、硼等元素。 4. 氨基酸和活性蛋白:南瓜中含有人体所需的多种氨基酸,其中赖氨酸、亮氨酸、异亮氨酸、苯丙氨酸、苏氨酸等含量较高。此外,南瓜中的抗坏血酸氧化酶基因型与烟草相同,但活性明显高于烟草,表明了在南瓜中免疫活性蛋白的含量较高。 5. 脂类物质:研究发现,在南瓜种子中的脂类物质对泌尿系统疾病及前列腺增生具有良好的治疗和预防作用。
黄精为百合科黄精属植物滇黄精Polygonatμm kingianum Coll. et Hemsl.、黄精P. sibiricum Delar. ex Redoute、多花黄精P. cyrtonema Hua的干燥根茎。黄精富含多糖、多酚、皂苷、氨基酸等活性物质和各种微量元素。传统中医认为黄精具有好颜色、润泽,除风湿、安五脏,久服轻身、延年、不饥等药效,可炮制后直接食用,或煎熬成汁而服。现代药理学研究表明,黄精具有预防糖尿病、抑制癌症、治疗老年痴呆、抗炎抗菌、抗氧化活性、增强免疫力、预防骨质疏松等功效[1-3]。 鲜黄精有强烈刺激性,能致使口舌麻木,故需炮制,方可入药或食用。黄精的炮制过程必然伴随着物质成分的变化,多数研究都针对各地产黄精的五羟甲基糠醛(5-hydroxymethylfurfural,5-HMF)、多糖、皂苷、浸出物含量变化上进行讨论[4-8]。滇黄精产品和市场份额在黄精品种中占比最大,主产于云南,在《滇南本草》《云南植物志》中均有记载,是一味重要的“云药”[7]。滇黄精与黄精和多花黄精具备相似的生理活性,如抗氧化、降血糖、增强免疫力等功效。但是滇黄精炮制工艺众多,炮制过程中化学成分变化规律不清晰,亟待解决。 代谢组学是近年来新兴的一门组学技术,应用高通量检测和数据处理相结合,来分析整体代谢物的变化,进而推测其背后的生理和病理机制[9]。由于代谢组学的整体观与多组分、多靶点的特点相一致,为植物学和食品功能营养学研究提供了有力的工具[10]。代谢组学不仅在阐明植物生长过程中的生理、病理现象和代谢途径方面发挥着重要作用,而且在分析采后加工功能成分的代谢变化机制方面也发挥着重要作用。 本实验以滇黄精为研究对象,采用传统“九蒸九晒”炮制工艺,以分光光度检测、HPLC和代谢组等技术研究炮制过程化学物质变化规律以探究炮制机制,以期揭示炮制过程中物质变化规律,为滇黄精炮制工艺的规范化、炮制品质量的标准化提供理论依据。 1 仪器与试药 1.1 仪器 TU-190型双光束紫外可见分光光度计,上海析谱仪器有限公司;SHZ-DIII型循环水式真空泵,巩义市于华仪器有限责任公司;DHG-9070A型台式鼓风干燥箱,上海东麓仪器设备有限公司;ZL2-80A型超声波清洗器,上海左乐仪器有限公司;Applied Biosystems 4500 QTRAP型串联质谱,美国赛默飞公司;Agilent 1200型高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],美国安捷伦公司。 1.2 材料与试剂 天冬氨酸(Asp)、谷氨酸(Glu)、丝氨酸(Ser)、组氨酸(His)、甘氨酸(Gly)、苏氨酸(Thr)、精氨酸(Arg)、丙氨酸(Ala)、酪氨酸(Tyr)、半胱氨酸(Cys)、甲硫氨酸(Met)、苯丙氨酸(Phe)、异亮氨酸(Ile)、亮氨酸(Leu)、赖氨酸(Lys)、脯氨酸(Pro),批号5061-3330,规格1 nmol/μL,1 mL/支,标准品购自安捷伦公司;齐墩果酸(批号SO8030,规格20 mg,质量分数≥98%)、没食子酸(批号SG8040,规格20 mg,质量分数≥98%)、芦丁(批号SR8250,规格20 mg,质量分数≥98%)、D-无水葡萄糖(批号G8150,规格250 g,质量分数≥99.8%)对照品购自索莱宝生物科技有限公司;色谱级甲醇、乙醇、乙腈购自德国默克(Merck)公司;其余试剂均为国产分析纯。 滇黄精药材,3年生,采收于2022年10月,采自云南普洱,经云南农业大学农学与生物技术学院杨生超教授鉴定,为百合科黄精属植物滇黄精P. kingianum Coll. et Hemsl.的干燥根茎。 2 方法与结果 2.1 滇黄精炮制样品的制备 将滇黄精去杆,清洗干净晾干去皮,切至3 mm厚的薄片,用蒸汽蒸制4 h,最后放入鼓风干燥箱风干至含水量≤8%,得到滇黄精原料干片。 原料干片与黄酒5∶2混合后,需要待黄酒被吸收完全后,利用蒸汽蒸制4 h,焖润5 h,自然晾晒干燥至含水量≤15%即可,重复9次,新鲜样品编号S0,每蒸晒1次进行取样,编号S1~S9,得到“九蒸九晒”的炮制样品,备用。记录滇黄精炮制过程中外观变化。《食疗本草》[11]记载:“蒸之若生,则刺人咽喉。曝使干,不尔朽坏”。生黄精味干,咀嚼后舌根味麻,咽喉刺痛,几乎无甘甜味。九蒸九制后成品气味浓郁,入口甜酸味为主,略带苦味,无麻味,咽喉无刺激感,质地软糯有韧劲。 如图1所示,生滇黄精(S0)为黄白色,具有麻味,随着炮制次数的增加,样品颜色越来越深,在第3蒸(S3)之后颜色变化不明显,变成了黑褐色,第4蒸(S4)之后麻味消失,产生甜味,在第7蒸(S7)之后逐渐产生苦味和酸涩味。有研究表明,热处理可以改变样品的颜色并影响所得产物的质量[12],这与美拉德反应有关。 图片 2.2 总多糖、总皂苷、总多酚、总黄酮和游离氨基酸的含量测定 2.2.1 总多糖 多糖具有控制血糖、抑制癌症等活性,是黄精重要的药效物质[13]。参考Su等[14]的苯酚-硫酸法并稍作改动,测定滇黄精中总多糖含量。精确称量0.1 g滇黄精干粉,置于圆底烧瓶中,加入30 mL 80%乙醇水溶液,沸水浴冷凝回流加热1 h。取出后滤过,去除滤液,留固体和滤纸一并塞回圆底烧瓶中,加入30 mL纯水,再次沸水浴冷凝回流加热1 h,滤过,取滤液,定容到50 mL,即为待测液。取待测液0.5 mL,加入1.5 mL纯水稀释4倍,配制为检测液。取2 mL检测液,按照上述方法进行检测。实验重复3次,计算总多糖含量。由表1可知,随着炮制次数的增加,总多糖质量分数显著降低(P<0.05)。总多糖质量分数在S1后显著降低,S2~S8蒸制过程中,总多糖质量分数无明显波动,S9又显著减少。S0中总多糖质量分数为(198.39±17.96)mg/g,S9中总多糖质量分数为(66.31±25.12)mg/g,下降66.58%。结果与杨圣贤等[15]研究相比,总体质量分数变化趋势基本吻合,在前2次蒸制过程中多糖质量分数明显减少(P<0.05),S2~S9中总多糖质量分数变化趋于稳定,在小范围内波动,且之间没有显著差异。 2.2.2 总皂苷 皂苷具有抗菌、抗肿瘤等药理活性,也是黄精中重要的活性物质,在药物和功能性食品中具有广阔的应用前景[16]。参考苑璐等[17]建立的香草醛-高氯酸-冰乙酸法,以齐墩果酸作为对照品,测定皂苷含量。精确称量1.0 g滇黄精干粉,置于锥形瓶中,加入30 mL 80%乙醇溶液,60 ℃水温,超声处理1 h。滤过,取滤液定容到50 mL,即为检测液。取检测液100 μL,挥干溶剂,按照上述方法进行检测,实验重复3次,计算含量。由表1可知,滇黄精皂苷质量分数在前2次蒸制过程中无显著性差异,在S3和S4蒸制时显著上升(P<0.05),之后的蒸制过程中质量分数基本保持不变。S0中皂苷质量分数为(33.65±3.04)mg/g,S9中皂苷质量分数为(75.49±4.66)mg/g,增长2.24倍,其质量分数变化与杨圣贤等[15]的研究基本吻合。 2.2.3 总多酚 参考Xia等[18]建立的福林酚法,没食子酸作为对照品,测定总多酚含量。精确称量1.0 g滇黄精干粉,置于锥形瓶中,加入40 mL 60%乙醇水溶液,封口,50 ℃水浴加热提取2 h,滤过后定容至50 mL,摇匀后即为检测液。取检测液1 mL于25 mL棕色量瓶内,实验重复3次,计算含量。炮制过程中总多酚含量整体呈上升趋势,如表1所示。随着炮制次数的增加,多酚质量分数上升,在S5时明显增加(P<0.05),在S7之后趋于稳定。S0中多酚质量分数为(2.98±0.49)mg/g,S9中质量分数为(8.45±0.47)mg/g,增加2.84倍,增加显著(P<0.05)。 2.2.4 总黄酮 参考Jia等[19]建立的硝酸铝-亚硝酸钠法,以芦丁作为对照品,测定黄酮含量。称取1.0 g滇黄精干粉样品,加入40 mL甲醇和4 mL盐酸于圆底烧瓶85 ℃回流提取90 min,趁热滤过,冷却后用甲醇定容至50 mL,摇匀即为检测液。取检测液1 mL于25 mL棕色量瓶内,实验重复3次,计算含量。炮制过程中总黄酮含量整体呈上升趋势,结果如表1所示。其中第S1~S5次炮制缓慢上升,S6开始趋于平缓,在S9时达到最高。S0中黄酮质量分数为(8.19±0.30)mg/g,炮制结束后黄酮质量分数为(19.60±0.22)mg/g,增长2.39倍,增长显著。梁焕焕等[20]发现炮制过程中总黄酮含量整体呈上升趋势,其中S0~S2缓慢上升,S2~S4黄酮含量变化较大,之后趋于平缓,总体上升趋势与其研究基本相同。 图片 2.2.5 游离氨基酸 根据本实验室已报道的分析方法[21],通过HPLC法测定制备样品中16种游离氨基酸的含量。检测结果如表2所示。氨基酸是重要的营养成分,作为一种药食同源的药材,氨基酸对于黄精的营养价值非常重要。从各组分含量变化趋势可以看出,前2次蒸制,各氨基酸组分变化不显著,其中Ala和Ser在第2次蒸制结束后,可能由于蛋白水解作用质量分数反增。从第3次蒸制开始,所有氨基酸组分质量分数逐渐减少,最后趋近于0。 图片 2.3 滇黄精炮制前后代谢物的比较 2.3.1 滇黄精代谢提取物采集与处理 收集炮制前无霉变原料干片15 g,标号FPK。炮制9次结束后无霉变干片15 g,标号PPK。进行冷冻干燥处理,参数设定为?55 ℃、0.12 MPa、12 h。冷冻干燥后研磨至粉末状。称取粉末50 mg,加入0.3 mL提取液,放在4 ℃冰箱中冷藏12 h,期间涡旋提取6次。之后在10 000 r/min,离心半径为10 cm的条件下离心溶液10 min,取上清液,过滤膜(孔径0.22 μm)保存,用于UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS分析。 2.3.2 色谱质谱检测 (1)[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]条件:色谱柱为Waters Acquity UPLC HSS T3 C18柱(100 mm×2.1 mm,1.8 μm);流动相为超纯水(加入0.04%乙酸,A)-乙腈(加入0.04%乙酸,B),洗脱梯度:初始5% B;0~10.00 min,5%~95% B;10.00~11.00 min,95% B;11.00~11.10 min,95%~5% B;11.10~14.00 min,5% B;体积流量0.35 mL/min;柱温40 ℃;进样量4 μL。 (2)质谱条件:电喷雾离子源(ESI+/?),温度550 ℃,质谱电压5 500 V,帘气(CUR)206.843 kPa(30 psi),碰撞诱导电离参数设置为高。在三重四级杆中,每个离子对是根据优化的去簇电压和碰撞能进行扫描检测。 2.3.3 代谢物定性与定量分析 迈维代谢自建数据库MWDB(metware database),根据二级谱信息进行物质定性,分析时去除了同位素信号,含K+离子、Na+离子、NH4+离子的重复信号,以及本身是其他更大相对分子质量物质的碎片离子重复信号。代谢物定量是利用三重四级杆质谱的多反应监测(multi reaction monitoring,MRM)模式分析完成。该模式中,通过四级杆筛选目标物质的前体离子,排除干扰离子。诱导前体离子在碰撞室内碰撞和电离,形成碎片离子,再通过三重四级杆过滤筛选出所需要的一个特征碎片离子,排除其他离子的干扰,使定量结果更为可靠。获得不同样本的代谢物质谱分析数据后,对所有物质质谱峰进行峰面积积分,并对其中同一代谢物在不同样本中的质谱出峰进行积分校正。 2.3.4 代谢物的检测与鉴定 从FPK和PPK中共鉴定出代谢物419个,如黄精素A、延龄草素、新西伯利亚黄精苷、阿魏酸、咖啡酰对香豆酰酒石酸、没食子酸等。从类别来看,共分为12类,这些代谢物主要为氨基酸及其衍生物66个,脂质65个,酚酸类52个,黄酮类51个,有机酸42个,生物碱41个,核苷酸及其衍生物32个,甾体9个,木脂素和香豆素7个,异黄酮1个,萜类3个,其他类物质50个。这些化合物被进一步分为28个亚类,包括黄烷醇、游离脂肪酸糖及醇类和甾体皂苷等(图2)。其中氨基酸及其衍生物的物质组成最为丰富,占总代谢产物组成的15.75%。此外,还检测到10种苯乙醇苷类化合物,如松果苷和毛蕊花苷,并将其归类于苯丙类化合物。 图片 梁泽华等[22]应用固相萃取结合超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-电喷雾四级杆飞行时间质谱联用技术(ultra-high performance liquid chromatography-quadrupole time- of-flight mass spectrometry,UHPLC-Q-TOF-MS),共鉴定炮制前后黄精中的61个化学成分,Sharma等[23]通过超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-光电二极管阵列检测器-电喷雾电离质谱法(ultra-high performance liquid chromatography-photodiode array detector electrospray ionization mass spectrometry,UHPLC- PDA-ESI/MS)在黄精根茎中鉴定了314种化合物,用这2种方法都鉴定了比本研究更少的代谢产物,说明本研究方法具有较高的识别鉴定效率。 为了更好地了解各炮制过程对滇黄精代谢产物的影响,2组样品的主成分分析(principal component analysis,PCA)得分图见图3,质量控制(quality control,QC)样品聚类在一起,PC1和PC2的总和为83.4%,表明该方法具有良好的稳定性和可重复性。在该主成分中,FPK组和PPK组显著分离。这一结果表明,FPK和PPK组的代谢产物存在着显著差异。进一步利用变化倍数(fold change,FC)、特征变量投影重要性(variable importance in projection,VIP)和P值来筛选差异代谢物,代谢物同时满足FC>2或者FC<0.5、VIP>1、P<0.05被认为是差异代谢物。结果表明在PPK与FPK的对比中,一共有209种差异代谢物。 图片 为了探究炮制前后各类差异代谢物的变化趋势,对差异代谢产物做了蜂群图分析。由图4可知,在PPK与FPK的比较组中,有112种代谢物相对含量增加(FC>2,VIP>1,P<0.05),包括7个生物碱,10个氨基酸及其衍生物,5个黄酮,1个木脂素和香豆素,26个脂质,8个核苷酸及其衍生物,12个有机酸,20个酚酸,2个萜类和21个其他类;有97种代谢物相对含量降低(FC<0.5,VIP>1,P<0.05),包括9个生物碱,26个氨基酸及其衍生物,9个黄酮,18个脂质,13个核苷酸及其衍生物,8个有机酸,10个酚酸和4个其他类。经过九蒸九晒之后,产生了48个新化合物,有35个化合物被降解。 图片 2.3.5 差异代谢物相对含量变化 从差异代谢产物中共鉴定到11个糖类化合物(表3),经过炮制,9种糖类物质的相对含量显著增加。通过筛选一共鉴定到36个氨基酸及其衍生物相对含量显著变化,其中4个升高,17个下降。相对含量增加的物质分别是3-羟基-3-甲基谷氨酸、5-氧化脯氨酸、O-乙酰丝氨酸和脯氨酸甜菜碱。减少的物质包括L-缬氨酸、L-高胱氨酸、L-正亮氨酸等。此外,炮制后氨基酸以二肽或者多肽的形式存在,其中9种氨基酸被降解,新产生6个多肽,包括5-氨基戊酸、N-乙酰天冬氨酸和N-苯乙酰甘氨酸等。被降解物质包括L-犬尿氨酸、N-甘氨酰-L-亮氨酸和L-组氨酸等。各物质具体信息见表3所示。 图片 图片 图片 L-缬氨酸、L-高胱氨酸、L-正亮氨酸、L-亮氨酸、L-异亮氨酸、L-苯丙氨酸等为人体常见氨基酸,在炮制过程中,随着高温蒸制次数增加,氨基酸含量逐渐降低。同时发现被降解物质中,如苏氨酸、组氨酸等氨基酸种类丰富,检测结果与HPLC检测结果一致。此外,在新生成和被降解物质中,N-苯乙酰甘氨酸和己酰甘氨酸,甲氧基犬尿氨酸和L-犬尿氨酸之间推测存在转化关系,结构式如图5。 图片 分析发现,20个有机酸化合物中共有6个相对含量增加,6个相对含量减少。此外,有2个被降解,有6个新生成。新生成的化合物包括2-呋喃甲酸、2-甲基丁二酸和2-羟基丁酸等,被降解的化合物为5-羟基己酸和犬尿氨酸。各物质的具体信息见表3。 2-呋喃甲酸常以其衍生物的形式出现,即5-芳基-2-呋喃甲酸,该物质具有调节植物生长、抑菌等作用,常用于医药领域,而2-呋喃甲酸也被应用在农业和香料方面[24],同时根据前人研究发现,该物质为美拉德反应的中间产物,推测滇黄精炮制过程发生了该反应,消耗可溶性糖和氨基酸,使得氨基酸含量大量减少,颜色逐渐变深。上述实验中发现,氨基酸含量在第3次蒸制后被消耗殆尽,而颜色变化从第四次蒸制开始,变化不明显,也可推测滇黄精炮制颜色变化与美拉德反应相关。 3 讨论 滇黄精经过九蒸九晒之后变得气味浓郁,入口以酸甜味为主,无麻舌感,咽喉无刺激味,质地变得软糯有韧劲。随着炮制的进行,样品发生美拉德反应[12],颜色越来越深,第3次蒸晒之后颜色变化不明显,变成黑褐色。在九蒸九晒过程中,黄精中的还原糖与氨基化合物发生反应,生成棕色甚至黑色的大分子物质,导致黄精颜色变深[8]。在滇黄精九蒸九制过程中,多糖、氨基酸含量的下降也与美拉德反应有关,皂苷、黄酮和多酚含量呈上升趋势。 由于蒸制过程长时间处于高温状态,根据王倩等[25]研究可以推测加热导致结构不同的甾体皂苷发生转化作用,薯蓣皂苷转化为苷元和次级苷,从而使皂苷含量增加。此外,张洪坤等[26]和李瑞等[27]发现黄精皂苷变化在1次蒸制和生品中最高,推测是黄精品种和炮制方式所导致的差异。 有研究表明,多酚的结构决定了其稳定性,多酚结构多为2-连(或邻)基酚基苯并吡喃类衍生物,除间位外,其酚羟基多为邻位和连位,并不是单羟基酚。重复的高温蒸制处理可能促进了组织细胞的破碎和共价键的断裂,促进更多酚类物质的释放[28]。高温会导致某些内源酶失活,阻止了酚类物质进一步被氧化,因此多酚的含量在处理后增加[29]。 通过广泛靶向代谢组学技术从滇黄精炮制前后的样品中鉴定到419个代谢物,筛选得到112种化合物相对含量增加,97种化合物相对含量降低。炮制后小分子糖类物质相对含量增加,且多糖含量减少,导致滇黄精炮制后变甜。因为乳糖是新生成的糖,其甜度约为蔗糖的70%,主要用于制造婴儿食品和配制药物,例如制药片、药粉时用作稀释剂[30]。异麦芽酮糖是一种多功能的新型甜味剂,同时也是国际上公认安全的蔗糖替代品,在医药、食品等行业中具有广阔的应用前景[31]。乳糖,异麦芽酮糖,葡萄糖等单糖都可以充当甜味剂使用。炮制之后总多糖含量降低,这些单糖的相对含量增加,说明大分子糖转化成为了小分子的单糖[22]。此外,检测到部分糖苷相对含量减低,而新产生部分三萜皂苷化合物。推测总皂苷含量增加的原因是加热导致结构不同的甾体皂苷发生转化作用,部分薯蓣皂苷转化为苷元和次级苷,还可能因为新产生部分三萜皂苷,从而使皂苷含量增加。 有机酸相对含量增加导致炮制后期滇黄精产生酸味。酚酸是一类分子中具有羧基和羟基的芳香族化合物,酚酸类化合物是茶叶多酚类物质中的重要物质[32]。多酚类化合物主要呈现苦味和涩味,滇黄精经过炮制之后酚酸类物质相对含量显著增加,与分光光度法检测结果一致,此结果说明炮制后产生的苦涩味可能来自于酚酸类。氨基酸及其衍生物相对含量降低最明显,与HPLC检测结果一致。吴毅等[33]和王淳等[6]发现炮制过程滇黄精发生了美拉德反应,推测氨基酸含量的减少与美拉德反应有关。 滇黄精生品会刺激咽喉,有麻舌感,九蒸九晒可降低滇黄精的刺激性,增强其补益功效,然而目前对九蒸九晒炮制机制的研究尚不明确。本实验从化学和风味层面研究了九蒸九晒前后滇黄精的变化,并认为滇黄精炮制之后的“减毒”和“增效”作用可能是滇黄精九蒸九晒过程中化学成分的变化所引起的,在九蒸九晒炮制过程中大分子化合物分解成为易于人体吸收的小分子化合物。本研究系统阐述了滇黄精九蒸九晒炮制过程中化学成分的变化,为炮制滇黄精有效成分的筛选与质量评价提供参考,同时差异性成分的发现为研究滇黄精生熟饮片中差异性物质的分析提供新思路,对滇黄精的扩大开发利用有重要意义。
美国食品药品管理局(FDA)日前已经证实,食品和饮料中使用的蓝色加州(Blue California)生产的L-TeaActive 品牌L-茶氨酸成分为安全可靠产品(GenerallyRecognized as Safe,GRAS)。氨基酸L-茶氨酸(c-glutamylethylamide) 几乎仅被发现在茶树中存在。该化合物仅以自由形态存在,是茶叶中主要的游离氨基酸,大约占所有游离氨基酸的一半。包括放松、神经保护作用和提高注意力在内的各种对健康的不同效果都和L-茶氨酸相关。休息时,L-茶氨酸能增加脑电(EEG)模型中α 的活动,这表明可以使人更加放松。同时,氨基酸能引起α 活动的变化,这表明在处理需要注意力的工作时,能集中注意力来处理问题。根据由俄勒冈GRAS Associates 拟就和提交GRAS 申请,“提议的食品用途是食品成分,作为茶氨酸的饮食来源,在果汁和饮料、非草药茶、运动饮料、有特殊功能的瓶装水、巧克力条和口嚼片、硬糖和薄荷糖以及口香糖中使用。”GRAS 申请中提到,“L-茶氨酸(98%)的预期用途将使得1284毫克的日摄取量预计在第90 百分位数(“百分位数”为统计学术语——译者注)。从茶中摄入L-茶氨酸的第90 百分位数估计为825 毫克/天。估计的日摄入量与美国目前最喜欢饮茶者所摄入的L-茶氨酸水平相似。”蓝色加州称该公司的这种食品成分来自绿茶叶和其他天然成分,使用有专利权的生产工艺,最终产品是含98%的L-茶氨酸的标准化产品。蓝色加州的副总裁塞西莉亚·麦科勒姆(Cecilia McCollum)说:“我们非常高兴美国食品药品管理局对我们的产品的确认。我们的目标就是为源自绿茶的天然的L-茶氨酸的纯净度设立新的标准,我们已经做到了。”L- TeaActive 成分是依照良好生产规范(GMP)和美国国家卫生基金会(NSF)的ISO-9001:2000 质量认证进行生产的,并且蓝色加州是经Kosher 认证(一种犹太食品认证)的公司。
[center]高同型半胱氨酸血症致胰岛素抵抗机理研究取得创新进展[/center]胰岛素抵抗是糖尿病前期症状,广泛危害人类健康,但其机制尚未完全阐明。北京大学医学部生理与病理生理学系王宪教授领导的研究室从脂肪细胞因子的角度,就抵抗素在致炎因素高同型半胱氨酸血症促进脂肪组织胰岛素抵抗发病机制中的作用,进行了系列研究并取得创新进展。研究成果论文最近已发表在本领域国际顶级杂志《糖尿病》(《Diabetes》)上。 研究结果显示,在小鼠饮水中补充同型半胱氨酸造成高同型半胱氨酸血症模型4周后,可以观察到任意血糖的明显升高和胰岛素敏感性的显著下降;同型半胱氨酸处理的脂肪细胞,对胰岛素刺激下的葡萄糖摄取能力亦明显降低。高同型半胱氨酸血症小鼠附睾白色脂肪组织中抵抗素基因及蛋白表达显著上调,血中的抵抗素水平显著增高;给予原代培养的大鼠附睾脂肪细胞同型半胱氨酸刺激,结果发现同型半胱氨酸可以呈时间、剂量依赖性上调脂肪细胞中抵抗素的表达。抵抗素是脂肪组织特异性分泌的脂肪细胞因子,具有强烈的致胰岛素抵抗作用,与2型糖尿病的发生密切相关。以上结果证实,致炎因素高同型半胱氨酸血症的致胰岛素抵抗作用是通过抵抗素来实现的,从而为阐明高同型半胱氨酸血症致胰岛素抵抗发生的机制提供了新证据。 据该研究室李茵博士介绍,同型半胱氨酸是体内蛋氨酸脱甲基生成的一种含巯基的氨基酸,如果与同型半胱氨酸代谢有关的酶或辅助因子(如叶酸和维生素B12等)缺乏,则会使同型半胱氨酸代谢受阻,导致高同型半胱氨酸血症。亚洲人可能因遗传和环境因素的不同,高同型半胱氨酸血症的发病率明显高于欧洲人。我国现阶段由于精细食品的过度加工,造成大量B族维生素流失,同型半胱氨酸代谢受阻,高同型半胱氨酸血症的发病率显著增加。因此,该研究成果将有助于阐明胰岛素抵抗的发生和发展中致炎因素高同型半胱氨酸的作用和地位,为早期预防与缓解胰岛素抵抗的发生、发展和今后筛选干预胰岛素敏感性的药物提供新途径。信息来源:中国医药报
肽 链 设 计简 介 多肽是复杂的大分子, 因此每条序列在物理和化学特性上都是独特的。有些多肽合成很困难, 另有些多肽虽然合成相对容易, 但纯化困难。最常见的问题是许多肽不溶于水溶液, 因此在纯化中, 这些疏水肽必须溶于非水溶剂中,或特殊的缓冲液, 而这些溶剂或缓冲液很可能不适合应用于生物实验系统, 因此研究人员不能使用该多肽达到自己的目的, 因此下面是对于研究人员设计多肽的一些建议。合成困难肽的选择1. 减少序列长度 由于肽的长度增加导致粗产物纯度降低, 小于15个残基的肽能较容易得到。当肽链长度增加到20个残基以上时, 正确产物的量就是一个主要考虑的问题。在许多实验中, 降低残基数低于20往往能得到更好的结果。2. 减少疏水残基数 疏水残基占明显优势的肽,尤其在距C端7-12个残基的区域,常常引起合成困难。这通常被认为是由于合成中形成b折叠片,这样产生不完全配对。在这些例子中, 用1个或几个极性残基置换, 或加入Gly或Pro以打开肽结构可能会有帮助。3. 减少"困难"残基 有多个Cys、Met、Arg、Try残基通常难于合成。Ser通常可作为Cys的非氧化替换。改善可溶性的选择1. 改变N端或C端 对于酸性肽 (即pH值为7时带负电荷), 我们推荐乙酰化(N端乙酰化, C端保持自由羧基), 以增加负电荷。而对于碱性肽 (即pH值为7时带正电荷), 我们推荐氨基化 (N端自由氨基, C端氨基化), 以增加正电荷。2. 缩短或加长序列 某些序列含有大量疏水氨基酸, 如Trp、Phe、Val、Ile、Leu、Met、Tyr和Ala等, 当这些疏水残基大于50%通常难于溶解。为了增加肽的极性, 加长序列可能会有帮助。另外一种选择是通过减少疏水残基的方法降低肽链的长度以增加极性。肽链极性越高, 就越有可能溶于水。3. 加入可溶性残基 对于某些肽链而言, 加上一些极性氨基酸能改善可溶性。我们推荐给酸性肽的N端或C端加上Glu-Glu。给碱性肽的N端或C端加上Lys-Lys。如果不能加入带电荷基团, 可以将Ser-Gly-Ser加到N端或C端。但是, 肽链的两端不能改变时, 该方法则不可行。4. 通过置换一个或多个残基改变序列 肽链的可溶性可通过改变序列内某些残基来改善。通常单个残基的替换就能显著改善其疏水性, 而这种改变通常是较为保守的, 如用Gly代替Ala。5. 通过选用不同"框架"来改变序列 如果能用某个序列来制备许多长度一定的相互串连或重叠的多肽, 则可以用改变各个多肽起始点的方法来实现改变序列的目的。其原理是: 在同一多肽的亲水和疏水残基间创造新的更好的平衡, 或将同一多肽内的"困难"残基(比如2个Cys)放进两个不同的多肽而不是集于同一分子内。特殊氨基酸残基对肽链特性影响的一些要点 对于由遗传密码编码的二十种氨基酸及蛋白质中常见的其他氨基酸, 按其特性可以用几种方法进行分类。下面列出了最常见的氨基酸的三字母代码和单字母代码,以及不同的分类方法。氨基酸的代码丙氨酸 Ala A 甲硫氨酸 Met M半胱氨酸 Cys C 天门冬酰胺 Asn N天门冬氨酸 Asp D 脯氨酸 Pro P谷氨酸 Glu E 谷氨酰胺 Gln Q苯丙氨酸 Phe F 精氨酸 Arg R甘氨酸 Gly G 丝氨酸 Ser S组氨酸 His H 苏氨酸 Thr T异亮氨酸 Ile I 缬氨酸 Val V赖氨酸 Lys K 色氨酸 Trp W亮氨酸 Leu L 酪氨酸 Tyr Y蛋白质中常见的其他氨基酸羟脯氨酸胱氨酸焦谷氨酸肽链设计中常见的其它氨基酸1. α-氨基丁酸 (Cys的置换物)2. β-氨基丙氨酸 (Ala的直链异构物)3. 正亮氨酸 (亮氨酸的线性侧链异构物)氨基酸按其亲水性、疏水性可分亲水性氨基酸: D, E, H, K, Q, R, S, T, 羟脯氨酸, 焦谷氨酸疏水性氨基酸: A, F, I, L, M, P, V, W, Y, α-氨基丁酸, β-氨基丙氨酸, 正亮氨酸C和G属于未定类其它的分类方法在温和条件下氧化的氨基酸--C, M脱氨或脱羧基的氨基酸--N, Q蛋白制备中易降解的氨基酸--M, W带正电荷的氨基酸--K, R, H带负电荷的氨基酸--D, E 当下列疏水氨基酸, 即Ala, Val, Leu, Ile, Pro, Met, Phe, Trp存在于C端时,通常引起合成及纯化的困难, 这主要是因为它们难溶于水。如果您看见这些氨基酸, 即Cys、His、Pro 普遍存在于序列中或在C端时, 则在常规的固相合成中需要特殊的固相支持物。在用普通的固相支持物时, 在二肽阶段, 由于环化引起的损失非常高。在许多例子中, 甚至导致所有链从固相支持物上损失, 但是若C端为氨基化Pro时, 或者用特殊的PEG-聚苯乙烯固相支持物时, 能使产量大为提高, 则不会发生这种现象。
公司环境扩项,做这个五日生化需氧量标准物质验证试验的时候,标准值始终没办法测定出来,请教大家可能哪里有问题?(所有操作都有按照标准,同时做的葡萄糖/谷氨酸标液都是没问题的)
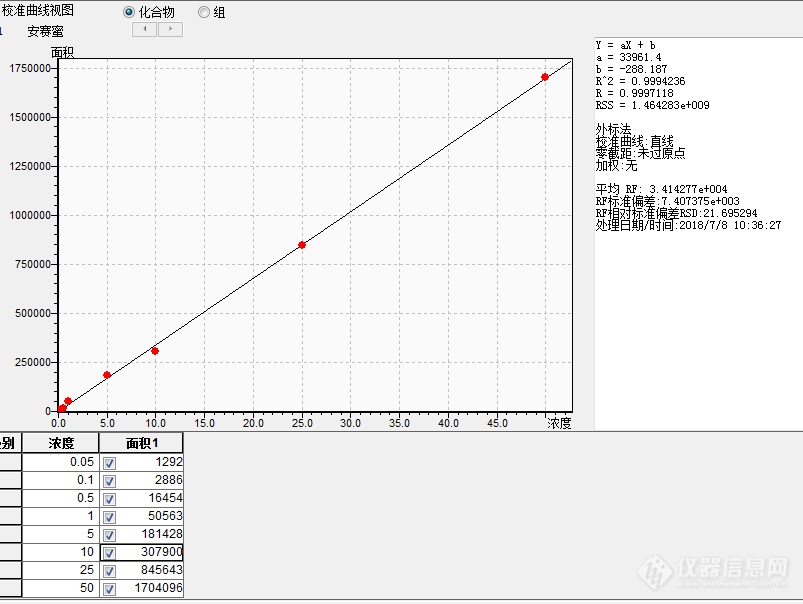
[align=center][b]饮料中乙酰磺氨酸钾检测方法验证报告[/b][/align][align=center][b]GB/T5009.140-2003[/b][/align][align=center][b]李晓东[/b][/align]一、[b]方法概述1 范围[/b]本标准规定了饮料中乙酰磺氨酸钾的测定方法。本标准适用于汽水、可乐型饮料、果汁、果茶等食品中乙酰磺氨酸钾的测定。[b]2 原理[/b]试样中乙酰磺氨酸钾经高效液相反相C18柱分离后,以保留时间定性,峰高或峰面积定量。二、[b]仪器与试剂[/b]1.仪器1.1高效液相色谱仪:配有紫外检测器,仪器编号:UNQD-YQF-1471.2超声波振荡器1.3抽滤瓶1.4 G3耐酸漏斗1.5高速离心机:转速不低于4000r/min。1.6微孔滤膜0.45μm1.7层析柱:可用10ml注射器筒代替,内装3cm高中性氧化铝。2. 试剂除非另有说明,本方法所有实际均为分析纯,水为GB/T 6682规定的一级水。2.1甲醇(CH3OH ):色谱纯。2.2乙腈(CH3CN) : 色谱纯。2.3 10%硫酸溶液2.4 中性氧化铝:层析用100目-200目2.5 0.02mol/L硫酸铵溶液:称取硫酸铵2.642g,加水溶解至1000mL。三、[b]分析步骤[/b]1.标准曲线绘制1.1 乙酰磺酸钾:纯度大于99.9%1.2标准储备液:准确称取100.0mg(精确到0.1mg)乙酰磺酸钾标准品于100ml容量瓶中,用流动相溶解并定容至刻度,配置成浓度为1mg/ml的标准储备液。1.3标准工作液:量取标准储备液适量,用流动相稀释成浓度为0.05μg/mL、0.1μg/mL、0.5μg/mL/1.0μg/mL、5.0μg/mL、10.0μg/mL、25.0μg/mL、50.0μg/mL标准工作液。2.样品的处理2.1汽水:将试样温热,搅拌除去二氧化碳,吸取2.5mL试样于25mL容量瓶中,加流动相至刻度,摇匀后,溶液通过微孔滤膜过滤,滤液做HPLC备用。2.2可乐型饮料:将试样温热,搅拌除去二氧化碳,吸取已除去二氧化碳的2.5mL试样通过中性氧化铝柱,待试样液流至柱表面时,用流动相洗脱,收集25mL洗脱液,摇匀后超声脱气,此液做HPLC备用。2.3果茶、果汁类食品称取2.5ml试样,加水20mL混匀后,离心(4000r/min)15 min,上清液全部转入中性氧化铝柱,待水溶液流至柱表面时,用流动相洗脱,收集洗脱液25mL,混匀后,超声脱气,此液做HPLC分析用。3.仪器测定条件3.1色谱柱:C18柱, 150mm×4.6mm,5μm,或相当者。3.2流动相:0.02mol/L硫酸铵(740ml-800ml)+甲醇(90ml-50ml)+10%硫酸(1ml)3.3流速:0.7ml/min3.4波长:214nm3.5进样量:10μL四、[b]结果处理[/b]分析结果的表述[b]1、计算公式[/b][table][tr][td=1,2]X(mg/L)=[/td][td]c× V×1000×f[/td][/tr][tr][td]m×1000[/td][/tr][/table]式中:X-试样中乙酰磺酸钾的含量mg/L或mg/L;C-标准溶液中乙酰磺酸钾的浓度,μg/mL;m-试样质量,g或ml;V-试样最终定容体积,mL;f-稀释倍数。五、验证结果1.线性结果将标准系列工作溶液分别注入液相色谱仪中, 测定相应的峰面积,以混合标准系列工作溶液的质量浓度为横坐标,以峰面积为纵坐标,绘制标准曲线。[u]Y=33961.4*X-288.187 R^2=0.9994236[/u][align=center][img=,690,519]http://ng1.17img.cn/bbsfiles/images/2018/07/201807242046125748_6268_2904018_3.png!w690x519.jpg[/img] [/align][align=center]表1 乙酰磺酸钾标准系列试验结果[/align][table][tr][td]C(μg/mL)[/td][td][align=center]0.05[/align][/td][td][align=center]0.1[/align][/td][td][align=center]0.5[/align][/td][td][align=center]1.0[/align][/td][td][align=center]5.0[/align][/td][td][align=center]10.0[/align][/td][td][align=center]25.0[/align][/td][td][align=center]50.0[/align][/td][/tr][tr][td][align=center]A[/align][/td][td][align=center]1292[/align][/td][td][align=center]2886[/align][/td][td][align=center]16454[/align][/td][td][align=center]50563[/align][/td][td][align=center]181428[/align][/td][td][align=center]307900[/align][/td][td][align=center]845643[/align][/td][td][align=center]1704096[/align][/td][/tr][/table] 以上结果表明乙酰磺酸钾在0.05μg/mL ~50.0μg/mL范围内,R=0.9997118,吸光值与浓度呈线性关系,线性良好,符合要求。2.检出限结果将0.5μg/mL标准溶液逐级稀释至S/N=3±1,得出乙酰磺酸钾的方法检出限为 1.7μg/ml[color=#ff0000],[/color]此检出限结果满足条件。[b]六、重复性测定[/b]对样品F1807000284进行7次进样,其乙酰磺酸钾测试值如下表所示:[table][tr][td][align=center]编号[/align][/td][td][align=center]m(ml)[/align][/td][td]C(μg/ml)[/td][td]V(ml)[/td][td][align=center]X(mg/L)[/align][/td][td][align=center]X[sub]平[/sub](mg/L)[/align][/td][td][align=center]RSD(%)[/align][/td][/tr][tr][td][align=center]1[/align][/td][td][align=center]2.5[/align][/td][td][align=center]1.857[/align][/td][td]25[/td][td]18.57[/td][td=1,7][align=center]18.67[/align][/td][td=1,7][align=center]0.35[/align][/td][/tr][tr][td][align=center]2[/align][/td][td][align=center]2.5[/align][/td][td][align=center]1.866[/align][/td][td]25[/td][td]18.66[/td][/tr][tr][td][align=center]3[/align][/td][td][align=center]2.5[/align][/td][td][align=center]1.876[/align][/td][td]25[/td][td]18.76[/td][/tr][tr][td][align=center]4[/align][/td][td][align=center]2.5[/align][/td][td][align=center]1.865[/align][/td][td]25[/td][td]18.65[/td][/tr][tr][td][align=center]5[/align][/td][td][align=center]2.5[/align][/td][td][align=center]1.874[/align][/td][td]25[/td][td]18.74[/td][/tr][tr][td][align=center]6[/align][/td][td][align=center]2.5[/align][/td][td][align=center]1.865[/align][/td][td]25[/td][td]18.65[/td][/tr][tr][td][align=center]7[/align][/td][td][align=center]2.5[/align][/td][td][align=center]1.863[/align][/td][td]25[/td][td]18.63[/td][/tr][/table]本方法的精密度为 0.35% ,符合《饮料中乙酰磺氨酸钾的测定方法》GB/T5009.140-2003中给出的精密度要求。因此,本次测定均符合要求。[b]七、准确度验证(加标回收)[/b]对样品F1807000284加标,取乙酰磺酸钾浓度100 .0 μg/mL的标液 0.02mL、0.04mL和0.08ml同样品同步处理后,结果见下表[table][tr][td=2,1][align=center]测定编号[/align][/td][td=6,1]乙酰磺酸钾[/td][/tr][tr][td][align=center]序号[/align][/td][td][align=center]m(g)[/align][/td][td][align=center]V(mL)[/align][/td][td][align=center]C(μg/mL)[/align][/td][td][align=center]X(mg/L)[/align][/td][td][align=center]X[sub]平[/sub](mg/L)[/align][/td][td][align=center]加标量(mg/L)[/align][/td][td][align=center]回收率%[/align][/td][/tr][tr][td][align=center]1#[/align][/td][td][align=center]2.5[/align][/td][td]25[/td][td][align=center]N.D[/align][/td][td][align=center]N.D[/align][/td][td=1,2][align=center]N.D[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]2#[/align][/td][td][align=center]2.5[/align][/td][td]25[/td][td][align=center]N.D[/align][/td][td][align=center]N.D[/align][/td][td][align=center]/[/align][/td][td][align=center]/[/align][/td][/tr][tr][td][align=center]加标1#[/align][/td][td][align=center]2.5[/align][/td][td]25[/td][td][align=center]1.863[/align][/td][td][align=center]18.63[/align][/td][td][align=center]/[/align][/td][td][align=center]20[/align][/td][td][align=center]93.2[/align][/td][/tr][tr][td][align=center]加标2#[/align][/td][td][align=center]2.5[/align][/td][td]25[/td][td][align=center]3.561[/align][/td][td][align=center]35.61[/align][/td][td][align=center]/[/align][/td][td][align=center]40[/align][/td][td][align=center]89.0[/align][/td][/tr][tr][td][align=center]加标3#[/align][/td][td][align=center]2.5[/align][/td][td]25[/td][td][align=center]6.978[/align][/td][td][align=center]69.78[/align][/td][td][align=center]/[/align][/td][td][align=center]80[/align][/td][td][align=center]87.2[/align][/td][/tr][/table]由上表可以看出乙酰磺酸钾的加标回收范围在 87.2%-93.2% ,RSD值为3.43%符合规定要求。七、总结本方法的检出限为1.7μg/ml。小于GB/T5009.140-2003中给出的最低检出浓度4μg/ml。本方法的精密度为 3.45%,符合《饮料中乙酰磺氨酸钾的测定方法》GB/T5009.140-2003中给出的精密度要求.通过对饮料中乙酰磺氨酸钾的测定方法的检出限、精密度和准确度的评价,本方法测定乙酰磺酸钾据准确,结果可信。此方法的准确性好,测定结果真实可靠,可用于饮料中乙酰磺氨酸钾的测定。
与运输,维持视网膜色素上皮的正常组织状态,维护正常视力功能。含锌较多的食物有牡蛎、肉类、肝、蛋类、花生、小麦、豆类、杂粮等。(6)珍珠,珍珠含95%以上的碳酸钙及少量氧化镁、氧化铝等矿物质,并含有多种氨基酸、如亮氨酸、蛋氨酸、丙氨酸、甘氨酸、谷氨酸、天门冬氨酸等,珍珠性味甘咸寒,用珍珠粉配龙脑、琥珀等配成的“真珠散”点眼睛可抑制白内障的形成。(7)海带,海带除含碘外还含有1/3的甘露醇,晒干的海带表面有一层厚厚的“白霜”,它就是海带中的甘露醇,甘露醇有利尿作用,可减轻眼内压力,用来治疗急性青光眼有良好的功效。其他海藻类如裙带菜也含有甘露醇,也可用来作为治疗急性青光眼的辅助食品。