在解红外光谱时常分不出来胺基(酰胺基)是与苯环相连的。还是在苯环侧链上。
大家好!我是个新手,我现在在做一个化学品——3-环已胺基丙胺的含量分析我用的是标准样品,可是我所采用的方法在我们公司的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]上打不出原有浓度,所以求助大家给点宝贵意见。谁能提供一下关于该化学品——3-环已胺基丙胺的含量分析方法
xiayu861网友问:二乙基己基丁酰胺基三嗪酮是在哪买的?
各位老师们好,我现在要测叔丁胺盐类的叔丁胺残留量,盐类是配位化合物,加酸加碱加水加热都会解离出叔丁胺,试过用乙酸乙酯做溶剂,但是不溶,请问下老师们有没有合适的方法?
我现在在做有机叔胺的非水滴定,遇到一个头疼的问题,想请教高人,先谢谢了.样品是一个含三个氮的六元环,三个氮上分别又连有含叔氨基的丙烷基,也就是一个六个氮,三个在环上,三个在支链上,都是叔胺.用0.1M高氯酸滴定 ,100ml醋酸+7ml醋酐作溶剂,出两个峰,第一个峰最大,比理论值小1/3,第二个峰小很多,和理论值接近,我想问下是该取第二个峰吗?做平行样时发现, 第一个峰很好平行,第二个峰会差比较多,想用第二个峰又不好平行,疑惑于到底该取哪个峰,跪求赐教!
化妆品中二乙基己基丁酰胺基三嗪酮的检测方法
如何改善条件让其出峰时间慢点。色谱条件是:正在分析一药物,该药物含有一羰基和一胺基、一苯基,流动相为甲醇:水=95:5,流速0.8ml/min,出峰时间为2.7min
请问,有谁做过顶空气相测定N,N-二甲基环己胺吗?用安捷伦7890A测定,条件给怎么设定呢?还有就是实验室现有色谱柱是HP-5和DB-5HT,这两根柱子的固定相是一样的,能用来分离N,N-二甲基环己胺吗?因为有文献直接用气相色谱测定,用的是SE-30柱子,SE-30的极性更弱一点,想知道一定是用这种柱子才能测吗?很着急,坐等,非常感谢!!!
请教各位大佬,做叔丁胺方法验证,柱子是DB-624,30*0.53*3,02是空白(DMA),04、5、6、7、8是同浓度溶液,为什么峰面积一针比一针高,怎么能使峰面积稳定?谢谢各位大佬[img]https://ng1.17img.cn/bbsfiles/images/2019/06/201906191634487412_9425_3909958_3.png[/img]
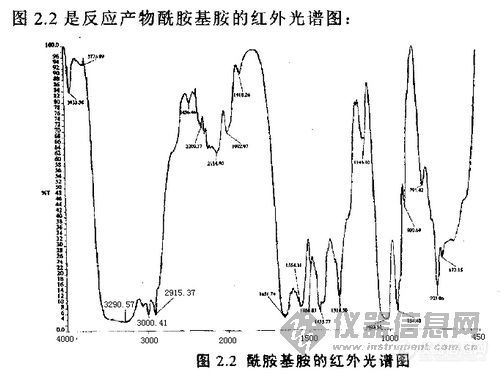
间苯二甲胺 和 己二酸反应生成 酰胺基胺,可是红外光谱上只能看见仲酰胺基的特征吸收峰,为什么看不到伯胺的峰?3000.41和2915.37处是不是伯胺吸收峰?是不是往后挪了?[img]http://ng1.17img.cn/bbsfiles/images/2009/06/200906080958_154498_1608859_3.jpg[/img][img]http://ng1.17img.cn/bbsfiles/images/2009/06/200906080958_154497_1608859_3.jpg[/img]
请大家帮我看看这个问题:把一个化合物(有苯环、仲酰胺、胺基NH2)的胺基(伯胺)变为硝基-NO2,然后用红外分析,能看出是否变化了?即硝基存在。

[font='宋体'][size=24px][color=#000000]仲丁胺简介[/color][/size][/font][font='宋体'][size=24px]杨磊[/size][/font][font='宋体'][size=24px]2021年7月21日[/size][/font][align=center][size=18px]摘要[/size][/align]仲丁胺(Sec-Butylamine)是一种保护性杀菌剂,对多种真菌有抑菌、抗菌活性,广泛应用于水果、蔬菜的贮藏期防腐保鲜。市售的保鲜剂如克霉灵、保果灵、桔腐净等,其主要有效成分为仲丁胺。2-AB对柑桔采后病害有着有效而广泛的作用,同时对苹果、梨、桃、香蕉的采后腐烂也有同样的控制作用。在绿色食品生产上,农业行业标准NY/T392-2013《绿色食品食品添加剂使用准则》要求不应使用仲丁胺,NY/T844-2010《绿色食品温带水果》要求仲丁胺不得检出。GB2760-2011《食品安全国家标准食品添加剂使用标准》中对仲丁胺的限量为鲜水果柑橘≤0.005mg/kg,荔枝≤0.009mg/kg,苹果≤0.001mg/kg;新鲜蔬菜(仅限蒜薹和青椒)≤3mg/kg,更新后GB2760-2014《食品安全国家标准食品添加剂使用标准》将仲丁胺从添加剂中删除,意味着仲丁胺为非法添加剂。之后GB-2019又将仲丁胺加入。关键词:仲丁胺,添加剂,防腐。[size=21px]一、仲丁胺概述[/size][size=16px]1[/size][size=16px].[/size][size=16px]仲丁胺的简介[/size]仲丁胺(2-aminobutane,简称2-AB),又名2-氨基丁烷,是一种保护性杀菌剂,对多种真菌有抗菌活性,广泛应用于柑桔、苹果、梨、桃、香蕉、马铃薯、青椒等果品蔬菜贮藏期的防腐保鲜。也是一种具有氨臭味的无色易挥发的液体,能与水和多种有机溶剂混溶。它的分子中含有一个不对称的碳原子,因而具有两种旋光异构体。仲丁胺的结构性质:[font='arial'][color=#333333][back=#ffffff]仲丁胺,是一种有氨臭的无色液体,溶于水、乙醇、乙醚、丙酮[/back][/color][/font][font='arial'][color=#333333][back=#ffffff],[/back][/color][/font][font='arial'][color=#333333][back=#ffffff]熔点-104.5[/back][/color][/font][font='宋体'][color=#333333][back=#ffffff]℃[/back][/color][/font][font='arial'][color=#333333][back=#ffffff]、沸点:62.5[/back][/color][/font][font='宋体'][color=#333333][back=#ffffff]℃[/back][/color][/font][font='arial'][color=#333333][back=#ffffff],[/back][/color][/font][font='arial'][color=#333333][back=#ffffff]主要用于有机合成的中站体、化学试剂,属于易燃物品。[/back][/color][/font][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262023517499_3936_1608728_3.gif[/img][size=16px]2[/size][size=16px].[/size][size=16px]仲丁胺的发现:[/size]1962年,美国Eckert博士首次发现2-AB处理对柑桔由Penicilliumdigitatum引起的腐烂有较好的的控制作用。1963年,Eekert等人进一步研究了21种挥发性低级脂肪胺(C2-C10)对柑桔由Penicilliumdigitatum引起的腐烂的控制作用,发现2-AB的防腐效果最好(EckertJ..W&KolbezenM.J.,1963)。1964年Eekert等人用2-AB的磷酸盐对31种病原微生物,包括半知菌类、子囊菌和藻状菌纲的真菌以及细菌进行了抑菌实验,发现有7种病原真菌对2-AB磷酸盐敏感,2-BA浓度为50-100μg/ml时,即可阻止菌丝生长达50%;有5种真菌比较敏感,2-AB浓度为250μg/ml时,可阻止菌丝生长达50%;细菌对2-AB磷酸盐不敏感,同时还发现2-AB盐酸盐、硫酸盐、磷酸盐、醋酸盐、丙酸盐和柠檬酸盐的效果无明显差异。结合防腐试验确认应用2-AB中性盐可以有效地控制8种病原真菌引起的果蔬采后腐烂。这八种病原真菌分别是Penicilliumdigitatum(指状青霉,柑桔绿霉)、Penicilliumexpansum(扩张青霉,苹果青霉)、Penicilliumitdicum(意大利青霉,柑桔青霉),它们属于青霉属真菌,主要危害柑桔、苹果、梨、葡萄等,引起青绿霉病。Monilinafructicola属于串孢盘菌属真菌,核果褐腐菌,主要危害桃、李等,引起褐腐;Glomerellafructicola属于小丛壳属真菌,炭疽病菌,主要危害柑桔、苹果、梨、山碴、桃、葡萄、柿和番茄等果实,产生褐色腐烂斑;Gloeospriummusarum盘长孢属真菌,主要危害香蕉,引起炭疽病;Phomopsiscitri拟茎点属真菌,主要危害柑桔,引起果实褐色蒂腐;Thielaviopsisparadoxa拟黑根霉属真菌,危害香蕉和菠萝,分别引起果柄腐烂和黑腐(EekertJ..W&KolbezenM.J.,1964)。此外,Scooft(1967)报道,0.05~2%的2-AB浸果处理几乎能完全控制Gloeospriummusarum对香蕉的危害。McDonnell(1971)报道,5mg/ml2-AB可有效控制Nectria(丛赤壳属真菌)引起的苹果采后腐烂。Boyd(1975)报道,用2-AB熏蒸马铃薯,对Helminthosporium(长蠕抱霉属真菌)引起的银粗皮病也有效(叶凤阁与张忠源,1991)。[size=16px]3[/size][size=16px].[/size][size=16px]仲丁胺的限量:[/size]在1975年FAO/WHO联合会议上,暂时人体ADI值规定为0.2mg/kg,并同时规定了在柑桔和柑桔制品中2-AB的最大残留量:干制柑桔果肉及糖蜜为50mg/kg,柑桔果实为30mg/kg,柑桔果汁为0.5mg/kg。在1975年发表的FAO/WHO专题文章里,明确指出2-AB对柑桔采后病害有着有效而广泛的作用,同时对苹果、梨、桃、香蕉的采后腐烂也有同样的控制作用。当时英国大部分马铃薯种植区采用的种薯来自苏格兰地区,在那里最严重的组织病害是由Phomaexiguavar.foveata引起的坏疽和由Oosporapustulans引起的组织斑点病害。这两种真菌能够长期潜伏在组织内部,不容易被发现,且很难控制。最常用的控制方法就是将马铃薯组织浸在有机汞消毒剂溶液中以控制大部分的病原体和坏疽,但是使用这种毒性极高的溶液,操作上存在很大的困难。研究表明当2-AB的使用量为200mg/kg马铃薯组织时,处理30-40min就能有效的控制这两种病害,因此2-AB首先在欧洲得到广泛应用。我国自从1976年河北农业大学首次合成这种防腐保鲜剂以来,全国许多单位相继开始应用2-AB对采后果蔬进行防腐保鲜处理。除上述果品蔬菜外,还对龙眼,葡萄,蒜苔,西红柿及青椒等进行了防腐效果测试,均得到了令人满意的效果。为此,相继研制开发出应用于不同果蔬的2-AB系列制剂,其用途不断扩大,市场需要量也逐年递增,有关2-AB研究的报道也逐年增多。[size=21px]二、仲丁胺的毒理学评价:[/size]1967年,Eli研究了以含有不同剂量2-AB的饲料喂养处在哺乳期的奶牛,然后检测它们的粪便、血液、牛奶、尿、肝脏、肾脏、脂肪和肌肉中的2-AB残留量,发现这些组织中的2-AB含量与饲料中2-AB的添加量有剂量关系,并且已经被吸收到了牛奶和尿液里,但在牛奶中的残留量低于饲料中添加量的1%。虽然实验组的瘦肉中2-AB残留量并没有明显高于对照组,但是在肾脏和肝脏中有明显的2-AB残留。通过分析表明:2-AB易于被吸收,并且大部分都随尿液排出,结果见表1。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262023518388_8296_1608728_3.png[/img][/align]1968年,Eli又设计了另一组实验,他以2-AB处理过的柑桔制成干饲料,定量喂给哺乳期的奶牛,然后测定牛奶、肌肉、肝脏、脂肪和肾脏中的2-AB含量。七头Holsetin奶牛中有三头作为对照,四头定期接受含有剂量为16mg/kg2-AB的饲料,在7d的试验期间,所有的奶牛均喂以对照饲料,实验结果见表2。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262023519808_6736_1608728_3.png[/img][/align]1975年,联合国粮农组织(FAO)和世界卫生组织(WHO)推荐将2-AB应用于柑桔的采后防腐保鲜,并指出对控制苹果、梨、桃及香蕉的采后病害同样有效。在制定ADI之前,经过了一系列的动物试验,证明在以下水平内不会发生毒理学反应:鼠:35mg/kg体重(63mg醋酸盐/kg体重)。狗:69mg/kg体重(125mg醋酸盐/kg体重)。但由于缺乏人体的临床实验观察,只制定了对人体的临时ADI值,为.02mg/kg体重。关于2-AB有无三致(致癌、致畸、致突变)危险的问题,还需作进一步的人体新陈代谢的实验观察。[size=21px]三、仲丁胺的检测[/size]果蔬中一定量的防腐剂、保鲜剂可保证贮藏期间的果蔬品质,仲丁胺作为常用的果蔬防腐剂具有一定的毒性,人们食用含有仲丁胺的食品后,仲丁胺一部分随尿排出,而另一部分会积累在肾脏中。国际上已将其对人体健康的危害列为三级,对其限量标准也在不断提升,已成为农产品进出口贸易技术壁垒的瓶颈。农业部行业标准NY/T946-2006采用薄层色谱法检测仲丁胺残留量,最低检出限量为0.672mg/kg。我国农业行业标准(NY/T844-2010)规定仲丁胺在绿色食品葡萄中不得检出(<0.7mg/kg)。因此,建立一种前处理更为简便安全,检测方法灵敏度更高的仲丁胺残留检测分析方法是非常必要的。目前,国内外关于仲丁胺的检测方法主要包括薄层色谱法(TLS)、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法(GC)、[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]-质谱法(GC-MS)、高效液相色谱法(HPLC)、高效液相色谱-质谱法(HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url])等。但TLS法检测程序复杂,灵敏度低,分离度和重现性差。GC和GC-MS法对样品前处理条件要求苛刻,重复性不理想,且GC-MS和HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]仪器昂贵。相对于其他方法,HPLC-UV具有抗干扰能力强、分析时间较短、灵敏度高的优点。由于仲丁胺的分子量小,且结构上无生色基团用于最终检测,因此多采用柱前衍生法。常用于仲丁胺检测的衍生剂有丹酰氯(DNS-Cl)、荧光胺、2,4-二硝基氟苯(DNFB)和9-氯甲酸芴甲酯(FMOC)。这些衍生剂一般都有较强的紫外吸收基团和荧光发射基团,可与仲丁胺的NH2反应生成相应的衍生物。但有些衍生剂具有一定的缺陷,如丹酰氯(DNS-Cl)需在避光条件下衍生,且试剂本身易降解,很难定量;2,4-二硝基氟苯(DNFB)的衍生化反应时间长,衍生物的稳定性差。而9-氯甲酸芴甲酯(FMOC)在温和条件下即可与伯胺、仲胺迅速发生定量反应,衍生化产物稳定,且过量的衍生剂及其水解产物不干扰测定,是一种理想的衍生化试剂。经典的仲丁胺提取法是采用凯氏定氮法检测仲丁胺,该法操作步骤繁琐耗时、操作误差偏大、难以实现自动化。[size=16px]柱前衍生/高效液相色谱法[/size]1.溶液配制:硼酸盐缓冲溶液。FMOC衍生溶液:称取25.0mgFMOC,用乙腈定容至5mL容量瓶中,浓度为5g/L,相应低浓度的衍生试剂用乙腈稀释而成。标准溶液:准确称取0.200g(精确至0.001g)仲丁胺标准品,用乙腈溶解,配成40g/L的标准储备液,在4℃下保存。用乙腈将仲丁胺标准储备液逐级稀释成0.001,0.01,0.05,0.1,1.0mg/L系列质量浓度的标准溶液。2.样品前处理:参考农业行业标准的方法,称取均匀样品25.0g(精确至0.1g)于300mL蒸馏管中,加入35mL1mol/L的CaCl2溶液、5.0gMgO与25mL水,混合均匀。将蒸馏瓶连到自动凯氏定氮仪上进行蒸馏,蒸馏时间为8min,用装有10mL0.15mol/L的H2SO4溶液和10mL蒸馏水的烧杯接收馏出液约150mL,用0.3mol/LNaOH溶液将蒸馏液调至pH7.0,最后用超纯水定容至200mL备用。3.衍生化方法:准确吸取标准溶液或样品0.2mL,加入0.3mL0.5g/L衍生试剂及0.3mL0.3mol/L硼酸盐溶液(pH8.0),用乙腈定容至1mL,涡旋振荡1min,使其充分反应。10000r/min离心5min,上清液过滤膜供液相色谱测定,测定应在48h内完成。4.HLPC条件:色谱柱:AgilentEclipseplusC18柱(250mm×4.6mm,5μm) 流动相:A为H2O,B为ACN,流速:1.0mL/min 梯度洗脱程序:0~18min,10%~95%B 18~22min,95%B 22~22.1min,95%~10%B。柱温30℃ 进样量10μL 紫外检测波长265nm。5.结果讨论:①衍生剂浓度的影响为保证检测仲丁胺时衍生化试剂完全过量,在0.30mol/L硼酸盐缓冲溶液pH值为8.0,反应时间为15min的条件下,考察了室温下不同浓度FMOC对0.2mL0.1mg/L仲丁胺标准溶液衍生化反应的影响。分别配制0.01,0.05,0.10,0.50,1.00,2.50,5.00g/L的衍生剂,与仲丁胺标准溶液进行衍生化反应。结果显示,当衍生剂浓度为0.50g/L时,仲丁胺衍生物色谱峰的峰面积最大,衍生反应最完全,而且氨基酸衍生物的峰形良好。故选择衍生剂的最佳浓度为0.50g/L。②硼酸盐缓冲溶液pH值的影响选用硼砂溶液作为缓冲溶液,分别考察了0.30mol/L硼酸盐缓冲溶液的pH值(5.0,6.0,7.0,8.0,9.0,10.0,11.0)对仲丁胺衍生化反应的影响。结果表明,当硼酸盐缓冲溶液pH值为7.0,8.0,9.0时,仲丁胺衍生产物的峰面积最高且趋于平缓。同时发现当pH值分别为5.0,6.0,7.0时仲丁胺衍生产物附近会出现1个杂峰,这可能是衍生化反应在pH≤7.0(酸性)条件下会导致产物不够稳定,产生一些副产物,故实验选择硼酸盐缓冲溶液的最佳pH值为8.0。③衍生温度与时间的影响FMOC的衍生化反应十分迅速,且条件温和,本实验考察了不同反应温度(4,10,室温(20~30℃),40,50,60℃)下仲丁胺衍生产物的色谱行为。结果发现,在4℃或10℃下衍生化样品会析出结晶,而室温(20~30℃),40,50℃时,衍生化反应产物一致,峰面积无显著变化且不会析出晶体 当温度为60℃时,峰面积会下降,说明高温下反应更倾向于FMOC的水解,因此反应温度过高会导致产物衍生化不完全,衍生化效率降低,测定结果不准确。由于在4~50℃条件下均可以进行衍生化反应,故本方法选择室温作为衍生化反应温度。吸取0.2mL0.1mg/L仲丁胺标准溶液于离心管中,在室温下分别衍生5,10,15,20,25,30min,考察不同反应时间的影响。结果显示,10min时衍生产物的峰面积明显高于5min时衍生产物的峰面积 而10min后的衍生化反应趋于完全,色谱峰的峰面积无显著变化。综合考虑实验的平行性和重现性,选择最佳衍生化时间为15min。④衍生产物的稳定性按照上述优化的衍生条件衍生后进行测定,在室温下考察测定溶液的稳定性,测定时间间隔为1,6,12,24,48,96h。结果表明,在1~48h范围内,目标物峰面积的差距很小 而96h的目标物峰面积约减少4%。为保证检测的准确性,应在48h内完成实验。⑤样品前处理方法的优化本实验采用全自动凯氏定氮仪代替原始的玻璃蒸馏装置,解决了前处理过程繁琐耗时、操作误差大等缺点,且该装置简便、安全、蒸馏速度快。由于蒸馏时间是影响该方法回收率的主要因素,故考察了凯氏定氮仪的不同蒸馏时间对回收率的影响。结果表明,最初随着蒸馏时间的延长,仲丁胺的回收率逐渐升高,当蒸馏8min时回收率达到最高值,此后继续延长蒸馏时间,仲丁胺的回收率则有所降低。因此本实验最终选择蒸馏时间为8min。⑥线性范围、检出限与定量下限采用乙腈将仲丁胺标准储备液逐级稀释成浓度为0.001,0.010,0.050,0.100,1.000mg/L的系列标准溶液,按照上述方法进行衍生化反应,衍生后分别得到仲丁胺衍生物标准工作溶液。将衍生后的溶液按浓度由低到高依次进样,以仲丁胺的质量浓度(X,mg/L)为横坐标,对应峰面积(Y)为纵坐标,得到校正曲线方程为Y=32524.7X-4.2,相关系数为0.9998,结果表明,仲丁胺在0.001~1.000mg/L范围内线性关系良好。通过加标实验,在空白基质中添加标准样品,按前述方法进行测定,以3倍信噪比(S/N=3)对应的目标物浓度作为检出限(LOD),以10倍信噪比(S/N=10)对应的目标物浓度作为定量下限(LOQ),得到仲丁胺的检出限为0.1μg/kg,定量下限为0.5μg/kg。该方法的灵敏度高,可满足样品的测定要求。⑦回收率、准确度与精密度分别选择黄瓜、西红柿、葡萄、橙、梨等作为空白样品,进行0.001,0.01,0.1mg/kg3个浓度水平的加标回收实验,每个浓度水平平行6次,结果见表1,空白样品和加标样品的色谱图见图1。仲丁胺在5种果蔬中的加标回收率为82.4%~95.2%,相对标准偏差为1.3%~6.8%。本方法的准确度和精密度均符合残留分析要求,能够满足果蔬中仲丁胺含量的测定要求。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2021/07/202107262023521821_627_1608728_3.png[/img][/align]采用全自动凯氏定氮仪代替原有的玻璃蒸馏仪进行蒸馏提取,FMOC作为柱前衍生剂,建立了高效液相色谱测定果蔬中仲丁胺含量的定量分析方法。由分析结果可知,本方法操作简单,灵敏度和稳定性高,检测周期短,可用于果蔬中仲丁胺的测定。[size=21px]四、参考文献[/size][1]He X H,Ji S J.Food Res.Dev.(何晓晗,纪淑娟.食品研究与开发),2004,25(4):144-146.[2]JiSJ,HeXH,FengH.PlantProtect.(纪淑娟,何晓晗,冯辉.植物保护),2005,(4):86-87.[3]NY/Y946-2006.Determination of sec-Butylamine Residues in Garlic Sprout Green Pepper Orangeand Grape.Agricultural Industry Standard of the People’sRepublic of China(蒜薹、青椒、柑橘、葡萄中仲丁胺残留量测定.中华人民共和国农业行业标准).[4]NY/T844-2010.Green Food-Temperatate Fruits.Agricultural Industry Standard of the People’s Republic of China(绿色食品温带水果.中华人民共和国农业行业标准).[5]HaoWX.Phys.Test.Chem.Anal.:Chem.Anal.(郝蔚霞.理化检验:化学分册),2012,48:46-48.[6]HanM,HuL,YangXF,WuXP.ActaAgric.Jiangxi(韩梅,胡莉,杨晓凤,吴显平.江西农业学报),2014,26(5):98-100.[7]ZhongJS,TangZY,YuWF.Mod.Chem.Ind.(钟九生,唐昭英,余婉凤.现代化工),2012,32(2):92-93.[8]JiSJ,YuLJ,LiuL,BaiB,ZhouD.FoodSci.(纪淑娟,于兰洁,刘玲,白冰,周丹.食品科学),2012,33(8):211-215.[9]ZhangYW,YangD,XieYM,LiuQS,WangX,SongH.Chin.J.Anal.Lab.(张义文,杨丹,谢永美,刘其松,王欣,宋航.分析试验室),2009,28(5):72-75.[10]ScudamoreKA.Analyst,1980,105:1171-1175.[11]HuJW,GaoR,CaoMJ,CaiQF,ZhangLJ,ShuWJ,LiuGM.FoodSci.(胡家伟,高榕,曹敏杰,蔡秋凤,张凌晶,苏文金,刘光明.食品科学),2014,35(8):283-288.[12]ZhangJH,OuyangL,PengXK,XiaLX,LiH,WangH.J.Instrum.Anal.(章建辉,欧阳丽,彭新凯,夏立新,李欢,汪辉.分析测试学报),2015,34(12):1430-1433.[13]YangHM,HangL,YangJG,ZhangXM,HuangWH,LiC,JiangXL.Chin.J.Anal.Chem.(杨华梅,杭莉,杨建国,张雪梅,黄为红,李晨,蒋晓丽.分析化学),2016,44(3):462-467.[14]HuangDM,HuangXY,GuRR,HuiYH,TianLL,FengB,ZhangX,YuHJ.Chin.J.Chromatogr.(黄冬梅,黄宣运,顾润润,惠芸华,田良良,冯兵,张璇,于慧娟.色谱),2014,32(8):874-879.[15]MohammadiB,TammariE,FakhriS,BahramiG.J.Chromatogr.B,2013,928:32-36.[16]RajiM,SharkhuuA,AmadM,MerzabanJ,GehringC.J.Anal.Bioanal.Technol.,2014,5(2):1-6.[17]ZieglerJ,AbelS.AminoAcids,2014,46:2799-2808.[18]BrücknerH,FlassigS,KirschbaumJ.AminoAcids,2012,42:877-885.[19]BáezME,FuentesE,EspinaMJ,EspinozaJ.J.Sep.Sci.,2014,37:3125-3132.
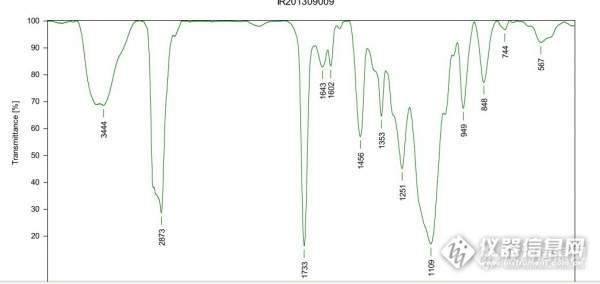
我的实验是这样的,我们在模仿国外一个丙烯酸酯聚合物的产品,从热裂解-GCMS的结果来看,里面还有丙烯酸丁酯,乙烯基吡啶等主要单体,但经过化学测试,里面胺基含量比较高,但图谱结果中却怎么也找不到含有胺基的化学物,所以一直很头疼,我想知道通过什么其他办法可以尝试知道里面的胺基到底是什么物质?谢谢!附件是该物质的红外!!http://ng1.17img.cn/bbsfiles/images/2013/11/201311181049_477794_2113729_3.jpg
[b][size=5]各位,关于氟啶胺、苯醚甲环唑、氟虫腈、丙环唑、嘧菌环胺这几种药你们有没有做过呢?我发现 几乎都是[color=#9b014f]双峰或者三个峰[/color]。。。。。在另一个检测器上都是单峰,在Agilent上就会呈现多峰,难道是程序参数问题?!。。。。讨论一下吧[/size][/b]
[color=#444444]苯胺基乙酸钾,原来一直使用重氮滴定,但是发现副产物影响,不能准确指导生产,如果用液相色谱分析,有没有朋友做过类似的分析,目前的基本思路是,加入缓冲溶液控制PH进C18柱,由于没有用缓冲盐的经验,不指导该用什么做缓冲溶液,流动相。最好能直接提供相关产品色谱分析文献。[/color]
根据GBZ/T 160.67-2004 扩项工作场所MDI。原理:空气中MDI用冲击式吸收管采集,水解后成4.4’-二氨基二苯甲烷(MDA),在碱性条件下用甲苯萃取,经七氟丁酸酐衍生后,取甲苯溶液进样,经色谱柱分离,电子捕获检测器检测,以保留时间定性,峰面积定量。标准曲线的绘制:在5 只干燥的具塞离心管中,0.0、0.25、0.50、1.0和2.0ml MDA标准溶液,用甲苯稀释至2.0ml,配制成0.0、0.025、0.050、0.10和0.20mg/ml MDA标准系列,各管加30ul 七氟丁酸酐,振摇2min,放置5min,加1ml 缓冲液,振摇2min,以除去过剩的七氟丁酸酐,放置2min,将甲苯层转移入另一离心管中,供测定。色谱柱 DB-5 柱温230℃ 进样器270℃,检测器250℃,结果只出甲苯溶剂峰。参考了些文献七氟丁酸酐与胺反应有加热55℃70分钟的,也有反应30min的。标准里衍生反应很短时间怀疑衍生反应有问题!
试问:硫酸铈能否氧化对叔丁基苯酚?可以直接电位滴定测对叔丁基苯酚的纯度吗?实验室电位滴定仪:梅特勒T50。若手动滴定,指示剂采用二苯胺磺酸钠还是邻二氮杂菲-亚铁?望指点
最近打算做蔬菜中仲丁胺的检测,标准只有农业部的行业标准,请教需要注意点什么
[color=#444444]本人在做格列喹酮原料药中环己胺残留的方法,对照品溶液环己胺的峰很好,但是在加样溶液中没有环己胺的峰。具体方法:使用DMSO做溶剂,顶空平衡温度80℃,平衡时间40min,624毛细管柱,柱温60℃保持1分钟,以5℃/min速率升到130℃,保持2分钟,然后30℃/min升到200℃。进样口温度230℃,检测器温度230℃。想问下大家知道怎么回事?怎么解决吗?[/color]
[img=,690,690]https://ng1.17img.cn/bbsfiles/images/2024/07/202407040947148726_4094_5604214_3.jpg!w690x690.jpg[/img] 沙丁胺醇检测仪的用途广泛且重要,尤其在食品安全、药品质量监控以及环境监测等领域发挥着不可或缺的作用。 在食品安全领域,沙丁胺醇检测仪主要用于检测肉类产品中是否含有过量的沙丁胺醇残留。沙丁胺醇作为一种常见的瘦肉精添加剂,如果被滥用,将对人体健康产生严重危害。因此,通过沙丁胺醇检测仪对肉类产品进行检测,可以有效防止含有过量瘦肉精的食品流入市场,保障消费者的饮食安全。 在药品质量监控方面,沙丁胺醇检测仪同样发挥着重要作用。沙丁胺醇作为一种常用的支气管扩张剂,在治疗哮喘等呼吸系统疾病方面有着广泛应用。然而,如果药品中沙丁胺醇的含量不足或超标,都将影响药品的治疗效果。因此,通过沙丁胺醇检测仪对药品进行检测,可以确保药品的质量符合标准,保障患者的用药安全。 此外,在环境监测领域,沙丁胺醇检测仪也具有一定的应用价值。虽然沙丁胺醇在环境中的含量通常较低,但长期暴露于含有沙丁胺醇的环境中也可能对人体健康产生潜在影响。因此,通过沙丁胺醇检测仪对环境中的沙丁胺醇进行检测,可以及时发现污染源,为环境治理提供科学依据。 综上所述,沙丁胺醇检测仪在食品安全、药品质量监控以及环境监测等领域具有广泛的应用价值,是保障人们健康和安全的重要工具。
[font=微软雅黑]点击链接查看更多:[url]https://www.woyaoce.cn/service/info-4155.html[/url]乙草胺(acetochlor),即2-乙基-6甲基--N-乙氧基甲基-α-氯代乙酰替苯胺,是一种广泛应用的除草剂,人体暴露在乙草胺每日摄取容许量以上的环境下会对造成一定的潜在危害影响,并且目前还不能排除基因毒性的存在。[/font][font=微软雅黑]乙草胺因其毒性,被美国环境保护局定为B-2类致癌物,规定在1个月的监测期,在20个监测井所谓地下水中残留浓度不得超过0.1μg/L,kolpin等报道了美国在乙草胺的施用期的样品检测结果,1994年雨水和喝水中最大检出浓度分别是2.5、1.2μg/L。乙草胺作为玉米、大豆、棉花和果树的除草剂,在我国的年使用量已超多10000t(原药)。[/font][font=微软雅黑]丁草胺(Butachlor),2-氯-N-(2,6-二乙基苯基)-N-(丁氧甲基)乙酰胺,是选择性芽前除草剂,植物吸收丁草胺后,在体内抑制和破坏蛋白酶,影响蛋白质的形成,抑制杂草幼芽和幼根正常生长发育,从而使杂草死亡。在粘壤土及有机质含量较高的土壤上使用,药剂可被土壤胶体吸收,不易被淋溶,特效期可达1-2个月。[/font][font=微软雅黑]丁草胺具有挥发性,它对人体皮肤和眼睛有轻微的刺激作用,中毒的主要表现为消化系统与神经系统症状。轻者可引起胃肠功能紊乱,出现恶心、呕吐、吞咽困难、头晕、头痛等;严重者可引起麻醉作用,表现为头痛、头晕、无力、面潮红,酒醉状态,恶心、呕吐、呼吸困难、眼和呼吸道刺激症状和四肢麻木等。严重时可出现意识蒙眬、抽搐、昏迷、心室纤颤,呼吸停止而即刻死亡。[/font][font=微软雅黑]鉴科检测参考《DB21T 1546-2007 土壤中乙草胺和丁草胺残留量的测定 [url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]法》,建立了利用全自动固相萃取仪(Fotector Plus)结合[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]检测沉积物中乙草胺和丁草胺残留量的方法。在40mL丙酮-正己烷(4+1)提取后过滤,再用30mL丙酮-正己烷(4+1)复提2次,合并提取液。使用Auto EVA-08IR浓缩至2mL后 Fotector Plus全自动固相萃取仪净化,自动完成 SPE 柱活化、样品上样、淋洗、收集等步骤,收集液再氮吹浓缩、溶剂转换、定容后,用GC检测。[/font]
磺胺药物对氨基苯磺酰胺的合成目的原理Ar-NHCOCH3 + 2HOSO2Cl → p-ClO2S-Ar-NHCOCH3+ HClp-ClO2S-Ar-NHCOCH3 + NH3 → p-CH3CONH-Ar-SO2NH2 + HClp-CH3CONH-Ar-SO2NH2 + H2O → p-H2N-Ar-SO2NH2 + CH2CO2H仪器药品乙酰苯胺(自制) 5g(0.037mol);氯磺酸(d=1.77) 22.5g(12.5ml,0.19mol);浓氨水(28%,d=0.9) 35ml 浓盐酸,碳酸钠。过程步骤(1)对乙酰氨基苯碘酰氯在100ml干燥的锥形瓶中,加入5g干燥的乙酰苯胺,在石棉网上用小火加热熔化。瓶壁上若有少量水气凝结,应用干净的滤纸吸去。冷却使熔化物凝结成块。将锥形瓶置于冰浴中冷却后,迅速倒入12.5ml氯磺酸,立即塞上带有氯化氢导气管的塞子。反应很快发生,若反应过于激烈,可用冰水浴冷却。待反应缓和后,旋摇锥形瓶使固体全溶,然后再在温水浴中加热10~15min使反应完全。将反应瓶在冷水中充分冷却后,于通风中在充分搅拌下,将反应液慢慢倒入盛75g碎冰的烧杯,用少量冷水洗涤反应瓶,洗涤液倒入烧杯中。搅拌数分钟,并尽量将大块固体粉碎,使成颗粒小而均匀的白色固体。抽滤收集,用少量冷水洗涤,压干,立即进行下一步反应。(2)对乙酰氨基苯磺酰胺将上述粗产物移入烧杯中,在不断搅拌中慢慢加入17.5ml浓氨水(在通风橱内),立即发生放热反应并产生白色糊状物。加完后,继续搅拌15min,使反应完全。然后加入19ml水,在石棉网上用小火加热10~15min,并不断搅拌,以除去多余的氨,得到的混合物可直接用于下一步合成。(3)对氨基苯磺酰胺(磺胺)将上述反应物放入圆底烧瓶中,加入3.5ml浓盐酸,在石棉网上用小火加热回流0.5h。冷却后,应得一几乎澄清的溶液,若有固体析出,应继续加热,使反应完全。如溶液呈黄色,并有极少量固体存在时,需加入少量活性炭煮沸10min,过滤。将滤液转入大烧杯中,在搅拌下小心加入粉状碳酸钠至恰呈碱性(约4g)。在冰水浴中冷却,抽滤收集固体,用少量冰水洗涤,压干。粗产物用水重结晶(每克产物约须12ml水),产量3~4g。熔点161~162℃。纯品对氨基苯磺酰胺为白色针状结晶,熔点163~164℃。注意事项1.氯磺酸对皮肤和衣服有强烈的腐蚀性,暴露在空气中会冒出大量氯化氢气体,遇水会发生猛烈的放热反应,甚至爆炸,故取用时需加小心。反应中所用仪器及药品皆需十分干燥,含有氯磺酸的废液不可倒入水槽,而应倒入废液缸中。工业氯磺酸常呈棕黑色,使用前宜用磨口仪器蒸馏纯化,收集148~150℃的馏分。2.酰磺酸于乙酰苯胺的反应非常剧烈,将乙酰苯胺凝结成快状,可使反应缓和进行,当反应过于激烈时,应适当冷却。3.在氯磺化过程中,将有大量氯化氢气体放出。为避免污染室内空气,装置应严密,导气管的末端要与接受器内的水面接近,但不能插入水中,否则可能倒吸而引严重事故!4.加入速度必须缓慢,必须充分搅拌,以免局部过热而使对乙酰胺基苯磺酰胺水解。这是实验成功的关键。5.尽量洗去固体所夹杂和吸附的盐酸,否则产物在酸性介质中放置过久,会很快水解,因此在洗涤后,应尽量压干,且在1~2h内将它转变为磺胺类化合物。6.粗制的对氨基苯磺酰氯久置容易分解,甚至干燥后也不可避免。若要得到纯品,可将粗产物溶于温热的氯仿中,然后迅速转移到事先温热的分液漏斗中,分出氯仿层,在冰水浴中冷却后即可析出晶体。纯品对氨基苯磺酰氯的熔点为149℃。7.为了节省时间,这一步的粗产物可不必分出。若要得到产品,可在冰水浴中冷却,抽滤,用冰水洗涤,干燥即可。粗品用水重结晶,纯品熔点为219~220℃。8.对乙酰胺基苯磺酰胺在稀酸中水解成磺胺,后者又与过量的盐酸形成水溶性的盐酸盐,所以水解完成后,反应液冷却时应无晶体析出。由于水解前溶液中氨的含量不同,加3.5ml盐酸有时不够,因此,在回流至固体全部消失前,应测一下溶液的酸碱性,若酸性不够,应补加盐酸回流一段时间。9.用碳酸钠中和滤液中的盐酸时,有二氧化碳产生,故应控制加热速度并不断搅拌使其逸出。磺胺是一两性化合物,在过量的碱溶液中也易变成盐类而溶解。故中和操作必须仔细进行,以免降低产量。分析思考 1.为什么在氯磺化反应完成以后处理反应混合物时,必须移到通风橱中,且在充分搅拌下缓缓倒入碎冰中?若在未倒完前冰就化完了,是否应补加冰块?为什么?2.为什么苯胺要乙酰化后在氯磺化?直接氯磺化行吗?3 .如何理解对氨基苯磺酰氨是两性物质?试用反应式表示磺胺与稀酸和稀碱的作用。
丙烯酰胺(1000ppm左右),氧化双三丁基锡TBTO(800ppm左右)怎么不出峰?用的是DB-XLB非极性的柱子15*0.25*0.25开始丙稀酰胺,氧化双三丁基锡试过几十ppm,没出峰,浓度加大到800-1000还是没出峰。做这些物质有哪些标准啊?升温程序:40度-保持1.5min; 120度/Min-155-保持1min; 20度/min-300度-保持8min; 进样口和传输线分别是270,280度。MS程序:0-18MIN采集信号(其中1.8-2.3关闭灯丝避开溶剂)峰难看一点没关系,但为什么会不出来呢,是分解掉了?还是化合物不稳定?查不到什么资料另外2-甲氧基乙醇和2-乙氧基乙醇虽然出峰了,但峰超级难看,是用DB-XLB这种非极性的柱子做不好吗?哪个做过的,分享下经验和注意事项?http://simg.instrument.com.cn/bbs/images/brow/em09511.gif修改:不好意思,刚才SIM时没把二甲苯麝香的离子加进去,现在出来了,但20ppm峰不高,估计要买固体标物配高浓度的来做
用TLC检测苯胺基乙腈和苯胺基乙酸钾,应该使用那种染色剂呢?基本的显色剂碘或者硫酸是否可以?
苯胺是苯分子中的一个氢原子为氨基取代而生成的化合物。分子式C6H5NH2。是最简单的一级芳香胺。无色油状液体。熔点-6.3℃,沸点184℃,相对密度 1.02173 (20/4℃),加热至370℃分解。稍溶于水,易溶于乙醇、乙醚等有机溶剂。暴露于空气中或日光下变为棕色。可用水蒸气蒸馏,蒸馏时加入少量锌粉以防氧化。提纯后的苯胺可加入 10~15ppm的NaBH4,以防氧化变质。[color=#000000][b]分子结构:[/b] 苯环上的C原子以sp2杂化轨道成键,N原子以sp3杂化轨道成键。[b] [/b][/color][color=#000000][b]苯胺[/b][/color][color=#000000][b]的化学性质:[/b]无色油状易燃液体,有强烈气味。 稍溶于水,与乙醇、乙醚、氯仿和其他大多数有机溶剂混溶。 [/color][b][color=#000000][color=#000000]苯胺[/color][/color][/b][color=#000000][b]的用途:[/b] 苯胺是重要的中间体。由苯胺生产的较重要产品达300种。世界苯胺生产厂家大约有80多个,年总生产能力已超过270万t/a,产量约230万t;主要消费领域为MDI,2000年其消费量约占苯胺总消费量的84%。我国苯胺主要消费于MDI、染料工业、橡胶助剂、医药、农药和有机中间体等方面。2000年苯胺消费量为18.5万t,产不足需,需靠进口解决。苯胺系列中间体和染料产品有:2,6-[/color][b][color=#000000][color=#000000]二乙基苯胺[/color][/color][/b][color=#000000][color=#000000]N-乙酰苯胺、对丁基苯胺、[b]邻苯二胺[/b]、二苯胺、重氮氨基苯、4,4'-二氨基三苯基甲烷、4,4'二氨基二苯基环己基甲烷、[/color][b][color=#000000]N,N-二甲基苯胺[/color][/b][color=#000000]、N-乙基苯胺、[/color][b][color=#000000]N,N-二乙基苯胺[/color][/b][color=#000000]、N,N-二丙基苯胺、对乙酰胺基苯酚、对氨基苯乙酮、4,4'-二乙氨基二苯甲酮、4-(对氨基苯)丁酸、对硝基苯胺、N-亚硝基二苯胺、[b]β-乙酰苯胺[/b]、1,4-二苯基氨基脲、2-苯基吲哚、对苯氨基苯胺、[/color][b][color=#000000]N-甲酰苯胺[/color][/b][color=#000000]、N-苯甲酰苯胺、N-乙酰苯胺、2,4,6-三氯苯胺、对碘苯胺、1-苯胺-3-甲基-5-吡唑酮、对苯二酚、二环己胺、2-(N-甲基苯胺基)丙腈、3-(N-乙基苯胺基)丙腈、2-(N-乙基苯胺基)乙醇、对氨基偶氮苯、[b]苯肼[/b]、[b]单苯基脲[/b]、双苯基脲、[b]对硫氰基苯胺[/b]、4,4'二苯基甲烷二异氰酸酯、多苯基多次甲基多异氰酸酯、4-氨基乙酰苯胺、N-甲基-N-(β-羟乙基)苯胺、N-甲-N(β-氯乙基)苯胺、[/color][b][color=#000000]N,N-二甲基对苯二胺[/color][/b][color=#000000]、N,N,N',N'-四甲基对苯二胺、N,N-二乙基对苯二胺、4,4'-甲撑双(N,N-二乙基苯胺、苯基硫脲、二苯基硫脲、对氨基苯磺酸、4,4'二氨基二苯甲烷苯醌、[/color][b][color=#000000]N,N-二乙醇基苯胺[/color][/b][color=#000000]、乙酰乙酰苯胺、对氨基酚、N-乙基苄基苯胺、N-甲基甲酰苯胺、N-甲基乙酰苯胺、对溴乙酰苯胺、双(对氨基环己基)甲烷、苯腙二苯卡巴腙、苯乙酮苯腙、[b]苯胺-2,4-二磺酸[/b]、对氨基偶氮苯-4'磺酸、苯肼-4-磺酸、硫代乙酰苯胺、[/color][b][color=#000000]2-甲基[/color][color=#000000]吲哚[/color][/b][color=#000000]、[/color][b]2,3-二甲基吲哚[/b]、N-甲基-2-苯基吲哚等。也可用作分析试剂,也用于染料、树脂、假漆及香料的合成。[/color]
蒜薹、青椒、柑橘、葡萄中仲丁胺残留量测定[b]1 范围[/b] 本标准规定了蒜薹、青椒、柑橘、葡萄中仲丁胺(2-AB)残留量的检测方法。 本标准适用于蒜薹、青椒、柑橘、葡萄中仲丁胺残留量的测定,其他果品蔬菜中仲丁胺残留量的测定可参照本标准。 本方法的最低检出限量为0.672mg/kg,测定浓度范围为0.672mg/kg~20.000mg/kg。[b]2 原理[/b] 通过水蒸气蒸馏,将样品中仲丁胺和其他挥发性胺类分离,用四氯化碳(CCL[sub]4[/sub])洗涤,除去干扰物质,在硼砂缓冲液中2-AB与2,4-二硝基氟苯(DNFB)反应,生产N-仲丁基-2,4-二硝基苯胺(BDNA),加减水解除去多余试剂,用环己烷萃取BDNA,经薄层色谱分离、净化,将2-AB色斑用三氯甲烷溶脱,用紫外/可见分光光度计在332nm处测定。[b]3 试剂与材料[/b] 除非另有说明,所用的试剂均为分析纯,所用的水均为无离子水。3.1 氧化镁固体3.2 无水硫酸钠3.3 正己烷3.4 乙醚3.5 三氯甲烷3.6 四氯化碳3.7 苯3.8 1,4-二氧六环3.9 1 mol/L氯化钙溶液 称取氯化钙(CaCl[sub]2[/sub])110.9g,溶于水中,定容至1000mL。3.10 0.05 mol/L四硼酸钠 精确称取四硼酸钠19.07g,溶于蒸馏水,定容至1000mL。3.11 0.2 mol/L硼酸 精确称取硼酸12.37g,溶于蒸馏水,定容至1000mL。3.12 硼酸盐缓冲液 将硼砂溶液与硼酸溶液按8+2比例混合制成硼酸盐缓冲液。3.13 2mol/L氢氧化钠溶液 准确称取8.00g氢氧化钠(NaOH),溶解定溶于100mL蒸馏水。3.14 0.3 mol/L氢氧化钠溶液 准确称取1.20g氢氧化钠(NaOH),溶解定溶于100mL蒸馏水。3.15 0.05mol/L碳酸钠溶液 准确称取5.30g碳酸钠(Na[sub]2[/sub]CO[sub]3[/sub]),溶解定溶于1000mL蒸馏水。3.16 0.15mol/L硫酸溶液 准确吸取9mL硫酸(H[sub]2[/sub]SO[sub]4[/sub]),溶解定容于1000mL蒸馏水。3.17 2,4-二硝基氟苯(DNFB) 在50mL蒸馏后的1,4-二氧六环中溶解0.75mL 2,4-二硝基氟苯(2,4-dinitrofluorobenzene)(简称DNFB)(当天配制)。3.18 环己烷 将500mL环己烷通过长125mm、直径25mm、填充粒径为0.2mm-0.5mm硅胶的层析柱层析,弃去开始的25mL,其余收集于干燥洁净的试剂瓶中。3.19 仲丁胺标准溶液(100μg/mL) 精确吸取14μL标准仲丁胺原液,用蒸馏水定容至100mL。3.20 仲丁胺标准使用液(100μg/mL) 精确吸取上述仲丁胺标准溶液10mL,用蒸馏水定容至100mL。[b]4 仪器[/b]4.1 高速电动组织捣碎机;4.2 恒温水浴锅(60℃±2℃);4.3 水蒸气蒸馏装置;4.4 薄层板:硅胶G(0.25mm);4.5 紫外-可见分光光度计;4.6 旋转蒸发仪。[b]5 操作方法[/b]5.1 样品处理 将果蔬样品切成小块,用组织捣碎机捣成浆状,称取50g匀浆,精确到0.1g,置于800mL蒸馏瓶中,依次加入75mL 1mol/L CaCl[sub]2[/sub]溶液、10gMgO与50mL水制成的浆状物,并用100mL水冲洗瓶壁,转动使之混合均匀。将蒸馏瓶连到水蒸气蒸馏装置上进行蒸馏,用装有10mL 0.15mol/L H[sub]2[/sub]SO[sub]4[/sub]溶液的带刻度的100mL烧杯接受馏出液约80mL,再用0.3mol/LNaOH溶液将蒸馏液调到pH=7(用pH计),最后用蒸馏水定容至100mL备用。5.2 标准工作曲线的绘制5.2.1 吸取仲丁胺标准使用液(3.19)0.0mL、1.0mL、2.0mL、4.0mL、6.0mL、8.0mL和10.0mL(相当于0.0μg、10.0μg、20.0μg、40.0μg、60.0μg、80.0μg、100.0μg),分别置于50mL具塞锥形瓶中,加蒸馏水至10mL。5.2.2 分别加入5mL硼酸盐缓冲液和2mL DNFB试剂,置60℃水浴反应30min,再加入2mL2mol/L NaOH溶液,继续恒温30min。将锥形瓶置于冰浴中冷却,在分液漏斗中用10mL环己烷萃取,弃去下层水相,再用15mL 0.05mol/L Na[sub]2[/sub]CO[sub]3[/sub]溶液洗涤环己烷萃取液,重复三次。将环己烷萃取液转移到50mL具塞锥形瓶中,加入2g无水硫酸钠,轻轻振摇,用气流蒸发除去溶剂,加入0.2mL苯将仲丁胺干燥物溶解。迅速将50μL上述溶液点在同一块薄层板上,用正己烷-乙醚(70+30)作展开剂一次展开,刮下待测组分斑点,用三氯甲烷溶解,并定容至5mL,于332nm处测吸光值,绘制标准曲线。5.3 样品测定 吸取样品溶液10mL置于50mL梨形分液漏斗中,用15mL CCl[sub]4[/sub]洗涤样品溶液,重复三次。然后转入50mL具塞锥形瓶中,以下按5.2.2方法操作,测定吸光度。从标准曲线上查出仲丁胺的残留量(μg)。[b]6 结果的表述[/b]6.1 计算计算见公式(1)[img=,182,46]https://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif[/img]………………………………………………(1)式中:X——样品2-AB的含量,单位为毫克每千克,mg/kg;c——在标准曲线上所查得的2-AB的含量,单位为微克,μg;V[sub]1[/sub]——点样体积,单位为毫升,mL;V[sub]2[/sub]——点半前苯的定容体积,单位为毫升,mL;V[sub]3[/sub]——吸取的样品蒸馏液体积,单位为毫升,mL;V[sub]4[/sub]——样品蒸馏液总体积,单位为毫升,mL;m——样品质量,单位为克,g。计算结果表示到小数点后三位。6.2 青椒、蒜薹、柑橘、葡萄检测的相对标准偏差RSD为3.4%~6.7%。6.3 青椒、蒜薹、柑橘和葡萄的回收率为85%~101%。
[em06] 各位大哥大姐:小妹急切寻找以下标准:工业甲醇,活性炭,醋酸乙酯,醋酸丁酯,叔丁胺的国家标准或行业标准.急急急.请大家帮帮忙啦!!!
[em63] 领导在催了,还有一个叔丁胺的标准还没找到,怎么办呀?大哥大姐们赶紧帮帮忙吧!!在这先感谢你们啦。
根据《食品安全法》及其实施条例的规定,按照卫生部等7部门《关于开展食品包装材料清理工作的通知》(卫监督发〔2009〕108号)的要求,经组织专家评估,现公布聚己二酰丁二胺等107种可用于食品包装材料的树脂名单。 聚己二酰丁二胺等107种可用于食品包装材料的树脂名单序号CAS号中文名称通用类别名特定迁移量/最大残留量备注 1. 50327-22-5;50327-77-0聚己二酰丁二胺PA 2. 9010-94-02-甲基-2-丙烯酸甲酯与1,3-丁二烯、苯乙烯和2-丙烯腈的共聚物ABS6 mg/kg(1,2-丙烯酸-2-甲基甲酯:SML);1 mg/kg(1,3-丁二烯:QM)或 ND(1,3-丁二烯:SML,DL=0.020 mg/kg);ND(2-丙烯腈:SML,DL= 0.020 mg/kg) 3. 68441-52-11,3-丁二烯低聚的均聚物BDR1 mg/kg(丁二烯:QM);ND(丁二烯:SML,DL= 0.020 mg/kg 4. 68441-14-52-甲基-1,3-丁二烯与溴化-2-甲基-1-丙烯的聚合物 BIIR 5. 26007-43-2乙烯与二环庚-2-烯共聚物 E/NB0.05 mg/kg(二环庚-2-烯:SML)
有哪位大神做过职业卫生的乙胺 乙二胺和环己胺的测定,我始终找不到乙二胺的峰,如果有做出来的,能发一下条件吗