新华社华盛顿8月7日电(记者林小春)两项7日发表在美国《科学-转化医学》杂志上的研究称,马兜铃酸会导致人体发生大量基因突变,从而引发癌症,其致癌性强于烟草和紫外线。 马兜铃酸天然存在于马兜铃、寻骨风、天仙藤和朱砂莲等马兜铃科植物中。20多年前,含有这类成分的中草药减肥药被发现会导致肾损害,后来人们又发现它还增加罹患尿路癌症的风险。约10年前,世界卫生组织下属的国际癌症研究中心将马兜铃酸列为一类致癌物。 美国约翰斯·霍普金斯大学与纽约州立大学石溪分校等机构研究人员在一项研究中报告说,他们对接触过马兜铃酸的19名上尿路癌症患者以及没有接触这种毒物的另7名患者进行了全外显子组测序。结果发现,马兜铃酸接触组每名患者平均发生753个基因突变,而非马兜铃酸接触组每名患者只有91个基因突变。研究表明,马兜铃酸能引发的基因突变数量高于烟草和紫外线。 另一项研究由来自新加坡、美国与中国台湾等多个医学机构的研究人员合作完成。他们利用全基因组和外显子组测序技术证实,接触马兜铃酸可能会引起过去被认为由其他致癌因素导致的癌症。例如,一种过去被认为是由吸烟引起的上尿路癌症和一种过去被归因于某种慢性肝炎感染所致的肝癌,可能均与马兜铃酸有关。研究人员表示,这是首次证实马兜铃酸与肝癌之间的相关性。 2004年,中国国家食品药品监督管理局根据对含马兜铃酸药材及其制剂不良反应的报道以及毒副作用研究和结果的分析,决定加强对含马兜铃酸药材及其制剂的监督管理,凡是含有马兜铃酸的中药制剂一律严格按处方药管理。
马兜铃酸和甲醇理论上会发生酯化反应,但是加过浓硫酸,加热至70℃左右和除水剂等都不发生反应,该怎么办
马兜铃酸的制备条件有人熟吗?小弟正在做希望熟悉的大虾都来帮忙啊
细辛中马兜铃酸的限量检查:按照药典的条件,由于含量特别低,旁边貌视有杂峰干扰(杂峰也是很小的),这样测出的结果准确吗?版友们有没有谁做过?
各位大虾,有谁有大黄蒽醌类的化合物和马兜铃酸A的图谱解析,主要是几个碎片离子峰的就可以了~~谢谢哦大黄酸:282.8 ,239,211,183芦荟大黄酸:269,240,223,181.1大黄素:269.1,241,225,210,197.1,181.9大黄酚:253.1,225大黄素甲醚:283.2,240.1
[size=18px][font=Arial, sans-serif]马兜铃酸,[/font][font=Arial, sans-serif]一类硝基菲羧酸.进行SPE固相萃取时,大量的样品被淋洗出来.[/font][/size][size=18px][font=Arial, sans-serif]具体步骤:3 mL甲醇活化,3 mL水平衡,上样1 mL,用1 mL水淋洗,1 mL水:甲醇=1:1淋洗,最后用1 mL纯甲醇洗脱.[/font][/size][size=18px][font=Arial, sans-serif]洗脱下来只有20%.后来发现1 mL淋洗的水中有50%的样品被冲下来.[/font][/size][size=18px][font=Arial, sans-serif]新人求助,这是怎么回事.老师之前这么做一点问题没有[img]https://simg.instrument.com.cn/bbs/images/default/em09509.gif[/img][/font][/size][size=18px][font=Arial, sans-serif]用的是C18小柱,C8的也试过了.牌子用过Simon的和艾杰尔的.[/font][/size][size=18px][font=Arial, sans-serif]中间也没有加负压抽干,马兜铃酸溶于甲醇,微溶于水.[/font][/size][size=18px][font=Arial, sans-serif][/font][/size]
求助1个标准,谢谢! 1、BJY 202108 龙胆泻肝丸中马兜铃酸I成分 检查项补充检验方法
[size=18px]目的 建立镇脑宁胶囊中马兜铃酸类成分的超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]-串联质谱联用检测分析方法。 方法 采用Phenomemex Kinetex (2.1 mm×100 mm,2.6 μm)色谱柱,以甲醇-体积分数0. 1%甲酸溶液(含1mmolL-1乙酸铵)为流动相梯度洗脱,流速0.3 mLmin-1,以正离子多反应监测模式,建立同时测定镇脑宁胶囊中马兜铃酸Ⅲa、7-羟基马兜铃酸Ⅰ、马兜铃酸Ⅳa、马兜铃酸Ⅱ、马兜铃内酰胺BⅡ、马兜铃内酰胺Ⅰ、马兜铃酸Ⅰ共7种马兜铃酸类成分的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]检测方法。 结果 马兜铃酸Ⅲa、7-羟基马兜铃酸Ⅰ、马兜铃酸Ⅳa、马兜铃酸Ⅱ、马兜铃内酰胺BⅡ、马兜铃内酰胺Ⅰ、马兜铃酸Ⅰ分别在1.241~1 240.572、1.034~1 034.056、2.109~2 108.709、1.070~1 070.378、1.064~1 064.000、2.154~2 154.022、1.086~1 085.922 ngmL-1 内线性关系良好 平均加样回收率分别为101.8% (RSD1.84%)、101.9% (RSD 2.67%)、102.2% (RSD 2.74%)、102.1%(RSD 2.13%)、101.8% (RSD 2.60%)、100.7% (RSD 0.96%)、104.1% (RSD 6.15%)。10批样品均检出马兜铃酸Ⅳa、马兜铃内酰胺Ⅰ和马兜铃酸Ⅰ等马兜铃酸类成分,含量范围分别为3.875~6.913,2.984~6.072 及0.350~1.719 ngg-1,而马兜铃酸Ⅲa、7-羟基马兜铃酸Ⅰ、马兜铃酸Ⅱ和马兜铃内酰胺BⅡ均未检出。 结论 建立的同时测定7种马兜铃酸类成分的[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]方法准确、可靠。镇脑宁胶囊中检出马兜铃酸Ⅳa、马兜铃内酰胺Ⅰ和马兜铃酸Ⅰ。其中,马兜铃酸Ⅳa、马兜铃内酰胺Ⅰ毒性较低或无明显毒性,而真正可能有毒性的是含硝基基团的马兜铃酸Ⅰ,因部分样品马兜铃酸Ⅰ含量超出限度,提示该制剂中需严格控制马兜铃酸Ⅰ的含量。[/size]
细辛药材中,用液相(岛津lc-2010c)作马兜铃酸I的出峰时间是多少?请做过的同志指导一下,或者麻烦您把图发上来研究一下。谢谢。
3-甲基戊烯二酸经BSTFA衍生可生成3-甲基戊烯二酸(1), 3-甲基戊烯二酸(2), 3-甲基戊烯二酸(3), 3-甲基戊烯二酸(4)4种产物,其中前3种分子量为288,另一种为360。只知一种分子量为288的结构式的可能,那另两种分子量288可能是什么结构,还是空间结构的不同?分子量360又是何结构?求高手帮忙!请见附件。
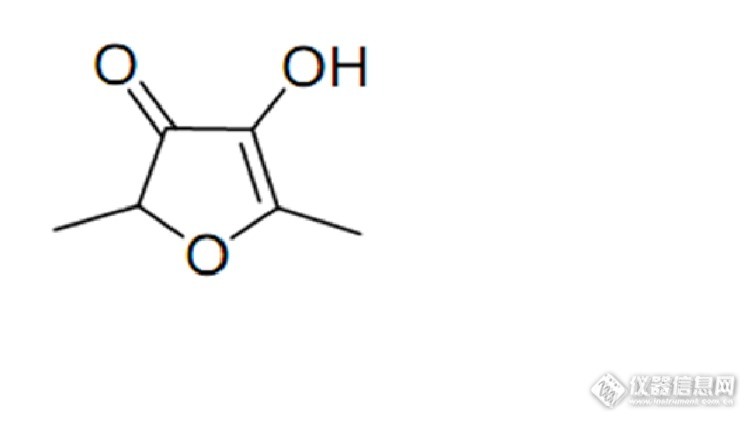
4-羟基-2,5-二甲基-3(2H)-呋喃酮的 代谢产物是啥http://ng1.17img.cn/bbsfiles/images/2015/09/201509231413_567309_1834473_3.png 英文名称是4-hydroxy-2,5-dimethyl-3(2H)-furanone CAS号是3658-77-3分子结构式是C6H8O3
如图 B是可以买到的标品从天然产物中分离得到A请问大家想制备A的标品可以用什么方法可以利用B去甲基吗 还是只能自己再分离纯化呢[img]https://ng1.17img.cn/bbsfiles/images/2022/03/202203311431441756_1050_5477041_3.png[/img]

“超高效液相色谱-串联质谱法测定大豆中草甘膦及其代谢物氨甲基膦酸的残留”是本人去年开展大豆中草甘膦检测项目整个试验过程的总结,欢迎各位老师和同行批评指正,该文章还未在任何刊物上发表。[align=center][b]超高效液相色谱-串联质谱法测定大豆中草甘膦及其代谢物氨甲基膦酸的残留[/b][/align][align=center][/align][align=center]户江涛[/align][align=center](黑龙江省农垦科学院测试化验中心,黑龙江 佳木斯 154007 )[/align]摘要:采用超高效液相色谱-串联质谱法建立了快速检测大豆中草甘膦和氨甲基膦酸残留量的分析方法。试样经水超声提取,二氯甲烷去除脂肪,C[sub]18[/sub]固相萃取柱净化后,在硼酸钠缓冲溶液中与9-芴甲氧羰酰氯(FMOC-Cl)进行衍生反应,其衍生产物在C[sub]18[/sub]色谱柱上以 2 mmol/L 乙酸铵溶液和乙腈为流动相,进行液相色谱分离:质谱检测采用电喷雾正离子化模式和多反应监测模式(MRM)。结果表明,草甘膦和氨甲基膦酸在0.001~0.5 mg/L范围内线性关系良好,相关系数(R)分别为0.9996和0.9993,定量限(LOQ)均为0.01mg/kg。在空白大豆样品添加浓度为0.02、0.2、2 mg/kg 时,草甘膦和氨甲基膦酸的平均回收率分别为80.2%~91.5%和77.7%~89.3%,相对标准偏差(RSD)分别为3.37%~6.96%和4.11%~8.27%(n=6)。本方法快速、简便、灵敏,适用于大豆中草甘膦和氨甲基膦酸残留的同时检测。关键词:超高效液相色谱-串联质谱;大豆;草甘膦;氨甲基膦酸;衍生反应[align=center]Determination of glyphosate and its metabolite aminomethyl-phosphonic acid residues in soybean by ultra performance liquid chromatography-tandem mass spectrometry[/align][align=center]HU Jiangtao[/align][align=center]([i]Testing and Analysis Center of Heilongjiang Academy of Land Reclamation Sciences, Jiamusi 154007,China[/i])[/align][b]Abstract:[/b]A method[b] [/b]was developed for the determination of glyphosate(PMG) and aminomethyl-phosphonic acid(APMA) residues in soybean by ultra performance liquid chromatography-tandem mass spectrometry(UP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url]/MS). After extracted with water under ultrasonication, the sample was defatted with dichloromethane and purified by C[sub]18 [/sub]solid phase extraction cartridge, and then PMG and APMA were derivatized using 9-fluorenylmethoxycarbonyl(FMOC-Cl) in borate buffer for 2 h.The derivatives of PMG and APMA were separated on a Waters BEH C[sub]18[/sub] column with gradient elution with the mobile phase of 2 mmol/L ammonium acetate and acetonitrile, and finally detected by positive eletrospray ionization-mass spectrometry(ESI[sup]+[/sup]-MS/MS) in multiple reaction monitoring(MRM) mode.The results showed the linearities of PMG and APMA were good in the concentration range of 0.001~0.5 mg/L ,and the correlation coefficients were 0.9996 and 0.9993 respectively. The limit of quantification(LOQ) of PMG and APMA was both 0.01mg/kg. At the spiked levels of 0.02、0.2、2 mg/kg in the blank soybean samples, the mean recoveries of PMG and APMA were 80.2%~91.5% and 77.7%~89.3% respectively, and the relative standard deviation(RSD) of PMG and APMA were 3.37%~6.96% and 4.11%~8.27% res-pectively(n=6).This method is fast,simple,sensitive, and suitable for simultaneous determination of PMG and APMA in soybean.[b]Key words: [/b]ultra performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS) soybean glyphosate(PMG) aminomethyl-phosphonic acid(APMA) derivatization草甘膦(Glyphosate,PMG)又名镇草宁、农达,分子式为C[sub]3[/sub]H[sub]8[/sub]NO[sub]5[/sub]P,是1971年美国孟山都公司研发的一种有机磷除草剂,因其兼具内吸、传导性、灭生性及非选择性,同时不易在生物体内累积,故广泛应用于农业生产中一年生和多年生杂草防除,是目前世界上应用最广、生产量最大的除草剂[sup][/sup]。草甘膦及其在植物中的主要代谢物氨甲基膦酸(Aminomethyl-phosphonic acid,APMA,分子式为CH[sub]6[/sub]NO[sub]3[/sub]P)均属于强极性、易溶于水的高沸点化合物,具有不易挥发、无紫外吸收等特性,因此用常规方法分析检测十分困难[sup][/sup]。 目前, PMG和APMA残留检测的方法主要有色谱法(GC[sup][/sup]、LC[sup][/sup]、IC[sup][/sup])、质谱法(GC/MS[sup][/sup]、ICP/MS[sup][/sup]、LC/MS/MS[sup][/sup])、光谱法[sup] [/sup]等。光谱法虽然操作简便,但其灵敏度不高,而[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]法[sup][/sup]只能适用于水样等简单基质,用于植物源样品检测时干扰太大;用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]和[url=https://insevent.instrument.com.cn/t/bp][color=#3333ff]气质联用[/color][/url]技术检测时,需要将PMG和APMA衍生转化为可气化物质,其引入试剂多、过程相对繁琐,效率较低[sup][/sup];用LC/MS/MS法直接检测时[sup][/sup],由于PMG和APMA分子量(分别为169、111)均较小,其主要碎片离子的质荷比多在100以下,检测实际样品时受基质干扰严重,灵敏度较低,因此柱前衍生——[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质联用[/color][/url]法成为近年来国内外检测PMG和APMA残留的主流方法[sup][/sup]。以9-芴甲氧羰酰氯(FMOC-Cl)做为衍生试剂,在硼酸盐缓冲溶液中与PMG和APMA水提取液相容性好,过程简单,其衍生产物在LC/MS/MS中响应信号高,碎片离子干扰小,适合定性定量分析。 目前,采用柱前衍生——LC/MS/MS法检测茶叶、稻米等基质中PMG和APMA残留的报道很多[sup][/sup],专门针对大豆基质的报道很少。行业标准[sup][/sup]的适用范围虽然包括了大豆基质,但该方法在实验过程中试剂用量大、操作繁琐(反复调pH值)、衍生时间长(需过夜),尤其是使用阳离子交换柱(CAX)洗脱时需要加入11 mL 1%的盐酸甲醇水(20/80,v/v),水分含量过高导致旋转蒸发时很难蒸干,容易造成PMG和APMA回收率不稳定。本文专门针对大豆这类高蛋白、高脂肪含量的特殊基质,采用纯水作为提取试剂,二氯甲烷去除脂溶性杂质,C[sub]18[/sub]固相萃取小柱净化后采用FMOC-Cl衍生,最后用UPLC/MS/MS测定。该方法前处理过程简便、快速、灵敏度高,适用于大豆中PMG和APMA的残留检测。[b]1 实验部分[/b]1.1 材料与试剂 草甘膦、氨甲基膦酸(纯度≥99%,德国Dr.Ehrensorfer公司);FMOC-Cl(纯度99%,Sigma公司),使用时配置成10g/L的丙酮溶液;乙腈、二氯甲烷、甲酸、乙酸铵(色谱纯,美国Fisher公司);十水四硼酸钠(优级纯,天津市科密欧化学试剂有限公司),使用时配置成50g/L的水溶液;实验用水为Millipore纯水仪制备;C[sub]18[/sub]固相萃取小柱(200mg/3ml,美国Agilent公司)。1.2 仪器与设备 Acquity UPLC型超高效液相色谱仪(Waters公司);XEVO TQ-S三重四级杆质谱仪(Waters公司);CR21GⅢ型高速离心机(HITACHI公司);KQ5200DB型台式超声波仪(昆山市超声仪器有限公司);涡旋混合器(IKA公司)。1.3 标准溶液的配置 分别称取草甘膦和氨甲基膦酸标准品10mg(精确到0.1mg),用水溶解并定容至10mL,配置成质量浓度为1.0 mg/mL标准储备液,于4℃冰箱保存待用;使用时用水逐级稀释成所需浓度的混合标准工作液。1.4 样品前处理 提取:称取粉碎均匀后的试样1.0g(精确到0.01g)于50mL聚乙烯离心管中,加入10.0mL超纯水,涡旋混合30 s并超声提取20 min后,以10000 r/min离心3 min,将上清液转移至另一离心管中,加入5 mL二氯甲烷涡旋混合30 s,以10000 r/min离心3 min,上清液待净化。 净化:取2.5 mL上清液加入到C[sub]18[/sub]固相萃取柱(使用前依次用3mL甲醇和3mL超纯水活化)中,弃去最初的几滴流出液(约0.5 mL),将剩余部分用5 mL玻璃管收集,待衍生。 衍生:取1.0 mL净化液于5 mL离心管中,依次加入1.0 mL 50g/L的硼酸钠溶液和 1.0 mL 10g/L的FMOC-Cl衍生液,混匀后室温下衍生2 h,以10000 r/min离心3 min,取上清液过0.22 mm有机系微孔滤膜后,供UPLC/MS/MS分析测定。1.5 液相色谱及质谱条件 液相色谱:色谱柱:Waters BEH C[sub]18[/sub](1.7 μm,50mm×2.1mm);柱温:30℃;流速:0.5 mL/min;进样量:2 μL;流动相A:乙腈;流动相B: 2 mmol /L 的乙酸铵水溶液。梯度洗脱程序:0~0.5min,10% A;0.5~3. 0 min,10%~100% A;3. 0 ~4. 0 min,100%A,4 ~4.1min,100% A~10% A,4.1 ~5.0min 10% A。 质谱:离子源:电喷雾离子源( ESI [sup]+[/sup] ) ;扫描方式:正离子扫描;检测方式:多反应监测( MRM);毛细管电压:3.2 kv;离子源温度:150℃;去溶剂气温度:500℃;去溶剂气流量:1000 L /h;定性、定量离子对及碰撞能量见表1。[align=center]表1 PMG-FMOC和 AMPA-FMOC的MRM质谱参数[/align][align=center]Table 1 MRM parameters of PMG-FMOC and AMPA-FMOC[/align][table][tr][td][align=center]Analyte[/align][/td][td][align=center]Cone/V[/align][/td][td][align=center]Parent ion/(m/z)[/align][/td][td][align=center]Daughter ion/(m/z) [/align][/td][td][align=center]Collision energy/V[/align][/td][/tr][tr][td][align=center]PMG-FMOC[/align][align=center] [/align][align=center]AMPA-FMOC[/align][/td][td][align=center]30[/align][align=center] [/align][align=center]30[/align][/td][td][align=center]392[/align][align=center][sup] [/sup][/align][align=center]334[/align][align=center][sup] [/sup][/align][/td][td][align=center]88[/align][align=center]214﹡[/align][align=center]112﹡[/align][align=center]179[/align][/td][td][align=center]14[/align][align=center]8[/align][align=center]11[/align][align=center]20[/align][/td][/tr][/table]﹡quantitative ion[b]2 结果与讨论[/b]2.1 色谱及质谱条件的优化 流动相的选择:对比了酸性体系(0.1%甲酸水溶液)与非酸性体系(乙酸铵水溶液)分别于甲醇、乙腈的流动相体系组合,结果发现两种分析物在酸性体系中分离效果欠佳,峰形拖尾严重,而在非酸性体系中其色谱分离效果得到明显改善,峰形对称;乙腈比甲醇体系洗脱能力更强,可以有效缩短分析时间。故本研究采用乙酸铵水溶液+乙腈流动相体系,并比较了1、2、5 mmol/L三种乙酸铵浓度与乙腈的组合,结果发现随着乙酸铵浓度的增加,目标物响应值虽略有提高但相差不大,而同时仪器背景值却显著升高,综合考虑目标物信号强度、信噪比、色谱分离效果以及分析时间等因素,本实验最终选择了2 mmol /L 乙酸铵水溶液+乙腈分析体系。质谱的选择:PMG、 AMPA对应的衍生物PMG-FMOC、AMPA-FMOC分子量分别为391、333。用超纯水配置10 mg/L 混合标准溶液直接注射到质谱中,在正负离子模式下分别进行母离子全扫描,发现正离子模式下392、334具有很好的响应,然后分别以392、334为母离子进行子离子全扫描,各得到两组丰度高、干扰小的子离子对进行MRM监测,最终确定的质谱条件见表1。2.2 前处理条件的优化 提取溶液的选择:PMG和APMA属于强极性物质,易溶于水,难溶于有机溶剂,故一般采用极性溶剂提取,如纯水及KOH、NaHCO[sub]3[/sub]溶液等[sup][/sup]。实验发现,用碱性溶液提取后,大豆中脂肪、蛋白等物质会与碱性物质发生反应,导致离心后的提取液异常浑浊,不利于后期净化和衍生,因此本实验采用纯水作为提取试剂,再经二氯甲烷液液萃取去除脂溶性杂质。 净化柱的选择:研究发现,对提取后的溶液不经SPE净化直接进行衍生, PMG和APMA的回收率均不足30%,且精密度很差,这可能是由于大豆中富含脂肪、蛋白质等物质干扰衍生过程,故本实验比较了对脂肪、蛋白质有很好去除效果的C[sub]18[/sub]、中性Al[sub]2[/sub]O[sub]3[/sub]、HLB固相萃取SPE柱的净化效果,结果发现提取液经中性Al[sub]2[/sub]O[sub]3[/sub]净化后,PMG和APMA几乎检测不到;而C[sub]18[/sub]净化后目标物回收率为92.7%、90.8%,HLB为83.6%、80.5%。故本实验选取了净化效果更好,成本相对低廉的C[sub]18[/sub]固相萃取小柱。 衍生条件的优化:FMOC-Cl的衍生机制是在碱性环境下(pH=9.0)通过FMOC-Cl基团取代目标化合物氮原子上的氢,从而生成较稳定的化合物FMOC-Cl。参照行业标准[sup][/sup]及文献报道[sup][/sup]所选用的缓冲液浓度,本实验采用50g/L的硼酸钠水溶液缓冲液体系,设置的衍生试剂质量浓度为1、2、5、10、20 g/L FMOC-Cl丙酮溶液,按照本文1.4步骤对PMG和APMA质量浓度为0.5 mg/L的纯水溶液和大豆空白基质溶液分别进行衍生,结果见图1。结果表明,在纯水溶液中,FMOC-Cl浓度为2 g/L时,PMG和APMA的峰面积已达到最大,随着衍生化试剂浓度的升高,其峰面积无明显变化;而在大豆空白基质溶液中,FMOC-Cl低浓度(1、2g/L)时,PMG和APMA几乎检测不到,其峰面积随衍生化试剂浓度增加而加大,浓度到达一定程度(10 g/L)时,峰面积不再变化。产生这种现象的原因,可能是由于尽管大豆提取液经过了二氯甲烷和C[sub]18[/sub]小柱的净化,但还是会有少量水溶性蛋白、脂肪等杂质残留在净化液中,这些杂质可能会与衍生试剂反应,影响目标物的衍生效果。研究还发现,当FMOC-Cl浓度为20 g/L时,得到的PMG和APMA色谱峰产生拖尾现象,可能是由于衍生试剂化学性质较活泼,其用量大时,过量的FMOC-Cl会迅速转化成FMOC-OH,干扰目标物峰形。在50g/L硼酸钠水溶液、10 g/L FMOC-Cl丙酮溶液条件下,考察不同时间(0.5h、1h、2h、4h、8h和16h)对衍生效果的影响,结果发现,2 h后PMG和APMA的测定值无明显增加。因此,本实验最终选定的衍生条件为50g/L硼酸钠水溶液、10 g/L FMOC-Cl丙酮溶液,室温下衍生2 h。[img=,596,378]http://ng1.17img.cn/bbsfiles/images/2017/07/201707020904_01_2984502_3.png[/img][img=,690,530]http://ng1.17img.cn/bbsfiles/images/2017/07/201707020904_02_2984502_3.png[/img]2.3 基质效应的考察 基质效应(主要是抑制)是LC/MS/MS仪器检测时经常遇到的现象。由于本实验采用极性很强的水作为提取剂,大豆中的色素、脂肪酸等极性较强的物质也有少部分进入到最后的上机液中,在离子化带电过程中会与目标物产生竞争,抑制目标物的离子化效率。实验考察了用PMG和APMA的纯水标样去标定经过本文1.4步骤处理后的大豆空白基质溶液配置的同浓度标样,其色谱图见图2。结果发现,PMG在纯水和大豆空白基质中峰面积基本一致,而APMA在大豆空白基质中的峰面积仅为纯水中的55.7%,产生了明显的基质抑制效应。为了消除基质干扰,本实验选用大豆样品空白基质配置不同浓度的标准溶液来绘制标准曲线进行校准。2.4 线性范围和定量限 用大豆空白基质溶液分别配置0.001、0.005、0.01、0.05、0.1、0.2、0.5 mg/L的PMG和APMA混合标准溶液,按本文1.4步骤衍生后测定,以各自定量离子的峰面积为Y对应质量浓度X(mg/L)做标准曲线,得到的线性方程和相关系数见表2。结果表明,这两种物质在0.001~0.5 mg/L浓度范围内线性良好,相关系数R分别为0.9996和0.9993。以10倍信噪比(S/N)计算,该方法PMG和APMA的定量限(LOQ)均为0.01 mg/kg。[align=center]表2 PMG和APMA大豆基质标准溶液的线性方程、相关系数和定量限(LOQ)[/align][align=center]Table 2 Linear equations,correlation and LOQ of PMG and APMA in the soybean matrix standard solutions[/align][table][tr][td][align=center]Analyte[/align][/td][td][align=center]Linear range/(mg/L)[/align][/td][td][align=center]Linear equation[/align][/td][td][align=center]R[/align][/td][td][align=center]LOQ/(mg/ kg )[/align][/td][/tr][tr][td][align=center]PMG[/align][align=center]AMPA[/align][/td][td][align=center][sup]0.001~0.5[/sup][/align][align=center][sup]0.001~0.5[/sup][/align][/td][td][align=center]Y=889809x+1671.3[/align][align=center]Y=476982x+1161.9[/align][/td][td][align=center]0.9996[/align][align=center]0.9993[/align][/td][td][align=center]0.01[/align][align=center]0.01[/align][/td][/tr][/table]2.5 回收率和精密度 称取大豆空白试样1.0 g,分别添加0.02、0.2、2 mg/kg水平的PMG和APMA混合标样,每个水平重复6次,按照本文1.4步骤前处理方法处理后上机检测,实验结果见表3。从表3可以看出,PMG的平均回收率为80.2%~91.5%,相对标准偏差(RSD,n=6)为3.37%~6.96%;APMA的平均回收率和RSD分别为77.7%~89.3%和4.11%~8.27%。[align=center]表3 大豆中PMG和APMA的加标回收率和相对标准偏差(n=6)[/align][align=center]Table 3 Recoveries and relative standard deviations(RSD)of PMG and APMA spiked in the soybean(n=6) [/align][table][tr][td][align=center]Analyte[/align][/td][td][align=center]Spiked level(mg/kg)[/align][/td][td][align=center]Recovery/%[/align][/td][td][align=center]RSD/%[/align][/td][/tr][tr][td]PMGAMPA[/td][td][align=center]0.02[/align][align=center]0.2[/align][align=center]2[/align][align=center]0.02[/align][align=center]0.2[/align][align=center]2[/align][/td][td][align=center]80.2[/align][align=center]91.5[/align][align=center]86.8[/align][align=center]77.7[/align][align=center]89.3[/align][align=center]85.9[/align][/td][td][align=center]6.96[/align][align=center]3.37[/align][align=center]3.95[/align][align=center]8.27[/align][align=center]4.25[/align][align=center]4.11[/align][/td][/tr][/table][b]3 结语[/b] 本文建立了超高效液相色谱-串联质谱法(UPLC/MS/MS)测定大豆中草甘膦及其代谢物氨甲基膦酸残留的分析方法。该方法灵敏度高,PMG和APMA定量限(LOQ)达到0.01 mg/kg,能满足大豆产品相关限量标准要求。同时该方法具有较高的准确度和精密度,前处理步骤简单快速,特别适合大批量大豆样品的检测。
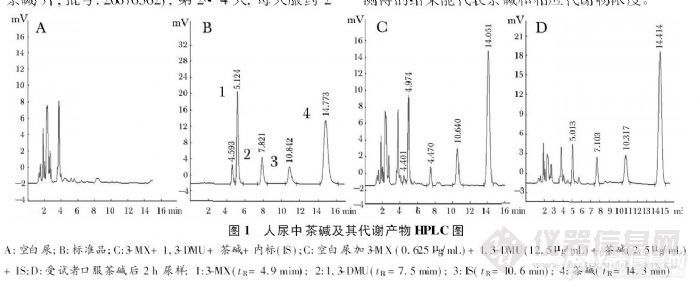
(这篇文章为什么那么贵?花费知网6元啊,心疼!!!)15.2 反相HPLC法同时测定人尿中茶碱及其两种代谢产物聂松柳1 , 刘海燕2 , 谢林安徽省六安市人民医院药剂科, 六安237005, 安徽中国药科大学药物代谢动力学重点实验室, 南京210009, 江苏摘要 目的: 建立一种同时测定人尿中茶碱及其1, 3-二甲基尿酸( 1, 3-DMU) 和3-甲基噻嗪( 3-MX)代谢产物的HPLC 方法。方法: 尿样用异丙醇二氯甲烷( 28) 混合液提取, 有机相在空气吹干, 用流动相复溶后进行HPLC 分析。色谱柱为DiamonsilODS C185 m, 150 mm 4. 6 mm I. D) , 流动相由0. 1% 甲酸液和乙腈( 95: 5 ) 组成, 流速1. 0 mLmin, 测定波长280 nm。测定12 名受试者单剂量和多剂量口服茶碱后24 h 内尿中茶碱及其代谢物累计排泄量。结果: 尿中茶碱及其代谢物1, 3 DMU 和3-MX 的线性范围分别为0. 312~40. 0、0. 156~ 20. 0、0 . 078~ 10. 0 gmL, 最低可定量浓度分别为0. 312、0. 156、0. 078 gmL。批间和批内的变异小于15%, 回收率大于70%。结论: 该方法的特异性、灵敏度能够满足临床上对人尿中茶碱及其代谢产物同时测定的要求。关键词 茶碱; 药代动力学;HPLC; CYP1A2http://ng1.17img.cn/bbsfiles/images/2012/07/201207232307_379304_2355529_3.jpg
我要测尿中有机磷农药的代谢产物,有磷酸二甲酯、磷酸二乙酯、二甲基硫代磷酸酯、二乙基硫代磷酸酯、二甲基二硫代磷酸酯、二乙基二硫代磷酸酯、以及内标物二丁基磷酸酯。在求助一下:有没有不需要衍生的方法测尿中的代谢产物。谢谢
离子阱质谱进行代谢产物的定性鉴识,在已经优化了色谱条件的情况下,质谱设定有没有什么特别的规定?问1:口服给药较高的剂量大鼠,收集尿液进行定性鉴识,采用固相萃取浓缩10倍,才可以检测到,浓缩5倍,2倍,检测的代谢产物较少,因此想知道在仪器设定上有什么特别的要求没有?就是质谱参数这一块,怎么能够提高检测灵敏度?问2:3级质谱扫描的结果往往都不好,很多的3级质谱都没有结果,也就是现在除了浓度特别高的以外,大多数的都是只有2级质谱的结果。请问是不是参数设定上有问题?因为实验对象是代谢产物,所以浓度低,但是也有在文献中看到别人尿液稀释后进样也有测定出结果的,因此想问问,代谢产物鉴识,离子阱质谱有什么特别的设定要求?
看到前人用GC-MS测的好像大部分都是初级代谢产物,如氨基酸、糖类等,不知可否测出植物的次级代谢产物。是否有人做过类似工作呢?求指点。
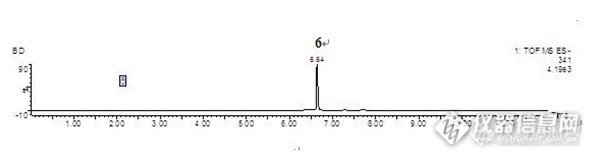
盐酸芬戈莫德在大鼠体内代谢的尿液及胆汁样品分析芬戈莫德最初是由冬虫夏草(子囊菌亚门赤僵菌)培养液中提取的抗生素成分经化学修饰后合成的免疫抑制剂。药物及实验动物:盐酸芬戈莫德为本所研制,实验用大鼠为Wistar雄性大鼠,6-8周龄,体重范围约200-250g/只,本所实验中心提供;大鼠代谢笼为苏州动物实验仪器厂产品。色谱条件色谱柱:Acquity BEH C18 (100mm×2.1mm,1.7μm)流动相:A:水(0.05%TFA)B:乙腈(0.05%TFA)质谱条件结果分析:通过比较大鼠灌胃盐酸芬戈莫德溶液后收集的尿液样品、空白尿液样品及分到的代谢产物的高分辨质谱和多级质谱数据,在给药后的尿液中共鉴定出了8个代谢产物(如下图)所有代谢产物的高分辨质谱数据的准确度均小于1PPm。通过比较大鼠灌胃盐酸芬戈莫德溶液后收集的胆汁样品、空白胆汁样品及分到的代谢产物的高分辨质谱和多级质谱数据,在给药后的胆汁中共推测出了4个代谢产物(如下图)。所有代谢产物的高分辨质谱数据的准确度均小于1PPm。结果与讨论:经过对于给药后大鼠尿液及胆汁样品分析,初步推测盐酸芬戈莫德在大鼠体内的代谢产物有8种。
喹乙醇(N-羟乙基-3-甲基-2-喹啉酰胺-1,4-二氧化物)是一种化学合成抗菌促生长剂。1965年由德国拜尔公司等首先发现它对动物具有促生长作用。由于喹乙醇有中度至明显的蓄积毒性,对大多数动物有明显的致畸作用,对人也有潜在的三致性,即致畸形,致突变,致癌。因此喹乙醇在美国和欧盟都被禁止用作饲料添加剂。《中国兽药典》(2010版)也有明确规定,喹乙醇被禁止用于家禽及水产养殖。农业部在2001年第168号公告中就作了严格规定:只能用于体重低于35千克的猪。由于喹乙醇曾经的广泛使用和较大危害性,对其进行残留监控十分必要。喹乙醇本身不稳定,在动物体内能够在短时间内代谢,其在动物体内有十多种代谢产物,其中3-甲基喹噁啉-2-羧酸(MQCA)是主要代谢物,在体内相对稳定。因此,在检测饲料时,可检测喹乙醇原形物,但在检测食品及动物产品(肉、肝脏、水产品等)时应检测喹乙醇代谢产物。目前喹乙醇及其代谢产物的液相色谱及液相色谱-质谱检测标准主要有:1.饲料类GB/T8381.7-2009 饲料中喹乙醇的测定 高效液相色谱法DB43/T 891-2014 饲料中喹乙醇、氰乙基-(2-亚甲基肼喹噁啉基)-N,N-二氧化物(喹赛多)、卡巴氧的测定 液相色谱-串联质谱法(暂无文本)农业部2086号公告-5-2014 饲料中卡巴氧、乙酰甲喹、喹烯酮和喹乙醇的测定 液相色谱-串联质谱法2.食品及动物产品GB/T 20746-2006 牛、猪的肝脏和肌肉中卡巴氧和喹乙醇及代谢物残留量的测定 液相色谱-串联质谱法GB/T 20797-2006 肉与肉制品中喹乙醇残留量的测定GB/T 22984-2008 牛奶和奶粉中卡巴氧和喹乙醇代谢物残留量的测定 液相色谱-串联质谱法SC/T 3019-2004 水产品中喹乙醇残留量的测定 液相色谱法SN/T 0197-2014 出口动物源性食品中喹乙醇代谢物残留量的测定 液相色谱-质谱/质谱法(暂无文本)农业部1077号公告-5-2008 水产品中喹乙醇代谢物残留量的测定 高效液相色谱法从上述标准可以看出,大部分食品及动物产品标准检测喹乙醇代谢物(MQCA)。但少数标准如GB/T 20797-2006、SC/T 3019-2004在动物产品及水产品中检测喹乙醇原形物,存在瑕疵,显得不是非常严谨。
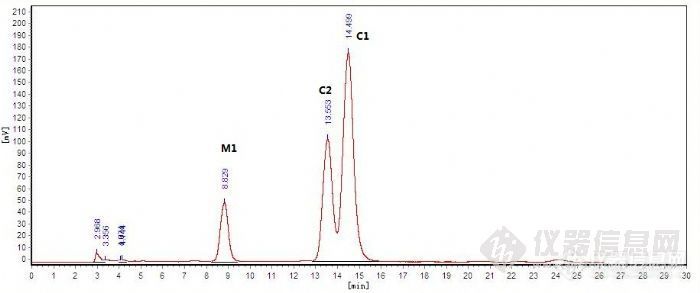
前言 代谢产物的鉴定在药物代谢研究过程中意义重大,如何准确地鉴定代谢产物的结构一直是广大药物代谢研究工作者致力攻克的难题。代谢产物的鉴定之所以难主要有以下几点原因:1.代谢产物在生物样品(血浆、尿液、胆汁、粪便等)中浓度极低。2.代谢产物容易受生物样品中内源性物质的干扰。3.代谢产物的不稳定性。4.仪器的灵敏度不够,等等。目前鉴定代谢产物的方式多为通过HPLC与质谱检测器进行联用推测代谢产物的结构,但该方法存在缺陷,如对同分异构体束手无策等。本实验前期通过专业的分离技术,得到某代谢产物M1,为重要的Ⅱ相代谢产物,该代谢产物因为量少(6mg)无法完全通过核磁鉴定,本文通过核磁给出的结构信息结合酶水解巧妙地鉴定了该代谢产物的结构,涉及保密,只给出有差别的部分结构信息。http://ng1.17img.cn/bbsfiles/images/2011/12/201112280311_341823_2160661_3.jpg1.试剂 色谱甲醇(Fisher),去离子水(Eyela Still Ace, SA-2100 E1, 日本),三氟乙酸(TFA,Dima),β葡萄糖苷酶(Sigma)。2.液相色谱条件 Shimadzu HPLC system, 由LC-10ATVP 泵, SPD-10AVP 紫外检测器, 以及CTO-10ASVP 柱温箱组成, 工作站为浙江大学N3000工作站。 色谱柱:Ultimate XB-C18柱(5μm, 4.6x250mm) 流动相:A通道:甲醇,B通道:水(0.05% TFA) 流 速:A通道0.500mL/min;B通道0.500mL/min 柱 温:30℃ 检测波长:275nm 进样量:20μL3.样品准备 对照品溶液的配置:取各纯品0.5mg,加入1mL50%甲醇水溶液,涡旋1mL,微孔滤膜过滤。水解过程:取代谢产物M1 0.5mg,溶于1mL水中,加入适量葡萄糖水解酶,37℃孵育2h,加入2mL的乙酸乙酯萃取,萃取2次,合并萃取液,45℃减压浓缩至干,用1mL50%甲醇水溶液溶解,进样分析。 4.结果与讨论http://ng1.17img.cn/bbsfiles/images/2011/12/201112280325_341830_2160661_3.jpg图1.代谢产物M1水解前的分析图谱(tR=8.951min)http://ng1.17img.cn/bbsfiles/images/2011/12/201112280315_341825_2160661_3.jpg图2.代谢产物M1水解后的分析图谱(tR=8.958min为剩余的未水解的M1,tR=14.720min为水解产物)http://ng1.17img.cn/bbsfiles/images/2011/12/201112280325_341831_2160661_3.jpg图3.已知化合物C1的分析图谱http://ng1.17img.cn/bbsfiles/images/2011/12/201112280325_341832_2160661_3.jpg图4.已知化合物C2的分析图谱http://ng1.17img.cn/bbsfiles/images/2011/12/201112280326_341833_2160661_3.jpg图5.水解产物与C1和C2合并进样分析图谱1.代谢产物M1只有6mg,理论上核磁是可以鉴定的,但基于一些原因,核磁谱图结果不理想,只能通过别的方法鉴定。但是从图1来看,代谢产物M1的纯度是很高的,如果用面积归一化法来计算的话,其含量至少在95%以上,但作者在此给大家透露点信息,代谢产物不同于植物中的化学成分,即使在色谱图上显示单一的色谱峰,但绝对纯度不一定很高,往往有未知的内源性成分如影子一样伴随着它,作者推测这可能是核磁图谱测试不理想的原因之一。2.机缘巧合的是,代谢产物M1两种水解产物均作为已知化合物被作者分离得到,并准确鉴定,因此剩余的实验就显得顺理成章。3.化合物C1和C2在结构上很相似,仅仅是葡萄糖醛酸基的位置不同,因此其表现在色谱行为上的差别也很小,如图5所示,二者没有达到基线分离。4.从各分析图谱可以看出,相同化合物的保留时间重现性非常高,且峰形之正太有目共睹,体现了Ultimate XB-C18柱的优越性能,保证了代谢产物结果鉴定的准确性。具体参数如:理论塔板数、分离度、对称因子等在此不一一列举。5.在整个分析过程中系统压力为19.4MPa左右,波动不超过0.2,换算为PSI也仅为2800左右,在流动相比例为50%的情况下,如此低的压力给测试者营造了“轻松的”实验氛围,避免了系统压力高产生的漏液报警的烦恼。6.一句话小结:本实验运用酶水解结合HPLC分析,成功鉴定了代谢产物M1的结构。
GCMS测植物叶片代谢产物(氨基酸、有机酸、糖))前,样品处理的标准化,应该怎么处理植物叶片,从采摘下后,越详细越好,非常感谢

前言 药物代谢(drug metabolism)是研究药物在生物体内的吸收、分布、生物转化和排泄等过程的特点和规律的一门科学,即药物分子被机体吸收后,在机体作用下发生的化学结构转化。也是药物研发产业链中的重要环节,贯穿药物研究过程的始终。排泄是药物代谢研究过程中的一个重要环节,本实验涉及的是某黄酮成分在大鼠体内排泄的研究。1.Chemical and reagents 甲醇(色谱纯,天津大茂),水(哇哈哈纯净水,杭州),三氟乙酸(TFA, Dikma, USA),其它试剂均为分析纯。2.animals Wista大鼠(220-250g,SPF级,由本校动物实验中心提供)3.HPLC analysis of two important metabolites Waters 高效液相色谱系统,由Waters Model 600 controller液相色谱,Millennium 32 工作站,Model Delta 600 泵,以及Waters 996 DAD检测器组成。 色谱柱:Ultimate XB-C18柱(5μm, 4.6x250mm) 流动相:A通道:甲醇,B通道:水(0.05%TFA) 梯度洗脱,具体流程未透露 流 速:1mL/min 柱 温:30℃ 检测波长:190-400nm扫描 进样量:20μL3.Sample preparation 大鼠灌胃给予该成分,剂量为30mg/200g,15min后用20%的乌拉坦溶液腹腔注射麻醉,行胆汁插管手术,缝合伤口,用规格为15mL的离心管收集12h内的胆汁,收集的胆汁过ODS,水洗脱,之后用甲醇洗脱,甲醇洗脱部分定溶到某体积,取一定体积过0.45μm微孔滤膜,HPLC分析,相同条件下与尿液中的代谢产物进行对照,确定该成分经大鼠灌胃后胆汁中排泄的代谢产物。4.Results and discussionhttp://ng1.17img.cn/bbsfiles/images/2011/10/201110042336_321120_2160661_3.jpgFig. 1. The HPLC chromatogram of blank bile.http://ng1.17img.cn/bbsfiles/images/2011/10/201110042337_321121_2160661_3.jpgFig. 2. The HPLC chromatogram of bile sample(12h).http://ng1.17img.cn/bbsfiles/images/2011/10/201110042338_321122_2160661_3.jpgFig. 3. The HPLC chromatogram of urine sample.讨论1. 首先要说明的是此部分实验是之前实验的续集,所以之前的实验请参考我以前发的体验贴,图3给出的是尿液中代谢产物的色谱图,从图中我们可以很明确地看到8个代谢产物的色谱峰,这8个色谱峰已经通过各种柱色谱手段分离得到,且结构已经用1D NMR和2D NMR以及MS等谱学手段进行了鉴定。讨论2. 图1和图2 分别为胆汁空白和样品色谱图,从该结果可知,有5种主要的代谢产物(M1 M2 M5 M6和M7)以及少量的M8经胆汁排泄,主要是通过保留时间,和紫外吸收进行了指认。讨论3. 此外我们还发现,尿液中大量存在的代谢产物M3不经胆汁排泄。讨论4. 通过对该成分在大鼠尿液中的代谢和胆汁排泄研究,我们可以得出这样的结果,尿液的内源性成分多为极性较大成分,多集中在保留时间靠前的范围,而胆汁中的内源性物质极性较小,如图2中50min左右的成分。讨论5.该实验尚未发表,因此代谢产物的结构不便透露,待发表之后,具体的结果会和广大息友进行交流。讨论6.最后也是最重要的,Ultimate XB C18柱对该类代谢产物表现了良好的保留能力和分离性能,代谢产物因为其结构中会结合亲水基团,如硫酸基,葡萄糖醛酸基等使其极性增加,易于从体内排出,因此这些成分往往表现了比较差的色谱行为,如强酸性导致的拖尾现象,因此需要在流动相中加入酸或者其它试剂进行调节,本实验流动相均为甲醇:水(含0.05%TFA),在此条件下,这些代谢产物在Ultimate XB C18柱上表现了良好的色谱行为。

前言 药物代谢(drug metabolism)是研究药物在生物体内的吸收、分布、生物转化和排泄等过程的特点和规律的一门科学,即药物分子被机体吸收后,在机体作用下发生的化学结构转化。也是药物研发产业链中的重要环节,贯穿药物研究过程的始终。本实验涉及黄酮类成分在大鼠体内代谢的研究,大鼠灌胃给予药物,累积24h尿液,尿液经处理,运用各种色谱手段,分离得到目标代谢产物。在此过程中有一关键的因素时刻威胁着我们,即代谢产物的降解,因此要设法保证代谢产物的稳定,如低温保存样品,调节尿液的酸碱性,等等。 本实验利用Ultimate XB-C18对两个重要的代谢产物在尿液中的稳定性进行简单的考察。1.Chemical and reagents 甲醇(色谱纯,天津大茂),水(哇哈哈纯净水,杭州),三氟乙酸(TFA, Dikma, USA),其它试剂均为分析纯。2.animals Wista大鼠(220-250g,SPF级,由本校动物实验中心提供)3.HPLC analysis of two important metabolites Waters 高效液相色谱系统,由Waters Model 600 controller液相色谱,Millennium 32 工作站,Model Delta 600 泵,以及Waters 996 DAD检测器组成。 色谱柱:Ultimate XB-C18柱(5μm, 4.6x250mm) 流动相:A通道:甲醇,B通道:水(0.05%TFA)=(20:80, v/v) 流 速:1mL/min 柱 温:35℃ 检测波长:190-400nm扫描 进样量:20μL3.Sample preparation 代谢产物M1和M2之前已制备分离得到,各取1mg,混合溶于2mL水中(M1和M2水溶性很强,也可溶于甲醇),取20μL进样分析;剩余部分置于250mL锥形瓶中,加入新鲜收集的大鼠尿液10mL,室温放置24h,之后该混合溶液,过ODS亲水柱,先用水洗脱,弃去,再用甲醇洗脱,收集甲醇洗脱溶液,45℃浓缩并定容至2mL。取20μL进样分析。4.Results and discussionhttp://ng1.17img.cn/bbsfiles/images/2011/07/201107010000_302457_2160661_3.jpg图1. M1与M2纯品混合色谱图http://ng1.17img.cn/bbsfiles/images/2011/06/201106302310_302433_2160661_3.jpg图2. M1与M2纯品混合色谱图(局部放大图10-20min)http://ng1.17img.cn/bbsfiles/images/2011/06/201106302310_302434_2160661_3.jpg图3. M1与M2在尿液中放置24h后色谱图http://ng1.17img.cn/bbsfiles/images/2011/06/201106302310_302435_2160661_3.jpg图4. M1与M2在尿液中放置24h后色谱图(局部放大图20-30min)5.conclusion 1. M1与M2在尿液中放置24h后发生了降解,在保留时间为25分钟左右,出现2个降解产物,其紫外吸收与M1和M2分别对应相似,M1紫外吸收(~271nm, ~310nm), M2紫外吸收(~273nm, ~343nm)。 2. 降解产物可能为M1与M2水解产物,因为M1与M2为极性较大的代谢产物,推测可能为葡萄糖醛酸或硫酸结合产物,其降解过程可能为水解脱掉葡萄糖醛酸基或硫酸基。 3. 这样的结果提示我们,在研究黄酮类成分的代谢过程中要注意样品的保存,在收集到尿液后要快速处理,或者在收集的过程中就进行预防,所采用的方法文献报道有加入乙醇或加酸调pH至5左右,可以防止该类代谢产物的降解。Acknowledgement感谢月旭公司提供Ultimate XB-C18柱。
今天,资娃将为大家带来日本总部实验室新近推出的数据——LC Café espresso之《CAPCELL CORE ADMES2.7对代谢产物的分析》。在这篇资料中,我们以对乙酰氨基酚的代谢产物作为样品,对资生堂的两款核壳型色谱柱CAPCELL CORE ADME S2.7和CAPCELLCORE C18 S2.7的溶出行为进行了比较。不论是酸性还是中性流动相条件下,CAPCELL CORE ADME S2.7色谱柱都能得到更强保留与更大分离度(这是CAPCELL CORE ADME S2.7色谱柱的特长)。通过对葡萄糖醛酸结合体的分析,对CAPCELL CORE ADME S2.7色谱柱在酸性流动相条件下具有的特征性溶出行为进行了阐述。在酸性流动相条件下,由于葡萄糖醛酸受到酸抑制,羧基的解离受到抑制,向分子态进行过渡,因此CAPCELL CORE ADME S2.7色谱柱的高表面极性的影响更强,对葡萄糖醛酸的保留也更强,因此得到了与CAPCELL CORE C18 S2.7相迥异的溶出模式(硫酸结合体和葡萄糖醛酸结合体的出峰位置发生了翻转)。而在中性流动相条件下,虽然CAPCELL CORE ADME S2.7色谱柱对葡萄糖醛酸结合体的保留同样有所增强(这是CAPCELL CORE ADME S2.7色谱柱的特长),但比在酸性流动相条件下对保留增强的程度较小,这让我们重新认识到解离平衡在色谱柱保留行为中的重要作用。在酸性⇔中性流动相条件下,CAPCELLCORE ADME S2.7色谱柱对于具有羧基的化合物会得到不同的分离模式。接下来对于硫酸结合体的溶出行为进行说明:在酸性和中性条件下,硫酸结合体的解离平衡没有较大差异,因此即使是在酸性条件下,也没有得到像葡萄糖醛酸结合体一样具有明显差异的保留行为,而只是显示出了从CAPCELL CORE C18 S2.7变更为CAPCELL CORE ADME S2.7时正常的保留增强。
? ?OPs通过消化道、皮肤及呼吸道等途径进入人体内后,可迅速分布于全身脏器并在肝内代谢,代谢方式主要为水解作用和氧化作用。大多OPs结构相似,进入体内后通常被代谢为6种二烷基磷酸盐(DAPs)中的一种或几种,包括磷酸二甲酯(DMP)、磷酸二乙酯(DEP)、二甲基硫代磷酸酯(DMTP)、二乙基硫代磷酸酯(DETP)、二甲基二硫代磷酸酯 (DMDTP)和二乙基二硫代磷酸酯(DEDTP),并在暴露后的6~24h内通过尿液排出。除上述DAPs外,OPs还会产生特殊代谢产物,特殊代谢产物通常对应一种或少数几种OPs,具有特异性。如马拉硫磷二羟基酸是马拉硫磷的特殊代谢产物,3,5,6-三氯-2-吡啶醇(3,5,6-TCP)是毒死蜱、甲基毒死蜱的特殊代谢产物等。
现在要分离极性很大的化合物,希望得到单体,是硫酸酯化的代谢产物,同分异构体,由于母药的极性比较大了,在柱子上的保留就不好。所以想知道代谢产物用什么样的制备柱分离好啊?谢谢。
需要检测II相代谢产物,质谱如何设置参数,做代谢产物的筛选。
3-氯-1,2-丙二醇(3-MCPD)为食品污染物,具有致癌性、肾脏毒性以及对男性生殖的不良作用。Lynch等进行了全面的综述,在酸水解植物蛋白调味液(HVP)、山羊乳、掺假西班牙烹饪等多种食物中均有检出,HVP、配制酱油污染尤其严重,因此近几年国际社会对氯丙醇的危害倍加关注,有关产生机理、来源、人群暴露、毒性作用成为研究的热点。3-MCPD膳食暴露估计值为为140~1100μg/人·天,均超过PMTDI值;目前尚无人群氯丙醇暴露的可靠资料,如能找到反应氯丙醇暴露的生物标志物,则能更好地评估人群氯丙醇暴露情况。Jones 等研究了3-MCPD的动物代谢情况,Lynch等认为3-MCPD在哺乳动物中部分转化为β-氯乳酸,进一步氧化为草酸,β-氯乳酸会引起大鼠睾丸、肾脏毒性,还会抑制呼吸作用和乳酸芽孢的代谢,从而抑制肾脏的代谢功能,引起肾脏持久性损伤,因此它对肾脏的毒性具有重要意义。大鼠尿中β-氯乳酸大约占摄入剂量的5%~25%,排泄时间在3~7天,有可能作为中、远期接触评价的指标之一,因此应首先建立生物材料中β-氯乳酸的检测方法。 β-氯乳酸在紫外、可见光区吸收弱,不能用HPLC常用的紫外或荧光检测器检测,一般是采用GC法分析;由于它带有羟基、羧基,极性大,沸点高,通常应将其衍生后再用GC检测。Jones等进行大剂量3-MCPD的药物代谢实验时,建立了β-氯乳酸的填充柱GC-FID方法,样品经过长时间的液-液萃取后用薄层层析进行分离、浓缩,甲酯化后用于GC分析,但检测限较高, 仅能测定尿液中高水平的量(mg/kg级),且样品量、溶剂使用量大,萃取时间长,不适于普通膳食暴露水平下的生物样品分析,因此需要建立生物样品中μg/kg级β-氯乳酸的测定方法并用来开展生物标志物的研究。
食品合成色素的代谢产物和代谢周期方面的研究的大侠们,有没有关于这方面的资料和检测方法。色素进入人体后是以原型排出还是以代谢产物排出体外?代谢产物有哪些?有什么检测方法?
早在2000年,TCC莱克多巴胺特异性专利单克隆抗体发明人Shelver(就职美国农业部)、Smith和Berry在农业食品化学(J. Agric. Food Chem.2000, 48.4020-4026)共同发表了文章《Production and Characterization of a Monoclonal Antibody against the β-Adrenergic Agonist Ractopamine》文中指出:1.莱克多巴胺葡萄糖苷酸是莱克多巴胺在不同物种体内的主要代谢物,而莱克多巴胺葡萄糖苷酸又分为莱克多巴胺葡萄糖苷酸A、莱克多巴胺葡萄糖苷酸B和莱克多巴胺葡萄糖苷酸C,其中:莱克多巴胺葡萄糖苷酸A由66%和33%(1S,3R)和(1R,3S) 莱克多巴胺组成;莱克多巴胺葡萄糖苷酸B由等量(1R,3R)和(1S,3S)两种莱克多巴胺异构体组成;莱克多巴胺葡萄糖苷酸C由27%(1R,3R)莱克多巴胺,19%(1S,3R)莱克多巴胺,28%(1S,3S) 莱克多巴胺,26%(1R,3S) 莱克多巴胺四种异构体混合组成2. TCC莱克多巴胺检测试剂盒的交叉反应率如下 TCC莱克多巴胺特异性专利单克隆抗体对三种主要莱克多巴胺代谢物: (1R,3R)-Ractopamine的交叉反应率为489% (1S,3R)-Ractopamine的交叉反应率为134% ractopamine glucuronide C的交叉反应率为384% 任何一种检测不出以上三种代谢产物的试剂盒会带来检测结果的假阴性! 大家如果需要这篇英文文献,可以发邮件给我 wyynjau@126.com 联系人 南京农水生物技术有限公司 吴园圆 13951613290 [em17]