【作者】 张晓云; 倪京满; 乔华; 孟庆刚; 王荷;【机构】 兰州大学药学院药剂教研室; 兰州大学第一医院药剂科; 兰州大学药学院药剂教研室 兰州730000; 兰州730000; 兰州730000;【摘要】 采用RP-HPLC法测定鬼臼毒素纳米脂质体的重要质控指标包封率。流动相:甲醇-水=60∶40;色谱柱:D ikm a公司的D iamonsil C18(150×4.6 mm,5μm);紫外检测波长:290 nm;流速:1 m l/m in。回收率为101.1%,RSD=1.94%(n=3)。本测定方法简便、快速,准确度高,可用于鬼臼毒素纳米脂质体的含量测定。 更多还原【关键词】 高效液相色谱; 鬼臼毒素; 纳米脂质体; 包封率;
眼部疾病的常用治疗方式是局部给以药物溶液(例如滴眼液),这些传统剂型占据市售制剂的90%左右。然而,眼部的生理屏障以及候选药物的低溶解性为眼部给药系统的发展带来许多难题。 最近,各种旨在提高难溶性药物生物利用度的眼部给药方式大量出现。中科院上海药物所甘勇课题组专题综述了这些眼部给药方式,包括水凝胶、聚合物胶束、纳米混悬液和脂质纳米载体等。同时,深入阐述了脂质纳米载体,包括乳液、脂质体、立方液晶、囊泡等,为眼部药物传递提供许多优势,比如提高难溶性药物的生物利用度、靶向给药、控制药物释放以及降低全身副作用等。(相关工作主要由甘莉、王静完成:Drug Discovery Today, in press.) 依据脂质体纳米粒作为眼用载体的独特优势,上海药物所甘勇课题组设计研究了一种新型双阳离子型核壳脂质体纳米粒(DLCS-NP)。采用薄膜分散水化-挤膜法,直接将旋干的脂质膜与分散的壳聚糖纳米粒(CS-NP)混悬液水化,自组装形成核壳结构的阴离子脂质体纳米粒(LCS-NP),随后利用阳离子N--N,N,N-三甲酰丙烷甲基硫酸盐与磷脂双分子层的亲和作用,在LCS-NP表面形成正电荷磷脂修饰层,形成DLCS-NP。该具有独特双阳离子型核壳脂质体纳米粒,能够显著延长载体角膜滞留时间,提高细胞摄取量,并具有一定的溶酶体逃逸能力,取得了理想的体内外眼表基因转染效果,为眼表疾病的基因治疗开辟了新途径。(相关工作主要由蒋敏、甘莉完成:Biomaterials, 2012, 33: 7621-7630.) 该项研究取得了上海市自然科学基金 (No.11ZR1444700)、国家自然科学基金资助项目(No.81102387)、国家科技重大专项“重大新药创制” (No.2009ZX09301-01) 和国家重点基础研究发展计划 (No.2009CB930300)的资助。 全文链接 1 2 http://www.cas.cn/ky/kyjz/201211/W020121127573032605614.jpgDLCS-NP的细胞摄取及摄取机制示意图
脂质体包覆的COX-2抑制剂纳米颗粒的靶向化疗脂质体确 (liposome) 是一种磷脂和胆固醇组成的双层膜球形囊泡. 脂质体可以用天然的磷脂和磷脂乙醇胺 (phosphatidylethanolamine, 源于鸡蛋) 或纯表面活性剂, 如 DOPE (dioleolylphosphatidylethanolamine) . 脂质体通常含有一个核心的水溶液 (但这并非脂质体定义). 不含有水溶性物质的脂质双膜体被称为胶束(miscell).脂质体 (Liposome) 是由两个希腊词'脂'和 '体' 的意思构成. 脂质体本身并不表明任何大小之特点, 因此不同于纳米体 (nanosome). 1961年英国剑桥大学巴巴拉汉姆学院血液学家Bangham先生首次描述脂质体. Bangham先生与其同事Horne为了测试研究所新到的电子显微镜, 加负染色剂(三氯醋酸,TCA)于干磷脂中, 随后他们观察到一种类脂双层结构, 酷似质膜, 这就是首次显微镜照片展示的细胞膜实质性证据. 由于其独特的性能脂质体可用于药物载体, 这是由于亲水溶解溶质不能轻易通过脂质双膜, 而疏水性化学物质,可以溶解到脂质体膜内, 所以脂质体既可携带疏水性分子, 也可亲水性分子. 脂质体双层可以与其他细胞膜双层融合, 从而传递携带内含物. 用脂质体来投递DNA (lipofection) 比 单独用DNA感染细胞要有效的多. 低(或高) pH脂质体中的水溶解药物都带有电荷 (即pH值是药物的等电点范围以外) . 随着pH值自然抵销 (质子能通过膜), 因药物能自由穿过细胞膜, 中和后的脂质体药物也会自由扩散, . 这一投递是借脂质体双层膜与细胞接触来扩散脂质体药物, 而不是直接的融合. 所以这种脂质体药物的生产与使用受到时间上的限制.另一种脂质体药物投递的方式是借巨吞噬细胞作用. 一定大小范围内的脂质体可被人体中巨噬细胞吞噬. 脂质体药物在脂质体被巨噬细胞的胞溶体溶解后释放出来.加上陪体 的脂质体更易激活这种内吞噬作用.另一脂质体的好处是它的癌细胞靶向能力, 所有健康人的血管内皮都是由内皮细胞所包裹, 严密阻止任何大颗粒从血液中漏出. 但肿瘤血管则不具有相同水平的密封效果,通常小于400nm的脂质体可可迅速从患者的血液进入肿瘤. 抗癌药物如阿霉素(Doxorubicin, Doxil) 和柔红霉素 (Daunorubicin, Daunoxome ) 就是利用脂质体给药系统. 脂质体可用磷脂水经超声波而制成. 低剪切率超声波制成像洋葱多层状脂质体, 如持续用高剪切超声波则倾向于形成较小的单层脂质体 (unilamellar). 超声波法被普遍认为是"毛, 粗"的制备方法, 较新的方法, 如挤出法(extrusion)制成的脂质体药物可供人类使用.当前研究已经能够使脂质体能躲避人体的免疫系统, 成为"隐形脂质体", 即脂质体外挂上惰性聚乙二醇( PEG ), PEG脂质体延长循环中的药物运送. 但是 目前的困难是PEG涂的厚度. 太厚则阻止脂质体与细胞的接合. 为了特异性接合脂质体可挂上单克隆抗体, 或特异性抗原. 这样脂质体药物只送到病变组织.
脂质体被用作病毒体的人工模型,能够对关键的膜结合药物目标进行系统梳理。隆德大学(瑞典)质子通道研究小组的副教授Sindra Peterson Årsköld博士及其同事的工作重点从事病毒蛋白质和抗病毒剂的脂质体研究。Peterson Årsköld博士表示,如果没有马尔文Zetasizer Nano ZS纳米颗粒分析系统快速、可靠而且高资源利用率的测定性能,在各种样品条件下精确的例行样品质量控制就不可能实现。作为一名蛋白质科学家,Peterson Årsköld博士解释了样品分析成本为何对其工作如此至关重要的原因:“水中超声降解磷脂产生的脂质体被用于获取极其详细的定量生物物理数据。因此极其重要的是,每批脂质体需要在窄分布粒径和单层方面具有相同的高品质,而且其形态也需要能够复制并始终如一。在脂质体生产方法的开发以及对脂质体进行优化以获得新型蛋白质体系的过程中,对这些参数的监测也很关键。举例来说,一些条件会形成多层脂质体,像洋葱一样有许多薄层。这意味着,我们每次生产一种新样品时,我们都必须进行质量检查以确保过程的一致性。”“虽然电子显微镜检查(EM)能为我们提供更加详细的数据,但获得图像要花一整天。因此使用EM进行常规样品检测的成本很高。Zetasizer Nano ZS应用动态光散射原理(DLS),既没有破坏性也很快速。"它能够在几分钟内对我们的样品进行检测,” Peterson Årsköld博士说。“实际上,这是一种有用而且易于使用的系统,自从我购入该仪器以来,我们系的蛋白质化学家们每天都使用它,而且现在再也不愿意在没有它的情况下工作了!”作为隆德大学生物化学及结构生物系的一部分,Peterson Årsköld博士 以及质子通道研究小组一直在研究甲型流感病毒产生的M2蛋白质,一种小型单跨横跨膜(TM)蛋白质的性状。Peterson Årsköld博士共同署名,发布在国家科学院会议论文集(PNAS)上的论文指出使多个质子能够侵入甲型流感病毒,引发宿主细胞感染,而不形成较大电位的神秘过程。结果证明M2蛋白质与pH值非常复杂、功能调谐关系,能够为成功的抗病毒药物的开发提供更好的机会。
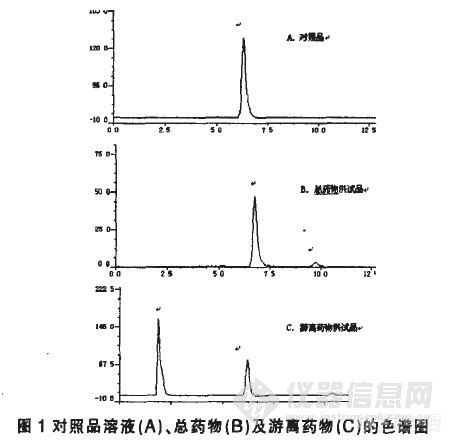
作者:李文秀;邓英杰;魏伟;高晓非;曹金娜(沈阳药科大学药学院 沈阳药科大学药学院 沈阳药科大学药学院 沈阳药科大学药学院 沈阳药科大学药学院)摘要:目的:建立灯盏花素前体脂质体胶囊的突释考察方法。方法:采用透析-高效液相色谱法(HPLC),水化前体脂质体后,用透析袋分析游离药物和脂质体,并用HPLC法测定含量。采用Diamonsil ODS C18色谱柱(4.6mm×250mm,5μm),流动相为甲醇-乙腈-40mmol/L KH2PO4(磷酸调pH至2.5)(18∶12∶70);检测波长335nm;流速1.0ml/min;柱温35℃。结果:游离药物在透析膜两侧均匀分布,而脂质体被截留于透析袋中。含量测定方法平均加样回收率为103.32%,RSD为1.12%(n=9)。结论:本法操作简便、准确,可用于灯盏花素前体脂质体胶囊突释的评价。谱图:http://ng1.17img.cn/bbsfiles/images/2012/08/201208211652_385078_1609970_3.jpg

作者:http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif宋笑丹 http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif刘红梅 http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif魏华 http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif董迪 http://vpn.library.shmtu.edu.cn:2308/Images/head_pic.gif吴琳华 Author:SONG Xiao-dan LIU Hong-mei WEI Hua DONG Di WU Lin-hua 作者单位:哈尔滨医科大学附属第二医院药学部,黑龙江省高校重点实验室,哈尔滨,摘要: 目的 考察β-榄香烯脂质体在大鼠体内的组织分布.方法 建立了大鼠体内β-榄香烯测定的HPLC.色谱条件为:Diamonsil C18色谱柱(4.6 mm×250 mm,5μm);流动相为甲醇-乙腈-水(40:57:3);检测波长:210 nm;柱温:30℃.并测定大鼠尾静脉注射β-榄香烯脂质体和榄香烯注射液后血浆及组织中的药物浓度.结果 此色谱条件下血浆与组织的标准曲线、精密度等实验结果表明,该方法适于分析生物样品中β-榄香烯含量.与榄香烯注射液相比,β-榄香烯脂质体在大鼠体内的分布特性有不同程度的改变,其中β-榄香烯脂质体在肝、脾、肾组织中分布相对较多.结论 β-榄香烯脂质体及榄香烯注射液在大鼠的心、脾、肾组织中分布具有显著性差异http://ng1.17img.cn/bbsfiles/images/2012/08/201208271803_386611_2379123_3.jpg
目前我们采用过柱子的方法纯化脂质体,效率不高,并且纯化产物纯度不高,想咨询一下是否可以采用制备[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]来对产物进行纯化。
请问有没有人测量脂质体的膜厚啊? 我想测量脂质体的膜厚,不知道有没有人测量过这个?我想测几个样品,有没有人知道哪里有这方面的经验?
【序号】:1【作者】:[url=http://yuanjian.cnki.com.cn/Search/Result?author=%E5%BC%A0%E5%B0%8F%E6%B4%AA]张小洪[/url] 【题名】:[b]脂质体、分散体和肠溶包衣替米考星体外释放和抑菌研究[/b]【期刊】:重庆大学硕士论文【年、卷、期、起止页码】: [color=#333333]2014[/color]【全文链接】:http://cdmd.cnki.com.cn/Article/CDMD-10611-1014043590.htm
有个问题,脂质体的不溶性微粒检测,是跟药典里面关于脂质体的不溶性微粒检测方法一样么?有没有什么文件可以看啊,哪位大神知道,求指导
如题,想问下,多相脂质体需要分析什么参数?今天被人问到,手边没有药典,不知论坛有没有做,帮忙看看药典有没有这个规定啊。看看附录里面。
测脂质体内相pH用什么仪器呢
要了解脂质体毛细管电泳(LCE),首先得给大家解释一个概念:生物膜(Biomembrane)。生物膜是指组成生物体细胞各个“构件”的膜,细胞内的细胞膜、核膜以及内质网、高尔基体、线粒体等细胞器,就是这台“机器”中一些功能相关的“部件”,它们都由膜构成,这些膜的化学组成相似,基本结构大致相同,统称为生物膜。生物膜色谱(Biomembrane Chromatography)是一种新型液相色谱模式,它以天然或人工模拟生物膜为固定相,主要用来研究溶质分子与生物膜间的相互作用。目前,最常用的生物膜色谱固定相是固定化脂质体,因为它能更好的模拟生物膜的脂双层结构,并具备生物膜的流动性特征。这种人工模拟的生物膜体系不仅可以精确地模拟生物膜的化学环境,而且其物理性能也可以通过调节温度,pH、离子强度等得到有效控制。LCE就是利用脂质体作为假固定相的毛细管电泳,主要用于分离蛋白质、手性分子及模拟药物-生物膜相互作用的新型毛细管电泳。与生物膜色谱相比,LCE方法简单,可操作性强,成本低廉,尤其是测定药物的Klw 准确、重现性好,具有更好的发展前景。目前,LCE 无论在理论还是技术方面都还不太成熟,应用范围也较为有限,因而其发展空间还很广阔。
如何用浊度法检测脂质体的稳定性。其中应用紫外可见分光光度计。浊度与吸光度之间有什么关系?
纳米中草药是指运用纳米技术制造的、粒径小于100nm的中药有效成分、有效部位、原药及其复方制剂,具有增加药物对血脑屏障或生物膜的穿透性等特点。纳米中草药技术(nanotechnology)是指在纳米尺度下对物质进行制备、研究和工业化,以及利用纳米尺度物质进行交叉研究和工业化的一门综合性的技术体系。纳米技术作为高新技术,可广泛应用于材料学、电子学、生物学、医药学、显微学等多个领域,并起着重要的作用。 一、纳米中草药的特点 1、原药纳米化后呈现新的药效或增强原有疗效中药被制成粒径0.1~100 nm大小,其物理、化学、生物学特性可能发生深刻的变化,使活性增强和产生新的药效。如灵芝通过纳米级处理,可将孢子破壁,并采用超临界流体萃取技术萃取出灵芝孢子的脂质活性物质,从而增强抗肿瘤的功效。 2、改善难溶性药物的口服吸收。在表面活性剂、水等存在下,直接将药物粉碎成纳米混悬剂,增加了药物溶解度,适于口服、注射等途径给药,以提高生物利用度。 3、增加药物对血脑屏障或生物膜的穿透性。纳米粒能够穿透大粒子难以进入的器官组织、血脑屏障及生物膜。如阿霉素α聚氰基丙烯酸正丁酯纳米粒(NADM)可以改变阿霉素的体内分布特征,对肝、脾表现出明显的靶向性,而血、心、肺、肾中的药物分布则减少。 4、靶向作用。在研究中发现,一味普通的中药牛黄,加工到纳米级水平后,其理化性质和疗效会发生惊人的变化,甚至可以治疗某些疑难杂症,并具有极强的靶向作用。 5、使药物达到缓释、控释。借助高分子纳米粒作载体等技术手段,可实现药物的缓释、控释。如雷公藤乙酸乙酯提取物固体纳米脂质粒有良好的缓释、控释功能。二、纳米中草药的制备技术及其进展 纳米中药的制备是研究纳米中药最基础的,也是最重要的问题。将纳米技术引入中药的研究,必须考虑中药组方的多样性、成分的复杂性,例如中药单味药可分为矿物质、植类药、动物药和菌物药等,中药的有效部位和有效成分又包括无机化合物和有机化合物、水溶性成分和脂溶性成分等,因此,针对不同的药物,在进行纳米化时必须采用不同的技术路线。此外,还必需考虑中药的剂型。纳米中药与中药新制剂关系十分密切,如何在中医理论的指导下进行纳米中药新制剂的研究,将中药制成高效、速效、长效、剂量小、低毒、服用方便的现代化制剂,也是进行中药纳米化所必须考虑的问题。纳米中药是针对中药的有效成分或有效部位进行纳米技术加工处理,开发中药的新功效。聚合物纳米粒可作为药物纳米粒子和药物纳米载体。药物纳米载体系指溶解或分散有药物的各种纳米粒,药物纳米载体包括纳米脂质体、固体脂质纳米粒以及纳米囊和纳米球。而对于不同类型的纳米中药,有不同的制备方法。三、纳米中草药的加工方法。 1、纳米超微化技术是改进某些药物的难溶性或保护某些药物的特殊活性,适用于不宜工业化提取的某些中药。如矿物药、贵重药、有毒中药、有效成分易受湿热破坏的药物、有效成分不明的药物。目前比较常用的是超微粉碎技术。所谓超微粉碎是指利用机械或流体动力的途径将物质颗粒粉碎至粒径小于10 μm的过程。根据破坏物质分子间内聚力的方式不同,目前的超微粉碎设备可分为机械粉碎机、气流粉碎机、超声波粉碎机。 2、机械粉碎法是利用机械力的作用来实现粉碎目的。边可君等采用自主开发的温度可控(-30~-50℃)的惰性气氛高能球磨装置系统制备纳米石决明。将石决明置于配有深冷外套的惰性气氛球磨罐中,同时装入磨球,磨球与石决明粉比保持在15:1~5:1范围,控制高能球磨机的转速(200~400 r/min)和时间(2~60 h),获得了平均粒度不大于100 nm的石决明粉末。 3、气流粉碎法是以压缩空气或过热蒸汽通过喷嘴产生的超音速高湍流气流作用为颗粒的载体。颗粒与颗粒之间或颗粒与固定板之间发生冲击性挤压、摩擦和剪切等作用,从而达到粉碎的目的。与普通机械冲击式超微粉碎机相比,气流粉碎产品粉碎更细,粒度分布范围更窄。同时气体在喷嘴处膨胀降温,粉碎过程中不会产生很大的热量。所以粉碎温升很低。这一特性对于低融点和热敏性物料的超微粉碎特别重要。 备注: 纳米中草药的常用方法较为普遍的有两种:一是喷雾干燥法,二是高能球磨法。 中药纳米超微化技术既丰富了传统的炮制方法,又能为中药的生产和应用带来新的活力。纳米产品目前已成为中药行业新的经济增长点。将这项技术应用于中药行业可以开发具有更好疗效、更优品种的纳米中药新产品。这将对中药行业的发展带来深远的理论和现实。
称量固体标准品配制标准曲线溶液,使用注射液脂质体来配制质控样品,怎么比较都是标准曲线高于质控,已经做过溶液准确度考察。两个处理方式不同只在于标准曲线是直接用溶液,后面再加基质,而质控是直接配制在基质中。已经做过脂质体破碎的考察,增加涡旋时间或者增加有机试剂都没有变化。前处理方式也比较过,没有变化。现在不知道原因出在哪了?
刚接触这个检测项目,用的马尔文的仪器,请问大家符合药典规定的粒径和zeta电位检测标准粒子用什么,大家购买的什么品牌的,标准粒径和电位是多少?做mRNA纳米脂质颗粒zeta电位检测大家用什么稀释剂,因为没有测物理常数的仪器,所以用不了较优的产品背景溶液,有什么别的稀释剂可以代替,使检测结果与真实值偏差较小。
[size=16px][color=#ff0000][b][url=https://www.instrument.com.cn/job/position-80721.html]立即投递该职位[/url][/b][/color][/size][b]职位名称:[/b]生物应用工程师[b]职位描述/要求:[/b]职位描述:?负责脂质体纳米颗粒合成仪研发阶段产品验证评价;?参与纳米脂质颗粒合成仪开发,能够从实际应用角度提出产品设计方向;?负责与用户做产品应用技术交流,结合产品特点为用户提供纳米脂质颗粒制剂开发技术支持;?负责撰写关于纳米脂质颗粒应用类文章,辅助产品推广;任职要求:? 博士课题研究方向为脂质体颗粒,包括但不仅限于LNP和LPP? 具有较强的药学基础和丰富的液体制剂、新型制剂研发经验;? 熟悉国内外新药研发的要求与法规。能够在有限的时间内高效的查询、把握具有前沿性的,与产品开发过程相关的大量英文文献;? 对工业药剂学、生物药剂学、新技术、新辅料、新设备和分析工作均有很好的了解。? 有脂质体纳米颗粒小试、中试、产业化经验优先。? 博士,药剂学或药学相关专业[b]公司介绍:[/b] 欧世盛(北京)科技有限公司,成立于2015年。是一家独特的技术型企业,我们致力于分析仪器核心器件开发及生产,为优秀厂家提供细致服务。我们在不断推出高品质产品的同时,强化服务队务建设,针对您的设备零部件需求,我们会用最专业的视角和最快的响应速度为您提出最佳解决方案。 公司现有产品包括微型柱塞泵、分析型高压恒流泵、[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱[/color][/url]泵、半制备高压恒流泵、制备高压恒流泵、工业级制备泵等系列产品。...[url=https://www.instrument.com.cn/job/position-80721.html]查看全部[/url][align=center][img=,178,176]https://ng1.17img.cn/bbsfiles/images/2021/08/202108160948175602_3528_5026484_3.png!w178x176.jpg[/img][/align][align=center]扫描二维码,关注[b][color=#ff0000]“仪职派”[/color][/b]公众号[/align][align=center][b]即可获取高薪职位[/b][/align]
【篇 号】:1【题 名】:制备方法对甲氧沙林脂质体体外性质的影响研究【作 者】:何文; 夏晶;【期刊名全称】:广东药学院学报, Journal of Guangdong College of Pharmacy, 编辑部邮箱 【文献页码】: 2005年 06期 【全文链接】:http://dlib.cnki.net/kns50/detail.aspx?dbname=CJFD2005&filename=GDYX200506005【篇 号】:2【题 名】:高压均质技术在纳米制剂制备中的应用【作 者】:艾秀娟; 陈建海; 平渊; 周红玲; 李平;【期刊名全称】:医药导报, Herald of Medicine, 编辑部邮箱 【文献页码】:2007年 09期【全文链接】:http://dlib.cnki.net/kns50/detail.aspx?dbname=CJFD2007&filename=YYDB200709041【篇 号】:3【题 名】:β-榄香烯脂质体的制备工艺研究及生产设备开发【作 者】:李庆武;【期刊名全称】: 中国优秀硕士学位论文全文数据库【文献页码】: 2007-05-29【全文链接】:http://dlib.cnki.net/kns50/detail.aspx?dbname=CMFD2007&filename=2007060601.nh【篇 号】:4【题 名】:羧甲基壳聚糖包衣尼莫地平纳米脂质体的制备及其在小鼠体内的组织分布【作 者】:罗勤辉; 何文; 孙安琪;【期刊名全称】:中国医院药学杂志, Chinese Journal of Hospital Pharmacy, 编辑部邮箱 【文献页码】:2010年 18期 【全文链接】:http://dlib.cnki.net/kns50/detail.aspx?dbname=CJFD2010&filename=ZGYZ201018015【篇 号】:5【题 名】:槲皮素纳米脂质体的处方工艺优化【作 者】:丁燕飞; 姚瑶; 陶昱斐; 冯秀珍;【期刊名全称】:中草药, Chinese Traditional and Herbal Drugs, 编辑部邮箱 【文献页码】: 2008年 04期【全文链接】:http://dlib.cnki.net/kns50/detail.aspx?dbname=CJFD2008&filename=ZCYO200804018
催化活性是目前商业铂纳米催化剂的4倍科技日报2007年5月10日讯:厦门大学化学化工学院孙世刚和美国佐治亚理工学院王中林等科学家采用新的电化学方法,首次制备出具有高表面能的二十四面体铂纳米晶粒催化剂,显著提高了铂纳米催化剂的活性和稳定性,在能源、催化、材料、化工等领域具有重大意义和应用价值。5月4日出版的美国《科学》杂志以长篇报道刊登了这项最新成果。 二十四面体是一种十分罕见的晶体形状,在自然界中,仅金刚石、萤石和铜矿等极少数矿物能以不完美的二十四面体形式存在。 上述研究发展了一种新的电化学方法,能够控制纳米晶体的表面结构和生长,合成具有高表面能的金属纳米晶体。 中美团队的电催化研究证实,所制备的二十四面体铂纳米晶体对甲酸、乙醇等有机小分子燃料电氧化的催化活性是目前商业铂纳米催化剂的2到4倍,在燃料电池、电催化等领域中具有重大应用价值。 孙世刚和王中林认为该研究的重大意义在于:所发展的表面结构控制生长的电化学方法可以拓展到其他铂族金属,如钯、铑等,也可以运用到制备其他高指数晶面组成的不同形状的金属纳米晶体。这将丰富纳米晶体表面结构控制生长的内涵,深化对金属晶体生长规律的认识,不仅开辟了一条通过控制纳米粒子表面原子排列结构提高催化剂性能的崭新途径,也将模型电催化剂的基础研究推进到实际催化剂设计和研制过程中的一个重大进展。 《科学》杂志的3位评审人认为,这一科研成果不仅指明了一种控制纳米粒子生长使高指数晶面暴露在外的新思路和新方法,而且将导致异相催化中的新发现。
【篇 号】:1【题 名】:羧甲基壳聚糖包衣尼莫地平纳米脂质体的制备及体外释药研究【作 者】:何文; 孙安琪;;【期刊名全称】:中国医院药学杂志, Chinese Journal of Hospital Pharmacy, 编辑部邮箱 【文献页码】: 2008年 17期 【全文链接】:http://dlib.cnki.net/kns50/detail.aspx?dbname=CJFD2008&filename=ZGYZ200817011【篇 号】:2【题 名】:紫杉醇冻干脂质体的制备及含量稳定性【作 者】:王浩; 邓英杰;;【期刊名全称】:沈阳药科大学学报, Journal of Shenyang Pharmaceutical University, 编辑部邮箱 【文献页码】:2008年 08期【全文链接】:http://dlib.cnki.net/kns50/detail.aspx?dbname=CJFD2008&filename=SYYD200808005【篇 号】:3【题 名】:乳脂肪球膜磷脂-免疫球蛋白G脂质体的制备【作 者】:李博群; 梁冰; 刘宁;;【期刊名全称】: 中国农业科技导报, Journal of Agricultural Science and Technology, 编辑部邮箱 【文献页码】: 2009年 03期【全文链接】:http://dlib.cnki.net/kns50/detail.aspx?dbname=CJFD2009&filename=NKDB200903014
最新发布的2013年1月国际学术期刊《控释杂志》(Journal of Controlled Release)发表了中国科学院深圳先进技术研究院生物医学与健康工程研究所生物医学超声研究组的最新成果:载紫杉醇的纳米脂质体-微泡复合物作为超声促发的药物载体及其抗肿瘤作用的研究。(在线发表于2013年1月7日) 超声不仅仅是一种重要的医学成像诊断工具,其机械波及辐射力特性也赋予其在声操控、给药及治疗领域的重要应用潜力。近年来,载药超声微泡的出现,使得微泡在作为超声造影剂用于疾病诊断的同时,也可作为药物载体用于疾病的治疗。一方面,载药超声微泡在受到低频超声辐照时,微泡会发生爆破从而释放其中携载的药物;另一方面,超声微泡在较低声压作用下产生的空化或声孔效应,可使临近细胞产生瞬间可修复的细胞膜空隙,从而大大增加药物的细胞摄取和生物利用度。迄今,超声靶向微泡爆破介导药物或基因的靶向传递已经成为一种新型的给药方法,是目前药物传递系统研究的热点课题。然而,现行应用的单层微泡脂质壳层的载药能力有限,往往难于达到疾病治疗的有效剂量。 针对这一问题,严飞等将紫杉醇药物包裹于具有高载药量的脂质体中,进而偶联到超声微泡的表面,获得了具有高载药量和具有超声爆破释放性能的载药脂质体-微泡复合物,从而巧妙地解决了这一问题。经过1年多的实验研究,研究人员对这一新型的声敏载药脂质体-微泡复合物进行了详细的表征,发现这种新型的脂质体-微泡复合物能够大大增加药物的载药量和包封率,并对其体外药物释放特性进行了测定、在优化的超声参数条件下可以显著增加肿瘤细胞对药物的摄取,在体外细胞以及体内动物实验证实了该载药脂质体-微泡复合物联合超声可以显著提高紫杉醇药物的抗肿瘤效果并增加药物在肿瘤部位的浓度,免疫组织化学进一步分析发现其抗肿瘤作用的机制主要是通过增加肿瘤组织的细胞凋亡和抑制肿瘤新生血管生成来实现的。 本研究进一步证实了载药脂质体-微泡复合物在体内的抗肿瘤疗效并揭示了其抗肿瘤效应的作用机制,为超声敏锐成像诊断/给药/治疗一体化应用研究奠定了基础。 http://www.cas.cn/ky/kyjz/201301/W020130124649211439309.jpg
纳米技术改善难溶性药物吸收前景光明 近日,由中国药学会和美国药学科学家协会主办、沈阳药科大学和辽宁省药学会承办的“第二届亚洲阿登制药技术研讨会暨中国药学会药剂专业委员会2010年学术年会”在沈阳召开,会议主题为“难溶药物的剂型策略”。在为期3天的研讨中,与会专家表示,改善难溶性药物的溶解度,促进药物的吸收,提高药物的生物利用度是药剂学领域亟待攻克的难题,而纳米技术这一助推器有助于加速该难题的解决,我国学者应加强相关研究。 溶解度成为制约瓶颈 药物的溶解性是影响药物生物利用度的重要因素之一,难溶性药物因在水中的溶解度小,难以被机体吸收,导致生物利用度较差。随着组合化学、基因技术、高通量筛选技术等在药物研发中的广泛应用,大量具有活性的候选药物被发现。但是,沈阳药科大学崔福德教授表示,由于存在水溶性差的缺陷,四成左右的侯选药物不能上市而限制了其在临床充分发挥疗效。据估计,全球每年约有650亿美元的药品因生物利用度差而造成治疗费用与疗效比例的严重失调。而实际上,许多难溶性药物有着很强的生物活性,在治疗肿瘤、心血管疾病等领域有着良好疗效。因此,如何提高药物的溶解度和吸收率,成为药剂学研究的热点与难点,迫切需要发展新的制剂技术和剂型来解决这一问题。 崔福德介绍,当前,在药剂学研究中提高难溶性药物的溶解度和溶解速率有多种方法,如加入助溶剂、增溶剂和亲水性介质(适用于液体制剂);制成固体分散体和包含物(适用于固体制剂);制成微粒分散系统(适用于液体和固体制剂);还可以采取减少粒径的措施,比如做成药物的纳米结晶(适用于各种剂型)。 “但是这些方法都有一定的局限性。”中国药学会药剂专业委员会主任委员、北京大学药学院张强教授具体分析说,比如成盐类的方法就只适用于一些难溶性弱酸或弱碱类药物,而不适用于所有分子结构的药物;加入助溶剂和亲水性物质的方法,可供选择的溶剂等也是有限的;增溶剂主要是表面活性剂,毒性问题也限制了其使用;包合物同样存在可供选择的品种较少和毒性问题;固体分散体也有老化现象和需要使用大量赋型剂的缺陷;而费用较高和稳定性问题又限制了微粒化方法的使用。 新技术助力难题解决 解决上述问题,纳米技术的应用优势日益显现:纳米化使药物的粒度大大减小,表面积大大增加,水溶性差的药物在纳米载体中可形成较高的局部浓度;药物的黏附性增强,在吸收部位的滞留时间延长;纳米载药系统可以提高药物的透膜能力和稳定性,也有利于提高药物的生物利用度,特别是对于生物药剂学分类体系(BCS)Ⅱ类(低溶解度、高通透性)和Ⅳ类(低溶解度、低通透性)的药物,这一技术越来越受到国内外一些研究机构、制药公司的青睐。 在药剂学领域,一般将制剂中纳米粒子的尺寸界定在1~1000纳米范围,主要包括纳米载体与纳米药物两个方面。纳米载体是指溶解或分散有药物的各种纳米粒,如纳米乳、聚合物纳米粒(纳米囊或纳米球)、脂质纳米粒等;纳米药物则是指直接将原料药物加工成的纳米粒,实质上是微粉化技术、超细粉技术的发展。 张强介绍,纳米乳/微乳是一种由水、油、表面活性剂和一些复合表面活性剂自组装成的粒径小于100纳米的半透明溶液,其易于制备、相对稳定,而且可使大多数水不溶性药物的生物利用度提高显著。自1943年被报道以来,纳米乳/微乳已经得到了广泛的研究,但上市的产品却不多,1995年诺华公司上市了环孢素A的微乳产品,在临床迅速得以推广。现在上市的同类品种还有雷帕霉素自微乳化给药系统。 纳米粒(纳米球或纳米囊)一般是指由天然或合成的高分子材料制成的、粒径在纳米级的固态胶体微粒,可用于包裹亲水性药物,也可包裹疏水性药物,具有在胃肠道中稳定、药物不易被破坏,以及能够调整药物的理化性质、释放和生物学行为等优点。自1976年Birrenbach等人首先提出了纳米粒和纳米囊的概念后,目前以合成高分子材料为聚合物的纳米粒研究得最为广泛。但张强遗憾地表示:“30多年来,这个研究领域没有取得实质性的突破,无论是口服制剂还是注射制剂都没有产品上市。”而天然聚合物的纳米粒所使用的材料包括壳多糖、白蛋白、右旋糖苷、明胶等,其中以口服壳聚糖纳米粒的研究最为广泛。值得一提的是,白蛋白结合紫杉醇纳米粒注射混悬液2005年上市,成为制剂领域的一个重大突破;但口服给药方面仍没有产品面市。 脂质纳米粒是以生物相容性良好的脂质材料为载体,将药物溶解、包裹于脂质核或是吸附于纳米粒表面的新型载药系统。第一代脂质纳米粒是固体脂质纳米粒(SLN),其性质稳定、制备较简便,具有一定的缓释作用,主要适合于难溶性药物的包裹;随后又发展了第二代纳米结构脂质载体(NCL),解决了第一代脂质纳米粒载药量不佳的问题,稳定性也更好。张强谈到,近年来,对脂质纳米粒的研究也相当广泛,特别是第二代脂质纳米粒自1999年开始研究以来,在外用领域如化妆品领域进展很快,开发程度好于脂质体,但至今还没有用于临床的产品。 在表面活性剂和水等附加剂存在下直接将药物粉碎加工成纳米微粒,可以提高药物的吸收或靶向性,特别适合于大剂量的难溶性药物的口服吸收和注射给药,能增加溶出度,提高生物利用度,增加稳定性。此外,它无需载体材料,只有少量的表面活性剂,安全性更高。此类技术分为纳米混悬剂和纳米结晶制备技术。其中,纳米结晶制备技术发展较快,目前已有5种产品利用这种技术生产并在美国上市,包括惠氏公司的Rapamune(西罗莫司)、默克公司的Emend(阿瑞吡坦)、雅培公司的Tricor(非诺贝特)以及Par公司的Megace ES(甲地孕酮)等。
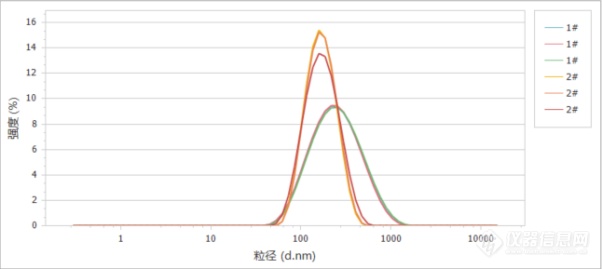
[align=center][font='arial'][size=21px][color=#548dd4]#[/color][/size][/font][font='arial'][size=21px][color=#548dd4]每日一篇分享一篇解决方案:[/color][/size][/font][/align][align=center][font='arial'][size=21px][color=#548dd4]今日行业领域:[/color][/size][/font][font='arial'][size=21px][color=#548dd4]制药[/color][/size][/font][/align][align=center][font='等线 light'][size=13px][color=#548dd4]BeNano[/color][/size][/font][font='等线 light'][size=13px][color=#548dd4] 180 [/color][/size][/font][font='等线 light'][size=13px][color=#548dd4]检测脂质纳米粒[/color][/size][/font][font='等线 light'][size=13px][color=#548dd4]LNP[/color][/size][/font][font='等线 light'][size=13px][color=#548dd4]的粒径[/color][/size][/font][/align][align=center]关键词:粒径、LNP、药物输送体系[/align]脂质纳米粒(Lipid Nanoparticles,LNP)是使用脂质形成纳米微粒的一种,作为一种高效、安全的药物递送体系,被广泛研究和应用,成为近年来发展最为迅速的制剂剂型之一,由于其制备过程需要进行特殊的工艺化定制,故而脂质纳米粒类制剂也被称为“高端复杂注射剂”。 在基因治疗领域,已经开始使用脂质纳米粒包裹核酸,如mRNA、siRNA、pDNA等,称为核酸脂质纳米粒。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310201333444187_1210_5996718_3.jpeg[/img][/align]在这篇应用报告中,我们使用丹东百特仪器公司最新推出的BeNano 180纳米粒度电位仪检测了分散在水性环境中的LNP的粒径。原理 [size=13px] [/size][size=13px] [/size][size=13px]我们[/size]采用丹东百特公司的BeNano 180纳米粒度仪进行测试。仪器使用波长671 nm,功率50 mW激光器作为光源,设置在173[font='arial']°[/font]角的背向检测器进行散射光信号采集,测试过程中,BeNano 180根据样品的散射特点自动确认检测点位置。[align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310201333446515_3271_5996718_3.jpeg[/img][/align]样品制备和测试条件该应用中检测了两个LNP采用微流控混合技术来制备核酸脂质纳米粒,该方法相对简便快速,条件温和,同时容易实现生产放大。1#和2#均为悬浮液,通过[url=https://insevent.instrument.com.cn/t/9p][color=#3333ff]移液枪[/color][/url]注入样品池后直接进行检测。通过BeNano 180内置的温度控制系统开机默认测试温度控制为25℃[font='宋体']±[/font]0.1℃,测试样品的光强、检测点位置、测试时间均通过预测试程序自动进行调节。每一个样品在放入样品池后进行至少三次测试,以检测结果的重复性和得到结果的标准偏差。测试结果和讨论表1. 动态光散射检测脂质体样品结果[table][tr][td]样品[/td][td]Z-均粒径[/td][td]PDI[/td][/tr][tr][td]1#[/td][td]215.9 [font='宋体']± [/font]3.54 nm[/td][td]0.303[/td][/tr][tr][td]2#[/td][td]144.6 [font='宋体']± [/font]0.43 nm[/td][td]0.129[/td][/tr][/table][align=center][/align][align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310201333450955_6423_5996718_3.png[/img][/align]图1. 1#样品和2#样品多次测试的粒径分布曲线通过使用动态光散射技术,得到了样品的粒径和粒径分布信息。通过表1中结果可以看到所有样品的粒径都在100-250 nm范围内,粒径结果重复性良好。PDI均在0.1-0.7范围内,说明两个样品均为适中分布。1#样品明显粒径更高,PDI更大,检测的标准偏差也相对较高,说明1#样品的均匀度不如2#样品。[font='宋体'][size=20px][color=#4f5862]产品配置单:[/color][/size][/font][align=center][img]https://ng1.17img.cn/bbsfiles/images/2023/10/202310201333451551_79_5996718_3.jpeg[/img][/align][align=center][url=https://www.instrument.com.cn/show/C476061.html]百特纳米 粒度仪BeNano 180[/url]([url=https://www.instrument.com.cn/netshow/SH100350/]丹东百特仪器有限公司[/url])[/align][align=center][/align][url=https://www.instrument.com.cn/application/Solution-949709.html][font='宋体'][size=16px]点击这里[/size][/font][/url][font='宋体'][size=16px][color=#000000]浏览[/color][/size][/font][font='宋体'][size=16px][color=#000000]或[/color][/size][/font][font='宋体'][size=16px][color=#000000]下载原[/color][/size][/font][font='宋体'][size=16px][color=#000000]文档,更多解决方案内容请浏览[/color][/size][/font][url=http://www.instrument.com.cn/application/][font='宋体'][size=16px][color=#0081d7]行业应用[/color][/size][/font][/url][font='宋体'][size=16px][color=#000000]栏目:[/color][/size][/font][align=left][url=http://www.instrument.com.cn/application/][font='宋体'][size=13px][color=#0081d7]http://www.instrument.com.cn/application/[/color][/size][/font][/url][font='宋体'][size=13px][color=#000000]行业应用栏目简介:[/color][/size][/font][font='宋体'][size=13px][color=#000000] [/color][/size][/font][font='宋体'][size=13px][color=#000000] [/color][/size][/font][font='宋体'][size=13px][color=#000000]【行业应用】[/color][/size][/font][size=13px][color=#333333]是仪器信息网[/color][/size][size=13px]专业的行业导购平台。汇聚了行业内国内外主流厂商的优质解决方案及相应的仪器设备。建立了兼顾国家相关规定和用户习惯的专业分类,涉及食品、药品、环境、石化等二十余个使用仪器相对集中的行业领域。并以样品和标准为主线,为用户查找仪器提供一个独特的维度,也为仪器产品提供一个全新的展示渠道。[/size][/align]
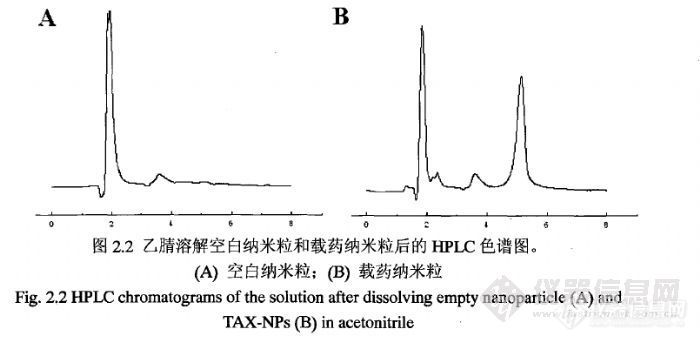
【作者】 吉顺莉;【导师】 戈延茹;金一;【作者基本信息】 江苏大学, 药剂学, 2010, 硕士【摘要】 紫杉醇(Paclitaxel,TAX)是抗肿瘤药物,在临床上已得到广泛应用,特别是对乳腺癌、卵巢癌的治疗作用明显。由于其水溶性差,临床使用的紫杉醇注射液中的紫杉醇是靠聚氧乙烯蓖麻油(CremophorEL)与无水乙醇以1:1的混合液来稳定和溶解。但聚氧乙烯蓖麻油可促进组胺释放,常引起严重的过敏反应和其他不良反应。为了解决上述问题,研究不含Cremophor EL并能提高紫杉醇生物利用度的制剂成为当前的热点。把紫杉醇制备成口服纳米给药系统后,则不仅能减少毒副作用,增加其稳定性,而且方便储存和运输。本文制备了紫杉醇纳米粒(TAX-NPs),优化了其处方和制备工艺,并对其进行了体内外评价。主要内容和结果如下:1.建立了紫杉醇样品HPLC测定方法,并对其线性范围、精密度、回收率等进行了验证,结果表明该方法符合分析要求。以生物可降解聚合物——聚丙交酯乙交酯共聚物(PLGA)为载体,采用乳化-分散法制备了TAX-NPs;以纳米粒的粒径和包封率为评价指标,考察了处方及其工艺因素对制剂质量的影响;对TAX-NPs的基本性质,体外稳定性和释药特征进行了考察;用差示扫描量热法(DSC)及X射线粉末衍射(X... 更多还原http://ng1.17img.cn/bbsfiles/images/2012/08/201208131346_383475_2379123_3.jpg
[font=宋体][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/nanobody][b]纳米抗体[/b][/url]是一种非常有前景的下一代治疗性抗体技术,受到越来越多的研究机构和制药公司的关注。为支持纳米抗体药物的早期发现,义翘神州利用噬菌体抗体库技术自主研发了纳米抗体开发平台,已成功开发了多个纳米抗体候选分子。另外,我们的高通量纳米抗体表达平台,已成功表达和生产了多种纳米抗体形式,包括单价、多价或多特异性[/font][font=Calibri]VHH[/font][font=宋体],满足客户的各种定制需求。[/font][/font][font=宋体] [/font][font=宋体][b]①纳米抗体开发服务[/b][/font][font=宋体][font=宋体]不同于经典的杂交瘤技术制备单克隆抗体,纳米抗体开发的整个流程主要包括羊驼免疫、噬菌体文库构建、抗体筛选、表达纯化及验证等阶段。羊驼免疫后,从羊驼外周血分离[/font][font=Calibri]B[/font][font=宋体]淋巴细胞,提取总[/font][font=Calibri]RNA[/font][font=宋体],反转录为[/font][font=Calibri]cDNA[/font][font=宋体],以[/font][font=Calibri]cDNA[/font][font=宋体]为模板[/font][font=Calibri][url=https://insevent.instrument.com.cn/t/jp][color=#3333ff]PCR[/color][/url][/font][font=宋体]扩增获得多样化的纳米抗体基因片段,然后将其连接到载体上,从而构建噬菌体文库。随后进行多轮淘洗步骤获得抗原特异性纳米抗体,并对其进行测序、表达和验证。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]义翘神州建立了纳米抗体开发平台,可提供一站式的纳米抗体定制服务,主要包括抗原设计与制备、羊驼免疫、文库构建、淘洗、单克隆鉴定、测序以及活性分析等实验步骤,已成功交付多个纳米抗体开发项目。获得的纳米抗体需要进行进一步的人源化改造,以降低其免疫原性,实现最佳的治疗效果。义翘神州提供的纳米抗体人源化服务,利用[/font][font=Calibri]CDR[/font][font=宋体]置换技术及计算机辅助结构模拟设计可对羊驼纳米抗体进行人源化改造,保证人源化程度 [/font][font=Calibri]95%[/font][font=宋体],成功率[/font][font=Calibri]100%[/font][font=宋体]。我们也提供体外药效评价解决方案,满足纳米抗体成药性评估、生物学活性测定等应用场景。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]②高通量纳米抗体表达服务[/b][/font][font=宋体][font=宋体]义翘神州自主研发的高通量重组抗体表达平台,结合了专业的高通量引物合成和载体构建等,可实现高通量抗体表达。除全长[/font][font=Calibri]IgG[/font][font=宋体]抗体外,义翘神州可表达多价[/font][font=Calibri]VHHs[/font][font=宋体]以及[/font][font=Calibri]VHH-Fc[/font][font=宋体]融合型抗体等多种形式,成功率很高,满足客户不同的个性化需求。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]具体流程如下:获得纳米抗体序列文库之后,通过高通量引物合成和载体构建建立纳米抗体表达文库,转至[/font][font=Calibri]HEK293[/font][font=宋体]细胞进行摇瓶培养,通过[/font][font=Calibri]Protiein A[/font][font=宋体]或[/font][font=Calibri]Ni[/font][font=宋体]亲和层析一步纯化,得到纯度大于[/font][font=Calibri]90%[/font][font=宋体]的纳米抗体,纯化后抗体均通过功能验证再进行放大生产。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]③无细胞系统纳米抗体表达服务[/b][/font][font=宋体][font=宋体]除了利用[/font][font=Calibri]HEK293[/font][font=宋体]细胞表达纳米抗体外,义翘神州还自主研发了[url=https://cn.sinobiological.com/services/cell-free-protein-synthesis-service][b]无细胞表达系统[/b][/url],也可实现纳米抗体高通量表达。该系统以外源[/font][font=Calibri]DNA[/font][font=宋体]或[/font][font=Calibri]mRNA[/font][font=宋体]为模板,通过在细胞抽提物的酶系中添加氨基酸、能量物质等实现纳米抗体的体外合成,将原本需要几天的表达过程缩短至几小时,更加快速、高效。义翘神州可提供优质的[/font][font=Calibri]VHH[/font][font=宋体]及[/font][font=Calibri]scFv[/font][font=宋体]快速表达服务,加速您的研发进程。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]具体服务流程如下:首先合成基因、构建载体[/font][font=Calibri]([/font][font=宋体]可选[/font][font=Calibri])[/font][font=宋体],接着利用无细胞合成系统合成纳米抗体,再经纯化以及可行性分析,得到可交付的高质量抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]原文出自:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/nanobody[/font][/font]
创新科技公司欢迎您参加2011年纳米科技大会2011 年 10 月 23-26日,创新科技(中国)有限公司将参加由国家外国专家局国外人才研究中心、中国医药生物技术协会主办,百奥泰国际会议(大连)有限公司承办的第一届纳米科技大会。地点在大连世界博览广场。本次大会的主题是“专业纳米科技盛会”。已邀请到来自中国、美国、加拿大、德国、英国、法国、日本、韩国、澳大利亚等 30 多个国家的院士、知名学者及企业家出席大会并做主题报告。大会瞄准前沿科技和国际热点,设置了十六大分会,包括:纳米科学与纳米技术的最新突破;量子纳米电子学与半导体技术;纳米材料与纳米结构;纳米能源;纳米涂层与胶粘剂;纳米印刷及包装;汽车工业中的纳米技术;纳米制造;纳米清洁技术,纳米环境等议题,将有400多位演讲人登台报告最新的研究进展。同时,创新科技(中国)有限公司将在2011年纳米科技大会上展出有机溶剂纯化系统,小型有机溶剂纯化系统,惰性气体手套箱和色谱仪等产品。届时,我们真诚的邀请您前来参观我们的产品。详情可登录网站:http://www.expo-china.com/pages/exhi/201106/43195/exhi_detail_gaikuang.shtml
[font=宋体][font=宋体]纳米抗体([/font][font=Calibri]nanobody, Nb[/font][font=宋体])是一种人工设计的抗体分子,又称为单域抗体([/font][font=Calibri]single-domain antibodies, sdAbs[/font][font=宋体])、[/font][font=Calibri]VHH[/font][font=宋体]抗体或[/font][font=Calibri]camelid[/font][font=宋体]抗体,是发现于羊驼、单峰驼等驼科以及鲨鱼、鳐鱼等软骨鱼中的一种天然缺失轻链的重链抗体([/font][font=Calibri]heavy-chain antibodies, HCAbs)[/font][font=宋体]。[/font][/font][font=宋体][font=宋体]纳米抗体分子量仅为传统抗体的[/font][font=Calibri]10%[/font][font=宋体],保留了[/font][font=Calibri]HCAbs[/font][font=宋体]完整的抗原结合能力,特异性强、亲和性好、稳定性高,广泛用于生化机制研究、结构生物学及肿瘤等疾病诊疗。[b]纳米抗体的优缺点具体如下:[/b][/font][/font][b][font=宋体]纳米抗体的优点:[/font][/b][font=宋体][font=宋体]([/font][font=Calibri]1[/font][font=宋体])在高温和[/font][font=Calibri]pH[/font][font=宋体]下的稳定性;[/font][/font][font=宋体][font=宋体]([/font][font=Calibri]2[/font][font=宋体])[/font][font=Calibri]VHH[/font][font=宋体]可以识别通常不被常规抗体识别的抗原位点;[/font][/font][font=宋体][font=宋体]([/font][font=Calibri]3[/font][font=宋体])它们的小分子片段有助于快速组织渗透和标记应用,包括跨越血脑屏障;[/font][/font][font=宋体][font=宋体]([/font][font=Calibri]4[/font][font=宋体])用于大规模生产节约成本的替代品。[/font][/font][font=宋体] [/font][font=宋体][b]纳米抗体的缺点:[/b][/font][font=宋体][font=宋体]由于纳米抗体的半衰期短,限制其临床应用,因此可将[/font][font=Calibri]VHH[/font][font=宋体]抗体与抗血清白蛋白或抗体的[/font][font=Calibri]Fc[/font][font=宋体]段融合表达以延长其在血液中的半衰期。[/font][/font][font=宋体] [/font][font=宋体][b]纳米抗体的制备主要分为两个方向:基于蛋白工程的方法和基于化学合成的方法。[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1. [/font][font=宋体]基于蛋白工程的方法:在[/font][font=Calibri]20[/font][font=宋体]世纪[/font][font=Calibri]80[/font][font=宋体]年代晚期和[/font][font=Calibri]90[/font][font=宋体]年代初期,科学家提出了单链抗体[/font][font=Calibri](scFv)[/font][font=宋体]的概念,并使用噬菌体显示技术实现了单链抗体的制备。随后,研究人员进一步改进了单链抗体的设计和优化,使其具有更好的稳定性和亲和力。这些单链抗体通过基因工程手段制备,可以实现在细菌或哺乳动物细胞中大规模生产。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2. [/font][font=宋体]基于化学合成的方法:随着化学合成技术的发展,科学家们开始探索利用化学合成方法制备纳米抗体。在[/font][font=Calibri]2003[/font][font=宋体]年,研究人员开发出了一种称为[/font][font=Calibri]DNA[/font][font=宋体]导向的抗体组装的方法,通过[/font][font=Calibri]DNA[/font][font=宋体]纳米结构的设计和组装,实现了纳米级抗体的制备。这种方法利用[/font][font=Calibri]DNA[/font][font=宋体]的互补配对性质将抗体片段组装在一起,形成稳定的纳米抗体结构。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3. [/font][font=宋体]其他制备方法的发展:随着纳米科技和纳米材料的发展,研究人员还尝试了其他制备纳米抗体的方法。例如,利用核酸适配体技术结合纳米材料,实现了纳米级别的适配体抗体复合物。此外,还利用纳米粒子和纳米材料作为载体,将传统抗体修饰在其表面,形成纳米抗体。[/font][/font][font=宋体] [/font][font=宋体][font=宋体]总的来说,纳米抗体的制备方式相对来说并不是特别的困难,但是和传统抗体的生产过程一样,它需要注意到的细节问题有很多。值得注意的是,纳米抗体的制备技术依然在飞速发展和创新中,并取得了不错的进展,也让我们制备抗体的时候,有了更多选择。更多详情可以关注义翘神州[url=https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins][b]纳米抗体[/b][/url]页面:[/font][font=Calibri]https://cn.sinobiological.com/resource/protein-review/transmembrane-proteins[/font][/font][font=Calibri] [/font]
[font=宋体][b]什么是纳米抗体?[/b][/font][font=宋体][font=宋体][url=https://cn.sinobiological.com/resource/antibody-technical/nanobody][b]纳米抗体[/b][/url]([/font][font=Calibri]nanobody, Nb[/font][font=宋体])是一种人工设计的抗体分子,又称为单域抗体([/font][font=Calibri]single-domain antibodies, sdAbs[/font][font=宋体])、[/font][font=Calibri]VHH[/font][font=宋体]抗体或[/font][font=Calibri]camelid[/font][font=宋体]抗体,是发现于羊驼、单峰驼等驼科以及鲨鱼、鳐鱼等软骨鱼中的一种天然缺失轻链的重链抗体([/font][font=Calibri]heavy-chain antibodies, HCAbs)[/font][font=宋体]。[/font][font=Calibri]1993[/font][font=宋体]年,比利时的科学家在骆驼的血清中发现了一种天然轻链缺失的重链抗体,分子量约[/font][font=Calibri]95 kDa[/font][font=宋体],其中包括两个恒定区([/font][font=Calibri]CH2[/font][font=宋体]和[/font][font=Calibri]CH3[/font][font=宋体])、一个铰链区和一个重链可变区([/font][font=Calibri]variable heavy chain domain, VHH[/font][font=宋体]),接着克隆得到只包含一个重链可变区的单域抗体,即[/font][font=Calibri]VHH[/font][font=宋体]抗体。[/font][font=Calibri]VHH[/font][font=宋体]抗体的晶体结构为[/font][font=Calibri]4 nm[/font][font=宋体]×[/font][font=Calibri]2.5 nm[/font][font=宋体]×[/font][font=Calibri]3 nm[/font][font=宋体]的椭圆形,分子量大小仅普通抗体的[/font][font=Calibri]1/10[/font][font=宋体],约[/font][font=Calibri]12-14 kDa[/font][font=宋体],是最小的完整抗原结合片段,因此又被称为纳米抗体。纳米抗体可用于肿瘤等疾病的治疗、疾病的检测、疫苗的研发等。[/font][/font][font=宋体] [/font][font=宋体] [/font][font=宋体][b]纳米抗体特性:[/b][/font][font=宋体] [/font][font=宋体][font=Calibri]1.[/font][font=宋体]高耐热性和稳定性[/font][/font][font=宋体] [/font][font=宋体][font=宋体]将不同的纳米抗体在[/font][font=Calibri]37[/font][font=宋体]℃放置[/font][font=Calibri]1[/font][font=宋体]周,结果其抗原结合活性均在[/font][font=Calibri]80%[/font][font=宋体]以上,表明纳米抗体在室温下保存相当稳定,这使其比常规抗体更易于储藏和运输。[/font][/font][font=宋体][font=宋体]比较了鼠单抗和纳米抗体在高达[/font][font=Calibri]90[/font][font=宋体]℃高温长时间处理的抗原结合活性,发现纳米抗体都保持了较高的活性仍能重新获得抗原结合能力,而所有常规抗体在[/font][font=Calibri]90[/font][font=宋体]℃处理后都丧失了活性,发生了不可逆的聚合。[/font][/font][font=宋体][font=宋体]在恶劣条件,如在高热、离液剂、存在蛋白酶和极度[/font][font=Calibri]pH[/font][font=宋体]值变性的条件下(如胃液和内脏中),正常抗体会失效或分解,而纳米抗体仍具有高度的稳定性。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]2.[/font][font=宋体]高抗原结合性:[/font][/font][font=宋体] [/font][font=宋体][font=宋体]纳米抗体独特的结构决定了其高抗原结合特性:纳米抗体较长的[/font][font=Calibri]CDR3[/font][font=宋体],可形成一稳定的暴露的凸环结构(凸环中具有稳定结构的二硫键),能够深入抗原内部以更好的结合抗原从而提高了其抗原特异性和亲和力。[/font][/font][font=宋体][font=宋体]而传统抗体[/font][font=Calibri]Fab[/font][font=宋体]片段及单链抗体[/font][font=Calibri]scFv[/font][font=宋体]的抗原结合表面常形成凹形拓扑结构[/font][font=Calibri], [/font][font=宋体]通常只能识别位于抗原表面的位点,因此纳米抗体[/font][font=Calibri]VHH[/font][font=宋体]单域具有更加广泛的抗原结合力,甚至当靶蛋白紧密包裹隐藏了普通抗体识别的位点时[/font][font=Calibri],[/font][font=宋体]纳米抗体也可以对其进行表位识别。[/font][/font][font=宋体] [/font][font=宋体][font=Calibri]3.[/font][font=宋体]较强的组织穿透力:[/font][/font][font=宋体] [/font][font=宋体]纳米抗体具有强而快的组织穿透能力,可以进入致密的组织如实体瘤发挥作用;并且多余未结合的纳米抗体能够很快的被清除,这相对于单克隆抗体组织穿透力差,不易被清除的不足,更有利于疾病的诊断。另外,纳米抗体能够有效的穿透血脑屏障,这样的特性为脑部给药提供了新方法,有望成为治疗老年痴呆症的新药。[/font][font=宋体] [/font][font=宋体][font=Calibri]4.[/font][font=宋体]高水溶性、高表达性[/font][/font][font=宋体] [/font][font=宋体][font=宋体]正常抗体[/font][font=Calibri]VH[/font][font=宋体]结构域单独表达时通常形成包涵体,或者暴露的疏水域相互黏附;而纳米抗体[/font][font=Calibri]VHH[/font][font=宋体]由于其[/font][font=Calibri]FR2[/font][font=宋体]中的疏水残基被亲水残基所取代,使得纳米抗体的水溶性增加,聚合性减少;而且即使以包涵体形式表达,也很容易复性,这样可以大大提高作为药物的利用率。[/font][/font][font=宋体][font=宋体]因纳米抗体分子量小、结构简单,由单一的基因编码,所以它很容易在微生物中合成,能在噬菌体、酵母等微生物中大量的表达,而且其相对价格低廉、可进行大规模生产,易于普及和应用。有报道,可通过酵母反应器酿造将纳米抗体的产量提高,每公升可达[/font][font=Calibri]1[/font][font=宋体]克的产量。[/font][/font][font=宋体] [/font][font=宋体][b]纳米抗体的应用优势[/b][/font][font=宋体] [/font][font=宋体][font=宋体]①用于生物医药研发(基因工程药物研发、[/font][font=Calibri]ADC[/font][font=宋体]药物研发);[/font][/font][font=宋体]②用于临床体外诊断(胶体金法、酶联免疫吸附法、电化学发光法);[/font][font=宋体]③用于肿瘤研究、免疫学研究等基础研究;申请具有自主知识产权的发明专利及科研奖项;[/font][font=宋体]④拓展研究思路、发表国际知名学术刊物。[/font][font=宋体] [/font][font=宋体][font=宋体]纳米抗体是一种非常有前景的下一代治疗性抗体技术,受到越来越多的研究机构和制药公司的关注。为支持纳米抗体药物的早期发现,义翘神州利用噬菌体抗体库技术自主研发了纳米抗体开发平台,已成功开发了多个纳米抗体候选分子。另外,我们的高通量纳米抗体表达平台,已成功表达和生产了多种纳米抗体形式,包括单价、多价或多特异性[/font][font=Calibri]VHH[/font][font=宋体],满足客户的各种定制需求。[/font][/font][font=宋体][font=宋体]更多详情可以关注:[/font][font=Calibri]https://cn.sinobiological.com/resource/antibody-technical/nanobody[/font][/font][font=Calibri] [/font]
木犀草素(luteolin),别称草木犀、黄示灵等,大多以糖苷的形式广泛存在于多种中药材、天然药用植物[1]及蔬菜[2]中的一种黄酮类化合物,是一种天然色素成分,可以作为食用色素添加于食品中。木犀草素的化学名为3′,4′,5,7-四羟基黄酮(3′,4′,5,7-tetrahydroxyflavone),物理状态为淡黄色结晶状粉末,熔点为330 ℃,包含4个酚羟基,具有弱酸性,可溶于碱性溶液中,因脂溶性高而难溶于水,从而阻碍了其在体内的吸收与利用[3]。木犀草素具有抗炎和抗菌[4-5]、抗氧化[6]、抗肿瘤[7]、神经保护[8]、抑制肺纤维化[9]及肺癌[10-11]和心血管疾病[12]等多种药理作用。由于水溶性差(仅为6.0 mg/L)、生物利用度率低等原因限制了其成药性和临床应用。针对这一问题,近年来许多学者开展了增加木犀草素溶解度的研究,如微球[13]、纳米胶束[14]、金属配合物[15]、自微乳[16]、脂质体[17]等,并明显提高了其生物利用度,这表明木犀草素的肠道渗透性不是限制其生物利用度的关键因素,其属于生物药剂学系统II类药物。因此,采用制剂技术提高木犀草素的溶解性是可以改善其成药性和生物利用度的,将有利于推广其临床应用。然而上述开发的剂型仍存在诸多的缺点,如工艺复杂、载药量低、生物安全性差、成本高等,难以大范围推广应用。近年来,逐步发展成熟的纳米混悬剂[18]作为一种新剂型,与传统纳米制剂相比,它具有载药量高、溶出度高、添加剂用量少、易于放大生产等优点。因此,本实验尝试将难溶性木犀草素制备成纳米混悬剂以提高其水溶性和生物利用度,改善其成药性和临床优势。 为此,本实验首先采用微沉淀-高压匀质法制备口服木犀草素纳米混悬剂(luteolin nano-suspension,LNS),并以纳米粒的粒径、稳定性、多分散性指数(polydispersity index,PDI)、ζ电位等为考察指标,采用单因素考察法筛选LNS的稳定剂和最优药物-稳定剂比;接着,对LNS的理化性质进行考察,并分析其物理状态和体外溶出行为;最后通过大鼠外翻肠模型考察药物在肠道不同部位的吸收转运情况,探索药物在肠道内的吸收速率和最佳部位,预测纳米混悬剂可能存在的体内吸收行为,既可以用于木犀草素口服给药的潜在剂型,也为其进一步加工成其他剂型研究提供基础。 1 仪器与材料 1.1 仪器 ZNCL-BS180型恒温磁力搅拌器,北京市永光明医疗仪器有限公司;AL104-1C型精密分析天平,上海鼎科科学仪器有限公司;NS1001L型高压匀质机,意大利GEA [url=https://insevent.instrument.com.cn/t/1p][color=#3333ff]NIR[/color][/url]o Soavi公司;Nanotrac wave II型激光粒度仪型激光粒度仪,美国麦奇克有限公司;LC3100型高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],安徽皖仪科技股份有限公司;ZWY-103D型恒温振荡仪,上海智诚分析仪器制造有限公司;H1650-W型医用离心机,湖南湘仪实验室仪器开发公司;DZF-6030型真空干燥箱,上海精宏实验设备有限公司。JEOL 2010型透射电子显微镜(TEM),日本JEOL公司。 1.2 试剂 木犀草素原料药,批号JZ19021403,质量分数97.0%,南京狄格尔医药科技有限公司;木犀草素对照品,批号ps1032-0025,HPLC质量分数≥98%,成都普思生物科技有限公司;十二烷基磺酸钠(sodium dodecyl sulfonate,SDS),医药级,河南圣拓实业有限公司;泊洛沙姆188(Poloxamer 188,Pluronic,F68),医药级,西安天正药用辅料有限公司;维生素E聚乙二醇琥珀酸酯(D-α-tocopherol polyethylene glycol 1000 succinate,TPGS),医药级,上海惠诚生物科技有限公司;二甲基亚砜(dimethyl sulfoxide,DMSO),分析纯,天津市德恩试剂有限公司。 1.3 动物 SD大鼠购买于河南省实验动物中心,体质量(200±20)g,合格证号:SCXK(豫)2017-0001。所有动物实验均经过河南大学动物伦理委员会审核批准(HUSOM2019-216)。 2 方法与结果 2.1 LNS的制备 2.1.1 LNS中稳定剂的选择 将40 mg木犀草素原料药超声溶解于1 mL的DMSO中作为有机相,再取等量的稳定剂(SDS、F68、TPGS)溶解于纯水中(作为水相,或称反溶剂相);在室温下,将有机相通过注射器快速注入转速为1 800 r/min的反溶剂相中,继续搅拌10 min,得到预混悬剂;将预混悬剂转移至高压匀质机中,分别以20.0、50.0、80.0 MPa的压力循环匀质5、5、25次,得到LNS。 利用动态光散射仪分别考察LNS的粒径、多分散系数(polydispersity index,PDI)、表面电荷(ζ电位)和稳定性。本实验以不同稳定剂(SDS、F68、TPGS)制备的LNS粒径大小、PDI、ζ电位结果如表1所示。3种稳定剂所制备的粒径均在100~500 nm。以SDS为稳定剂制备的纳米混悬剂粒径最大,以F68为稳定剂制备的纳米混悬剂PDI最大,以TPGS为稳定剂制备的纳米混悬剂ζ电位最大,但是3者没有较大的差异,因此对于预测稳定性来说,上述结果难以判断哪个稳定剂制备的LNS会有良好的贮存稳定性。 因此,本实验又对各种条件的贮存稳定性进行了研究,结果见图1。以SDS、F68为稳定剂制备的纳米混悬剂在1周内粒径呈现持续增长的趋势,而以TPGS为稳定剂制备的LNS粒径未出现明显变动,由此可知,本实验中以TPGS为稳定剂制备的LNS具有较好的物理稳定性。 2.1.2 LNS中药物-稳定剂质量比的筛选 将40 mg的木犀草素原料药超声溶解于1 mL的DMSO中作为有机相,再分别按照木犀草素与TPGS的质量比为1∶2、1∶1、2∶1称取TPGS,溶解于水中,得到反溶剂相;再按上述工艺制备LNS,得到不同药物-稳定剂质量比的LNS。利用动态光散射仪分别考察纳米混悬剂的粒径、分布、ζ电位和稳定性。不同药物-稳定剂比制备的LNS的理化性质研究结果见表2和图2。如表2所示,3种不同药物-稳定剂比制备的LNS的粒径分别为(289.3±6.6)、(210.7±2.0)、(34.6±3.7)nm,3种LNS的PDI接近,1∶2时ζ电位最大,2∶1时ζ电位没测到。虽然药物与稳定剂的质量比为2∶1时,其粒径与1∶2、1∶1时相差较大,但是粒径难以反映稳定性情况。因此,接下来考察了1∶2、1∶1、2∶1 3种不同比例下制备的LNS的稳定性,结果如图2所示。当药物-稳定剂比为2∶1和1∶2时,在2周内粒径变化幅度都较为明显,说明其稳定性表现均极差;而当药物-稳定剂比为1∶1时,制备的纳米混悬剂的粒径基本保持稳定,表明其稳定性较好。因此,本实验最终选用药物-稳定剂比为1∶1。 2.1.3 最优制备处方和方法的确定 依照LNS的稳定剂及药物-稳定剂比的筛选结果,初步确定LNS的最优制备处方与方法如下:将精密称取40 mg的木犀草素原料药超声溶解于1 mL的DMSO中作为有机相;将40 mg TPGS搅动溶解于40 mL纯水中作为水相,将有机相快速注入转速为1 800 r/min的水相中,搅动10 min,得到预混悬剂;将制备的预混悬剂倒入高压匀质机的导入槽中,分别以20.0、50.0、80.0 MPa的压力,分别循环匀质5、5、25次,得到LNS。重复制备3批,以粒径、PDI和ζ电位考察制剂处方和制备工艺的稳定性。 2.2 LNS的表征 2.2.1 粒径、ζ电位及形态分析 将最优处方制备的3批LNS分别通过激光粒度分析仪测定其粒径、PDI、ζ电位,结果LNS的粒径为(209.00±3.24)nm(n=3),PDI都低于0.228±0.013(n=3),粒径分布图见图3;ζ电位值为(?16.80±0.27)mV (n=3),较小的PDI和绝对值较大的ζ电位,意味着LNS可能具有较好的长期稳定性[19]。 再取适量的LNS加蒸馏水稀释到适当倍数后,滴在覆有支持膜的铜网上,自然环境下干燥后,通过TEM观察其形态特征及大小,并成像,结果见图4。LNS呈现均匀分散的球形或椭圆形颗粒,粒径约为180 nm,比动态光散射测定结果较小,这可能是由于TEM样品为干燥品,导致粒子外层亲水部分失水而收缩[20]。 2.2.2 储存稳定性 将制备的LNS分别放在4 ℃和室温环境中,在预定的时间点取样,通过激光粒度分析仪测定其粒径和PDI,连续考察14 d,每个样品平行操作3份,结果见表3。LNS在4 ℃和室温下储存2周后,粒径和PDI稍有增加,但变化范围都较小,说明该LNS的储存稳定性较好。 2.2.3 体外胃肠环境中的稳定性 以pH 1.2和pH 6.8的缓冲溶液模拟胃液和肠液,将制备的LNS分别以1∶1与上述2种缓冲溶液混合,并于37 ℃水浴中放置,在预定的时间点0、2、4、6、8、12、24 h时取样,通过激光粒度分析仪测定其粒径,连续考察24 h,每个样品平行操作3份,结果见表4。在2种37 ℃的缓冲溶液中孵育24 h内,LNS的粒径和PDI几乎无变化,表明LNS在2种环境中能保持稳定,这表示LNS口服给药后,在经胃肠道给药时能保持良好的稳定性,这有利于木犀草素到达肠道后仍以纳米晶存在,从而有利于木犀草素的快速释放而获得较高的生物利用度。 2.2.4 纳米混悬剂的物理状态研究 本实验选用DSC来确定LNS中的木犀草素晶型是否发生了改变,测试样品有木犀草素、TPGS、木犀草素与TPGS的物理混合物和LNS。以空铝盘作为空白对照,分别精密称取3~5 mg的木犀草素、TPGS、物理混合物(木犀草素+TPGS)、LNS干粉放于差式扫描量热分析(differential scanning calorimetry,DSC)仪中,N2流(40 mL/min)保护下,以10 ℃/min升温速度持续升温,升温范围设置为40~600 ℃,记录差式扫描量热分析图谱,所有测试样品重复分析3批,结果见图5。木犀草素和LNS、物理混合物均是结晶,其熔融温度为339.38 ℃,稳定剂对木犀草素的熔融温度基本无影响。这表明LNS中的木犀草素仍处于结晶状态,稳定剂的存在不会改变木犀草素的晶型。在木犀草素和LNS中,在50~150 ℃出现了1个宽峰,这可能是由于药物吸收了水分造成的。 再分别称取适量的木犀草素、TPGS、物理混合物(木犀草素+TPGS)、LNS置于X射线粉末衍射(X-ray powder diffraction,XRPD)仪中,以步进测定方式,散射角扫描范围设为5°~60°,电压设为40 kV,电流为30 mA,结果见图6。由图6可知,木犀草素在19.12、23.20、26.32 ℃有3个衍射峰,衍射峰的峰形较为尖锐,峰值较高,表明木犀草素的晶型为结晶型。稳定剂TPGS在15.72、17.48、22.86、25.60、29.26 ℃有衍射特征峰。制备成纳米混悬剂后,虽然LNS图谱中木犀草素的特征峰有所减弱,但与木犀草素相比,在相应位置特征峰均存在,进一步证实制备成LNS后木犀草素并未显著改变晶型,说明稳定剂的加入不会影响木犀草素的晶型,这与DSC分析的结果一致。 2.3 平衡溶解度与过饱和溶出度测试 为了测定木犀草素的平衡溶解度与木犀草素纳米混悬剂的过饱和溶出度,本实验参考文献方法[21]建立了HPLC法。 2.3.1色谱条件 色谱柱为Sino Chrom ODS-BP色谱柱(250 mm×4.6 mm,5 μm);流动相为甲醇-0.3%磷酸水溶液(60∶40);柱温30 ℃;检测波长350 nm;体积流量1 mL/min;进样量10 μL。 2.3.2对照品溶液的配制 精密称取木犀草素对照品2.50 mg,放入100 mL棕色量瓶中,以适量色谱甲醇使之完全溶解,并定容至刻度线,摇匀得到质量浓度为25 μg/mL的木犀草素对照品储备液。 2.3.3 线性关系考察 采用色谱甲醇稀释成质量浓度分别为0.5、1.0、2.0、5.0、7.0、10.0 μg/mL系列的木犀草素对照品溶液,按“2.3.1”项下色谱条件进行分析,以对照品质量浓度为横坐标(X)、峰面积为纵坐标(Y)进行线性回归,得线性回归方程为Y=44 670 X-2 498.3,R2=0.999 8,结果表明木犀草素在0.5~10.0 μg/mL线性关系良好。 2.3.4 专属性、精密度和准确度考察 在建立的HPLC色谱条件下,木犀草素色谱峰不会受pH 1.2和pH 6.8的溶出介质、稳定剂TPGS、Tyrode液以及肠吸收液中所有成分的干扰(图7),表明本实验所建立的含量测定方法具有较好的专属性,能够满足体外溶出和肠吸收试验中木犀草素的含量测定要求。另外,其精密度实验的RSD为1.2%,高、中、低3个质量浓度的样品加样回收率在99.67%~101.47%,RSD均小2%,符合《中国药典》2020年版的规定。 2.3.5 平衡溶解度的测定 为了测定木犀草素在pH值为1.2、6.8缓冲溶液中的平衡溶解度,取5 mL 2种缓冲溶液各3份于西林瓶中,加入过量的木犀草素,将西林瓶置于恒温振荡箱中,在温度为37℃,转速为75 r/min条件下振荡24 h。取出各样品,3 000 r/min下离心10 min后取上清液,然后用0.2 μm滤膜滤过,取续滤液于进样瓶中,按照“2.3.1”项下色谱条件进样测定,并计算木犀草素的平衡溶解度,结果可知,木犀草素在pH值为1.2、6.8的缓冲溶液中的平衡溶解度分别为(3.83±0.23)、(7.81±0.13)μg/mL。 2.3.6 过饱和溶出度的测定 为了考察LNS体外溶出行为,参照《中国药典》2020年版中桨法进行。具体操作如下:在智能溶出仪中,以500 mL模拟胃液为溶出介质,温度为37℃,桨旋转速度为75 r/min,将30 mL LNS加入溶出介质中,以相同质量浓度的木犀草素乙醇溶液作为对照,二者均平行操作3份。以药物刚接触溶出介质开始计时,分别于5、15、30、60、120、130、150、180、240、360、480 min时取样4 mL,取完样后立即补充4 mL相应的新鲜溶出介质。另外,于120 min取样后,每个溶出杯中分别加入适量的Na3PO4溶液,调节pH值为6.8,以模拟肠液。将所取样品溶液经0.2 μm微孔滤膜滤过,取续滤液置于进样瓶中,照“2.3.1”项下色谱条件测定,计算累积溶出度,结果见图8。为了测定过饱和溶出水平,在整个实验过程中,介质中药物的质量浓度都应保持远远大于药物的饱和溶解度[22]。结果如图8所示,在pH 1.2和pH 6.8时,木犀草素-原料药的过饱和溶出始终低于对应的平衡溶解度,LNS的过饱和溶出始终高于对应的平衡溶解度,说明制剂的过饱和度高;在溶出介质的pH值调为6.8后,过饱和溶出水平明显下降,在150 min后过饱和溶出水平逐渐稳定,说明LNS能维持较高的过饱和溶出水平。 结果表明,LNS较木犀草素原料药具有明显优势,其饱和溶出度约是木犀草素原料药的15倍,过饱和度高并能维持较长时间,可以延缓药物在体内因析出晶体而沉淀的过程,从而使稳定剂在较小用量下也能保证药物分子成溶解态,提高了原料药的溶解度,有利于增加其生物利用度[23]。 2.4 小肠吸收实验 为了探索LNS对木犀草素在胃肠道的吸收部位和吸收速率的影响,采用外翻肠囊法[24]研究LNS在肠道不同肠段的吸收特征,以探究药物在肠道内的最佳吸收部位。 2.4.1 对照品溶液的制备 精密量取“2.3.1”项下相应体积的储备液,置于50 mL棕色量瓶中,用Tyrode液定容至刻度,摇匀,配制出质量浓度为1、2、4、8、16、32、40 μg/mL木犀草素对照品溶液。 2.4.2 线性关系考察 按照“2.3.1”项下色谱条件测定,以木犀草素对照品质量浓度为横坐标(X),峰面积为纵坐标(Y)进行线性回归,得到回归方程为Y=45 475 X-19 575,R2=0.999 6,结果表明木犀草素在1~40 μg/mL线性关系良好。 2.4.3 供试品溶液的制备 大鼠按实验质量浓度随机分为3组,每组4只,实验前12 h禁食,自由饮水。颈椎脱臼处死,打开腹腔,小心分离出小肠,分别截取十二指肠、空肠、回肠、结肠相应肠段各10 cm,用生理盐水冲洗至无内容物流出。将肠段放入37 ℃ Tyrode液中,冲洗,在不损伤肠管的情况下,小心剥离肠表面的脂肪及血管,取出,用滤纸吸干表面水分。 将肠管一端结扎,用光滑的玻璃棒外翻,用Tyrode液冲洗过后,向不同肠段中注入3 mL的空白Tyrode液后将另一端也进行结扎形成囊状的肠管。将肠管放入盛有Tyrode液的烧杯中,实验中始终保持37 ℃的恒温,并不断通入95% O2/5% CO2的混合气体。平衡5 min后,将烧杯中的液体倒出,分别加入不同质量浓度(0.15、0.30、0.60 mg/mL)的木犀草素及LNS药液。以肠囊和药液接触时开始计时,取样时间点分别为15、30、45、60、75、90、105、120 min,每个时间点从肠囊内取样500 μL,同时补充同温同体积的空白Tyrode液。待试验结束后,将各段肠囊置于空白Tyrode液中孵育1 h,以清除掉肠囊及肠组织中残留的药物;随后将上述用于木犀草素和LNS吸收实验的各肠段互换,再按上述操作同法重复试验,以进行自身对照交叉试验的后段实验。取上述肠吸收液,加入甲醇500 μL,超声混匀,15 898×g离心(离心半径6.32 cm)2次,每次15 min,取上清液用0.2 μm滤膜滤过,取续滤液适量即得。 按照“2.3.1”项下色谱条件测定,并计算药物在各时间点的累积吸收量(Q,μg)和药物吸收速率常数[Ka,μg/(mincm2)],结果见图9。 由公式计算不同质量浓度下木犀草素在各个时间点的累积吸收量(Q)。 Q是每个时间点木犀草素的累积吸收量,Ci是每个时间点的实际检测质量浓度,V1是加入肠囊内的空白Tyrode液,V2是每次取样的体积 由图9可知,通过对比2种制剂在各肠段中不同质量浓度的药物吸收情况,可以发现药物的同一时间点的吸收量表现出质量浓度相关性。相同质量浓度下,在各肠段中2制剂组吸收量相比,LNS组的药物累积吸收量显著大于木犀草素溶液组,表明LNS相比于木犀草素溶液能够促进药物在肠道的吸收。 根据小肠内(4个肠段)的Q值,通过线性拟合,由公式Ka=L(斜率)/A(肠管平铺面积)求得吸收速率常数(Ka)和相关系数(R2),结果见表5。2种制剂中木犀草素在肠道的不同部位中的吸收速率大小顺序均为十二指肠>空肠>回肠>结肠,这可能归因于十二指肠和空肠肠段的吸收面积较大;这一结果还表明LNS并没有改变木犀草素在肠道内的主要吸收部位和机制。对比相同质量浓度、相同肠段中2种制剂的吸收情况可以发现,LNS中木犀草素的吸收速率显著高于木犀草素溶液的情况,尤其是十二指肠和空肠中LNS和木犀草素溶液的木犀草素吸收速率差异更加明显,这表明LNS可以增加木犀草素的肠吸收,且十二指肠和空肠是主要吸收部位。 另外,还可以发现2种制剂在每一肠段中的吸收速率都存在显著的质量浓度相关性(P<0.01),但是2种制剂在同一肠段中的吸收速率随质量浓度增加而提高的程度有明显差异,即木犀草素溶液随质量浓度的增加,各肠段中吸收速率增幅增大,而LNS随质量浓度的增加,各肠段中吸收速率增幅减小,这些结果表明2种制剂在各肠段中的吸收均有质量浓度相关性,但其吸收速率与质量浓度之间均存在非线性关系,且仅在Ka<0.052时,木犀草素的肠吸收过程可能只受木犀草素溶解度限制,而不受吸收速度限制。然而,木犀草素的实际口服吸收情况是否符合上述规律以及其具体吸收机制如何,将有待于后期开展体内外吸收途径探索和体内药动学研究来进一步证实。 3 讨论 3.1 稳定剂的选择及药物-稳定剂比的确定 由于不同的稳定剂中化学基团的差异,导致稳定剂与药物微粒之间的分子间作用力以及胶粒间的作用力都有明显差异,所以稳定剂种类会影响到纳米混悬剂的稳定性[25]。因此,本实验首先以粒径和稳定性为考察指标,通过单因素筛选法优化了LNS的稳定剂种类,并确定了以TPGS作为稳定剂能达到较好的预期效果;考虑到稳定剂用量对稳定效果的影响[26],随后本实验又考察了药物-稳定剂比对纳米混悬剂的粒径、稳定性、PDI、ζ电位的影响,最终确定最佳药物-稳定剂比为1∶1。 3.2 LNS体外分析方法的建立及研究 3.2.1 波长的选择 木犀草素对照品与稳定剂TPGS在紫外波长200~800 nm扫描,结果显示木犀草素在207、254、350 nm 3处波长处有强吸收;而TPGS在219、286 nm显示出强吸收,350 nm处没有显示出强吸收。为了排除稳定剂TPGS对木犀草素测定的干扰,选用350 nm作为木犀草素的测定波长。 3.2.2 Tyrode溶液的配制 在木犀草素的肠吸收情况研究中,虽有文献报道了外翻肠囊模型和在体单向肠灌流模型[27-29],但关于木犀草素及其制剂在大鼠不同肠段中的吸收情况鲜有报道,且大多数文献对其吸收情况所提甚少。 本实验采用离体外翻肠囊法,可操作性强、重复性好;能够保留较为完整的肠道组织和黏膜特性,其实验结果与机体药物吸收水平比较接近,具有说服力;但肠外翻肠囊法也存在缺点,如长时间暴露在体外,肠管没有血管和神经的控制,肠黏膜功能和形态会失去作用。因此,本研究为解决这一问题,利用Tyrode培养液改善肠管的存在环境,具体配制方法如下:将NaCl(8.0 g/L)、KCl(0.2 g/L)、CaCl2(0.2 g/L)、NaHCO3(1 g/L)、NaH2PO4(0.05 g/L)、MgCl2(0.1 g/L)、葡萄糖(1.0 g/L),用蒸馏水定容至1 000 mL,稀盐酸调pH值为7.2~7.4,由于CaCl2不好溶解,应在其他无机盐溶解完全后再加入,葡萄糖于临用前再加入。并且在实验过程中连续通入95% O2/5% CO2,保证了在实验期间肠管上肠黏膜的活性。实验证明用该模型了解药物的离体吸收,其结果可靠。 3.3 LNS的过饱和溶出 药物在纳米混悬剂中所处的物理状态关系着其粒径和溶出稳定性,通常无定形药物微粒具有较高的饱和溶出度,但其属于热力学不稳定状态,因此物理稳定性差,容易引起纳米混悬剂粒径分布发生变化,同时溶出速率和溶出度下降;而结晶型药物具有较好的热力学稳定性,随着其粒径的减小,其饱和溶出度会明显提高[30]。根据本实验对LNS中木犀草素物理状态的研究结果可知,本实验制备的LNS中木犀草素以结晶形式存在,这表明LNS可能存在稳定的粒径和溶出度。 在过饱和溶出实验中发现,相比于木犀草素原料药,LNS具有显著的长期高过饱和溶出水平,这可归因于LNS中药物以粒径远小于原料药的状态存在,正如开尔文定律所描述的小粒径药物具有高溶解度一样[31]。药物的长期高过饱和溶出水平将有助于避免或减少口服给药后因胃肠道pH变化而引起的析晶沉淀现象,从而增加药物的吸收速度和时间,提高药物的口服生物利用度。 综上所述,本实验制备的LNS,分散性和储存稳定性良好,方法也简单易行,本实验建立的木犀草素体外分析方法,经方法学验证可知,该方法快速、可靠、准确度高,适合LNS的体外溶出和外翻肠囊吸收实验研究。 同时,外翻肠实验表面,LNS能促进药物在肠道的吸收,可作为木犀草素口服给药的潜在剂型,也为其进一步加工成其他剂型研究提供坚实基础。同时,在木犀草素肠道吸收的具体机制方面还有很大的研究空间。