它是采用免疫原理和胶体金层析技术制成快速检测牛奶、食品、饲料中的霉菌毒素的残留量检测限是10ppb 饲料 谷物用黄曲霉毒素总量检测卡,黄曲霉毒素B1检测卡检测限是0.5 ppb 原奶生鲜奶 黄曲霉毒素M1检测卡检测限是50ppb 饲料 谷物 玉米赤霉烯酮检测卡检测限是1ppb 饲料 谷物 赭曲霉毒素检测卡检测限100ppb 伏马毒素检测卡检测限0.3毫克每千克 液态奶、奶粉 三聚氰胺检测卡
哪些物质会影响β-内酰胺酶检测卡的检测
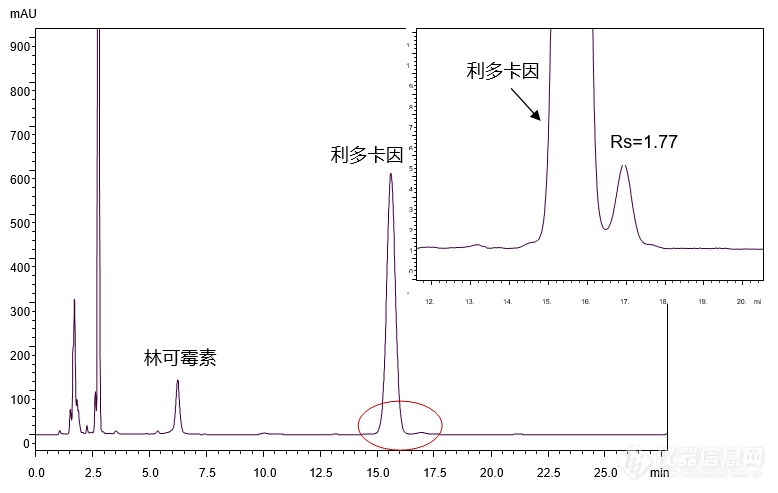
[align=center][b]【国家药品标准】林可霉素利多卡因凝胶的分析[/b][/align][align=center][b][/b][/align][align=right][b]——依据国家药品标准WS-10001-(HD-0140)-2002方法[/b][/align][b]林可霉素利多卡因凝胶[/b]为复方制剂,每克含林可霉素5毫克,利多卡因4毫克。适应症为用于轻度烧伤、创伤及蚊虫叮咬引起的各种皮肤感染。 [img=,193,127]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260834522166_2994_2222981_3.gif!w193x127.jpg[/img] [img=,140,64]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260834520028_3541_2222981_3.gif!w140x64.jpg[/img] 林可霉素 利多卡因 Lincomycin Lidocaine M.W.: 406.54 M.W.: 234.34客户提供林可霉素利多卡因凝胶样品,希望本实验室帮忙通过筛选色谱柱及调节分析条件,依据[color=#ff0000][b]国家药品标准WS-10001-(HD-0140)-2002[/b][/color]方法,实现林可霉素利多卡因凝胶样品的良好分析。首先,使用能在纯水条件下稳定使用的高极性色谱柱[color=#ff0000][b]CAPCELL PAK C[sub]18[/sub] AQ S5 4.6 mm i.d. × 150 mm[/b][/color],对林可霉素利多卡因凝胶样品进行分析,结果如图1所示,[color=#330099]利多卡因与其峰后杂质之间分离度为1.77[/color]。[align=center][img=,690,437]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260858200006_8607_2222981_3.png!w690x437.jpg[/img][/align][align=center]图1 CAPCELL PAK C[sub]18 [/sub]AQ分析所得色谱图[/align]注:峰上标数字为分离度。[img=,528,205]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260858202566_2695_2222981_3.png!w528x205.jpg[/img]为进一步提高利多卡因与其峰后杂质之间的分离度,在原条件基础上将柱温由30℃降低至25℃,并分别使用 CAPCELL PAK C[sub]18[/sub] AQ、CAPCELL PAK C[sub]18[/sub] MG及高含碳量ODS色谱柱SUPERIOREX ODS进行分析,结果如图2所示。[align=center][img=,690,490]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260859201516_7229_2222981_3.png!w690x490.jpg[/img][/align][align=center]图2 25℃条件下不同色谱柱分析结果对比[/align]注:峰上标数字为分离度。[img=,637,223]http://ng1.17img.cn/bbsfiles/images/2018/07/201807260859204236_7198_2222981_3.png!w637x223.jpg[/img]如图2所示,在柱温25℃条件下使用三款色谱柱进行分析,其中,[color=#ff0000][b]CAPCELL PAK C[sub]18[/sub] AQ色谱柱分析结果最好,利多卡因与其峰后杂质分离得到最佳分离,分离度为4.23[/b][/color];[color=#330099][b]使用CAPCELL PAK C[sub]18[/sub] MG色谱柱进行分析时,利多卡因与其峰后杂质分离度为3.27[/b][/color];而使用SUPERIOREX ODS色谱柱分析时,利多卡因与其峰后杂质未得到有效分离。综上,在国家药品标准WS-10001-(HD-0140)-2002方法基础上,将色谱柱柱温由30℃降低至25℃,使用高极性色谱柱CAPCELL PAK C[sub]18[/sub] AQ及中等极性色谱柱CAPCELL PAK C[sub]18[/sub] MG进行分析,均可在25 min内完成林可霉素利多卡因凝胶样品的分析,并得到利多卡因与其峰后杂质之间的良好分离结果。[align=right][/align][align=right][/align][align=right] [/align][align=right]三耀精细化工品销售(中国)有限公司[/align][align=right]技术开发部[/align][align=right]地址:北京经济技术开发区宏达南路5号[/align][align=right]宏达利德工业园1栋418室[/align][align=right]邮编:100176[/align]
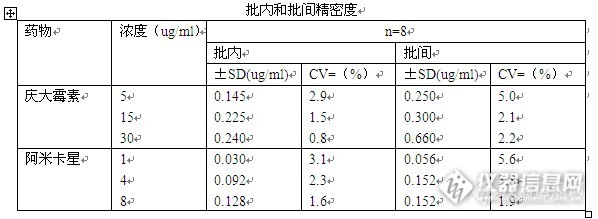
高效液相色谱法快速测定血清中的庆大霉素和阿米卡星庆大霉素和阿米卡星是用于严重革兰氏阴性细菌感染治疗的氨基糖苷类抗生素。像其他氨基糖苷类抗生素一样,庆大霉素和阿米卡星的有效治疗范围狭窄容易导致肾脏毒性和耳毒性。因此,监测庆大霉素和阿米卡星血清中的水平对于安全和有效的临床应用十分重要。最近,高压液相色谱法已被报道用于氨基糖苷类抗生素的测定。多数测定需要柱前或柱后衍生荧光检测。这些方法涉及耗时的预处理,如血清中氨基糖苷类抗生素的柱萃取以及溶剂。本实验开发了一种较为简单的预处理方法来测定血清中的庆大霉素和阿米卡星,并与荧光偏振免疫测定法进行了比较。材料和方法:庆大霉素和阿米卡星购自药店,邻苯二甲醛(瑞尔丰化工),2-巯基乙醇、庚烷磺酸钠、1,2-乙烷二磺酸二钠、色谱乙腈、蒸馏水。蛋白质沉淀剂(10mM辛烷磺酸钠溶解于3.5%高氯酸中)。庆大霉素的流动相为含有22 mM的1,2 - 乙烷二磺酸二钠和5mM辛烷磺酸钠的水 - 乙腈混合物(80:20,体积/体积),用乙酸调节pH至约3.5。阿米卡星的流动相为含有37 mM的1,2 - 乙烷二磺酸二钠和5mM辛烷磺酸钠的水 - 乙腈混合物(80:20,体积/体积),用乙酸调节pH至约3.5。仪器和色谱条件:安捷伦高效液相色谱仪1200,UV检测器,色谱柱:安捷伦Agilent液相色谱柱4.6﹡150﹡5u,流动相的流速保持在1毫升/分钟。邻苯二甲醛试剂用泵以0.6毫升/分钟的流速。实验部分:将50ul血浆加入到50ul蛋白质沉淀剂,涡旋混合数秒后,使用KM-15200离心机离心2分钟(15000rpm),离心后上清液进样。正常血清,分别加入已知量的庆大霉素和阿米卡星,进行分析,根据加入量和峰面积绘制标准曲线。荧光偏振免疫通过市售的试剂盒进行。结果:图1为庆大霉素的标准色谱图,庆大霉素加入对照血清的色谱图以及对照血清的色谱图。(其中交标庆大霉素的含量为15ug/ml)http://ng1.17img.cn/bbsfiles/images/2014/09/201409300949_516466_2188679_3.jpg图2为阿米卡星的标准色谱图,阿米卡星加入对照血清的色谱图以及对照血清的色谱图,经过蛋白质沉淀剂处理后的血清和未处理的色谱图基本形同,皆未见到影响抗生素检测的干扰杂质峰。http://ng1.17img.cn/bbsfiles/images/2014/09/201409300949_516467_2188679_3.jpg以峰面积作为纵坐标,血清中的药物浓度为横坐标得到庆大霉素的线性标准曲线(3-50ug/ml)为y =0.979x - 0.006,阿米卡星的线性标准曲线(0.5-10ug/ml)为y= 0.998x - 0.04根据庆大霉素和阿米卡星在血清中不同浓度的重复测定,得到庆大霉素和阿米卡星的批内变异系数分别为0.8 -2.9%和1.6-3.1%,批间变异系数为2.0-5.0%及1.9-5.6%。http://ng1.17img.cn/bbsfiles/images/2014/09/201409300949_516468_2188679_3.jpg回收率试验:分别将15ug/ml的庆大霉素水溶液加入含有15ug/ml阿米卡星的血清中和将4ug/ml的阿米卡星水溶液加入4ug/ml的血清中。将它们的峰面积进行比较。基于三个样品的平均值,庆大霉素和阿米卡星的分别为99.0%和98.5%.通过该方法获得的结果与用荧光偏振免疫测定法进行了比较,回归方程和相关系数分别为庆大霉素:y=1.027x - 1.090,n =44和r=0.996。阿米卡星y=0.998x - 0.206, n =42和r=0.957。讨论:本实验采用了蛋白质沉淀剂,排除干扰物,再将样品进行分析,优化的分析方法与荧光偏振免疫测定法进行了比较种,该方法方法的优点是速度快,操作简便,重复性好。因此,该方法可用于该药物的分析。
用检测卡检测β-内酰胺酶时,对样品有哪些要求?

[img=,690,293]https://ng1.17img.cn/bbsfiles/images/2019/04/201904251447420218_6149_3859729_3.jpg!w690x293.jpg[/img]简介树莓派是一种单板式计算机系统,可轻松连接鼠标、键盘、显示器等外设,并运行基于Linux的操作系统,低于300人民币的成本,使树莓派尤其适用于注重性价比的数据采集应用。现在,Measurement Computing大部分USB、以太网和蓝牙数据采集设备已兼容树莓派。目的在树莓派上运行应用程序,控制MCC DAQ设备执行数据采集任务。本文详细介绍了以下关键步骤:格式化SD卡安装操作系统配置树莓派安装Linux设备驱动安装MCC DAQ设备驱动,编译MCC提供的测试程序运行MCC测试程序适用人群工作于树莓派(Linux)平台,熟悉MCC数据采集卡,并希望在此平台上实现数据采集功能。必要条件请预先准备以下内容:树莓派硬件板卡(本文使用model B,您可根据实际情况,使用任何型号)SD卡(8GB或更大容量)PC 或 Mac,可接入互联网以太网电缆或无线适配器显示器或电视机供电电源鼠标或轨迹球键盘MCC DAQ设备(本文使用USB-1608FS)了解支持Linux和兼容树莓派的MCC数据采集卡:建议使用自供电USB Hub连接外设与树莓派。下图展示了本文所用到的树莓派的配置:[img=,552,370]https://ng1.17img.cn/bbsfiles/images/2019/04/201904251447537408_8528_3859729_3.jpg!w552x370.jpg[/img]鼠标和键盘通过USB Hub连接树莓派,并未在上图中显示。安装操作系统使用树莓派前必须安装操作系统。本文将安装Raspbian,基于Debian的开源操作系统,针对树莓派进行了大量优化,并通过NOOBS(New Out Of the Box Software)完成Raspbian的安装,NOOBS是树莓派官方发布的开源操作系统安装管理器。借助SD卡拷贝NOOBS至树莓派,首先需要格式化SD卡,请参考以下详细步骤:以下步骤将引领您下载NOOBS,并在树莓派上安装操作系统:1、访问 www.sdcard.org,点击Download2、下载页面底部的SD formatter for Windows or Mac3、将SD卡插入PC或MAC,运行setup.exe,格式化SD卡安装操作系统以下步骤将引领您下载NOOBS,并在树莓派上安装操作系统:1、点击Downloads。击NOOBS下的Download ZIP,保存至PC或MAC2、解压zip文件,拷贝所有文件至SD卡3、拔出SD卡,将其插入树莓派4、连接显示器、鼠标、键盘和电源上电后树莓派立即启动首先会看到树莓派的Logo,后面是NOOBS主窗口,列出了全部可安装的操作系统5、选中Raspbian复选框,点击Install,在Confirm对话框中选择Yes安装进度将实时显示6、选择OK,树莓派开始加载Raspbian首次引导Raspbian,将弹出Setup Options菜单,通过键盘上的方向按键进行操作7、根据需要配置相关选项,如语言、区域设置等8、配置完成后,切换至并按下命令行提示:pi@raspberrypi~$恭喜您!至此已成功为树莓派安装了操作系统。登陆信息每次启动树莓派,都将提示以下登陆信息:raspberrypi login: pipassword: raspberry命令行提示:pi@raspberrypi~$检查网络连接在树莓派上下载MCC驱动程序前,请确认树莓派网络连接正确。可以通过以太网电缆或USB WiFi适配器连接网络,本文使用WiFi适配器。1、双击桌面上WiFi Config图标,配置无线网络连接。Adapter:列出全部USB无线适配器(如wlan0) the Network:空2、点击Scan,查看可用的无线网络3、双击service set identifier (SSID)中待连接的无线网络4、验证当前窗口中的Authentication 和 Encryption,在PSK (pre-shared key)中输入密码5、点击Add 配置程序将自动连接至无线网络6、重新启动树莓派,并输入上述登陆信息登录之后,命令会立即显示pi@raspberrypi~$.升级树莓派软件包为确保您使用的是最新的树莓派软件包,输入以下命令sudo apt-get update下载 MCC的Linux驱动MCC USB,蓝牙和以太网设备的Linux驱动程序保存在GitHub中。登录到Git库,下载最新的驱动软件包。1、登录GitHub网页,获取Raspberry Pi的驱动:2、点击下载按钮,选择下载压缩包3、使用以下命令安装解压缩使用程序:sudo apt-get install unzip4、在终端窗口中,找到到下载目录(使用cd命令),并将驱动程序文件解压缩到home / pi目录:unzip Linux_Drivers-master.zip -d ~piMCC驱动程序将持续保持更新,以支持更多设备。单击下面的设备类型以转到安装驱动程序的过程:USBBluetoothEthernet安装MCC USB设备的Linux驱动,编译测试程序在变异USB驱动之前,您必须安装与USB设备通讯所需的软件包1、下载并安装libusb和libudev开发软件包libusb为USB设备提供了通用C语言库sudo apt-get install libusb-1.0-0 libusb-1.0-0-dev2、拷贝USB规则文件到如下路径/etc/udev/rules.d,将它重命名为99-mcc.rules (避免了树莓派上标准命名问题):sudo cp 61-mcc.rules /etc/udev/rules.d/99-mcc.rules3、将hidapi GIT存储库克隆到home / pi目录中HIDAPI需要与人机接口设备(HID)连接。git clone git://github.com/signal11/hidapi.git4、按照hidapi README.txt中的说明安装hidapi库:a. 安装autotools,这是一套编程工具,旨在帮助将源代码包移植到类Unix系统。autotools包是构建hidapi库所必需的。sudo apt-get install libudev-dev libfox-1.6-dev autotools-dev autoconf automake libtoolb. 编译hidapi库:cd ~pi/hidapi./bootstrap./configuremakesudo make install5、重启树莓派,根据提示输入登录信息6、安装Linux驱动。输入以下代码,安装USB驱动并编译测试应用程序:cd ~pi/usb/mcc-libusbmakesudo make installsudo ldconfig安装MCC USB设备的Linux驱动,编译测试程序执行以下步骤下载蓝牙库并编译蓝牙驱动程序。在执行此过程之前,请确保您已经使用“下载第三方MCC Linux驱动程序”程序下载了蓝牙驱动程序.1、安装蓝牙库要编译蓝牙库,您需要添加bluez-libs-devel软件包。sudo apt-get install libbluetooth-dev bluez-tools2、编译蓝牙驱动cd ~pi/Bluetoothmakesudo make install键入ls以列出所有文件。3、使用MCC蓝牙DAQ设备运行示例测试应用程序a. 插入MCC蓝牙设备。b. Enter the name of a test program exactly as it is written, for example:./test-bth1208LS测试应用程序将显示您可以执行的测试列表。c. 输入要执行的命令的字母。安装以太网Linux驱动程序并编译测试程序执行以下步骤编译以太网驱动程序。在执行此过程之前,请确保您已使用“下载第三方MCC Linux驱动程序”过程下载了以太网驱动程序。1、编译驱动cd ~pi/Ethernetmakesudo make install键入ls以列出所有文件。MCC以太网设备需要通过网络路由器进行连接。2、使用MCC以太网DAQ设备运行示例测试应用程序。a. 插入您的以太网设备b. 输入完整的测试程序名称,例如:cd ~pi/usb./test-E-1608测试应用程序将显示您可以执行的测试列表。c. 输入要执行的命令的字母。MCC测试程序为Linux而开发的测试程序支持大部分MCC USB设备。程序将执行模拟通道、计数器通道和数字通道的数据采集,同时测试设备功能以及显示设备信息。测试程序详见USB/Mcc-libusb,Bluetooth,Ethernet文件夹,程序命名涵盖对应的设备型号,若设备从属于某系列,则此程序支持该系列全部设备,运行程序时,务必按照所列设备名称,正确键入设备名。例如,使用USB-1608GX-2AO时,请运行程序”test-usb1608G”。在树莓派上运行MCC DAQ设备测试程序前往mcc-libhid目录,在命令提示符(pi@raspberrypi~)后输入以下命令,运行USB-1608FS测试程序:cd ~pi/mcc-libusb./test-usb1608FS测试程序首先检测设备,并创建一张包含设备模拟输入校准参数(斜率和偏移)的表格。[img=,544,408]https://ng1.17img.cn/bbsfiles/images/2019/04/201904251448137362_8213_3859729_3.jpg!w544x408.jpg[/img]表格建立完毕后,将显示全部可执行的设备测试功能[img=,336,228]https://ng1.17img.cn/bbsfiles/images/2019/04/201904251448282996_9123_3859729_3.jpg!w336x228.jpg[/img][img=,336,228]https://ng1.17img.cn/bbsfiles/images/2019/04/201904251448282996_9123_3859729_3.jpg!w336x228.jpg[/img]每项测试功能都有对应的热键,敲击键盘即可执行测试任务,程序有可能提示您输入更多信息,如通道数或频率大小,程序执行结果将打印在显示器上。如需了解更多内容请关注嘉兆科技
买来的农药毒死蜱-辛硫磷,根据农药的含量配成了0.5mg/kg, 5mg/kg,50mg/kg, 500mg/kg, 1000mg/kg五个浓度,每个浓度直接滴在农残速测卡上一滴,另加洗脱液一滴,发现浓度为50mg/kg 时才检出。这个检出限也太高了吧,早就超标N倍了。大家有没有用过农残速测卡的??这些快检的手段可信度有几何??各位发表一下意见,互相交流一下吧
β-内酰氨酶检测卡,哪里有卖?在检测过程中,要注意哪些?
各位大神,早上好!有个问题想请教下。我用速测仪检测生菜、菜心、葱、芥菜、西兰花等,检测第一次,抑制率为0,第二批样品检测,抑制率几乎都超过50,第二次检测,两批样品都不合格。之后,我用速测卡来测,都变蓝。刚开始以为是试剂过期、底物放多、比色皿没擦干净,但排除这些原因,还是不合格?难道是速测仪不灵敏了?坏了?请大神指教
一阶导数分光光度法测定盐酸普鲁卡因溶液的含量刘素琴(江苏省金坛市人民医院,江苏 金坛 213200)联系电话:0519-2266680 E-mail:Liusuqin666@163.com 文章编号:04040399摘要 目的:改进盐酸普鲁卡因溶液的含量测定方法。 方法:以一阶导数光谱在308.0nm波长处谷—零间的振幅为定量依据,测定盐酸普鲁卡因溶液的含量。结果:盐酸普鲁卡因溶液浓度在5~30μg/mL范围内与一阶导数谷—零间的振幅呈良好的线性关系,r=0.9999,平均回收率为100.04%,RSD=0.43%。结论:方法简便、准确,可用于测定盐酸普鲁卡因溶液的含量。关键词 一阶导数; 分光光度法; 盐酸普鲁卡因 ;含量[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=32338]一阶导数分光光度法测定盐酸普鲁卡因溶液的含量[/url]
[font=宋体][color=#222222]1.卡波姆凝胶性质[/color][/font][font=宋体][color=#222222]受到[/color][/font][font=宋体][color=#222222]PH值的影响[/color][/font][font=宋体][color=#222222][font=宋体]因为卡波姆聚合物有大量的游离羧基,所以[/font][font=宋体]pKa值通常很小。如果介质的pH小于4,羧基很少分离,pH大于4,羧基开始分离,聚合物溶解,粘度增加,pH值为8[/font][/color][/font][font=宋体][color=#222222]时[/color][/font][font=宋体][color=#222222],则基本[/color][/font][font=宋体][color=#222222]全部[/color][/font][font=宋体][color=#222222]分离,粘度最大。[/color][/font][font=宋体][color=#222222][font=宋体]介质[/font][font=宋体]pH值也影响卡波姆凝胶的粘附性,当pH值低于pKa时,凝胶的结合能力强,粘附性[/font][/color][/font][font=宋体][color=#222222]就会加大[/color][/font][font=宋体][color=#222222][font=宋体]。同时介质的离子强度可以改变卡波姆凝胶对[/font][font=宋体]pH值的敏感性,当离子强度较高时,卡波姆容易释放质子,其pKa值[/font][/color][/font][font=宋体][color=#222222]降低[/color][/font][font=宋体][color=#222222][font=宋体],因此可以在较低的[/font][font=宋体]pH值下溶解。[/font][/color][/font][font=宋体][color=#222222]2.卡波姆凝胶性质[/color][/font][font=宋体][color=#222222]受到[/color][/font][font=宋体][color=#222222]离子强度的影响[/color][/font][font=宋体][color=#222222][font=宋体]在一些药物中,药物对凝胶周围介质的[/font][font=宋体]pH值和离子强度的影响也不容忽视。药物的酸性也影响凝胶的性质,因此酸性药物的作用更加明显。[/font][/color][/font][font=宋体][color=#222222]3.卡波姆凝胶性质[/color][/font][font=宋体][color=#222222]受到[/color][/font][font=宋体][color=#222222]其他辅料的影响[/color][/font][font=宋体][color=#222222][font=宋体]在卡波姆凝胶中同时使用聚乙烯吡咯烷和聚氧乙烯作为助剂,可以降低卡波姆凝胶的黏膜粘附力,这种减少与共存辅料的浓度和分子量有关,辅料浓度高[/font][font=宋体](5%)可以大大降低卡波姆凝胶的粘附力,浓度降至0.5%的话,影响较小。通常,介质的pH值不会改变聚乙烯吡咯和聚氧乙烯的这一特性。硬脂酸镁具有疏水性,因此也能降低卡波姆凝胶的粘附性。[/font][/color][/font]
安捷伦G1888又卡瓶了,烦死了,有什么好方法没啊,我用的可是原装瓶啊
安捷伦G1888又卡瓶了,烦死了,有什么好方法没啊,我用的可是原装瓶啊
1.碳和氢 碳是煤中最重要的组成元素.碳含量(Cr)随煤化程度的升高而增加.泥炭的Cr为50~60% 褐煤为60~77% 烟煤为74~92% 无烟煤为90~98%.在煤化程度相同的煤中,丝质组的Cr最高,镜质组次之,稳定组最低.氢中煤中第二个重要的组成元素.腐泥煤的氢含量(HR)比腐植煤高,一般在6%以上,有时达11%,这是由于形成腐泥煤的低等生物富含氢.在腐植煤中,稳定组的HR最高,镜质组次之,丝质组最低.随煤化程度升高,它们的HR均逐渐减少. 2.氮 煤中的氮,主要是由成煤植物中的蛋白质转化而来.人们认为煤中的氮通常都是有机氮,其中有一些是杂环形的. 煤中的NR通常约为0.8~1.8%,但也随煤公程度的升高而略有下降.我国弱粘结煤和不粘结烟煤的NR多低于1%,可能是在泥炭化阶段受到不同程度的氧化作用,成煤植物中的蛋白质氧化分解,故NR普遍较低. 3.氧 氧是煤中主要元素之一,氧在煤中存在的总量和形态直接影响着煤的性质.
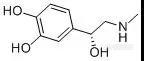
复方盐酸阿替卡因注射液为复方制剂,是盐酸阿替卡因与肾上腺素的灭菌水溶液,作为口腔用局部麻醉剂,适用于涉及切骨术及粘膜切开的外科手术过程。[img=,144,61]https://ng1.17img.cn/bbsfiles/images/2019/03/201903191545418661_4518_2222981_3.jpg!w144x61.jpg[/img][color=black] [/color][color=#3e3e3e]肾上腺素 L(-)-Epinephrine M.W. : 183.2 [/color][b]在国家药品标准(YBH17082004-2015Z)[/b]中,在对复方盐酸阿替卡因注射液中肾上腺素进行分析时,使用[b]甲醇-水[/b]进行梯度洗脱,但由于[b]肾上腺素极性较强[/b],即使初始梯度为纯水相条件,肾上腺素仍紧邻死时间出峰,[b]保留不佳,易受到溶剂峰干扰,无法进行准确定量。[/b]我们分别尝试使用反相柱CAPCELL PAK C18 MGII加离子对试剂,以及直接使用离子交换色谱柱CAPCELL PAK SCX UG80两种方式,对复方盐酸阿替卡因注射液中肾上腺素和硫酸肾上腺素进行保留分析(复方盐酸阿替卡因注射液由客户提供)。CAPCELL PAK C18 MGII液相色谱柱,其采用高纯度硅胶作为基质,通过减少硅胶微细孔的数量来增大有效比表面积;并且采用新包被技术Ultimate Polymer Coating,实现了对硅醇基极大程度的封锁,兼具分离性能和普适性能,通用性非常好。CAPCELL PAK SCX UG80是强阳离子交换柱,使用高纯度硅胶,填料中金属杂质很少,使配位化合物的吸附得到了极大程度抑制,兼具聚合物和硅胶填料的优点。[b][color=#0070c0]实验方法[/color][color=#0070c0]方法一[/color][color=#0070c0]使用[/color][color=#0070c0]CAPCELL PAK C18MGII[/color][color=#0070c0]色谱柱[/color][color=#0070c0]+[/color][color=#0070c0]离子对试剂[/color][/b]如图1,对肾上腺素对照品溶液进行分析,肾上腺素主峰保留时间为5.69 min,拖尾因子为1.19,理论塔板数为12538。在相同色谱条件下,尝试对亚硫酸肾上腺素标准品及注射液中的亚硫酸肾上腺素进行分析。如图3,亚硫酸肾上腺素标准品溶液能够得到良好分析结果,注射液(客户提供的样品)中未明显见亚硫酸肾上腺素出峰,保留时间为3.55min,拖尾因子为1.14,理论塔板数为14955。[b][color=#0070c0]方法二[/color][color=#0070c0] CAPCELL PAK SCX UG80[/color][color=#0070c0]色谱柱[/color][/b][color=#000000]考虑到使用离子对试剂的流动相条件具有流动相配制麻烦、有损色谱柱寿命、平衡时间长等缺点,我们也尝试使用键合磺酸基团的强阳离子交换柱 ——CAPCELL PAK SCX UG80进行分析。[/color][color=#000000]如图4,在流动相中添加磷酸二氢铵,通过对盐浓度进行调整,在5 mmol/L磷酸二氢铵(磷酸调pH=2.5)条件下,亚硫酸肾上腺素保留时间为3.32 min,然而出现峰形拖尾现象,拖尾因子为2.0,不如CAPCELL PAK C18 MGII色谱柱添加离子对试剂所得分析结果好。[/color][align=center][/align][align=left][img=,400,284]https://ng1.17img.cn/bbsfiles/images/2019/03/201903191547381421_926_2222981_3.jpg!w584x416.jpg[/img] [img=,400,276]https://ng1.17img.cn/bbsfiles/images/2019/03/201903191548310561_8067_2222981_3.jpg!w572x395.jpg[/img][/align][align=left][img=,400,166]https://ng1.17img.cn/bbsfiles/images/2019/03/201903191547576748_522_2222981_3.jpg!w612x254.jpg[/img] [img=,400,167]https://ng1.17img.cn/bbsfiles/images/2019/03/201903191548525761_4184_2222981_3.jpg!w624x262.jpg[/img][/align][align=left]图1 MGII分析肾上腺素对照品溶液结果(离子对条件) 图2 MGII分析注射液结果(离子对条件)[/align][align=center][/align][img=,400,258]https://ng1.17img.cn/bbsfiles/images/2019/03/201903191550354951_2539_2222981_3.jpg!w644x416.jpg[/img] [img=,400,250]https://ng1.17img.cn/bbsfiles/images/2019/03/201903191555486850_3396_2222981_3.jpg!w644x403.jpg[/img][img=,400,147]https://ng1.17img.cn/bbsfiles/images/2019/03/201903191551260881_9828_2222981_3.jpg!w696x256.jpg[/img] [img=,400,164]https://ng1.17img.cn/bbsfiles/images/2019/03/201903191556163846_9739_2222981_3.jpg!w632x260.jpg[/img][align=left]图3 MGII分析亚硫酸肾上腺素标准品和注射液结果(离子对条件) 图4 SCX UG80分析亚硫酸肾上腺素对照品溶液和供试品溶液[/align][align=left][/align][align=left]综上实验结果,使用中等极性色谱柱CAPCELL PAK C18 MGII S5 4.6 mm i.d. × 250 mm,在流动相中添加5 mM辛烷磺酸钠、30°C柱温条件下进行梯度洗脱,能够实现复方盐酸阿替卡因注射液中肾上腺素和亚硫酸肾上腺素的良好保留与分析。[/align][b][color=#0070c0][/color][/b][align=left][b][color=#0070c0] [/color][color=#0070c0] [/color][/b][/align]
有没有维生素类样品中辅酶Q10的液相检测色谱条件?
谁有蓝莓花青素液相色谱图?求一张
公司作克林酶素磷酸酯,分析过程依据药典,使用ZOBARX C8分析,可分离效果很不理想.不知大家有没有做相同产品的,使用的什么柱子,最好有谱图,谢谢了.
如题, 有做金葡菌 肠毒素监测的没,分享下子,最近想开展这个实验来着。

按领导要求,对市场上的蔬菜进行农药残留检测,现记录其中一次检测过程: 首先到各个菜市场去采集蔬菜样品,分别包装好带回实验室。然后就可以开始检测工作了,具体步骤如下:1、开机及设置接通电源,打开仪器后面的开关按钮即可开启仪器,设置反应温度40℃,反应时间10min,显色时间3min,仪器开启后立即加热,最后保持恒定温度40℃。2、速测卡片安装将速测卡对折后再展开、撕去盖膜,插入压纸条下的各通道加热板上。3、待测样品处理擦去蔬菜表面的泥土或是杂物,选择有代表性的菜叶尖5g,放入小烧杯中,用剪刀剪成1cm左右见方碎片,加入10mL纯净水,置于超声波清洗器中震荡2分钟,每批需要做一个纯净水的空白对照。用吸管吸取样品液2~4滴加到速测卡的白色药片上进行测试。4、样品测试在速测药片装好并已加了待测液后,按键,反应开始倒计时10分钟,此时为药物反应时间,当听到仪器发出关闭上盖提示音后关闭上盖,显色自动开始倒计时3分钟,显色结束时仪器再次发出打开上盖提示音,这时打开仪器上盖,进行结果判定。5、结果判定样品测试卡与空白对照卡比较,白色药片不变色或略有浅蓝色均为阳性结果,不变蓝为强阳性结果,说明农药残留量较高,显浅蓝色为弱阳性结果,说明农药残留量相对较低。白色药片变为天蓝色或与空白对照卡相同,为阴性结果。(结果如下图)http://ng1.17img.cn/bbsfiles/images/2014/12/201412111034_526668_2175233_3.jpg最后一个为空白对照卡,10个样品中有两个农残超标,看来食品安全问题还是蛮严重的。
请问国外有没有农药残留速测卡?好像比较少报道哦
有知道韩国美卡希斯的么?他们的快速检测组合怎么样?看起来蛮全的,就是不知道质量则么样?好用不?
[color=#333333]农药残留速测卡检测原理是什么?[/color]
[size=16px][color=#ff0000][b][url=https://www.instrument.com.cn/job/position-79168.html]立即投递该职位[/url][/b][/color][/size][b]职位名称:[/b]化学工程师[b]职位描述/要求:[/b]职位描述:1、按照国家标准、行业标准等对仪器的计量性能进行检测;2、负责部分检测项目的样品前处理;3、对检测结果进行数据分析;4、对检测操作过程中出现的问题进行有效分析,有自主解决问题的能力;5、对检测数据记录、汇总,并及时形成完整的、准确的、规范的原始记录归档;6、按照规程要求完成实验室常规操作,包括标准溶液配制、实验室5S管理等;7、完成主管安排的其他工作;任职要求:1、化学相关专业,本科以上学历,从事化学行业两年以上工作经验;2、熟悉掌握化学分析方法,对常用的化学分析仪器(AFS [url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]AAS[/color][/url] [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]IC[/color][/url] LC HP[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]LC-MS[/color][/url] [url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]IC[/color][/url]P FTIR的其中一种),会熟练使用者优先;3、具有较强的分析能力和解决问题能力,善于沟通和表达;4、有分析实验室、化学实验室、熟悉光谱类仪器原理及使用方法等工作经验优先考虑;[b]公司介绍:[/b] 苏州卡美利多仪器有限公司是专业从事实验室科学仪器研发、生产、销售、服务、具有自主知识产权的高新技术企业。卡美公司是一家高科技创业型企业,卡美的创业理念“科技点燃梦想,创新引领未来”,并以此为企业宗旨,不断探究、果敢创新。特别是在分析测试仪器领域,不断开发出先进的产品,使卡美成为优质仪器资源的供应商和领导者。公司现在的主要产品是元素分析仪,目前我们的产品已广泛应用于有机化学、无机化学、生物化学、医...[url=https://www.instrument.com.cn/job/position-79168.html]查看全部[/url][align=center][img=,178,176]https://ng1.17img.cn/bbsfiles/images/2021/08/202108160948175602_3528_5026484_3.png!w178x176.jpg[/img][/align][align=center]扫描二维码,关注[b][color=#ff0000]“仪职派”[/color][/b]公众号[/align][align=center][b]即可获取高薪职位[/b][/align]
这里有很多做农残的,其中做快速检测的人也不少,大家有没用过一种叫做农药速测卡的东东,好用否。。。。
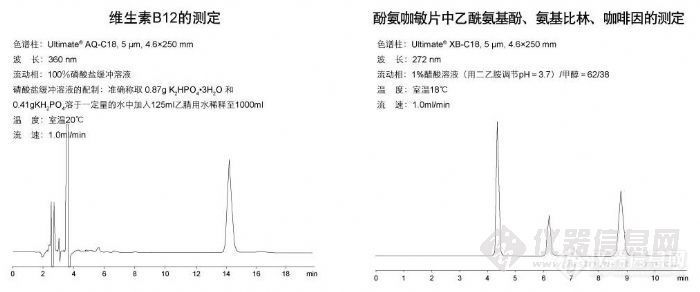
维生素B12的测定和酚氨咖敏片中乙酰氨基酚、氨基比林、咖啡因的测定http://ng1.17img.cn/bbsfiles/images/2009/11/200911021850_180185_1896702_3.jpg
酶制剂的酶活测定方法及影响因素随着我国畜牧业的发展和生物工程技术的不断进步,酶制剂在饲料工业中的应用越来越普遍。由于酶制剂能够消除饲料中的某些抗营养因子的负面作用,提高饲料消化率,改善动物生产性能,降低生产成本,因此日益受到饲料界的重视。但是,由于酶制剂来源比较复杂、分子结构不明确,分离提纯困难等多种原因,使这类产品有国家标准的不多,即使有国标也存在一些问题。给广大养殖用户和生产企业带来很大不便。本文简要介绍一下常用的酶活测定方法及测定过程的影响因素,仅供广大饲料工作者提供参考。1 酶制剂的定义及分类所谓的酶制剂就是通过产酶微生物发酵工程或含酶的动、植物组织提取技术生产加工而成,具有一种或多种底物清楚的酶催化活性,有助于改善动物对饲料营养成分的消化、吸收等,并有功效的生物学评定依据,符合安全性要求,作饲料添加剂用的酶制剂产品(NY/T 722-2003)。工业上应用的酶制剂大多为水解酶,按作用底物的不同,可分为淀粉酶、蛋白酶、脂肪酶、植酸酶、木聚糖酶、果胶酶、葡聚糖酶、纤维素酶等。按动物体内是否分泌,分为消化酶和非消化酶两大类。消化酶指动物自身能够分泌的淀粉酶、蛋白酶和脂肪酶等,在幼龄动物或特殊生理阶段时,动物也存在消化酶分泌不足需要外源供给的情况。非消化酶是指动物自身不能够分泌或很少分泌,必须由外源供给的酶,这类酶能消化动物自身不能消化的物质或降解一些抗营养因子,主要有植酸酶、木聚糖酶、果胶酶、葡聚糖酶、纤维素酶等。2 常见的酶活测定方法通常酶制剂活性的检测是采用实验室分析手段来进行评价,它可以用来筛选优质酶制剂、确定复合酶制剂的最佳组方及确定产品的最佳添加量等,酶制剂实验室评价技术是目前饲料厂家应用最为广泛的一种方法。其操作相对简单,检测所用时间短,便于生产实践应用。酶活测定结果虽不能完全反映酶的使用效果,但通过检测至少可以避免使用劣质的酶制剂。我国饲料工业标准中已经确立了饲用植酸酶(GB/T 18634)、纤维素酶(NY/T912)、β-葡聚糖酶(NY/T 911)的测定方法。另外,许多企事业单位为了生产研究的需要也制定了很多用于各种酶制剂活力的测定方法。目前测定酶制剂活性的方法主要有:2.1 比色法比色法是以反应生成有色化合物的显色反应为基础,通过比较或测量有色物质溶液颜色深度来确定待测组分含量的方法,根据原理不同可分为还原糖法和色原底物法。2.1.1 还原糖法 这种方法是通过酶作用于化学合成或从自然界提取出来的底物来进行测定的。非淀粉多糖酶与底物在特定的条件(温度、pH值和底物浓度)下反应,反应产物为还原糖,在与显色剂反应后,通过比色确定还原糖的生成量,同时制作标准曲线。酶的活性表示为单位时间产生一定浓度的产物所需要的酶量(mg 或mL)。该法可适用于大部分酶活力的测定,如淀粉酶、蛋白酶、脂肪酶、植酸酶、木聚糖酶、果胶酶、β-葡聚糖酶、纤维素酶等的测定。根据显色剂的不同又可分为DNS 法、钒钼酸铵法和地衣酚法。其中DNS 法由于操作简单、显色稳定,是目前众多实验室和饲料企业在测定非淀粉多糖酶时应用最多的测定方法。2.1.2 色原底物法 原理是利用人工合成的含色原基团的底物在酶的作用下释放出有色物质,利用分光光度计比色测定有色物质的含量计算酶活。如木聚糖酶活力的测定。该法操作简单、重现性好,但酶作用于合成底物与天然底物的效果有一定区别,用合成底物测定的酶活并不能代表酶制剂在应用于天然饲料时所能发挥的酶活大小。2.2 黏度法这种方法是根据酶能够降低一定浓度的标准底物(控制pH值、温度等条件)的黏度的能力来确定酶的活性。利用的底物主要有化学合成的底物(如CMC 用于纤维素酶的测定) 和自然提取的底物(如小麦阿拉伯木聚糖用于木聚糖酶的测定)。测定的酶的活性值是通过与同时测定的标准酶活性的比较,来确定酶的活性。该法可用于木聚糖酶、β-甘露聚糖酶、β-葡聚糖酶等酶活测定。这种方法的特点是通过降低底物的粘度来反映酶的活性,这也正是酶在体内起作用的重要特征。该法虽然灵敏度较高,但重现性差,操作复杂费时,应用难于普及。2.3 免疫学法用于酶活性分析的免疫学法包括ELISA 法和免疫凝胶扩散法。这两种方法是根据酶与抗体之间发生反应,然后ELISA 法通过第二步反应,凝胶扩散法则通过印染过程来确定酶的活性。这些方法非常灵敏,能够检测到极低水平的酶蛋白。但它们的缺点是对于每个产品的酶需要特殊的抗体,另外抗体能够与非酶蛋白质发生反应。由于抗体本身所用的蛋白质是特定的,因此,由不同生产者生产的同种类型的酶之间是没有交叉性的。另外,采用实验动物的敏感性也值得探讨。2.4 凝胶扩散法这种方法是将酶作用的底物与某种凝胶混合后倒入培养皿中,凝固之后,在凝胶上切开一条凿,倒入标准酶液和测试酶液。培养一定时间后,在切开的凝胶周围能够看到水解区域,区域的大小与酶的含量成正比。在某些情况下,还可以再加入其他试剂来显示水解的区域。如木聚糖酶活力的测定。这种方法虽然简单,但培养时间长。因为这种方法是根据区域的大小来确定酶的活性,所以其准确性要低于其他非扩散的方法。2.5 比浊法以酵母或酵母细胞壁在缓冲溶液中的浊度或吸光度的降低来表示酶活力,如β-葡聚糖酶活力的测定。2.6 体外模拟消化技术酶活测定毕竟不能反映外源酶在机体内真实的作用效果,因此,对于体外法评定饲料营养价值的研究不断增加。体外法评定饲料营养价值是通过模拟消化道内温度、pH、消化酶分泌、胃肠运动和养分吸收等参数,在体外建立一套与畜禽消化道内环境接近的操作程序,对饲料及酶制剂进行营养价值预测和评定。常用的体外模拟消化技术包括:①胃蛋白酶—胰酶法;②胃蛋白酶—小肠液法;③胃蛋白酶—胰酶—瘤胃液法;④胃蛋白酶—胰酶—碳水化合物酶法。由于不同的饲料用酶是不同的微生物通过发酵过程产生的,酶产品的酶学性质差别较大。并且各种微生物所分泌的酶的最佳pH 值、温度和对底物的亲和性都不相同。而目前,饲用酶除植酸酶、纤维素酶、木聚糖酶和β-葡聚糖酶有正式颁布的国标或行标酶活测定方法外,其他饲用酶制剂目前都还没有一个统一的定义及检测标准。因此,饲料厂家在比较不同厂家的酶制剂时,在没有统一的测定方法情况下,应首先确定自己认可的检测方法,然后在完全相同的测定条件进行检测,这样得出的结论才具有可比性。3 酶制剂活性测定影响因素的分析饲用酶制剂活性测定的主要影响因素有温度、pH、作用时间、底物等4大要素以及一些非定义要素,如酶液稀释度、标准曲线、显色剂、缓冲液等,下面就这几方面进行归纳分析一下:3.1 影响饲用酶制剂活性测定的四大要素所谓的酶活性就是指在特定的系统和条件下测到的反应速度。为了确保酶制剂测定结果的一致性,饲用酶制剂活性单位定义中对影响酶活大小的主要条件进行了规定,其中包括温度、pH 值、时间和底物,这些都是酶活力测定系统中最重要的因素,对酶促反应速度影响很大。3.1.1 温度对酶活测定的影响 酶制剂对温度非常敏感,在检测过程中对温度的控制则显得非常重要。温度对酶活性影响主要表现在两个方面:一方面,是当温度升高时,酶与底物的反应速率加快;另一方面,由于随着温度的升高将使酶的稳定性下降,部分酶蛋白分子逐渐变性而失去活性,引起酶反应速率下降。温度的这两种影响的综合作用而产生酶反应的“最适温度”。对于不同的酶制剂在不同的情况下最适温度是有一定的差别。研究木聚糖酶时发现,在30℃~40℃条件下酶活较稳定,50℃后随着温度的升高,酶活力开始下降,90℃时基本失活。研究纤维素酶最适酶解条件时发现,在36℃~58℃之间纤维素酶相对酶活随着温度升高而升高,当温度在58℃~62℃之间时,相对酶活性没有明显变化,曲线近似呈水平状态,在40℃、45℃、50℃条件下,其相对酶活分别为56%、70%、80%,而当温度大于58℃以上时相对酶活不再升高。同时,酶在不同条件下适宜温度也可能要受到酶的纯度、底物、激活剂、抑制剂以及酶促反应时间等因素的影响。3.1.2 pH 对酶活测定的影响 pH 值在酶活测定时对测定结果影响很大,各种酶制剂在一定条件下都有其特定的最适酶解pH,酶的最适pH 会随着底物种类和浓度、缓冲液种类和浓度的不同而改变,因此最适pH 也只有在一定条件下才有意义。pH 影响酶活力的原因可能有以下几个方面:① 过酸或过碱可以使酶的空间结构破坏,引起酶构象的改变,也影响酶活性部位催化基团和结合基团的解离状态,酶活性丧失;② 当pH 改变不是很剧烈时,酶虽未变性,但酶活受到了影响。pH 影响了底物的解离状态,或者使底物不能和酶结合,或者结合后不能生成产物。pH 影响酶分子活性部位上有关基团的解离,从而影响与底物的结合或催化,使酶活性降低可能影响到中间络合的解离状态,不利于酶解生成产物;③ pH 影响维持酶分子空间结构的有关基团解离,从而影响了酶活性部位的构象,进而影响酶的活性;④ pH 影响底物的带电状态。这些都直接影响酶和底物的亲和力,影响酶解反应速度。有文献报道,很多酶最适酶解pH 都在3.0~6.0。研究不同pH 值对嗜热毛壳菌木聚糖酶活性的影响发现,在pH 值3.6 以下,随着pH 值的增大,木聚糖酶的活性逐渐升高;pH 值为3.6 时,木聚糖酶的活性最高,且在3.
市面上有很多的生物毒素快速检测卡,求助,试剂盒里的稀释液是什么成分,可以自己配制吗?
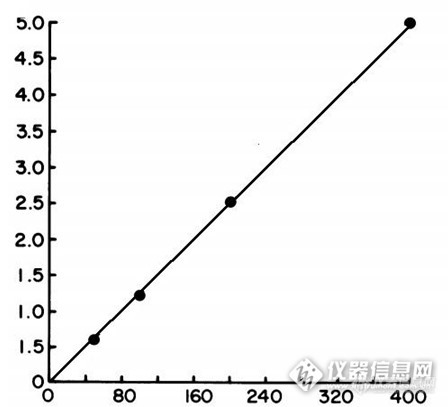
高效液相色谱法测定测定血清中替卡西林水平 卡替西林是一种半合成的抗假单胞菌青霉素,对于严重革兰阴性菌感染特别有效,除了用于治疗单胞菌感染,替卡西林也用于经验用于免疫受损的宿主。通常,这两种情况下,卡替西林总是与氨基糖苷类或头孢菌素联合应用。与青霉素联用的毒性一般是最小的,但当血清中水平高时,也会出现中枢神经系统的副作用。虽然不是常规要求,但是对于肾功能不全患者,特别与其他的β-内酰胺类抗生素联合用药时血清水平监测是很有必要的。 传统替卡西林的测定是通过微生物分析方法测定,该方法虽然划算,但这些方法总是缺乏与生化测定或免疫测定联用的特异性和精确度,而且需要最少8小时的孵育过程,不利于剂量调整。高效液相色谱法定量测定血清中替卡西林水平以及药剂中青霉素和头孢菌素和血清及尿液中替卡西林的测定在文献中均有报道,但均对于临床应用不宜,本实验做了调整优化,对于临床应用实用性较强。材料和方法: 替卡西林/替莫西林均购自药店,甲醇,氯仿,冰乙酸,盐酸,正戊醇,醋酸铵,磷酸二氢钠为分析纯或色谱纯。流动相为85(醋酸铵液):15(甲醇)醋酸铵液:醋酸铵液浓度为0.1M,并以冰醋酸调节PH为4 样品提取溶液预先配置室温保存:包含0.4N的盐酸,氯仿:正戊醇(3:1),0.1M磷酸盐缓冲液(PH=7),磷酸盐缓冲液用前按1:10用水稀释,去离子水。 标准,对照的配置:替卡西林二钠用灭菌的去离子水溶解后加入加热灭活的人血清中,配置浓度为50,100,200,400ug/ml,,并以同样方法配置250ug/ml作为对照。标准和对照血清分别以0.5ml分装,-70度保存。替莫西林以去离子水溶解于灭菌去离子水制成150ug/ml.,同法保存。标准和对照血清以及内标替莫西林用前融化。 样品制备:血清样品,标准和对照血清分别为0.35ml,加入0.15ml内标溶液,0.25ml 0.4N的盐酸,3.5ml的氯仿-正戊醇于带有螺旋盖的试管中。混合均匀后离心10分钟。上层弃去留下层。下层再加入0.35ml的磷酸盐缓冲液,混合均匀后离心10分钟。移取上层,4度保存备用。 液相条件:沃特斯2487配DAD检测器 water bondapak C18柱 (10um×4.6mm×150mm),检测波长242nm. 进样量20ml, 流速1.5ml/min 定量:标准曲线通过替卡西林的峰高与内标峰高的比率以及内标峰浓度进行绘制。 提取效率:替卡西林和内标的回收率通过比较血清提取以及相同浓素的含水制剂的峰高 精密度:日内通过向正常血清中加入替卡西林,(75ug/ml,150 ,ug/ml,300ug/ml),进行测定,日间通过三周内10次测定获得。 样品获得:该试验中应用的血清样本来自临床上那些替卡西林水平需要监测的患者。结果:1、血清中内标和替卡西林的提取后分析图谱如下:(内标和替卡西林的保留时间分别为5.4min,6.8min。http://ng1.17img.cn/bbsfiles/images/2014/10/201410300942_520789_2204138_3.png2、绝对回收率替卡西林血清回收率在29-385ug/ml范围内平均值为71%,而内标的回收率为67%,相对回收率,替卡西林在75-300ug/ml范围内平均为97%,如下图:http://ng1.17img.cn/bbsfiles/images/2014/10/201410300943_520790_2204138_3.png3、下图为替卡西林标准曲线http://ng1.17img.cn/bbsfiles/images/2014/10/201410300943_520791_2204138_3.png讨论: 1、本实验开发了一种运用高效液相测定血液中替卡西林水平的方法,将血清加入替卡西林作为内表。采用氯仿-正戊醇进行萃取,后反萃取于磷酸盐缓冲液中。以反向C18柱,乙酸铵-甲醇水为流动相,240nm下进行检测。虽然头孢西丁,头孢噻吩,头孢呋辛等与替卡西林保留行为相似,但抗生素联合使用对于替卡西林的检测没有影响。试验表明本方法对于单用及联用抗生素时对于卡替西林的快速检测是准确,可重现的 2、本试验所采用的高效液相法分析血清中替卡西林的方法准确、重现性好,当患者联合用药时也能快速检测不干扰。 3、本试验采用内标的方法,从而克服了样品到样品间提取的变数,因为结构相似我们采用替莫西林作为内标。在提取过程和色谱行为方面也证明了采用替莫西林的可靠性。 4.该方法可用于抗生素联合用药时患者血清中替卡西林的水平测定,在患者的服用剂量调整范围内也是可适用的。
[color=#444444]市面上有很多的生物毒素快速检测卡,求助,试剂盒里的稀释液是什么成分,可以自己配制吗?[/color]