GB-T 7473-1987 水质 铜的测定 2,9-二甲基-1,10-菲罗啉分光光度法[img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=48153]GB-T 7473-1987 水质 铜的测定 2,9-二甲基-1,10-菲罗啉分光光度法[/url]
邻菲罗啉测总铁时,滴加饱和乙酸钠溶液至刚果红试纸刚刚变红,饱和乙酸钠的多少影不影响显色程度?
本人求助邻菲罗啉分光光度法测铁时的铁标准曲线,相应的吸光度值。
请教: 邻非罗琳、EDTA和二价铁的络合常数是多少?谢谢
我最近被调到实验室测定水中总铁,公司之前采用的是邻菲罗啉法,之前的实验员没留下任何资料且联系不上,我看实验室有之前配好的试剂:HCL、盐酸羟胺、邻菲罗啉0.1%、乙酸铵不知道该怎么办,做了几次标准曲线每次都不一样且数值差距很大,求救大家有没有此方法的具体操作流程啊,我现在用的参比溶液是蒸馏水,我的操作流程是:①铁贮备液(100μg/mL):准确称取0.7022克分析纯硫酸亚铁铵于100毫升烧怀中,加50毫升1+1 H2SO4,完全溶解后,移入1000ml的容量瓶中,并用水稀释到刻度,摇匀,此溶液中Fe的质量浓度为 100.0μg/mL。(实验室准备好)② 铁标准溶液(100.00 μg·mL-1) 移取 100.0μg·mL-1铁标准溶液100.00mL于100mL容量瓶中,并用蒸馏水稀释至标线,摇匀。 ③ 10%盐酸羟胺水溶液:(用时配制)。④ 0.1%邻菲罗啉水溶液⑤ HAc-NaAc缓冲溶液(pH≈5.0):称取40克纯醋酸铵加到50毫升冰醋酸中,加水溶解后稀释至100毫升。 五、测定步骤: 1、标准曲线的绘制:(1)分别吸取铁的标准溶液0.00、0.25、0.5、1.00、2.00、3.00、4.00/5.00ml于8支50ml容量瓶中,加适量蒸馏水;(2)依次分别加入10%盐酸羟胺溶液1ml,0.1%邻菲罗啉溶液2ml、5ml pH≈5.0缓冲溶液,摇匀,加蒸馏水定容至50ml,(3)放置10-15分钟后,在510nm波长处,用1cm比色皿,以纯水作为参比,测定各溶液的吸光度,以铁的浓度(mg/l)为横坐标,吸光度为纵坐标绘制标准曲线另取10ml待测水样加入1ml1:1的盐酸1ml加热10ml,冷却依次加入10%盐酸羟胺溶液1ml,0.1%邻菲罗啉溶液2ml、5ml pH≈5.0缓冲溶液,摇匀,加蒸馏水定容至50ml,放置10-15分钟后,在510nm波长处,用1cm比色皿,测定溶液的吸光度,从标准曲线查出对应吸光度下铁的浓度C。则待测样中铁的浓度为5C大家帮忙看下我的过程有什么错误???急急急谢谢
我用盐酸邻菲罗啉显色测定污水中铁的含量数值和[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]测定的结果相差好大,有几十倍的区别,可见光测的是1.8%,原子测得是0.07%,个人认为简单的六价铬、二价铜、钴离子,镍离子的干扰都不会造成这样大的误差。而我的标准曲线做得还不错,试剂无混浊,显色也明显,就是不明原因。因为此事,我还被领导批评工作不认真,唉。请教各位高手!可能出现的原因都跟我说说,请教请教!感激不尽
[font=宋体]发帖人:[/font][back=white]11456654[/back][font=宋体]链接:[/font]https://bbs.instrument.com.cn/topic/7808561[font=黑体][b]问题描述:[/b][/font][font=宋体]采用邻菲罗啉比色法测定土壤全铁的含量,使用什么消解方法,如果测定铁的二价和三价分别采用什么方法[/font][font=黑体][b]解答:[/b][/font][font=宋体]建议采用《土壤和沉积物[/font] [font=宋体]铜、锌、铅、镍、铬的测定[/font] [font=宋体]火焰原子吸收分光光度法》[/font](HJ 491-2019[font=宋体])中的消解方法。[/font]1. [font=宋体]消解方法:称取[/font]0.50g[font=宋体]风干土壤样品,精确至[/font]0.0001g[font=宋体]。置于[/font]30 mL[font=宋体]聚四氟乙烯坩埚中,加[/font]2~3[font=宋体]滴水湿润试样。加[/font]8 mL[font=宋体]氢氟酸、[/font]10 mL[font=宋体]浓硝酸和[/font]1 mL[font=宋体]高氯酸,先低温消煮,随后加温,待坩埚内连续出现小气泡逸出,蒸发至冒尽高氯酸烟。用[/font]2 mL[font=宋体]([/font]1+1[font=宋体])盐酸溶液溶解残渣,将坩埚内容物移入[/font]50 mL[font=宋体]容量瓶中,用水稀释至刻度,摇匀,放置澄清或干过滤。[/font]2. [font=宋体]关于二价铁和三价铁的测定有以下方法:[/font][font=宋体]([/font]1[font=宋体])土壤中二价铁的测定[/font][font=宋体]:称取[/font]10.0000 g[font=宋体]新鲜土壤样品(精确至[/font]0.0001 g[font=宋体],同时测定含水量)置于[/font]250 mL[font=宋体]锥形瓶中,加入[/font]200.00mL[font=宋体]硫酸铝浸提剂,加塞,摇匀。放置[/font]5 min[font=宋体]后用慢速滤纸干过滤于另一[/font]250mL[font=宋体]锥形瓶中,加塞,滤液立即进行[/font]Fe[sup]2[/sup][sup][font=宋体]+[/font][/sup][font=宋体]的测定;滤液还可作还原性物质总量、活性还原性物质、二价锰的测定使用;同时作空白试验。吸取[/font]20.00 mL[font=宋体]滤液置于[/font]50 mL[font=宋体]容量瓶中,加入[/font]1 mL[font=宋体]盐酸羟胺溶液,摇匀。放置数分钟后,加入[/font]5 mL[font=宋体]邻菲罗啉溶液,再加水稀释至刻度,摇匀。放置[/font]30 min[font=宋体]以上,在分光光度计上,于[/font]520 nm[font=宋体]波长处,用[/font]1 cm[font=宋体]比色皿测定吸光度,从工作曲线上查得相应的[/font]Fe[sup]2[/sup][sup][font=宋体]+[/font][/sup][font=宋体]含量。分别取[/font]0[font=宋体]、[/font]50 [font=Symbol]m[/font]g[font=宋体]、[/font]100 [font=Symbol]m[/font]g[font=宋体]、[/font]150 [font=Symbol]m[/font]g[font=宋体]、[/font]200 [font=Symbol]m[/font]g[font=宋体]、[/font]250 [font=Symbol]m[/font]g[font=宋体]、[/font]300 [font=Symbol]m[/font]g[font=宋体]二价铁标准溶液置于[/font]50 mL[font=宋体]容量瓶中,按上面操作步骤操作,绘制工作曲线。注意二价铁极易被氧化,需要测定新鲜土壤。建议参考[/font] [font=宋体]《土壤农业化学分析方法》(鲁如坤,北京,中国农业科技出版社,[/font]2000[font=宋体]年)。[/font][font=宋体]([/font]2[font=宋体])土壤中全铁的测定[/font][font=宋体]:称取[/font]0.50 g [font=宋体]风干土壤样品,精确至[/font]0.0001 g[font=宋体]。置于[/font]30 mL[font=宋体]聚四氟乙烯烧杯中,加[/font]2~3[font=宋体]滴水湿润试样。加入[/font]8 mL[font=宋体]氢氟酸、[/font]10 mL[font=宋体]浓硝酸和[/font]1 mL[font=宋体]高氯酸,先低温消解,随后加温,待坩埚内连续出现小气泡逸出,蒸发至冒尽高氯酸烟。用[/font]2 mL[font=宋体]([/font]1+1[font=宋体])盐酸溶液溶解残渣,将坩埚内容物移入[/font]50 mL[font=宋体]容量瓶中,用水稀释至刻度,摇匀。放置澄清或干过滤。取配制的样品溶液[/font]0.20mL[font=宋体]移到[/font]50 mL[font=宋体]的容量瓶中,加[/font]1 mL[font=宋体]盐酸羟胺溶液([/font]100 g/L[font=宋体]),放置[/font]2 min[font=宋体],摇匀后加[/font]8 mL[font=宋体]乙酸钠溶液([/font]100 g/L[font=宋体]),使溶液的[/font]pH[font=宋体]为[/font]5[font=宋体],再加[/font]10 mL[font=宋体]邻菲罗啉溶液([/font]1 g/L[font=宋体])进行显色,用水稀释至刻度,摇匀。[/font]40 min[font=宋体]后在分光光度计上以试剂空白为参比,在[/font]513 nm[font=宋体]的波长下测定溶液的吸光度,从校准曲线查出相应全铁的含量。[/font][font=宋体]([/font]3[font=宋体])土壤中三价铁的测定:[/font][font=宋体]三价铁的含量就是全铁含量减去二价铁含量。[/font][font=宋体]邻菲罗啉比色法测定铁的方法是一个灵敏的方法,土壤中铁的含量比较高,在操作过程中,可根据实际情况适当减小取样量,加大定容体积。[/font]
我用盐酸邻菲罗啉显色测定污水中铁的含量数值和[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收光谱[/color][/url]测定的结果相差好大,有几十倍的区别,可见光测的是1.8%,原子测得是0.07%,个人认为简单的六价铬、二价铜、钴离子,镍离子的干扰都不会造成这样大的误差。而我的标准曲线做得还不错,试剂无混浊,显色也明显,就是不明原因。因为此事,我还被领导批评工作不认真,唉。请教各位高手!可能出现的原因都跟我说说,请教请教!感激不尽
我一直用邻菲罗啉分光光度法测定水中的铁,但标准曲线都做得不理想,请问大家这是什么原因呢?
1.我用邻菲啰啉测总铁的含量 国标上是说显色15min后就可以测吸光度 但是我发现吸光度一直在随时间延长而变大 15min的时候吸光度并没有达到一个稳定的状态 请问这个情况是怎么回事呢 2.用邻菲啰啉测总铁可重复性差 一样的水样和操作 测出来的结果差得挺多 有可能是什么原因造成的呢
大学生求助邻啡罗啉测土壤中全铁的含量注意事项是什么?
我们想改变测铁的方法,我查到用邻菲啰啉测定铁的方法,可是我们的试样中铜和锌的含量都很高,假如不掩蔽的话,根本就不显色,最后的颜色比试剂空白的颜色还浅,我想知道,用什么掩蔽它们,PH值是多少,最好能给我一个具体操作的方法,谢谢!~~补充,我们的液样的PH值是5
求助:土壤全铁的测定-邻菲罗啉法,土壤的前处理是如何的?土壤是用什么方法消解?如果测定全铁和2价.3 价分别怎么样做?
[em20] 我需要购买 (学名:4、7-2苯基-1、10菲罗啉)不知道哪里有卖的我是济南的手机号:13064091134谢谢
求Vc还原3价铁的反应式和2价铁与邻菲罗啉的反应式
求助HG/T4018-2008 化学试剂 1,10菲啰啉
邻菲啰啉分光光度计法测铁中,关于0.1(m/V)的盐酸羟胺溶液如何配置?同时对于缓冲溶液:40g乙酸铵加50ml冰乙酸用水稀释至100ml,对于加入的乙酸铵好像难以完全溶解?最好能够详细说明使用什么方法可使其溶解,同时0.1(m/V)的溶液如何配置?
[b][size=18px]GB/T 3049-2006 铁含量测定的通用方法 1,10-菲啰啉分光光度法 中提到:“如有必要……调至pH为2”,看着似乎是非必需的步骤,可以省略吗?为啥要初调pH?[/size][size=18px]谢谢![/size][/b]
邻菲罗啉和铁离子发色时,为什么PH值要控制在4.5?应该是在2-9都行才对吗?
我想用铁-1,10菲啰啉法测果汁中Vc,有哪位可以介绍一下具体怎么测啊,文献上都没有具体操作,我做不出来,能不能帮我细化到配试剂啊。或者有没有什么更好的方法可以测呢,我是实验室测,仪器可能没有先进的,要传统方法,谢谢,急急急
检测柠檬酸铁胺里面的铁离子时,为什么原吸法比邻菲啰林法做的数值小(请专业的机构做的数据)
求标准GB 2365-1980—工业有机产品中的铁含量测定法(邻菲啰啉法)
邻啡罗啉([color=#DC143C][size=4]C12H8N2[/size][/color])氧化还原指示剂是如何显色的,那位LS知道,可否告知。
[list][*] 铜锌锰等离子也能与邻二氮菲生成有色配合物,量少时不影响测定,量大时可通过加EDTA掩蔽或预先分离。 加入试剂的顺序不能随意改变,否则会因三价铁离子水解等原因造成较大误差。[list][*]①实验原理:试样消解后,在pH为2-9的溶液中,二价铁离子与邻二氮菲生成稳定的橙红色化合物,在510nm处有最大吸收,其吸光度与铁含量成正比,外标法定量。 [/list][list][*]②试剂仪器:盐酸、盐酸羟胺、邻二氮菲、乙酸钠、铁标准溶液;分光光度计。 [/list][list][*]③分析步骤:试样制备,试样消解,吸取呈梯度的铁标准使用液至容量瓶中,并与一定量的试样溶液及试剂空白溶液完全相同的实验操作,分别测其吸光度,绘制标准曲线。 实验操作:加入盐酸羟胺溶液、邻二氮菲溶液、乙酸铵溶液,每加入一种试剂都要摇匀,加水稀释定容。 测定吸光度:10分钟后,以不加铁的试剂空白做参比,在510nm处,用1cm比色皿测吸光度。[/list][list][*]④结果计算:从标准曲线上查出试样溶液铁的质量,除以样品质量即为铁的含量,若试样溶液稀释则乘以相应的稀释倍数。 [/list] [/list]
用邻菲罗啉分光光度法测定水中铁,若水样是以Fe2O3和Fe(OH)3沉淀形式存在,须加盐酸煮沸使其溶解?
1 范围 本标准规定了氧化铝中三氧化二铁含量的测定方法。 本标准适用于氧化铝中三氧化二铁含量的测定。测定范围:0.005%-0.100%, 2 方法原理 三价铁用盐酸经胺还原为二价铁,在乙酸一乙酸钠缓冲溶液中加人邻二氮杂菲使形成络合物,于分光光度计波长 510nm处测量其吸光度,借以测定三氧化二铁含量。 3 试剂 3.1 硼酸:优级纯。 3.2 无水碳酸钠:优级纯。 3.3 硝酸(3.00mol/L), 3.4 盐酸羟胺溶液(10g/L) 3.5邻二氮杂菲溶液(1g/L):称取1g邻二氮杂菲溶于1.5mL--2.5mI冰乙酸中(ρl.05g/mL),移入1000mL容量瓶中,用水稀释至1000mL,混匀。 3.6 缓冲溶液(pH=4.9):称取272g乙酸钠(CH3COONa3H20)溶于500mL水中,加人240mL 冰乙酸(pl.05g/mL),用水稀释至1000mL,混匀。 3.7 三氧化二铁标准贮存溶液:称取0.50g三氧化二铁(含量)99.99%,预先于600℃灼烧2h,并于干燥器(4.4)中冷却至室温)置于150mL烧杯中,沿杯壁加人20mL盐酸(ρ.19g/mL),盖上表皿微热使全部溶解,冷却至室温,将溶液移人1000mL容量瓶中,用水洗净烧杯,洗液并人容量瓶中,用水稀释至刻度,混匀。此溶液1mL含0.5mg三氧化二铁。 3.8 三氧化二铁标准溶液:移取25.00mL三氧化二铁标准贮存溶液(3.7)于500mL容量瓶中,加人30.0ml硝酸((3.3),用水稀释至刻度,混匀。此溶液1mL含0.025mg三氧化二铁,用时配制。 4 仪器、装置及器具 4.1铂坩埚:30mL,带盖。 4.2 分光光度计。 4.3 电热板:用调压器控制加热温度不高于250℃ 4.4 干燥器:用新活性氧化铝作干燥剂。 5 试样 5.1 试样应通过0.125mm孔径筛网。 5.2试样预先在300℃士100℃烘干2h,置于干燥器((4.4)中冷却至室温。 6 分析步骤 6.1 试料 称取约0.50g试样(5),精确至0.0001g 6.2 测定次数 独立地进行两次测定,取其平均值。 6.3 空白试验 随同试料 (6.1)做空白试验 6.4 测定 6.4.1将试料(6.1)置于铂坩埚(4.1)中,加人0.500g硼酸(3.1)和1.300g碳酸钠(3.2),用铂勺搅匀。盖卜坩埚盖,置于约700℃的高温炉中,升温至1000℃熔融20min,取出稍冷 空白试验直接在1000℃熔融2min-3min,取出稍冷。 6.4.2 向坩埚中加人沸水,加热至近沸,使熔块全部溶解,将溶液移人预先盛有22.3mL(随同试料空白则为12.6mL)硝酸(3.3)的150m工聚四氟乙烯烧杯中,坩埚用热水冲洗二次,用聚四氟乙烯棒搅拌使沉淀尽量溶解,坩埚用3ml一硝酸(3.3)和热水充分洗净,洗涤液并人烧杯中,盖上表皿,置电热板(4.3)上加热至沉淀全部溶解,取下,置冷水槽中冷却至室温。将溶液移人100ml容量瓶中,用水洗净烧杯,洗液并人容量瓶中,并用水稀释至刻度,混匀(此溶液也可用以测定二氧化硅量)。 6.4.3 分取50.00 mL试液于100mL容量瓶中[当三氧化二铁含量大于0.05%时,取25.00m工试液,补加1.5mI硝酸(3.3)加水至约50mL。并随同做对应的空白试验)。 6.4.4 向容量瓶中加人5.0mL盐酸经胺溶液(3.4),混匀。加人5.0mL邻二氮杂菲溶液(3.5)和25.0mL缓冲溶液((3.6),用水稀释至刻度,棍匀,放置10min。 6.4.5 将部分溶液移人3cm吸收池中,以水为参比,于分光光度计波长510nm处,测量其吸光度,将测得的吸光度减去随同试料空白试验溶液的吸光度后,从工作曲线上查出相应的三氧化二铁量。 6.5 工作曲线的绘制 于一组100mL容量瓶中,分别加人 0, 1.00, 2.00 ,3.00, 4.00, 5.00ml三氧化二铁标准溶液(3.9),加人3.0mI.硝酸((3.3),用水稀释至体积约50mL,混匀,以下按6.4.4进行。将部分系列标准溶液移人3cm吸收池中,以水为参比,于分光光度计波长510nm处,测量系列标准溶液的吸光度。以所测吸光度减去试剂空白溶液的吸光度,以三氧化二铁量为横坐标,吸光度为纵坐标,绘制工作曲线。 7 分析结果的计算 按下式计算三氧化二铁含量w(Fe2O3)(%): 式中:m1-----自工作曲线上查得的三氧化二铁量,单位为毫克(mg) m0-----试样的质量,单位为克(g) V1------分取试液的体积,单位为毫升(mL) V0------试液的总体积,单位为毫升(mL), 8.1 重复性 在重复性条件下获得的两次独立测试结果的测定值,在以下给出的平均值范围内,这两个测试结果的绝对差值不超过重复性限((r),超过重复性限(r)的情况不超过5%,重复性限((r)按以下数据采用线性内插法求得: w(Fe2O3) (%) 0.0087 0.0222 0.046 8 重复性限r (%) 0.0005 0.0003 0.001 3 8.2 允许差 实验室之间分析结果的差值应不大于表1所列允许差。 w(Fe2O3) 允 许 差 0.005--0.015 0.004 0.015--0.030 0.005 0.030--0.050 0.006 0.060--0.100 0.010 9 质量保证与控制 应用标准样品或控制样品,每月至少对本标准的有效性校核一次。当失效时应找出原因。纠正后重新进行校核。
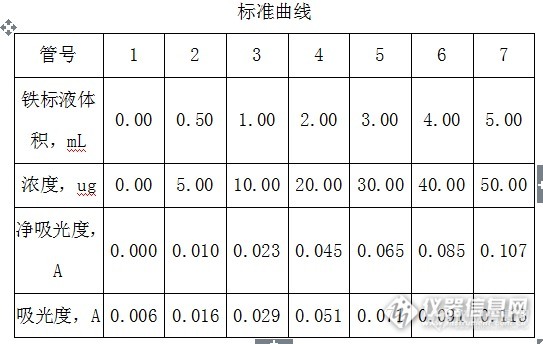
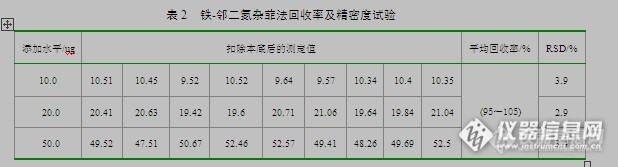
[align=center]用1,10-菲啰啉分光光度法测定氢氧化钠中铁含量[/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]化工室-张苗苗[/align][align=left]一、方法原理[/align]将抗坏血酸将试样溶液中三价铁还原成二价铁,在pH值为4-6时,二价铁同1,10-菲啰啉生成橙红色络合物。在分光光度计最大吸收波长处测定吸光度。二、实验仪器1.电子天平2.容量瓶:100mL3.紫外可见分光光度计三、试剂1.盐酸2.氨水3.盐酸溶液:1+34.氨水溶液:1+95.抗坏血酸溶液:10g/L 该溶液现用现配。6.乙酸乙酸钠缓冲溶液:pH=4.5称取164g无水乙酸钠,用500mL水溶解,加240mL冰乙酸,用水稀释1000mL。7.铁标准溶液:0.010mg/mL 吸取1.00mL1000mg/L铁标准溶液与100mL容量瓶中,加水定容。8.对硝基酚指示剂:2.5g/L称取0.25g对硝基酚,溶于乙醇(95%),用乙醇(95%)稀释至100mL。9.1,10-菲啰啉:1g/L 称取1.0g1,10-菲啰啉一水合物或1,10-菲啰啉盐酸一水合物,用水溶解并稀释至1000mL。该溶液避光保存。使用无色溶解。四﹑绘制标准曲线在一系列100mL容量瓶中分别加入铁标准溶液,加水约至60mL,再加0.2mL的盐酸溶液和1mL抗坏血酸溶液,然后加入20mL缓冲溶液和10mL1,10-菲啰啉溶液,用水稀释至刻度,摇匀,放置10min。与波长510nm处,以水为参比,进行吸光度的测定。[align=center][img=,543,344]http://ng1.17img.cn/bbsfiles/images/2017/09/201709071119_01_2904018_3.png[/img][/align][align=left]以铁含量和吸光度绘制标准曲线,R[sup]2[/sup]=0.9992。[/align][align=center][img=,495,297]http://ng1.17img.cn/bbsfiles/images/2017/09/201709071120_01_2904018_3.png[/img][/align]五、计算[align=center][img=,270,64]http://ng1.17img.cn/bbsfiles/images/2017/09/201709071121_01_2904018_3.png[/img][/align]m[sub]2[/sub]-扣除空白后试样吸光度相对应的标准曲线上查得的铁含量的质量数,ugm[sub]1[/sub]-试样的质量的数值,g1.4297-铁和氧化铁的换算系数。六、方法检出限连续测定7个空白,测定结果如下:1、 测定结果: [align=center][img=,573,229]http://ng1.17img.cn/bbsfiles/images/2017/09/201709071121_02_2904018_3.png[/img][/align] 2、检测限计算及结果表计算公式:MDL=S×t(n-1,0.99) [align=center][img=,577,152]http://ng1.17img.cn/bbsfiles/images/2017/09/201709071122_01_2904018_3.png[/img][/align]经过多次空白实验得出本方法的最低检出限是0.00003%,小于标准给出的0.00006%,符合标注要求。七、方法精密度对于样品进行6次测定,测定结果如下:[align=center]铁含量精密度测定结果[/align][align=center][img=,604,371]http://ng1.17img.cn/bbsfiles/images/2017/09/201709071123_01_2904018_3.png[/img][/align]本方法中铁含量的重复性为:0.0001% 于GB/T 4348.3-2012标准中允许的差值0.0001%一至,符合标准要求。八、方法准确度此样品与进行实验室之间比对测试,比对结果如下:[align=center][img=,490,364]http://ng1.17img.cn/bbsfiles/images/2017/09/201709071124_01_2904018_3.png[/img][/align]本方法中铁含量的性对误差为:0.00%;均小于化工产品的相对误差15%,符合标准要求。九、总结 通过对整体确认,包括方法的检出限、精密度、准确度三个方面,本次验证结果符合GB/T 4348.3-2012中的要求,因此用该标准方法测定工业用氢氧化钠中铁含量的结果是准确的,可靠的。
铁-邻二氮杂菲间接分光光度法检测食品甲醛含量摘要 建立了一种用铁-邻二氮杂菲间接分光光度法检测食品甲醛含量的方法。该法是基于在碱性条件下,甲醛与水合氧化银发生氧化还原反应,生成的银定量还原铁(Ⅲ)为铁(Ⅱ),铁(Ⅱ)与邻二氮杂菲形成稳定的桔红色络合物。此络合物的ε510为1.1×104L·mol-1·cm-1,方法用于食品样品中游离甲醛的测定,取得了满意的结果。关键词 铁-邻二氮杂菲;间接分光光度法;甲醛;食品中图分类号: 文献标识码: 文章编号:Iron-phenanthrolineIndirect Spectrophotometric Detection Method for Formaldehyde in FoodAbstract:An iron-phenanthroline indirect spectrophotometric detection method forformaldehyde in food was established. This method is based on the fact that aredox reaction occurs between formaldehyde and hydrated silver oxide underalkaline conditions, the generated silver make a reduction of iron (III) toiron (II) quantitatively, then iron (II) reacts with phenanthroline to form astable orange-red complex. This complex of ε510 is 1.1 × 104 L • mol-1 • cm-1 in detection. The results indicated that this method wassuitable for the determination of free formaldehyde in food.KeywordsIron -phenanthroline; indirect spectrophotometric; formaldehyde; food甲醛的检测方法目前主要有乙酰丙酮分光光度法,变色酸法,气相色谱法,甲醛与2,4-二硝基苯肼衍生后液相色谱法,离子色谱法等。其中乙酰丙酮分光光度法,变色酸法的方法灵敏度不高,其最大吸收波长处ε分别为7.2×103和2.1×103 L·mol-1·cm-1。本文主要讲述的是基于在碱性条件下,甲醛与水合氧化银发生氧化还原反应,生成的银定量还原铁(Ⅲ)为铁(Ⅱ),铁(Ⅱ)与邻二氮杂菲形成稳定的桔红色络合物。此络合物的ε510为1.1×104L·mol-1·cm-1,故该法的灵敏度较乙酰丙酮分光光度法,变色酸法高。应用于食品中游离甲醛的测定具有一定的实际意义。1实验部分1.1 仪器与试剂UV7504紫外可见分光光度计(上海欣荣仪器厂生产);HH-8型恒温水浴锅(江苏省金坛市鸿科仪器厂生产);Al204电子分析天平(瑞士梅特勒-托利多公司);蒸馏装置。甲醛标液溶液:10.0mg/mL(由中国计量科学研究院提供),使用时将其稀释成10ug/mL甲醛标准使用液;硝酸银液:0.01mol/L;氢氧化钠液:0.1mol/L;硫酸铁铵液:0.004mol/L;硫酸介质:0.1mol/L;pH4.5NaAc-Hac缓冲液;0.1%1,10-邻二氮杂菲溶液;以上所用试剂均为分析纯,均为上海国药集团试剂厂生产;去离子水。1.2 试验步骤1.2.1工作曲线分别移取0.0,1.0,2.0,4.0,6.0,8.0mL甲醛标准使用液于50mL比色管中,依次加入1.0mL0.01mol/L的硝酸银液,1.5mL0.1mol/L的氢氧化钠液,摇匀,置于沸水中10min(否则会有Ag2O沉淀),取出,冷却;依次加入0.5mL0.004mol/L的硫酸铁铵,0.5mL pH4.5NaAc-Hac缓冲液,0.3mL邻二氮杂菲,加水稀释至刻度,摇匀。放置10分钟后,用1cm比色皿于510nm波长处,以试剂空白为参比测定各溶液的吸光度。1.2.2样品分析称取1g粉碎好的样品,放入500mL碘量瓶中,加入100mL水,盖上塞子,在40±1℃ 水浴中萃取1h,中间摇动3~4次,取出冷至 室温。移取上述溶液10mL,置于50mL比色管中,依1.2.1的方法进行样液甲醛含量的测定。2结果与讨论2.1 方法原理 在碱性条件下,甲醛与水合氧化银发生氧化还原反应,生成的银定量还原铁(Ⅲ)为铁(Ⅱ),铁(Ⅱ)与邻二氮杂菲形成稳定的桔红色络合物。反应式如下:http://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gif HCHO + Ag2O H2O + CO↑ + 2Ag↓ (1)http://bbs.instrument.com.cn/xheditor/xheditor_skin/blank.gifFe3+[/su
用什么可以使邻二氮菲与三价铁反应生成的蓝色浑浊溶液,变为红色澄清溶液。
请问什么东西能让邻二氮菲与三价铁反应生成的蓝色溶液,变成红色,请做过高人指点