刘琦[align=center][/align][align=center]第[size=21px]1[font='times new roman'][size=21px]章基本信息[/size][/font][/size][/align]山梨糖醇别名山梨醇,英文名是Sorbitol、D-Glucitol、Sorbol、D-Sorbitol。分子式是C6H14O6,分子量为182.17,密度为1.489 g/cm3,沸点为295℃。是蔷薇科植物的主要光合作用产物。山梨糖醇液是含67%~73% D-山梨糖醇的水溶液。毒性试验显示,内服过量会引起腹泻和消化紊乱。[img]https://ng1.17img.cn/bbsfiles/images/2021/06/202106161539566336_8129_1608728_3.jpeg[/img]1.1 理化性质1.1.1物理性质山梨糖醇为无色针状结晶,或白色晶体粉末,无臭,有清凉甜味,难溶于有机溶剂,它耐酸,耐热性能好,与氨基酸,蛋白质等不易起美拉德反应。山梨糖醇液为无色,透明稠状液体。依结晶条件不同,熔点在88~102℃范围内变化,相对密度约1.49。易溶于水(1g 溶于约0.45mL水中),微溶于乙醇和乙酸。山梨糖醇液为清亮无色糖浆状液体,有甜味,对石蕊呈中性,可与水、甘油和丙二醇混溶[1],pH值为6~7。山梨糖醇有清凉的甜味,其甜度约为蔗糖的50%~70%。1g 山梨糖醇在人体内产生16.7kJ热量。食用后在血液内不转化为葡萄糖,也不受胰岛素影响。作为甜味剂使用不会引起龋齿。山梨糖醇具有良好的保湿性能,可使食品保持一定的水分,防止干燥,还可防止糖,盐等析出结晶,能保持甜,酸,苦味强度的平衡,增强食品的风味,由于它是不挥发的多元醇,所以还有保持食品香气的功能。[size=14px]1.1.2[size=14px]化学性质山梨糖醇的化学性质相对稳定,不燃烧,不腐蚀,不挥发;浓度高时具有抗微生物的特性。有旋光性,略有甜味,具有吸湿性,能溶解多种金属,高温下不稳定。能参与酐化、酯化、醚化、氧化、还原和异构化等反应[color=#333333],并能与多种金属形成络合物[4]。山梨糖醇不含醛基,不易被氧化,加热时不与氨基酸产生美拉德反应。[/color][/size][/size][align=center]第[size=21px]2[font='times new roman'][size=21px]章功能及应用[/size][/font][/size][/align]山梨糖醇有吸湿,保水作用,在口香糖[color=#333333],糖果[color=#333333]生产中加入少许可起保持食品柔软,改进组织和减少硬化起砂的作用。用量为百分之八左右,在面包,糕点中用于保水目的,使用量为百分之二左右,用于甜食和食品中能防止在物流过程中变味,还能螯合金属离子,用于罐头饮料和葡萄酒[color=#333333]中,可防止因金属离子而引食品混浊。根据《食品安全国家标准 食品添加剂使用标准》(GB2760-2014)中规定:山梨糖醇和山梨糖醇液的功能有甜味剂、膨松剂、乳化剂、水分保持剂、稳定剂、增稠剂(如表1[2])。[/color][/color][/color][align=center]表1山梨糖醇和山梨糖醇液 sorbitol and sorbitol syrup[/align]CNS号 19.006,19.023 INS号 420(i),420(ii)功能 甜味剂、膨松剂、乳化剂、水分保持剂、稳定剂、增稠剂[align=center]允许使用范围及限量[/align]食品分类号食品名称最大使用量/(g/kg)备注01.04炼乳及其调制产品按生产需要适量使用淡炼乳(原味),调制炼乳02.0302.02类以外的脂肪乳化制品,包括混合的和(或)调味的脂肪乳化制品(仅限植脂奶油)按生产需要适量使用仅限植物奶油03.0冷冻饮品(03.04食用冰除外)按生产需要适量使用03.04食用冰块除外04.01.02.05果酱按生产需要适量使用 04.02.02.03腌渍的蔬菜按生产需要适量使用 04.05.02.01熟制坚果与籽类(仅限油炸坚果与籽类)按生产需要适量使用仅限油炸坚果与籽类05.01.02巧克力和巧克力制品,除外05.01.01以外的可可制品按生产需要适量使用 05.02糖果按生产需要适量使用 06.03.02.01生湿面制品(如面条、饺子皮、馄饨皮、烧麦皮)30.0 07.01面包按生产需要适量使用 07.02糕点按生产需要适量使用月饼除外07.03饼干按生产需要适量使用 07.04焙烤食品馅料及表面用挂浆(仅限焙烤食品馅料)按生产需要适量使用仅限焙烤食品馅料09.02.03冷冻鱼糜制品(包括鱼丸等)0.5仅当水分保持剂使用时,其最大使用量调整为20g/kg12.0调味品按生产需要适量使用 14.0饮料类(14.01包装饮用水除外)按生产需要适量使用14.01包装饮用水除外。固体饮料按稀释倍数增加使用量16.06膨化食品按生产需要适量使用 16.07其他(豆制品工艺)按生产需要适量使用仅限豆制品工艺16.07其他(制糖工艺)按生产需要适量使用仅限制糖工艺16.07其他(酿造工艺)按生产需要适量使用仅限酿造工艺09.04.01熟干水产品按生产需要适量使用仅限使用山梨糖醇09.04.02经烹调或油炸的水产品按生产需要适量使用仅限使用山梨糖醇09.04.03熏、烤水产品按生产需要适量使用仅限使用山梨糖醇[table][/table]它是在日本最早允许作为食品添加剂使用的糖醇之一,用于提高食品保湿性,或作为稠化剂之用。可作甜味剂,如常用于制造无糖口香糖。也用作化妆品及牙膏的保湿剂、赋形剂,并可用作甘油代用品。2.1功能2.2.1甜味剂山梨醇是一种只含羟基官能团的碳水化合物,具有低热甜味剂的性质。2000年6月国际粮农和卫生组织食品法典委员会确认山梨醇、木糖醇、麦芽糖醇、乳糖醇、甘露醇等可作为食品添加剂加到食品中,制作无糖甜食品。在欧美发达国家中,以山梨醇等替代食糖生产糖果、点心等各类食品已十分普遍,发展趋势非常明显,其中最突出的是口香糖。在日本,各种食品和糖果都广泛使用山梨醇为甜味剂[3]。2.1.2膨松剂具有多羟基结构的山梨糖醇还具有降低水分活度,控制结晶、改善或保持柔软度的性质[],故在食品工业中经常将山梨糖醇作为一种膨松剂使用。在糖果制造中使用山梨糖醇可抑制蔗糖结晶,加上山梨糖醇本身具有的保湿性,可赋予糖果柔软的质感。在冰制品和冰激凌中可降低冰点,使产品柔软,易于勺食,且同样可抑制产品中糖类重新结晶[5]。2.1.3乳化剂山梨糖醇含有6个羟基,可与许多有机酸发生酯化作用。山梨糖醇脱水与脂肪酸合成的山梨醇脂肪酸酯统称为司盘类表面活性剂,是优良的食品乳化剂[6],可改善缩短乳化进程。在面包生产过程中可防止面包中淀粉凝沉,改善面团的加工性能;生产的糕点外观美,食用性好。还可以广泛应用于冰淇淋以及豆奶生产中。山梨糖醇制取脱水山梨醇酐,再与棕榈酸单酯化制得的司盘40,可用作印刷油墨及多种油品的乳化剂。其中,作为食品添加剂,山梨醇酐硬脂酸酯(司盘60)、山梨醇酐单棕榈酸酯(司盘65)、山梨醇酐单油酸酯(司盘80)均已经列入食品添加剂使用卫生标准中,可应用于椰子汁、果汁、牛乳、奶糖、冰淇淋、面包、糕点、麦乳精、人造奶油和巧克力等食品中[5]。2.1.4水分保持剂山梨醇的多羟基结构使其具有与水结合的性质,并具有控制食品黏度和质构、保持湿度、改善脱水食品的复水性质等作用。山梨醇的良好吸湿性,使其在潮湿的环境下会吸收一些水分,当湿度降低时,山梨醇则释放一些水分,进而建立一种湿度平衡[7],能够防止食品干裂,使食品柔软,保持新鲜度,延长有效期,防止变质。因此,山梨糖醇经常作为保湿剂应用于焙烤食品中。在饼干蛋糕和酥皮糕点中加入适量的山梨糖醇,可防止产品干裂,且有助于产品的外观。但山梨糖醇不适宜用于脆酥食品中。此外,山梨糖醇与其他糖类共存时会出现吸湿性增加的现象,使用时需特别注意[5]。2.1.5稳定剂山梨糖醇不含有醛基,不易被氧化,加热时不与氨基酸产生美拉德反应。有一定的生理活性,能防止类胡萝卜素和食用脂肪及蛋白质的变性。在浓缩牛乳中加入山梨糖醇可延长保存期,对鱼肉酱、果酱蜜饯也有明显地稳定和长期保存的作用,山梨糖醇属于不挥发性多元醇在保持食品香气方面有较好的作用。粉末和液体形式的山梨糖醇均可保持香气和滋味,因而可作咖啡、茶、巧克力饮料和加香饮料等产品的稳定性的无糖载体[8]。山梨糖醇还能螯合金属离子,用于饮料和葡萄糖酒,可以防止金属离子引起的浑浊[font='calibri'][[font='calibri']9]。近年开发成功的中成药产品,如双黄连口服液、双黄连粉针和安宫牛黄丸、清开灵输液等,既保持了中药的综合药效,又具有西药使用方便的特点,添加少量山梨糖醇,可起到稳定药效和防止沉淀的作用。2.1.6[size=14px]增稠剂可用于酒类、清凉饮料的增稠。2.1.7其他作用①山梨糖醇与甘露醇都是具有扩张细胞外液容积作用的高渗脱水利尿药。中国药典规定[10],临床用甘露醇输液为20%的过饱和溶液。温度较低时,甘露醇易结晶析出 (见表2[11] )。[/size][/font][/font][align=center][size=12px]表2甘露醇在水中溶解度与温度的关系[/size][/align]温度[font='calibri'] /[font='calibri']℃ 010203040D-[size=14px]甘露醇10.413.718.625.234.6/g ( 100 g H2O) - 1[/size][/font][/font][table][/table]可见甘露醇输液20℃以下易结晶析出,而我国大部分地区冬季室温低于20℃,用药前需预热使之溶解,不仅给临床用药尤其是急救用药造成困难,也易引起患者的猜疑,造成医患之间的矛盾。在甘露醇输液生产中加适量山梨醇,配成复方甘露醇输液,即可防止甘露醇结晶析出,且疗效相同[12]。②冷冻保护剂:美国批准的 Neupogen(人粒细胞集落刺激因子)的新剂型,即是在其制剂中用山梨糖醇代替甘露醇作为保护剂,可使 Neupogen在冷冻环境时,仍能保持其生物活性[13]。目前甘露醇的价格是山梨糖醇的3~5倍(最高时达 10倍),用山梨糖醇代替甘露醇能达到同样效果,既可降低成本,而且原料来源更广。随着基因工程的高速发展,大量的基因因子需要保护,山梨糖醇在这方面的应用将更为广阔。2.2山梨糖醇的价值[font='calibri']2[font='calibri'].2.1山梨糖醇的直接药用价值山梨糖醇具有利尿、脱水的特性,能降低颅内压,防止水肿,可作为药物直接使用,用于脑水肿、青光眼;也用于心肾功能正常的水肿少尿;口服可作缓泻剂或糖尿病患者的蔗糖代用品。临床制剂有山梨醇注射液、山梨醇铁注射液、复方氨基酸注射液等。山梨醇在复方氨基酸中所起的作用主要有: ①可提高氨基酸的利用率;②平衡注射液中碳氮之比;③可避免葡萄糖灭菌时引起糖中醛基与氨基酸中的氨基发生美拉德反应而产生焦色素,并且也不易产生热原;④使伤口、创面部位尽量保持干燥,加快愈合,避免感染等。2[size=14px].2.2山梨糖醇可作为药用辅料山梨糖醇能与多种辅助形剂配伍 (与氧化剂禁配 ),广泛用于药物的固体分散剂、填充剂、湿润剂、稀释剂、胶囊的增塑剂、甜味剂、矫味剂、软膏的基质等作辅料。其不同用途的用量见表3[14]。[/size][/font][/font][align=center]表3山梨醇在药用辅料中不同用途和用量[/align]用途代替甘油和丙二醇润滑剂口服和外用溶液的赋形剂防止糖浆和酏剂结顶无糖甜昧剂增稠剂片剂粘结度和水份控制剂明胶和纤维膜增塑剂供注射用稀释剂DSS、四环素、抗坏血酸、复合维生素 B、维生素和铁盐的赋形浓度/%25~903~1525~90 15~3025~9025~903~105~2010~25以下25~90[table][/table][size=14px]2.2.3[size=14px]山梨糖醇的其他用途①制备维生素C[color=#333333]山梨糖醇可用于生产维生素C的原料,其经发酵和化学合成可制得维生素C。制药行业,VC合成消耗山梨醇的量最大,占全世界山梨糖醇总消耗量的16% (我国高达50% )。[img]https://ng1.17img.cn/bbsfiles/images/2021/06/202106161539569529_9169_1608728_3.jpeg[/img]以传统山梨糖醇制备维生素C的工艺过程(二步发酵法)如下:[/color][/size][/size][align=center][/align]②其他合成树脂和塑料,分离分析低沸点类含氧化合物等。也用作[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]固定液、稠化剂、硬化剂、杀虫剂等。用作[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]固定液,用于低沸点含氧化合物、胺类化合物、氮或氧杂环化合物的分离分析。还用于有机合成。利用山梨醇所具有的保湿性能,用作牙膏、化妆品、烟草的调湿剂。是甘油的代用品,保湿性较甘油缓和,口味也较好。可以和其他保湿剂并用,以求得协同的效果。也用于医药工业作为制造维生素C的原料。也可用于工业表面活性剂的原料,用它生产斯盘和吐温类的表面活性剂。以山梨糖醇和环氧丙烷为原料,可以生产具有一定阻燃性能的聚氨酯硬质泡沫塑料。[color=#333333]在医药工业中,山梨[color=#333333]糖[color=#333333]醇经过硝化生成的失水山梨醇酯是治疗冠心病的药物。[/color][/color][/color][align=center][font='times new roman'][size=21px]第三章[font='times new roman']来源和合成[/font][/size][/font][/align]3.1 自然来源山梨糖醇广泛分布于自然界植物果实中,在梨、桃、苹果中广泛分布,含量约为1%~2%,1872年法国化学家Joseph Boussingault首先从山梨树果汁中分离而得[15]。常温下有液体和固体2种状态:液体山梨醇为50%~70%的水溶液,无色、无臭、味甜,pH值为6~7,10%水溶液的旋光度[a] 20d为-1.98°;固体山梨醇为白色针状、片状、粒状结晶粉末,极易溶于水,味道清凉爽口,甜度约为蔗糖的60%[15]。3.2人工合成山梨糖醇的产品规格主要有50%山梨醇液、70%山梨醇液和结晶山梨醇等[3]。山梨糖醇的生产包括氢化法、电化学法和发酵法。3.2.1催化加氢法氢化法是目前最常用的生产方法。催化加氢法所用原料主要是葡萄糖,少数工艺以淀粉、蔗糖、纤维素等为原料。以淀粉、蔗糖等生产山梨糖醇。步骤:①通过酶法或酸法将其转化成葡萄糖,②再催化加氢制备山梨糖醇[16]。1942年,日本首次采用葡萄糖催化加氢法生产山梨醇;其后,德国罗莱班公司采用固定床反应器催化加氢生产山梨醇[17-18]。目前,国内外普遍采用葡萄糖催化加氢法工业化生产山梨醇。生产装置:①间歇式,②连续式。工业上目前较多采用高压柱形反应器的连续式氢化新技术。将葡萄糖溶液通过高压泵连续注入装有固体块状催化剂的柱式反应器中,反应一段时间后排出即为山梨糖醇。催化器在反应器中处于静状态,没有搅拌和冲击的影响,而葡萄糖溶液和氢气连续不断的通过催化剂的表面,使氢化反应均匀完全。连续氢化所得的山梨糖醇溶液经过离子交换树脂精制通过升膜式或降膜式蒸发器脱水浓缩即可得液体山梨糖醇成品,进一步结晶即为结晶状山梨糖醇。催化剂是该技术的关键因素[19],传统工艺多使用Ni基催化剂。3.2.2山梨糖醇的电化学法生产技术[20]电化学法制备山梨糖醇,是通过电解法在阴极上将葡萄糖或果糖还原为山梨糖醇。与催化加氢法相比,电化学法具有工艺流程短、安全性高、产物易分离提纯、生产过程中废物排放少等优点。但由于转化率低(约70%),且每次电解只能在一个电极上合成一种产品,导致成本较高,因此电化学法生产山梨糖醇至今仍未实现工业化。直到20世纪80年代中叶,Park和Pintauro等提出了成对电氧化和还原工艺,即在同一个电解槽内同时合成葡萄糖酸盐和山梨糖醇,使得电化学法制备山梨糖醇的技术有了巨大的进步。成对电氧化和还原工艺以葡萄糖为原料,以NaBr为催化剂,加入辅助电解质Na2SO4,在50℃~60℃进行成对电化学反应。溴离子首先在阳极表面上失去电子生成溴分子,继而与葡萄糖作用,生成葡萄糖酸内酯中间体,在水溶液中与葡萄糖酸存在平衡,由于溶液中还有Na盐或Ca盐,则进一步生成葡萄糖酸盐,以避免葡萄糖酸内酯在阴极被还原。葡萄糖在阴极表面上获得2个电子被还原成山梨糖醇。因为山梨醇和甘露醇是同分异构体,所以有小部分的葡萄糖还原会成为甘露醇。3.2.3山梨糖醇的发酵法生产技术[20-21]长期以来山梨糖醇的生产都只有氢化法,直到1984年有报道利用一种生成乙醇的微生物Zymomonasmobilis可将果糖和葡萄糖的混合物转化为乙醇,且山梨糖醇的生成是与葡萄糖脱氢形成葡萄糖内酯的反应同时进行。Zymomonasmobilis最初是从发酵龙舌兰、棕榈和蔗糖等植物汁中分离得到的,经过生物转化来生产山梨糖醇和葡萄糖酸。用渗透性试剂(如甲醇或洗涤剂等)浓缩Zymomonasmobilis细胞处理后,葡萄糖酸和山梨醇产率分别为94%~95%和98%~99%。但这种生产方法操作麻烦,成本也高,目前仅限于实验室研究。[size=14px]3.2.4[size=14px]其他合成方法(1):将配制好的53%葡萄糖水溶液加入高压釜,加入葡萄糖重量0.1%的镍催化剂。经置换空气后,在约3.5MPa、150℃、pH8.2-8.4条件下加氢,终点控制残糖在0.5%以下。沉淀5min后,将所得山梨糖醇溶液通过离子交换树脂精制即得。原料消耗定额:盐酸19kg/t、液碱36kg/t、固碱6kg/t、铝镍合金粉3kg/t、口服糖518kg/t、活性炭4kg/t。(2):采用淀粉糖化所得精制葡萄糖,中压连续或间歇加氢制得。(3):将53%的葡萄糖水溶液(事先用碱液调pH=8.2~8.4)和葡萄糖质量0.1%的镍铝催化剂加入高压釜,排尽空气后进行反应,控制温度150℃,压力3.5MPa:当葡萄糖含量达0.5%以下,反应即达终点。静置沉淀、过滤。滤液用强酸性苯乙烯系阳离子交换树脂001×7及强碱性系铵Ⅰ型[color=#333333]阴离子交换树脂201×7进行精制,去除镍、铁等杂质,即得成品D-山犁醇。[/color][/size][/size][align=center][font='times new roman'][size=21px]第四章[font='times new roman']对人体的影响[/font][/size][/font][/align]4.1 [font='calibri']利尿作用山梨糖醇在人体内小部分被转变成糖原,大部分不被代谢,以原形经肾小管排出。山梨糖醇静滴后,可使血浆渗透压增高、组织脱水,经肾小球滤过,几乎不被肾小管重吸收,从而起到利尿作用。[font='calibri']4.2防止龋齿由于蔗糖能被口腔中的微生物利用,易引起龋齿,多吃不利牙齿健康。而山梨糖醇在口腔中不被龋齿的链球菌所利用,并能使口腔中的pH值略微上升,是一种防龋齿的甜味剂。4.3[size=14px]代替蔗糖,适用于一些特殊人群由于蔗糖能直接引起血糖浓度的变化,高血压、高血脂、糖尿病患者和肥胖症患者等对蔗糖敏感的人群不适用。而在哺乳动物及人体系统中,山梨糖醇通过山梨醇脱氢酶氧化成果糖,然后进入果糖-1-磷酸酯途径代谢,代谢与机体内的胰岛素无关,不受胰岛素的控制,最终代谢物为二氧化碳和水,在血液中不转化为葡萄糖,对血糖值和尿糖没有影响。因而使用山梨糖醇代替蔗糖,对糖尿病患者山梨醇比蔗糖更易忍受。所以可避免糖尿病、肥胖症、肝病、胆囊炎等患者的不适。Wheeler等研究了2种氢化淀粉水解物14:8:78和7:60:33(山梨糖醇:麦芽糖醇:其他更高聚合度的低聚糖醇)与葡萄糖相比,对无糖尿病者、非胰岛素依赖型糖尿病患者及胰岛素依赖型糖尿病患者血糖的影响,结果表明,对于所有的试验组,因摄入氢化淀粉水解物而增加的胰岛素量显著低于葡萄糖,氢化淀粉水解物引起的总血糖反应也都显著低于葡萄糖。这除了氢化淀粉水解物中葡萄糖含量较低的原因外,还可能由于山梨糖醇对葡萄糖吸收有抑制作用[22-23]。4.4其他此外,山梨糖醇还可刺激胰腺分泌胰脂肪酶等,促进胰岛素释放,使肝胆汁分泌增加,山梨糖醇不被胃酶分解,在肠中滞留时间比葡萄糖长,有润肠作用[24]。但是人体肠道可能吸收的山梨醇量不多于10g~20g,如摄入量过多,会引起渗透性腹泻[20]。[/size][/font][/font][align=center][font='times new roman'][size=21px]第五章[font='times new roman']违规事件[/font][/size][/font][/align]5.1 EBay停售在线拍卖公司EBay Inc(EBAY)2012年3月22日宣布,在意大利周末发生患者服用网购有毒山梨糖醇致死事件后,已在全球范围阻止在其网站上出售这种产品。而此前,国内也曾爆出味千就包装面过量使用添加剂的报道,当时味千回应称,2010年1月内地机构宣布在面制品允许添加山梨糖醇[25]。[size=14px]5.2[size=14px]雀巢添加剂2013年1月份的《进境不合格食品、化妆品信息》显示,雀巢一批巧克力棒因违规使用化学物质山梨糖醇而被销毁。2013年3月上海出入境检验检疫局销毁了2.7吨雀巢巧克力棒。被销毁的雀巢巧克力棒含有过高的山梨糖醇,这是一种甜味剂,过量使用可能导致肠道问题。上海出入境检验检疫局宣传部工作人员表示,上海出入境检验检疫局确销毁过一批雀巢巧克力棒,但外媒报道的时间不对。该工作人员称,在国家质量监督检验检疫总局的官方网站公布了这一信息。“外媒的报道也是从总局网站上摘抄的,但不知为什么他们把时间说成了本周。”经调查得知,被检出问题的雀巢产品具体是“雀巢奇巧榛子味牛奶巧克力脆谷棒”这款产品,产地意大利,不合格原因是违规使用化学物质山梨糖醇。信息显示,上海出入境检验检疫局总共查获2.7吨雀巢巧克力棒,已采取销毁方式处理。在日本山梨糖醇作为食品甜味剂,使用范围和限量如下:清凉饮料为百分之一到三,蛋白在百分之三左右,巧克力为百分之四左右。山梨糖醇的最大使用量是40g/kg,但一般都不会达到那么高的值,所以一般情况就是分为可用和不可用,“违规使用[color=#333333]”应该就是不可用。那么既然按照《食品添加剂使用标准》的规定,山梨糖醇可以用于巧克力和巧克力制品,而巧克力棒属于糕点,因而推测可能是进口申报的时候报的不是糕点,而导致与我国质量标准不符[26]。[/color][/size][/size][align=center][font='times new roman'][size=21px]第六章发展前景[/size][/font][/align]我国山梨糖醇产业发展迅猛,20世纪90年代,产能约为30 kt/a,2005年约为550 kt;2013年达到1200 kt[27];2015年年末,全国总产能突破3000 kt。我国山梨糖醇产能大幅跃升,成为山梨醇出口大国[28]。 近年来,国内产能超过100 kt/a的山梨糖醇生产厂家主要有:长春大成实业集团有限公司(350 kt/a)、山东天力药业有限公司(400 kt/a)、茌平县同创生物技术有限公司(200 kt/a)、利达(柳州)化工有限公司(160 kt/a)、山东青援食品有限公司(140 kt/a)、罗盖特(中国)精细化工有限公司(120 kt/a)、秦皇岛骊华淀粉股份有限公司(100 kt/a)、诸城兴贸玉米开发有限公司(100 kt/a)、山东鲁维制药有限公司(100 kt/a)、山东鲁洲集团(100 kt/a)等[27]。随着山梨醇产能的激增,其下游产业的需求量趋于饱和,因此,对山梨醇的下游应用及提高产品附加值提出了更高的要求[29]。6.1[font='calibri']前景期望[font='calibri']山梨糖醇具有优良的性能,低廉的价格,是全球消费量最大的糖醇,约占糖醇总消费量的1/3。山梨[size=14px]糖醇近年已成为世界食品工业界的新宠,随着经济技术在我国快速发展,山梨醇行业将呈快速上升趋势,其市场前景也将是一片光明。[/size][/font][/font][align=center][font='times new roman'][size=21px]参考文献[/size][/font][/align][1] 李凤林、黄聪亮、余蕾.食品添加剂:化学工业出版社,2008.[2] 《食品安全国家标准食品添加剂使用标准》(GB2760-2014).[3] 周日尤,伍玉碧. 我国山梨醇工业的现状与发展 [J]. 现代化工, 2000(9):49-51.[4] 山梨醇化学性质.化学网[引用日期2014-6-20].[5] Smith.Jim,Hong-Shum.L. ,姜竹茂.食品添加剂实用手册 [M]. 北京:中国农业出版社,2005:396-406.[6] 张晓英,赵统领. 山梨醇的制备与应用 [J]. 中国食品添加剂, 2001(5):49-50.[7] O. R. Fennema,王璋,等. 食品化学(第三版)[M]. 北京:中国轻工业出版社,2003:664-666.[8] 金树人. 中国糖醇行业的形势与发展动态[J]. 牙膏工业, 2006(2):47-48.[9] 潘道东. 功能性食品添加剂 [M]. 北京:中国轻工业出版社, 103-105.[10] 中华人民共和国药典 ( 95年版二部 ) [ M ].北京: 化学工业出版社 , 1995.[11] 丁绪淮 ,等 .工业结晶 [ M ]. 北京: 化学工业出版社 , 1995.[12] 郑云鹏 .复方甘露醇注射液防止结晶试验 [J]. 中国药学杂志 , 1989, ( 7): 417-418.[13] 罗青波. 国内外“三醇”产销现状分析 [ N ].医药经济报 , 1999-12-27(3).[14] 上海医药管理局科技情报所 . 药用辅料手册 [ M ]. 1988.[15] 汪薇,罗威,罗立新,等. 山梨醇的研究开发进展 [J]. 中国食品添加剂,2004(1):77-80.[16] 孙然,刘超超,李海亮. 山梨醇的主要应用及生产工艺分析 [J]. 中国高新技术企业,2008(9):99-100.[17] Klein J C,Hercules D M. Surface analysis by X-ray photoelectron spectroscopy and auger electron spectroscopy of molybdenum-doped Raney nickel catalysts[J]. Anal Chem, 1984,56(4):685-689.[18] 徐三魁,王向宇,梁丽珍. 葡萄糖加氢制山梨醇催化剂研究 及发展趋势[J]. 现代化工,2006,26(11):29-31.[19] 袁长富,李仲良,卢春山,等. 山梨醇制备及转化催化剂研 究进展[J]. 化工生产与技术,2007,14(1):34-37.[20] 郑建仙. 功能性糖醇 [M]. 北京:化学工业出版社,2005: 114-145.[21] 朱建良,吴振兴. 生物法制备山梨醇的研究进展 [J]. 化工时刊, 2006(5):47-51.[22] 杨程芳,郑建仙. 功能性糖醇—氢化淀粉水解物 [J]. 中国食品 添加剂,2005(3):113-117.[23] WHEELER M L, FINEBERG S E, FINEBERG N S, et al. Animal versus plant protein meals in individuals with type 2 diabetes and microalbuminuria: effects on renal, glycemic, and lipid parameters [J]. Diabetes Care, 2002,25:1277-1282.[24] 尤新. 淀粉糖品生产与应用手册(第一版)[M]. 北京:中国轻工业出版社,1997:326-342.[25] EBay全球停售山梨糖醇,因意大利发生致死事件.[26] 2.7吨雀巢产品山梨糖醇超标被销毁. 新华网[引用日期2013-03-08].[font='calibri'][27] [font='calibri']江镇海. 山梨醇的市场应用现状与发展趋势[J]. 上海化 工,2014,39(12):33-35.[28] [size=14px]王成福,庞颂,杜瑞锋. 异山梨醇制备技术研究[J]. 轻工 科技,2017(6):52-54.[29] Ruppert A M,Weinberg K. Hydrogenolysis goes bio:from carbohydrates and sugar alcohols to platform chemicals[J]. Angew Chem Int Edit,2012,51(11):2564-2601.[/size][/font][/font]
木糖醇、山梨醇、甘露醇标准品那里可以买到?如何用液相分离?
根据国标做的,然后每次标样的第一针都在山梨糖醇峰的前面出现一个不明峰,但是第二针标样开始就没有那个不明峰了。请问为什么啊?
GB 7658-2005 食品添加剂 山梨糖醇液
[size=5]GB 7658—1987 食品添加剂 山梨糖醇液[/size]
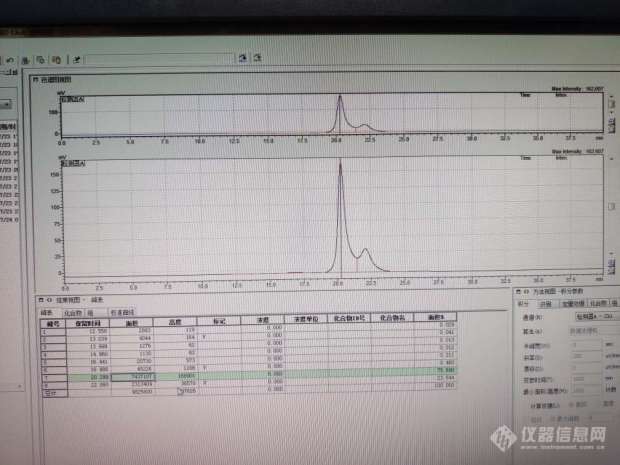
[img=,620,465]https://ng1.17img.cn/bbsfiles/images/2019/07/201907241532473183_6059_3071652_3.jpg!w620x465.jpg[/img]大家检测山梨糖醇含量有没有出现过上面的这种情况?傍边多出一个小峰,厂家说明书提供的纯度是98.5。按面积归一化,如果不计算后面那个小峰,纯度只有75%。如果傍边也计算的话刚好98.5。大家帮忙分析下
请问下有人提供木糖醇和山梨醇吗?价格大概是多少?需要大概五斤左右,实验用。希望不要太贵。我是湖南长沙的。谢谢。
大家好,新手提个问题,我现在用安捷伦液相色谱1260测量果实中的糖组分,发现葡萄糖和山梨醇很难分开,我用的柱子是安捷伦的糖柱(ZORBAX CarbohydrateAnalysis Column),有懂得麻烦分享下方法,谢谢大家了
GB7658-2005食品添加剂 山梨糖醇液.pdf
[font=SimSun, STSong, &]山梨糖醇在长保面包中添加后出现苦味?这个原因和机理?[/font]
甘露醇检测时先出哪个峰?在检测甘露醇时是先出甘露醇的峰还是先出山梨醇的峰?
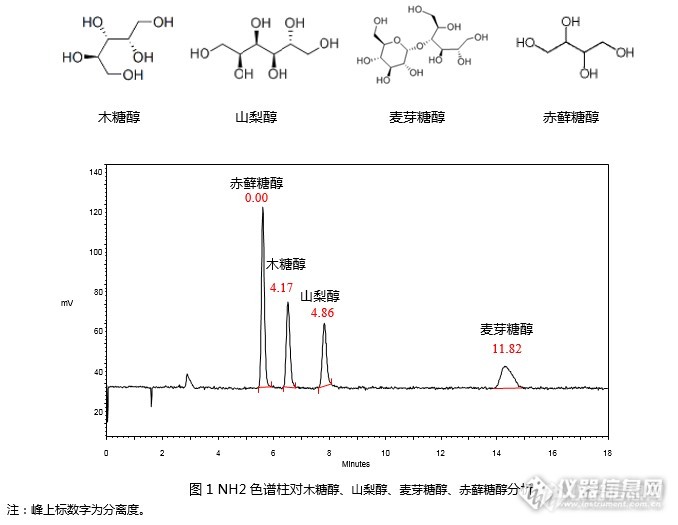
[align=center][b][color=black]GB 5009.279-2016 [/color][color=black]食品安全国家标准[/color][color=black] [/color][color=black]食品中木糖醇、山梨醇、麦芽糖醇、赤藓糖醇的测定([/color][color=black]RI[/color][color=black])[/color][/b][/align][align=center][b][color=black][/color][/b][/align][align=left][/align][color=black][/color][align=left][color=black]本实验根据《[/color][color=black]GB 5009.279-2016 [/color][color=black]食品安全国家标准[/color][color=black] [/color][color=black]食品中木糖醇、山梨醇、麦芽糖醇、赤藓糖醇的测定》第一法,使用示差折光检测法[/color]对[color=black]木糖醇、山梨醇、麦芽糖醇、赤藓糖醇[/color][color=black]4[/color][color=black]种[/color]标准品进行分析,并对标准曲线进行考察。[/align][align=center][/align][align=center][img=,600,163]http://ng1.17img.cn/bbsfiles/images/2017/08/201708100910_01_2222981_3.png[/img][/align][align=left]使用资生堂氨基柱CAPCELL PAK NH2 UG80 S5 4.6 mm i.d. [color=black]× [/color]250 mm(GQAD 05507)依据国标方法进行分析,可以实现4种糖醇的良好分析(见图1)。 [/align][align=center][/align][align=center][img=,690,336]http://ng1.17img.cn/bbsfiles/images/2017/08/201708100911_01_2222981_3.png[/img][/align][align=center][/align][align=center][/align][align=left]进一步,依据标准,配制1.6 mg/mL, 2.4 mg/mL, 3.2 mg/mL, 4.0 mg/mL, 4.8 mg/mL, 6.0 mg/mL系列标准工作液,以峰面积为纵坐标,标准工作液浓度为横坐标,绘制标准曲线。[/align][align=left]如图2~5,[color=black]赤藓糖醇、木糖醇、山梨醇、麦芽糖醇[/color]在1.6mg/mL~6.0 mg/mL浓度范围内线性良好,相关系数R[sup]2[/sup]均在0.999以上。[/align][align=center][/align][align=center][img=,582,328]http://ng1.17img.cn/bbsfiles/images/2017/08/201708100911_03_2222981_3.png[/img][img=,547,322]http://ng1.17img.cn/bbsfiles/images/2017/08/201708100912_01_2222981_3.png[/img][/align][align=center][img=,563,326]http://ng1.17img.cn/bbsfiles/images/2017/08/201708100913_01_2222981_3.png[/img][/align][align=center][img=,560,320]http://ng1.17img.cn/bbsfiles/images/2017/08/201708100917_01_2222981_3.png[/img][/align][align=center][/align]综上,依据《[color=black]GB 5009.279-2016 [/color][color=black]食品安全国家标准[/color][color=black] [/color][color=black]食品中木糖醇、山梨醇、麦芽糖醇、赤藓糖醇的测定》第一法,[/color]使用资生堂CAPCELL PAK NH2 UG80 S5 4.6 mm i.d. × 250 mm(GQAD 05507)色谱柱,以示差折光检测器进行检测,对[color=black]木糖醇、山梨醇、麦芽糖醇和赤藓糖醇[/color]标准品能够得到良好分析结果。在1.6 mg/mL~6.0 mg/mL浓度范围内绘制标准曲线,相关系数R[sup]2[/sup]均在0.999以上,能够得到良好线性关系。[align=center][/align]注: 图中色谱峰线条不平滑是由于图像在复制过程中解像度问题引起的。
关于批准1,3:2,4-二-O-(对氯苯亚甲基)-D-山梨糖醇等3种食品包装材料用添加剂新品种的公告2012年 第11号 根据《食品安全法》和《食品相关产品新品种行政许可管理规定》的规定,经审核,现批准1,3:2,4-二-O-(对氯苯亚甲基)-D-山梨糖醇等3种食品包装材料用添加剂新品种,批准食品包装材料用添加剂均苯四甲酸二酐扩大使用范围。 特此公告。附件: 1. 1,3:2,4-二-O-(对氯苯亚甲基)-D-山梨糖醇等3种食品包装材料用添加剂新品种 2.食品包装材料用添加剂均苯四甲酸二酐扩大使用范围卫 生 部 2012年7月2日
[align=center]GB 5009.279-2016 食品安全国家标准 食品中木糖醇、山梨醇、麦芽糖醇、赤藓糖醇的测定-NQAD[/align]《GB 5009.279-2016 食品安全国家标准食品中木糖醇、山梨醇、麦芽糖醇、赤藓糖醇的测定》第二法中推荐使用蒸发光散射检测器对4种糖醇进行检测。本实验室使用资生堂高灵敏度气溶胶通用型检测器NQAD对该项目进行检测。使用资生堂氨基柱CAPCELL PAK NH2 UG80 S5 4.6 mm i.d. × 250 mm(GQAD 05507)依据国标方法进行分析,可以实现4种糖醇的良好分析(见图1)。[img=,678,525]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030937_01_2222981_3.png[/img][img=,611,257]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030937_02_2222981_3.png[/img]进一步对标准曲线进行绘制,依据国家标准,以峰面积为纵坐标,标准工作液浓度为横坐标,以赤藓糖醇浓度为0.14 mg/mL, 0.21 mg/mL, 0.28 mg/mL, 0.35 mg/mL, 0.42 mg/mL, 0.49 mg/mL,木糖醇、山梨醇、麦芽糖醇浓度为0.10 mg/mL, 0.15 mg/mL, 0.20 mg/mL, 0.25 mg/mL, 0.30 mg/mL, 0.35 mg/mL的混合系列标准工作液,进行标准曲线绘制。如图2~5所示,赤藓糖醇在0.14 mg/mL~0.49 mg/mL浓度范围内,木糖醇、山梨醇、麦芽糖醇在0.1 mg/mL~0.35 mg/mL浓度范围内线性良好,相关系数R[sup]2[/sup]均在0.99以上。[img=,534,330]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030938_01_2222981_3.png[/img][img=,573,327]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030938_02_2222981_3.png[/img][img=,573,326]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030938_03_2222981_3.png[/img][img=,556,342]http://ng1.17img.cn/bbsfiles/images/2017/08/201708030938_04_2222981_3.png[/img]注:图中色谱峰线条不平滑是由于图像在复制过程中解像度问题引起的。
[size=5]GB 13482-1992 食品添加剂 山梨醇酐单油酸酯(斯潘80)[/size]
大家好,我第一次按照药典四部聚山梨酯80(供注射用)中乙二醇二甘醇和三甘醇检测,称量还是按照聚山梨酯20的方法称量配制,浓度一致,使用DB-17色谱柱,其他按照药典方法去做的,然而4个峰的相应值都很低,特别是乙二醇大约在0.6其他几个面积也只有几,面积太小误差非常大,想请教下,这是什么情况,做了几次结果也都是这样,大神们帮忙解答一下,谢谢!
有一根磺化交联的苯乙烯基苯共聚物为填充剂的强阳离子钙型交换柱,按药典在做甘露醇和山梨醇分离度时,两峰重叠,保留时间几乎相同,不知如何处理?减流速?降柱温?请教各位。
在做国标 GB5009. 28 — 2016 食品安全国家标准食品中苯甲酸、山梨酸和糖精钠的测定对照品配制疑惑 标准溶液配制:苯甲酸、山梨酸和糖精钠(以糖精计)标准储备溶液( 1000mg / L ):分别准确称取苯甲酸钠、山梨酸钾和糖精钠 0.118g 、 0. 134g 和 0.117g (精确到 0.0001g ),用水溶解并分别定容至 100mL 。于 4℃贮存,保存期为 6 个月。当使用苯甲酸和山梨酸标准品时,需要用甲醇溶解并定容。红色这句话的意思是想用适量的甲醇溶解,然后在用水定容,还是用甲醇定容,感觉怪怪的?有那位老师可以指导一下, 共享一下经验,谢谢。
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-1996,糖精钠的检测参照GB/T 5009.28-1996,即可开展实验。苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。2 样品前处理的注意事项 GB/T5009.28-1996和GB/T5009.29-1996 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。GB/T5009.29-1996使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。具体操作步骤如下:取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。3 检测仪器的选择虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下:3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29-1996所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。5 选用液相色谱仪的注意事项 按照GB/T5009.29-1996,流动相应为5:95的甲醇:0.02M醋酸铵溶液,但是这个比例仅是个参考值,我们在工作中应根据实际情况进行调节。 为什么用甲醇溶液?甲醇有两个作用,(1)防腐,液相色谱柱最怕流动相长菌,尤其霉菌。甲醇可使蛋白质变性,有杀菌作用。(2)调节流动相极性,这是最重要的一点。甲醇在溶液中比例的较小变化都会使苯甲酸、山梨酸、糖精钠的保留时间发生明显的改变,因此可以通过改变流动相中甲醇含量,以调节这几个组分的出峰和分离,以得到较理想的色谱图。5:95是一个通用的比例,如减少甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间变慢,扩散效应增大,峰形较差,但这三组分的分离情况较好。如增加甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间提前,扩散效应较小,峰形尖锐,但这三组分的分离情况可能受影响,产生重叠。在选择条件时,只能通过实验手段,如配制3:97,4:96,5:95,6:96,7:93的流动相,综合考虑分离效果和分离时间选择最佳比例。不同柱的最适比例不同,举例来说,色谱科公司的液相柱最适比例为4:96,而岛津公司液相柱的最佳比例为7:93。就是同一根柱,一年前和一年后的极性也会有变化,需调节溶液配比。为什么使用0.02M醋酸铵溶液?加入醋酸铵是为了调节离子强度,使待测物的峰形不致于变坏。如果单独检测苯甲酸和糖精钠,加不加醋酸铵没有什么关系,都可以得到较好的峰形;但是检测山梨酸时流动相一定要加醋酸铵,否则得不到一个完整的色谱峰,峰形呈破裂状。醋酸铵溶液浓度不需严格控制,0.01M、0.02M、0.04M均可。苯甲酸、山梨酸、糖精钠在液相上的出峰次序很有特点。在流动相5:95及以下比例时,次序是苯甲酸、山梨酸、糖精钠(注意一下[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]的出峰次序),逐步增大甲醇含量,苯甲酸、山梨酸的出峰时间逐步提前,而糖精钠是出峰时间迅速提前,随着甲醇比例的逐步增大(15%-30%),原先在最后出峰的糖精钠集次和前面的山梨酸、山梨酸重叠,并位于最前面,其次序变为糖精钠、苯甲酸、山梨酸。再提高甲醇浓度,次序不变。用高甲醇比例条件(甲醇15%以上)做出的三种标准物质色谱图峰形较好,出峰时间也较快,但做实际样品时干扰较大;因此建议尽量使用低甲醇比例条件(甲醇5%左右)。6 苯甲酸、山梨酸超标时的判断苯甲酸、山梨酸超标的样品较多,由于它们往往牵涉到一批货物是否合格,因此责任重大。由于该方法定量较准确,因此遇到超标样品时应将精力集中于定性方面。如同时有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]和液相色谱仪,建议用这两种性质相差较大的仪器进行对照,如定量结果差不多,即可确认。如只有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],应利用其在填充柱保留时间稳定的特性,同时进五针标准液和五针样品液(注:峰面积应差不多,否则需对一方按比例稀释),如标准和样品液的保留时间相差时间超过1 秒,可认为不是。(如进针的技术不过关,请不要做此实验)如用液相色谱仪,当检测器为二极管阵列检测器时,根据保留时间和紫外吸收图结合定性,当只有紫外检测器时,改检测波长为220nm,230nm,250nm,重复进标准和样品液,由标准和样品在不同波长的峰高比值看是否吻合。如有微生物检测手段,可加样品于有菌培养基中,观察有无抑菌现象,如无抑菌现象则无防腐剂。不是很推荐用双柱法,因为有时柱极性相差不大,反而会影响最终判断。7 糖精钠超标时的判断当检测糖精钠超标时,除了采用二极管阵列检测器或波长验证,还可以利用糖精钠的荧光特性,用荧光检测器进行验证。荧光条件是激发波长为277nm,荧光波长为410nm。只有当用荧光检测器和用紫外检测器做出的定量结果相差不多,才可以判断为是。还有一个简单粗糙、却也行之有效的验证方法,即感官法。糖精钠是一种甜味剂,用舌头可以感觉到它的甜味,如果含量超标,一定能尝出来。8 标准溶液的配制贮存问题苯甲酸、山梨酸、糖精钠的标准溶液如用水、乙醇作基体,一般几个月后会严重降解,。如用甲醇溶解再放于冰箱冷冻层,可保持稳定一两年。因此推荐用甲醇作溶剂。在配制标准溶液时,初学者常犯的错误多为用甲醇溶解苯甲酸钠,用水溶解苯甲酸,晃了半天才发现怎么也不没溶解。应该用弱碱性水溶解苯甲酸钠、山梨酸钾,用甲醇溶解苯甲酸、山梨酸。9 苯甲酸、山梨酸的应用范围首先应注意到,并不是所有食品都需要加入防腐剂,只有那些富含营养物质,且需要长时间暴露于空气的才有这样的需要,否则对厂家来说会增加不必要的成本。酱油、酱料、咸菜、浓缩果汁等由于开封后不可能短期内吃完,月饼等需在货架上摆放,如不加防腐剂很快会发霉变质,有添加防腐剂的必要。而利乐装或易拉罐装的饮料由于很快可以食用完毕,即在细菌大量繁殖前己被消化了,因而没有添加的必要。苯甲酸、山梨酸如果要起到防腐的作用,含量就不能太低。如果我们检测样品时只有几个ppm的浓度,有可能是从原料中带来的或由其它添加剂转化来的,而不是厂家出于防腐目的加入的。苯甲酸、山梨酸也只是防腐剂中的两种。并不是所有需要加入防腐剂的食品都会添加苯甲酸、山梨酸,有可能使用防霉剂或其它种类的防腐剂,或自行规定需冷藏(如某些月饼)。因此有些食品检测不出也属正常。另外,我们应该比较清楚地理解苯甲酸与苯甲酸钠、山梨酸与山梨酸钾之间的关系。在食品中添加防腐剂通常以苯甲酸钠、山梨酸钾形式加入,它们不易汽化,易溶于水,但不溶于甲醇等有机试剂;而苯甲酸、山梨酸易汽化,易溶于有机试剂,但
[size=5]GB 13481-1992 食品添加剂 山梨醇酐单硬脂酸酯(斯潘60)[/size]
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-1996,糖精钠的检测参照GB/T 5009.28-1996,即可开展实验。苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。2 样品前处理的注意事项 GB/T5009.28-1996和GB/T5009.29-1996 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。GB/T5009.29-1996使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。具体操作步骤如下:取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。3 检测仪器的选择虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下:3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29-1996所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。5 选用液相色谱仪的注意事项 按照GB/T5009.29-1996,流动相应为5:95的甲醇:0.02M醋酸铵溶液,但是这个比例仅是个参考值,我们在工作中应根据实际情况进行调节。 为什么用甲醇溶液?甲醇有两个作用,(1)防腐,液相色谱柱最怕流动相长菌,尤其霉菌。甲醇可使蛋白质变性,有杀菌作用。(2)调节流动相极性,这是最重要的一点。甲醇在溶液中比例的较小变化都会使苯甲酸、山梨酸、糖精钠的保留时间发生明显的改变,因此可以通过改变流动相中甲醇含量,以调节这几个组分的出峰和分离,以得到较理想的色谱图。5:95是一个通用的比例,如减少甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间变慢,扩散效应增大,峰形较差,但这三组分的分离情况较好。如增加甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间提前,扩散效应较小,峰形尖锐,但这三组分的分离情况可能受影响,产生重叠。在选择条件时,只能通过实验手段,如配制3:97,4:96,5:95,6:96,7:93的流动相,综合考虑分离效果和分离时间选择最佳比例。不同柱的最适比例不同,举例来说,色谱科公司的液相柱最适比例为4:96,而岛津公司液相柱的最佳比例为7:93。就是同一根柱,一年前和一年后的极性也会有变化,需调节溶液配比。为什么使用0.02M醋酸铵溶液?加入醋酸铵是为了调节离子强度,使待测物的峰形不致于变坏。如果单独检测苯甲酸和糖精钠,加不加醋酸铵没有什么关系,都可以得到较好的峰形;但是检测山梨酸时流动相一定要加醋酸铵,否则得不到一个完整的色谱峰,峰形呈破裂状。醋酸铵溶液浓度不需严格控制,0.01M、0.02M、0.04M均可。苯甲酸、山梨酸、糖精钠在液相上的出峰次序很有特点。在流动相5:95及以下比例时,次序是苯甲酸、山梨酸、糖精钠(注意一下[url=https://insevent.instrument.com.cn/t/Mp]气相[/url]的出峰次序),逐步增大甲醇含量,苯甲酸、山梨酸的出峰时间逐步提前,而糖精钠是出峰时间迅速提前,随着甲醇比例的逐步增大(15%-30%),原先在最后出峰的糖精钠集次和前面的山梨酸、山梨酸重叠,并位于最前面,其次序变为糖精钠、苯甲酸、山梨酸。再提高甲醇浓度,次序不变。用高甲醇比例条件(甲醇15%以上)做出的三种标准物质色谱图峰形较好,出峰时间也较快,但做实际样品时干扰较大;因此建议尽量使用低甲醇比例条件(甲醇5%左右)。6 苯甲酸、山梨酸超标时的判断苯甲酸、山梨酸超标的样品较多,由于它们往往牵涉到一批货物是否合格,因此责任重大。由于该方法定量较准确,因此遇到超标样品时应将精力集中于定性方面。如同时有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]和液相色谱仪,建议用这两种性质相差较大的仪器进行对照,如定量结果差不多,即可确认。如只有[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url],应利用其在填充柱保留时间稳定的特性,同时进五针标准液和五针样品液(注:峰面积应差不多,否则需对一方按比例稀释),如标准和样品液的保留时间相差时间超过1 秒,可认为不是。(如进针的技术不过关,请不要做此实验)如用液相色谱仪,当检测器为二极管阵列检测器时,根据保留时间和紫外吸收图结合定性,当只有紫外检测器时,改检测波长为220nm,230nm,250nm,重复进标准和样品液,由标准和样品在不同波长的峰高比值看是否吻合。如有微生物检测手段,可加样品于有菌培养基中,观察有无抑菌现象,如无抑菌现象则无防腐剂。不是很推荐用双柱法,因为有时柱极性相差不大,反而会影响最终判断。7 糖精钠超标时的判断当检测糖精钠超标时,除了采用二极管阵列检测器或波长验证,还可以利用糖精钠的荧光特性,用荧光检测器进行验证。荧光条件是激发波长为277nm,荧光波长为410nm。只有当用荧光检测器和用紫外检测器做出的定量结果相差不多,才可以判断为是。还有一个简单粗糙、却也行之有效的验证方法,即感官法。糖精钠是一种甜味剂,用舌头可以感觉到它的甜味,如果含量超标,一定能尝出来。8 标准溶液的配制贮存问题苯甲酸、山梨酸、糖精钠的标准溶液如用水、乙醇作基体,一般几个月后会严重降解,。如用甲醇溶解再放于冰箱冷冻层,可保持稳定一两年。因此推荐用甲醇作溶剂。在配制标准溶液时,初学者常犯的错误多为用甲醇溶解苯甲酸钠,用水溶解苯甲酸,晃了半天才发现怎么也不没溶解。应该用弱碱性水溶解苯甲酸钠、山梨酸钾,用甲醇溶解苯甲酸、山梨酸。9 苯甲酸、山梨酸的应用范围首先应注意到,并不是所有食品都需要加入防腐剂,只有那些富含营养物质,且需要长时间暴露于空气的才有这样的需要,否则对厂家来说会增加不必要的成本。酱油、酱料、咸菜、浓缩果汁等由于开封后不可能短期内吃完,月饼等需在货架上摆放,如不加防腐剂很快会发霉变质,有添加防腐剂的必要。而利乐装或易拉罐装的饮料由于很快可以食用完毕,即在细菌大量繁殖前己被消化了,因而没有添加的必要。苯甲酸、山梨酸如果要起到防腐的作用,含量就不能太低。如果我们检测样品时只有几个ppm的浓度,有可能是从原料中带来的或由其它添加剂转化来的,而不是厂家出于防腐目的加入的。苯甲酸、山梨酸也只是防腐剂中的两种。并不是所有需要加入防腐剂的食品都会添加苯甲酸、山梨酸,有可能使用防霉剂或其它种类的防腐剂,或自行规定需冷藏(如某些月饼)。因此有些食品检测不出也属正常。另外,我们应
样品主成分是葡甲胺 杂质是有葡萄糖 山梨醇 葡萄糖酸 葡亚胺 自制中间体 有没有合适的色谱柱?
做苯甲酸,山梨酸和糖精钠很长时间了,一直分离的很好,峰形也很好,但最近一个月,几个峰开始拖尾严重,以致到现在山梨酸的保留时间延长和糖精钠根本分不开了,请问大家有碰到这种现象吗?我用的流动相是甲醇:乙酸铵=5.5:94.5。我最近换了针筒过滤器,它会带来这样的影响吗?请大家多给宝贵意见。谢谢!
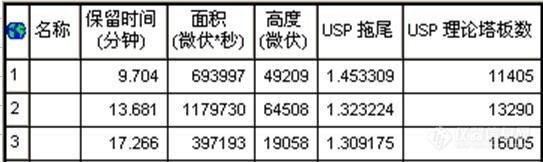
很多版友经常会发帖说苯甲酸、山梨酸、糖精钠的检测遇到问题,这次也有幸拿了月旭公司自主研发的新柱子Topsil C18柱试用,在对柱子评价的同时,也谈谈这3个项目的检测吧。色谱条件:流动相:甲醇+0.02mol/L乙酸铵溶液=5+95色谱柱:Topsil C18柱(4.6*250mm,5u)流速:1.0mL/min检测器:UV 230nm先看看国家标准的参考谱图吧,你可以跟我的图谱对照一下保留时间,峰行,峰位置等http://ng1.17img.cn/bbsfiles/images/2011/05/201105031108_291948_1608710_3.jpg这个是我用Topsil C18柱在这个色谱条件下测试的色谱图,附有理论塔板数的计算结果http://ng1.17img.cn/bbsfiles/images/2011/05/201105031111_291950_1608710_3.jpghttp://ng1.17img.cn/bbsfiles/images/2011/05/201105031111_291951_1608710_3.jpg下面这个图是用其他品牌的进口色谱柱的测试色谱图,已经不记得是不是全新的色谱柱测试的图了,供评价参考吧http://ng1.17img.cn/bbsfiles/images/2011/05/201105031113_291952_1608710_3.jpghttp://ng1.17img.cn/bbsfiles/images/2011/05/201105031113_291953_1608710_3.jpg柱子评价:1.很多版友都说,推荐一个好点的色谱柱做苯甲酸、山梨酸、糖精钠,那你的要求又是什么呢?分离度好、柱效高?其实这3个项目是很好做的,随便用一根C18柱就可以做,到是有一点,好的色谱柱寿命长啊,可是这点评试用是体现不出来的,而且跟你的样品基质也有很大关系。2.如果说分离度、柱效,这个Topsil C18柱子还是挺不错。苯甲酸、山梨酸、糖精钠检测的几点看法:1.有些人经常说山梨酸和糖精钠分不开,问题会出在哪里呢?几个可能的原因:一是你的柱子可以根据保留时间减少流动相甲醇的量,二是过滤流动相的过滤器尽量不要含甲醇,所以过滤前用水过滤下冲洗,三是柱温的设定,不要太高,温度对糖精钠的保留影响很大2.如果你走了2个泵,有些仪器泵精度不够高,5%的甲醇本身就很小,走仪器混合会出现重现不好。这个原因也是存在的,并不是不可能,尽量采用配置混合好的流动相。3.如果是3个混合在一起的标准溶液,苯甲酸很容易降解,放置时间不长

李少晖目录第1章 认识D-甘露糖醇11.1 D-甘露糖醇的性质1第2章 D-甘露糖醇的生产22.1生产工艺22.1.1海带提取法22.1.2葡萄糖电化学还原22.1.3蔗糖水解催化氢化法2第3章D-甘露糖醇在食品中的应用43.1 D-甘露糖醇在食品中的优点4第4章 D-甘露糖醇在其他领域上的应用64.1生产聚醚64.2大功率的电解电容64.3在医药方面上的应用6第5章 D-甘露糖醇的发展趋势75.1市场情况75.2 近年产品货紧价扬的原因分析75.2.1提取法生产成本的增高和产量的降低75.2.2国际市场供货量的降低75.2.3人工合成法的普及不足7第6章 对D-甘露糖醇的展望8第7章 D-甘露醇的产品标准、限量标准及检测标准介绍97.1产品标准及最大使用量97.2甘露醇的检验97.2.1定性检测97.2.2定量检测97.2.2.1碘量法97.2.2.2薄层层析法97.2.2.3比色法10[align=left][font='times new roman'][size=21px][color=#000000]第1章 [/color][/size][/font][font='times new roman'][size=21px][color=#000000]认识D-甘露糖醇[/color][/size][/font][/align][font='calibri'][size=14px]长期以来,[/size][/font][font='calibri'][size=14px]D-[/size][/font][font='calibri'][size=14px]甘露[/size][/font][font='calibri'][size=14px]糖[/size][/font][font='calibri'][size=14px]醇生产的发展受到原料来源的限制,与山梨醇相似,生产工艺短,主要用途成本低的影响。[/size][/font][font='calibri'][size=14px]但[/size][/font][font='calibri'][size=14px]随着[/size][/font][font='calibri'][size=14px]D-[/size][/font][font='calibri'][size=14px]甘露[/size][/font][font='calibri'][size=14px]糖[/size][/font][font='calibri'][size=14px]醇应用的不断发展,原料来源的多样化、成本的降低以及[/size][/font][font='calibri'][size=14px]D-甘露糖[/size][/font][font='calibri'][size=14px]醇的独特用途,预示着[/size][/font][font='calibri'][size=14px]D-[/size][/font][font='calibri'][size=14px]甘露[/size][/font][font='calibri'][size=14px]糖[/size][/font][font='calibri'][size=14px]醇将是一种前景广阔的精细化工产品。[/size][/font][font='calibri'][size=14px]1.1 [/size][/font][font='calibri'][size=14px]D-甘露糖醇的性质[/size][/font][font='calibri'][size=14px]D-[/size][/font][font='calibri'][size=14px]甘露[/size][/font][font='calibri'][size=14px]糖[/size][/font][font='calibri'][size=14px]醇[/size][/font][font='calibri'][size=14px]([/size][/font][font='calibri'][size=14px]D- mannitl、D- mannita[/size][/font][font='calibri'][size=14px]l、[/size][/font][font='calibri'][size=14px]mannite、manna sugar)学名己六醇[CH[/size][/font][font='calibri'][size=14px]8[/size][/font][font='calibri'][size=14px](OH)[/size][/font][font='calibri'][size=14px]6[/size][/font][font='calibri'][size=14px]],又称甘露醇、木蜜醇,分子式C[/size][/font][font='calibri'][size=14px]6[/size][/font][font='calibri'][size=14px]H[/size][/font][font='calibri'][size=14px]14[/size][/font][font='calibri'][size=14px]O[/size][/font][font='calibri'][size=14px]6[/size][/font][font='calibri'][size=14px]。[/size][/font][font='calibri'][size=14px]D-甘露糖醇的化学性质稳定,对稀酸、稀碱、热较稳定,在空气中不氧化。具有多元醇的通性,其羟基具有较强的反应性能,可以通过取代、醇化、醚化、缩合等生成一系列的衍生物或中间体,中间体再进一步合成获得更多的衍生物。[/size][/font][font='calibri'][size=14px]D-甘露糖醇是一种[/size][/font][font='calibri'][size=14px]无色至白色针状或斜方柱状晶体或结晶性粉末。无臭,具有清凉甜味[/size][/font][font='calibri'][size=14px],[/size][/font][font='calibri'][size=14px]甜度约为蔗糖的57%~72%[/size][/font][font='calibri'][size=14px],[/size][/font][font='calibri'][size=14px]每g产生8.37J热量,约为葡萄糖的一半。含少量山梨糖醇。相对密度1.49[/size][/font][font='calibri'][size=14px],[/size][/font][font='calibri'][size=14px]吸湿性极小。水溶液稳定。溶于水(5.6g/100ml,20℃)及甘油(5.5g/100ml)[/size][/font][font='calibri'][size=14px],[/size][/font][font='calibri'][size=14px]略溶于乙醇(1.2g/100ml)[/size][/font][font='calibri'][size=14px],[/size][/font][font='calibri'][size=14px]溶于热乙醇。几乎不溶于大多数其他常用有机溶剂。20%水溶液的pH值为5.5~6.5。[/size][/font][font='calibri'][size=14px]D-甘露糖醇的红外光谱图见图1。[/size][/font][font='calibri'][size=14px][1][/size][/font][font='calibri'][size=14px]甘露醇与山梨醇[D (L)- sorbitol]、艾杜糖醇[D (L)- iditol]、 塔里糖醇 [D (L)- talitd][/size][/font][font='calibri'][size=14px]、[/size][/font][font='calibri'][size=14px]卫矛醇[dulcitol]、蒜糖醇[allitd ]互为同分异构体[/size][/font][font='calibri'][size=14px],因[/size][/font][font='calibri'][size=14px]具有多元醇的化学性质,[/size][/font][font='calibri'][size=14px]所以[/size][/font][font='calibri'][size=14px]在医药食品、纺织化工、火工等方面大量应用。[/size][/font][align=center][/align][align=center][/align][align=center][font='times new roman'][size=21px][color=#000000]第2章 [/color][/size][/font][font='times new roman'][size=21px][color=#000000]D-甘露糖醇的生产[/color][/size][/font][/align][font='calibri'][size=14px]2.1[/size][/font][font='calibri'][size=14px]生产工艺[/size][/font][font='calibri'][size=14px]D-甘露糖醇是第一个从自然界发现的结晶糖醇,也是目前唯一从自然界植物提取具有工业价值的精醇。D-甘露糖醇广泛存在于自然界的海藻、水果、植物的叶和杆中,它最早发现存在于南瓜、洋葱、蘑菇以及褐海藻中。1806年,普鲁斯特(Proust)首先从甘露蜜树(manna ash)中分离得到,甘露醇由此得名,也由此开创了用热乙醇或其他可选溶媒从以树汁或其他天然原料中提取甘露醇的先例。[/size][/font][font='calibri'][size=14px][2][/size][/font][font='calibri'][size=14px] D-甘露糖醇的生产方法颇多,但大部分产物都不是纯净物,是山梨醇和甘露醇的混合物,如果要得到单一产品,必须经过分离提纯。[/size][/font][font='calibri'][size=14px]2.1.1海带提取法[/size][/font][font='calibri'][size=14px] 其工艺过程:将提碘后的海带浸泡、加碱中和,经电渗析、蒸发浓缩、冷却结晶、分离,除去无机盐得粗品。再溶解、脱色、过滤、离子交换、精过滤、蒸发浓缩、冷却结晶、分离干燥得到成品。原料海带可生产三种化工产品:海参藻酸钠、精制碘、甘露醇。甘露醇是在前两种产品加工完后,在废液中进一步提取而制成,约10t海带可得1t甘露醇。[/size][/font][font='calibri'][size=14px]2.1.2葡萄糖电化学还原[/size][/font][font='calibri'][size=14px] 以葡萄糖为原料,将葡萄糖电解,再中和、蒸发、除盐、结晶、精制、干燥得到甘露醇,此法电解转化率为98%-99.6%。[/size][/font][font='calibri'][size=14px]2.1.3蔗糖水解催化氢化法[/size][/font][align=left][font='宋体'][size=16px]蔗糖与水1:1比例投入溶解锅,加热溶解,用盐调pH至2.5-4.0,然后继续加热至沸,温度控制在90-105[/size][/font][font='宋体'][size=16px][color=#000000]℃[/color][/size][/font][font='宋体'][size=16px][color=#000000]下1-2小时(预处理),冷却备用。[/color][/size][/font][font='宋体'][size=16px]经预处理后的糖水经阴、阳离子交换树脂提纯,再进入氢化釜。以雷尼镍为催化剂,用量为投料量的5-10%,在氢气压力为4.0MPa、温度100-150℃、pH值为6-8的条件下进行氢化反应,反应时间1-2小时。[/size][/font][/align][align=left][font='宋体'][size=16px]分离出催化剂后的反应物料,再经阴-阳离子交换树脂净化,以除去残余的催化剂和反应生成的色素,然后进入真空浓缩器将物料浓缩至60-70%,送至第一结晶釜结晶,结晶温度控制在10-30℃,时间10-16小时,然后离心分离,结晶为粗甘露醇 母液即为工业山梨醇。[/size][/font][font='宋体'][size=16px] 将上述第一次结晶的粗甘瞎醇投人二次结晶釜,加水配成50-60%浓度进行第二次结晶,结晶条件与第一次相同,母液为山梨醇和甘露醇混合液,并人第一次结晶物料,得到的晶体在90-105℃温度下烘干,即得工业级甘露醇。[/size][/font][font='宋体'][size=16px][3、4][/size][/font][font='宋体'][size=16px] 将第二次结晶的甘露醇用蒸馏水配至40-50%浓度,加人1-2%活性炭,搅拌加热至90-105℃,保持1-1.5小时,趁热压滤进行第三次结晶,结晶条件控制与第一、二次相同。再经离心分离,在90-105℃温度下烘干,即得到医药级甘露醇,质量符合国家药典85版标准。[/size][/font][font='宋体'][size=16px] 将上述第一次结晶的山梨醇母液真空蒸发,浓缩至浓度为70-80%,进行重结晶,结晶温度控制在10-30℃,时间24-48小时,同时加人1-2%甘露醇作晶种,结晶完毕进行压滤,滤液经阴-阳交换柱处理,即得到医药级山梨醇,比旋度小于5.3,滤饼并人第一次结晶物料中。[/size][/font][font='宋体'][size=16px][5][/size][/font][font='宋体'][size=16px] 采用该工艺生产甘露醇比海带提取法成本降低50%,且原料不受地区限制,各地均可生产。[/size][/font][/align][align=left][font='times new roman'][size=17px]2.1.4[/size][/font][font='times new roman'][size=17px]果糖催化氢化制甘露醇[/size][/font][/align][align=left][font='times new roman'][size=17px]将淀粉水解为葡萄糖后,在异构酶存在下,或者化学法转化成果糖、葡萄糖、甘露糖的混合液,然后催化加氢制甘露醇。上述方法,氢化后得到的产物是以山梨醇、甘露醇为主的混合物,通常采用结晶法或吸附分离法精制提纯。[/size][/font][/align][align=left][font='宋体'][size=16px]在上述生产方法中,海带提取法,采用海带碘和海藻酸钠废水提取,作为一种综合利用,这种方法不会被淘汰,但由于海藻资源的限制,难以扩大产量。葡萄糖电化学还原法的电解能耗较高,目前已停止工业生产。果糖糖浆的催化还原法,虽然甘露醇收率高,但由于工艺时间长,技术难度大,成本高,不适合推广采用。以蔗糖为原料,将果糖和葡萄糖进行水解,然后部分葡萄糖转化为甘露糖,[/size][/font][font='宋体'][size=16px]成为[/size][/font][font='宋体'][size=16px]果糖、葡萄糖和甘露糖的混合[/size][/font][font='宋体'][size=16px]液[/size][/font][font='宋体'][size=16px],然后氢化生成甘露醇[/size][/font][font='宋体'][size=16px],[/size][/font][font='宋体'][size=16px]原料来源丰富,相对工艺时间短,生产成本低。这是今后发展甘露醇生产的一种很有前途的方法。[/size][/font][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=center][font='黑体'][size=21px]第3章D-甘露糖醇在食品中的应用[/size][/font][/align][font='黑体'][size=18px]3.1 [/size][/font][font='黑体'][size=18px]D-甘露糖醇在食品中的优点[/size][/font][align=left][font='宋体'][size=16px]多年来,人们对甘露醇的医学作用进行了许多研究。然而,由于甘露醇来源的短缺和市场供应的波动,甘露醇在食品中的应用研究较少。[/size][/font][font='宋体'][size=16px]但如今[/size][/font][font='宋体'][size=16px]随着合成甘露醇生产工艺的发展,甘露醇的生产规模[/size][/font][font='宋体'][size=16px]的[/size][/font][font='宋体'][size=16px]扩大,生产成本和价格趋于稳定[/size][/font][font='宋体'][size=16px],[/size][/font][font='宋体'][size=16px]甘露醇进入食品行业势在必行。[/size][/font][/align][font='times new roman'][size=17px]D-甘露糖醇作为食品添加剂可用于食品工业中,具有以下优点:[/size][/font][font='calibri'][size=17px]①D-甘露糖醇在人体中的一次代谢途径与胰岛素无关,摄入后不会引起血液葡萄糖与胰岛素水平太大幅度的波动,可以给糖尿病病人食用。[/size][/font][font='cambria'][size=16px]②D-甘露糖醇具有清凉的甜味,其甜度相当于蔗糖的0.6倍,其溶解吸热为-29Cal/g,相当于木糖醇的76%,利用这点,可以应用在口香糖上,作为甜味剂使用。[/size][/font][font='calibri'][size=16px]③D-甘露糖醇不会作为口腔微生物的营养源,还可以抑制突变链球菌的生长繁殖,可以用于防止牙齿龋变的食品。[/size][/font][font='宋体'][size=16px]④D-甘露糖醇与山梨醇、木糖醇等不同,它不易吸潮,20℃时,其溶解度仅为18克/100克,远比山梨醇、木糖醇与麦芽糖醇等低。因此,它可以用作隔潮剂,当用于口香糖、胶姆糖等其他食品中,可防止加工使用过程中的粘连。[/size][/font][font='宋体'][size=16px]⑤D-甘露糖醇没有还原基,不参与美拉德反应,所以用于烘烤食品,可以保持良好的颜色,不容易焦化。[/size][/font][font='宋体'][size=16px][6][/size][/font][font='宋体'][size=16px]由于上述优点,甘露醇在食品工业中得到了广泛的应用。比如可作为一种低热值和低糖的甜味剂,用于糖尿病肥胖患者的食品使用,也适合减肥者服用。甘露醇在食品中被用作无糖口香糖的甜味剂,因为它不吸收水分。用于防粘剂也得到了广泛的应用。另外,甘露醇是用来制作冰淇淋、糖果巧克力的风味糖主,也就是所谓的巧克力皮酥脆,可以保持产品硬皮,效果很好。甘露醇还可以隐藏其他食品添加剂的坏味道,如糖精的铁锈味和其他物质的苦味,因此可以用高倍甜味剂混合用于饮料、糖浆及其他食品。如蜜饯、果酱、果冻等等。[/size][/font][font='宋体'][size=16px]目前,甘露醇是食品中使用最多的无糖口香糖甜味剂或抗粘剂。[/size][/font][font='宋体'][size=16px]其次[/size][/font][font='宋体'][size=16px],它可以为冰淇淋和糖果制作巧克力糖果外套。甘露醇还可用作充填剂和质量改良剂,防止结块。此外,它还可以添加到各种食物中。为了延长保质期[/size][/font][font='宋体'][size=16px],[/size][/font][font='宋体'][size=16px]甘露醇与食品中其他成分相容性好,与其他甜味剂有协同作用。与[/size][/font][font='宋体'][size=16px]高倍[/size][/font][font='宋体'][size=16px]甜味剂相结合,可获得最佳甜度,降低成本,提高产品稳定性和贮存性能。制作巧克力糖衣时,如果使用甘露醇,可添加其他乙二醇(如麦芽糖醇氢化淀粉水解物等),以提高人体耐受性,降低吸热效应。[/size][/font][font='宋体'][size=16px]甘露醇作为多元醇是不能被口腔微生物利用的,服用后也不会增加口腔酸度。这就意味着,不会促成牙垢与形成龋齿。美国牙医协会认为,包括甘露醇在内的多元醇可作为蔗糖的替代品,可以保护牙齿。美国食品与医药管理局同意在使用甘露醇等多元醇的无糖食品上标注“不形成龋齿”的宣传。[/size][/font][font='宋体'][size=16px]而D-甘露糖醇也是国际上公认的在食品工业上使用是安全的。目前我国食品添加剂使用标准中糖果制品最大的使用量是可按生产需要适量使用。[/size][/font][font='宋体'][size=16px][7][/size][/font][align=left][font='宋体'][size=16px]但是,多元糖醇在服用时,有一个共同特点,即超过一定量时,会引起肠胃不适或腹泻。这是因为大部分糖醇在肠道中吸收速度要比糖难得多,小肠内壁未被吸收的糖醇会产生很高的渗透压,这样导致小肠壁粘膜表面产生水流,故引起了腹泻。而未消化吸收的糖醇进入大肠中,,被肠道细菌利用,发酵又产生大量挥发性物质,如果超出了能通过血液重新吸收和随粪便排出的数量极限,就会产生肠胃胀气。这方面,甘露醇和木糖醇、山梨醇都有相同情况。所以美国政府规定,如果一次性服用甘露醇可能超过20克时,必须在食品标志上加以说明。[/size][/font][font='宋体'][size=16px][6][/size][/font][/align][align=left][font='宋体'][size=16px]在美国,50%的糖醇用于食品,在日本,60%的糖醇用于食品,而我国现在食品中糖醇的应用还不到10%。中国有13亿人口,对甜味剂及功能性甜味剂的需求量大,市场潜力巨大,大力开发糖醇在食品中的应用是食品生产商及糖醇企业的当务之急。[/size][/font][/align][align=left][/align][align=center]第4章 [font='黑体'][size=21px]D-甘露糖醇在其他领域上的应用[/size][/font][/align][align=left][font='黑体'][size=18px]4.1生产聚醚[/size][/font][/align][align=left][font='宋体'][size=16px]在精细化工上,甘露醇可用于生产聚醚,作为制造耐高温泡沫塑料,用于保温与消防。甘露醇聚醚制造的泡沫塑料其品质优良,并可以耐温高达180[/size][/font][font='宋体'][size=16px]℃[/size][/font][font='宋体'][size=16px],这是其他多元醇生产的聚醚制造的泡沫塑料所无法比较的,所以用于特殊管道保温时,必须要采取甘露醇聚醚。[/size][/font][/align][align=left][font='黑体'][size=18px]4.2大功率的电解电容[/size][/font][/align][align=left][font='宋体'][size=16px]如大型铝电解用的电解电容器,其中的电解液中必须加入甘露醇,以降低电解液的饱和蒸汽压,抑制氧化膜的水合作用,提高电容器的高温稳定性和电解液的高低温特性。南通江海电容器厂使用国产甘露醇配制的中高压工作电解液,使得在105℃下的铝电解电容器寿命从2000小时突破到5000小时。[/size][/font][/align][align=left][font='黑体'][size=18px]4.3在医药方面上的应用[/size][/font][/align][align=left][font='宋体'][size=16px]甘露醇的利尿脱水作用。甘露醇可以减轻脑水肿,使血糖度下降和离血管舒张,从而发送离血流,保持了脑的自动调节作用。还可增加冠脉的血流,最大程度地降低缺血心肌的损害程度和范围。正因为甘露醇在医疗上有以上重要作用,所以在所有的医院里,甘露醇是利尿排水的首选药物,甘露醇注射液都属必备药物之一。[/size][/font][font='宋体'][size=16px] [/size][/font][font='宋体'][size=16px]由于甘露醇在血管中,可以从体液中吸收水份,从而起到了扩张血管的作用。所以在医药方面[/size][/font][font='宋体'][size=16px],[/size][/font][font='宋体'][size=16px]甘露醇广泛用于脑血管舒张剂,用于治疗脑血管梗塞。由于它的扩张血管作用,甘露醇可以间接起到降低血压,舒筋活血的作用。[/size][/font][font='宋体'][size=16px] [/size][/font][font='宋体'][size=16px]甘露醇在人的肠胃中不易吸收,所以它还是一种温和的轻泻剂,对于长期性的便泌有良好的治疗作用。[/size][/font][/align][align=left][font='宋体'][size=16px]甘露醇可用于制备醒酒剂,目前在市场上可 以见到的醒酒药片, 其80%以上成分是甘露醇,再加一些葛根提取液或葛根粉制成。[/size][/font][font='宋体'][size=16px][6][/size][/font][/align][align=left][font='宋体'][size=16px]甘露醇具有保健功能性的作用,也越来越多的人了解它,而且随着甘露醇生产的扩大以及人们的保健意识的提高,甘露醇的功能与作用也会有愈来愈多的人认识,甘露醇也将开始大规模应用与各个领域。[/size][/font][/align][align=left][/align][align=left][/align][align=left][/align][align=left][/align][align=center]第5章 [font='黑体'][size=21px]D-甘露糖醇的发展趋势[/size][/font][/align][font='黑体'][size=18px]5.1市场情况[/size][/font][align=left][font='宋体'][size=16px]目前,我国甘露醇生产能力小,生产企业大多是中小企业,生产成本无法与国外先进企业相竞争,必须实现规模化、系列化生产,提高经济效益,同时亟须实现下游产品系列化、装置通用化、上下游一体化。[/size][/font][font='宋体'][size=16px] [/size][/font][font='宋体'][size=16px]国内化学合成法比较成熟。南宁化工研究设计院已成功开发出以蔗糖为原料,经水解氢化、分离结晶制备甘露醇的方法和以葡萄糖为原料,异构后加氢,分离结晶制备甘露醇技术,并建有数套工业化装置,其工艺技术简单,环境污染小,产品质量好,收率高,生产成本低、适合大规模工业化生产。南宁化学制药公司已经采用该技术,开工建设1万t/a的装置。无锡轻工大学以淀粉为原材料,采用化学-酶双异构化法、制备高含量的甘露糖和果糖(质量分数分别为43.0%[/size][/font][font='宋体'][size=16px]和[/size][/font][font='宋体'][size=16px]21.5%),将反应液氢化可获得质量分数为53.5%的甘露醇。该工艺投资少,生产易连续化、甘露醇得率高,从而较大程度降低了甘露醇的生产成本,是一个有应用价值的新生产方法。[/size][/font][font='黑体'][size=16px][8][/size][/font][/align][align=left][font='黑体'][size=18px]5.2[/size][/font][font='黑体'][size=18px] 近年产品货紧价扬的原因分析[/size][/font][/align][align=left][font='黑体'][size=17px]5.2.1提取法生产成本的增高和产量的降低[/size][/font][/align][align=left][font='宋体'][size=16px]传统工艺仍然是我国甘露醇的主导生产方法,我国甘露醇生产地的沿海地区,劳动力成本大幅度上涨,海藻类植物随着过度开发导致产量日益减少,加剧了甘露醇产品成本的上扬,带动其它辅料价格也相应上涨,对甘露醇价格的,上涨产生了很大影响。虽然近年来甘露醇产量有一定的增长,但仍远远不能满足市场日益增长的需要。我国以传统的生产方式产出的甘露醇,在今后较长时期内,产量将会逐年下降,市场用量则不断上升,使供求缺口继续扩大。[/size][/font][/align][align=left][font='黑体'][size=17px]5.2.2国际市场供货量的降低[/size][/font][/align][align=left][font='宋体'][size=16px]世界上甘露醇最大的生产国家及出口国-智利、巴西的产量大幅度减少,导致国际市场供求总量失衡,牵动价格上扬。我国是甘露醇的出口大国之一,国际市场上的甘露醇货稀价扬,必然会牵动国内市场的上涨。此外海带资源日趋减少,也导致价格上涨。[/size][/font][/align][align=left][font='黑体'][size=17px]5.2.3人工合成法的普及不足[/size][/font][/align][align=left][font='宋体'][size=16px]目前我国的人工合成甘露技术已经与世界同步,但生产能力和产量还比较低,[/size][/font][/align][align=left][font='宋体'][size=16px]没有发挥出应有的潜力,这也是造成甘露醇货紧价扬的重要原因[/size][/font][font='宋体'][size=16px];[/size][/font][font='宋体'][size=16px]值得庆幸的是在广西南宁一条5 kt/a( 总醇)甘露醇-山梨醇生产线已经投人运行,这将对缓和我国甘露醇供不应求的局面产生积极的作用。[/size][/font][/align][align=left][/align][align=center]第6章 [font='黑体'][size=21px]对D-甘露糖醇的展望[/size][/font][/align][align=center][/align][align=left][font='宋体'][size=16px]目前,我国的甘露醇市场-直呈现供不应求的局面,预计这种供不应求的现象在一定范围内还将持续一段时间,而且随着人们生活水平的提高,这种供不应求的局面还可能进一步加强。因此有条件的企业可以考虑新建或扩建生产装置,以提高我国的甘露醇的生产能力,满足国内外市场的需求。[/size][/font][/align][align=left][font='宋体'][size=16px]但是,也应该清醒地看到:由于甘露醇的市场状况,目前国内不少企业正在投资建设生产装置或在现 有装置上进行扩产改造,国家一定要加强宏观调控,防止一哄而上,出现生产能力和产量过剩的局面。此外,在市场经济条件下,企业的自主权增大,筹集资金的渠道较多,要想避免出现能力和产量过剩的局面,除国家进行必要的宏观调控外,主要依靠企业自律。“九五”期间,我国的医药中间体行业对于这一问题已有了深刻的认识,甘露醇市场也经历了亚洲金融危机之后的一个相当长的市场低谷,一度出现产品亏本的现象。[/size][/font][font='宋体'][size=16px][9][/size][/font][/align][align=center]第7章 [font='黑体'][size=21px]D-甘露醇的产品标准、限量标准及检测标准介绍[/size][/font][/align][font='黑体'][size=18px]7.1[/size][/font][font='黑体'][size=18px]产品标准及最大使用量[/size][/font][img]https://ng1.17img.cn/bbsfiles/images/2021/06/202106112258138869_1163_1608728_3.png[/img][font='宋体'][size=16px][7][/size][/font][font='黑体'][size=18px]7.2[/size][/font][font='黑体'][size=18px]甘露醇的检验[/size][/font][font='黑体'][size=17px]7.2.1定性检测[/size][/font][font='黑体'][size=17px] [/size][/font][font='宋体'][size=16px]在实际的分析检测工作中,有时仅需要对未知样品进行定性判定。甘露醇的定性检测基本原理是:晶体甘露醇在碱性条件下与三氯化铁反应生成棕黄色沉淀,振荡不消失,加过量的碱液即溶解生成棕色溶液,这种现象可以作为甘露醉的定性检测,该方法简便、快捷,但是这种方法仅局限于纯度较高的甘露醇晶体,如果样晶中所含杂质较多,则这种检测方法的准确性将无法保证,因此这种定性的检测方法在实际应用中亦有较大的局限性。[/size][/font][font='黑体'][size=17px]7.2.2定量检测[/size][/font][font='黑体'][size=16px]7.2.2.1碘量法[/size][/font][font='黑体'][size=16px] [/size][/font][font='宋体'][size=16px]即中华人民共和国药典中规定的容量法,其原理是:甘露醇与过量的高碘酸盐反应,反应完全后再加入过量的碘化钾,剩余的高碘酸盐及反应生成的碘酸盐都能与碘化钾作用生成游离碘出来,游离碘用硫代硫酸钠标准溶液滴定。碘量法可用于纯度较高的甘露醇样品,如一定浓度的注射液等,但对于含有其他还原性物质如单糖等的样品来说,这些还原性物质也可以被高碘酸氧化,测定结果偏高。此外,碘量法虽然简便快捷,不需要特殊的检测仪器,但操作较为繁琐。近年来也有将碘量法用于测定发酵制品或中草药等复杂体系中的甘露醇含量,这种方法一般需要对样品进行预处理,通过溶剂将样品中的甘露醇提取、纯化,然后对提取液中的甘露醇进行测定。如蔡仲军等人研究了使用不同溶剂处理样晶对虫草甘露醇测定结果的影响,结果表明,在虫草甘露醇含量的测定中,样品预处理采用水提法的准确性和精确性均大大高于醇提取法。[/size][/font][font='黑体'][size=16px]7.2.2.2薄层层析法[/size][/font][font='黑体'][size=16px] [/size][/font][font='宋体'][size=16px]薄层层析是一种微量、快速和简便的色谱方法。其原理是:根据各种化合物的极性不同,吸附能力不相同,在展开剂上移动,进行不同程度的解析。这种方法既可以用于定性检测,也可以用于定量检测。汪宝琪等人采用薄层色谱法,对冬虫夏草中甘露醇进行分离后,用高碘酸钾-联苯胺显色,采用薄层扫描法,在λs =295nm λμ=370nm的条件下进行双波长反射锯齿形扫描,测得西藏产冬 虫夏草中甘露醇的含量为8.4% ,回收率98% - 101.6%。[/size][/font][font='黑体'][size=16px]7.2.2.3比色法[/size][/font][font='宋体'][size=16px] 比色法分析测定甘露醇,是利用高碘酸钠与甘露醇反应产生黄色的3,5-乙酰-1,4-脱氣二甲基吡啶,此化合物在412nm左右处有最大吸收,并且单糖如半乳糖、葡萄糖、甘露糖等对甘露醇的影响很少。李雪芹、包天榈等人比较了测定冬虫夏草中甘露醉含量的两种方法,认为用比色法测定虫草中甘露醇含量较容量法更具特异性且快速简便。在一些较为复杂的体系中,如果含有一定量的果糖,果糖会对甘露醇测定产生较大的干扰,这是因为甘露醇、果糖都可以参与高碘酸氧化反应呈色,且在412nm处有重叠,但通过--定的处理手段可以去除检测体系中的这种影响。蒋华、陈卫等人建立了一种比较简便和精确的分光光度分析法,用以测定乳酸菌发酵体系中的甘露醇含量,通过与盐酸共热脱水反应去除发酵体系中果糖对甘露醇分析测定的干扰和影响,精密度实验和回收率实验表明,此法准确可靠。[/size][/font][font='宋体'][size=16px][10][/size][/font][align=center][/align][align=center][/align][align=center][font='宋体'][size=16px][color=#000000]参考文献[/color][/size][/font][/align][font='calibri'][size=14px][1] [/size][/font][font='calibri'][size=14px][color=#231f20]黎颖.甘露醇的性质、生产与发展建议[J].广西化工[/color][/size][/font][font='calibri'][size=14px][color=#231f20]1999,28(4):29[/color][/size][/font][font='calibri'][size=14px][color=#231f20].[/color][/size][/font][font='calibri'][size=14px][2] [/size][/font][font='calibri'][size=14px]Leen W . W right Sorbitol and M annitol[ J] CHEM TECH, [/size][/font][font='calibri'][size=14px]1944, 4(1): 42-[/size][/font][font='calibri'][size=14px]46[/size][/font][font='calibri'][size=14px].[/size][/font][font='calibri'][size=14px][3] [/size][/font][font='calibri'][size=14px][color=#231f20]黄云翔.ICIA公司蔗糖水解还原法制山梨醇和甘露醇的生产技术[J].广东化工,1995,(1):33-36[/color][/size][/font][font='calibri'][size=14px][4] [/size][/font][font='calibri'][size=14px][color=#231f20]张应茂.李再资.一步法蔗糖直接转化成山梨醇和甘露醇的研究[J].现代化工,1999,19(8):26-27[/color][/size][/font][font='calibri'][size=14px][color=#231f20][5]何燕.精细化工原料及中间体.开发指南.甘露醇生产与应用[J]浙江省巨化集团公司,[/color][/size][/font][font='calibri'][size=14px][color=#231f20]2003,10:15-16[/color][/size][/font][font='calibri'][size=14px][color=#231f20].[/color][/size][/font][align=left][font='calibri'][size=14px][color=#231f20][6]陈为民.甘露醇的性质与应用[J]黑龙江省轻工科学研究院,2009,10(19):41-42.[/color][/size][/font][/align][font='calibri'][size=14px][color=#231f20][7]中华人民共和国国家卫生和计划生育委员会.GB2760-2014食品安全国家标准,食品添加剂使用标准[s].北京:中国标准出版社,2014.[/s][/color][/size][/font][font='calibri'][size=14px][8] [/size][/font][font='calibri'][size=14px]吴国荃.聂美丽.罗书凯.我国甘露醇的生产状况与发展趋势[J]化工技术经济,2004,22(4):5[/size][/font][font='calibri'][size=14px][9] [/size][/font][font='calibri'][size=14px]赵美法.我国甘露醇的生产、市场分析与发展建议[J].山东青岛,2004,(1):4-7.[/size][/font][font='calibri'][size=14px][10] [/size][/font][font='calibri'][size=14px]林成真.甘露醇分析检测技术研究进展[J].河南化工,2010,27(2):5[/size][/font][align=center][/align][align=center][/align][align=center][/align][align=center][/align][align=center][/align][align=center][/align][align=center][/align][align=center][/align][align=center][/align][align=center][font='times new roman'][size=21px][color=#000000]致谢[/color][/size][/font][/align][font='宋体'][size=16px]在完成毕业***是他们的悉心指导,让我对这个课题有了明确的方向。[/size][/font][font='宋体'][size=16px]尤其要感谢我**文的贡献和教导。[/size][/font][font='宋体'][size=16px]同时感谢所**论文。[/size][/font][font='宋体'][size=16px]感谢这篇**篇论文。[/size][/font][font='宋体'][size=16px]最后再次向*最衷心的感谢![/size][/font]
苯甲酸、山梨酸、糖精钠是衡量食品卫生质量的重要指标,苯甲酸、山梨酸的检测参照GB/T5009.29-2003,糖精钠的检测参照GB/T 5009.28-2003,即可开展实验。 苯甲酸、山梨酸、糖精钠虽是较常见的检测项目,但是要得到一个准确可靠的结果,也存在一定的难度,许多新手常出现因对方法理解发生偏差而检测出错的事故。笔者根据自己多年该方面工作的实际经验出发,以苯甲酸、山梨酸为着重点,从样品前处理、检测仪器的选择、超标时的判断等几个易出问题的方面,进行了详细的阐述。 2 样品前处理的注意事项 GB/T5009.28-2003和GB/T5009.29-2003 在文字结构上有缺陷,在涉及用仪器法测定苯甲酸、山梨酸、糖精钠时,只讲述了液体样品的前处理方法,没有涉及对固体样品的前处理。 食品样品往往含有大量的油脂、蛋白质,对提取极为不利;如处理不干净也会污染色谱柱,影响检测工作。这类样品处理的关键在于如何找到一种较理想的沉淀剂,尽量排除待测样品中的油脂、蛋白质,且不影响待测物组分的回收率。 GB/T5009.29-2003使用5%硫酸铜溶液沉淀蛋白,对于蛋白质含量较低的食品尚可,对于豆粉、奶粉、月饼等高油脂、高蛋白样品则沉淀效果不理想。如用10%钨酸钠溶液作为沉淀剂,效果好些;如用10%亚铁氰化钾溶液和20%醋酸锌溶液则效果更理想(这是笔者目前用过最理想的沉淀剂)。 具体操作步骤如下: 取一定量样品,捣碎,利用四分法原理称取样品5.0 克于50ml比色管中,加水20ml,浸泡、振荡均匀,加入氢氧化钠溶液(1mol/L)1.0 ml,加入9.5mL10%亚铁氰化钾溶液, 9.50mL 20%乙酸锌溶液,定容,振荡使其充分混匀后,用滤纸初滤除去沉淀物, 初滤液过0.45μm微孔滤膜,收集滤液于样品瓶中,样品处理液和标准有溶液各进样5uL测定。 用这种方法简单易行,接触有机试剂少,重复性和回收率都令人满意;缺点是一定要用液相色谱法检测,有一定局限。 3 检测仪器的选择 虽然液相色谱仪操作起来比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]要复杂,但笔者建议如条件许可仍尽量用液相色谱法检测。原因如下: 3.1 液相色谱法所用的样品处理方法远比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法简单,且不需使用有机试剂。尤其对于高油脂样品(如月饼)若采用碱化-排油-酸化-提取-挥干-溶解等步骤,再上[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]检测,工作量大,试剂毒性也大,且结果由于处理步骤太多而难以保证准确。 3.2 用液相色谱法还可同时完成糖精钠项目的检测,而[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]法只能做苯甲酸、山梨酸的检测。 3.3 液相色谱仪所用的紫外检测器比[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]的氢火焰检测器灵敏,可进行更低含量的检测。如用二极管阵列检测器,还可辅助定性,这更是[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]氢火焰检测器不可比拟的。 4 选用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]时的注意事项 GB/T5009.29所用的[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]柱为 5%DEGS+1%磷酸固定液的60-80目 Chromosorb W AW,。这种柱有性能稳定、重复性好、保留时间稳定的优点,但同时也有稳定时间较长的缺点。 该柱的适用的样品提取溶剂为石油醚或乙醚,如果用甲醇或乙醇,则溶剂峰拖尾效应较大,对山梨酸的测定有影响。 如用毛细管柱,能取得更好的峰形和灵敏度,但其稳定性及特异性不如填充柱。一般可用非极性毛细管柱,0.530mm内径,10-15m长度。色谱条件可能需用程序升温。 在[url=https://insevent.instrument.com.cn/t/Mp]气相色谱仪[/url]上的出峰次序为先出山梨酸,后出苯甲酸。 糖精钠不能直接用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]进行检测,必须衍生化后才能汽化进样。 5 选用液相色谱仪的注意事项 按照GB/T5009.29,流动相应为5:95的甲醇:0.02M醋酸铵溶液,但是这个比例仅是个参考值,我们在工作中应根据实际情况进行调节。 为什么用甲醇溶液?甲醇有两个作用,(1)防腐,液相色谱柱最怕流动相长菌,尤其霉菌。甲醇可使蛋白质变性,有杀菌作用。(2)调节流动相极性,这是最重要的一点。甲醇在溶液中比例的较小变化都会使苯甲酸、山梨酸、糖精钠的保留时间发生明显的改变,因此可以通过改变流动相中甲醇含量,以调节这几个组分的出峰和分离,以得到较理想的色谱图。 5:95是一个通用的比例,如减少甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间变慢,扩散效应增大,峰形较差,但这三组分的分离情况较好。如增加甲醇含量,苯甲酸、山梨酸、糖精钠的出峰时间提前,扩散效应较小,峰形尖锐,但这三组分的分离情况可能受影响,产生重叠。在选择条件时,只能通过实验手段,如配制3:97,4:96,5:95,6:96,7:93的流动相,综合考虑分离效果和分离时间选择最佳比例。 不同柱的最适比例不同,举例来说,色谱科公司的液相柱最适比例为4:96,而岛津公司液相柱的最佳比例为7:93。就是同一根柱,一年前和一年后的极性也会有变化,需调节溶液配比。 为什么使用0.02M醋酸铵溶液?加入醋酸铵是为了调节离子强度,使待测物的峰形不致于变坏。如果单独检测苯甲酸和糖精钠,加不加醋酸铵没有什么关系,都可以得到较好的峰形;但是检测山梨酸时流动相一定要加醋酸铵,否则得不到一个完整的色谱峰,峰形呈破裂状。 醋酸铵溶液浓度不需严格控制,0.01M、0.02M、0.04M均可。

在选用Ecosil Sugar Ca2+色谱柱分析甘露醇和山梨醇有关物质小记分享按照药典要求用磺化的聚苯乙烯-二乙烯基苯共聚物填料进行有关物质分析实验室前人用的是Bio-Rad的Aminex HPX-87H 7.8*300mm 8μm(2012年买的但是标签花了),由于好久没人用它来做过实验了,测试后发现柱压高、峰型坍塌,用二次蒸馏水50℃,0.5ml/min冲洗再生仍然无效。故向上头申购对应的柱子,由销售商推荐了两款进口规格相当的Ecosil sugar Ca2+和Shodex SC1011 8.0*300mm 6μm,一问发现这类柱子还蛮贵的(近万),选择了价格便宜得多些的Ecosil sugar Ca2+;谁知道买回来马上问题不断啊,但也因为该事而对该类型色谱柱有了新的认识。故障:情况有些曲折,首先是拿到柱后进行活化平衡后,开始进一定浓度标样,结果峰型不是很好,理论塔板不足800,出峰时间有些晚,两目标峰(20和22min出峰)分离不开,同时谱图上还有稳定的脉冲峰出现,重复进样几次,问题依然存在。http://ng1.17img.cn/bbsfiles/images/2016/07/201607141827_600563_2543272_3.jpg针对脉冲峰初步怀疑是流动相脱气不足的问题,因为毕竟是新购置的示差光检测器,同时也没有在线脱气机,故将二次蒸馏水进行超声+真空脱气;换上新的流动相,置换完系统后,尖脉冲峰的问题解决了,但是甘露醇和山梨醇两个峰还是没分开,分离度完全达不到2以上。致电销售商询问解决方法,提到是否色谱柱在刚启用前,未能冲洗干净系统或是水中引入其他类型的金属离子,与Ecosil sugar Ca2+填料里面的钙离子产生了交换效应,导致色谱柱性能下降,同时还询问温度是否正常,建议用0.1M硝酸钙溶液,85℃,低流速冲洗30-60倍柱体积看是否有改善;按照如上方法进行冲洗和平衡后再次进行测试,没想到做出来的谱图一塌糊涂,柱压力还算正常,但又有气泡的痕迹(小倒峰,看来还是得买脱气机才行),峰型明显坍塌分叉了。http://ng1.17img.cn/bbsfiles/images/2016/07/201607141831_600564_2543272_3.png打开柱头发现里面已经发生了严重的填料坍塌!http://ng1.17img.cn/bbsfiles/images/2016/07/201607141831_600565_2543272_3.jpg将谱图发至销售商,一并排查后发现是自己操作中未注意到流速与温度的次序的问题(低温时候流速升的过快造成的)。他们的技术人员提到:1)分析开始时,低流速持续送液,待色谱柱升至高温时,才可逐步提高流速。色谱柱低温时快速升高流速至0.6ml/min,会导致压力骤升,冲击填料。2)分析结束时,降低流速至0.2ml/min,关闭柱温箱。低流速持续送液,待色谱柱充分冷却至室温时,停泵。否则如果色谱柱高温时,直接停泵,也会导致填料坍塌。这是我首次使用聚合物填料的色谱柱,聚合物填料的色谱柱还果真是没有硅胶基质的机械强度高耐不了高压;还好该销售商不错,见我如此诚实,虽才用几下就给倒霉的我弄坏了,但是比起其他人遇到问题就直指就是色谱柱人员的要可爱多,所以很感激能给我申请换了一支新的,问题完美解决。嗯,看来做分析实验还是要本着胆大心细的态度,尊重科学和事实,才能有所收获。
苯甲酸、山梨酸、糖精钠是最常见的食品添加剂,在液相色谱柱的标准出峰顺序是苯甲酸、山梨酸、糖精钠,通过改变流动相的比例可不可以对出峰顺序及分离度造成影响?
公司对我们采购进来的原料和液晶单体都要进行定量分析,请问如何用[url=https://insevent.instrument.com.cn/t/Mp]气相色谱[/url]分析山梨醇!用面积归一法能做吗?我看了相关的文章说是关于用衍生化法毛细管分离山梨醇和甘露醇的,用的是内标法。可是关于内标法的分析我还从来没有做过呢,
木糖醇、山梨醇、麦芽糖醇……这样的名词越来越多出现在了食品中,普通消费者根本搞不清。记者昨从宁波市质监局获悉,宁波马上将启动《食品中木糖醇、山梨醇、麦芽糖醇、甘露糖醇、乳糖醇和异麦芽酮糖醇的测定》的国家方法标准起草工作。 有关专家介绍,许多食品生产企业在食品中添加木糖醇等代糖物质,但相关研究表明某些代糖物质对人体有致病的可能性。我国目前在检测代糖食品方面的方法标准尚属空白。宁波将启动的这项国家方法标准起草工作将于2008年年底前完成。