中科院化学所汪铭研究员解析2020年诺贝尔化学奖
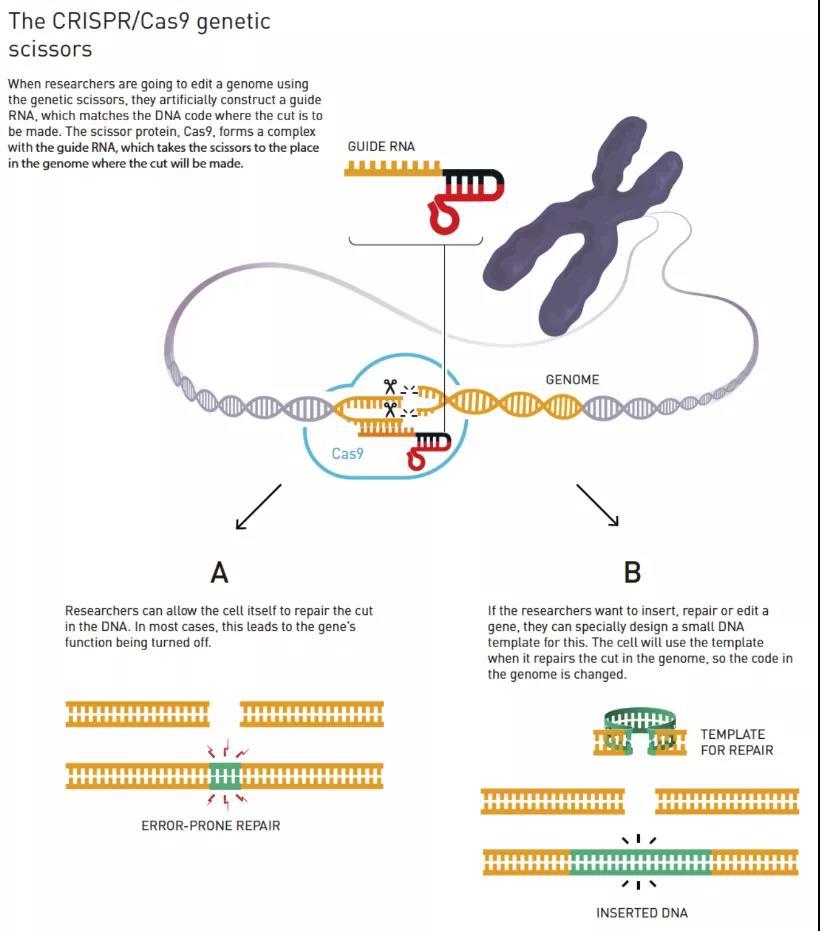
p style=" text-align: justify text-indent: 2em line-height: 1.75em " 瑞典皇家科学院2020年10月7日宣布今年的诺贝尔化学奖授予美国加州大学教授詹妮弗· 杜德纳(Jennifer Doudna)和现在德国工作的法国科学家埃曼纽尔· 卡彭蒂耶(Emmanuelle Charpentier), 以表彰她们在基因编辑领域做出的突出贡献。两位科学家合作发展了新型CRISPR/Cas9基因编辑方法, 并精准地应用于改变动物、植物、微生物的DNA。这项技术对生命科学产生了革命性影响, 有望催生创新性癌症治疗策略, 并可能让治愈遗传性疾病这一人类梦想成真。(“This technology has had a revolutionary impacton the life sciences, is contributing to new cancer therapies and may make the dream of curing inherited diseases come true.”)。 /p p style=" text-align: center" img style=" max-width:100% max-height:100% " src=" https://img1.17img.cn/17img/images/202010/uepic/6fdcbf32-a434-465d-92ab-a0210b6eae57.jpg" title=" 1.jpg" alt=" 1.jpg" / /p p style=" text-align: center " span style=" text-align: justify text-indent: 2em " CRISPR/Cas9基因编辑技术示意图& nbsp (图片来源:www.nobelprize.org) /span /p p style=" text-align: justify text-indent: 2em line-height: 1.75em " 随着生物技术的不断发展, 对活细胞DNA进行精准操作, 实现碱基或DNA片段的插入、删除、替换等, 即基因编辑成为可能。同时, 运用基因编辑技术可以改变基因的序列和功能, 从而调控细胞的命运和生物特征, 为遗传性疾病的治疗提供新方法。CRISPR/Cas9基因编辑技术是继“锌指核酸酶(ZFN)”、“类转录激活因子效应物核酸酶(TALEN)”之后出现的新一代基因组定点编辑技术。与前两代技术相比, CRISPR/Cas9具有操作简单、快捷高效等优势, 自发现之后迅速发展成为当今最主流的基因编辑方法。CRISPR是Clustered Regularly Interspaced Short Palindromic Repeats(成簇规律间隔短回文重复序列)的首字母缩写。 /p p style=" text-align: justify text-indent: 2em line-height: 1.75em " CRISPR序列是由日本分子生物学家石野良纯(Yoshizumi Ishino)1987年在大肠杆菌中偶然发现的, 西班牙微生物学家弗朗西斯科· 莫伊卡(Francisco Mojica)2003年进一步发现CRISPR中独特的非重复的序列与各种病毒的遗传密码相匹配。随着研究的不断深入, 研究人员确定了CRISPR是一种源自细菌的适应性免疫系统。CRISPR能够识别(通过crRNA)入侵细菌的病毒, 并通过一种特殊的核酸酶(Cas9蛋白)降解入侵病毒的DNA序列, 从而保护古细菌免受病毒侵害。Emmanuelle Charpentier在研究化脓性链球菌(Streptococcus pyogenes)的调控性RNA过程中发现化脓性链球菌中存在一些新型小RNA分子, 其遗传密码与CRISPR序列存在部分匹配。进一步她们发现这些未知的RNA分子(后来被称为反式激活的CRISPR RNA, tracrRNA)可以帮助基因组中的CRISPR序列转录产生的长RNA分子加工为成熟的, 具有活性的RNA(crRNA), 对CRISPR作用及细菌的免疫系统具有决定性意义。 /p p style=" text-align: justify text-indent: 2em line-height: 1.75em " 然而, 第一次全面解析CRISPR/Cas9基因编辑的原理则来自于Emmanuelle Charpentier和美国分子生物学家Jennifer Doudna的合作。 span style=" text-indent: 2em " 她们发现使用重组Cas9蛋白(来自在大肠杆菌里表达的化脓性链球菌[S. pyogenes]的基因)和体外转录的crRNA及tracrRNA可以在体外切割纯化的DNA, 并成功编辑了大肠杆菌基因。此外, 她们证明crRNA和tracrRNA对Cas9发挥作用都是必需的, 两种RNA在被融合为单一的导向RNA(single guide RNA, sgRNA)时也可以在体外发挥作用, 并提到“利用这一系统来进行可设计的基因组编辑的潜力”。这一结果发表半年之后, 研究人员首次报道可以将CRISPR/Cas9基因编辑技术应用于哺乳动物和人类细胞的基因编辑, 从而促进了这一技术的爆发性发展。此前, 改变细胞基因是一项非常耗时, 甚至是难以完成的工作。使用CRISPR基因编辑方法, 研究人员理论上可以通过设计不同的sgRNA引导Cas9核酸酶在他们想要的任何基因位点进行基因编辑。由于这一方法的简单、廉价和高效, CRISPR迅速发展成为最主流的基因编辑技术, 应用于高效、精确地改变、编辑或替换植物、动物甚至是人类基因, 被称为编辑基因的“魔剪”。 /span /p p style=" text-align: justify text-indent: 2em line-height: 1.75em " CRISPR/Cas9基因编辑技术改变了我们在不同物种活细胞中操纵基因表达的能力, 短短十几年间便从CRISPR机制研究发展到临床试验应用。与ZFN和TALEN等基因编辑技术相比, CRISPR/Cas9在基因编辑和基因治疗等方面具有非常明显的优势:设计极其简单, 只需要设计一段几十个碱基构成的gRNA序列即可实现靶标基因编辑, 而传统方法多需要复杂的分子生物工程设计蛋白质识别基因组;基因编辑效率高, 可以通过设计多个sgRNA实现多个基因位点的同时基因编辑;多功能化, 随着CRISPR/Cas9的不断发展, 这一技术不仅可以实现对特定基因组位点的删除、修复、替换等功能, 还进一步被应用于基因组成像、表观遗传修饰、核酸检测及疾病诊断(如新冠病毒检测)等方面。2020年诺贝尔化学奖颁发给两位从事基因编辑研究的科学家, 不仅仅是对她们个人成就的表彰, 更是对整个研究领域成果的肯定。当前, CRISPR/Cas9基因编辑技术已经显示出巨大的生物医学应用价值, 但其在生物安全性、基因编辑脱靶效应以及临床应用等方面仍面临很多函待解决的问题。如人体可能对细菌来源的基因编辑核酸酶Cas9产生免疫反应;高效、安全地将CRISPR/Cas9基因编辑系统导入活细胞甚至活体层次至关重要。 /p p style=" text-align: justify text-indent: 2em line-height: 1.75em " 病毒载体在人类基因治疗中获得了广泛应用, 但是其装载容量有限, 而常规的Cas9蛋白过大, 对利用病毒载体实现CRISPR/Cas9递送提出了挑战。因此, 发展新型CRISPR/Cas9递送系统对在体基因编辑及其临床转化应用尤为重要;在降低脱靶效应方面, 通过对Cas9蛋白进行定点突变或者发展新型基因编辑技术(如碱基编辑等)则有望实现突破。这些研究虽然仍面临众多挑战, 但也是未来基因编辑技术发展和其生物医学应用的机遇和突破口。 /p p style=" text-align: center" img style=" max-width: 100% max-height: 100% width: 300px height: 399px " src=" https://img1.17img.cn/17img/images/202010/uepic/9c41b08e-4372-4f94-a6e2-604f574bf3e4.jpg" title=" 2.jpg" alt=" 2.jpg" width=" 300" height=" 399" border=" 0" vspace=" 0" / /p p style=" text-align: center line-height: 1.75em " 中科院化学所研究员 汪铭 /p p style=" line-height: 1.75em " 研究方向主要包括:1)蛋白质化学修饰及其活体功能调控 2)CRISPR/Cas9基因编辑递送及其化学生物学应用 3)金属配位导向的蛋白质组装及其生物医学应用。 /p p style=" line-height: 1.75em " 课题组主页: a href=" http://mingwang.iccas.ac.cn/home" target=" _blank" http://mingwang.iccas.ac.cn/home /a /p p br/ /p