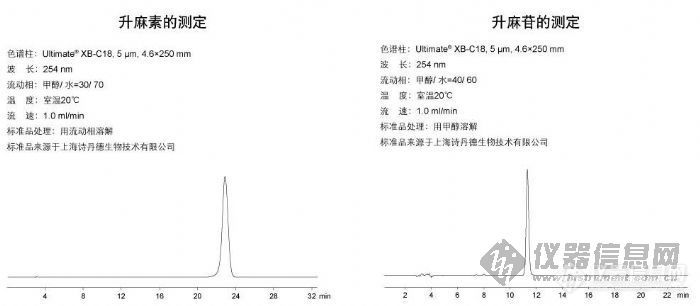
升麻素的测定和升麻苷的测定http://ng1.17img.cn/bbsfiles/images/2009/10/200910130312_175404_1896702_3.jpg
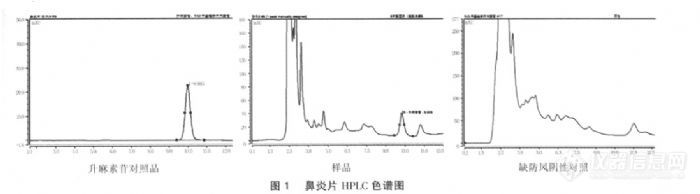
【作者】:何巧君,高幼衡,魏志雄【摘要】:目的建立高效液相色谱(HPLC)法测定鼻炎片中升麻素苷含量的方法。方法采用HPLC法,色谱柱为迪马Diamonsil C18分析柱(4.6mm×250mm,5μm),流动相为甲醇-乙腈-水(18∶12∶70);流速为1.0mL/min;检测波长为254nm。结果升麻素苷在0.1888~1.534μg范围内与峰面积积分值呈良好的线性关系,相关系数r=0.9997,加样回收率为101.74%,RSD为2.97%。结论该方法快速、准确,可用于鼻炎片的质量控制。关键词:鼻炎片;升麻素苷;高效液相色谱法【作者单位】: 广州中医药大学中药学院【关键词】:鼻炎片;升麻素苷;高效液相色谱法http://ng1.17img.cn/bbsfiles/images/2012/07/201207311352_380873_1838299_3.jpg
[font=宋体] [font=宋体]升麻为毛茛科植物大三叶升麻[/font][i]Cimicifuga heracleifolia[/i] Kom.[font=宋体]、兴安升麻[/font][i]C. dahurica [/i](Turcz.) Maxim.[font=宋体]或升麻[/font][i]C. foetida [/i]L.[font=宋体]的干燥根茎,含有三萜皂苷、黄酮、生物碱和色酮等化学成分,具有缓解潮热、抗骨质疏松、抗人类免疫缺陷病毒、抗炎、抗糖尿病、抗疟疾和保护血管等多种生物活性[/font][sup][4][/sup][font=宋体]。同属植物黑升麻[/font][i]C. racemosa[/i] L.[font=宋体]在欧洲广泛应用于防治更年期综合征和骨质疏松症[/font][sup][5][/sup][font=宋体]。有研究表明升麻具有与黑升麻相似的缓解去卵巢大鼠更年期综合征和抗骨质疏松作用,其有效成分为三萜皂苷[/font][sup][6-7][/sup][font=宋体]。升麻三萜皂苷能够增加成骨细胞的骨形成[/font][sup][8][/sup][font=宋体],但其对破骨细胞形成分化和骨吸收的影响及机制尚不清楚。[/font] 破骨细胞为从骨髓巨噬细胞分化的,唯一具有骨吸收功能的细胞。破骨细胞活性增强,骨吸收大于骨形成,骨重建的平衡破坏,导致骨量减少和骨质疏松症的发生[/font][sup][9-10][/sup][font=宋体]。破骨细胞的典型特征为分泌[/font]TRAP[font=宋体]和形成[/font]F-actin[font=宋体]进行骨吸收。[/font]TRAP[font=宋体]是由破骨[/font][font=宋体]细胞分泌的酸性磷酸酶,具有溶解骨矿化基质的作用,是破骨细胞分化成熟的特异性标志酶[/font][sup][11][/sup][font=宋体]。[/font]F-actin[font=宋体]环是破骨细胞特有的进行骨吸收的细胞骨架蛋白,是破骨细胞附着于骨基质表面的重要结构[/font][sup][12][/sup][font=宋体]。培养的破骨细胞通过骨吸收,可在共培养的骨片上形成骨吸收陷窝,其数目和面积常用于表征破骨细胞的骨吸收活性。本研究以[/font]RANKL[font=宋体]及[/font]M-CSF[font=宋体]诱导[/font]BMMs[font=宋体]形成的破骨细胞为模型,观察升麻三萜皂苷对破骨细胞形成、分化和骨吸收的作用,结果表明升麻三萜皂苷阿克特素、升麻环氧醇苷、升麻醇可显著抑制[/font]RANKL[font=宋体]诱导的破骨细胞[/font]TRAP[font=宋体]活性,减少[/font]TRAP[font=宋体]染色阳性的破骨细胞的数目,抑制[/font]F-actin[font=宋体]环的构建,降低破骨细胞在骨片上形成的骨吸收陷窝的数目和面积,显示出了确切的抑制破骨细胞骨吸收的作用。[/font] [font=宋体]破骨细胞由骨髓巨噬细胞分化形成的过程中,受[/font]c-Fos[font=宋体]和[/font]NFATc1[font=宋体]的调控[/font][sup][13][/sup][font=宋体]。[/font]c-Fos[font=宋体]是破骨细胞分化早期所必需的激活蛋白[/font]-1[font=宋体]家族的关键转录因子,可诱导破骨细胞[/font]NFATc1[font=宋体]的表达,调控前破骨细胞最终分化为成熟破骨细胞[/font][sup][14][/sup][font=宋体]。[/font]NFATc1[font=宋体]参与调控破骨细胞特异性基因[/font][i]TRAP[/i][font=宋体]、[/font][i]CTSK[/i][font=宋体]、树突状细胞特异性跨膜蛋白([/font]dendritic cell-specific transmembrane protein[font=宋体],[/font][i]DC-STAMP[/i][font=宋体])和降钙素受体([/font]calcitonin receptor[font=宋体],[/font][i]CTR[/i][font=宋体])等的表达,刺激破骨细胞的形成、分化和骨吸收[/font][sup][15-16][/sup][font=宋体]。升麻三萜皂苷阿克特素、升麻环氧醇苷、升麻醇能够抑制破骨细胞转录因子[/font]NFATc1[font=宋体]和[/font]C-fos[font=宋体]的表达,抑制破骨细胞的形成分化。[/font]CTSK[font=宋体]是破骨细胞分泌的胶原降解酶,可降解骨基质中的胶原纤维[/font][sup][17][/sup][font=宋体]。[/font]MMP9[font=宋体]也是破骨细胞产生的参与骨基质胶原降解的蛋白酶[/font][sup][18][/sup][font=宋体]。升麻三萜皂苷阿克特素、升麻环氧醇苷、升麻醇可显著抑制破骨细胞[/font]MMP9[font=宋体]和[/font]CTSK[font=宋体]的表达,进一步明确了其对破骨细胞骨吸收的抑制作用。[/font] [font=宋体]网络药理学是预测中药活性成分作用靶点及机制的重要手段[/font][sup][19-20][/sup][font=宋体]。本研究应用网络药理学预测了升麻三萜皂苷抑制破骨细胞骨吸收的潜在靶点和机制。[/font]KEGG[font=宋体]分析显示升麻三萜皂苷可能通过调控[/font]IL-17[font=宋体]、[/font]TNF-α[font=宋体]、脂质和动脉粥样硬化、[/font]MAPK[font=宋体]信号通路发挥抑制破骨细胞功能的作用。[/font]IL-17[font=宋体]和[/font]TNF-α[font=宋体]通路是机体调节炎症的重要机制[/font][sup][21][/sup][font=宋体]。衰老和雌激素缺失导致炎性细胞因子水平升高,抑制成骨细胞的骨形成,增加破骨细胞的骨吸收,导致骨量减少和骨质疏松症的发生[/font][sup][22][/sup][font=宋体]。升麻三萜皂苷参与[/font]IL-17[font=宋体]和[/font]TNF-α[font=宋体]通路的调控,表明其可能通过抑制炎症发挥抗骨质疏松的作用。[/font] [font=宋体]升麻三萜皂苷也可能参与脂质和动脉粥样硬化通路的调控。骨髓间充质干细胞在向成骨细胞分化的过程中,成脂和成骨分化程序具有竞争性平衡,促进脂肪生成的机制会主动抑制成骨细胞的形成与分化[/font][sup][23][/sup][font=宋体]。骨髓脂肪细胞可通过分泌破骨细胞活化因子促进破骨细胞的形成、分化和骨吸收作用[/font][sup][24][/sup][font=宋体]。绝经后骨质疏松患者存在骨量减少、成骨细胞的数量和功能下降、骨髓脂肪增加等现象,表明脂肪细胞的分化可能会影响成骨细胞或破骨细胞的形成分化[/font][sup][25][/sup][font=宋体]。[/font][font=宋体]因此,升麻三萜皂苷也可能通过抑制骨髓基质干细胞向脂肪细胞的分化,增加成骨细胞的骨形成、抑制破骨细胞的骨吸收,发挥抗骨质疏松的作用。[/font] MAPK[font=宋体]是[/font]RANKL/RANK/TRAF6[font=宋体]信号传导下游的一条通路[/font][sup][26][/sup][font=宋体],[/font]RANKL[font=宋体]与[/font]RANK[font=宋体]的结合导致[/font]MAPK[font=宋体]的[/font]p38[font=宋体]、[/font]JNK[font=宋体]和[/font]ERK[font=宋体]磷酸化,诱导破骨细胞的形成分化[/font][sup][27][/sup][font=宋体]。[/font]p38 MAPK-[font=宋体]环磷腺苷效应元件结合蛋白([/font]adenosinecyclophosphate-response element binding protein[font=宋体],[/font]CREB[font=宋体])通路在[/font]RANKL[font=宋体]介导的破骨细胞分化中发挥重要作用,[/font]p38 MAPK[font=宋体]抑制剂可抑制[/font]TNF-α[font=宋体]或[/font]RANKL[font=宋体],通过[/font]CREB[font=宋体]磷酸化调节[/font]c-Fos[font=宋体]和[/font]NFATc1[font=宋体]的表达,抑制破骨细胞的形成分化[/font][sup][28][/sup][font=宋体]。[/font]p38[font=宋体]可刺激破骨细胞成熟所必需的小眼相关转录因子([/font]microphthalmia-associated transcription factor[font=宋体],[/font]MITF[font=宋体])的下游激活,调控破骨细胞[/font][i]TRAP[/i][font=宋体]和[/font][i]CTSK[/i][font=宋体]的基因表达[/font][sup][29][/sup][font=宋体]和骨吸收。[/font]ERK[font=宋体]激活是成熟破骨细胞存活的关键[/font][sup][30][/sup][font=宋体],[/font]M-CSF[font=宋体]刺激的[/font]ERK1[font=宋体]和[/font]ERK2[font=宋体]激活,直接磷酸化[/font]MITF[sup][31][/sup][font=宋体],影响破骨细胞的骨吸收活性。[/font]RANKL[font=宋体]诱导破骨前细胞[/font]ERK[font=宋体]的激活,通过[/font]TRAF6[font=宋体]诱导[/font]MMP9[font=宋体]的表达和活性,调节破骨细胞迁移和骨吸收[/font][sup][32][/sup][font=宋体]。[/font]JNK[font=宋体]的激活参与破骨细胞的分化、融合和骨吸收的调节,也通过[/font]B[font=宋体]淋巴细胞瘤[/font]-2[font=宋体]([/font]B-cell lymphoma-2[font=宋体],[/font]Bcl-2[font=宋体])通路调节破骨细胞的凋亡和自噬[/font][sup][33][/sup][font=宋体]。在破骨细胞融合前阶段阻断[/font]JNK[font=宋体]活性会导致[/font]TRAP[font=宋体]阳性细胞(代表融合前阶段的破骨细胞)逆转为[/font]TRAP[font=宋体]阴性细胞(代表破骨细胞前体)[/font][sup][34][/sup][font=宋体]。[/font][font=宋体]本研究发现升麻三萜皂苷阿克特素、升麻环氧醇苷、升麻醇与[/font]ERK1/ERK2[font=宋体]、[/font]JNK[font=宋体]、[/font]p38[font=宋体]均有较好的结合特性,可显著抑制[/font]RANKL[font=宋体]和[/font]M-CSF[font=宋体]诱导[/font]BMMs[font=宋体]分化的破骨细胞[/font]p38[font=宋体]、[/font]JNK[font=宋体]和[/font]ERK[font=宋体]的磷酸化和激活,进一步明确了升麻三萜皂苷通过[/font]MAPK[font=宋体]通路抑制破骨细胞的形成分化和骨吸收的作用机制。[/font] [font=宋体]三萜皂苷是升麻属植物的特征性化学成分,目前已从升麻属多种植物中分离鉴定了[/font]400[font=宋体]余个三萜皂苷类成分,其中[/font]44[font=宋体]个化合物显示出抗骨质疏松、抗肿瘤、抗炎、抗氧化及免疫调节等多种生物活性[/font][sup][35][/sup][font=宋体]。本研究考察了升麻三萜皂苷阿克特素、升麻环氧醇苷、升麻醇抑制破骨细胞骨吸收的作用,并通过网络药理学预测了其作用机制。后续还应该深入研究这些化合物抑制破骨细胞活性的靶点及对成骨细胞的作用及机制,为其临床用于骨质疏松症的防治奠定基础。另外,鉴于升麻属植物含有结构多样的三萜皂苷类成分,应采用现代化学生物学的思路和方法,研究升麻三萜皂苷抗骨质疏松的作用靶点、构效关系及深入的机制,为抗骨质疏松新药的研发提供先导化合物。[/font]
防风Saposhnikoviae Radix为伞形科植物防风Saposhnikovia divaricata (Turcz.) Schischk.的干燥根,具有祛风解表、胜湿止痛、止痉的功效[1]。防风含有多种化学成分,主要包括色原酮类、香豆素类、多糖类、挥发油类等[2],这些成分具有解热、镇痛、抗炎、抗菌、抗氧化、抗肿瘤等多种药理作用[3-6]。升麻素苷、升麻素、5-O-甲基维斯阿米醇苷为主的色原酮类成分是防风的主要活性物质,具有解热、镇痛、抗炎等多种药理活性[7-10],其中升麻素苷、5-O-甲基维斯阿米醇苷已作为《中国药典》2020年版中防风质量控制的标志物。课题组前期已对5-O-甲基维斯阿米醇苷体内外的代谢进行了全面的研究[11],但尚未见对升麻素苷的研究报道。有研究表明升麻素苷是防风抗炎作用的主要成分[12],而防风为《中国药典》2020年版收录的中成药齿痛消炎灵颗粒的君药,齿痛消炎灵颗粒具有治疗牙周炎的作用[13-14],故本研究采用超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]-四极杆-飞行时间质谱联用技术(UPLC-Q-TOF-MS/MS)与MetabolitePilot 2.0、PeakView 2.0软件,对升麻素苷在牙周炎模型大鼠和正常大鼠的体内外代谢进行研究,并比较代谢差异,为防风的药效物质基础提供依据。 1 材料 1.1 动物 SPF级雄性SD大鼠,体质量(220±20)g,由河北石家庄伊维沃生物技术有限公司提供,动物生产许可证号SYXK(冀)2020-002。动物于温度(22±2)℃、相对湿度(50±3)%、12 h光照/12 h黑暗循环环境下饲养。动物实验通过河北医科大学动物伦理委员会的伦理审查(批准号DW2019003)。 1.2 药品与试剂 升麻素苷对照品(批号BD121316,质量分数≥98%),购自上海毕得医药科技股份有限公司;升麻素对照品(批号HR1638W2)购自宝鸡市辰光生物科技有限公司;右美沙芬对照品(批号Y03S11W120802,质量分数>98%)购自上海源叶生物科技股份有限公司;甲醇、乙腈(色谱纯)购自美国Tedia公司;甲酸(色谱纯)购自美国Diamond公司;纯净水购自娃哈哈有限公司。 1.3 仪器 Triple TOF 5600+型高分辨质谱仪(美国AB Sciex公司);超高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]系统包括CBM20A型控制器、DGU-20A5R型在线脱气模块、LC-30AD型二元梯度高压泵系统、SIL-30AC型自动进样器和CTO-30A型柱温箱(日本岛津公司);D3024R型高速冷冻离心机(美国SCILOGEX公司);KQ-5200E型台式超声波清洗器(昆山市超声仪器有限公司);十万分之一分析天平(瑞士METTLER TOLEDO公司);MTN-2800D型氮吹仪(天津奥特赛恩斯仪器有限公司);MX-S型涡旋混匀器[大龙兴创实验仪器(北京)有限公司];SkyScan 1176型小动物Micro-CT扫描影像系统、NRecon软件、3D重建软件CTvox(德国Bruker公司)。 1.4 数据处理软件 Analyst® TF 1.7软件、MetabolitePilot 2.0软件、PeakView 2.0软件(美国AB Sciex公司)。 2 方法 2.1 溶液的制备 2.1.1对照品溶液的制备 精密称取升麻素苷、升麻素对照品适量,甲醇溶解制成质量浓度为1 mg/mL的贮备液,并用甲醇稀释成质量浓度为100 μg/mL的对照品溶液。 2.1.2内标(IS)溶液的配制 精密称取右美沙芬对照品适量,甲醇溶解制成质量浓度为1 mg/mL的贮备液,临用前用甲醇稀释成质量浓度为2.0 μg/mL的IS溶液。 2.1.3大鼠ig溶液的配制 精密称取升麻素苷对照品600 mg,加入60 mL纯净水,配成质量浓度为10 mg/mL的ig溶液。 2.2 牙周炎模型的建立 大鼠适应性喂养1周,采用吸入式2%~3%异氟烷实施麻醉,麻醉成功后采用0.2 mm正畸结扎丝结扎大鼠上颌左侧第一磨牙牙颈部,诱导实验性牙周炎[15-17],对侧同名牙作为对照不结扎。手术后,待大鼠全部苏醒,喂其常规鼠粮及水,并定期检查结扎丝牢固程度,整个实验持续8周。 在整个实验过程,注意大鼠精神状态,定期检查牙龈炎症、颜色、水肿、探针是否出血及牙周袋是否形成等。造摸8周后随机抽取牙周炎模型大鼠,处死,取上颌左侧第一磨牙及牙龈组织,同时取其对侧对比,置于4%多聚甲醛固定,常规脱钙,脱水透明,浸蜡包埋,制作切片,常规苏木素-伊红(HE)染色后,于显微镜下观察病理变化。同时采用微型计算机断层成像技术(micro computed tomography,Micro-CT)重建大鼠牙槽骨三维图像,观察牙槽骨吸收情况。 2.3 动物给药及生物样品采集 实验前,将正常大鼠随机分为4组,每组3只,第1组为空白正常胆汁组,第2组为给药正常胆汁组,第3组为空白正常血浆、尿液及粪便组,第4组为给药正常血浆、尿液及粪便组。模型组按与正常组相同的方法随机分为4组。给药前大鼠禁食12 h,自由饮水。根据大鼠体质量,以100 mg/kg的剂量进行ig给药。空白组ig等体积的纯净水溶液。 分别于ig给药后0.167、0.333、0.5、0.75、1、2、4、6、8、12、24 h自眼内眦取血0.3 mL,置肝素化的离心管中,4 ℃、3 500 r/min离心10 min,取上清液获得血浆样品,并将各组不同时间点获得的血浆样品合并,即得空白血浆和含药血浆。ig给药后,收集大鼠0~72 h每4个小时的尿液和粪便样本,并将来自同组大鼠的所有尿液和粪便分别进行混合,即得空白和给药尿液、粪便。ig给药后,通过ip 20%乌拉坦生理盐水溶液(1.5~2.0 g/kg)麻醉,实施胆汁插管引流手术收集0~24 h的胆汁样品,将来自同组大鼠的所有胆汁进行混合,即得空白和给药胆汁。所有样品置于?80 ℃冰箱备用。 分别取正常大鼠及牙周炎模型大鼠新鲜粪便3 g,加入30 mL厌氧培养液[18],用玻璃棒研碎并搅拌均匀,经医用纱布滤过,即得肠道菌培养液。取肠道菌培养液1 mL,加入100 μL(1.0 mg/mL)升麻素苷溶液,通入氮气置于无氧并充满氮气的厌氧袋中,在提前预热至37 ℃的摇床中孵育12 h,即得肠道菌孵育样品。空白组用100 μL超纯水代替升麻素苷溶液。 2.4 样品前处理 取血浆、尿液、胆汁样品各1 mL,分别加入100 μL的IS溶液(2 μg/mL),混合均匀,加入3倍量甲醇,涡旋5 min,4 ℃、15 000 r/min离心10 min,取上清液。取肠道菌孵育液1 mL、粪便样品0.5 g(加1 mL蒸馏水超声30 min制备成匀浆),分别加入100 μL的IS溶液(2 μg/mL),加入3倍量的醋酸乙酯,涡旋5 min,4 ℃、15 000 r/min离心10 min,收集上层萃取液,重复萃取3次,合并萃取液。将离心后所得的各生物样品上清液置另一清洁离心管中,N2流吹干,200 μL 50%甲醇复溶,涡旋5 min,15 000 r/min离心10 min,取上清液即得。 2.5 检测条件 2.5.1 色谱条件 COSMOCORE C18柱(150 mm×2.1 mm,2.6 μm);流动相为0.1%甲酸水溶液(A)- 甲醇(B),梯度洗脱:1~3 min,5%~20% B;3~25 min,20%~95% B;25~30 min,95% B。预平衡5 min,柱温40 ℃,体积流量0.3 mL/min,进样量5 μL。 2.5.2 质谱条件 电喷雾离子源(electro-spray ionization,ESI),正离子模式下进行全扫描,参数设置如下:离子源喷雾电压5 500 V;源温度550 ℃;气帘气压力241.325 kPa;雾化气(Gas1)压力379.225 kPa;加热气(Gas2)压力379.225 kPa;解簇电压70 V;碰撞能量40 eV;碰撞能量扩展15 eV。TOF-MS扫描的扫描范围为m/z 100~1 200,积累时间设置为250 ms。每个扫描周期选择8个响应最高的离子进行MS/MS扫描。产物离子扫描范围为m/z 50~1 200,积累时间为100 ms。 2.6 数据处理 正常大鼠和牙周炎模型大鼠ig升麻素苷后,各生物样本的总离子流图见图1。采用以下5个步骤来鉴定和分析升麻素苷在正常大鼠及牙周炎模型大鼠体内外的代谢物:①基于UHPLC-Q-TOF-MS/MS技术,在线进行全扫描数据采集,并利用多重质量亏损(MMDF)和动态背景扣除(DBS)设置获得准确的MS/MS质谱信息。②利用Peak View、Metabolite Pilot软件中的多种数据挖掘工具,自动过滤出升麻素苷的可能代谢物。③从准确的质谱数据、母体药物的裂解模式以及相关文献描述代谢物的推断过程。④ClogP值用作区分具有相同分子式和相似质谱数据的代谢物异构体的参数。ClogP值越大,在反相色谱系统中的洗脱时间就越长。⑤根据Peak View软件提供的代谢物的峰面积,用峰面积相对定量法比较代谢物在正常大鼠及牙周炎模型大鼠各生物样品中的含量差异。3 结果 3.1 CT成像 应用Micro-CT扫描、三维图像重建显示,与对照组(图2-B、D)相比,模型组(图2-A、C)牙槽骨吸收明显,同时有水平和垂直向吸收。对大鼠上颌第一、第二磨牙兴趣区域[19](本实验选取的兴趣区域(region of interest,ROI)为第一、第二磨牙近中牙槽嵴吸收情况)进行测量,对照组牙近中釉牙骨质界(cemento-enamel juction,CEJ)到牙槽嵴顶(alveolar bone crest,ABC)的平均距离为0.394 mm(图2-D),与对照组相比,模型组CEJ到ABC的距离平均增至0.813 mm。分析大鼠CEJ至ABC的垂直距离(图2-A、B),即分别取对照组与模型组样本牙齿颊侧的近中、中央及远中共3个位点的CEJ至ABC的距离,测量统计分析结果显示,与对照组相比,模型组CEJ-ABC距离明显增加(P<0.05,图2-E)。 图片 3.2 升麻素苷质谱裂解规律分析 升麻素苷(M0,C22H28O11)的保留时间为8.80 min,M0通过重排生成准分子离子峰[M+H]+m/z469.170 2。母离子m/z 469.170 2失去18(-H2O)、72(-C4H8O)分别形成特征碎片离子m/z 451.173 2、397.125 0。M0通过丢失162(-glu)、234(-glu-C4H8O)分别产生特征碎片离子m/z307.128 6、235.068 0,其中特征碎片离子m/z 235.068 0是特征碎片离子m/z307.128 6通过二氢吡喃环失去C4H8O发生RDA裂解反应产生。通过连续丢失O和C3H6O后,m/z 235.068 0产生碎片离子m/z 219.072 5、161.065 4。苷元离子m/z307.126 8有2种脱水方式(-H2O),分别产生m/z289.116 6的2种结构不同碎片离子,苷元离子在失去水的基础上连续失去2个CH3分别产生m/z274.092 3、259.068 8。通过连续丢失C3H6、CH2、C2H2、CO和O后,m/z 289.116 6产生了一系列碎片离子m/z247.068 1、233.052 3、221.051 7、219.072 5、205.056 3、193.056 0、189.061 1、177.060 6。升麻素苷可能的裂解途径见图3。 3.3 升麻素苷在大鼠体内外代谢物的分析鉴定 采用上述分析策略,共鉴定出30个升麻素苷的代谢物(其中I相代谢物25个、II相代谢物5个)。在健康大鼠中,共发现25个代谢产物(血浆中8个、尿液中17个、粪便中11个、胆汁中19个、体外肠道菌群3个)。在牙周炎模型大鼠中,共发现27个代谢产物(血浆中8个、尿液中18个、粪便中12个、胆汁中22个、体外肠道菌中2个)。升麻素苷原型及30种代谢物的详细信息见表1。 3.3.1 I相代谢物的鉴定 (1)水解(M1):M1的保留时间为10.14 min,准分子离子为m/z 307.118 0,推测其分子式为C16H18O6。M1的相对分子质量比M0少162(C6H10O5),此外,M1的特征碎片离子m/z 307.118 0、289.107 4、274.085 0、259.059 5、247.061 9、235.059 4、233.044 1、221.043 9、217.050 3、205.049 6、189.055 0、177.054 3、161.059 2均与M0相同,这表明M1在M0基础上发生了糖基化反应。且经过对照品比对,确认M1是M0脱糖产生的水解产物升麻素。 (2)水解-羟基化:M2~M5的保留时间分别为5.98、7.12、7.92、8.65 min,准分子离子峰分别为m/z323.113 4、323.111 2、323.112 8、323.113 0,均比M1多16,表明M2~M5可能为M1的单羟基化产物,推测其是分子式C16H18O7的同分异构体。M2的特征碎片离子m/z323.113 4、305.101 9、275.085 0、263.064 4均比M1的特征碎片离子m/z307.118 0、289.107 4、259.059 5、247.061 9多16,此外M2的特征碎片离子m/z 247.060 2、235.059 4、233.046 2、221.044 1、177.054 9均与M1的特征碎片离子保持一致,尤其特征碎片m/z263.064 4的存在,说明该羟基化反应发生在C-2′位。M3的特征碎片离子m/z 323.111 2、305.109 0、275.055 4均比M1的特征碎片离子m/z 307.118 0、289.107 4、274.085 0、259.0595多16,且其特征碎片离子m/z 235.031 5、233.035 6、205.072 2、193.050 1均与M1的特征碎片保持一致,说明该羟基化反应可能发生在C-5′位或者C-2′位。M4的特征碎片离子m/z259.060 0、247.060 0、235.060 2、233.044 6、221.044 8、205.048 5、189.054 3、177.054 9、161.060 1与M1具有相同的裂解途径,且根据其特征碎片m/z 305.1015的存在,推测羟基化的位置可能在C-3′位。M5的碎片离子m/z323.113 0、305.102 6与M1相比增加了16,其特征碎片离子m/z 259.061 1、247.060 1、235.060 3、233.043 9、221.044 7、205.050 2、189.054 9、177.054 5均与M1具有相同的裂解途径,尤其特征碎片离子275.054 8的存在,推测M5的羟基化反应可能发生在C-8位上。通过计算ClogP值发现,M2~M5的ClogP值分别为?0.859 1、?0.756 5、?0.364 7、?0.018 9,与保留时间的大小具有一致性,证明了推测的合理性。 (3)水解后失去CH2:M6保留时间为12.85 min,准分子离子峰为m/z293.102 3,推测其分子式为C15H16O6,是在M1的基础上丢失1个CH2。M6主要的二级碎片离子m/z 293.102 3、275.091 6、245.043 7、221.044 8均比M1的碎片离子m/z307.118 0、289.107 4、274.085 0、259.059 5、235.059 4少14,且由于特征碎片m/z 275.091 6、233.044 7的存在,提示反应位点可能在C-5。 (4)水解后失去CH2+O:M7、M8的保留时间分别为7.19、9.67 min,准分子离子峰分别为m/z 309.096 6、309.097 7,推测其分子式为C15H16O7。与M6相比多了16。因此,代谢物M7、M8被初步鉴定为M6的羟基化产物。M7的特征碎片离子m/z233.026 8、221.029 1、205.031 9均与M6保持一致,且其特征碎片离子m/z309.096 6、291.099 1与M6相比增加了16,提示羟基化的位置发生在侧链上,推测反应位点在C-5′位。M8的特征碎片m/z 233.050 8、221.045 6、177.083 7均与M6的特征碎片离子保持一致,说明M8与M6具有相同的裂解途径,且有特征碎片m/z 249.164 1的存在,说明羟基化的位置在环上,推测反应位点可能在C-8位。此外,根据上述所推结构,计算M7、M8的ClogP值分别为?0.320 8、0.337 1,与出峰时间保持一致,证明了推测的合理性。 (5)水解后去甲基化成羧酸:M9、M10的保留时间分别为7.78、9.30 min,准分子离子峰分别为m/z337.092 9、337.091 9,推测其分子式为C16H16O8。与M1相比多了30,推测M9、M10是M1结构中的1个甲基被氧化成羧酸后得到的代谢产物。根据M1的结构特征推测发生反应的位点可能是与C-5连接的甲氧基及C-5′位的甲基上。M9的特征碎片离子m/z 337.092 9、319.082 3、304.060 0、289.032 9、277.071 1、265.032 2、263.056 3、235.024 3、219.029 1、207.043 8均比M1的特征碎片离子离子m/z 307.118 0、289.107 4、274.085 0、259.059 5、247.061 9、235.059 4、233.044 1、205.049 6、189.055 0、177.054 3多30,因此证明M9氧化位点发生在C-5位连接的甲氧基上。M10在正离子模式下形成的准分子离子峰为m/z 337.091 9,与M1相比多30,其特征碎片离子m/z274.130 1、259.063 0、247.060 7、235.061 7、233.045 8、205.051 7、161.061 8均与M1的特征碎片离子保持一致,说明其氧化位点发生在M1的侧链上而不在环上,故推测反应位点发生在C-5′位。根据以上推测的结构,计算两者的ClogP值分别为?1.233 0、?0.585 6。计算结果与出峰时间顺序保持一致,进一步确证了推测的合理性。 (6)水解后去甲基化成酮:M11保留时间为10.96 min,准分子离子峰为m/z 291.086 3,推测其分子式为C15H14O6。与M1相比少了16,推测在M1的基础上失去了1个甲基进一步将连接在中心碳原子上的羟基氧化成酮。M11的特征碎片离子m/z 291.086 3、273.076 7、258.058 0与M1相比均少16,特征碎片离子m/z 259.062 8、235.096 5、233.044 7、221.041 4、177.052 1与M1保持一致,说明反应发生在侧链上,因此推测反应发生在C-4′位。 (7)水解脱羟基:M12的保留时间为9.83 min,其准分子离子峰m/z 291.122 6,推测其分子式为C16H18O5。与M1相比少了16(O),推测M12在M1的基础上发生了脱羟基反应,M12的特征碎片离子m/z 273.076 0、263.092 2、219.025 6、217.159 5均比M1的特征碎片离子m/z 289.107 4、247.061 9、235.059 4、233.044 1少16,说明脱羟基位发生在C-9位。 (8)水解后失去CH2O:M13的保留时间为8.24 min,其准分子离子峰为m/z277.106 7,推测其分子式为C15H16O5。与M1相比少了30(CH2O),推测M13可能是在M1的基础上丢失甲氧基产生的代谢物。M13的特征碎片离子m/z 259.101 8、217.054 2、205.052 8、181.089 7可能是M1的特征碎片离子m/z289.107 4、247.061 9、235.059 4、221.043 9丢失1个甲氧基产生的,根据M1的结构特点推测丢失位点在C-5位。 (9)水解后脱羟基失去CH2O:M14的保留时间6.48 min,其准分子离子峰为m/z261.112 5,推测其分子式为C15H16O4。与M12相比少了16,与M1相比少了46(M1-O-CH2O),推测M14可能是在M1的基础上先失去羟基又失去甲氧基产生的。M14的特征碎片离子m/z 243.215 1、228.206 8、189.090 3与M1的特征碎片离子m/z 289.107 4、274.085 0、235.059 4相比均少46,且M14的特征碎片离子m/z243.215 1正好比M12的特征碎片离子少16,证明推测合理。 (10)水解脱羟基后被氧化成醛:M15的保留时间为8.23 min,其准分子离子峰为m/z 305.102 4,推测其分子式为C16H16O6。M15的特征碎片离子m/z 287.132 8比M12的特征碎片离子m/z 273.076 0多14,水解后脱羟基位点与M12保持一致。且其特征碎片离子m/z290.071 9、275.054 4、247.058 3、233.044 4可能是在M15的准分子离子m/z 305.102 4的基础上通过连续丢失2个甲基、CO和亚甲基产生的。因此,推测M15是代谢物M12中的1个甲基被氧化成醛产生的。根据母药结构特点,结合π-π共轭体系可能使结构更加稳定的规律,推测氧化反应位点最可能发生在2位的CH3上。 (11)失去C4H8O:M16的保留时间为8.80 min,其准分子离子峰为m/z397.113 6,推测其分子式为C18H20O10。与M0相比少了72,根据其结构特点推测M16可能是M0失去C4H8O所得到的代谢产物,其特征碎片m/z 235.05 51、205.136 9与M0保持一致,且特征碎片m/z72.086 6(-C4H8O)的存在,初步认为推测M16的结构合理。 (12)水解脱羟基后去甲基成羧酸:M17的保留时间为11.08 min,其准分子离子峰为m/z 321.097 4,推测其分子式为C16H16O7。与M9相比少了16,与M1相比多了14,推测M17可能是M1脱羟基后的1个甲基被氧化成羧酸的产物。其特征碎片离子m/z 321.097 4、303.085 9正好比M1的特征碎片离子m/z289.107 4多14,比M9的特征碎片离子m/z 319.082 3少16,特征碎片离子m/z273.039 5比M9的特征碎片离子m/z 289.032 9少16,且其含有特征碎片离子m/z 235.022 7、205.049 6,与M1和M9一致。说明M17与M9结构相似,氧化位点与M9一致。 (13)单羟基化反应:M18~M20的保留时间分别为6.24、6.93、9.00 min,其准分子离子峰分别为m/z 485.166 2、485.166 5、485.164 7,推测其分子式为C22H28O12。与M0相比多了16(O),因此推测他们可能是M0的单羟基化产物。根据母药的结构特点可以看出羟基化反应发生在C-3′、C-5′和C-8位时相对稳定。M18的特征碎片离子m/z247.060 0、235.058 3、233.043 8、205.048 4均与M1的特征碎片离子保持一致,且其特征碎片

问题:暑湿感冒颗粒中5-O-甲基维斯阿米醇苷、升麻素苷的检测对照品分析中5-O-甲基维斯阿米醇苷的理论塔板数是?答案:24128.072【活动奖励】幸运奖(2钻石币):抽奖软件,当天随机抽取3个回答正确的版友ID号(最后一个ID号,截止至下午3:00),每人奖励2个钻石币zengzhengce163(注册ID:zengzhengce163)ZHAOGUANGXI(注册ID:ZHAOGUANGXI)caishendao(注册ID:caishendao)http://ng1.17img.cn/bbsfiles/images/2016/03/201603021507_585734_1610895_3.pnghttp://ng1.17img.cn/bbsfiles/images/2016/03/201603021507_585735_1610895_3.png积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================暑湿感冒颗粒中5-O-甲基维斯阿米醇苷、升麻素苷的检测样品制备 制备方法1. 对照品:取5-O-甲基维斯阿米醇苷对照品、升麻素苷对照品适量,精密称定,加甲醇制成每1 mL各含20 μg的溶液,即得。2. 供试品:溶液取装量差异项下的本品,研细,取约4 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 mL,称定重量,加热回流2小时,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。分析条件 色谱柱Diamonsil C18 150 x 4.6 mm,5 μm (Cat#:99901)流动相A:甲醇 B:水 梯度流速1 mL/min柱温30 ℃检测器UV 290 nm 进样量10 μL 色谱图对照品 http://ng1.17img.cn/bbsfiles/images/2016/03/201603020958_585675_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 26.320 311583 8810 12825.336 0.927 -- 2 49.733 341906 7082 24128.072 0.905 21.185 *药典要求理论板数按5-O-甲基维斯阿米醇苷峰计算应不低于5000供试品 http://ng1.17img.cn/bbsfiles/images/2016/03/201603020959_585676_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 26.289 39166 1313 16830.923 0.935 -- 2 49.737 62730 1428 25652.736 0.937 22.846 *药典要求理论板数按5-O-甲基维斯阿米醇苷峰计算应不低于5000
白升麻【英文名】root of Tomentoseflower Larkspour【来源】药材基源:为毛茛科植物须花翠雀花的根。拉丁植物动物矿物名:Delphinium delavayi Franch.var.pogonanthum(Hand.-Mazz.)W.T.Wang采收和储藏:秋季采挖,取根部,除去茎叶、杂质,先净,晒干。【原形态】须花翠雀花,多年生草本。茎高60-100cm,与叶柄密被平展的硬毛,毛长达2-3mm。茎下部叶具长柄,基部有狭鞘;叶片五角形,长4.5-6cm,宽7.5-11cm,3深裂,中深裂片菱形,再3浅裂,浅裂片有缺刻状小裂片和牙齿,侧深裂片斜扇形,不等2深裂,两面疏被糙伏毛。茎上部叶稀疏,渐变小。总状花序狭长,通常具多数花;基部苞片线状,其他苞片线状披针形,密被糙毛;花梗被毛,长1.2-3.5cm;萼片蓝紫色,宽椭圆形,外面疏被硬毛,距钻形;花瓣蓝色;退化雄蕊蓝色,瓣片长方形,2浅裂,腹面有白色或黄色髯毛;雄蕊无毛;子房密被柔毛。蓇葖果;种子倒卵球形,密生鳞状横翅。【生境分布】生态环境:生于海拔2600-3600m间山地灌丛、林中或林边草坡上。资源分布:分布于云南、四川、贵州。【化学成份】须花翠雀花含翠雀它灵(deltaline),翠雀它明(deltamine),甲基牛扁碱(methyllycaconitine),氨茴酰牛扁碱(anthranoyllycaconitine),狼毒乌头碱(lycoctonine),翠雀色明碱(delsemine),核替生酮(hetisinone),核替生(hetisine),洋翠雀康宁(ajaconine),还含滇川翠雀碱(delavaine)A、B。【性味】辛;凉【归经】肺经【功能主治】清热解表;升阳。主风热头痛;水泻
核苷类成分含量测定,有鸟苷、尿苷、腺苷,10mmol/L磷酸二氢钠(1%磷酸调pH 2.6-2.7):甲醇(97:3);C18柱,检测波长254nm,25℃柱温当时我把ph调到2.60,样品中(板蓝根注射液)三种核苷类均能很好的分开;今天ph2.61,结果腺苷和鸟苷的保留时间均延长了3min左右,而且样品图谱中鸟苷的峰与其它峰合并在一起了。想来想去其它的条件都是一样的,唯独pH不同,是不是核苷类真的对ph敏感?
[size=16px][font=宋体]人参首载于《神农本草经》,性味甘、微苦、微温,归脾、肺、心、肾经,具有大补元气、复脉固脱、补脾益肺、生津养血、安神益智的功效。人参为五加科植物人参[/font][i]Panax ginseng[/i] C. A. Mey.[font=宋体]的干燥根及根茎[/font][sup][1][/sup][font=宋体]。栽培人参俗称[/font][font=宋体]“[/font][font=宋体]园参[/font][font=宋体]”[/font][font=宋体],播种在山林野生状态下自然生长的称林下山参,习称[/font][font=宋体]“[/font][font=宋体]籽海[/font][font=宋体]”[/font][sup][2][/sup][font=宋体],林下参有人为干扰少、生长周期长和绿色安全的优点。[/font] [font=宋体]人参皂苷有多种生物学活性,为人参中主要有效成分,同时也被认为是人参的药效物质基础[/font][sup][3-4][/sup][font=宋体]。人参皂苷根据皂苷元的结构分为原人参二醇型、原人参三醇型、齐墩果酸型[/font]3[font=宋体]类。原人参二醇型包括人参皂苷[/font]Rb[sub]1[/sub][font=宋体]、[/font]Rc[font=宋体]、[/font]Rb[sub]2[/sub][font=宋体]、[/font]Rb[sub]3[/sub][font=宋体]、[/font]Rd[font=宋体],人参三醇型包括人参皂苷[/font]Rg[sub]1[/sub][font=宋体]、[/font]Re[font=宋体]、[/font]Rf[font=宋体]、[/font]Rg[sub]2[/sub][font=宋体],齐墩果酸型包括人参皂苷[/font]Ro[sup][5-10][/sup][font=宋体]。近年来,国内外学者对于人参化学成分的[/font][font=宋体]研究逐渐向非药用部位发展[/font][sup][11][/sup][font=宋体]。有研究表明,人参花蕾和人参茎叶中的部分皂苷含量远远高于人参根中[/font][sup][6-8][/sup][font=宋体]。[/font][font=宋体]据统计,我国每年人参茎叶总产量可达人参产量的[/font]40%[font=宋体]~[/font]48%[font=宋体],且近年来产量逐年增加,市场价格却只有人参的[/font]1/50[font=宋体]。研究发现,林下山参茎叶中含有更为丰富的化学成分[/font][sup][7,10,12-13][/sup][/size][font=宋体][size=16px],其药用价值优于园参茎叶。因此,深度开发林下参茎叶对人参资源的综合开发具有十分重要意义. [font=宋体]结果显示,在林下参茎中未检测到人参皂苷[/font]Rb[sub]2[/sub][font=宋体]、[/font]Rb[sub]3[/sub][font=宋体],林下参叶中[/font]10[font=宋体]种皂苷含量远高于林下参茎中。在[/font]4[font=宋体]种年限林下参叶中,[/font]10[font=宋体]种人参皂苷总量在[/font]60[font=宋体]~[/font]100 mg/g[font=宋体],[/font]20[font=宋体]年时含量最高;在[/font]4[font=宋体]中年限林下参茎中,除人参皂苷[/font]Rb[sub]2[/sub][font=宋体]、[/font]Rb[sub]3[/sub][font=宋体]外的[/font]8[font=宋体]中人参皂苷总量在[/font]20[font=宋体]年最高;原人参二醇型皂苷[/font]20[font=宋体]年林下参中最高。原人参三醇型皂苷在[/font]15[font=宋体]年林下参叶中皂苷含量最高;[/font]4[font=宋体]种年限林下参茎、叶中差异性成分为人参皂苷[/font]Re[font=宋体]、[/font]Rd[font=宋体]、[/font]Rg[sub]1[/sub][font=宋体]和[/font]Rc[font=宋体]。林下参茎叶总皂苷可通过促进免疫低下小鼠的细胞免疫、体液免疫来增强免疫抑制小鼠的免疫功能,林下参茎叶总皂苷还可通过增强免疫发挥抗肿瘤活性[/font][sup][13,16][/sup][font=宋体]。本研究发现,林下参茎叶中皂苷类成分主要集中在叶,不同年限的林下参叶中皂苷含量不同可能会导致药效的不同,因此不同年限林下参叶间的药效差异仍需进一步探讨。[/font][font=宋体]生长年限对林下山参茎、叶皂苷含量影响显著,同时,[/font]10[font=宋体]种皂苷、原人参二醇型、原人参三醇型、齐墩果酸型皂苷含量随生长年限变化规律差异很大,皂苷增加的量并不是与年生长量呈等比关系,原因可能是人参生长到一定年限,其活性物质的累计率会降低[/font][sup][17][/sup][font=宋体]。我国的人参种植面积、总产量均居世界首位,每年用于出口、医药健康领域及功能性食品开发方面逐年加大,药用植物资源需求明显增多[/font][sup][14][/sup][font=宋体]。由于人参产量的大幅增加,人参茎叶等非药用部位的产量逐年增加,现代工业生产人参单体皂苷多选择以人参茎叶为原料,提取总皂苷,再进一步纯化、结构修饰得到人参单体皂苷[/font][sup][18-19][/sup][font=宋体]。研究发现,人参叶质量占人参茎叶质量的[/font]25%[font=宋体],其中总皂苷含量远高于人参茎中皂苷含量[/font][sup][20][/sup][font=宋体]。[/font][font=宋体]由此可推断,可根据提取的皂苷成分不同,有针对性的选择不同生长年限的林下参茎、叶,可有效提高提取效率。人参非药用部位的开发与利用势在必行。本研究从不同生长年限林下参茎、叶出发,考察其中[/font]10[font=宋体]种皂苷含量及其变化规律。为林下参非药用部位资源的开发与利用提供理论依据。[/font][/size][/font]
香草醛-冰醋酸显色针对的苷类包括黄酮苷、蒽醌苷、皂苷吗?因为我做的UV里面苷类成份特别多,而我只想测黄芪总苷,但阴性有干扰,现在解决不了,谁能帮我解决一下,谢谢
甘薯类能用761来做前处理吗?这类样品糖分大,含水量低。
大家好,最近在帮药厂做一个一类原料药,主成分是β构型的苷。我们都知道糖优势构型是β构体,但也存在少量α构体,两者会互相转化,成苷后就不会转化。现在在做这原料药的有关物质项,想问下要把α构体当做杂质专门建方法去控制吗?α构体和主成分(β构体)在目前的色谱条件下分不开。问过药厂,他们没做过α构体的药理和毒理。谢谢~
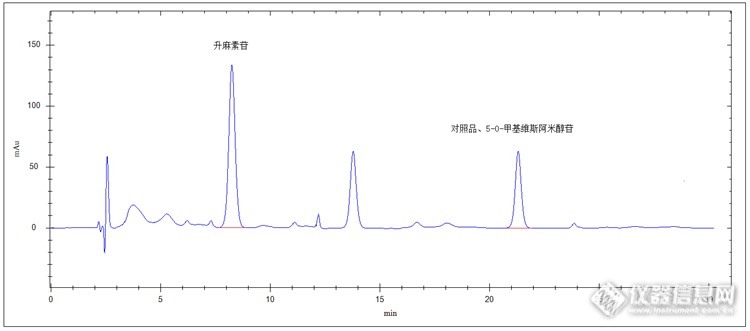
防风药品高效液相色谱检测 防风为伞形科植物,生于草原、干燥山坡等地。主产区位于黑龙江、吉林、内蒙、河北等地。 防风具有解表祛风,胜湿止痉,解热止痛、抗菌消炎等功效。用于治疗感冒头疼、风湿痹痛、四肢拘挛、风疹瘙痒、破伤风等病症。 药物成分及含量是大事,不得马虎。检测很重要,准确的检测更重要。下面我们就看下防风药材高效液相色谱法检测。检测原理 取防风药品适量,加甲醇溶解,恒温水域回流提取,由进样器进入高效液相色谱系统,C18色谱柱分离,紫外检测器检测,保留时间定性,峰面积定量(外标法)计算。对照品溶液的制备 分别精密称取升麻素苷(C22H28011)对照品、5-0-甲基维斯阿米醇苷(C22H28010)对照品3mg于50ml容量瓶中,分别加甲醇至刻度,配制成60μg/ml升麻素苷对照品及5-0-甲基维斯阿米醇苷对照品溶液,备用。供试品溶液的制备[/fon
请问大家酚苷类化合物属于酚类吗?有些文献里酚类包含酚苷,有些却不包含,好头疼
http://simg.instrument.com.cn/bbs/images/default/em09502.gif今天终于把十三种β-兴奋剂的药做出来了,下午开始摸索氨基糖苷类的药物,我们主要做的药是庆大霉素,丁胺卡那霉素,安谱霉素,链霉素,新霉素这几种药!做的时候发现他们的响应值不高,200ppb的响应值只有10的2次方,还有如果按照标准使用大比例的水相,那么一分钟就会所有的药都出来了,我是用C18的柱子。难道这些氨基糖苷类的药物要用大比例的有机相出峰时间才能够控制?还有我配置标准溶液的时候,用小比例的水把这些什么霉素溶解后,再用甲醇定容会出现很多沉淀,做过这些药的亲们,你们是怎么个定容法?

http://ng1.17img.cn/bbsfiles/images/2017/01/201701091458_620587_676_3.jpg通常市面上常见乳酸菌的营养食品,今天在一篇文章中发现还有芽袍杆菌类微生态制剂,除具有营养价质外,还有耐高温的性能与大家分享一下。根据菌种类型不同,微生态制剂可分为单一菌种微生态制剂、复合微生态制剂。单一菌种微生态制剂又可分成乳酸菌类、芽孢杆菌类、酵母菌类、霉菌类和光合细菌等。芽孢杆菌在逆境下可以产生芽孢来抵抗不良生长环境的影响,因此是很好的微生态制剂生产菌种,人们对芽抱杆菌的研究也越来越多。利用芽孢杆菌生产微生态制剂具有很多的优点:一当芽孢杆菌以芽抱的形式存在时,进入人或动物胃肠道时可以耐受胃酸和胆盐且保持高活性。二由于芽孢的存在可以耐受100℃的高温,在生产制剂制粒的过程中损失率比较小,活性高,保存时间长。三,芽孢杆菌类可以产生活性很强的淀粉酶、蛋白酶、脂肪酶、纤维素酶等多种酶类物质,还可以产生某些小环肤类细菌素或者一些多肤类物质,其对肠道中的致病均有拮抗作用。
请问我想处理含药血浆,也就是想从血浆中提取该药,药为环烯醚帖苷类,我选何种SPE小柱?还有其他处理方法吗?
兄弟姐妹们,求助一篇文献:利用液相色谱/三重串联四极杆质谱多反应监测优化离子选择评估油橄榄类保健品
齐墩果酸五环三萜类极性很小,人参皂苷类极性较大,但是两者都同属三萜类,都是末端吸收203~210nm,按道理说可以采用紫外检测器同时检测。这几天走了几个梯度条件都不理想http://emuch.net/bbs/images/smilies/cry.gif,我的思路是这样的:先采用中国药典2010版人参项下条件走60min(主要是乙腈-水,水比例较高80~45),然后梯度增加乙腈的比例,走至100min,但是齐墩果酸还是走不出来,请教各位能不能把保留时间限定在100min内,把上述两类成分分离呢?http://emuch.net/bbs/images/smilies/work.gif
氨基糖苷类的抗生素大家都用什么展开剂配比啊?显示剂用什么好啊? 我现在用正丁醇冰醋酸水感觉效果不好,物质拖成带了。 显色剂不知道用什么好。各位帮帮忙啊。
最近在开展氨基糖苷类(包括卡那霉素\庆大霉素\链霉素\双氢链霉素\新霉素\安普霉素等)的检查,虽然有国标使用c18在做,但考虑到七氟丁酸容易污染到质谱,很是怕怕,所以就选择了hilic色谱柱。第一次接触hilic色谱柱,遇到了以下问题:现象:1. 使用等度洗脱,乙腈:水=90:10,所有项目的保留时间都在2.6min附近。2. 使用梯度洗脱,流动相还是乙腈:水,每个项目出现了两个保留时间,一个还是在2.6min附近,另一个在9min附近,两个保留时间都是在乙腈比例最高的时候出现。3.怀疑出现的峰是色谱柱被洗脱掉的物质,使用空白水进行测试(以上标准品使用水溶解),未出峰。排除是色谱柱及液相系统的问题,说明这些峰应该是想要的标准品峰。4.从论坛资料查询到的,有人说是用乙酸铵或甲酸铵可以,经测试,加入铵后,标准品不出峰或惨不忍睹。我使用的是10mM的浓度,不清楚是否是浓度太高的问题,但我觉得可能性不大。疑问:1。所有的标准品保留时间一样,非常奇怪,很是怀疑这到底是不是我要的标准品峰。2。跑标准曲线,不成线性,甚至部分项目低浓度的感度高于高浓度的,郁闷。。。3。保留时间无法再向后拖了,因为乙腈的比例够高了,应该再怎样改变保留时间呢?自己也搜索了一些资料,可是还没有一个比较完善的关于HILIC色谱柱的使用方法的资料,论坛中有人说使用HILIC是可以分析这些物质的,但给出的资料或说明又难以让人信服。所以,希望对HILIC了解或正在使用HILIC的大侠多多给点意见,如果有人确实在做这几种物质的话(使用HILIC),小生那更是感激不尽了。。。。欢迎大家在此热烈讨论。。。更新:在论坛上搜到了个HILIC方法开展指南,给大家分享下。欢迎继续探讨,希望这个帖子能够成为hilic开展方法的探讨贴。。。更新: 看了些资料,hilic色谱柱使用需要以下注意事项:1。流动相至少需要5%的极性溶剂(如水,甲醇等)2。流动相需要不低于40%的有机相(如乙腈)3。使用甲酸铵或乙酸铵能得到较好的重现性。4。定溶液不能使用100%的水5。平衡时间比较长,一般需要10倍以上的柱体积平衡更新: 经过一段时间的测试,通过使用hilic色谱柱目前还没有得到良好的效果。使用资生堂的一款链霉素专用色谱柱,保留特性不错,只是感度还有点差,需要再进行优化。由于最近忙于粘杆菌素的开展,氨基糖苷类的测试需要拖一拖了,如果,谁也在做粘杆菌素,不妨也来讨论下。
第一次接触HPLC-ELSD,现打算做皂苷类含量测定,请问需要注意什么?氮气流速、气压条件如何定的?诸位多帮忙,急啊[em0808]
[align=center][b]韩国对肉干类强化检查[/b][/align] 韩国食品医药品安全局2010年3月23日发出通报称,韩国近期通过对流通中的进口肉干类进行调查,得出结论认为有强化该类产品卫生管理的必要性,所以食药局决定对该类产品强化监控检查。 主要内容: - 检查对象:肉干类(调味干鱼脯类、干鱼脯类、其他肉干类)。
主成分甾体皂苷除杂如色素,甾醇,脂类有什么方法啊
本人[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]新手,要建立一种中药成分 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]鉴定方法;使用仪器是waters,鉴定的物质是皂苷类,打算用一种方法测定6种不同皂苷含量流动相为乙腈A-水B,流速0.6ml/min,柱温25℃,波长203nm,进样量20ul梯度洗脱 0~12min 20%~35%A 12~32min 35%~40%A ;32~36min 40%A;36~37min 40~20%A 37~42 20%A。目前标品目标峰分离良好,测量样品无法与目标峰对应,无法完全分离,且杂质影响较大。请问大神们,像这种情况应该如何优化
[font=仿宋][color=#222222]黑[/color][/font][font=仿宋][color=#222222](紫)色食物含有丰富的花色苷、多酚类等植物化学物质,比如白黎芦醇、斛皮素等,这类物质都有抗氧化作用,减少自由基对身体的损伤,抗炎症、保护血管内皮细胞,改善认知、提高记忆功能,对于防治阿尔茨海默病、帕金森病等神经退行性病变的发生有重要意义。[/color][/font]
各位师兄师姐,有没有拿二级测氨基糖苷类(我做庆大霉素、依替米星和阿米卡星)吗?柱子和流动相用的什么呀?七氟丁酸实验室不给用,HPLC实验室只有紫外和荧光检测器,不能做ELSD和FID。我的课题刚上手,好多不太懂,老师催着摸方法,好纠结。。。谢谢各位师兄师姐~
请问有人做氨基糖苷类药物残留吗?[url=https://insevent.instrument.com.cn/t/Yp][color=#3333ff]液质[/color][/url]方法?液相条件请不吝赐教!太让人头疼了谢谢了!!!!!!!!
在学习防风,可没找到升麻素苷和5-O-甲基维斯阿米醇苷的相关性质。求教!!![em0910]
十二酰N甲基甘氨酸钠是属于椰油酰甘氨酸钠一类吗?它不是也是肌氨酸吗?求助各位大神
谁能提供一些防风中有效成分[b][color=#f10b00]升麻素苷[/color][/b]和[b][color=#f10b00]5-O-甲基维斯阿米醇苷[/color][/b]的具体资料?