[配法] 麦芽糖40g,蛋白胨10g,琼脂20g,蒸馏水1L。 (本培养基如不加入琼脂,即为沙保罗液体培养基) 将上述成分溶于水,加热溶解,调pH至6.0±0.2,分装三角瓶或试管中,118℃灭菌15min,倾注平板或置斜面,无菌试验后备用。注:⑴ 本培养基如不加入琼脂,即为沙保罗液体培养基,供真菌及念珠菌的增菌培养用。⑵ 增加氯霉素0.05~0.125mg/ml或放线菌酮0.5mg/ml,可抑制细菌和污染的霉菌及隐球菌生长。此二种药均耐热,可直接加入培养基内高压灭菌。⑶ 添加酵母浸膏5mg/ml,可促进皮肤癣菌生长。增加维生素B 0.1mg/ml,可促进紫色癣菌和断发癣菌生长。⑷ 将麦芽糖减少到20g/L,为沙保罗20g/L麦芽糖琼脂培养基,可供诱导真菌产生孢子用。⑸ 该培养基呈酸性,应提高20%的琼脂用量。
DM培养基PP:DM培养基是一种好氧反硝化培养基,该培养基中在为好氧反硝化菌提供丰富的碳源及氮源的同时,也提供了多种微量元素。该培养基还具用良好缓冲效果。具体配方如下:DM(g/L):NaB2BHPOB4B •7HB2BO 7.9;KHB2BPOB4B 1.5;NHB4BCl 0.3;微量元素溶液 1mL;pH值 7.2。微量元素溶液( g/L ) : EDTA 50.0 ; ZnSOB4B 2.2 ; CaClB2B 5.5 ;MnClB2B • 4HB2BO 5.06 ; FeSOB4B • 7HB2BO 5.0 ; (NHB4B)B6BMo7OB2B • 4HB2BO 1.1 ;CuSOB4B•5HB2BO 1.57;CoClB2B•6HB2BO 1.61;pH值 6.0。2.FM培养基PP:FM培养基是好氧反硝化菌的富集培养基,是在牛肉膏及蛋白胨培养基基础上添加硝酸钾配置而成。对好氧反硝化菌具有富集及诱导好氧反硝化酶表达的效果。具体配方如下:FM(g/L):牛肉膏1.0;蛋白胨5.0;KNOB3B 1.0;pH值 7.2。
培养基是人工配制的供微生物或动植物细胞生长、繁殖、代谢和合成人们所需产物的营养物质和原料,同时,培养基也为微生物等提供除营养外的其它生长所必须的环境条件。常用的培养基都应符合一些基本要求:1 ) 都必须含有作为合成细胞组成的原料;2 ) 满足一般生化反应的基本条件,如碳源、氮源、无机盐、生长因素;3 ) 一定的pH等条件。 2 培养基的组成 2.1 碳源 碳源是组成培养基的主要成分之一。常用的碳源有糖类、油脂、有机酸和低碳醇。在特殊情况下( 如碳源贫乏时) ,蛋白质水解产物或氨基酸等也可被某些菌种作为碳源使用。葡萄糖是碳源中最易利用的糖,几乎所有的微生物都能利用葡萄糖,所以葡萄糖常作为培养基的一种主要成分,并且作为加速微生物生长的一种有效的糖。但是过多的葡萄糖会过分加速菌体的呼吸,以致培养基中的溶解氧不能满足需要,使一些中间代谢物不能完全氧化而积累在菌体或培养基中,如丙酮酸、乳酸、乙酸等导致pH下降,影响某些酶的活性,从而抑制微生物的生长和产物的合成。 2.2 氮源 氮源主要用于构成菌体细胞物质( 氨基酸、蛋白质、核酸等) 和含氮代谢物。常用的氮源可分为两大类: 有机氮源和无机氮源。 2.2.1 有机氮源 常用的有机氮源有玉米浆、玉米蛋白粉、蛋白胨、酵母粉和酒糟等。它们在微生物分泌的蛋白酶作用下,水解成氨基酸,被菌体吸收后再进一步分解代谢。 有机氮源除含有丰富的蛋白质、多肽和游离氨基酸外, 往往还含有少量的糖类、脂肪、 无机盐、 维生素及某些生长因子, 因而微生物在含有机氮源的培养基中常表现出生长旺盛, 菌丝浓度增长迅速的特点。大多数发酵工业都借助于有机氮源,来获得所需氨基酸。 玉米浆是一种很容易被微生物利用的良好氮源。因为它含有丰富的氨基酸( 丙氨酸、 赖氨酸、谷氨酸、缬氨酸、苯丙氨酸等) 、还原糖、磷、微量元素和生长素。玉米浆是玉米淀粉生产中的副产物,其中固体物含量在50%左右,还含有较多的有机酸,如乳酸,所以玉米浆的 pH在4左右。 2.2.2 无机氮源 常用的无机氮源有铵盐,硝酸盐和氨水等。微生物对它们的吸收利用一般比有机氮源快, 所以也称之谓迅速利用的氮源。但无机氮源的迅速利用常会引起pH的变化。 氨水在发酵中除可以调节pH外,它也是一种容易被利用的氮源,在许多抗生素的生产中得到普遍使用。氨水因碱性较强,因此使用时要防止局部过碱,加强搅拌,并少量多次地加入。 2.3 无机盐微生物在生长繁殖和生产过程中,需要某些无机盐和微量元素如磷、 镁、 硫、 钾、 钠、 铁、氯、锰、锌、钙等,以作为其生理活性物质的组成或生理活性作用的调节物,这些物质一般在低浓度时对微生物生长和产物合成有促进作用,在高浓度时常表现出明显的抑制作用。在培养基中,镁、磷、钾、硫、钙和氯等常以盐的形式( 如硫酸镁、磷酸二氢钾、磷酸氢二钾、碳酸钙、氯化钾等) 加入,而钴、铜、铁、锰、锌、钼等缺少了对微生物生长固然不利,但因其需要量很少,除了合成培养基外,一般在复合培养基中不再另外单独加入。 2.3.1 磷 是核酸和蛋白质的必要成分,也是重要的能量传递者——三磷酸腺苷的成分;在代谢途径的调节方面,磷起着很重要的作用,磷有利于糖代谢的进行,因此它能促进微生物的生长。但磷若过量时,许多产物的合成常受抑制。2.3.2镁 除了组成某些细胞的叶绿素的成分外,并不参与任何细胞物质的组成。但它处于离子状态时,则是许多重要酶( 如己糖磷酸化酶、柠檬酸脱氢酶、羧化酶等) 的激活剂,镁离子不但影响基质的氧化,还影响蛋白质的合成。镁常以硫酸镁的形式加入培养基中。 2.3.3 氯 氯离子在一般微生物中不具有营养作用,但对一些嗜盐菌来讲是需要的,在一些产生含氯代谢物的发酵中,除了从其它天然原料和水中带入的氯离子外,还需加入约0.1%氯化钾以补充氯离子。 2.3.4钠、钾、钙 钠、钾、钙等离子虽不参与细胞的组成,但仍是微生物发酵培养基的必要成分。钠、钾离子与维持细胞渗透压有关,故在培养基中常加入少量钠盐、钾盐,但用量不能过高,否则会影响微生物生长。钙离子能控制细胞透性,它不能逆转高浓度无机磷对某些产品的抑制作用。 2.4前体、 促进荆和抑制剂发酵培养基中某些成分的加入有助于调节产物的形成,而并不促进微生物的生长。这些添加的物质包括前体、抑制剂和促进剂/ 包括诱导剂、生长因子等) 。2.4.1前体 指某些化合物加入到发酵培养基中,能直接被微生物在生物合成过程中结合到产物分子中去,而其自身的结构并没有多大变化,但是产物的产量却因加入前体而有较大的提高。 2.4.2促进剂 指那些既不是营养物又不是前体,但却能提高产量的添加剂。 2.4.3抑制剂 在发酵过程中加入抑制剂会抑制某些代谢途径的进行, 同时会使另一代谢途径活跃,从而获得人们所需的某种产物或使正常代谢的某一代谢中间物积累起来。 2.5 水 除了少数微生物如蓝细菌能利用水中的氢作为还原CO2时的还原剂外,其他微生物都不是利用水作为营养物质。即使如此,由于水在微生物的生命活动过程包括营养过程中的重要性,它仍应属于营养要素之一,为培养基的重要组成之一。 3 结束语 对某一微生物和产品来讲,究竟用哪些原料作培养基还需经过一系列实验的摸索,能确定一种既有利于微生物生长,又能保证得到高产优质的较为理想的培养基配方。另外,工业生产培养基所用的原材料还必须来源丰富、价格低廉、质量稳定。当然一种好的培养基配方还应随菌种的改良、发酵控制条件( pH、溶解氧、中间补料等工艺条件) 和发酵设备的变化而作相应的变化。
1.目的了解外源基因在原核细胞中表达的特点和方法。2.原理外源基因克隆在含有lac启动子的表达系统中。先让宿主菌生长,lac I产生的阻遏蛋白与lac操纵基因结合抑制下游的外源基因转录。向培养基中加入诱导物IPTG(异丙基硫代-b-D-半乳糖),解除抑制使外源基因大量表达。表达的蛋白可经SDS-PAGE或Western-blotting检测。3.器材旋涡混合器,微量移液取样器,移液器吸头,50ml 微量离心管,1.5ml 微量离心管,双面微量离心管架,台式冷冻离心机,制冰机,恒温摇床,分光光度计,超净工作台,恒温培养箱,摇菌试管,三角烧瓶,接种环。4.试剂LB培养基(加抗菌素),100mg/ml IPTG,20%葡萄糖。5.实验准备无菌ddH2O,1.5ml离心管装入铝制饭盒(灭菌)、移液器吸头装入相应的吸头盒(灭菌),牙签(灭菌),摇菌管(灭菌),100mg/ml IPTG (过滤灭菌)(100ml分装,-20°C保存),100mg/ml氨苄青霉素(过滤灭菌)(100ml分装,-20°C保存),配制20%葡萄糖(8磅灭菌20分钟,添加至上述LB中,终浓度为0.2%)。6.操作步骤(1) 晚上9:00接种。在超净工作台中接种含有Pinpoint™xa-3-CHI重组载体的菌株,培养于两个三角烧瓶各20ml LB-葡萄糖培养基(含抗菌素Amp 120μg/ml)的摇菌管中,慢速70~90转/分钟30°C摇菌过夜。(2) 至第二天上午8:30 OD600约为0.5,加IPTG至 100μg/ml,150~170转/分钟37°C诱导1.5-3h。同时做不加IPTG诱导和非转化的空菌诱导的对照培养。(3) 4000rpm离心15min弃掉上清液,收获菌体,用SDS-PAGE电泳分析(表达蛋白分子量为30kDa)。菌体也可放在-20°C以下保存备用。(4) 在被细菌污染的桌面上喷洒70%乙醇,擦干桌面。
培养基是发酵过程或动植物细胞大量培养中供微生物或动、植物细胞的生长、繁殖或积累代谢产物,以合成生物化工产品所必需的营养基质。培养基的选择应根据微生物生长代谢活动的需要,并有利于合成细胞物质和生物化工产品的生成。培养基中主要含有水、碳源(能源)、氮源、矿物质,有的还需要提供维生素等。在酶反应过程中,原料液中被转化的物质亦即酶的作用物,亦可称为底物。 培养基的选择一般尽可能要满足以下要求:①单位质量基质,应能产生最大量的生物物质或生物化工产品,并且要使所产生的生物物质或生物化工产品在发酵液中的浓度最高,产率最高,使不需要的其他代谢产物的生成,限在最低范围内。②培养基成本低、质量均一并随时保证提供使用。③培养基使用时,对通气、搅拌、后处理和三废治理等方面所产生的问题最少。 分类 按其组成成分分成三类:①天然培养基,全由天然产物组成,例如含淀粉、黄豆饼粉等天然物质;②复合培养基,由部分天然产物和部分已知成分的化合物组成,例如其中的氮源既有天然物质黄豆饼粉,又有合成化合物硫酸铵;③合成培养基,全由已知成分的化合物所组成,例如以纯的碳水化合物或碳氢化合物为碳源,以铵盐为氮源。天然培养基和复合培养基常用于工业生产,而合成培养基(偶尔包括复合培养基)则常用于试验。 按用途分类包括:①基础培养基,营养需求相似的一些生物其所需的营养物大体相同,因之可配制一种适合于它们共同需要的含有基本营养成分的基础培养基;②增殖培养基,又称丰富培养基,常用于菌种选育方面。它是由基础培养基,再加入特殊的营养物质,以使某种差异型微生物在其中迅速生长繁殖;③鉴别培养基,即在培养基中加入某种试剂,从而在培养过程中表现出特殊反应,用以鉴别不同类型的微生物,如无菌试验用的酚红肉汤培养基,就是一种鉴别培养基;④选择培养基,根据某些微生物具有特殊营养要求,或对某些化学物质具有抗性而设计的,例如在配方中加入某种化学药物,以限制对敏感菌的生长繁殖,而将对其不敏感的所需的微生物分离出来。如在分离酵母菌时,可加入青霉素、链霉素等以抑制细菌的生长。 培养基还可根据其形态分成液体或固体培养基。例如用于无菌试验的肉汤培养基为液体培养基。用于培养青霉菌孢子的小米或大米为固体培养基,在培养基中加入适量琼脂而形成的凝胶培养基,也称固体培养基。 成分 培养基的成分包括:碳源、氮源、矿物质,以及其他必需物质。这些成分通过生物反应过程,生成生物物质、生物化工产品,并放出CO2、H2O和热量。 培养基的成分还可以由发酵过程中所需的元素出发,如C、H、O、N、S、P、Mg、K等。此外,必要时还有一些需要量很少的微量元素,如Fe、Zn、Cu、Mn、Co、Mo、B等。在发酵过程中某些生物本身不能合成的物质,如氨基酸、维生素或核苷酸等,必要时亦作为营养物质加入到培养基中。 碳源 具有双重作用。生物在产生生物物质或生物化工产品过程中,它不仅为其提供碳源,也为其提供能源。碳水化合物是微生物发酵中的主要碳源,包括淀粉、葡萄糖、蔗糖和乳糖等。此外,植物油如豆油、棉籽油、玉米油等亦常被应用作为碳源。这类油常与表面活性剂合用,以消除发酵过程中所产生的泡沫。甲醇可用以生产单细胞蛋白。正烷烃类可用以生产有机酸、氨基酸和维生素等,甚至二氧化碳也可作为光合细菌的碳源。 氮源 包括无机氮源和有机氮源。无机氮源包括氨、铵盐及硝酸盐等,它们在被应用时应注意发酵中pH的变化;有机氮源包括氨基酸、蛋白质及尿素等,有机氮源的加入往往加快了生物的生长。因考虑到成本因素,一些有机氮源,如黄豆饼粉、花生饼粉、棉籽饼粉、玉米浆、鱼粉、酵母粉等常被选用。 培养基的组成中除了水分外,碳源和氮源的含量是最大的。碳源含量一般不超过10%,氮源含量较低,一般碳氮比应为3[
用灭菌剪刀剪去棉拭子与手接触的部分,将棉拭子置相应的液体培养基内。这个液体培养基可以是LST吗,还是只能是无菌生理盐水或PBS
1、各位老师请教一下,一般培养基瓶子上标的都是三年,打开的培养基,有效期是多长时间了,过期的培养基怎么处理。2,紫外线指示卡用完之后直接扔了就可以吗?属于危险废品吗?
首先需了解微生物需要的营养物质。 (1)微生物需要的营养物质营养物质应满足微生物的生长、繁殖和完成各种生理活动的需要。它们的作用可概括为形成结构(参与细胞组成)、提供能量和调节作用(构成酶的活性和物质运输系统)。微生物的营养物质有六大类要素,即水、碳源、氮源、无机盐、生长因子和能源。① 水水是微生物的重要组成部分,在代谢中占有重要地位。水在细胞中有两种存在形式:结合水和游离水。结合水与溶质或其他分子结合在一起,很难加以利用。游离水(或称为非结合水)则可以被微生物利用。② 碳源碳在细胞的干物质中约占50%,所以微生物对碳的需求最大。凡是作为微生物细胞结构或代谢产物中碳架来源的营养物质,称为碳源。作为微生物营养的碳源物质种类很多,从简单的无机物(CO2、碳酸盐)到复杂的有机含碳化合物(糖、糖的衍生物、脂类、醇类、有机酸、芳香化合物及各种含碳化合物等)。但不同微生物利用碳源的能力不同,假单孢菌属可利用90种以上的碳源,甲烷氧化菌仅利用两种有机物:甲烷和甲醇,某些纤维素分解菌只能利用纤维素。大多数微生物是异养型,以有机化合物为碳源。能够利用的碳源种类很多,其中糖类是最好的碳源。异养微生物将碳源在体内经一系列复杂的化学反应,最终用于构成细胞物质,或为机体提供生理活动所需的能量。所以,碳源往往也是能源物质。自养菌以CO2、碳酸盐为唯一或主要的碳源。CO2是被彻底氧化的物质,其转化成细胞成分是一个还原过程。因此,这类微生物同时需要从光或其他无机物氧化获得能量。这类微生物的碳源和能源分别属于不同物质。③ 氮源凡是构成微生物细胞的物质或代谢产物中氮元素来源的营养物质,称为氮源。细胞干物质中氮的含量仅次于碳和氧。氮是组成核酸和蛋白质的重要元素,氮对微生物的生长发育有着重要作用。从分子态的N2到复杂的含氮化合物都能够被不同微生物所利用,而不同类型的微生物能够利用的氮源差异较大。固氮微生物能利用分子态N2合成自己需要的氨基酸和蛋白质,也能利用无机氮和有机氮化物,但在这种情况下,它们便失去了固氮能力。此外,有些光合细菌、蓝藻和真菌也有固氮作用。许多腐生细菌和动植物的病原菌不能固氮,一般利用铵盐或其他含氮盐作氮源。硝酸盐必须先还原为NH+4后,才能用于生物合成。以无机氮化物为唯一氮源的微生物都能利用铵盐,但它们并不都能利用硝酸盐。有机氮源有蛋白胨、牛肉膏、酵母膏、玉米浆等,工业上能够用黄豆饼粉、花生饼粉和鱼粉等作为氮源。有机氮源中的氮往往是蛋白质或其降解产物。氮源一般只提供合成细胞质和细胞中其他结构的原料,不作为能源。只有少数细菌,如硝化细菌利用铵盐、硝酸盐作氮源和能源。④ 无机盐无机盐也是微生物生长所不可缺少的营养物质。其主要功能是:① 构成细胞的组成成分;② 作为酶的组成成分;③ 维持酶的活性;④ 调节细胞的渗透压、氢离子浓度和氧化还原电位;⑤ 作为某些自氧菌的能源。磷、硫、钾、钠、钙、镁等盐参与细胞结构组成,并与能量转移、细胞透性调节功能有关。微生物对它们的需求量较大(10-4~10-3 mol/L),称为“宏量元素”。没有它们,微生物就无法生长。铁、锰、铜、钴、锌、钼等盐一般是酶的辅因子,需求量不大(10-8~10-6 mol/L),所以,称为“微量元素”。不同微生物对以上各种元素的需求量各不相同。铁元素介于宏量和微量元素之间。在配制培养基时,可通过添加有关化学试剂来补充宏量元素,其中首选是K2HPO4和MgSO4,它们可提供需要量很大的元素:K、P、S和Mg。微量元素在一些化学试剂、天然水和天然培养基组分中都以杂质等状态存在,在玻璃器皿等实验用品上也有少量存在,所以,不必另行加入。⑤ 生长因子一些异养型微生物在一般碳源、氮源和无机盐的培养基中培养不能生长或生长较差。当在培养基中加入某些组织(或细胞)提取液时,这些微生物就生长良好,说明这些组织或细胞中含有这些微生物生长所必须的营养因子,这些因子称为生长因子。生长因子可定义为:某些微生物本身不能从普通的碳源、氮源合成,需要额外少量加入才能满足需要的有机物质,包括氨基酸、维生素、嘌呤、嘧啶及其衍生物,有时也包括一些脂肪酸及其他膜成分。各种微生物所需的生长因子不同,有的需要多种,有的仅需要一种,有的则不需要。一种微生物所需的生长因子也会随培养条件的变化而变化,如在培养基中是否有前体物质、通气条件、pH和温度等条件,都会影响微生物对生长因子的需求。从自然界直接分离的任何微生物,在其发生营养缺陷突变前的菌株,均称为该微生物的野生型。绝大多数野生型菌株只需简单的碳源和氮源等就能生长,不需要添加生长因子;经人工诱变后,常会丧失合成某种营养物质的能力,在这些菌株生长的培养基中,必须添加某种氨基酸、嘌呤、嘧啶或维生素等生长因子。⑥ 能源能源是指为微生物的生命活动提供最初能量来源的营养物或辐射能。化能异养型微生物的能源即碳源;化能自养型微生物的能源都是还原态的无机物,如NH4+、NO2-、S、H2S、H2、Fe2+等,它们分别属于硝化细菌、亚硝酸细菌、硫化细菌、硫细菌、氢细菌和铁细菌等。一种营养物常有一种以上营养要素的功能,即除单功能营养物外,还有双功能,甚至三功能营养物。辐射能是单功能;还原态无机养分常是双功能的(NH4+既是硝化细菌的能源,又是它的氮源)甚至是三功能的(能源、氮源和碳源);有机物常有双功能或三功能作用。(2)配制培养基必须遵循的原则微生物的培养基通常指人工配制的适合微生物生长繁殖,或积累代谢产物的营养基质。广义上说,凡是支持微生物生长繁殖的介质或材料,均可作为微生物的培养基。一个适当的培养基配方,对发酵产品的产量和质量有着极大的影响。针对不同微生物,不同的营养要求,可以有不同的培养基。但它们的配制必须遵循一定原则。① 营养物质应满足微生物的需要。不同营养类型的微生物对营养的需求差异很大,应根据菌种对各营养要素的不同要求进行配制。② 营养物的浓度及配比应恰当。营养物浓度太低,不能满足微生物生长的需要;浓度太高,又会抑制微生物生长。糖和盐浓度高有抑菌作用。碳氮比(C∶N,以还原糖含量与粗蛋白含量的比值表示):一般培养基为C∶N=100∶0.5~2。在设计培养基配比时,还应考虑避免培养基中各成分之间的相互作用,如蛋白胨、酵母膏中含有磷酸盐时,会与培养基中钙或镁离子在加热时发生沉淀作用;在高温下,还原糖也会与蛋白质或氨基酸相互作用而产生褐色物质。③ 物理、化学条件适宜。pH:各种微生物均有其生长繁殖的最适pH,细菌为7.0~8.0,放线菌为7.5~8.5,酵母为3.8~6.0,霉菌为4.0~5.8。对于具体的微生物菌种,都有各自的特定的最适pH范围,有时会大大突破上述界限。在微生物生长繁殖过程中,会产生能够引起培养基的pH改变的代谢产物,尤其是不少微生物有很强的产酸能力,如不适当地加以调节,就会抑制甚至于杀死其自身。在设计培养基时,要考虑培养基的pH调节能力。一般应加入缓冲液或CaCO3,使培养基的pH稳定。其他:培养基的其他理化指标,如水活度、渗透压也会影响微生物的培养。在配制培养基时,通常不必测定这些指标,因为培养基中各种成分及其浓度等指标的优化,已间接地确定了培养基的水活度和渗透压。此外,各种微生物培养基的氧化还原电位等也有不同的要求。④ 培养目的:培养基的成分直接影响培养目标。在设计培养基时,必须考虑是要培养菌体,还是要积累菌体代谢产物;是实验室培养,还是大规模发酵等问题。用于培养菌体的种子培养基营养成分应丰富,氮源含量宜高,即碳氮比值应低;相反,用于大量积累代谢产物的发酵培养基,氮源应比种子培养基稍低;当然,若目的产物是含氮化合物时,有时还应该提高培养基的氮源含量。在设计培养基时,还应该特别考虑到代谢产物是初级代谢产物,还是次级代谢产物。如果是次级代谢产物,还要考虑是否需加入特殊元素(如维生素B12中Co)或特殊的前体物质(如生产青霉素G时,应加入苯乙酸)。在设计培养基,尤其是大规模发酵生产用的培养基时,还应该重视培养基组分的来源和价格,应该优先选择来源广、价格低廉的培养基。(3)几种培养基的配制原则① 种子培养基:适用于微生物菌体生长的培养基,目的是为下一步发酵提供数量较多,强壮而整齐的种子细胞。一般要求氮源、维生素丰富,原料要精。② 发酵培养基:用于生产预定发酵产物的培养基,一般的发酵产物以碳源为主要元素。发酵培养基中的碳源含量往往高于种子培养基。如果产物的含氮量高,应增加氮源。在
在日常实验称取培养基时,很难称到刚刚好,总会多一点少一点。有没有关于称量培养基允许差多少克的规定呢
用于菌数计数的半固体琼脂培养基促菌生长(灵敏度)检查的方法:对每个不同批号的脱水培养基均应进行灵敏度检查(促菌生长检查)。取预先制备好的琼脂培养基平皿3~5个,用表面涂布法每块平板表面接种30~100个试验菌,同时用已知质量保证的同型号培养基平皿3~5个(如较著名的如MERCK,DIFICOL,青岛海博产品)做对照试验,待培养基表面的菌液被琼脂培养基吸干或风干后,将培养皿倒置于培养箱的使用温度下培养48~72小时,(也可采用浇碟法进行)取出培养后的平皿点计菌落数。样品培养基上的微生物数量应不得低于对照培养基上微生物生长数量的70%。否则,需重新检查,或该培养基被视为不符合促生长要求。
一、培养基的历史体外培养(in vitro culture)包括:组织培养(tissue culture)、细胞培养(cell culture)、器官培养(organ culture)。顾名思义,就是将活体结构成分(如活体组织、活体细胞或者活体器官等)从体内或其寄生体内取出,放在类似于体内生存环境的体外环境中,让其生长发育的方法。广义组织培养与体外培养同义。体外培养已经历了约一百年的发展历史,但发展初期进程比较缓慢,没有引起很多学者的重视。直到上世纪50年代后期,体外培养技术才广泛应用于生物学研究的各个领域,使这项技术得到飞速发展。现在体外培养已成为细胞工程、基因工程、抗体工程的重要组成部分。细胞培养指从生物机体取出部分组织分散成单个细胞或直接从机体取出单个细胞,也可把体外培养细胞分散成单个细胞在体外条件下培养,细胞能继续存活与增殖。培养过程中细胞不再形成组织。发展与完善细胞培养技术围绕防止污染、改进培养方法、设计新型培养容器、设计不同的培养液等几个方面进行。1885年Roux温生理盐水培育鸡胚组织;1903年Jolly,1906年Beebe等发明了盖片悬滴培养;1907年Harrison培养蛙胚神经成功,开始创建盖片凹玻璃悬滴培养法; 1910、1912年Carrel采用无菌操作、更新培养基、传代,完善了悬滴培养法; 1924年Maximow采用双盖片悬滴培养法; 1923年Carral设计创立了卡氏瓶培养法,用此法可根据需要随时更换培养液,既有利于组织不断生长,又可以运用不同种类的营养液培养不同的细胞,极大地推动了当时组织培养研究。Earle等加以改进,使大量细胞能直接生长于玻璃瓶壁上,培养了正常细胞与肿瘤细胞的细胞株。至此大多数研究人员都采用培养瓶培养细胞。组织培养从二十世纪40年代起迅速发展,在培养容器、培养基和培养技术等方面出现了很多革新。在培养容器方面, 由简单的用试管、旋转管培养,发展到多种培养瓶培养,近年来,塑料瓶、皿、多孔培养板的使用已日趋普遍。在培养基方面,从50年代初,Parke、Eagle等设计出合成培养基后,从纯天然培养基到合成培养基、从鸡胚浸出液发展到动物血清(促细胞生长物),直至60年代设计出无血清培养基。首先反映在设计不同种类的缓冲盐溶液,以用来培养不同的细胞和洗涤细胞。Earle在1948年设计了含有碳酸氢钠等盐类的Earle氏盐溶液,Hank’s在1949年设计了Hank’s氏盐溶液。在培养技术方法方面,革新进展更为迅猛,Earle、Dulbecco等于1943年创建单层细胞培养法,首建长期传代的L-细胞系。 1948年Sanford创建单细胞分离培养法,获L-细胞纯系。 1951年Gey首建人肿瘤细胞——Hela细胞系。 1961年Hayflick首建人二倍体细胞系25种,开辟了应用新方向。 从50年代末开始,组织培养技术应用进入了一个繁盛的阶段,广泛应用于生物学和医学研究各个领域。 诱变建立遗传缺陷细胞株、杂交瘤技术制备单抗、发展细胞大量培养技术、利用重组技术构建工程细胞株,已成为生物工程的重要生产手段。 在连续灌注培养工艺方面,美国Ohashi,Ryo等人2001年报道采用2L一次性生物反应器灌注培养杂交瘤细胞生产单克隆抗体,以Becton Dickenson Cell Mab+10%胎牛血清+1%聚醚F-68为培养基,最高活细胞密度超过1×107cells/ml;2001年瑞士Heine, Holger等人用带超声细胞分离器(UCS)的连续灌注搅拌罐生物反应器培养鼠杂交瘤细胞生产单克隆抗体,稳态培养时活细胞密度超过2×107cells/ml;2004年德国Thomas等人在1L搅拌罐生物反应器中培养rCHO细胞生产人MUC-1糖蛋白,采取葡萄糖浓度限制的高产率灌注工艺减少有害代谢物,代谢转向TCA循环增加,活细胞密度保持在(1~2)×107cells/ml。在流加悬浮培养工艺方面,美国麻省理工Xie Liangzhi等人2000年报道在2L生物反应器中流加培养杂交瘤细胞,通过营养控制降低氨和乳酸的比生成速率,补充培养基包括营养成分、胎牛血清和痕量金属,最大活细胞密度达到1.7×107cells/mL。
如何有效管理微生物实验室干粉培养基在微生物检验中,培养基的质量关乎微生物的检验结果。加强对培养基的质量管理,能够有效提升微生物检验结果的准确性和科学性,因此需要注重培养基的质量管理工作。?本文从培养基的采购验收、质量控制、培养基制备后的质量控制以及培养基的灭菌和储存等环节简要分析了培养基的质量控制工作。1、培养基供应商选择培养基应当从可靠的供应商处采购,必要时应当对供应商进行评估。评估应确定其生产工艺,运输条件是否符合规定,资质是否齐全,质量保证能力和生产能力是否符合需求。如果新增培养基供应商,应对该厂家所生产的不同批次的培养基理化及微生物指标进行检测,并进行审计评估,评估合格后才可以将该品牌纳入合格供应商名录。2、培养基初步验收在培养基到达实验室后,应安排专业的人员对培养基进行验收,首先查看培养基的名称是否正确、配方是否符合药典或国标等相应的法规文件的要求、是否临近有效期、生产批号是否清晰、能否提供商品质检报告、检查包装是否完整,规格、数量是否与采购申请一致。在接收完毕后安排管理人员进行入库保存,并尽快安排对培养基进行入厂检测。3、培养基理化及微生物检测培养基的理化指标主要包括pH值、澄明度以及凝胶强度(琼脂类),培养基的微生物指标一般包括:灵敏度、促生长能力、抑制能力以及指示特性,即培养基适用性检查。这些指标供应商在培养基出厂前就已经进行了检测,合格后放行。使用单位验收时仍需进行培养基适用性检查,并与厂家提供的质检报告进行对比,看与报告内容是否一致。使用单位也可采用有资质的第三方检测报告。4、干粉培养基储存对入库保存的培养基应张贴标签,以区分验收与未验收的培养基,避免混淆与差错。在此为大家提供一个简单的标签,仅供参考:?点击重新加载使用单位存储培养基时标签也可以做编号处理,例如购进100瓶TSB,产品号为11104,其编号为11104-100-1、11104-100-2、...、11104-100-100按照流水号领用培养基,可减少对培养基的盘点,方便管理。培养基的储存条件一般为常温、干燥、密闭,当然不同供应商的存储条件稍有差别,按照标识执行即可。称量后应及时旋紧瓶盖,避免后期存储因空气湿度较大受潮或结块,如出现结块现象,该瓶培养基不可继续使用。培养基开瓶后在称量和存储的过程中会不可避免的吸收空气中的水分,而水分含量的增加,培养基的微生物负载可能亦随之增大,进而影响到干粉培养基的质量。所以干粉培养基在开瓶后,应定期进行复检,并对复检结果进行统计分析,确定开瓶有效期。如果实验室所在地区湿度较大(相对湿度高于75%),开瓶后的培养基应采取适宜的保护措施,如果数量较少,可放置于干燥器内,如果数量较多,可使用封口膜瓶口位置缠绕数匝。5、培养基配制--称量培养基的制备环节,应当严格按照培养基配方制备,在培养基的称量过程中,建议在干爽、无风的区域或者通风柜中进行,这样能够避免培养基吸潮使称量结果不准。应当选择灵敏度较高的称重天平,这样能够保证称量的准确性,同时称量过程中要选择专用的称量匙,避免其他杂质混入培养基中。操作人员应当对称量过程进行详细的记录,记录中应该体现培养基名称、批号、称量数量、具体配制方法、制备人姓名日期、复核人姓名日期等信息,方便后期的溯源调查。6、培养基配制--容器和水配制培养基所用的容器不得影响培养基质量,一般为玻璃容器,培养基配制所用的容器和配套器具应洁净,可用纯化水冲洗玻璃器皿以消除清洁剂和外来物质残留。在大体积配制培养基时,企业也可根据自己的情况采用不锈钢容器,建议专锅专用,且容器应洁净。不建议使用陶瓷或搪瓷容器。培养基用水是培养基制备过程中非常重要的一个物质。不可以使用自来水,自来水中的杂质可能会对检验结果有一定的影响。许多法规在培养基配方中采用蒸馏水作为配制用水,实际上纯化水的洁净程度不差于蒸馏水,甚至更优,所以不必单独制备蒸馏水,直接使用纯化水即可,配制用纯化水应按药典的要求定期进行检测。在制备过程中,可先加入培养基,再将纯化水倒入容器内,同时需要将器具内壁上的培养基粉末一同带到容器中,然后根据说明书的要求进行操作。涉及到大体积配制后要分装的培养基(例如TSA、TSB、FTM等),分装前一定要将培养基加热至完全溶解,避免后续可能会出现的瓶间差异。7、培养基的灭菌培养基的灭菌过程是影响培养基质量的关键环节。大部分培养基需要高温高压湿热灭菌,但部分选择性培养基由于一些组分不可高温高压灭菌,所以会采用煮沸灭菌,因此灭菌前应阅读培养基使用说明。?点击重新加载培养基灭菌应采用验证过的灭菌程序,灭菌参数应通过无菌性试验和促生长试验的验证。此外,对高温高压灭菌器的蒸汽循环系统也要加以验证,以保证其在一定装载方式下的正常热分布。温度缓慢上升的高压灭菌器可能导致培养基过度加热,过度灭菌会影响绝大多数的细菌和真菌培养基的促生长质量。灭菌器中培养基的容积和装载方式也会影响加热的速度。因此应根据灭菌培养基的特性,进行全面的灭菌程序验证。煮沸灭菌的培养基建议现配现用,高温高压湿热灭菌的培养基可以大量配制,在适宜的条件下储存,固体培养基灭菌后只允许一次再融化。灭菌后培养基的储存效期应进行验证。制备好的培养基,使用前需进行pH的监测。对于固体培养基pH监测,可使用平头电极或固液两用电极。
培养结核杆菌的培养基,从性状上分主要有固体培养基、液体培养基、半流体培养基、固液双相培养基等类型,这些培养基各有特点。 1.1 固体培养基 最常用的是罗氏(Lownstein-Jenson,L-J)培养基,也是最具代表性的一种,其他的还有小川辰次(Tatsujiogawa)鸡蛋培养基和Middle brook 7H10、7H11等琼脂培养基等。在固体培养基中,由于可以直接观察菌落的形态并可做鉴别用,因此常用于临床标本的分离培养、鉴别、保存菌种及对抗结核药物的敏感性测定等方面,缺点是结核菌生长缓慢。 1.2 液体培养基 常用的有苏通(Sauton)培养基、Middle brook 7H9等液体培养基。结核杆菌在液体培养基中能够更广泛的接触营养成分,因此在液体中生长相对较快,主要在液体表面生长,搅动时下沉至管底,可获得大量的结核杆菌。主要缺点是:在对临床标本的收集、采样、运输方面有不利的一面;不能根据肉眼观察菌落形态;培养基污染机会多,影响结核杆菌的生长,污染时不易与结核杆菌鉴别,需涂片染色镜检判断结核杆菌是否生长。 1.3 半流体培养基 改良苏通半流体琼脂培养基是一种人工综合培养基,基质透明,呈半流体状态,生长的结核杆菌形成白色颗粒状菌落悬浮于培养基中段,便于观察。 1.4 固液双向培养基 Septi-Check AFB双相培养基是国外应用较早的一种培养基,采用BD专利式封闭式固液双相一体化培养基设计。液相为Middle brook 7H9分枝杆菌专用增菌培养基,可迅速繁殖分枝杆菌,固相为3种固体培养基平面:Middle brook 7H11和改良的L-J培养基用于及时将增菌肉汤内分枝杆菌进行分离纯化以获得单个菌落,巧克力琼脂用于早期发现污染菌,避免时间浪费。由于有液相作为基础,因此结核杆菌生长较快,也是一种非常有效的培养基。国内有用平菇制备的平菇双相培养基是利用平菇浸出液为基础,加小牛血清、琼脂等成分而配制的一种培养基,根据琼脂的量不同制成液相、固相培养基。在国内应用较少,主要特点是成本低,制备简单,适合于基层使用,有一定的研究价值。
(一)按培养基用途分 1.营养培养基。含微生物生长繁殖所需基本营养物质的培养基常用以牛肉浸粉、蛋白胨、氯化钠为基础,也可增加所需的其他营养物质,如血液等。琼脂是培养基中常用的凝固剂,以支撑细菌的生长形态形成菌落,它对细菌无营养价值。 2.增菌运送培养基。将可疑标本接种于运送培养基中。增菌培养基为液体,是扩大培养的手段,也是细菌生化反应的主要培养方法。 3.选择鉴别培养基。在培养基中加入指示剂或化学物质,抑制某些细菌生长而有助于需要的细菌生长,或通过指示剂颜色变化分离鉴别细菌。 4.特殊培养基。包括厌氧培养基及其他(抗生素效价测定和药敏试验)培养基。 (二)按培养基物理性状分 1.液体培养基。将营养物质溶解于液体中,调整pH灭菌后即为液体培养基。常用于细菌增菌或观察细菌的生化反应。 2.固体培养基。液体培养基中加入13~15g/L琼脂,溶化后凝固成固体培养基。制成平皿,用于分离培养、活菌计数、选择培养、药敏试验。固体培养基可在试管中制成斜面用于菌种传代和短期保存。 3.半固体培养基。液体培养基中加入2~5g/L琼脂。用于细菌动力观察和菌种保存
培养基的成分还可以由发酵过程中所需的元素出发,如C、H、O、N、S、P、Mg、K等。此外,必要时还有一些需要量很少的微量元素,如Fe、Zn、Cu、Mn、Co、Mo、B等。在发酵过程中某些生物本身不能合成的物质,如氨基酸、维生素或核苷酸等,必要时亦作为营养物质加入到培养基中。 碳源 具有双重作用。生物在产生生物物质或生物化工产品过程中,它不仅为其提供碳源,也为其提供能源。碳水化合物是微生物发酵中的主要碳源,包括淀粉、葡萄糖、蔗糖和乳糖等。此外,植物油如豆油、棉籽油、玉米油等亦常被应用作为碳源。这类油常与表面活性剂合用,以消除发酵过程中所产生的泡沫。甲醇可用以生产单细胞蛋白。正烷烃类可用以生产有机酸、氨基酸和维生素等,甚至二氧化碳也可作为光合细菌的碳源。 氮源 包括无机氮源和有机氮源。无机氮源包括氨、铵盐及硝酸盐等,它们在被应用时应注意发酵中pH的变化;有机氮源包括氨基酸、蛋白质及尿素等,有机氮源的加入往往加快了生物的生长。因考虑到成本因素,一些有机氮源,如黄豆饼粉、花生饼粉、棉籽饼粉、玉米浆、鱼粉、酵母粉等常被选用。 培养基的组成中除了水分外,碳源和氮源的含量是最大的。碳源含量一般不超过10%,氮源含量较低,一般碳氮比应为3~4:1。碳、氮源含量不能过高的原因是避免产生基质或产物对反应的抑制和因渗透压过高引起细胞失水而死亡。 矿物质 培养基中 Mg、P、K、S、Ca、Cl常是主要的矿物质的组成成分,其他如Co、Cu、Fe、Mn、Mo及Zn也往往不可少,但需要量很小,可从其他主要培养基成分中得到。如是使用合成培养基就需要把这些微量元素加进去。它们不仅为生物生长所必需,也是为了得到某些产物所必不可少者。例如生物合成青霉素或头孢菌素需要一定量的硫;生物合成维生素B1需要一定量的钴。 维生素 某些生物在培养过程中需要某些维生素,往往在天然培养基中已经提供了必要的维生素,但在某些特殊情况下需单独加入维生素。例如在谷氨酸生产过程中需加入生物素,某些植物细胞培养中需要硫胺素(维生素B1)。 缓冲剂 由于发酵过程中pH对形成生物产物的影响很大,为维持稳定的pH,常采用缓冲剂,例如碳酸钙或磷酸盐。后者除能调节pH外,还为培养基提供磷源。
单个微生物在适宜的固体培养基表面或内部生长、繁殖到一定程度可以形成肉眼可见的、有一定形态结构的子细胞生长群体,称为菌落(colony)。当固体培养基表面众多菌落连成一片时,便成为菌苔(lawn)。不同微生物在特定培养基上生长形成的菌落或菌苔一般都具有稳定的特征,可以成为对该微生物进行分类、鉴定的重要依据。大多数细菌、酵母菌、以及许多真菌和单细胞藻类能在固体培养基上形成孤立的菌落,采用适宜的平板分离法很容易得到纯培养。所谓平板,即培养平板(culture plate)的简称,它是指固体培养基倒入无菌平皿,冷却凝固后,盛固体培养基的平皿。这方法包括将单个微生物分离和固定在固体培养基表面或里面。固体培养基用琼脂或其它凝胶物质固化的培养基,每个孤立的活微生物体生长、繁殖形成菌落,形成的菌落便于移植。最常用的分离、培养微生物的固体培养基是琼脂固体培养基平板。这种由Kock建立的采用平板分离微生物纯培养的技术简便易行,100多年来一直是各种菌种分离的最常用手段。 1. 稀释倒平板法(pour plate method) 先将待分离的材料用无菌水作一系列的稀释(如1:10、1:100、1:1,000、1:10,000......),然后分别取不同稀释液少许,与已熔化并冷却至50℃左右的琼脂培养基混合,摇匀后,倾入灭过菌的培养皿中,待琼脂凝固后,制成可能含菌的琼脂平板,保温培养一定时间即可出现菌落。如果稀释得当,在平板表面或琼脂培养基中就可出现分散的单个菌落,这个菌落可能就是由一个细菌细胞繁殖形成的。随后挑取该单个菌落,或重复以上操作数次,便可得到纯培养。 2. 涂布平板法(spread plate method) 由于将含菌材料先加到还较烫的培养基中再倒平板易造成某些热敏感菌的死亡,而且采用稀释倒平板法也会使一些严格好氧菌因被固定在琼脂中间缺乏氧气而影响其生长,因此在微生物学研究中更常用的纯种分离方法是涂布平板法。其做法是先将已熔化的培养基倒入无菌平皿,制成无菌平板,冷却凝固后,将一定量的某一稀释度的样品悬液滴加在平板表面,再用无菌玻璃涂棒将菌液均匀分散至整个平板表面,经培养后挑取单个菌落。 3. 平板划线法(streak plate method) 用接种环以无菌操作沾取少许待分离的材料,在无菌平板表面进行平行划线、扇形划线或其他形式的连续划线,微生物细胞数量将随着划线次数的增加而减少,并逐步分散开来,如果划线适宜的话,微生物能一一分散,经培养后,可在平板表面得到单菌落。 4. 稀释摇管法(dilution shake culture method) 用固体培养基分离严格厌氧菌有它特殊的地方。如果该微生物暴露于空气中不立即死亡,可以采用通常的方法制备平板,然后置放在封闭的容器中培养,容器中的氧气可采用化学、物理或生物的方法清除。对于那些对氧气更为敏感的厌氧性微生物,纯培养的分离则可采用稀释摇管培养法进行,它是稀释倒平板法的一种变通形式* 。先将一系列盛无菌琼脂培养基的试管加热使琼脂熔化后冷却并保持在50℃左右,将待分离的材料用这些试管进行梯度稀释,试管迅速摇动均匀,冷凝后,在琼脂柱表面倾倒一层灭菌液体石蜡和固体石蜡的混合物,将培养基和空气隔开。培养后,菌落形成在琼脂柱的中间。进行单菌落的挑取和移植,需先用一只灭菌针将液体石蜡--石蜡盖取出,再用一只毛细管插入琼脂和管壁之间,吹入无菌无氧气体,将琼脂柱吸出,置放在培养皿中,用无菌刀将琼脂柱切成薄片进行观察和菌落的移植。
为什么我倒的培养基一边厚一边薄,培养之后还有裂缝,求各位大神指点迷津
最近想总结下微生物检测指标用到的一些培养基的有效期,比如菌落总数用的营养琼脂培养基,标准有的写了有的没写,所以大家有没有知道的,告诉我一下呀~我现在知道的是品红亚硫酸钠培养基是冷藏两周,MFC是96小时,其他的营养琼脂,乳糖蛋白胨,伊红美蓝,EC培养基有没有知道的小伙伴?
1 外观控制制备好的培养基应有相应的颜色,一般的培养基应澄清、无浑浊、无沉淀。使用前应检查培养基的颜色是否发生变化,是否蒸发/脱水。2 污染控制 从每批制备好的培养基中选取部分进行污染测试(无菌试验),确定无微生物生长方可使用。3 性能测试3.1 测试菌株选择测试菌株是具有其代表种的稳定特性并能有效证明实验室特定培养基最佳性能的一套菌株,应来自国际/国家标准菌种保藏中心ATCC标准菌株,菌株的选择参考卫生行业标准WS/T232-2002《商业性微生物培养基质量检验规程》。3.2 定量测试方法改良Miles-Misra法测试菌株过夜培养物10倍递增稀释;测试平板和参照平板划分为4个区域并标记;从最高稀释度开始,分别滴一滴稀释液于试验平板和对照平板标记好的区域;将稀释液涂满整个1/4区域,37℃培养18小时;对易计数的区域计数,按公式计算生长率(生长率=待测培养基平板上得到的菌落总数/参考培养基平板上获得的菌落总数)。非选择性培养基上目标菌的生长率应不低于0.7,该类培养基应易于目标菌生长;选择性培养基上目标菌的生长率应不低于0.1。3.3 半定量测试方法 改进的划线法接种法平板分ABCD四区,共划16条线,平行线大概相隔0.5cm,每条有菌落生长的划线记作1分,每个仅一半的线有菌落生长记作0.5分,没有菌落生长或生长量少于划线的一半记作0分,分数加起来得到生长指数G。目标菌在培养基上应呈现典型的生长,而非目标菌的生长应部分或完全被抑制, 目标菌的生长指数G大于6时,培养基可接受。3.4 定性测试方法平板接种观察法用接种环取测试菌培养物,在测试培养基表面划平行直线。按标准中规定的培养时间和温度对接种后的平板进行培养, 目标菌应呈现良好生长,并有典型的菌落外观、大小和形态,非目标菌应是微弱生长或无生长。
检查药品时发现其中有一瓶培养基竟然结块了捣了半天都没散开想咨询下各位所用的干粉培养基平时是怎么存放的
01糖发酵管:包括蔗糖发酵管,乳糖发酵管,水杨苷发酵管等等02 ONPG培养基:现常配制成现成的生化管03西蒙氏柠檬酸盐培养基 04缓冲葡萄糖蛋白胨水(MR和VP试验用) 05克氏柠檬酸盐培养基 06丙二酸钠培养基 07葡葡糖铵培养基 08 Hugh-Leifson培养基(O/F试验用) 09 马尿酸钠培养基 10营养明胶 11苯丙氨酸培养基 12 氨基酸脱羧酶试验培养基 13蛋白胨水(靛基质试验用) 14 硫酸亚铁琼脂(硫化氢试验用) 15 尿素琼脂 16 氰化钾(KCN)培养基 17 氧化酶试验 18 硝酸盐培养基 19 细胞色素氧化酶试验 20 过氧化氢酶试验 21 过氧化物酶试验 22 磷酸盐缓冲液 23明胶磷酸盐缓冲液 24 乳酸-苯酚溶液 25 肉浸液肉汤 26肉浸液琼脂 27牛肉(或牛心)消化汤 28血消化汤 29豆粉琼脂 30血琼脂 31营养琼脂 32营养肉汤 33 乳糖胆盐发酵管 34乳糖发酵管 35 EC肉汤 36 缓冲蛋白胨水(BP) 37 氯化镁孔雀绿增菌液(MM) 38 四硫磺酸钠煌绿增菌液(TTB) 39 四硫磺酸钠煌绿增菌液(换用方法) 40 亚硒酸盐胱氨酸增菌液(SC) 41 GN增菌液 42 肠道菌增菌肉汤 43 亚硫酸铋琼脂(BS) 44 DHL琼脂 45 HE琼脂 46 SS琼脂 47 WS琼脂 48 麦康凯琼脂 49 伊红美蓝琼脂(EMB) 50三糖铁琼脂(TSI) 51 三糖铁琼脂(换用方法) 52 克氏双糖铁琼脂(KI) 53 克氏双糖铁琼脂(换用方法) 54 葡萄糖半固体发酵管 55 5%乳糖发酵管 56 CAYE培养基 57 Honda氏产毒肉汤 58 Elek氏培养基(毒素测定用) 59 氯化镁孔雀绿羧苄青霉素培养基 60 胰蛋白胨水 61 Rustigian氏尿素培养液 62 氯化钠结晶紫增菌液 63 氯化钠蔗糖琼脂 64 嗜盐菌选择性琼脂 65 3.5%氯化钠三糖铁琼脂 66 氯化钠血琼脂 67 3.5%氯化钠生化试验培养基 68 改良磷酸盐缓冲液(小肠结肠炎耶尔森氏菌专用) 69 CIN-1培养基 70 嗜盐性试验培养基
01糖发酵管:包括蔗糖发酵管,乳糖发酵管,水杨苷发酵管等等02 ONPG培养基:现常配制成现成的生化管03西蒙氏柠檬酸盐培养基 04缓冲葡萄糖蛋白胨水(MR和VP试验用) 05克氏柠檬酸盐培养基 06丙二酸钠培养基 07葡葡糖铵培养基 08 Hugh-Leifson培养基(O/F试验用) 09 马尿酸钠培养基 10营养明胶 11苯丙氨酸培养基 12 氨基酸脱羧酶试验培养基 13蛋白胨水(靛基质试验用) 14 硫酸亚铁琼脂(硫化氢试验用) 15 尿素琼脂 16 氰化钾(KCN)培养基 17 氧化酶试验 18 硝酸盐培养基 19 细胞色素氧化酶试验 20 过氧化氢酶试验 21 过氧化物酶试验 22 磷酸盐缓冲液 23明胶磷酸盐缓冲液 24 乳酸-苯酚溶液 25 肉浸液肉汤 26肉浸液琼脂 27牛肉(或牛心)消化汤 28血消化汤 29豆粉琼脂 30血琼脂 31营养琼脂 32营养肉汤 33 乳糖胆盐发酵管 34乳糖发酵管 35 EC肉汤 36 缓冲蛋白胨水(BP) 37 氯化镁孔雀绿增菌液(MM) 38 四硫磺酸钠煌绿增菌液(TTB) 39 四硫磺酸钠煌绿增菌液(换用方法) 40 亚硒酸盐胱氨酸增菌液(SC) 41 GN增菌液 42 肠道菌增菌肉汤 43 亚硫酸铋琼脂(BS) 44 DHL琼脂 45 HE琼脂 46 SS琼脂 47 WS琼脂 48 麦康凯琼脂 49 伊红美蓝琼脂(EMB) 50三糖铁琼脂(TSI) 51 三糖铁琼脂(换用方法) 52 克氏双糖铁琼脂(KI) 53 克氏双糖铁琼脂(换用方法) 54 葡萄糖半固体发酵管 55 5%乳糖发酵管 56 CAYE培养基 57 Honda氏产毒肉汤 58 Elek氏培养基(毒素测定用) 59 氯化镁孔雀绿羧苄青霉素培养基 60 胰蛋白胨水 61 Rustigian氏尿素培养液 62 氯化钠结晶紫增菌液 63 氯化钠蔗糖琼脂 64 嗜盐菌选择性琼脂 65 3.5%氯化钠三糖铁琼脂 66 氯化钠血琼脂 67 3.5%氯化钠生化试验培养基 68 改良磷酸盐缓冲液(小肠结肠炎耶尔森氏菌专用) 69 CIN-1培养基 70 嗜盐性试验培养基
请教一个小白问题:实验需要半固体培养基,能否在直接购买来干粉培养基(肉汤培养基)中添加一定量的琼脂?琼脂的加入会改变培养基的Ph值吗?
中国药典现在的方法是每批次的成品培养基做一次灵敏度复核就行。那么EP和USP的现行版本是否也是这样,我们现在同一批号的成品培养基每次新配都做,太麻烦了。还有,灭好菌装在密闭瓶子的培养基保质期为半年是否符合USP
整天都在和培养基打交道,大家有注意到培养基对人体的危害吗?
真菌培养基培养基真菌培养基的成分有碳源、氮源和其他营养物质。葡萄糖提供碳源,硝酸盐、亚硝酸盐、氨、尿素、氨基酸和其他化合物提供氮源。1.普通培养基(1)改良沙氏琼脂、多选择沙氏琼脂(Sabouraud dextrose agar , SDA): 含有放线菌酮和氯霉素,放线菌酮可抑制腐生性真菌(多数可能为条件致病菌),氯霉素可抑制大多数细菌(并非所有细菌) 。放线菌酮也抑制新型隐球菌、一些念珠菌、烟曲霉等。(2) 马铃薯葡萄糖培养基(potato dextrose agar , PDA) : 天然培养基。(3)脑心浸膏琼脂 临床常用脑心浸膏琼脂(brain-heart infusion agar , BHI) 分离深部真菌、双相真菌如皮炎芽生菌等,也可以在其中加入抗生素和血液制品。(4) 抑制性霉菌琼脂(inhibitory mold agar , IMA ) : 含有氯毒素,可抑制细菌的生长,是用于临床真菌培养标本初次增菌的理想培养基,常用于筛选放线菌酣敏感的真菌,如隐球菌、组织胞浆菌和接合菌等。2. 选择培养基(1)咖啡酸琼脂(CAA) : 用于鉴定新型隐球菌。由于该菌含有靛酚氧化酶,在CAA 培养基中菌落呈黑色。CAA 培养基对光敏感,应避光保存。(2) 鸟食琼脂(BA) : 用于从痰等标本中分离新型隐球菌。新型隐球菌在培养基上产生棕黑色色素,但是其他隐球菌在延长培养时也可产生色素。其他真菌也可在此培养基上生长,但不产生色素。(3) KT 培养基:由吐温、蛋白、烟酸和0.3 %水解酪蛋白氨基酸组成,用于皮炎芽生菌转相(为酵母相)培养时使用。(4) Kelley 琼脂:用于皮炎芽生菌( B. dermatitidis) 转相(为酵母相)时使用。(5) CHROM 琼脂: 念珠菌显色培养基。是一种用于鉴定培养念珠菌的培养基,不同念珠菌在此培养基上生长显不同颜色。
最近要购买培养基,有一种遇到一点问题,和大家讨论一下。2010版药典中新增试剂大豆酪蛋白琼脂培养基(TSA),和对方沟通时却说TSA代表的是胰酪胨大豆琼脂培养基,搞晕了不知道是不是同一种培养基。同一种培养基往往有好几种名字,不同的药典名称不一样吧,现在就比较头大这个请大家帮我分析一下!药典中这样写的:大豆酪蛋白琼脂培养基(TSA)配方:酪蛋白胰酵消化物 15g大豆粉木瓜蛋白酶消化物 5g氯化钠 5g琼脂 5g纯化水 1000mlPH值 7.3±0.2我查到的胰酪胨大豆琼脂培养基(TSA)配方:胰酪蛋白胨 15g/l大豆蛋白胨 5g/l氯化钠 5g/l琼脂 5g/lPH 7.3 ±0.2综合以上请各位帮我分析一下是不是一种培养基?
条件有限的情况下,怎么让能让培养基快递凝固,我每次做实验培养基至少要半个小时才能凝固,有些样品需要再覆盖一层培养基至少一个小时
微生物常用培养基中英文对照一、显色培养基:大肠杆菌显色培养基 E.Coli Chromogenic Medium大肠菌群显色培养基 Coliform Chromogenic Medium大肠杆菌/大肠菌群显色培养基 E.Coli/Coliform Chromogenic Medium细菌总数显色培养基 Total Genes Chromogenic MediumO157显色培养基 O157 Chromogenic Medium沙门氏菌显色培养基 Salmonella Chromogenic Medium李氏菌显色培养基 Listera Chromogenic Medium金黄色葡萄球显色培养基Staphylococcus Chromogenic Medium霉菌和酵母菌显色培养基 Mould and Yeast Chromogenic Medium弧菌显色培养基Vibrio Chromogenic Medium坂崎杆菌显色培养基Enterobacter sakazakii Chromogenic Medium二、常用检测培养基:平板计数琼脂(PCA) Plate Count Agar月桂基硫酸盐胰蛋白胨肉汤(LST) Lauryl Sulfate Tryptose Broth煌绿乳糖胆盐肉汤(BGLB) Brilliant Green Lactose Bile BrothEC 肉汤 E.Coli Broth伊红美蓝琼脂 (EMB) Eosin-Methylene Blue Agar营养肉汤 (NB) Nutrient Broth营养琼脂 (NA) Nutrient Agar乳糖胆盐发酵培养基 Lactose Bile Broth乳糖发酵培养基 Lactose Broth结晶紫中性红胆盐琼脂 (VRBA) Violet Red Bile Agar去氧胆酸盐琼脂 Desoxycholate Lactose Agar肠道菌计数琼脂 (VRBDA) Violet Red Bile Dextrose Agar肠道菌增菌肉汤(EE) Enterobacteria Enrichment Broth7.5%氯化钠肉汤 7.5% Sodium Chloride BrothBaird-Parker琼脂基础 Baird-Parker Agar Base胰蛋白胨大豆肉汤(TSB) Trypticase (Tryptic) Soy Broth胰蛋白胨大豆琼脂(TSA) Tryptose Soya Agar胰月示-亚硫酸盐-环丝氨酸琼脂基础 (TSC) Tryptose Sulfite Cycloserine Agar Base甘露醇卵黄多粘菌素琼脂基础(MYP)Mannitol-Egg-Yolk-Polymyxin Agar Base亚碲酸盐卵黄增菌液 Egg-Yolk Tellurite Emulsion缓冲蛋白胨水(BPW) Buffered Peptone Water亚硒酸盐胱氨酸增菌液(SC) Selenite Cystine Broth四硫磺酸盐煌绿增菌液基础(TTB) Tetrathionate Broth Base胆硫乳琼脂(DHL) Deoxycholate Hydrogen Sulfide Lactose AgarSS 琼脂 Salmonella Shigella Agar亚硫酸铋琼脂(BS) Bismuth Sulfite Agar亚利桑那菌琼脂(SA) Salmonella Arizona AgarHE 琼脂(HE) Hekton Enteric Agar三糖铁琼脂(TSI) Triple Sugar Iron Agar马铃薯葡萄糖琼脂 (PDA) Potato Dextrose Agar高盐察氏琼脂 Salt Czapek Dox Agar沙氏琼脂培养基 Sabouraud’s Agar孟加拉红培养基 Rose Bengal MediumYPD琼脂Yeast Peptone Dextrose Agar胰酪胨大豆多粘菌素肉汤基础Trypticase-Soy-Polymyxin Broth Base酪蛋白琼脂Casein Agar产芽孢肉汤Sporulation Broth溴甲酚紫葡萄糖蛋白胨水培养基 Glucase Peptone Water Medium李氏菌增菌肉汤(LB1,LB2)基础Listeria Enrichment Broth Base半固体动力培养基Motility Test三、培养基基础:胰蛋白胨Tryptone酪蛋白胨Peptone from Casein植物(大豆)蛋白胨Peptone from soy月示胨Proteose peptone多价蛋白胨Polypeptone特殊蛋白胨Peptone Special牛心浸粉Beef Heart Infusion肝浸粉Liver Infusion牛肉浸粉Beef Extract Powder酵母浸粉Yeast Extract Powder酸水解酪蛋白Casein acid Hydrolysate细菌琼脂粉Bacterial Agar牛胆盐Bile Salt
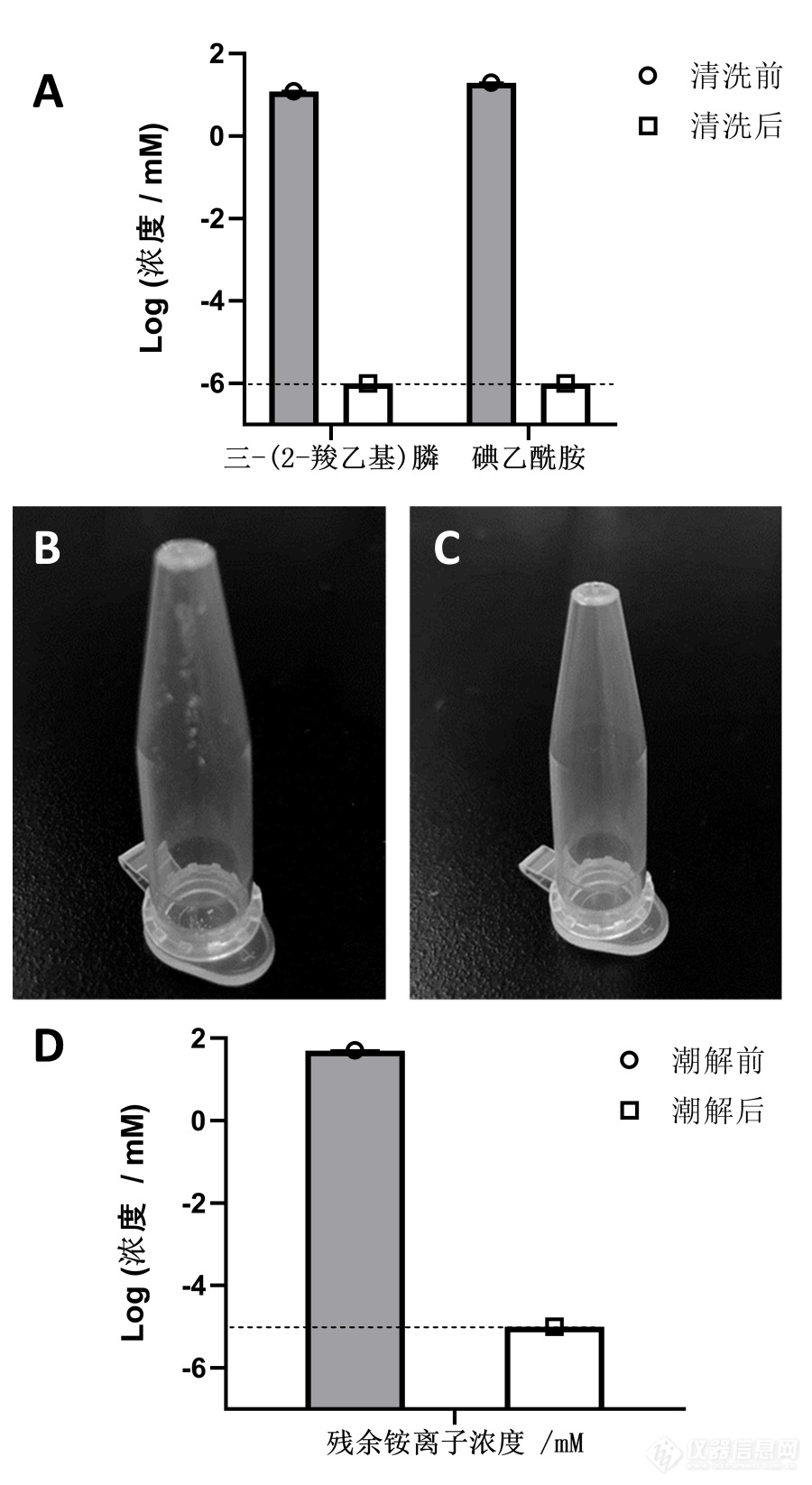
[align=center]双歧杆菌高密度培养的补料培养基及补料方法[/align][align=center]季学猛[/align][align=center](南开大学 医学院, 天津 300071)[/align]摘 要:双歧杆菌在维护宿主健康方面具有重要作用,因此对其高密度培养条件的探索具有重要意义。目前,双歧杆菌的高密度培养主要受到培养基组分和培养条件的优化的影响。这里报道了一种用于双歧杆菌高密度培养的补料培养基及补料方法。该方法使用补料与碱泵耦合的方法进行补料,通过控制发酵培养基的pH值来调节补料培养基的补入量。此外,本研究还进行了补料培养基的优化实验,通过调整氢氧化钠和葡萄糖浓度的比例,比较了不同补料培养基的发酵性能。实验结果表明该补料培养基及补料方法适用于两歧双歧杆菌、青春双歧杆菌、动物双歧杆菌、长双歧杆菌等多种双歧杆菌,而且能够达到较高的活菌密度。本研究提出的补料培养基及补料方法可为双歧杆菌的高密度培养提供有效的解决方案。关键词:双歧杆菌;高密度培养;补料培养基;补料方法;碱泵耦合中图分类号:G482[color=gray] [/color]文献标识码:A[align=center]A supplementary culture medium and supplementation method for high-density cultivation of Bifidobacterium[/align]JI Xuemeng(School of Medicine, Nankai University, Tianjin 300071, China)Abstract: Bifidobacterium plays a significant role in maintaining host health, making the exploration of high-density cultivation conditions crucial. Currently, the high-density cultivation of Bifidobacterium is mainly influenced by the optimization of culture medium components and cultivation conditions. Here, we report a supplementary culture medium and supplementation method for high-density cultivation of Bifidobacterium. The method utilizes coupling of supplementation with an alkaline pump to control the supplementation rate of the culture medium by adjusting its pH value. Furthermore, optimization experiments of the supplementation culture medium were conducted by varying the ratio of sodium hydroxide to glucose concentrations, comparing the fermentation performance of different supplementation culture media. Experimental results demonstrate that this supplementation culture medium and supplementation method are applicable to various Bifidobacterium strains such as Bifidobacterium bifidum, Bifidobacterium adolescentis, Bifidobacterium animalis, and Bifidobacterium longum, achieving high viable cell densities. The proposed supplementation culture medium and supplementation method in this study offer an effective solution for high-density cultivation of Bifidobacterium.Key words: Bifidobacterium high-density cultivation supplementary culture medium supplementation method alkaline pump coupling双歧杆菌广泛分布于动物和人类的肠道中,已经发现双歧杆菌在维护宿主健康方面起着极其重要的作用,双歧杆菌作为益生菌的功能特性已经引起了越来越多的关注[sup][back=yellow][1-3][/back][/sup]。双歧杆菌的益生菌制剂有潜力通过选择和加强有益菌群来调节肠道微生物群的组成和微生物平衡,从而更有利于人体健康。双歧杆菌制剂已被报道能改善肥胖相关特征、缓解便秘和增强免疫力[sup][back=yellow][4-6][/back][/sup]。双歧杆菌已经成为国内外正在快速发展的微生态制剂中的主要菌种之一。努力探索双歧杆菌的高密度生长条件,对于提高该菌的生产效率和应用推广具有重要意义。双歧杆菌的高密度培养条件的摸索主要涉及培养基组分和培养条件的优化。目前,MRS培养基是最常用的双歧杆菌等乳酸菌培养基,被广泛地用于双歧杆菌的发酵中[sup][back=yellow][7][/back][/sup]。双歧杆菌的最适生长 pH 值在 6.0-7.0 之间[sup][back=yellow][8][/back][/sup],然而,由于双歧杆菌发酵过程中会产生有机酸等代谢副产物,导致培养过程中培养基的 pH 值不断地降低,限制细菌的生长[sup][back=yellow][9-11][/back][/sup]。为解除酸等代谢副产物对双歧杆菌生长的限制,一些创新型的发酵培养方法已经被提出,比如细胞周期培养、透析培养、细胞固定培养和嵌入法[sup][back=yellow][12-15][/back][/sup]。然而,这些方法在工业应用中受到了各种因素的限制。目前,分批的发酵罐内恒定pH培养方法仍然是主流,在发酵中通过添加碱性溶液来控制培养基的pH值,以减轻酸性生长抑制。在解除酸性生长抑制后,双歧杆菌的生长还受到渗透压和底物不足的限制[sup][back=yellow][16][/back][/sup]。许多营养物在高浓度下导致的高渗透压对细胞有抑制作用,而为了达到高细胞密度,又必须供给大量的营养物质。因此,为了双歧杆菌培养中有效地利用底物,必须优化培养过程以解决底物浓度和渗透压之间的矛盾。将浓缩营养物以与其消耗速率成比例地加入反应器中是一种有效的解决底物浓度和渗透压之间的矛盾的方法,为此产生了多种形式的补料喂养模型:间歇喂养,恒定喂养和指数喂养[sup][back=yellow][17-19][/back][/sup]。在间歇补料喂养中,通过周期性检查并补充生长基质中的葡萄糖含量达到稳定葡萄糖浓度的目的,然而,这种补料模型决定了必然需要大量人力。而且在对数生长阶段,细菌细胞快速消耗葡萄糖,因此在任何两个测量间隔期间可能发生底物缺乏,可能会导致补料不及时,进而影响细菌的生长。在恒定补料喂养中,饲料介质以恒定的流速持续添加到发酵培养基中。这种方法优点是减少了人力需求。但是,益生菌对葡萄糖的消耗速率不是恒定的,这就导致了低喂养速率可能导致细菌生长的底物不足,而高喂养速率会引起过量底物积累,也会抑制细菌生长。对于指数喂养模型,在益生菌前期生长阶段,指数喂养能够很好的耦合细菌对数生长。然而,在细菌对数生长后期,细菌生长速率趋缓,而流加速率继续指数增加会导致底物浓度迅速增加,进而对细菌菌株的生长能力造成不良影响。因此,指数喂养模型也不是合理的方法。综上所述,在益生菌菌株生长期间,这些方法均不能准确控制生长介质中的葡萄糖含量。目前,针对双歧杆菌等厌氧菌发酵过程中产酸,而且产酸与消耗的碳源成正比的特性[sup][back=yellow][20][/back][/sup],通过将补料与碱泵偶联,可实现了补碱的同时补加碳源。然而,补料与碱泵偶联对于发酵罐技术要求高,该技术仍没有在实验室和工厂中得到广泛推广。1? 补料系统的设计为克服现有技术中的缺陷,这里提出了一种用于双歧杆菌高密度培养的补料培养基及补料方法,技术方案如下:一种用于双歧杆菌高密度培养的补料培养基,该补料培养基包括质量比为1:10的氢氧化钠与葡萄糖。其中氢氧化钠浓度小于等于50 g/L,葡萄糖浓度小于等于500g/L。可减少补料培养基中氢氧化钠、葡萄糖和溶氧氧化还原反应产生的副产物浓度。为了减少补料培养基中氢氧化钠、葡萄糖和溶氧的氧化还原反应,配制补料培养基的水应尽可能减少溶氧。可通过高温灭菌、煮沸、通氮气或通二氧化碳的方法减少溶氧。氢氧化钠和葡萄糖溶液应分别进行灭菌后进行混合。使用所述的补料培养基的补料方法,需将补料培养基通过碱泵与发酵培养基连接,根据所述的发酵培养基的pH值控制所述的补料培养基的补入量即成。碱泵的流速为5-10mL/min;碱泵的每次开启时间小于等于30s;发酵培养基的pH值的检测周期为20s。补料培养基补入后发酵培养基的pH值与补入前发酵培养基的pH值之差小于等于0.1。用于双歧杆菌高密度培养的发酵的方法包括如下步骤:(1)将双歧杆菌种子液接种至发酵培养基中进行发酵;(2)将补料培养基通过碱泵与发酵培养基连接,根据所述的发酵培养基的pH值控制所述的补料培养基的补入量;(3)在发酵过程中,间隔1小时对发酵培养基取样,检测580nm-620nm下的吸光度值,并检测葡萄糖浓度与活菌数目,当吸光度值大于0.5且相邻2次取样的吸光度值相等或降低即为发酵结束。2? 补料培养基的优化制备如下5种补料培养基,其中氢氧化钠浓度(g/L)和葡萄糖浓度(g/L)比值分别为1:2、1:5、1:10、1:20、1:40,以比较发酵性能。发酵培养基组成如下:1000mL蒸馏水、14.3g大豆蛋白胨、16.7g酵母粉,10g葡萄糖,0.5g可溶性淀粉,1g氯化钠,1g磷酸氢二钾,1g磷酸二氢钾,0.01g FeSO4?7H2O,0.005g MnSO4,0.2gMgSO4,0.5g L-半胱氨酸,使用50g/L的氢氧化钠溶液调节pH至6.8;其中L-半胱氨酸配制为50g/L浓度,膜过滤除菌,在发酵培养基灭菌结束后再按照1/100(v/v)加入L-半胱氨酸。发酵罐通气孔中接入氮气,使得溶氧降至1mg/L以下;设置发酵参数:发酵温度设为37.0℃范围内,搅拌转速200r/min,培养基温度达到37.0℃后,在火焰圈的无菌环境下按照5%(v/v)的接种量加入种子液,同时,加入3滴消泡剂;开启发酵罐搅拌器,设置种子液加入后的培养基的当前pH值6.6为发酵设定pH值。补料设置参数:将补料培养基中碱泵利用软管连接,设置碱泵最大流速为10mL/min,设置碱液根据pH自动控制加入,设置碱泵启动参数为pH值小于6.55,设置每隔10秒测定一次pH值,设置每次碱泵开启时间15秒;发酵中,每隔3小时测OD,每隔5小时取样监测培养液葡萄糖浓度,检测到15小时。如[back=yellow]图1[/back]所示,发现在发酵前5小时,各补料培养基都可以维持葡萄糖浓度处于适宜双歧杆菌快速生长的浓度(灰色范围),而从发酵10小时开始,氢氧化钠浓度(g/L)和葡萄糖浓度(g/L)比值为1:2的补料出现了葡萄糖浓度的下降,说明该碱碳比例在发酵后期不足以满足双歧杆菌开始生长对碳源的需求。同样的,从发酵10小时开始,氢氧化钠浓度(g/L)和葡萄糖浓度(g/L)比值为1:40的补料出现了葡萄糖浓度的过高,说明该碱碳比例在发酵后期不足可能产生高渗透压,不适合双歧杆菌的生长。而氢氧化钠浓度(g/L)和葡萄糖浓度(g/L)比值1:5至1:20补料可以维持发酵过程中葡萄糖浓度的稳定。综合下来,我们发现了补料培养基中氢氧化钠浓度(C碱,g/L)和葡萄糖浓度(C料,g/L)的合适比值为1:5至1:20。[align=center][back=yellow]图1[/back] 不同配比的补料培养对发酵体系葡萄糖浓度的影响的柱状图[/align]3? 补料系统的应用实践3.1? 两歧双歧杆菌高密度培养如[back=yellow]图2[/back]所示,使用本方法,发酵体系中pH值始终保持在6.6±0.1,葡萄糖浓度始终维持在9-13g/L,发酵结束时,发酵液总体积达到4.9L,吸光度达到OD620 12.8,活菌密度最高达到 8.5±0.2 ×10[sup]9[/sup] cfu/mL。[back=yellow]图2[/back] 两歧双歧杆菌的高密度培养的曲线图3.2? 长双歧杆菌高密度培养如[back=yellow]图3[/back]所示,使用本方法,发酵体系中pH值始终保持在6.9±0.1,葡萄糖浓度始终维持在8.5-13g/L,发酵结束时,发酵液总体积达到4.4L,吸光度达到OD[sub]620[/sub] 9.2,活菌密度最高达到 6.4±0.2 ×10[sup]9[/sup] cfu/mL。[back=yellow]图3[/back] 长双歧杆菌的高密度培养的曲线图3.3? 青春双歧杆菌高密度培养如[back=yellow]图4[/back]所示,使用本方法,发酵体系中pH值始终保持在6.7±0.1,葡萄糖浓度始终维持在7-11g/L,发酵结束时,发酵液总体积达到4.6L,吸光度达到OD[sub]620[/sub] 15.3,活菌密度最高达到 1.2±0.1 ×10[sup]10[/sup] cfu/mL。[back=yellow]图4[/back] 青春双歧杆菌的高密度培养的曲线图3.4? 动物双歧杆菌的高密度培养如[back=yellow]图5[/back]所示,使用本方法,发酵体系中pH值始终保持在6.5±0.1,葡萄糖浓度始终维持在7-12g/L,发酵结束时,发酵液总体积达到4.2L,吸光度达到OD[sub]620[/sub] 20.5,活菌密度最高达到 1.7±0.1 ×10[sup]10[/sup] cfu/mL。[back=yellow]图5[/back] 动物双歧杆菌的高密度培养的曲线图4? 结语该研究提供了一种用于双歧杆菌高密度培养的补料培养基及补料方法,补料方法包括如下步骤:将补料培养基通过碱泵与发酵培养基连接,根据发酵培养基的pH值控制补料培养基的补入量即成。通过优化补料培养基及补料方法,无需发酵罐补料偶联技术便实现了根据pH值变化,利用碱泵自动补充碳源和碱液,实现了保持pH值和碳源浓度的稳定;该补料方法对发酵罐的设备技术要求低,操作简单,降低了发酵成本。参考文献(References):[1]杨硕,唐宗馨,段勃帆,陈禹含,郭欢新,孟祥晨.双歧杆菌及其制剂对炎症性肠病作用机制研究进展[J].食品科学,2023,44(05):275-281.[2]马岩,王中江,杨靖瑜,李哲,彭霞,单秀峰,李柏良,马微微.动物双歧杆菌乳亚种XLTG11对克林霉素诱导的抗生素相关性腹泻的改善作用[J].食品科学,2023,44(03):170-178.[3]李虔全,罗京,周江,刘亭,陈于彪,彭霞,杨建,胡闵山.孟鲁司特钠联合双歧杆菌四联活菌治疗儿童过敏性紫癜有效性Meta分析[J].海峡药学,2023,35(01):127-133.[4]石英,拉巴普尺,张丹瑛,翁书强,刘心怡,汪皓琪.双歧杆菌对高脂饮食诱导的C57BL/6小鼠非酒精性脂肪肝的影响[J].中国临床医学,2022,29(03):473-480.[5]陆敏,袁琳,胡娜,钟霄毓,姜逸,林敏,陆雄.双歧杆菌三联活菌对肥胖小鼠慢性低度炎症的影响[J].卫生研究,2022,51(05):797-802.DOI:10.19813/j.cnki.weishengyanjiu.2022.05.020.[6]李亦汉,王琳琳,赵建新,张灏,王刚,陈卫.两歧双歧杆菌CCFM1167通过提升肠道中乙酸水平以抑制炎症从而缓解便秘[J].食品与发酵工业,2023,49(06):35-41.DOI:10.13995/j.cnki.11-1802/ts.031238.[7]Umar Farooq. 小米膳食纤维作为主要碳源对益生菌生长和发酵过程中短链脂肪酸产量的影响研究[D].江南大学,2013.[8]杨玲,张栋,齐世华,马新颖,周帅康,艾连中,王世杰.两歧双歧杆菌TMC3115冻干菌粉生产工艺优化[J].乳业科学与技术,2021,44(05):12-17.DOI:10.15922/j.cnki.jdst.2021.05.003.[9]熊三玉. 两歧双歧杆菌驯化及培养条件优化的研究[D].中国海洋大学,2007.[10]冯诗诗. 长双歧杆菌F16的益生特性及其在酸浆豆腐制备中的应用[D].河南工业大学,2022.DOI:10.27791/d.cnki.ghegy.2022.000088.[11]武婷,郭帅,杨阳等. 动物双歧杆菌乳亚种Probio-M8在发酵山羊乳中的应用[C]//中国食品科学技术学会.第十七届益生菌与健康国际研讨会摘要集.[出版者不详],2022:149-150.DOI:10.26914/c.cnkihy.2022.018592.[12]赵春燕,张颖,王丹,刘臻.乳酸菌细胞固定化发酵的研究进展[J].中国酿造,2009(05):11-14.[13]李秀凉,雷虹,张龙丰,周东坡,平文祥.从L-乳酸菌酸菜发酵液中初步分离肽类抑菌物质[J].食品工业科技,2008(07):91-93.DOI:10.13386/j.issn1002-0306.2008.07.022.[14]邓鹏超. 乳酸菌的高密度培养及酸奶冻干发酵剂的研究[D].华中农业大学,2008.[15]于修鑑. 乳酸菌高密度培养及浓缩型发酵剂研究[D].南京工业大学,2004.[16]黄晓英. 传统发酵食品中具有抑菌特性乳酸菌的筛选、抑菌机理及其在泡菜发酵中的应用[D].西南民族大学,2022.DOI:10.27417/d.cnki.gxnmc.2022.000050.[17]彭海芬. 阿维拉霉素高产菌株的选育及其发酵条件优化[D].河南工业大学,2022.DOI:10.27791/d.cnki.ghegy.2022.000511.[18]吴斌.罗非鱼无乳链球菌SIP-pET32a基因工程菌高密度发酵工艺及SIP蛋白提取方及SIP蛋白提取方法研究[J].中国水产,2022(11):73-78.[19]熊华仪,陈曦,刘月锋,陈雄,李沛,王志.补料策略优化促进乳球菌HB03发酵合成Nisin[J/OL].食品科学:1-11[2023-05-18].http://kns.cnki.net/kcms/detail/11.2206.ts.20230428.1620.026.html[20]孙东霞,周子安,冯志合,胡修玉,祁光霞,董黎明.pH值调控柠檬酸污泥厌氧发酵产酸及碳源潜力研究[J].中国环境科学,2022,42(11):5198-5207.DOI:10.19674/j.cnki.issn1000-6923.20220620.001.收稿日期:2023-10-19 修改日期:第一作者简历:季学猛,硕士,实验师,研究方向为生物化工、机器学习;生物信息学。E-mail:jixuemeng@nankai.edu.cn。