
黄连上清片高温灭菌后,黄连对照药材薄层鉴别的点变红是怎么回事?[img=,690,388]https://ng1.17img.cn/bbsfiles/images/2019/07/201907101138123673_5943_1782490_3.jpg!w690x388.jpg[/img]
石柱黄连指纹图谱研究 黄小平,李隆云,瞿显有,崔广林(重庆市中药研究院,重庆400065)摘要目的:建立石柱道地药材黄连的HPLC指纹图谱,为科学评价与有效控制黄连质量提供新方法。方法:RP—HPLC法测定石柱GAP基地10批黄连样品。色谱条件:迪马Diamonsil C18。色谱柱,乙腈一0.05 molfL磷酸二氢钾(磷酸调pH值3)为流动相进行梯度洗脱,检测波长270 am,流速0.8 ml/min,柱温25。C。结果:10批黄连样品得到的指纹图谱有16个共有峰,通过与对照品的保留时间及紫外光谱比较,11,12,13,14,15号峰分别为伪小檗碱、药根碱、黄连碱、巴马汀和小檗碱。结论:建立的HPLC指纹图谱分析法能较好反映黄连中的主要生物碱成分,可用于黄连的质量控制。关键词 黄连;高效液相色谱法;指纹图谱PS:该文献也没有谱图
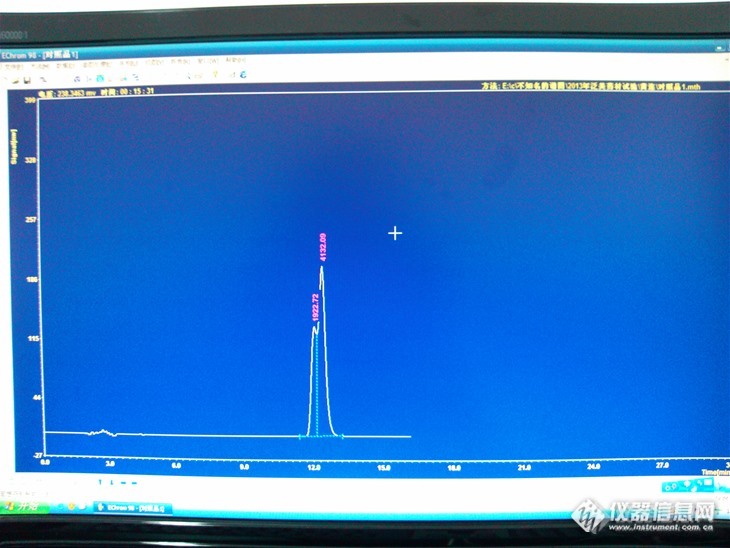
大家好,最近做了黄连的色谱图,配制的 盐酸小檗碱的对照品,做的头三个对照品竟然是这样的图,,这可是一个成分啊,后来又打了几针又变成一个峰,峰型也很好了,但是药材的小檗碱的峰 也不好,这是怎么回事呢,是什么原因啊,大家帮我分析下啊,有做过的吗?在流动相配制方面或者别的方面有需要特别注意的吗?谢谢啦http://ng1.17img.cn/bbsfiles/images/2013/08/201308042203_455996_2732277_3.jpg
黄连味苦性寒,具有清热燥湿、泻火解毒的功效。《中国药典》2020年版规定黄连为毛茛科黄连属植物黄连Coptis chinensis Franch.、三角叶黄连C. deltoidea C. Y. Cheng et Hsiao或云连C. teeta Wall.的干燥根茎。以上3种分别习称“味连”“雅连”“云连”,经课题组前期调研以味连产量最多,主产于我国重庆、湖北、四川等地[1]。现代研究表明,黄连含有多种活性成分,可发挥多种药理作用[2],包括抗炎、抗病毒、抗菌、抗癌、镇痛、抗抑郁、降血糖等作用,临床应用极广[3]。苦参性寒、味苦,为豆科苦参属植物苦参Sophora flavescens Ait.的干燥根,主产于我国内蒙古、河南、山东、安徽等地[1],具有抗菌、抗肿瘤、镇痛、抗炎、防治心力衰竭、心律失常及心肌缺血等多种功效[4-5]。 现代研究表明,生物碱类化合物是黄连及苦参的主要活性成分。苦参碱、氧化苦参碱可发挥抗炎、镇痛效果[6-7],其机制可能与降低促炎因子,升高抗炎因子有关;氧化苦参碱、苦参碱也可发挥抗肿瘤作用,其机制可能与抑制癌症基因表达,促进肿瘤细胞凋亡,抑制肿瘤细胞生长有关[8];而苦参碱、氧化苦参碱、槐定碱也可对多种菌株具有一定的抑菌作用[9]。木兰花碱可通过活性氧(reactive oxygen species,ROS)/鼠类肉瘤病毒癌基因(Kirsten rat sarcoma viral oncogene,KRAS)/单磷酸腺苷活化蛋白激酶(adenosine monophosphate activated protein kinase,AMPK)通路抑制结直肠癌SW480细胞的增殖和有氧糖酵解,从而发挥对结直肠癌的治疗效果[10];药根碱、巴马汀、表小檗碱、黄连碱、小檗碱可联合发挥降糖作用[11],其效果可能与调控丝氨酸-苏氨酸激酶1(serine/threonine kinase 1,LKB1)/ AMPK/CREB分子调节转录共激活剂2(CREB-regulated transcription coactivator 2,TORC2)信号通路抑制肝脏糖异生等有关[12];小檗碱具有抗炎作用,可保护螺旋神经节细胞免受巨细胞病毒诱导的凋亡作用,其机制与通过途径抑制线粒体活性氧的产生有关[13]。 除此之外,小檗碱、表小檗碱、巴马汀等生物碱类成分也可联合发挥抗心律失常作用[14]。基于此,选择苦参中苦参碱、槐定碱、氧化苦参碱及黄连中木兰花碱、非洲防己碱、药根碱、表小檗碱、黄连碱、巴马汀、小檗碱来作为黄连-苦参药对的代表性药效成分,用于研究该类成分溶出量与药对配比的关系。药对作为中药配伍的最小单元,是复方研究的重要组成部分之一[15]。用于不同疾病的治疗时,不同量的配比会有不同效果的相关呈现,因此,首先需要对黄连-苦参药对配比的不同物质基础,即量-质[16]相关性进行剖析比较,为进行量-效[17]相关性提供依据,为临床合理配比提供参考[18]。 1 仪器与试药 1.1 主要仪器 Waters e2695型高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]系统,Waters 2998型二极管阵列检测器(PDA),美国Waters公司;BBA224S-CW型电子天平,赛多利斯科学仪器(北京)有限公司;TGL-16C型离心机,上海安亭科学仪器厂;EPED-E2-20TS型超纯水一体机系统,南京易普易达科技发展有限公司;GM-0.5B型真空泵,天津市津腾实验设备有限公司;KH-500V型超声器,昆山禾创超声仪器有限公司。 1.2 药品及试剂 1.2.1 药材与饮片 本研究所选择黄连(产地重庆石柱黄水,批号20230411)及苦参(产地内蒙古赤峰市,批号2020121604)药材,均经南京中医药大学药学院刘圣金教授鉴定,分别为毛茛科黄连属植物黄连C. chinensis Franch.的干燥根茎和豆科苦参属植物苦参S. flavescens Ait.的干燥根。 1.2.2 对照品 表小檗碱(批号J24HB186173)、盐酸小檗碱(批号S01A10K94340)、盐酸黄连碱(批号T21S11C125202)、药根碱(批号D18GB171805)、盐酸巴马汀(批号Z16J10X79792)、非洲防己碱(批号W14J8Z37548)、木兰花碱(批号R21M9F61834)、苦参碱(批号M14GB141405)、氧化苦参碱(批号G14N11KL130769)、槐定碱(批号F18F7S9784),HPLC质量分数均≥98%,均购自上海源叶生物科技有限公司。 1.2.3 试剂 乙腈、甲醇,色谱纯,安徽天地高纯溶剂有限公司;磷酸、盐酸、无水乙醇,分析纯,国药集团化学试剂有限公司;纯净水,屈臣氏集团(香港)有限公司;磷酸二氢钾,分析纯,南京化学试剂股份有限公司。 2 方法与结果 2.1 不同配比黄连-苦参药对指纹图谱的建立 2.1.1 色谱条件 色谱柱为Venusil XBP C18(2)(250 mm×4.6 mm,5 μm);柱温30 ℃;体积流量0.8 mL/min;流动相为乙腈-3 g/L磷酸二氢钾溶液(加入200 μL磷酸调节pH值),梯度洗脱:0~10 min,10%乙腈;10~25 min,10%~24%乙腈;25~35 min,24%乙腈;35~60 min,24%~35%乙腈;60~62 min,35%~60%乙腈;62~65 min,60%~10%乙腈;65~70 min,10%乙腈;分析时间70 min,进样量10 μL;检测波长220 nm。 2.1.2 混合对照品溶液的制备 取非洲防己碱、药根碱、表小檗碱、盐酸小檗碱、盐酸巴马汀、盐酸黄连碱、木兰花碱、苦参碱、氧化苦参碱、槐定碱对照品各适量,分别置于10 mL量瓶中,加甲醇溶解并定容,即得各对照品储备液。分别取适量上述11种对照品储备液,置于同一10 mL量瓶中,加甲醇稀释并定容,制得上述成分质量浓度分别为0.20、0.16、0.24、0.25、0.25、0.44、0.26、0.21、0.80、0.36 mg/mL的混合对照品溶液。 2.1.3 供试品溶液的制备 制备黄连药材粉末(过二号筛)及苦参药材粉末(过三号筛),将上述黄连及苦参依照5∶1、4∶1、3∶1、2∶1、1∶1、1∶2、1∶3、1∶4、1∶5共9个质量比例,进行称取后分别充分混合,并称取单一黄连药材粉末及单一苦参药材粉末作为对照药材,各比例药对总质量及单一药材质量均为12 g。每个比例平行称取各药对3份,将药对以10倍量水浸泡0.5 h后,煎煮1.5 h,取1次滤液;将滤渣加入8倍量水煎煮1.5 h,取2次滤液。将2次滤液混合后抽滤,12 000 r/min离心(离心半径10.4 cm)10 min,取上清液,取1 mL上清液加入4 mL甲醇,以0.45 μm微孔滤膜滤过,即得供试品溶液。 2.1.4 精密度试验 依照黄连与苦参比例1∶3,精密称取黄连药材粉末3 g及苦参药材粉末9 g,按照“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样测定6次,考察特征峰的保留时间和峰面积一致性。以盐酸小檗碱的保留时间和峰面积为参照分别计算相对保留时间及相对峰面积。计算得各共有峰相对保留时间的RSD<0.20%,相对峰面积的RSD<2.13%,结果表明仪器精密度良好。 2.1.5 稳定性试验 依照黄连与苦参比例1∶3,精密称取黄连药材粉末3 g及苦参药材粉末9 g,按照“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件每隔4 h进样1次,共测定24 h,考察特征峰保留时间和峰面积的一致性。以盐酸小檗碱的保留时间和峰面积为参照分别计算相对保留时间及相对峰面积。计算得各共有峰相对保留时间的RSD<0.21%、相对峰面积的RSD<2.46%,结果表明该供试品溶液在室温放置24 h内稳定性良好。 2.1.6 重复性试验 依照黄连与苦参比例1∶3,精密称取黄连药材粉末3 g及苦参药材粉末9 g,平行制6份,按照“2.1.3”项下方法制备供试品溶液,分别按“2.1.1”项下色谱条件进样分析,考察特征峰保留时间和峰面积的一致性。以盐酸小檗碱的保留时间和峰面积为参照分别计算相对保留时间及相对峰面积。计算得各共有峰相对保留时间的RSD<0.18%、相对峰面积的RSD<1.57%,表明该方法重复性较好。 2.1.7 黄连-苦参药对指纹图谱的建立及相似度评价分析 将黄连及苦参药材依照“2.1.3”项下方法制备成供试品溶液(S1~S9依次为黄连-苦参比例为5∶1、4∶1、3∶1、2∶1、1∶1、1∶2、1∶3、1∶4、1∶5),再按“2.1.1”项下色谱条件进样分析,记录色谱图。将图谱输入《中药色谱指纹图谱相似度评价系统(2012版)》,设置编号S7的样品(黄连-苦参为1∶3)图谱为参照,采取中位数法[19],将时间窗宽度设置为0.1 s,进行多点校正,建立黄连-苦参药对的HPLC指纹图谱和对照指纹图谱(R,图1),指认9批黄连-苦参药对的16个共有峰。采用《中药色谱指纹图谱相似度评价系统(2012版)》对9批黄连-苦参药对进行相似度评价[20]。结果显示,9批黄连-苦参药对和R之间的相似度均大于0.95,这表明各批次黄连-苦参药对的相似性较好,整体质量稳定,可以用于考察黄连-苦参药对水煎液。以分离度较好、峰面积较大的小檗碱(峰16)为参照峰(S),得到9批黄连-苦参药对16个共有峰相对保留时间的RSD为0.175%~0.894%,提示各批次黄连-苦参药对共有峰的保留时间稳定 2.1.8 黄连-苦参药对指纹图谱色谱峰归属认定 通过比对单味药的色谱峰[21],不同比例配伍黄连-苦参药对HPLC指纹图谱16个共有峰中峰2~6号共5个峰均来源于单味药苦参,峰1、7~16号共11个峰来源于单味药黄连(图1)。通过对比混合对照品溶液色谱图(图2)及黄连、苦参及样品HPLC叠加图(图2)对各样品指纹图谱的各峰进行定性认证[22],得到2、3、6号峰分别为苦参碱、槐定碱、氧化苦参碱,属于单味药苦参;8、11~16号峰分别为木兰花碱、非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱,属于单味药黄连。 2.1.9 黄连-苦参药对各共有峰相对峰面积差异分析 将各比例药对中黄连-苦参药对生药量以黄连、苦参单煎样品的生药量为标准,换算成一致的量,并以黄连及苦参单煎样品峰面积作为参比,比较不同配比黄连-苦参药对的共有峰相对峰面积,结果见表2。可知在不同程度配比下,各共有峰相对峰面积均有不同程度的变化,绝大部分表现出显著性差异。除属黄连药材的10、13号峰各相对峰面积相比药材单提均有所下降外,其余峰均表现为升高,表明配比后成分的溶出对苦参总体表现为促进作用,而对黄连的不同成分表现为促进和抑制的不同作用。1、5、7号峰在黄连-苦参为2∶1时相对峰面积最大;2~4、8、10号峰在黄连-苦参为5∶1时相对峰面积最大;11~16号峰在黄连-苦参为4∶1时相对峰面积最大;6号峰在黄连-苦参为1∶3时相对峰面积最大;9号峰在黄连-苦参为3∶1时相对峰面积最大,提示在方剂中使用不同配比黄连-苦参药对治疗疾病,可能与不同配比下药对中成分的溶出变化有关[23]。 2.2 不同配比黄连-苦参药对中差异性成分含量测定 2.2.1 色谱条件 按照“2.1.1”项下色谱条件进行测定。设定在波长为205 nm时,对苦参碱、槐定碱、氧化苦参碱进行测定;在波长为220 nm时,对木兰花碱进行测定;345 nm时,对非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱进行测定。此时各指标性成分均为最大吸收波长。 2.2.2 混合对照品溶液的制备 依照“2.1.2”项下方法制备混合对照品溶液。 2.2.3 供试品溶液的制备 依照“2.1.3”项下方法制备9个比例的黄连-苦参药对供试品溶液,每个比例制备3个供试品溶液作为平行对照。 2.2.4 线性关系考察及检测限、定量限 对照品母液的配制:取苦参碱、槐定碱、氧化槐果碱、木兰花碱、非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱对照品各适量,分别置于10 mL量瓶中,加甲醇溶解并定容,制得上述成分质量浓度分别为0.98、0.40、0.85、0.35、0.31、0.35、0.36、0.36、0.35、0.81 mg/mL的对照品溶液。 取各对照品母液,逐级稀释0、2、4、8、16、32、64倍,按照“2.1.1”项下色谱条件进行测定。以各差异性成分的质量浓度为横坐标(X)、峰面积为纵坐标(Y)绘制标准曲线,进行线性回归,得回归方程,结果见表3,表明各成分线性关系良好。 依照信噪比,即S/N为3∶1及S/N为10∶1对各成分的检测限及定量限进行检测,结果见表3。 2.2.5 精密度试验 依照黄连与苦参比例1∶3,精密称取黄连药材粉末3 g及苦参药材粉末9 g,按照“2.1.3”项下方法制备供试品溶液,按“2.1.1”项下色谱条件连续进样6次,记录各差异性成分的峰面积。结果显示,苦参碱、槐定碱、氧化苦参碱、木兰花碱、非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱峰面积的RSD分别为1.40%、2.13%、1.37%、2.11%、0.91%、0.69%、1.25%、1.19%、0.17%、0.14%,结果表明仪器精密度良好。 2.2.6 稳定性试验 依照黄连与苦参比例1∶3,精密称取黄连药材粉末3 g及苦参药材粉末9 g,按照“2.1.3”项下方法制备供试品溶液,于室温放置0、4、8、12、16、20、24 h,按“2.1.1”项下色谱条件进样分析,记录各差异性成分的峰面积。结果显示,苦参碱、槐定碱、氧化苦参碱、木兰花碱、非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱峰面积的RSD分别为1.57%、2.24%、2.22%、2.46%、0.22%、0.16%、0.65%、0.05%、0.14%、0.20%,表明各差异性成分在室温放置24 h内稳定性较好。 2.2.7 重复性试验 依照黄连与苦参比例1∶3,精密称取黄连药材粉末3 g及苦参药材粉末9 g,按照“2.1.3”项下方法平行制备供试品溶液6份,再按“2.1.1”项下色谱条件进样分析,记录各差异性成分的峰面积,并根据标准曲线计算含量。结果显示,苦参碱、槐定碱、氧化苦参碱、木兰花碱、非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱质量分数的RSD分别为1.16%、1.24%、1.33%、1.57%、1.05%、1.19%、1.42%、1.30%、1.21%、1.22%,表明该方法重复性良好。 2.2.8 加样回收率试验 依照黄连与苦参比例1∶3,精密称取黄连药材粉末3 g及苦参药材粉末9 g,平行称取6份,分别加入含有苦参碱0.31 mg、槐定碱0.20 mg、氧化苦参碱1.52 mg、木兰花碱0.07 mg、非洲防己碱0.08 mg、表小檗碱0.27 mg、药根碱0.06 mg、黄连碱0.22 mg、巴马汀0.21 mg、小檗碱0.79 mg的对照品溶液5 mL,按照“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样分析,记录各标志性成分的峰面积,并计算平均加样回收率。结果显示,苦参碱、槐定碱、氧化苦参碱、木兰花碱、非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱的平均加样回收率分别为100.2%、100.1%、100.3%、100.2%、101.2%、100.7%、99.8%、101.1%、100.60%、101.0%,RSD分别为0.67%、0.97%、0.89%、0.97%、0.56%、0.70%、0.57%、0.71%、0.99%、0.85%,表明该方法准确度良好。 2.2.9 不同配比黄连-苦参药对水煎液成分含量测定及比较 取9个不同比例的黄连-苦参药对药材粉末,精密称定,按照“2.1.3”项下方法制备供试品溶液,再按“2.1.1”项下色谱条件进样分析,记录各差异性成分的峰面积,并根据标准曲线计算苦参碱、槐定碱、氧化苦参碱、木兰花碱、非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱的含量。将各比例药对中黄连-苦参药对生药量以黄连、苦参单煎样品的生药量为标准,换算成一致的量,计算各特征性成分的含量。通过SPSS 27.0软件,对数据进行单因子方差分析和显著性检验[24],结果见表4。 对含量测定结果进行系统分析。黄连-苦参比例为4∶1时,所得非洲防己碱、表小檗碱、巴马汀、小檗碱含量为各比例最高,且黄连总生物碱含量最高,与单药材提取具有显著性差异(P<0.05);黄连-苦参比例为5∶1时,所得苦参碱、槐定碱、木兰花碱含量为各比例最高,与单药材提取具有显著性差异(P<0.05);黄连-苦参比例为1∶3时,氧化苦参碱含量为各比例最高,与单药材提取具有显著性差异(P<0.05);黄连-苦参比例为1∶1时,苦参总生物碱含量为各比例最高。与黄连、苦参各药材单提相比,各比例下苦参中总生物碱类成分的溶出均有不同程度的提升,黄连中总生物碱类成分在黄连-苦参5∶1及4∶1比例下溶出表现为提升,其他比例表现为降低。随着药对中黄连比例的降低,黄连中整体生物碱类成分呈现下降趋势。对苦参中差异性成分进行比较,随着药对中黄连比例的降低,苦参碱、槐定碱在药液中的溶出降低,而氧化苦参碱的溶出提升,3种成分呈现“U”型分布,提示3者之间的相互影响关系。 3 讨论 本研究考虑与临床应用一致,黄连-苦参药对选择水回流提取法,选择分离效果最佳的乙腈-磷酸二氢钾溶液体系,对黄连及黄连-苦参药对的色谱条件进行优化,并在190~440 nm进行全波长扫描,于220 nm下进行指纹图谱建立以求全面对待测样品的差异性成分进行测定。结果表明,本研究建立的黄连-苦参药对指纹图谱稳定有效,可全面的测定黄连-苦参药对中的标志性成分。 大量文献研究发现,黄连-苦参药对在方剂中多采用1∶5至5∶1区间配比,故选择典型的9个配比进行量-质传递对比性研究。生物碱类成分作为黄连-苦参药对的主要药效成分,研究生物碱类成分在传统方剂煎煮过程中的溶出差异,可以为临床用药提供参考。故采用建立指纹图谱方式进行定性验证,确定稳定可测的生物碱类成分,并根据“2.1.8”项下结果,选择苦参中苦参碱、槐定碱、氧化苦参碱及黄连中木兰花碱、非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱进行研究[25-26]。 本研究在最佳吸收波长下,对黄连-苦参药对不同配比中10个差异性成分进行含量测定,分析差异性成分在不同配比下的溶出变化。苦参中3种差异性成分的溶出量随黄连比例的降低呈现“U”型分布,而黄连中7种差异性成分溶出量随黄连比例的降低整体呈现降低趋势。在黄连-苦参药对中,高黄连比例更容易促进药对中差异性成分的溶出。初步分析,当黄连-苦参药对中黄连占比的降低,可能会通过改变溶液中pH值、酸碱度等性质,对二者差异性成分的溶出产生影响,也可能对其中成分的相互转化产生促进作用,其具体产生机制有待深入研究。黄连-苦参药对被应用与各类中医经典方及现代经验方剂中[27-28],但其配伍面对临床不同疾病的合理应用仍需深入研究。 本研究首次将黄连-苦参相须药对与中医传统经验方剂药效相结合,探究差异性成分药理作用与临床疾病治疗的联系。黄连-苦参比例为5∶1时,所得苦参碱、槐定碱、木兰花碱含量为各比例最高;非洲防己碱、表小檗碱、药根碱、黄连碱、巴马汀、小檗碱含量较高,相比各药材单提含量有所提升,与单药材提取均具有显著性差异(P<0.05),与《普济方》中“相须为用,其效益彰”的方解一致,发挥各成分共同药效,达到“清热燥湿”效果。氧化苦参碱具有抗肿瘤作用,当黄连-苦参比例为1∶3时,其溶出量达到最大并与单药材提取具有显著性差异(P<0.05),与临床上使用参白解毒方进行抗结直肠道腺瘤[29]的治疗方式一致。药根碱可发挥降糖作用,在黄连-苦参比例为1∶1时含量最高,与国医大师李玉奇治疗消渴症时采用方剂中黄连-苦参药对[30]的配比一致,证明了方剂中黄连-苦参使用该比例配比的合理性。 综上所述,本研究成果预期可为开展黄连-苦参药对的量-效关系研究提供数据支撑,为临床不同疾病采用药对适宜配比用量、开发黄连-苦参药对新方剂提供借鉴。
[size=20px][color=#93c6bc][b]鉴别[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size] [font=宋体][/font] [font=宋体](1)取本品粉末0.5g,置适宜器皿中,60~80℃升华4小时,置显微镜下观察,可见针状、针簇状、棒状、板状结晶及黄色球状物。[/font] [font=宋体](2)取〔鉴别〕(1)项下的升华物,加三氯甲烷数滴使溶解,作为供试品溶液。另取香草酸对照品、肉桂酸对照品,加三氯甲烷制成每1ml各含1mg的[color=var(--weui-LINK)]混合溶液[i][/i][/color],作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各5[/font]μ[font=宋体]l[/font][font=宋体],分别点于同一硅胶[/font]GF[sub]254[/sub][font=宋体]薄层板上,以正己烷-乙醚-冰醋酸(5:5:0.1)为展开剂,展开,取出,晾干,置紫外光灯(254nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点。[/font] [font=宋体][/font] [size=20px][color=#93c6bc][b]检查[/b][/color][/size][size=16px][color=#e2a4a4]|[/color][/size][font=宋体][/font] [b][font=宋体][/font] [font=宋体]水分[/font][/b][font=宋体] [/font][font=宋体]不得过13.0%(通则0832第二法)。[/font] [b][font=宋体]总灰分[/font][/b][font=宋体] [/font][font=宋体]不得过7.0%(通则2302)。[/font] [b][font=宋体]酸不溶性灰分[i][/i][/font][/b][font=宋体] [/font][font=宋体]不得过3.0%(通则2302)。[/font] [b][font=宋体]【[color=var(--weui-LINK)]浸出物[i][/i][/color]】[/font][/b][font=宋体] 照醇溶性浸出物测定法(通则2201)项下的热浸法测定,用乙醇作溶剂,不得少于30.0%。[/font] [b][font=宋体]【含量测定】[/font][/b][font=宋体] 照高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]法(通则0512)测定。[/font] [b][font=宋体]色谱条件与系统适用性试验[/font][/b][font=宋体] [/font][font=宋体]以[color=var(--weui-LINK)]十八烷基硅烷键合硅胶[i][/i][/color]为填充剂;以甲醇-水-磷酸(35:65:0.1)为流动相;检测波长为275nm。理论板数按胡黄连苷Ⅱ峰计算应不低于3000。[/font] [b][font=宋体]对照品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取胡黄连苷Ⅰ对照品、胡黄连苷Ⅱ对照品适量,精密称定,加甲醇制成每1ml各含40[/font]μ[font=宋体]g[/font][font=宋体]的混合溶液,即得。[/font] [b][font=宋体]供试品溶液的制备[/font][/b][font=宋体] [/font][font=宋体]取本品粉末(过三号筛)约0.1g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,密塞,称定重量,超声处理(功率250W,频率33kHz)30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液1ml,置5ml量瓶中,加甲醇至刻度,摇匀,即得。[/font] [b][font=宋体]测定法[/font][/b][font=宋体] [/font][font=宋体]分别精密吸取对照品溶液与供试品溶液各10[/font]μ[font=宋体]l[/font][font=宋体],注入[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url],测定,即得。[/font] [font=宋体]本品按干燥品计算,含胡黄连苷Ⅰ[/font][font=宋体]([/font]C[sub]24[/sub]H[sub]28[/sub]O[sub]11[/sub][font=宋体])与胡黄连苷Ⅱ([/font]C[sub]23[/sub]H[sub]28[/sub]O[sub]13[/sub][font=宋体])的总量不得少于9.0%。[/font]
摘要:建立胡黄连中香草酸和桂皮酸的含量测定方法。方法用双波长扫描法测定胡黄连中香草酸和桂皮酸的含量。结果香草酸。桂皮酸斑点峰面积3Il内稳定,香草酸回收率为103.86%,RSD=1.33%,桂皮酸回收率为103.16%,RSD=1.28%。结论该方法稳定,可行。具有实用性。 关键词:胡黄连 薄层扫描法 香草酸 桂皮酸 胡黄连具有保肝利胆、抗炎、抗真菌等药理作用。胡黄连含胡黄连素、胡黄连苷(I II III)、D-甘露醇、香草酸、肉桂酸、胡黄连醇成分。香草酸和桂皮酸是其中的两种抗菌成分。我们对胡黄连中香草酸、桂皮酸含量建立了薄层扫描法,以达到控制胡黄连的质量,从而为临床疗效提供保证。 1 仪器与试剂 药材:胡黄连,太原市药材公司;仪器:日本岛津CS--9301PC薄层扫描仪;手提式荧光灯(上海固村电光仪器厂);对照品:香草酸对照品(中国药品生物制品检定所);桂皮酸对照品溶液(省药检所提供e=0.604mg/50ml);硅胶GF254(青岛海洋化工厂)所用试剂均为分析纯。 2 实验条件 2.l 薄层层析条件:分别以石油醚-氯仿-丙酮-冰醋酸(10:4.4:10.1);正己烷-乙醚-冰醋酸(5:5:0.1);正己烷-氯仿-乙醚-冰醋酸(5:3:2:0.1)以及氯仿:甲醇(2:1)展开,多次比较发现正己烷。氯仿-乙醚-冰醋酸(5:3:2:0.4)分离效果好。 2.2 测定波长及主要扫描参数,分别对香草酸,桂皮酸对照品斑点在200nm-370nm扫描,在290nm处有最大吸收,350nm处无吸收,固定350nm为参比波长,290nm为测定波长。
求助,配制盐酸表小檗碱和盐酸黄连碱对照液时,发现其很难溶解,文献中溶剂用的甲醇或甲醇-盐酸,我试了,也很难溶,超声加热溶解性也不好,有什么办法可以帮助溶解啊?
方法名称: 香连丸—黄连素的测定—高效液相色谱法 应用范围: 本方法采用高效液相色谱法测定香连丸中黄连素的含量。本方法适用于中成药香连丸。 方法原理: 供试品于容量瓶中,加HCl-CH3OH超声提取,放冷,摇匀,滤过,滤液注入高效液相色谱仪进行色谱分离,用紫外吸收检测器,于波长345nm处检测黄连素的吸收值,计算出其含量。 试剂: 1.甲醇(色谱纯)2.乙腈(色谱纯)3.盐酸 仪器设备: 1仪器1.1高效液相色谱仪1.2色谱柱μBONDAPAK-C18(3.9mm×250mm,10μm)1.3紫外吸收检测器2色谱条件2.1流动相:乙腈 磷酸盐缓冲液(PH5.2) 甲醇 +1.3%SDS = 5 6 1 12.2检测波长:345nm 试样制备: 1.称取供试品 精密称取香连丸(过3号筛)1.116g。2.对照品溶液的制备精密称取105℃干燥至恒重的盐酸小檗碱对照品11.36mg置于50mL容量瓶中,加适量乙醇使溶解,并加乙醇至刻度,作为盐酸小檗碱对照品溶液。3. 标准溶液的制备分别精密吸取上述盐酸小檗碱对照品溶液1mL,2mL,3mL,4mL置10mL容量瓶中,用乙醇稀释至刻度,摇匀,作为绘制标准曲线的系列浓度标准溶液。4.供试品溶液的制备 将供试品置50mL容量瓶中,加HCl-CH3OH(1:100)至刻度超声处理30min,放冷至室温,加HCl-CH3OH至刻度,摇匀,滤过,取续滤液作为供试品溶液。注:“精密称取”系指称取重量应准确至所取重量的千分之一。“精密量取”系指量取体积的准确度应符合国家标准中对该体积移液管的精度要求。 操作步骤: 1.标准曲线绘制 将上述系列标准浓度的对照品溶液,各进样10μL,以峰面积积分值对浓度进行回归,绘制标准曲线。2.供试品溶液的测定分别精密吸取上述对照品溶液与供试品溶液各10μL注入高效液相色谱仪,用紫外吸收检测器,于波长345nm处测定黄连素的峰面积积分值,用外标法计算出黄连素的含量。
求助,配制盐酸表小檗碱和盐酸黄连碱对照液时,发现其很难溶解,文献中溶剂用的甲醇或甲醇-盐酸,我试了,也很难溶,超声加热溶解性也不好,有什么办法可以帮助溶解啊?
最近在做黄连薄层鉴别,遇到以前未发生过的事情,以前用药典展开剂跑得效果挺好的,可是现在怎么也跑不上去,用的是对照药材,不知最近是否也有人在做黄连,是否遇到相同的情况
[font=宋体]黄连味苦性寒,具有清热燥湿、泻火解毒的功效。《[color=var(--weui-LINK)]中国药典[i][/i][/color]》[/font]2020[font=宋体]年版规定黄连为毛茛科黄连属植物黄连[/font][i]Coptis chinensis[/i] Franch.[font=宋体]、三角叶黄连[/font][i]C. deltoidea [/i]C. Y. Cheng et Hsiao[font=宋体]或云连[/font][i]C. teeta[/i] Wall.[font=宋体]的干燥根茎。以上[/font]3[font=宋体]种分别习称“味连”“雅连”“云连”,经课题组前期调研以味连产量最多,主产于我国重庆、湖北、四川等地[/font][sup][1][/sup][font=宋体]。现代研究表明,黄连含有多种活性成分,可发挥多种药理作用[/font][sup][2][/sup][font=宋体],包括抗炎、抗病毒、抗菌、抗癌、镇痛、抗抑郁、降血糖等作用,临床应用极广[/font][sup][3][/sup][font=宋体]。苦参性寒、味苦,为豆科苦参属植物苦参[/font][i]Sophora flavescens [/i]Ait.[font=宋体]的干燥根,主产于我国内蒙古、河南、山东、安徽等地[/font][sup][1][/sup][font=宋体],具有抗菌、抗肿瘤、镇痛、抗炎、防治心力衰竭、心律失常及心肌缺血等多种功效[/font][sup][4-5][/sup][font=宋体]。[/font] [font=宋体]现代研究表明,生物碱类化合物是黄连及苦参的主要活性成分。苦参碱、氧化苦参碱可发挥抗炎、镇痛效果[/font][sup][6-7][/sup][font=宋体],其机制可能与降低[color=var(--weui-LINK)]促炎因子[i][/i][/color],升高抗炎因子有关;氧化苦参碱、苦参碱也可发挥抗肿瘤作用,其机制可能与抑制癌症基因表达,促进肿瘤细胞凋亡,抑制肿瘤细胞生长有关[/font][sup][8][/sup][font=宋体];而苦参碱、氧化苦参碱、槐定碱也可对多种菌株具有一定的抑菌作用[/font][sup][9][/sup][font=宋体]。木兰花碱可通过活性氧([/font]reactive oxygen species[font=宋体],[/font]ROS[font=宋体])[/font]/[font=宋体]鼠类肉瘤病毒癌基因([/font]Kirsten rat sarcoma viral oncogene[font=宋体],[/font]KRAS[font=宋体])[/font]/[font=宋体]单磷酸腺苷活化蛋白激酶([/font]adenosine monophosphate activated protein kinase[font=宋体],[/font]AMPK[font=宋体])通路抑制结直肠癌[/font]SW480[font=宋体]细胞的增殖和有氧糖酵解,从而发挥对结直肠癌的治疗效果[/font][sup][10][/sup][font=宋体];药根碱、[color=var(--weui-LINK)]巴马汀[i][/i][/color]、表小檗碱、黄连碱、小檗碱可联合发挥降糖作用[/font][sup][11][/sup][font=宋体],其效果可能与调控丝氨酸[/font]-[font=宋体]苏氨酸激酶[/font]1[font=宋体]([/font]serine/threonine kinase 1[font=宋体],[/font]LKB1[font=宋体])[/font]/ AMPK/CREB[font=宋体]分子调节转录共激活剂[/font]2[font=宋体]([/font]CREB-regulated transcription coactivator 2[font=宋体],[/font]TORC2[font=宋体])信号通路抑制肝脏糖异生等有关[/font][sup][12][/sup][font=宋体];小檗碱具有抗炎作用,可保护螺旋神经节细胞免受巨细胞病毒诱导的凋亡作用,其机制与通过途径抑制线粒体活性氧的产生有关[/font][sup][13][/sup][font=宋体]。[/font][font=宋体]除此之外,小檗碱、表小檗碱、巴马汀等生物碱类成分也可联合发挥抗心律失常作用[/font][sup][14][/sup][font=宋体]。基于此,选择苦参中苦参碱、槐定碱、氧化苦参碱及黄连中木兰花碱、非洲防己碱、药根碱、表小檗碱、黄连碱、巴马汀、小檗碱来作为黄连[/font]-[font=宋体]苦参药对的代表性药效成分,用于研究该类成分溶出量与药对配比的关系。[/font][font=宋体]药对作为中药配伍的最小单元,是复方研究的重要组成部分之一[/font][sup][15][/sup][font=宋体]。用于不同疾病的治疗时,不同量的配比会有不同效果的相关呈现,因此,首先需要对黄连[/font]-[font=宋体]苦参药对配比的不同物质基础,即量[/font]-[font=宋体]质[/font][sup][16][/sup][font=宋体]相关性进行剖析比较,为进行量[/font]-[font=宋体]效[/font][sup][17][/sup][font=宋体]相关性提供依据,为临床合理配比提供参考[/font][sup][18][/sup][font=宋体]。 [/font][b][back=#d6a841]1 [font=黑体]仪器与试药[/font][/back][/b]1.1 [font=黑体]主要仪器[/font]Waters e2695[font=宋体]型高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]系统,[/font]Waters 2998[font=宋体]型二极管阵列检测器([/font]PDA[font=宋体]),美国[/font]Waters[font=宋体]公司;[/font]BBA224S-CW[font=宋体]型电子天平,赛多利斯科学仪器(北京)有限公司;[/font]TGL-16C[font=宋体]型离心机,上海安亭科学仪器厂;[/font]EPED-E2-20TS[font=宋体]型超纯水一体机系统,南京易普易达科技发展有限公司;[/font]GM-0.5B[font=宋体]型真空泵,天津市津腾实验设备有限公司;[/font]KH-500V[font=宋体]型超声器,昆山禾创超声仪器有限公司。[/font]1.2 [font=黑体]药品及试剂[/font]1.2.1 [font=宋体]药材与饮片[/font] [font=宋体]本研究所选择黄连(产地重庆石柱黄水,批号[/font]20230411[font=宋体])及苦参(产地内蒙古赤峰市,批号[/font]2020121604[font=宋体])药材,均经南京中医药大学药学院刘圣金教授鉴定,分别为毛茛科黄连属植物黄连[/font][i]C. chinensis[/i] Franch.[font=宋体]的干燥根茎和豆科苦参属植物苦参[/font][i]S. flavescens[/i] Ait.[font=宋体]的干燥根。[/font]1.2.2 [font=宋体]对照品[/font] [font=宋体]表小檗碱(批号[/font]J24HB186173[font=宋体])、盐酸小檗碱(批号[/font]S01A10K94340[font=宋体])、盐酸黄连碱(批号[/font]T21S11C125202[font=宋体])、药根碱(批号[/font]D18GB171805[font=宋体])、盐酸巴马汀(批号[/font]Z16J10X79792[font=宋体])、非洲防己碱(批号[/font]W14J8Z37548[font=宋体])、木兰花碱(批号[/font]R21M9F61834[font=宋体])、苦参碱(批号[/font]M14GB141405[font=宋体])、氧化苦参碱(批号[/font]G14N11KL130769[font=宋体])、槐定碱(批号[/font]F18F7S9784[font=宋体]),[/font][color=var(--weui-LINK)]HPLC[i][/i][/color][font=宋体]质量分数均≥[/font]98%[font=宋体],均购自上海源叶生物科技有限公司。[/font][b][/b]1.2.3 [font=宋体]试剂[/font] [font=宋体]乙腈、甲醇,色谱纯,安徽天地高纯溶剂有限公司;磷酸、盐酸、无水乙醇,分析纯,国药集团化学试剂有限公司;纯净水,屈臣氏集团(香港)有限公司;磷酸二氢钾,分析纯,南京化学试剂股份有限公司。[/font][size=17px][b][back=#d6a841]2 [font=黑体]方法与结果[/font][/back][/b][/size]2.1 [font=黑体]不同配比黄连[/font][b]-[/b][font=黑体]苦参药对指纹图谱的建立[/font]2.1.1 [font=宋体]色谱条件[/font] [font=宋体]色谱柱为[/font]Venusil XBP C[sub]18[/sub][font=宋体]([/font]2[font=宋体])([/font]250 mm[font=宋体]×[/font]4.6 mm[font=宋体],[/font]5 μm[font=宋体]);柱温[/font]30 [font=宋体]℃;体积流量[/font]0.8 mL/min[font=宋体];流动相为乙腈[/font]-3 g/L[font=宋体]磷酸二氢钾溶液(加入[/font]200 μL[font=宋体]磷酸调节[/font]pH[font=宋体]值),梯度洗脱:[/font]0[font=宋体]~[/font]10 min[font=宋体],[/font]10%[font=宋体]乙腈;[/font]10[font=宋体]~[/font]25 min[font=宋体],[/font]10%[font=宋体]~[/font]24%[font=宋体]乙腈;[/font]25[font=宋体]~[/font]35 min[font=宋体],[/font]24%[font=宋体]乙腈;[/font]35[font=宋体]~[/font]60 min[font=宋体],[/font]24%[font=宋体]~[/font]35%[font=宋体]乙腈;[/font]60[font=宋体]~[/font]62 min[font=宋体],[/font]35%[font=宋体]~[/font]60%[font=宋体]乙腈;[/font]62[font=宋体]~[/font]65 min[font=宋体],[/font]60%[font=宋体]~[/font]10%[font=宋体]乙腈;[/font]65[font=宋体]~[/font]70 min[font=宋体],[/font]10%[font=宋体]乙腈;分析时间[/font]70 min[font=宋体],进样量[/font]10 μL[font=宋体];检测波长[/font]220 nm[font=宋体]。[/font]2.1.2 [font=宋体]混合对照品溶液的制备[/font] [font=宋体]取非洲防己碱、药根碱、表小檗碱、盐酸小檗碱、盐酸巴马汀、盐酸黄连碱、木兰花碱、苦参碱、氧化苦参碱、槐定碱对照品各适量,分别置于[/font]10 mL[font=宋体]量瓶中,加甲醇溶解并定容,即得各对照品储备液。分别取适量上述[/font]11[font=宋体]种对照品储备液,置于同一[/font]10 mL[font=宋体]量瓶中,加甲醇稀释并定容,制得上述成分质量浓度分别为[/font]0.20[font=宋体]、[/font]0.16[font=宋体]、[/font]0.24[font=宋体]、[/font]0.25[font=宋体]、[/font]0.25[font=宋体]、[/font]0.44[font=宋体]、[/font]0.26[font=宋体]、[/font]0.21[font=宋体]、[/font]0.80[font=宋体]、[/font]0.36 mg/mL[font=宋体]的混合对照品溶液。[/font]2.1.3 [font=宋体]供试品溶液的制备[/font] [font=宋体]制备黄连药材粉末(过二号筛)及苦参药材粉末(过三号筛),将上述黄连及苦参依照[/font]5[font=宋体]∶[/font]1[font=宋体]、[/font]4[font=宋体]∶[/font]1[font=宋体]、[/font]3[font=宋体]∶[/font]1[font=宋体]、[/font]2[font=宋体]∶[/font]1[font=宋体]、[/font]1[font=宋体]∶[/font]1[font=宋体]、[/font]1[font=宋体]∶[/font]2[font=宋体]、[/font]1[font=宋体]∶[/font]3[font=宋体]、[/font]1[font=宋体]∶[/font]4[font=宋体]、[/font]1[font=宋体]∶[/font]5[font=宋体]共[/font]9[font=宋体]个质量比例,进行称取后分别充分混合,并称取单一黄连药材粉末及单一苦参药材粉末作为对照药材,各比例药对总质量及单一药材质量均为[/font]12 g[font=宋体]。每个比例平行称取各药对[/font]3[font=宋体]份,将药对以[/font]10[font=宋体]倍量水浸泡[/font]0.5 h[font=宋体]后,煎煮[/font]1.5 h[font=宋体],取[/font]1[font=宋体]次滤液;将滤渣加入[/font]8[font=宋体]倍量水煎煮[/font]1.5 h[font=宋体],取[/font]2[font=宋体]次滤液。将[/font]2[font=宋体]次滤液混合后抽滤,[/font]12 000 r/min[font=宋体]离心(离心半径[/font]10.4 cm[font=宋体])[/font]10 min[font=宋体],取上清液,取[/font]1 mL[font=宋体]上清液加入[/font]4 mL[font=宋体]甲醇,以[/font]0.45 μm[font=宋体]微孔滤膜滤过,即得供试品溶液。[/font]2.1.4 [font=宋体]精密度试验[/font] [font=宋体]依照黄连与苦参比例[/font]1[font=宋体]∶[/font]3[font=宋体],精密称取黄连药材粉末[/font]3 g[font=宋体]及苦参药材粉末[/font]9 g[font=宋体],按照“[/font]2.1.3[font=宋体]”项下方法制备供试品溶液,再按“[/font]2.1.1[font=宋体]”项下色谱条件进样测定[/font]6[font=宋体]次,考察特征峰的保留时间和峰面积一致性。以盐酸小檗碱的保留时间和峰面积为参照分别计算相对保留时间及相对峰面积。计算得各共有峰相对保留时间的[/font]RSD[font=宋体]<[/font]0.20%[font=宋体],相对峰面积的[/font]RSD[font=宋体]<[/font]2.13%[font=宋体],结果表明仪器精密度良好。[/font]2.1.5 [font=宋体]稳定性试验[/font] [font=宋体]依照黄连与苦参比例[/font]1[font=宋体]∶[/font]3[font=宋体],精密称取黄连药材粉末[/font]3 g[font=宋体]及苦参药材粉末[/font]9 g[font=宋体],按照“[/font]2.1.3[font=宋体]”项下方法制备供试品溶液,再按“[/font]2.1.1[font=宋体]”项下色谱条件每隔[/font]4 h[font=宋体]进样[/font]1[font=宋体]次,共测定[/font]24 h[font=宋体],考察特征峰保留时间和峰面积的一致性。以盐酸小檗碱的保留时间和峰面积为参照分别计算相对保留时间及相对峰面积。计算得各共有峰相对保留时间的[/font]RSD[font=宋体]<[/font]0.21%[font=宋体]、相对峰面积的[/font]RSD[font=宋体]<[/font]2.46%[font=宋体],结果表明该供试品溶液在室温放置[/font]24 h[font=宋体]内稳定性良好。[/font]2.1.6 [font=宋体]重复性试验[/font] [font=宋体]依照黄连与苦参比例[/font]1[font=宋体]∶[/font]3[font=宋体],精密称取黄连药材粉末[/font]3 g[font=宋体]及苦参药材粉末[/font]9 g[font=宋体],平行制[/font]6[font=宋体]份,按照“[/font]2.1.3[font=宋体]”项下方法制备供试品溶液,分别按“[/font]2.1.1[font=宋体]”项下色谱条件进样分析,考察特征峰保留时间和峰面积的一致性。以盐酸小檗碱的保留时间和峰面积为参照分别计算相对保留时间及相对峰面积。计算得各共有峰相对保留时间的[/font]RSD[font=宋体]<[/font]0.18%[font=宋体]、相对峰面积的[/font]RSD[font=宋体]<[/font]1.57%[font=宋体],表明该方法重复性较好。[/font]2.1.7 [font=宋体]黄连[/font]-[font=宋体]苦参药对指纹图谱的建立及相似度评价分析[/font] [font=宋体]将黄连及苦参药材依照“[/font]2.1.3[font=宋体]”项下方法制备成供试品溶液([/font]S1[font=宋体]~[/font]S9[font=宋体]依次为黄连[/font]-[font=宋体]苦参比例为[/font]5[font=宋体]∶[/font]1[font=宋体]、[/font]4[font=宋体]∶[/font]1[font=宋体]、[/font]3[font=宋体]∶[/font]1[font=宋体]、[/font]2[font=宋体]∶[/font]1[font=宋体]、[/font]1[font=宋体]∶[/font]1[font=宋体]、[/font]1[font=宋体]∶[/font]2[font=宋体]、[/font]1[font=宋体]∶[/font]3[font=宋体]、[/font]1[font=宋体]∶[/font]4[font=宋体]、[/font]1[font=宋体]∶[/font]5[font=宋体]),再按“[/font]2.1.1[font=宋体]”项下色谱条件进样分析,记[/font][font=宋体]录色谱图。将图谱输入《中药色谱指纹图谱相似度评价系统([/font]2012[font=宋体]版)》,设置编号[/font]S7[font=宋体]的样品(黄连[/font]-[font=宋体]苦参为[/font]1[font=宋体]∶[/font]3[font=宋体])图谱为参照,采取中位数法[/font][sup][19][/sup][font=宋体],将时间窗宽度设置为[/font]0.1 s[font=宋体],进行多点校正,建立黄连[/font]-[font=宋体]苦参药对的[/font]HPLC[font=宋体]指纹图谱和对照指纹图谱([/font]R[font=宋体],图[/font]1[font=宋体]),指认[/font]9[font=宋体]批黄连[/font]-[font=宋体]苦参药对的[/font]16[font=宋体]个共有峰。[/font][font=宋体]采用《中药色谱指纹图谱相似度评价系统([/font]2012[font=宋体]版)》对[/font]9[font=宋体]批黄连[/font]-[font=宋体]苦参药对进行相似度评价[/font][sup][20][/sup][font=宋体]。结果显示,[/font]9[font=宋体]批黄连[/font]-[font=宋体]苦参药对和[/font]R[font=宋体]之间的相似度均大于[/font]0.95[font=宋体],这表明各批次黄连[/font]-[font=宋体]苦参药对的相似性较好,整体质量稳定[/font],[font=宋体]可以用于考察黄连[/font]-[font=宋体]苦参药对水煎液。以分离度较好、峰面积较大的小檗碱(峰[/font]16[font=宋体])为参照峰([/font]S[font=宋体]),得到[/font]9[font=宋体]批黄连[/font]-[font=宋体]苦参药对[/font]16[font=宋体]个共有峰相对保留时间的[/font]RSD[font=宋体]为[/font]0.175%[font=宋体]~[/font]0.894%[font=宋体],提示各批次黄连[/font]-[font=宋体]苦参药对共有峰的保留时间稳定,结果见表[/font]1[font=宋体]。[/font][font=黑体][/font][img=图片,1,]data:image/svg+xml,%3C%3Fxml version='1.0' encoding='UTF-8'%3F%3E%3Csvg width='1px' height='1px' viewBox='0 0 1 1' version='1.1' xmlns='http://www.w3.org/2000/svg' xmlns:xlink='http://www.w3.org/1999/xlink'%3E%3Ctitle%3E%3C/title%3E%3Cg stroke='none' stroke-width='1' fill='none' fill-rule='evenodd' fill-opacity='0'%3E%3Cg transform='translate(-249.000000, -126.000000)' fill='%23FFFFFF'%3E%3Crect x='249' y='126' width='1' height='1'%3E%3C/rect%3E%3C/g%3E%3C/g%3E%3C/svg%3E[/img][img=图片,1,]data:image/svg+xml,%3C%3Fxml version='1.0' encoding='UTF-8'%3F%3E%3Csvg width='1px' height='1px' viewBox='0 0 1 1' version='1.1' xmlns='http://www.w3.org/2000/svg' xmlns:xlink='http://www.w3.org/1999/xlink'%3E%3Ctitle%3E%3C/title%3E%3Cg stroke='none' stroke-width='1' fill='none' fill-rule='evenodd' fill-opacity='0'%3E%3Cg transform='translate(-249.000000, -126.000000)' fill='%23FFFFFF'%3E%3Crect x='249
hplc方法检测复方制剂中胡黄连苷1.2,标准品单独可以检测出来,样品单药也可以检测出来,但是复方的检测不到,标准品加到样品里面也检测不到,是的均用甲醇处理的。是什么原因,请大家指教,多谢
双黄连口服液是由金银花、黄芩、连翘组成的纯中药口服液。中药口服液是近十多年来开发的新剂型。 紫外分光光度计定量分析1 波长的选择 吸取黄芩苷对照品溶液在200nm~400nm作光谱扫描,确定最大吸收波长。2 标准曲线的绘制精密称取干燥至恒重的黄芩苷对照品粉末20mg,溶于25mL棕色量瓶中,加甲醇定容至刻度,摇匀,作为对照品原液。再分别精密量取黄芩苷对照品原液用蒸馏水配制成最终浓度为0.016mg/mL、0.02mg/mL﹑0.032mg/mL、0.04mg/mL、0.08mg/mL的标准溶液,在波长为276nm下测吸光度,以黄芩苷浓度为横坐标,吸光度为纵坐标,绘制标准曲线。3 黄芩苷含量检测采用紫外分光光度法分别对过滤后的提取液、醇沉后过滤的产品,黄芩的重复性试验,精密度试验,在波长为276nm下测定黄芩苷吸光度,以黄芩苷作为指标来衡量提取、纯化分离工艺的优劣。4 精密度试验取0.04mg/mL黄芩苷对照品溶液连续用紫外分光光度计在276nm波长下测其吸光度。5 供试品的稳定性试验取双黄连口服液1.0mL,按样品含量测定项下的方法操作的供试品溶液于0、1、2、4、8h测吸光度值。6 回收率试验采用加样回收率试验,精密量取已测定含量(含量为0.0163mg)的双黄连口服液1.0mL共五份,精密加入黄芩苷对照品溶液1.0mL五份,按含量测定项的方法制备供试液,测回收率。 以上是做实验的方法。此过程中主要用到分光光度计。下面谈谈使用心得:一,接通分光光度计电源,预热半小时后,先调节所用到的物质最大波长。二,测样品中黄芩苷的吸光度值,首先制作黄芩苷标准品的标准曲线。以黄芩苷标准品的浓度为横坐标,所测吸光度值为纵坐标。制作此曲线要保持各浓度下吸光度值介于0.3至0.7范围内,这样制作的标准曲线能准确测样品中黄芩苷。所以,要选择合适的各浓度值。三,使用容量瓶操作准确,规范,减少实验误差。

10,抽取5个版友);中奖名单:20071940xu(注册ID:20071940xu)夏天的雪(注册ID:bingwang228)捌道巴拉巴巴巴(注册ID:v3082413)http://ng1.17img.cn/bbsfiles/images/2017/01/201701221521_01_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2017/01/201701221521_02_1610895_3.jpg【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================黄连上清片方法:HPLC基质:动物提取物应用编号:102801化合物:盐酸小檗碱固定相:Platisil ODS色谱柱/前处理小柱:Platisil ODS 5u 250 x 4.6 mm样品前处理:对照品溶液:取盐酸小蘖碱对照品适量,精密称定,加甲醇制成每1 ml含厚朴酚20 μg的溶液。 供试品溶液:取本品10片,研细,精密称定,置具塞锥形瓶中,精密加入盐酸-甲醇(1:100)混合溶液10 ml,称定重量,置50 ℃水中加热15 min,取出,放冷,超声处理(功率250 W,频率33 kHz)30 分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密取续滤液2 ml,低温挥干溶剂,残渣用甲醇适量溶解,加在碱性氧化铝柱(100-200 目,8g,内径为1 cm)上,用甲醇35 ml洗脱,收集洗脱液,蒸干,残渣加甲醇溶解,并转移至10 ml 量瓶中,加甲醇稀释至刻度,摇匀,即得。色谱条件:色谱柱:Platisil C18,250×4.6 mm,5 μm (Cat#:99503) 流动相:乙腈:0.033mol/L磷酸二氢钾溶液=35:65 流速: 1.0 mL/min 柱温: 30 ℃ 检测器:UV 345 nm 进样量:10 μL文章出处:迪马科技关键字:盐酸小檗碱;黄连上清片;Platisil C18;铂金;hplc谱图:http://www.dikma.com.cn/Public/Uploads/images/1(104).JPGhttp://www.dikma.com.cn/Public/Uploads/images/2(53).JPG
多多药业有限公司生产的双黄连注射液被叫停。今天,国家食品药品监督管理局在其网站上发出通知,要求各地暂停销售使用标示为多多药业有限公司生产的双黄连注射液。 16日,国家药品不良反应监测中心报告称,标示为黑龙江多多药业有限公司生产的双黄连注射液在使用中出现严重不良事件。为确保公众用药安全,决定暂停销售和使用标示为多多药业有限公司生产的双黄连注射液。 目前,国家食品药品监督管理局和卫生部正在对该事件发生的原因进行调查。 大家对此事件如何看待的,有什么想法、看法、观点,说说,晒晒![em09502]
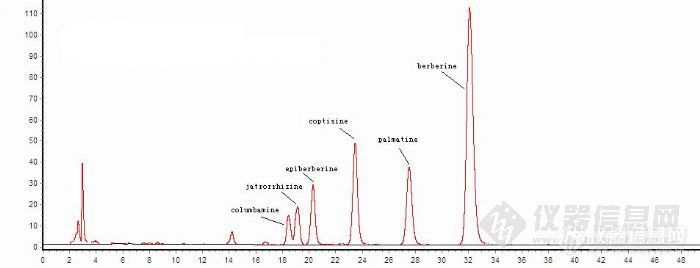
维权声明:本文为holiogodness原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。黄连中非洲防己碱色谱条件浅析背景介绍 黄连为毛茛科植物黄连Coptis chinensis Franch.、三角叶黄连Coptis deltoidea C.Y.Cheng et Hsiao或云南黄连Coptis teetoides C.Y.Cheng的干燥根茎。以上三种分别习称“味连”、“雅连”、“云连”。黄连苦、寒。归心、脾、胃、肝、胆、大肠经。能够清热燥湿,泻火解毒。用于湿热痞满,呕吐,泻痢,黄疸,高热神昏,心火亢盛,心烦不寐,血热吐衄,目赤吞酸,牙痛,消渴,痈肿疔疮,外治湿疹,湿疮,耳道流脓。 黄连中生物碱是黄连中的主要活性成分,因此建立黄连中生物碱含量测定方法尤为重要, 为黄连及其制剂的工艺研究与质量控制提供评价指标与评价方法。在黄连属植物中发现的生物碱,绝大部分为苄基异喹啉类,如:原小檗碱类、阿朴菲类、双苄基异喹啉类、苯菲啶类等,其中原小檗碱类又包括有原小檗碱型、甲基原小檗碱型、假原小檗碱型、氧化原小檗碱型和四氢原小檗碱型等,这些大多是季铵型生物碱。 以下是黄连中含量较高生物碱的结构式(第4个为非洲防己碱): http://ng1.17img.cn/bbsfiles/images/2010/10/201010191307_252215_2165312_3.jpg非洲防己碱色谱条件 非洲防己碱是黄连中分离得到的季铵型生物碱中的一个(第四个结构)。 此图为非洲防己碱三维液相分析图谱,色谱条件(乙腈:水=4:6;甲酸调PH=3) 色谱柱:YMC C18(250×4.6mm,5μm); 检测器:紫外 流速:1ml/min 温度:30http://ng1.17img.cn/bbsfiles/images/2010/10/201010181250_252050_2165312_3.jpg谱图分析及改善 本人曾一度认为样品已变,之后查阅文献才分析得出结论:非洲防己碱为季胺型生物碱,其存在解离与游离两种不同的形式,若色谱条件不能满足,非洲防己碱只存在一种形式,就有可能一个化合物出现两个色谱峰。故季胺型生物碱色谱分析时要求流动相中加入离子对试剂SDS,使其只存在一种形式而呈现单峰。色谱条件: 流动相: 0.05mol ·L - 1 磷酸二氢钾溶液(磷酸调节pH值至3.0)-乙腈( 60∶40,含SDS 1.0g/L); 流速: 1.0ml/min; 检测波长:345nm; 色谱柱: YMC C18(250×4.6mm,5μm); 检测器: 紫外 室温: 30℃ 下图为非洲防己碱二维分析图谱:(色谱条件如上所述)http://ng1.17img.cn/bbsfiles/images/2010/10/201010192207_252330_2165312_3.jpg小结与讨论 此色谱条件配制繁琐,且需现配现用。若长期放置会影响分析结果。SDS加入量会影响出峰时间,SDS增多,出峰时间提前,最佳浓度为1.5g/ml。SDS最好先加入到有机相中,否则可能会出现不溶.参考文献胡 敏,黄连的生药学鉴定,Strait Pharmaceutical Journal,2009,Vol21(14):89- 90
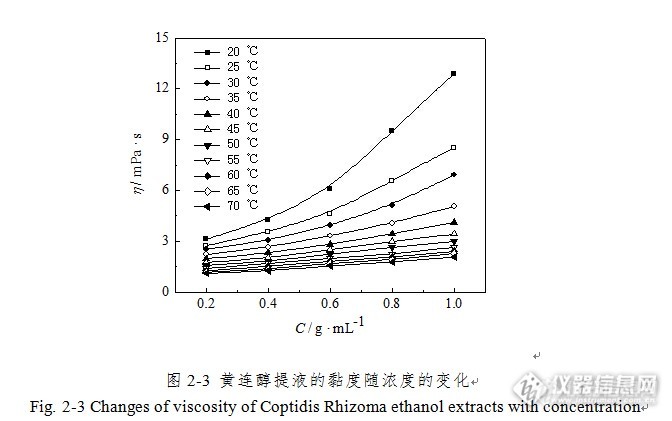
黄连提取液物性参数的测定及相关性研究摘要 黄连为毛茛科植物黄连(Coptis chinensis Franch.)、三角叶黄连(Coptis deltoidea C.Y.Cheng et Hsiao)、或云连(Coptis teeta Wall.)的干燥根茎,首载于《神农本草经》,列为上品,是临床最常用的清热类药物之一。其性味苦寒,入心、肝、胆、脾、胃、大肠诸经,具有清热燥湿、泻火解毒之功效。临床上多用于治疗湿热痞满、呕吐、泻痢、黄疸、心火亢盛、高热神昏、心烦不寐、目赤吞酸、牙痛、消渴及痈肿疔疮;外治湿疹、湿疮、耳道流脓。黄连的主要有效成份为异喹啉类生物碱,包括小檗碱(berberine)、黄连碱(coptisine)、药根碱(iatrordfizine)、巴马亭(palmatine)等。现代药理研究发现,黄连具有抗病原微生物、抗氧化、抗炎、抗血栓形成、降血糖、抗溃疡、抗癌、防治动脉硬化、保护胃黏膜、提高机体免疫功能等药理作用。 黄连的提取方法有:稀硫酸法、石灰水法、乙醇浸提法、超声波提取法、酶解法、微波-索氏工艺联合提取法、解吸-内部沸腾两步法、液膜法等。本实验采用回流提取的方法进行黄连提取液的制备,用旋转蒸发仪进行减压浓缩。1实验部分1.1仪器及试药1.1.1仪器RE-2000A旋转蒸发器(上海亚荣生化仪器厂);密度计(燕河仪器仪表有限公司);NDJ-5S旋转黏度计(上海伦捷机电仪表有限公司);DRE-2A导热系数测试仪(湘潭市仪器仪表有限公司)。1.1.2试药黄连片(北京同仁堂健康药业股份有限公司),经北京中医药大学刘春生教授鉴定符合2010版《中国药典》的要求;乙醇(95%),分析纯,北京化工厂;去离子水,自制。1.2样品的制备1.2.1不同浓度黄连水提液的制备 分别称取30、60、90、120、150 g黄连片,加入8倍量的水,加热回流提取3次,每次1 h,过滤,合并滤液。将滤液分别浓缩至150 mL,得到含生药质量浓度分别为0.2、0.4、0.6、0.8、1.0 g/mL的黄连水提液。1.2.2不同浓度黄连醇提液的制备 分别称取30、60、90、120、150 g黄连片,加入10倍量体积分数为60%的乙醇,加热回流提取3次,每次1 h,过滤,合并滤液。将滤液分别减压浓缩至稠膏状,用60%乙醇少量多次溶解洗出,再加60%乙醇至150 mL,得到含生药质量浓度分别为0.2、0.4、0.6、0.8、1.0 g/mL的黄连醇提液。1.3物性参数的测定方法 用浮子式密度计在20°C下测量各浓缩液的密度;在20~75°C下,用NDJ-5S型数显旋转黏度计分别测定不同浓度黄连水提液和醇提液的黏度;采用DRE-2A型导热系数测试仪在20~70°C下分别测定不同浓度黄连水提液和醇提液的导热系数。1.4分析方法 采用Excel对实验数据进行一元线性回归分析(ρ-C、η-C、η-T、λ-C、λ-T);采用1stOpt数据分析软件进行二元非线性拟合(η-C-T);采用SPSS数据分析软件进行二元线性回归(λ-C-T)。2结果与讨论2.1密度与浓度的关系 测定不同浓度的黄连水提液和黄连醇提液密度(表2-1),以线性回归分别考察其密度与浓度的关系(图2-1)。黄连水提液和醇提液密度与浓度关系的回归方程分别为ρ = 0.1105C+ 1.0002(r = 0.9992),ρ = 0.1157C + 0.9067(r = 0.9967)。结果表明,提取液的浓度与密度呈正相关,提取液浓度越高,提取液密度越大,二者具有良好的直线回归关系。http://ng1.17img.cn/bbsfiles/images/2015/09/201509171041_566383_3004888_3.jpg2.2黏度与浓度、温度的关系 测定不同温度不同浓度黄连水提液和黄连醇提液的黏度,结果分别见表2-2、2-3。http://ng1.17img.cn/bbsfiles/images/2015/09/201509171043_566384_3004888_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/09/201509171043_566385_3004888_3.jpg2.2.1黏度与浓度的关系 以浓度C为横坐标,黏度η为纵坐标,作出黄连水提液和黄连醇提液黏度随浓度的变化关系(图2-2、2-3)。结果显示,在同一温度水平下,提取液的黏度随浓度的增大而上升;温度越高,黏度随浓度增大而上升的幅度越小;在较高温度下,黄连醇提液浓度增大,黏度的变化不明显,曲线趋近于一条直线。http://ng1.17img.cn/bbsfiles/images/2015/09/201509171045_566386_3004888_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/09/201509171045_566387_3004888_3.jpg3结论3.1密度与浓度 黄连水提液和醇提液的密度与浓度均为直线正相关关系,即黄连提取液的密度随浓度的增大而增大,说明提取液的浓缩程度与其含固量直接相关。由于溶剂本身密度及其提取强度的影响,相同浓度的黄连水提液密度均大于醇提液密度。二者密度与浓度的回归方程分别为ρ = 0.1105C+ 1.0002 (r = 0.9992) 和ρ = 0.1157C + 0.9067(r = 0.9967)。3.2黏度与浓度、温度 比较黄连水提液和醇提液的黏度实测值发现,在相同温度下,相同浓度(0.2、0.4、0.6、0.8g/mL)的水提液黏度均小于醇提液黏度。这一点与黄芩相反,在相同温度下,相同浓度的黄芩水提液黏度均大于醇提液黏度。出现差异的原因可能是溶剂本身性质及提取液中所含成分的综合影响导致。 根据实测黏度值作出黄连提取液黏度随浓度、黏度随温度的变化关系曲线,结果显示:(1) 在同一温度水平下,提取液的黏度随浓度的增大而上升;温度越高,黏度随浓度增大而上升的幅度越小。(2) 在同一浓度水平下,提取液的黏度随温度的上升而降低;浓度越高,黏度随温度升高而下降的幅度越大。用实测值验证浓度对黏度影响的2种经典数学模型η = a1 Cb1和η = a2 exp(b2C),二者分别为幂和指数的形式,并得到各温度下η-C拟合方程。结果说明,实测值对后者的拟合度明显高于前者,即指数形式更能准确反映黄连提取液黏度与浓度的变化关系特征。
上海市食品药品监督管理局27日公布了2006年第四季度药品监督检查抽验不合格的药品公告,标识为哈尔滨中药四厂生产的批号为051112的10ml规格双黄连口服液、标识为长春经开药业有限公司生产的批号041101的1g/10丸规格青果丸等41个批次的药品“黑榜”有名,其原因为含量测定、可见异物等原因。 据文汇报报道,在此次抽检不合格产品中,除外地企业产品之外还有不少上海本地制药企业生产的产品。标识为上海通用药业股份有限公司生产的批号为030401的1ml:2mg规格的苯甲酸雌二醇注射液、标识为上海第一生化药业有限公司生产的批号为060602的40mg规格注射用奥美拉唑钠等产品均属于上海企业生产。部分医疗机构也抽检出不合格药品。在上海松江普照门诊部抽检发现的标识为安徽三超药业有限公司生产的批号为060101的8ml:8mg规格利巴韦林滴眼液就因PH值、可见异物不合格而上榜,在上海市杨浦区精神卫生中心、上海市浦东新区梅园社区卫生服务中心、上海博康生殖医学医院等医院也发现了不合格药品。 本次抽验分类情况为:药品抽验不合格率3.55%;医疗器械抽验不合格率9.48%;药包材抽验不合格率11.84%。对抽验出不合格药品、药包材和医疗器械的单位,各区(县)分局、稽查大队将依法查处并对其实施跟踪抽样检验。
中药标准品等中英文名称对照货号 英文名称 中文名称019-14621 Aconitine std. 乌头碱012-14091 Albiflorin std 芍药内酯苷018-13231 Alisol B acetate,98.0% 乙酸泽泻酯B010-13431 Alisol B std 泽泻醇B015-11921 Arbutin std 熊果苷012-14611 Atractylenolide III std. 苍术内酯016-11691 Atropine sulfate std. 硫酸阿托品016-10351 Aucubin std. 桃叶珊瑚苷027-07751 Baicalein std. 黄岑素020-07741 Baicalin std. 黄岑苷022-08161 Barbaloin std. 芦荟苷022-07681 Berberine chloride std. 氯化黄连素028-12051 Bergenin std. 岩白菜内酯025-10121 Bufalin std. 蟾毒灵024-10691 Bufotalin std. 蟾毒它灵030-10611 Capillarisin std. 茵陈色原酮036-10613 Capillarisin std. 茵陈色原酮031-15141 Capsaicin std. 辣椒素032-10551 Catalpol std. 梓醇038-13711 Cinobufagin std. 华蟾毒精035-13721 Cinobufotalin std. 华蟾毒它灵036-11311 Coptisine chloride 氯化黄连碱036-14971 Corydaline std. 紫堇碱032-13731 Costunolide std. 木香烃内酯043-27611 Dehydrocorydaline nitrate std. 硝酸脱氢紫堇碱040-21881 Dehydrocostuslactone std. 脱氢广木香内酯044-25321 Dihydrocapsaicin std. 二氢辣椒素042-18911 Dimethylesculetin std. 二甲基七叶树内酯052-04921 Ergosterol std. 麦角甾醇056-05161 β-Eudesmol std. β-桉油醇050-04601 Evodiamine std. 吴茱萸碱070-02241 Geniposide std. 京尼平苷078-02301 Geniposidic acid std. 京尼平苷酸077-02871 6-Gingerol std. 6-姜辣醇079-02191 Ginsenoside Rb1 std. 人参皂苷Rb1078-03261 Ginsenoside Rc 人参皂苷Rc072-03301 Ginsenoside Rd std. 人参皂苷Rd075-03271 Ginsenoside Re std. 人参皂苷Re072-02201 Ginsenoside Rg1 std. 人参皂苷Rg1071-02271 Glycyrrhizin std. 甘草甜素089-04951 Honokiol std. 和厚朴酚081-06851 (E)-10-Hydroxy-2-decenoic acid std. (E)-10-羟基-2-癸烯酸084-07061 Hypaconitine 次乌头碱099-03651 Isofraxidine std. 125-03361 Liquiritin std. 甘草甙125-03621 Loganin std. 番木鳖苷137-09081 Magnolol std. 厚朴酚130-12261 Mesaconitine 中乌头碱140-06211 Naringin std. 柚皮甙151-01801 Osthole std. 甲氧基欧芹酚150-01511 Oxymatrine std. 氧化苦参碱167-11711 Paeoniflorin std. 芍药苷163-11713 Paeoniflorin std. 芍药苷169-12871 Paeonol std. 牡丹酚166-17641 Palmatine chloride std. 氯化巴马亭164-14091 (+)-phyllodulcin std. (+)-叶甜素162-14071 Puerarin std. 葛根素184-00951 Resibufogenin std. 残余蟾蜍配基183-00921 Rutaecarpine std. 吴茱萸次碱190-08411 Saikosaponin a std. 柴胡皂甙a194-10021 Saikosaponin b2 std. 柴胡皂甙b2197-08421 Saikosaponin c std. 柴胡皂甙c194-08431 Saikosaponin d std. 柴胡皂甙d192-10441 Schizandrin std. 五味子素197-09261 Scopolamine hydrobromide, 99.0% 氢溴酸莨菪胺190-08531 Sennoside A std. 番泻苷A194-09271 Sennoside B, 96% 番泻苷B199-11811 Sennoside B std. 番泻苷B191-08681 Shikonin std. 紫草素193-09361 Sinomenine std. 青藤碱197-08541 Swertiamarin std. 獐牙菜苦苷231-00811 Wogonin std. 汉黄岑素
需要用的对照品,中检所没有的话,你们怎么办?购买国外大厂家的对照产品,还是自己精制对照???
项目概况宜春市检验检测中心试剂及耗材和标准品及对照品采购项目(第二次)(第二包:标准物质、对照品) 招标项目的潜在投标人应在 江西省公共资源交易网 获取招标文件,并于 2023年02月09日 09点00分 (北京时间)前递交投标文件。一、项目基本情况:项目编号:明月-YC2022-042-2-1项目名称:宜春市检验检测中心试剂及耗材和标准品及对照品采购项目(第二次)(第二包:标准物质、对照品)采购方式:公开招标预算金额:400000.00 元最高限价:400000.00采购需求:[table=100%][tr][td]采购条目编号[/td][td]采购条目名称[/td][td]数量[/td][td]单位[/td][td]采购预算(人民币)[/td][td]技术需求或服务要求[/td][/tr][tr][td][font=inherit]宜购2022F000814837[/font][/td][td][font=inherit]2022年食品药品监管中央及省级补助资金(标准品、对照品)[/font][/td][td][font=inherit]1[/font][/td][td][font=inherit]批[/font][/td][td][font=inherit]400000.00元[/font][/td][td][font=inherit]详见公告附件[/font][/td][/tr][/table]合同履行期限:详见招标文件本项目不接受联合体投标。
项目概况宜春市检验检测中心试剂及耗材和标准品及对照品采购项目(第二次)(第二包:标准物质、对照品) 招标项目的潜在投标人应在 江西省公共资源交易网 获取招标文件,并于 2023年02月09日 09点00分 (北京时间)前递交投标文件。一、项目基本情况:项目编号:明月-YC2022-042-2-1项目名称:宜春市检验检测中心试剂及耗材和标准品及对照品采购项目(第二次)(第二包:标准物质、对照品)采购方式:公开招标预算金额:400000.00 元最高限价:400000.00采购需求:[table=100%][tr][td]采购条目编号[/td][td]采购条目名称[/td][td]数量[/td][td]单位[/td][td]采购预算(人民币)[/td][td]技术需求或服务要求[/td][/tr][tr][td][font=inherit]宜购2022F000814837[/font][/td][td][font=inherit]2022年食品药品监管中央及省级补助资金(标准品、对照品)[/font][/td][td][font=inherit]1[/font][/td][td][font=inherit]批[/font][/td][td][font=inherit]400000.00元[/font][/td][td][font=inherit]详见公告附件[/font][/td][/tr][/table]合同履行期限:详见招标文件本项目不接受联合体投标。
中检所对照品常见问题与答复1、标准物质的用途和应用范围药品标准物质不能作为药物或医疗器械而施用于人或动物。药品标准物质主要用于法定药品质量标准中的相关项目的检测用,详细内容请见使用说明书。2、有效期除了说明书上注明有效期的品种外,药品标准物质一般没有像药品一样设置有效期。在规定的储存和使用条件下,定期进行特性量值的稳定性核查,若发现影响使用将及时处理。3、储存标准物质一般应密闭、避光保存,对有特殊储存要求(如低温、避光等)的标准物质,说明书上均有说明,今后标签上也将注明。建议不要一次购买大量的标准物质,以免储存不当出现问题。需要冷藏或冷冻保存的品种,短时间短距离的冰盒运输对特性不会造成影响。4、纯度目前含量测定用的化学对照品的标签及说明书均赋有量值,以前的部分中药化学含量测定用未赋值的品种,按 100.0%计。5、是否能用于说明书用途范围外的检验、科研需要用户进行分析与验证。6、使用前是否需要干燥标准物质说明书上对使用前是否需要干燥等情况,均有相关说明。除另有规定外,对照药材不需要特殊处理。7、标准物质证书或测试报告暂时还不能提供证书或者测试报告。8、新批号标准品出来后旧批号能否继续使用 新旧批号更换过程中,部分品种将设置3-6个月以上的缓冲期。9、用五氧化二磷干燥的标准物质是否要在相同条件下保存不需要。按说明书的条件保存即可。10、从哪里可以查到标准物质的结构、物理化学特性等中药化学对照品的说明书大多附有结构,化学药品的可以通过中国药典二部查阅。另外,分发的标准物质都提供了英文名,可以通过文献查阅有关详情。11、内毒素标准品是否有10EU一支的 标准品均为100EU/支,10EU的工作品是鲎试剂生产企业生产的,低效价的内毒素稳定性差,我们不建议使用这种工作品进行检验工作。12、为什么对照品在色谱上不出峰? 请按国家标准中提供的条件考察自己的色谱条件因素。色谱不出峰一般来讲有如下原因:一是色谱条件不合适;二是信号采集时衰减过高,建议减小衰减;三是采集时间过短,建议增加采集时间。13、为什么对照品出2个或多个峰 标准物质除多组分的以外,均只有一个主峰,杂质峰不会超过赋值的范围。如果杂质峰超过赋值的范围,可能属于以下原因:① 配置对照品溶液的容器或溶剂被污染;② 盛放流动相的容器或配置溶剂被污染;③ 进样器被污染;④ 高效液相进样阀被污染;⑤ 色谱柱填充物出现断裂等。
在检测注射用甲磺酸左氧氟沙星含量时:中间体检测时用紫外检测,成品用的是高效液相检测,之前中间体用原料做工作对照,对照品A值一般在所配浓度下一般为0.39左右,F值在1.26左右,成品没什么问题,可是现在用中检所的对照品,中间体测定时对照品在相同浓度下A值才有0.35左右,这样的话F值就接近1.3了,结果含量就会高很多甚至不合格,但是成品上液相时又是合格的,也就是说对照品应该没问题,是不是中检所的对照品不适合用紫外分光光度法来检测呢?请各位帮忙分析分析,谢谢!!!补充:在这之前,该产品中间体检测都是用中检所的对照品上高效液相测定的,为了节省时间改用了紫外分光光度法检测工艺没改,液相测出来接过肯定会更精确些,但是奇怪的是,同样的对照品中间体检测超标,成品检测合格,不过之前用原料做工作对照检中间体时,成品标示量一般在100%以下,用中检所对照品检测中间体,成品标示量一般在105%,规定上限是110%没我是在想我们的中间体检测方法是不是不太合理制药工艺中没有纯化过程的,但是原料工作对照77.54%,中检所对照品97.3%,都是根据所需浓度换算好了再配制检测的,我是想应该里面所含杂质吸收影响就不明显了吧?您觉得呢?
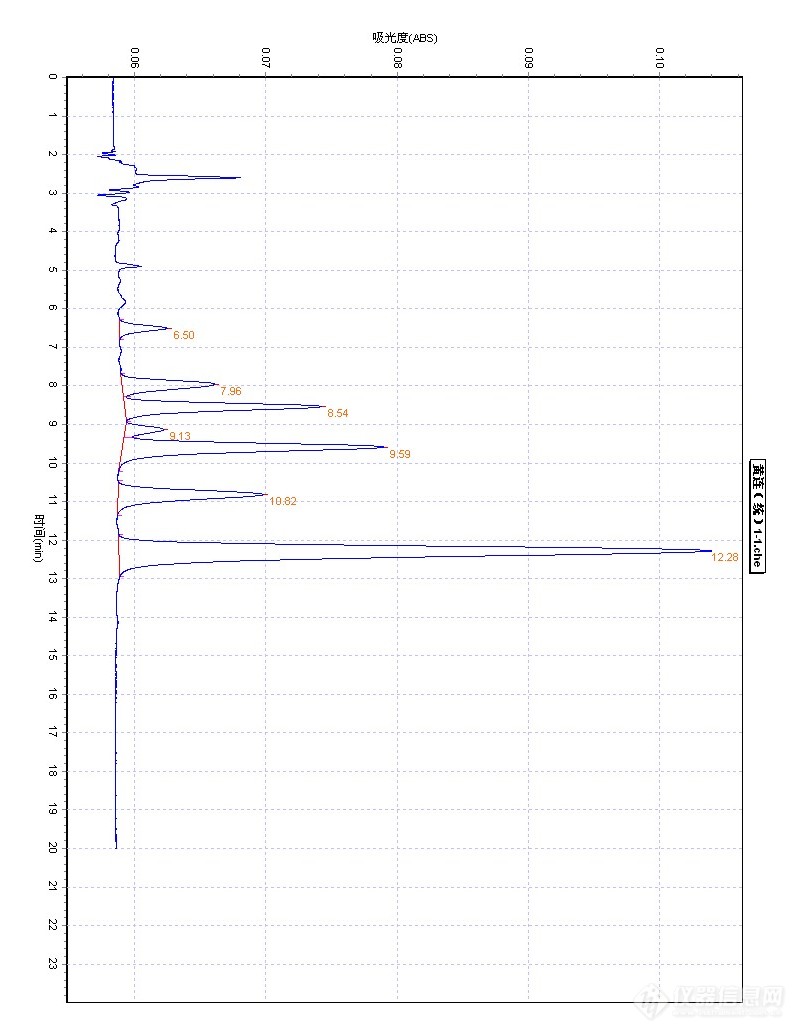
这么多的峰怎么区分表小檗碱、黄连碱、巴马汀、小檗碱的峰位???[img=,690,893]https://ng1.17img.cn/bbsfiles/images/2019/09/201909021342419590_7849_1853141_3.jpg!w690x893.jpg[/img]
对照品:用于鉴别、检查、含量测定和校正检定仪器性能的标准物质;对照品由国家药品检定机构审查认可,其标准应不低于制品的质量标准。 标准品:用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示。 对照品与标准品概念不清?对照品与标准品是2个不同的概念,中国药典凡例中已有明确的定义:对照品系指用于鉴别、检查、含量测定和校正检定仪器性能的标准物质。标准品:用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示。文献中常将2种概念混淆,认为对照品就是标准品,是1种物质2种提法而已,造成错误的原因,可能是有的药品既有对照品,又有标准品。 例如:当用微生物法测定头孢克罗效价时,用头孢克罗标准品,用HPLC或UV法测定时,则用对照品;非那西丁当用作熔点校准物质时,用熔点标准品,测定含量时,用对照品。即使是同一种物质的标准品和对照品,它们的规格、标定方法以及用途都可能是不同的。
最近公司要采购中检所出的对照品,不知道从哪里购买?公司要求如果是从经销商购买需要经销商提供药检所的授权书,和检验报告,但是经询问经销商证书和报告都没有,那我怎么证明对照品就是药检所出的, 如果是我们做认证用,我们怎么证明这东西的来源?没有报告没有授权书似乎这东西没有说服力。 如果直接从药检所购买,似乎也很困难,服务差不说,还要托熟人帮忙购买,否则钱打过去都没人理,经销商说药检所都不乐意做生意,遇到这种情况我该怎么办呢?希望大家给出出主意!
TLC级别的对照品可以用于液相的检验吗?我们检验用的对照品都是TLC级别的,但现在做出来含量超过100%,可能是对照品的问题?
实验室做方法转移的时候是用了A和B品牌的对照品,某一次检测时,这两个品牌的都没有了,又用了C品牌的对照品,这样有什么风险吗?更换检测用对照品需要发变更吗?
[color=#333333]对照品与标准品概念[/color][color=#333333]对照品与标准品是2个不同的概念,中国药典凡例中已有明确的定义:对照品系指用于鉴别、检查、含量测定和校正检定仪器性能的标准物质,而标准品系指用于生物检定、抗生素或生物药品中含量或效价测定的标准物质,以效价单位(U)表示.文献中常将2种概念混淆,认为对照品就是标准品,是1种物质2种提法而已[1,2],造成错误的原因,可能是有的药品既有对照品,又有标准品.例如,当用微生物法测定头孢克罗效价时,用头孢克罗标准品,用HPLC或UV法测定时,则用对照品;非那西丁当用作熔点校准物质时,用熔点标准品,测定含量时,用对照品.即使是同一种物质的标准品和对照品,它们的规格、标定方法以及用途都可能是不同的.[/color]