根据《中华人民共和国工业和信息化部公告》2013年第71号,《润肤膏霜》、《护发素》、《爽身粉、祛痱粉》、《化妆品中黄芩苷的测定高效液相色谱法》4项化妆品行业标准已发布,现将标准相关信息予以公布,请各单位抓紧做好标准实施前的准备工作。附件:3项新发布的化妆品标准一览表序号标准编号标准名称标准主要内容代替标准采标情况实施日期1QB/T 1857-2013润肤膏霜本标准规定了润肤膏霜的分类、要求、试验方法、检验规则及标志、包装、运输、贮存、保质期。本标准适用于滋润人体皮肤(或以滋润人体皮肤为主兼具修饰作用)的具有一定稠度的乳化型膏霜。QB/T 1857-20042014-07-012QB/T 1975-2013护发素本标准规定了护发素的分类、要求、试验方法、检验规则及标志、包装、运输、贮存和保质期。本标准适用于由抗静电剂、柔软剂和各种护发剂等原料配制而成,用于保护头发、使头发有光泽,易于梳理的乳液状或膏霜状护发产品。QB/T 1975-2004QB/T 2835-20062014-07-013QB/T 1859-2013爽身粉、祛痱粉本标准规定了爽身粉、祛痱粉的术语和定义、分类、要求、试验方法、检验规则和标志、包装、运输、贮存、保质期。本标准适用于以粉体原料为基质,添加其他辅料成分配制而成的爽身粉、祛痱粉。QB/T 1859-20042014-07-014QB/T 4617-2013化妆品中黄芩苷的测定 高效液相色谱法本标准规定了用高效液相色谱法测定化妆品中黄芩苷的含量。本标准适用于水剂、乳剂化妆品中黄芩苷的测定。本方法黄芩苷的检出限、定量下限分别为10.0 mg/kg、30.0 mg/kg。使用固相萃取时检出限、定量下限分别为3.0 mg/kg、10.0 mg/kg[fo
[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相[/color][/url]测复方中黄芩苷和天麻素含量,在做混标标曲的时候,天麻素用甲醇作溶剂跑标准品,该成分峰前面会连有一个小包,怀疑是溶剂效应,换了50%甲醇溶解后,峰形改善且小峰消失;黄芩苷含量用50%甲醇溶解后会析出,此时浓度约500ug/ml,稀释后也无法溶解,超声或升温都尝试过,但文献和药典均有用50%甲醇配制,我想尝试用相同溶剂溶解天麻素和黄芩苷,但好像无法兼得,请问有什么好的办法吗?
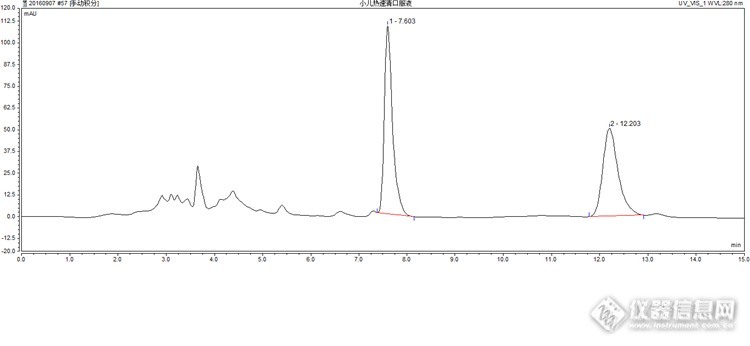
小儿热速清口服液,中成药名。为清热剂,具有清热解毒,泻火利咽之功效。主治小儿外感风热所致的感冒,症见发热、头痛、咽喉肿痛、鼻塞流涕、咳嗽、大便干结。由柴胡、黄芩、板蓝根、葛根、金银花、水牛角、连翘、大黄组成。方中柴胡疏散退热;黄芩清热袪火,袪上焦热毒;板蓝根清热解毒,凉血利咽;葛根发汗解表,助柴胡解肌退热;水牛角苦咸性寒,清热凉血解毒,寒而不遏,且能散瘀;金银花、连翘清热解毒,清宣透邪,使营分之邪透出气分而解;大黄清热解毒,泻下攻积,釜底抽薪。全方共奏清热解毒,泻火利咽之功。目前2015版药典中测定小儿热速清口服液黄芩苷是通过大孔树脂来分离,过程较为繁琐。为此,我们探索出了一种简便的方法来测定其中的黄芩苷,结果证实方法稳定可靠!1. 仪器与试药1.1仪器Ultimate 3000 高效液相色谱仪(赛默飞公司,DAD检测器)、KQ-250B超声波清洗器(昆山市超声仪器有限公司)1.2 试药黄芩苷对照品购于中国食品药品检定研究院,批号:110715-201117,纯度91.7%甲醇为色谱纯,其余为分析纯,水位重蒸水。2. 方法与结果2.1 对照品溶液的制备:精密称取黄芩苷对照品,加甲醇制成每1ml 约含0.1mg的溶液。2.2 供试品溶液的制备:精密量取小儿热速清口服液3Ml,置于50ml量瓶中,加入50%甲醇适量,超声处理20min,,放冷,用50%甲醇补足至刻度,摇匀,即得。2.3色谱条件:色谱柱:Phenomennex Luna C18 (250mm×.4.6mm.×5um)流动相:甲醇-0.2%磷酸水=40:60检测波长:280nm柱温:35℃2.4系统适用性试验考察分别精密吸取对照品溶液2ul、4ul、6ul、8ul、10ul以及样品溶液按2.3项下的色谱条件进行测定,记录色谱图,发现黄芩苷与其他成分完全分开,色谱峰的分离度大于1.5。2.5 线性关系考察分别精密吸取2ul、4ul、6ul、8ul、10ul按2.3项下注入液相色谱仪,以对应色谱峰面积为纵坐标,浓度为纵坐标,绘制标准曲线,得回归方程,y=42.699x+0.140,r=0.9998,结果表明黄芩苷在0.2164ug-1.0820ug之间线性关系良好。2.6精密度试验取对照品溶液进样,连续进样 5 次,得黄芩苷对照品面积RSD为0.67%,表明精密度良好。2.7稳定性试验,取按2.2项下制备的供试品溶液,分别与配制后的0、2、6、8、10、12、24h按2.3项下测定供试品中的黄芩苷的面积,结果表明峰面积的RSD为0.82%,表明供试品溶液在24h稳定。2.8重复性试验按2.2项下制备6份供试品溶液,按2.3项下进行测定,结果样品中黄芩苷含量分别为3.02mg/ml,3.08 mg/ml,3.06 mg/ml,3.04 mg/ml,3.03mg/ml,3.01mg/ml,RSD为0.68%,表明该测定方法重复性较好。2.9 加样回收率试验精密量取6份供试品取1ml,分别精密加入对照品适量,按2,.2方法项下制备6份供试品溶液,按2.3项下进行测定计算黄芩苷的平均回收率和RSD。结果黄芩苷的平均回收率为98.5%,RSD为1.43%2.10 样品测定见表1 样品黄芩苷含量(mg/ml)13.0223.1333.2443.0953.1163.04http://ng1.17img.cn/bbsfiles/images/2016/09/201609190821_610555_1839779_3.png 图1 黄芩苷对照品的HPLC图http://ng1.17img.cn/bbsfiles/images/2016/09/201609190821_610556_1839779_3.png 图2 小儿热速清口服液的HPLC图3小结与讨论:3.1 本文采用超声提取方法,改进了药典中小儿热速清口服液黄芩苷测定方法,结果表明改进的方法提取效率较高,方法稳定、可靠。3.2 本文比较了甲醇-水-磷酸,乙腈-水,甲醇-水系统,结果表明甲醇-0.2%磷酸进行分析效果较好,基线平稳,分离度较好.
大家都用那些容积配置过黄芩苷对照品啊?怎么我们用稀乙醇溶液溶解的时候不易溶解啊,超声半小时还会有很多不容物?
我现在在做HPLC法检测黄芩素组织分布,需要用内标,我选的是白杨素,黄芩素出峰时间是8min,白杨素出峰时间14min,请问从出峰时间来看,选用白杨素做内标合理吗?谢谢!
[size=15px]黄芩根为清热解毒的常用中药,从其中分离出的化合物有黄芩苷(含4.0-5.3%)、黄芩素、汉黄芩苷、汉黄芩素、木蝴蝶素A、黄芩黄酮Ⅰ、黄芩黄酮Ⅱ等。其中,黄芩苷是主要有效成分,具有清热、泻火、抗菌、消炎、退黄疸和降转氨酶作用,是中药“银黄片”的主要成分,现已应用于临床作为治疗急性、迁延性和慢性肝炎的药物。黄芩苷元磷酸脂钠盐可以用于治疗过敏、哮喘等疾病。 [/size][size=15px]黄芩苷为淡黄色针晶,熔点223℃,微溶于热冰乙酸,难溶于甲醇、乙醇、丙酮,几乎不溶于水、乙醚、苯和氯仿。黄芩苷有羧基,呈酸性,故可溶于碳酸氢钠、碳酸钠和氢氧化钠等碱性溶液中,在碱液中初显黄色,然后逐渐变为暗棕色。[/size][size=15px]黄芩素为黄色针晶,熔点264-265℃,易溶于甲醇、乙醇、丙酮、乙酸乙酯,微溶于乙醚、氯仿,较难溶于苯。黄芩素分子中具有邻三酚羟基,易被氧化转为醌类衍生物而显绿色,这是保存或炮制不当的黄芩呈绿色的原因。黄芩变绿色后,有效成分受到破坏,质量随之降低。 [/size][size=15px]黄芩苷和汉黄芩苷都是C7位上羟基与葡萄糖醛酸结合的苷,分子中有羧基,酸性较强,在植物中多以镁盐的形式存在,所以能用沸水作为溶剂提取,然后在提取液中加酸酸化,使黄芩苷(总黄酮)析出。 [/size][align=center] [/align]
根据国家药典委员会官方网站发布的2015药典“灯盏花素片”公示方法,迪马科技率先进行了此项目的检测,详细应用如下:灯盏花素片中野黄芩苷色谱柱:Diamonsil Plus 5 μm C18, 250 x 4.6 mm流动相:乙腈: 1% 冰醋酸= 20:80流速:1.0 mL/min柱温:30 ℃检测器:UV 335 nm进样量:10 μL对照品溶液http://mmbiz.qpic.cn/mmbiz/sZguaRbQouv2HerhsR5EcrFIEicAd5N1Fzv2psc2UpqhhuibITLiaXia533ZudbBEVY09HStfAV1hQgyYfAdicibqzlw/640?tp=webp&wxfrom=5药典要求理论塔板数按野黄芩苷峰计算应不低于4000,而Diamonsil Plus C18 检测的理论塔板数为9874.567,高出药典要求。供试品溶液http://mmbiz.qpic.cn/mmbiz/sZguaRbQouv2HerhsR5EcrFIEicAd5N1FBFVPCOwbT8iaI230IJsUnMHusibB0qd4WDrUqfuPIdhluSw8e9pGAOVA/640?tp=webp&wxfrom=5药典要求理论塔板数按野黄芩苷峰计算应不低于4000,而Diamonsil Plus C18 检测的理论塔板数为9425.165,也高出药典要求。
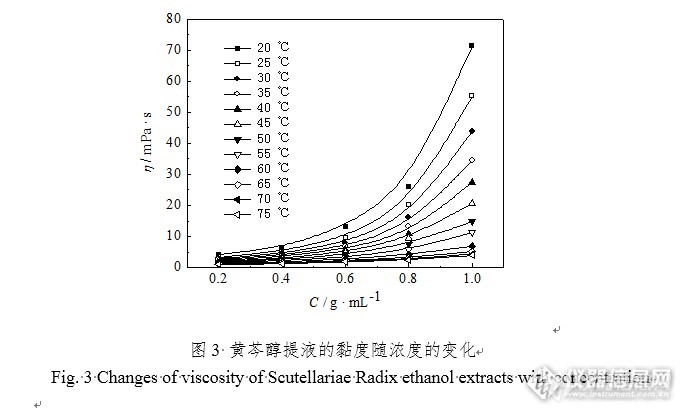
前言 黄芩是唇形科植物黄芩(Scutellariabaicalensis Georgi.)的干燥根,首载于《神农本草经》。味苦性寒,入肺、胆、胃、大肠诸经,能清热燥湿,泻火解毒,凉血止血,安胎。临床常用来治疗肺热咳嗽、目赤肿痛、血热吐衄、湿热泻痢、黄疸、痈疮肿毒、胎动不安等。黄芩的主要有效成分为:黄芩苷(baicalin)、汉黄芩苷(wogonoside)、黄芩素(baicalein)、汉黄芩素(wogonin)。现代药理研究发现,黄芩具有抗氧化、抗炎抗病毒、抗肿瘤、阻止钙离子通道、抑制醛糖还原酶、抗过敏等作用,对免疫、心脑血管、消化、神经等系统均有保护作用。黄芩及其提取物在中药制剂中应用广泛,如固体制剂木香理气片、牛黄上清片、清热止咳颗粒等,液体制剂柴黄口服液、银黄口服液、双黄芩口服液等。 黄芩常用的提取方法有煎煮法、回流提取法、超声提取法、微波提取法、酶提取法、半仿生提取法等。本实验采用回流提取的方法进行黄芩提取液的制备,用旋转蒸发仪进行减压浓缩。1实验部分1.1仪器及试药1.1.1仪器RE-2000A旋转蒸发器(上海亚荣生化仪器厂);密度计(燕河仪器仪表有限公司);NDJ-5S旋转黏度计(上海伦捷机电仪表有限公司);DRE-2A导热系数测试仪(湘潭市仪器仪表有限公司)。1.1.2试药黄芩片(北京同仁堂健康药业股份有限公司),经北京中医药大学刘春生教授鉴定符合2010版《中国药典》的要求;乙醇(95%),分析纯,北京化工厂;去离子水,自制。1.2样品的制备1.2.1不同浓度黄芩水提液的制备 分别称取30、60、90、120、150 g黄芩片,加入8倍量的水,加热回流提取3次,每次1 h,过滤,合并滤液。将滤液分别浓缩至150 mL,得到含生药质量浓度分别为0.2、0.4、0.6、0.8、1.0 g/mL的黄芩水提液。(黄芩中的黄芩苷酶在冷水中可使黄芩苷分解,故第一次提取需将水煮沸后再加入黄芩片以杀酶保苷。)1.2.2不同浓度黄芩醇提液的制备 分别称取30、60、90、120、150 g黄芩片,加入10倍量体积分数为60%的乙醇,加热回流提取3次,每次1 h,过滤,合并滤液。将滤液分别减压浓缩至稠膏状,用60%乙醇少量多次溶解洗出,再加60%乙醇至150 mL,得到含生药质量浓度分别为0.2、0.4、0.6、0.8、1.0 g/mL的黄芩醇提液。1.3物性参数的测定方法 用浮子式密度计在20°C下测量各浓缩液的密度;在20~75°C下,用NDJ-5S型数显旋转黏度计分别测定不同浓度黄芩水提液和醇提液的黏度;采用DRE-2A型导热系数测试仪在20~70°C下分别测定不同浓度黄芩水提液和醇提液的导热系数。1.4分析方法 采用Excel对实验数据进行一元线性回归分析(ρ-C、η-C、η-T、λ-C、λ-T);采用1stOpt数据分析软件进行二元非线性拟合(η-C-T);采用SPSS数据分析软件进行二元线性回归(λ-C-T)。2结果与讨论2.1密度与浓度的关系 测定不同浓度的黄芩水提液和黄芩醇提液密度(表1),以线性回归分别考察其密度与浓度的关系(图1)。黄芩水提液密度与浓度关系的回归方程为ρ = 0.1582C + 1.0043,线性相关系数r = 0.9970;醇提液密度与浓度关系的回归方程为ρ = 0.1839C + 0.9072,线性相关系数r = 0.9995。结果表明,提取液的浓度与密度呈正相关,提取液浓度越高,提取液密度越大,二者具有良好的直线回归关系。http://ng1.17img.cn/bbsfiles/images/2015/09/201509272154_568164_1255490_3.jpg 表1-1 不同浓度黄芩提取液的密度(20°C) (g/cm3)Table 1-1 The density of Scutellariae Radix extracts(20°C) (g/cm3) 浓度C / g·mL-1 黄芩水提液 黄芩醇提液 0 0.9982 0.9094 0.2 1.0415 0.9405 0.4 1.0695 0.9815 0.6 1.0990 1.0170 0.8 1.1345 1.0560 1.0 1.1580 1.0905 2.2黏度与浓度、温度的关系不同温度下,测定不同浓度黄芩水提液的黏度,结果见表2;不同温度下,测定不同浓度黄芩醇提液的黏度,结果见表3。 表2不同温度下不同浓度黄芩水提液的黏度(mPa·s)Table 2 The viscosity of Scutellariae Radix water extracts(mPa·s) 温度T /°C 浓度C / g·mL-1 水 0.2 0.4 0.6 0.8 1.0 20 1.01 2.96 7.39 20.1 56.0 124.7 25 0.89 2.

黄芩提取物-黄芩苷的测定http://ng1.17img.cn/bbsfiles/images/2012/12/201212091347_411149_2369266_3.jpg http://ng1.17img.cn/bbsfiles/images/2012/12/201212091349_411153_2369266_3.jpg 黄芩茎叶 http://ng1.17img.cn/bbsfiles/images/2012/12/201212091348_411151_2369266_3.jpg http://ng1.17img.cn/bbsfiles/images/2012/12/201212091350_411154_2369266_3.jpg黄芩根部http://ng1.17img.cn/bbsfiles/images/2012/12/201212091350_411155_2369266_3.jpg黄芩提取物-黄芩苷黄芩提取物-黄芩苷C21H18O11446.37黄芩苷药理作用:⑴抗炎抗变态反应,黄芩甙、黄芩甙对豚鼠离体气管过敏性收缩及整体动物过敏性气喘,均有缓解作用;⑵抗病毒、抗微生物(菌)作用;⑶镇静、解热、解痉作用;⑷抗癌、降压、利尿作用;⑸对血脂及血糖上升的作用;⑹利胆、保肝作用;⑺可降低乙醇所致的甘油三酸酯水平等。实验室测定方法名称:黄芩提取物-黄芩苷的测定-高效液相色谱法应用范围:本方法采用高效液相色谱法测定黄芩提取物中黄芩苷的含量。本方法适用于黄芩经加工制成的提取物。方法原理:本品加甲醇溶解、稀释,摇匀,滤过,续滤液进入高效液相色谱仪进行色谱分离,用紫外吸收检测器,于波长280nm处检测黄芩苷的吸收值,计算出其含量。试剂:1.甲醇2.磷酸仪器设备:高效液相色谱仪(配带紫外检测器)色谱条件:1.色谱柱:Xtimate C18柱2.流动相:甲醇 水 磷酸 =47 53 0.23.流速:1.0ml/min4.检测波长:280nm5.柱温:室温样品的制备:1.对照品溶液的制备精密称取黄芩苷对照品适量
求助各位大侠!我现在在做黄芩素的液相分析,用的Agilent 1100,色谱柱TC C18(250mm×4.6mm),柱温40C,流动相=甲醇:0.2%甲酸=60:40,流速1ml/min,检测波长276nm,但是我的结果在11分钟左右出峰,但是峰宽竟然达到5min,半峰宽2.3min,请问这是怎么回事?另外我看药典用的流动相是甲醇:水:磷酸=53:47:0.2,磷酸0.2那么pH会低于2,超出了TC柱的pH范围,但是我看到好多人都用这个流动相和TC柱,请问这是怎么回事?谢谢大家!
今天做感冒止咳糖浆中黄芩苷含量测定时碰到了难题色谱条件:岛津10A的机子,N2000工作站,流动相是甲醇:水:磷酸(35:65:0.3),检测波长280nm,理论板不少于3000。对照品配制:取黄芩苷对照品适量,加50%甲醇制成每1ml含15ug的溶液。 供试品制备:精密量取1ml,置50ml容量瓶中,加50%的甲醇至刻度,摇匀,过滤即得。 供和对各进10ul。问题出现:第一针对照品,跑了一小时,没任何峰出现,就是基线。 第二针对照品,我把波长调到278,保留时间为22.998时出峰,不过峰形难看,而且理论板数只有600多。。。 第三针对照品,把波长调到276(因为之前我测黄芩药材黄芩苷含量时用的波长就是276),但保留时间变成31.082???理论板数同2针 第四针对照品,把波长调到279,保留时间为34.673??理论板数同2针 第五针对照品,把波长再调至276,保留时间为22.948??理论板数同2针我昨天做了样品,系统应该是没问题的,对照品溶液也是新配的!!!问题1:为什么按照药典标准的波长测定无任何峰出现(当然进样也没问题)?问题2:为什么改变波长会造成保留时间改变这么多?问题3:为什么柱效这么差?(我用的柱子才用2星期,而且之前所做的样品柱效都不错)现在都没法做下去了,到底是哪些方面的问题???大家帮忙看看!!!http://simg.instrument.com.cn/bbs/images/brow/em09509.gif

问题:迪马科技哪几款色谱柱可满足2015中国药典灯盏花素片中野黄芩苷的检测?答案:Leapsil C18、Platisil ODS【活动奖励】幸运奖(2钻石币):dahua1981(注册ID:dahua1981)——6楼吕梁山(注册ID:shih20j07)——沙发大川之子,纵横四海(注册ID:chuangu120)——7楼http://ng1.17img.cn/bbsfiles/images/2015/11/201511181559_574214_1610895_3.jpghttp://ng1.17img.cn/bbsfiles/images/2015/11/201511181559_574215_1610895_3.jpg积分奖励:所有回答正确的版友奖励10个积分(幸运奖获得者除外)。【注意事项】同样的答案,每人只能发一次PS:该贴浏览权限为“回贴仅作者和自己可见”,回复的版友仅能看到版主的题目及自己的回答内容,无法看到其他版友的回复内容。下午3点之后解除,即可看到正确答案、获奖情况及所有版友的回复内容。=======================================================================灯盏花素片中野黄芩苷的检测样品制备 制备方法1. 对照品:取野黄芩苷对照品适量,精密称定加甲醇制成每1 mL含20 μg的溶液,即得。2. 供试品:取本品10片,精密称定,研细,精密称取适量(约相当于灯盏花素30 mg),置50 mL量瓶中,加甲醇适量超声处理(功率250 W,频率40 kHz)30分钟,放冷,加甲醇至刻度,摇匀,滤过,精密量取续液1 mL,置25 mL量瓶中,加甲醇至刻度,摇匀,即得。分析条件 色谱柱Platisil ODS 250 x 4.6 mm,5 μm (Cat#:99503)流动相乙腈:1% 冰醋酸=20:80流速1.0 mL/min柱温30 ℃检测器UV 335 nm 进样量10 μL色谱图对照品 http://ng1.17img.cn/bbsfiles/images/2015/11/201511181006_574036_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 16.151 591739 30112 15651.800 1.008 — *药典要求理论板数按野黄芩苷峰计算应不低于4000供试品http://ng1.17img.cn/bbsfiles/images/2015/11/201511181006_574039_1610895_3.jpg 峰号 保留时间 min 峰面积 μV*s 峰高 μV 理论塔板数* N USP拖尾因子 分离度 1 16.058 636165 32070 15604.684 0.999 -- *药典要求理论板数按野黄芩苷峰计算应不低于4000本品种同时使用了Leapsil C18色谱柱,在药典规定条件下进行野黄芩苷的检测,满足药典要求。
各位大侠,我在做中药银黄片中黄芩苷含量测定时,做出来含量挺高,但有抽检到说含量不够标准,有两批都是。我们化验室复检过好几次,专门买的新对照品进行复检都合格,请教各位能否指点一二。具体做法如下:色谱条件与系统适应性试验 以十八烷基硅烷键合硅胶为填剂;以甲醇-水-磷酸(47:53:0.2)为流动相;检测波长为280nm。理论板数按黄芩苷峰计算应不低于2500。对照品溶液的制备 精密称取在60℃减压干燥4小时的黄芩苷对照品适量,加甲醇制成每1ml含60ug的溶液,即得。供试品溶液的制备 取本品10片,除去糖衣,研细,取约0.1g,精密称定,置具塞锥形瓶中,精密加入70%甲醇50ml,称定重量,超声处理(功率250W,频率40kHz)30分钟,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,精密量取续滤液1ml,置5ml容量瓶中,加70%甲醇至刻度,摇匀,滤过,取续滤液即得。测定法 分别精密吸取对照品溶液与供试品溶液各10ul,注入液相色谱仪,测定,即得。
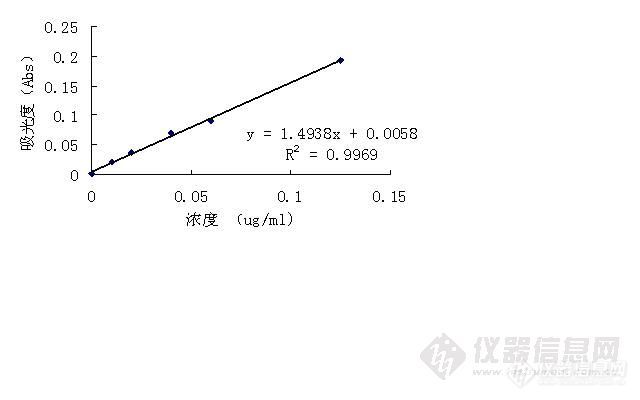
维权声明:本文为qweaxi原创作品,本作者与仪器信息网是该作品合法使用者,该作品暂不对外授权转载。其他任何网站、组织、单位或个人等将该作品在本站以外的任何媒体任何形式出现均属侵权违法行为,我们将追究法律责任。【摘要】 目的:测定黄芩中镉和铅的含量。方法:采用石墨炉原子分光光度法测定含量。结果:镉标准品在0.000~0.010 µg/ml范围内线性关系良好(r=0.9980);铅标准品在0.000 µg/ml~0.125 µg/ml范围内线性关系良好(r=0.9984)。结论:通过研究三组施含有光合细菌的药材和对照药材所得数据分析,施含有光合细菌肥料的药材和对照药材重金属含量有一定差异,具体表现为:喷洒光合细菌的药材比对照药材重金属含量少。【关键词】 黄芩;含量测定;原子分光光度法;镉;铅1.引 言http://ng1.17img.cn/bbsfiles/images/2010/11/201011231531_261517_2160429_3.jpg中药黄芩是唇形科植物黄芩(Scutellaria baicalensis Georg)的干燥根,本品呈圆锥形,扭曲,长8~25cm,直径1~3cm。表面棕黄色或深黄色,有稀疏的疣状细根痕,上部较粗糙,有扭曲的纵皱或不规则的网纹,下部有顺纹和细皱。质硬而脆,易折断,断面黄色,中间红棕色;老根中间呈暗棕色或棕黑色,枯朽状或已成空洞。气微,味苦。【性味与归经】苦,寒。归肺、胆、脾、大肠、小肠经,【功能与主治】清热燥湿,泻火解毒,止血,安胎。用于湿温、暑温胸闷呕恶,湿热痞满,泻痢,黄疸,肺热咳嗽,高热烦渴,血热吐衄,痈肿疮毒,胎动不安。首载于《神农本草经》。《纲目》:洁古张氏言黄芩泻肺火,洽脾湿;东垣李氏言片芩治肺火,条芩治大肠火;丹溪朱氏言黄芩治上中二焦火;而张仲景治少阳证小柴胡汤,太阳、少阳合病下利黄芩汤,少阳证下后心下满而不痛:泻心汤并用之;成无己言黄芩苦而入乙,泄痞热,是黄芩能入手少阴、阳明、手足太阴、少阳六经矣。盖黄苹气寒味苦,苦入乙,寒胜热,泻心火,治脾之湿热,一则金不受刑,一则胃火不流入肺,即所以救肺也:肺虚不宜者,苦寒伤脾胃,损其母也。杨士瀛《直指方》云,柴胡退热,不及黄芩,盖亦不知柴胡之退热,乃音以发之,散火之标也,黄尊之热,乃寒能胜热,拆火之本也。黄芩得酒上行,得猪胆汁除肝胆热,得柴胡退寒热,得芍药治下痢,得桑白皮泻肺火,得白术安胎。 《滇南本草》:上行泻肺火,下行泻膀胱火,(治)男子五淋,女子暴崩,调经清热,胎有火热不安,清胎热,除六经实火实热。洪志强做的黄芩的质量标准研究和指纹图谱。中药铅、镉因其取自于天然而日益成为世界各国广泛推崇的药物品种。如今中药在世界各地的声誉和影响越来越大,对中药的需求也不断增加,人们不仅对中药的治疗、保健作用给予了广泛关注,也逐渐开始重视中药不良反应。由于中药材其种类的自身特点,都含有一定量的重金属等有害元素,如铅(Pb)、镉(Cd)、砷(As)、银(Ag)、汞(Hg)、锡(Sn)等,同时近年来我国中药材受到有害重金属元素的严重污染,中药材质量下降。重金属含量超标成为中药不良反应中最突出的问题之一,已严重影响到中药的声誉及出口。现代科学已证明了重金属残留能够进入人体并与酶蛋白牢固结合,导致组织细胞出现结构和功能上的损害。其中尤以铅和镉含量超标最为普遍。黄芩在临床上,清热燥湿,泻火解毒,止血安胎等功效。用量大,用药广堪称中成药之最,特别是现代人们生活习惯的改变湿热病更常见,因此这种广泛应中药更应该重视其重金属含量。 光合细菌是水生圈微生物的一类,广泛分布在水田、池塘、湖泊等各个角落,可进行光合成、有氧呼吸、发酵,具有固氮、固碳、放氢等生理功能,促进有益共生菌的增殖,有抑制病原菌的能力,可有效降解土壤中的残留农药、H2S、过剩氨氮等,无污染无公害,净化土壤促进根系发育,是良好的土壤调节剂。其营养成分丰富,含有多种生物活性物质,具有独特的生物转化功能,且能把一些有害有毒物质转化成具有营养价值的无害物质和营养元素供作物利用,从而改善了植物的营养状况。因此,光合细菌具有广阔的应用前景。实验部分2[font
配制两个黄芩苷对照品溶液第一个是用50%的甲醇溶解,我感觉这个好难溶,超声了也不见得全部溶解,如果全部溶解配制出来的应该是澄清的吧?该如何处理好呢??第二个要用减压干燥器60度干燥4小时再配制,我觉得涂了凡士林在60度会溶了吧,就不能减压了,我可以直接打开对照品瓶盖直接在烘箱里烘4小时不?这样做会有很大的影响吗?
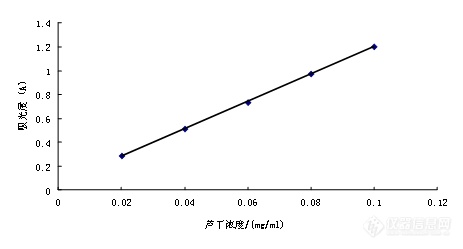
[align=center]从黄芩中提取黄酮类化合物的工艺研究[/align][align=center]西安国联质量检测技术股份有限公司[/align][align=center]食品事业部:李灿[/align][b]摘要:[/b]探讨超声波辅助法提取黄芩中总黄酮的最佳提取条件及对提取物的抗氧化性活性研究,这为黄芩作为天然抗氧化剂和功能性食品的开发利用提供理论基础和实验依据。[b][/b] 通过设计正交试验,采用超声波辅助法提取黄芩中总黄酮的最佳工艺条件条件,并通过对羟自由基、超氧自由基和DPPH自由基的清除效果研究其抗氧化活性。[b][/b]超声波辅助提取黄芩中总黄酮的最佳条件为:乙醇浓度为50%,时间为25min,料液比为1∶10,温度为30℃,黄芩总黄酮的提取率为3.25%。并且研究了黄芩提取物中的黄酮类物质对O[sub]2[/sub]-• 、• OH和DPPH自由基的抗氧化性能。研究结果表明洋葱提取物中黄酮类物质的抗氧化性较VC强。在浓度为0.0125mg/ml下,对羟基自由基的清除率为88.30%,对超氧基自由基的清除率为90.01%,对DPPH自由基的清除率为93.87%。[b]关键词[/b]:黄芩;超声波提取;总黄酮;抗氧化活性 [align=center][b] Study on extraction technology of flavonoids from Scutellaria[/b][/align][align=center]Li Can[/align][align=center] (Department of Chemistry and Chemical Engineering, Xi′an University of [/align][align=center]Arts and Science, Xi′an 710065)[/align][b]Abstract: [/b]To investigate the ultrasonic assisted extraction optimum extraction conditions of total flavonoids from Scutellaria and to extract antioxidant activity, which is a skullcap as a natural antioxidant and functional food development and utilization of theoretical and experimental evidence provided . [b][/b] Through orthogonal experiment, the optimum conditions using ultrasonic assisted extraction conditions of total flavonoids from Scutellaria, and to study its antioxidant activity by hydroxyl radicals, superoxide radicals and DPPH radical scavenging effect. Optimal conditions . [b] [/b]Ultrasonic assisted extraction of total flavonoids from Scutellaria: ethanol concentration of 50%, the time is 25min, solid-liquid ratio of 1:10, the temperature is 30 ℃, extraction of total flavonoids was 3.25%. And studied the extract of Scutellaria flavonoids on O2-• , • OH and DPPH radical antioxidant properties. The results show that the onion extract antioxidant flavonoids than VC strong. At a concentration of under 0.0125mg/ml, hydroxyl radical scavenging rate of 88.30% for super-group was 90.01% scavenging of DPPH radical scavenging rate was 93.87%.[b][color=#2b2b2b]Key Words[/color][/b][color=#2b2b2b]:[/color][color=#2b2b2b] [/color][color=#2b2b2b]Skullcap [/color][color=#2b2b2b]U[/color][color=#2b2b2b]ltrasonic extraction [/color][color=#2b2b2b]T[/color][color=#2b2b2b]otal flavonoids [/color][color=#2b2b2b]A[/color][color=#2b2b2b]ntioxidant activity[/color][b]1 前言[/b]黄岑主要生长在陕西秦岭,为常用中草药之一,性寒,味苦。具有清热燥湿,泻火解毒,止血安胎[sup][/sup]等功效,它的主要成分为黄酮类化合物[sup][/sup],黄酮类化合物主要存在于双子叶及裸子植物的叶、果、实、根、皮中,在植物中主要与糖结合成苷的形式存在[sup][/sup]。目前从黄酮类物质有很多种,黄酮类化合物的结构特点是具有 C[sub]6[/sub]- C[sub]3[/sub]- C[sub]6[/sub]的基本骨架,根据中间三碳链的氧化程度、B 环( 苯基) 连接位置( 2-或3-位) 以及三碳链是否呈环状等特点,主要有黄酮醇,二氢黄酮,二氢黄酮醇,黄烷,黄烷醇,异黄酮等,被广泛应用在医药、功能食品添加剂、兽药和农药等领域。在医药方面,根据其在心血管系统、内分泌系统、抗肿瘤方面的药理作用,很多以黄酮类成分为主的制剂已作为成药上市[sup][/sup]。在食品中它们应用于功能性食品添加剂,如天然甜味剂、天然抗氧化剂、天然色素等;应用于功能食品,如生物类黄酮口香糖、银杏叶袋泡茶等防衰、抗癌、提高免疫力食品;在兽药、农药等领域,现已开发出些具有特效功能的含有黄酮类化合物药品和驱虫、杀虫剂等[sup][/sup]。目前国内侧重于对黄酮类化合物的研究,但他们常被当作残渣而扔掉,因而就造成了黄芩的浪费,没有使黄芩得到充分利用,本文主要针对黄芩总黄酮的提取方法及其抗氧化能力测定方法进行研究,以期为黄芩黄酮类成分的进一步开发利用从黄岑中提取黄酮类化合物的方法有很多种,传统提取方法有煎煮法[sup][/sup]、有机溶剂提取法[sup][/sup]、浸渍法、渗漉法、回流提取法[sup][/sup]、水提法等,新的提取方法有超声波提取法、微波提取法、索氏提取法、超临界萃取法、大孔树脂吸附法、酶解法提取[sup][/sup]。黄芩黄酮的提取主要为溶剂萃取法,包括无机溶剂萃取法和有机溶剂萃取法。其主要原理是利用黄芩黄酮能溶于碱水或甲醇等有机溶剂的特性来提取黄芩中的黄酮[sup][/sup],考虑到该法提取时间长,提取率较低的缺点,我们采用超声波辅助提取法。因为超声波提取法是一种新型方法,它具有能耗低、效率高、不破坏有效成分的特点,在低温下可以强化水浸提效率,达到省时高效节能的目的,而且是目前广泛使用的方法。超声提取的主要理论依据是超声的空化效应、热效应和机械作用。当大能量的超声波作用于介质时,介质被撕裂成许多小空穴,这些小空穴瞬时闭合,并产生高达几千个大气压的瞬间压力,即空化现象。超声空化中微小气泡的爆裂会产生极大的压力,使植物细胞壁及整个生物体的破裂在瞬间完成,缩短了破碎时间,同时超声波产生的振动作用加强了胞内物质的释放、扩散和溶解,从而显著提高提取效率。因此本实验拟决定用超声波提取法来提取黄酮类化合物。黄酮类化合物的测定方法也多种多样,目前有薄层扫描法、紫外分光光度法、液相色谱法等[sup][/sup]。但是以上方法测定黄芩提取液中总黄酮的含量都比较繁琐,非黄酮类物质干扰比较大。由于Al[sup]3+[/sup]仅与黄酮类物质有特征反应,使用这种显色方法可以使黄酮类化合物溶液在510nm左右出现吸收峰,采用紫外分光光度法测定黄芩提取液中总黄酮含量,方法简单快速[sup][/sup]。对于黄酮类化合物的抗氧化性研究,国内外所做研究也比较多。方法可分为体外抗氧化与体内抗氧化,其中体外抗氧化运用较为广泛,体外抗氧化还可分为直接清除活性氧自由基、抑制油脂过氧化反应[sup][/sup]等;体内抗氧化是用受试物连续喂饲大鼠或小鼠1个月~3个月,然后处死动物,测定其血或组织(如肝、脑)中各物质的含量,同对照组进行比较,间接地说明受试物的抗氧化活性。采用体外抗氧化性研究,常用到的自由基有OH[sup] [/sup],O[sub]2[/sub][sup]-[/sup], DPPH等,由于直接清除活性自由基的方法易行且效果直观,本次实验采用该种方法。本实验将从两个方面研究黄芩黄酮类化合物。第一部分为黄芩总黄酮最佳提取方法的研究。本环节采取超声辅助提取法,采用料液比(A),乙醇浓度(B), 超声时间(C),超声温度(D)作为研究因素,采用四因素三水平,选择L[sub]9[/sub](3[sup]4[/sup])设计正交试验。用芦丁做标准曲线测定黄芩提取液中总黄酮的含量。第二部分为总黄酮类化合物抗氧化性的研究,采用对OH,O[sub]2[/sub][sup]-[/sup]自由基和DPPH自由基的清除作用研究其抗氧化性。[b]2 实验部分2.1 材料与仪器2.1.1 材料和试剂[/b] 黄芩(购于西安同仁堂大药房),芦丁(分析纯,上海试剂药品厂),亚硝酸钠(分析纯,成都市科龙化工试剂厂),硝酸铝(分析纯,成都市科龙化工试剂厂),氢氧化钠(分析纯,成都市科龙化工试剂厂),邻苯三酚(分析纯,成都市科龙化工试剂厂),盐酸(分析纯,天津市天力化学试剂有限公司),双氧水(天津市天力化学试剂有限公司),硫酸亚铁(分析纯,成都市科龙化工试剂厂),水杨酸(分析纯,天津市天力化学试剂有限公司),无水乙醇(分析纯,天津市天力化学试剂有限公司),三羟基甲基氨基甲烷(分析纯,天津市福晨化学试剂厂),邻二氮菲(分析纯,天津市福晨化学试剂厂),DPPH(购于阿拉丁试剂)。[b]2.1.2 仪器[/b] 高速粉碎机(FW80型,北京中兴伟业仪器有限公司);紫外可见分光光度计(722N,上海精密科学仪器有限公司) 电子天平(YP202W,上海精密科学仪器有限公司);循环水式多用真空泵(SHB-Ⅲ,郑州长城科工贸有限公司);超声波清洗机(11—1404,宁波新芝生物科技股份有限公司);智能型恒温鼓风干燥箱(CMD-20X型,上海琅轩试验设备有限公司);玻璃仪器气流烘干器(TH48SYBQ-1型,北京中兴伟业仪器有限公司)。[b]2.2实验方法2.2.1黄芩样品的制备[/b] 将黄芩在烘箱中60℃干燥8h,干燥后的黄芩用粉碎机粉碎成粉末,用分样筛(40目)筛分黄芩粉末,保证粉末均匀一致,密封保存,待用。[b]2.2.2 总黄酮的测定方法2.2.2.1 芦丁标准曲线的绘制[/b] 准确称取干燥至恒重的芦丁4.0mg 于小烧杯中,用50%乙醇溶解,并定容于25ml的容量瓶,摇匀,得浓度0.16mg/ml的标准液。准确吸取标准应用液0、1.0、2.0、3.0、4.0、5.0ml 于6 个10ml容量瓶中,与上述容量瓶中分别加入5% NaNO[sub]2[/sub]0.3ml,摇匀,放置6min后,分别加入10% Al(NO[sub]3[/sub])[sub]3[/sub] 溶液0.3ml,摇匀,放置6min后,再分别加入4% NaOH 溶液4ml,加50%乙醇定容至10ml,摇匀,以试剂空白为参比,放置10~15min,用紫外可见分光光度计进行全波长扫描,在最大吸收波长510nm处测定吸光度,得到吸光度Y与芦丁浓度X(mg/ml)间标准曲线回归方程。[b]2.2.2.2 提取液总黄酮含量的测定 [/b]准确称取1.00g黄芩粉末,在不同的提取条件下提取黄芩总黄酮,提取液用乙醇稀释定容至50ml。准确吸取提取液1.0ml于25ml容量瓶,按上述方法显色后测定吸光度,代入标准曲线回归方程中可以得到黄芩中黄酮类物质的含量(mg/ml),从而计算出黄芩中黄酮类物质的提取率,即:黄芩中黄酮类物质的提取率= ×100%[b]2.2.3 单因素试验[/b] 主要研究料液比、乙醇浓度、超声波时间、超声波温度4个因素,在保持其他因素相同的条件下分别进行单因素试验,研究各因素对黄芩总黄酮提取效果的影响,筛选最佳的提取条件。 准确称取黄芩粉末,在不同的条件下进行超声提取,提取液冷却后用乙醇定容,按照2.2.2的测定方法,计算黄芩中总黄酮的含量。[b]2.2.4 正交试验[/b]在单因素试验基础上,选择料液比、乙醇浓度、超声时间、超声温度4因素,设计L[sub]9[/sub](3[sup]4[/sup])正交试验,以总黄酮的含量为评价指标,确定黄芩总黄酮超声辅助法的最佳提取工艺。[b]2.2.5 总黄酮体外抗氧化性的研究2.2.5.1 对羟自由基清除作用的研究[sup][/sup][/b]原理:通过反应所产生的羟基自由基可将Fe[sup]2+[/sup]氧化为Fe[sup]3+[/sup], Fe[sup]2+[/sup]和邻二氮菲反应可产生有色络合物,向有色沉淀加入抗氧化剂后,其反应效果会相对减弱。羟基自由基对二价铁离子的氧化作用,会导致吸光值不断变化,从而评价样液消除羟基自由基的能力。步骤:取0.75 mmoL/L邻二氮菲溶液1 mL,加入不同浓度的样液,再加0.75 mmoL/L硫酸亚铁1 mL混匀,加0.75mmol/l的过氧化氢1 mL,于37 ℃ 水浴下,水浴60 min后,在536 nm处测其吸光度,所得吸光度A[sub]b[/sub]。 反应方程式:H[sub]2[/sub]O[sub]2[/sub] + Fe[sup]2+[/sup]=OH[sup]-[/sup] +OH + Fe[sup]3+ [/sup]清除率S(%)=「Ax- A[sub]b[/sub]]/[As- A[sub]b[/sub]] ×100% 其中 A[sub]b[/sub]:标准体系的吸光度 Ax:不含黄芩提取液的吸光度As:不含过氧化氢的标准体系吸光度本底吸光度[b]2.2.5.2 对超氧自由基清除作用的研究 [sup][/sup][/b] 原理:在碱性条件下,邻苯三酚能迅速发生自氧化反应,生成超氧阴离子自由和有色中间产物,且邻苯三酚自氧化速率与生成超氧阴离子自由基的浓度呈正相关,该有色中间产物在300nm处有一特征吸收峰。当加入抗氧化剂能催化超氧阴离子自由基与H[sup]+[/sup]结合生成O[sub]2[/sub]和H[sub]2[/sub]O[sub]2[/sub] ,从而阻止了中间有色产物积累,溶液在320nm 处的吸收减弱。因此可通过测定添加试样前后吸光度[i]A[/i]的变化来表示抗氧化剂对超氧阴离子自由基的清除效果。步骤:取0.05mol/L三羟甲基氨基甲烷盐酸缓冲液(pH =8.2)4.5mL,置于25℃水浴中预热20min,分别加入0.1mL试样和0.4mL2.5mmol/L邻苯三酚溶液,混匀后于25℃水浴中反应4min,加入8mol/L HCl溶液两滴终止反应,于波长299nm处测定吸光度As,空白对照组以相同体积的蒸馏水代替样品,并计算清除率。 清除率计算公式: S(%)=[(1-(As-A[sub]0[/sub] )/A[sub]b[/sub]]×100%其中 A[sub]b[/sub]:不含黄芩提取物的标准体系吸光度 As:标准体系的吸光度值 Ao:不含邻苯三酚的标准体系吸光度[b]2.2.5.3 对DPPH自由基清除作用的研究[sup][/sup] [/b]原理:DPPH 在有机溶液中是一种稳定的自由基,其乙醇溶液呈深紫色,当 DPPH 溶液中加入自由基清除剂时,其孤对电子被配对,溶液颜色变浅,可由此来检测自由基的清楚状况,从而评价物质的抗氧化能力。步骤:将样品储备液适当稀释得到不同浓度的黄芩黄酮溶液。 向一系列 10 mL比色管中加入 3.5 mL 1.0×10[sup]-4[/sup]mol/L 的 DPPH 溶液和 0.5 mL 样品液,摇匀避光反应30 min,与波长517 nm下测定吸光度 A s。空白对照组以无水乙醇代替样品,并计算清除率。清除率计算公式: 清除率S(%)=[(1-(As-A[sub]0[/sub] )/A[sub]b[/sub]]×100% 其中 A[sub]b[/sub]:不含黄芩提取物的标准体系吸光度 A[sub]s[/sub]:标准体系的吸光度值 A[sub]0[/sub]:不含DPPH的标准体系吸光度[b]3. 结果与分析 3.1 芦丁标准曲线[/b]由图可得,芦丁在0.02—0.10mg/ml浓度范围内与吸光度呈良好的线性关系,R[sup]2[/sup]= 0.9998。回归方程为Y= 11.47X+ 0.0554 [align=center]表1 芦丁浓度与吸光度的关系[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]芦丁浓度/(mg/ml)[/align][/td][td][align=center]0.02[/align][/td][td][align=center]0.04[/align][/td][td][align=center]0.06[/align][/td][td][align=center]0.08[/align][/td][td][align=center]0.10[/align][/td][/tr][tr][td][align=center]吸光度(A)[/align][/td][td][align=center]0.288[/align][/td][td][align=center]0.514[/align][/td][td][align=center]0.736[/align][/td][td][align=center]0.976[/align][/td][td][align=center]1.204[/align][/td][/tr][/table][align=center] [/align][align=center] [/align][align=center] [/align][align=center][img=,463,249]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091813421003_7187_2904018_3.png!w463x249.jpg[/img] [/align][align=center]图1 芦丁标准曲[/align]Fig.1 Standard curve of rutin[b]3.2 总黄酮提取条件的优化3.2.1 料液比对黄酮类化合物提取效果的影响[/b]在料液比为1:6,1:8,1:10,1:12,1:14时,50%乙醇作为提取剂,超声波时间为20min,超声波温度为60℃,冷却后采用超声波提取法提取黄芩中黄酮类化合物含量,研究料液比对提取效果的影响。[align=center]表2 料液比与提取率的关系[/align][align=center][img=,394,250]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091815178933_5515_2904018_3.png!w394x250.jpg[/img][/align][align=center] 图2 料液比对黄芩黄酮提取的影响[/align][align=center]Fig.2 Solid-liquid ratio on the extraction of flavonoids from Scutellaria impact[/align]由图2可见,随着料液比的增加,黄酮类化合物的提取率也逐渐升高,当料液比为1:10时,黄酮类化合物的提取率达到最高值,继续增加料液比,提取率会有一定的降低。在一定范围内料液比的增加有利于物料中黄酮类物质的溶出,但料液比过大的时候,会导致溶液浓度太小,从而影响到黄酮类物质对超声波能的吸收,导致黄酮得率下降。因此选定料液比在1:10的条件下进行实验。[b]3.2.2 乙醇浓度对黄酮类化合物提取效果的影响[/b]当乙醇浓度为30%,40%,50%,60%,70%时作为提取剂,超声波时间为20min,超声波温度为60℃,料液比为1:10的条件下,冷却后采用超声波提取法提取液中总黄酮含量,研究料液比对提取效果的影响。结果如图2所示[align=center]表3 乙醇浓度与提取率的关系[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]乙醇浓度(%)[/align][/td][td][align=center]30[/align][/td][td][align=center]40[/align][/td][td][align=center]50[/align][/td][td][align=center]60[/align][/td][td][align=center]70[/align][/td][/tr][tr][td][align=center]提取率(%)[/align][/td][td][align=center]2.08[/align][/td][td][align=center]2.44[/align][/td][td][align=center]3.18[/align][/td][td][align=center]2.15[/align][/td][td][align=center]1.28[/align][/td][/tr][/table][align=center][img=,457,289]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091815413326_3128_2904018_3.png!w457x289.jpg[/img][/align]图3 乙醇浓度对黄芩总黄酮提取的影响[align=center] Fig.3 The effect of ethanol concentration on the extraction of flavonoids from Scutellaria[/align]由图3可见,随着乙醇浓度的增加,黄酮类化合物的提取率逐渐升高,在乙醇浓度为50%时提取率最高,再增加乙醇浓度,提取率逐渐降低。这主要是随着乙醇浓度的增加导致溶液极性的改变,使提取液中杂质含量增加,因此选择50%的乙醇溶液作为提取剂。[b]3.2.3 超声波时间对黄酮类化合物提取效果的影响[/b]当超声波时间为5min,10min,15min,20min,25min,料液比为1:10,乙醇浓度为50%,超声波温度为60℃的条件下,冷却后采用超声波提取法提取液中总黄酮含量,研究料液比对提取效果的影响。[align=center]表4 超声波时间与提取率的关系[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]超声波时间(min)[/align][/td][td][align=center]5[/align][/td][td][align=center]10[/align][/td][td][align=center]15[/align][/td][td][align=center]20[/align][/td][td][align=center]25[/align][/td][/tr][tr][td][align=center]提取率(%)[/align][/td][td][align=center]1.67[/align][/td][td][align=center]1.82[/align][/td][td][align=center]1.93[/align][/td][td][align=center]2.19[/align][/td][td][align=center]2.08[/align][/td][/tr][/table][align=center][img=,420,258]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091815572952_9256_2904018_3.png!w420x258.jpg[/img][/align]图4 超声时间对黄芩总黄酮提取的影响[align=center]Fig.4 Ultrasonic time of total flavonoids extracted[/align]由图4可见,随着超声波时间的延长,黄酮类化合物提取率逐渐升高,在20min时提取率最高,继续延长超声波提取时间提取率几乎不变,主要是因为在初期,黄芩中黄酮类化合物没有完全浸提到溶剂中,而随着时间的增加,黄酮类化合物逐渐完全溶于提取剂中,因此提取率几乎不变。所以选择超声波时间为20min时进行实验。[b]3.2.4 超声波温度对黄酮类化合物提取效果的影响[/b]当超声波温度为20℃,30℃,40℃,50℃,60℃,料液比为1:10,乙醇浓度为50%,超声波时间为20min的条件下,冷却后采用超声波提取法提取液中总黄酮含,研究料液比对提取效果的影响。[align=center]表5 超声波温度与提取率的关系[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]超声波温度(℃)[/align][/td][td][align=center]20[/align][/td][td][align=center]30[/align][/td][td][align=center]40[/align][/td][td][align=center]50[/align][/td][td][align=center]60[/align][/td][/tr][tr][td][align=center]提取率(%)[/align][/td][td][align=center]1.87[/align][/td][td][align=center]2.34[/align][/td][td][align=center]2.44[/align][/td][td][align=center]2.25[/align][/td][td][align=center]2.31[color=#ff0000] [/color][/align][/td][/tr][/table][align=center][img=,360,256]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091816171242_5784_2904018_3.png!w360x256.jpg[/img][/align][align=center] [/align][align=center] [/align]图5 超声温度对黄芩黄酮提取的影响[align=center]Fig.5 Skullcap ultrasonic extraction temperature on impact[/align] 由图5可见,随着超声波温度的升高,黄酮类化合物提取率逐渐升高,在40℃时提取率最高,继续升高超声波提取温度,提取率反而略有下降。高温提取的过程是先使物料升温,保持一定时间后,利用温度使细胞壁破碎,乙醇溶剂溶入细胞内部,黄酮充分溶解,再继续升高温度,反而使更多的杂质释放出来,导致黄酮提取率不再上升。所以选择超声波温度为40℃进行实验。[b]3.3 正交试验确定最佳工艺3.3.1 正交试验结果[/b]通过上述单因素试验,得出各个单因素的最佳条件,其中料液比为1:10,乙醇浓度为50%,超声时间为20min,超声温度为40℃。选择料液比、乙醇浓度、超声波时间、超声波温度4因素3水平,设计L[sub]9[/sub](3[sup]4[/sup])正交试验,因素与水平见表1,试验结果见表2为了进一步判断上述4类因素对试验结果的影响是否存在,将以正交试验数据进行方差分析,找出这些因素中起主导作用的来源。表1 正交试验因素及水平表Tab 1 Factors and levels of the orthogonal tests[table][tr][td=1,2]水平[/td][td] 因素[/td][/tr][tr][td]A B C D料液比(g/ml) 乙醇浓度(%) 超声时间(s) 超声温度(℃)[/td][/tr][tr][td=2,1]1 1:8 40 15 302 1:10 50 20 403 1:12 60 25 50[/td][/tr][/table]表2 正交试验结果及分析 Tab 2 The results and analysis of orthogonal tests [table][tr][td=1,2]试验号[/td][td] 因素[/td][td=1,2]提取量(%)[/td][/tr][tr][td]A B C D料液比(g/ml) 乙醇浓度(%) 超声时间(s) 超声温度(℃)[/td][/tr][tr][td=3,1]1 1:8 40 15 30 2.622 1:8 50 20 40 2.903 1:8 60 25 50 2.764 1:10 50 25 30 3.255 1:10 60 15 40 2.626 1:10 40 20 50 2.507 1:12 60 20 30 2.408 1:12 40 25 40 2.589 1:12 50 15 50 2.85K[sub]1[/sub]/3 2.76 2.57 2.70 2.76K[sub]2[/sub]/3 2.79 3.00 2.60 2.70K[sub]3[/sub]/3 2.61 2.59 2.86 2.70R 0.18 0.43 0.26 0.06[/td][/tr][/table]由表1、2可知,主次因素由极差大小确定:B>C>A>D,即影响黄芩总黄酮提取效率的因素贡献率为乙醇浓度>超声时间>料液比>超声温度。以总黄酮含量为评价指标,得最佳提取工艺条件为A[sub]2[/sub]B[sub]2[/sub]C[sub]3[/sub] D[sub]1[/sub],即乙醇浓度为50%、超声时间为25min、料液比为1∶10、超声温度为30℃。最佳条件为正交表中的第四组,因此测抗氧化性实验选择此组数据。[b]3.4 总黄酮的抗氧化性3.4.1 对羟自由基的清除作用[/b][align=center]表6 提取液浓度对羟基自由基清除率[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]提取液浓度/(mg/ml)[/align][/td][td][align=center]0.0025[/align][/td][td][align=center]0.0050[/align][/td][td][align=center]0.0075[/align][/td][td][align=center]0.0100[/align][/td][td][align=center]0.0125[/align][/td][/tr][tr][td][align=center]VC清除率(%)[/align][/td][td][align=center]20.54[/align][/td][td][align=center]42.88[/align][/td][td][align=center]59.39[/align][/td][td][align=center]74.44[/align][/td][td][align=center]79.09[/align][/td][/tr][tr][td][align=center]黄酮清除率(%)[/align][/td][td][align=center]40.39[/align][/td][td][align=center]67.21[/align][/td][td][align=center]78.42[/align][/td][td][align=center]85.29[/align][/td][td][align=center]88.30[/align][/td][/tr][/table][align=center][img=,360,256]http://ng1.17img.cn/bbsfiles/images/2018/07/201807091816376703_5430_2904018_3.png!w360x256.jpg[/img][/align]图6 黄芩总黄酮对羟自由基的清除Fig.6 Scutellaria Flavonoids on Scavenging of Hydroxyl Radicals黄芩总黄酮对羟自由基的清除作用,结果见图6。由图6可知,黄芩总黄酮对羟基自由基具有一定的清除作用。在相同的浓度范围下,清除能力大小为:提取物VC溶液。在0.0025—0.0125mg/ml浓度下,各溶液的清除能力都随浓度的增大而增大。当提取液浓度为0.0125mg/ml下,黄芩提取液的清除率达到了88.30%。3.4.2 [b]对超氧自由基的清除作用[/b][align=center]表7 提取液浓度对超氧基自由基清除率[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]提取液浓度/(mg/ml)[/align][/td][td][align=center]0.0025[/align][/td][td][align=center]0.0050[/align][/td][td][align=center]0.0075[/align][/td][td][align=center]0.0100[/align][/td][td][align=center]0.0125[/align][/td][/tr][tr][td][align=center]VC清除率(%)[/align][/td][td][align=center]26.77[/align][/td][td][align=center]43.09[/align][/td][td][align=center]61.73[/align][/td][td][align=center]78.69[/align][/td][td][align=center]80.20[/align][/td][/tr][tr][td][align=center]黄酮清除率(%)[/align][/td][td][align=center]49.81[/align][/td][td][align=center]75.29[/align][/td][td][align=center]84.38[/align][/td][td][align=center]89.21[/align][/td][td][align=center]90.01[/align][/td][/tr][/table]黄芩总黄酮对超氧自由基的清除作用,结果见图7。由图7可知,黄芩总黄酮对邻苯三酚自氧化产生的超氧自由基有一定的清除作用,其清除率随浓度的增大而增大。在相同的浓度范围下,清除能力大小为:提取物VC溶液。各溶液的清除能力都随浓度的增大而增大。当提取液浓度为0.0125mg/ml下,黄芩提取液的清除率达到了90.01%。3.4.3 [b]对DPPH自由基的清除作用[/b][align=center]表8 提取液浓度对DPPH自由基清除率[/align][table][tr][td][align=center]序号[/align][/td][td][align=center]1[/align][/td][td][align=center]2[/align][/td][td][align=center]3[/align][/td][td][align=center]4[/align][/td][td][align=center]5[/align][/td][/tr][tr][td][align=center]提取液浓度/(mg/ml)[/align][/td][td][align=center]0.0025[/align][/td][td][align=center]0.0050[/align][/td][td][align=center]0.0075[/align][/td][td][align=center]0.0100[/align][/td][td][align=center]0.0125[/align][/td][/tr][tr][td][align=center]Vc清除率(%)[/align][/td][td][align=center]27.36[/align][/td][td][align=center]52.41[/align][/td][td][align=center]79.98[/align][/td][td][align=center]80.49[/align][/td][td][align=center]81.31[/align][/td][/tr][tr][td][align=center]黄酮清除率(%)[/align][/td][td][align=center]55.7[/align][/td][td][align=center]82.3[/align][/td][td][align=center]89.78[/align][/td][td][align=center]93.74[/align][/td][td][align=center]93.81[/align][/td][/tr][/table][b] [/b]黄芩总黄酮对DPPH的清除作用,结果见图8。由图8可知,黄芩总黄酮对DPPH有一定的清除作用,其清除率随浓度的增大而增大。相同的浓度范围下,清除能力大小为:提取物VC溶液。各溶液的清除能力都随浓度的增大而增大。当提取液浓度为0.0125mg/ml下,黄芩提取液的清除率达到了93.81%。[b]4.总结[/b]1.通过单因素实验,得出各个单因素的最佳条件,其中料液比为1:10,乙醇浓度为50%,超声时间为20min,超声温度为40℃,为正交试验奠定了基础。然后用设计正交试验,确定了超声辅助法提取黄芩总黄酮的最佳工艺条件:乙醇浓度为50%、超声时间为25min、料液比为1∶10、超声温度为30℃。黄芩总黄酮的提取率为3.25%。2.本实验分别就黄芩提取物对羟基自由基,超氧阴离子自由基和DPPH自由基的抗氧化性进行了测定,并与VC进行了对比实验,得到如下结论:在0.0025—0.0125mg/ml浓度下,提取物对各自由基清除能力为:DPPH O[sub]2[/sub][sup]-[/sup]• • OH ,同浓度黄芩提取物清除能力普遍高于VC溶液,黄芩黄酮提取液和VC溶液对自由基清除率随其浓度的增大而增大。在浓度为0.0125mg/ml下,对羟基自由基的清除率为88.30%,对超氧基自由基的清除率为90.01%,对DPPH自由基的清除率为93.87%,由此可知黄芩总黄酮是一种天然有效的自由基清除剂。黄芩中黄酮类化合物的利用已经有一定的规模,但黄芩中黄酮化合物的提取方法和工艺尚未成熟,所以充分利用黄芩资源是我国药用研究的科学发展方向。基于提取率、成本等因素的影响,通过对各种因素的比较分析,从而探索开发出适合工业化生产应用的方案,提高黄芩利用率,仍是研究工作的重点之一。随着人们对健康的日渐重视,因黄芩中的黄酮化合物有着极高的药用营养及良好的保健作用,具有极为广阔的市场前景[b]。[/b]本文旨在研究黄芩中黄酮类物质的提取工艺及其体外抗氧化活性,为黄芩中黄酮类化合物作为天然抗氧化剂和功能性药品得到开发利用提供理论基础和实验依据。[align=center][b] [/b][/align] 刘雄,高建德.黄芩研究进展.甘肃中医学院,2007,24(2):46-50. 罗小文.黄芩中黄酮类成分提取工艺研究进展.中国现代中药.2010,12(7):5-8. 张睿,徐雅琴,时阳.黄酮类化合物提取工艺研究.食品与机械.2003,15(1):21-22. 梁丹,张保东.黄酮类化合物提取和分离方法研究进展.周口师范学院学报,2007,24(5):87-89. 龙春,高志强,陈凤鸣,等.黄酮类化合物的结构-抗氧化活性研究进展.重庆文理学院学报.2006,5(2):13-15. 刘雄,高建德.黄岑研究进展.甘肃中医学院学报,2007,24(2):46-50. 郭雪峰, 岳永德. 黄酮类化合物的提取-分离纯化和含量测定方法的研究进展. 安徽农业科学. 2007, 35(26): 8083- 8086.. 唐德智.黄酮类化合物的提取、分离、纯化研究进展.中药与天然产物,2009,21(12):101-104.. 张岩, 曹国杰, 张燕,等. 黄酮类化合物的提取以及检测方法的研究进展.天食品研究与开发,2008,29(1):154-157. 韩雅慧,陶宁萍.甘草黄酮提取及其抗氧化能力测定方法研究进展.山西农业科学,2010, 38(11):89- 93. 崔永明,余龙江,等. 甘草总黄酮的提取技术及其抑菌活性研究.中药材,2006, 29(8): 838-840. 孙墨珑, 宋湛谦, 方桂珍. 核桃楸总黄酮的提取工艺.东北林业大学学报, 2006, 34 (1) : 38 - 39. 徐清萍,钟桂,芳孟君. 抗氧化剂抗氧化方法研究进展.食品工程,2007,6(7):23-25. 安卓,贾昌喜.苦苣菜总黄酮提取、纯化工艺优化抗氧化活性研究.食品科学. 赵新淮.大黄醇提取物对三种自由基的清除能力的研究.东北农业大学学报.1998,29(3):284-288 杨立琛,李荣.花椒叶黄酮的微波提取及其成分分析.食品科学. CHI Ru-an,ZHOU Fang,HUANG Kun,ZHANG Yue-fei.Separation of baicalin form Scutellaria Baicalensis Georgi with polyamide.Key Laboratory for Green Chemical Process of Ministry of Education.2008,15(1):606-611.
最近在做黄芩中黄芩苷的含量测定,发现黄芩苷对照品不管是50%甲醇,纯甲醇还是DMSO都很难溶解,我称量的是15mg的黄芩苷,想溶解到10ml容量瓶中,水浴锅加热60度,超声都试过了,就是不溶,求问有做过的大哥吗,麻烦指点一二
HPLC法同时测定肠肛舒口服液中芍药苷和黄芩苷的含量周桂芳H,夏建洪,凌明 (1.浙江金华市人民医院,金华市321000;2.浙江金华市药品检验所,金华市321000)中图分类号 R927.2;R283.61 文献标识码 A 文章编号 1001—0408(2007)24—1876—02摘要 目的:建立以高效液相色谱法同时测定肠肛舒口服液中芍药苷和黄芩苷含量的方法。方法:色谱柱为Ultimate® XB—C18(250mm×4.6mm,5μm),流动相为甲醇-水-醋酸(35:65:1),流速为1.0mL/min ,检测波长为244nm。结果:芍药苷和黄芩苷分别检测浓度在0.025-0.25mg·mL-1 范围内与峰面积积分值呈良好线性关系,相关系数(r)分别为0.9997和1.0000;平均回收率分别为98.4%和97.0%,RSD分别为1.43%和1.20%(n =9)。结论:本法可同时测定肠肛舒口服液中芍药苷和黄芩苷的含量,方法简便、准确,可为制定肠肛舒口服液质量标准及产品质量控制提供依据。关键词 高效液相色谱法;肠肛舒口服液;芍药苷;黄芩苷;含量测定HPLC法同时测定肠肛舒口服液中芍药苷和黄芩苷的含量不好意思,现在补发一下
百科名片http://b.hiphotos.baidu.com/baike/s%3D220/sign=ead8207cb2119313c343f8b255390c10/f2deb48f8c5494ee4984e1a72df5e0fe98257eee.jpg 黄芩别名山茶根、土金茶根。为唇形科植物黄芩(Scutellaria baicalensis Georgi),以根入药。有清热燥湿,凉血安胎,解毒功效。主治温热病、上呼吸道感染、肺热咳嗽、湿热黄胆、肺炎、痢疾、咳血、目赤、胎动不安、高血压、痈肿疖疮等症。黄芩的临床应用抗菌比黄连还好,而且不产生抗药性。我们借助广谱抗菌作用强的特点,用在真菌培养杂菌感染特厉害,用黄芩提取液效果很好,它是农业病害防治最理想的一味药。产于河北、辽宁、陕西、山东、内蒙古、黑龙江等地。色谱柱:Ultimate xB-C18 4.6*250 PN:00201-31043 SN:211202195色谱条件与系统适用性试验 以十八烷基硅烷键合硅胶为填充剂;以甲醇-水-磷酸(47:53:0.2)为流动相;检测波长为280nm。理论板数按黄芩苷峰计算应不低于2500。对照品溶液的制备 取在60℃减压干燥4小时的黄芩苷对照品适量,精密称定,加甲醇制成每1ml含60μg的溶液,即得。供试品溶液的制备 取本品中粉约0.3g,精密称定,加70%乙醇40ml,加热回流3 小时,放冷,滤过,滤液置100ml 量瓶中,用少量70%乙醇分次洗涤容器和残渣,洗液滤入同一量瓶中,加70%乙醇至刻度,摇匀。精密量取1ml,置10ml量瓶中,加甲醇至刻度,摇匀,即得。测定法 分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。 本品按干燥品计算,含黄芩苷(C21H18O11) 不得少于8.0% 。1.对照品典型色谱图:http://ng1.17img.cn/bbsfiles/images/2013/08/201308161552_458030_2771408_3.gif2.样品1典型色谱图:http://ng1.17img.cn/bbsfiles/images/2013/08/201308161553_458031_2771408_3.gif3.样品2典型色谱图:http://ng1.17img.cn/bbsfiles/images/2013/08/201308161553_458032_2771408_3.gif3.样品3典型色谱图:http://ng1.17img.cn/bbsfiles/images/2013/08/201308161553_458033_2771408_3.gif5.典型色谱图对比图:http://ng1.17img.cn/bbsfiles/images/2013/08/201308161554_458034_2771408_3.gif6.结论:月旭色谱柱能满足含量测定分析要求。

http://ng1.17img.cn/bbsfiles/images/2013/02/201302192328_426024_2160661_3.jpgIntroduction首先要严重自我检讨一下,每次谈钱不上感情都名列榜首,是负分的榜首,哈哈,非常对不起小S,之前是一直忙毕业,后来毕业上班了发现还是很忙。唉,希望能多回来看看参与参与,过段时间说不定又把kaikaifeng忽悠回来啊,哈哈。进入主题,本体验介绍我毕业课题的一章,活性天然产物的纯化与分离,整个实验的成功充分体现了Ultimate XB-C18色谱柱的卓越性能,真材实料献给大家。黄芩苷和汉黄芩苷为中药黄芩的两大主要成分,其良好的药理活性长期吸引着研究者的兴趣,虽然二者在黄芩药材中的含量较高,但目前仍然没有一种有效的方法来获得纯品黄芩苷和汉黄芩苷。本论文应用吸附和解吸附原理,开发了一种大量富集纯化和分离这两个化合物的方法,为纯品的获得迈出了极其重要的一步。整个纯化过程中的定量工作均由Ultimate XB-C18色谱柱完成,其良好的性能保证了结果的可重现性和准确性,在此简要介绍一下论文的精髓,细节大家可以下载论文进行研究讨论。1.Materials 色谱甲醇(Fisher),去离子水(Eyela Still Ace, SA-2100 E1, 日本),三氟乙酸(TFA,Dima),黄芩苷和汉黄芩苷纯品为笔者实验室自制,纯度均达到98%以上,其结构同时经过核磁和质谱确认,其它材料略。2.HPLCanalysis of baicalin and wogonoside Shimadzu HPLC system, 由LC-10ATVP 泵, SPD-10AVP 紫外检测器, 以及CTO-10ASVP 柱温箱组成, 工作站为浙江大学N3000工作站。色谱柱:Ultimate XB-C18柱(5μm, 4.6x250mm)----见下图原论文阐述http://ng1.17img.cn/bbsfiles/images/2013/02/201302192333_426025_2160661_3.jpg 流动相:A通道:甲醇,B通道:水(0.05% TFA)流速:1.0 mL/min柱温:30℃检测波长:277nm进样量:20μL3.Resultshttp://ng1.17img.cn/bbsfiles/images/2013/02/201302192327_426023_2160661_3.jpg[font='Times New

【作者】 栾爽; 王冬梅; 赵怀清; 高靥; 申涛; 石健;【Author】 LUAN Shuang,WANG Dong-mei,ZHAO Huai-qing,GAO Ye,SHEN Tao,SHI Jian(School of Pharmacy,Shenyang Pharmaceutical University,Shenyang 110016,China)【机构】 沈阳药科大学药学院;【摘要】 目的利用梯度洗脱,建立高效液相色谱法测定心脑联通胶囊中葛根素、虎杖苷和野黄芩苷含量的方法。方法采用高效液相色谱法。Diamonsil ODS柱(4.6mm×200mm,5μm),流动相为乙腈(A)和0.05%磷酸水溶液(B)梯度洗脱,流速1.0m L.min-1,检测波长336nm。结果葛根素的线性范围为0.0232~0.1856g.L-1(r=0.9995),平均回收率为100.0%,RSD=1.3%,虎杖苷的线性范围为0.0152~0.1216g.L-1(r=0.9996),平均回收率为98.7%,RSD=0.9%,野黄芩苷的线性范围为0.0046~0.0369g.L-1(r=0.9998),平均回收率为100.4%,RSD=0.9%。结论本方法操作简便,测定结果准确可靠,可用于心脑联通胶囊的质量控制。 更多还原http://ng1.17img.cn/bbsfiles/images/2012/08/201208271705_386562_2379123_3.jpg
作者:张雅贤(辽宁东方人药业有限公司, 辽宁 本溪, 117000)摘要:为了控制该制剂的质量,本文采用HPLC0法.以黄芩苷为对照品,测定其制剂中黄芩苷含量.目的 建立清热化毒丸中黄芩苷的含量测定方法.方法 采用高效液相色谱法测定,Diamonsil C18色谱柱,检测波长为315 nm.其结果平均回收率为99.81%.,RSD=0.93%.结论 本方法测定清热化毒丸中黄芩苷的含量,方法简便、准确,结果稳定,可用于控制该丸剂的质量.谱图:无
【文章来源】北京普源精电科技有限公司(RIGOL) http://www.instrument.com.cn/netshow/SH101945/index.asp【摘要】 本文根据中华人民共和国药典(2010 版)第一部中牛黄上清片中黄芩苷的含量测定方法,对某厂家生产的牛黄上清片进行含量测定及方法学验证。实验结果为:以黄芩苷峰计理论塔板数为12050(药典要求理论塔板数按黄芩苷峰计算应不低于4000),牛黄上清片产品中黄芩苷含量为1.7mg/片(药典要求黄芩苷含量以每片计,不得少于1.0mg/片)。黄芩苷的线性范围为4μ g/mL~200μ g/mL (r=0.9991),平均回收率为98.8%。实验结果表明:采用RIGOL L-3000高效液相系统进行牛黄上清片中黄芩苷含量测定,能完全满足中华人民共和国药典要求,方法准确、灵敏。完整应用文档,请点击如下链接下载 ======================= 点击打开链接 ==========================针对大家所关心的问题,RIGOL应用中心会持续为大家开展分析http://simg.instrument.com.cn/bbs/images/brow/em09511.gif部分谱图:对照品标准工作溶液及样品溶液http://ng1.17img.cn/bbsfiles/images/2011/03/201103111726_282164_2248886_3.jpg定性及定量重复性 http://ng1.17img.cn/bbsfiles/images/2011/03/201103111726_282165_2248886_3.jpg欢迎大家积极讨论哈~~http://simg.instrument.com.cn/bbs/images/brow/em09510.gif

【作者】 刘喆;【机构】 山东中医药大学附属医院;【摘要】 目的建立测定小儿肾病合剂黄芩苷含量的高效液相色谱(HPLC)法。方法采用HPLC法,色谱柱为Diamonsil C8柱(250mm×4.6mm,5μm),流动相为乙腈-水-磷酸(30∶100∶0.04),流速1mL/min,柱温35℃,检测波长280nm,进样量10μL。结果黄芩苷进样量在0.100~1.300μg范围内与峰面积线性关系良好,r=0.9993(n=5),平均回收率为98.90%,RSD为1.40%(n=6)。结论HPLC法专属性强、灵敏准确、重现性好,可作为小儿肾病合剂的质量控制方法。 更多还原【关键词】 小儿肾病合剂; 质量标准; 高效液相色谱法; 黄芩苷; 含量; http://ng1.17img.cn/bbsfiles/images/2012/08/201208271545_386443_2352694_3.jpg
我想用HPLC测定复方中野黄芩苷的含量,但前面老有一个杂质峰分不开,请问用什么样的条件可以改善分离呢?
高效液相色谱定量分析1 黄芩苷含量检测(1)色谱条件与系统适应性试验 以十八烷基硅烷键合硅胶为填充剂;流动相:甲醇-水-磷酸(47:53:0.2);检测波长:276nm。柱温:30℃;流速:1mL/min。理论板数按黄芩苷峰计算应不低于4500。(2)测定方法对照品溶液的制备 取黄芩苷对照品适量,精密称定,置棕色量瓶中,加50%甲醇适量,置水浴中振摇使溶解,放置至室温,稀释至刻度,摇匀,制成每1mL含40μg的溶液,即得。 供试品溶液的制备 精密量取样品溶液,置容量瓶中,加水稀释至一定浓度,摇匀,用0.45μm滤头过滤即得。测定法 分别精密吸取对照品溶液10μL与供试品溶液10μL,注入色谱仪,测定,即得。2 高效液相色谱的定量分析药典规定:本品每支10mL含黄芩苷(C21H18O11)计,不少于80mg。本品每1mL含金银花以绿原酸(C16H18O9)计,不得少于0.60mg。(1)黄芩苷高效液相图 见附件1 [img]http://www.instrument.com.cn/bbs/images/affix.gif[/img][url=http://www.instrument.com.cn/bbs/download.asp?ID=101403]附件1 [/url]

作者:胡建华:黑龙江省中医研究院摘要:为了确定芩百粉针剂中黄芩药材的产地,保证其质量的稳定、可控,本课题采用HPLC法对芩百粉针剂的原料药(黄芩药材)的指纹图谱进行了初步研究:以黄芩苷为参照物,对10个不同产地的黄芩药材进行了HPLC指纹图谱分析。并采用RPHPLC法同时测定了黄芩药材中4种黄酮类成分黄芩苷、汉黄芩苷、黄芩素和汉黄芩素的含量。 方法:色谱柱:Dikma钻石C18(5μm,250mm×4.6mm);流动相:乙腈与水-四氢呋喃-磷酸(80:10:0.2)溶剂系统,梯度洗脱;检测波长:280nm;流速:1.0ml/min;柱温:30℃;进样量:10μl。 结果:共标出9个共有峰,不同产地黄芩药材之间各共有峰的相对保留时间重现性较好,而峰面积比值的可比性较差。非共有峰面积不超过总峰面积的10﹪。黄芩苷、汉黄芩苷、黄芩素和汉黄芩素在一定范围内均具有良好的线性相关性。其线性范围分别为0.16~6.25μg(r=0.9999),0.14~5.47μg(r=0.9999),0.08~3.12μg(r=0.9999),0.02~0.78μg(r=0.9999);平均回收率(n=5)分别为99.80﹪,100.28﹪,100.74﹪,98.89﹪;RSD分别为1.76﹪,1.99﹪,2.54﹪,1.51﹪。本方法重现性好,专属性强。 结论:比较10个不同产地黄芩药材的指纹图谱及其4种黄酮类成分的含量,表明山东莒县、甘肃陇西和山东沂水的指纹图谱中4种黄酮类成分的色谱峰面积总和占总峰面积的比例较高,而且通过含量测定也表明这三个产地中4种黄酮类成分的总量较高。所以可以判定山东莒县、甘肃陇西和山东沂水的黄芩药材质量较优,可以作为芩百粉针剂中黄芩的原料药材。而且本研究所建立的黄芩药材的指纹图谱及含量测定的方法也可为黄芩药材的质量控制提供科学依据。http://ng1.17img.cn/bbsfiles/images/2012/07/201207161733_377938_2379123_3.jpghttp://ng1.17img.cn/bbsfiles/images/2012/07/201207161734_377939_2379123_3.jpg
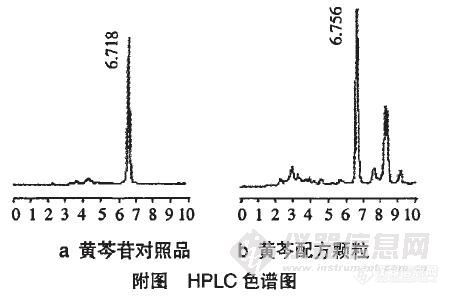
【作者】 雷鹏; 刘韶; 李新中; 徐平声(中南大学湘雅医院药剂科; 中南大学湘雅医院药剂科 湖南长沙410008; 湖南长沙410008)【摘要】 目的建立黄芩配方颗粒中黄芩苷含量测定方法。方法采用高效液相法测定黄芩配方颗粒中黄芩苷含量,色谱柱:DiamonsilC18(4.6×250mm);流动相:甲醇-0.05%磷酸(65∶35);流速:1mL/min;柱温:30℃;检测波长:280nm。结果黄芩苷在0.215~2.150μg范围内线性关系良好,平均回收率为98.30%。结论该方法简便可行、重复性好,可作为黄芩配方颗粒质量评价的依据。【谱图】http://ng1.17img.cn/bbsfiles/images/2012/08/201208211704_385093_1609970_3.jpg
【作者】 李平; 杨应勇; 李江; 肖书伟;【机构】 贵阳中医学院第二附属医院; 贵州神奇药业集团苗药工程中心; 贵阳中医学院;【摘要】 目的:通过HPLC测定黄芩和半夏不同配伍比例后黄芩苷溶出量的变化,以探讨中药药性配伍的科学内涵。方法:采用Diamonsil C18(2)柱(4.6 mm×250 mm,5μm),乙腈-0.4%磷酸溶液(26∶74)为流动相,检测波长280 nm,流速1.0 mL.min-1,柱温30℃。建立黄芩与半夏配伍后黄芩苷的含量测定方法,并比较不同配伍后黄芩苷溶出量的大小。结果:黄芩苷质量浓度在0.010 25~0.102 5 g.L-1线性关系良好(r=0.999 9),平均回收率99.21%(n=9),RSD 2.0%;黄芩配伍半夏后和黄芩单煎后黄芩苷平均含量分别为64.018,63.6805,0.581,62.529 mg.g-1。结论:黄芩配伍半夏后黄芩苷的HPLC检测方法可靠、稳定、重复性好。不同比例配伍后黄芩苷的溶出量有较大差异,尤其是以热为主配伍(6∶9)对黄芩苷的溶出影响最大,溶出最低,体现了中药药性配伍中以半夏的温热之性抑制黄芩之寒凉之性的科学内涵。
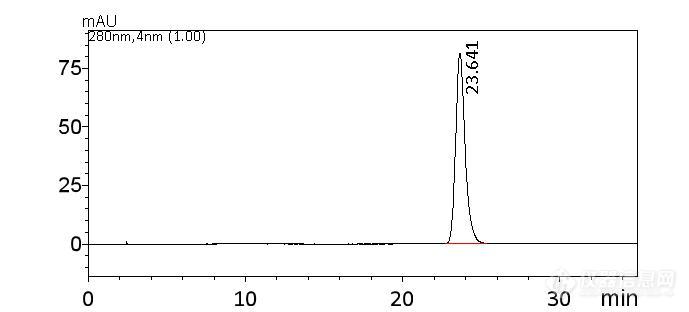
[align=center][font='Times New Roman'][size=12pt][color=#333333]黄芩中黄芩苷[/color][/size][/font][font='Times New Roman'][size=12pt][color=#333333]含量测定[/color][/size][/font][/align][font='Times New Roman'][size=12.0000pt]1 [font=宋体]材料[/font][/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体]黄芩药材[/font][/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体](送检样)[/font][/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体],甲醇(色谱级),[/font][/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体]乙醇[/font][/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体],[/font][/size][/font][font=宋体][size=12.0000pt]磷[/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体]酸[/font][/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体](分析纯)[/font][/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体];[/font][/size][/font][font=宋体][size=12.0000pt]黄芩苷[/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]对照品[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333](购自中检院)[/color][/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体]。[/font][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]2 仪器与设备[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333] 岛津液相LC-20AT配制[/color][/size][/font][font=宋体][size=12.0000pt][color=#333333]DAD[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]检测器,[/color][/size][/font][font=宋体][size=12.0000pt][color=#333333]安捷伦[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]Eclipse XDB [/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]C18[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]色谱柱[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333](250mm*4.6μm*5μm)[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333],[/color][/size][/font][font=宋体][size=12.0000pt][color=#333333]恒温[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]水浴锅[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]([/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]北京中兴[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333])[/color][/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体]。[/font][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]3 实验方法[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]3.1 色谱条件[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333] 流动相(参照中国药典2015年第一部):[/color][/size][/font][font='Times New Roman'][size=12pt][color=#333333]以甲醇-水-磷酸(47:53:0.2)为流动相;检测波长为280nm[/color][/size][/font][font=宋体][size=12pt][color=#333333];[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]柱温:35 [/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]℃[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333];流速:1.0mL/min,进样量:10[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]μ[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]L。[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]3.2[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]对照品溶液制备[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333] 取[/color][/size][/font][font=宋体][size=12.0000pt][color=#333333]黄芩苷[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]对照品适量,精密称定,加流动相制成每1ml含[/color][/size][/font][font=宋体][size=12.0000pt][color=#333333]6[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]0μg的溶液,即得[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]。色谱图如下:[/color][/size][/font][align=center][img=,689,312]https://ng1.17img.cn/bbsfiles/images/2020/06/202006012239045184_9789_1858223_3.jpg!w689x312.jpg[/img][/align][align=center][font='Times New Roman'][size=12.0000pt][color=#333333]图1[/color][/size][/font][font=宋体][size=12.0000pt][color=#333333]黄芩苷[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]标准品图[/color][/size][/font][/align][font='Times New Roman'][size=12.0000pt][color=#333333]3.3 [/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]供试品溶液的制备 [/color][/size][/font][font='Times New Roman'][size=12pt][color=#333333] 取本品中粉约0.3g,精密称定,加70%乙醇40ml,加热回流3小时,放冷,滤过,滤液置100ml量瓶中,用少量70%乙醇分次洗涤容器和残渣,洗液滤入同一量瓶中,加70%乙醇至刻度,摇匀。精密量取1ml,置10ml量瓶中,加甲醇至刻度,摇匀,[/color][/size][/font][font=宋体][size=12pt][color=#333333]过滤膜,[/color][/size][/font][font='Times New Roman'][size=12pt][color=#333333]即得。[/color][/size][/font][font='Times New Roman'][size=12.0000pt][color=#333333]色谱图如下[/color][/size][/font][align=center][font='Times New Roman'][size=12.0000pt][color=#333333][img=,689,312]https://ng1.17img.cn/bbsfiles/images/2020/06/202006012239291711_5958_1858223_3.jpg!w689x312.jpg[/img][/color][/size][/font][/align][align=center][font='Times New Roman'][size=12.0000pt][font=宋体]图[/font]3 [/size][/font][font=宋体][size=12.0000pt]黄芩[/size][/font][font='Times New Roman'][size=12.0000pt][font=宋体]样品的色谱图[/font][/size][/font][/align][font='Times New Roman'][size=12.0000pt]4 [font=宋体]结果与讨论[/font][/size][/font][font=宋体][size=12.0000pt][color=#333333](1)[/color][/size][/font][font=宋体][size=12.0000pt][color=#333333]黄芩苷标准品容易吸潮,一般买回来都要减压干燥5-6小时;[/color][/size][/font][font=宋体][size=12.0000pt][color=#333333](2)[/color][/size][/font][font=宋体][size=12.0000pt][color=#333333]做样的时候发现,测黄芩苷比较废溶剂,所以我就参照药典进行了方法探讨,节约溶剂的同时,又得保证数据的稳定和正确性,样品溶液可以直接加50ml回流提取,过滤,取续滤液0.5ml然后定容至10ml,结果与药典方法一致,所以为了节约试剂,可以减少提取剂的用量。[/color][/size][/font]