国产非特殊用途化妆品备案实施细则一、项目名称国产非特殊用途化妆品备案二、法律依据(一)《化妆品卫生监督条例》(二)《化妆品卫生监督条例实施细则》三、收费标准不收费四、受理范围化妆品生产企业生产的国产非特殊用途化妆品在投放市场后二个月以内,向省级食品药品监管部门申请备案。五、申请资料1.《国产非特殊用途化妆品备案申请表》(下载打印);2.产品中文名称命名依据;(应附合国家食品药品监督管理局制定的《化妆品命名规定》及《化妆品命名指南》的有关要求)3.产品全成份配方(示例);4.产品质量安全控制要求(应注明是否已在省质量技术监督局进行标准备案);5.工艺流程简述和简图(标明所用到的生产设备、原料,并标明主要质控点);6.与产品生产有关的生产设备清单(标明设备的名称、规格、型号、用途);7.产品设计包装(含产品标签、产品说明书);8.近半年的省级食品药品监督管理部门认定的检验机构出具的检验报告原件、复印件;(查看原件,留复印件)9.产品中可能存在的安全性风险物质的有关安全性评估资料;10.生产企业卫生许可证原件及复印件(委托生产的,由受托方即实际生产企业提供生产企业卫生许可证复印件);(查看原件,留复印件)11.委托生产加工协议复印件及受托方的有关情况说明(委托加工产品提供);12.经办人不是法定代表人或负责人本人的,企业应当提交《授权委托书》和经办人的身份证复印件;13.其他有助于备案的材料。六、资料要求(一)产品配方资料应符合下列要求:①应以表格形式在同一张表中提供包含标准中文名称、百分含量、使用目的等内容的配方表;②应提供全部原料的名称,实际含量以百分比计,并注明有效物含量(未注明者均以有效物含量100%计);复配原料(香精除外)必须以复配形式申报,并应标明各组分在其中的含量(以百分比计);特殊情况,如含结晶水、原料存在不同的分子式或结构式等应加以说明,全部原料按含量递减顺序排列;③配方原料(含复配原料中的各组分)的中文名称应按《国际化妆品原料标准中文名称目录》使用标准中文名称,无INCI名称或未列入《国际化妆品原料标准中文名称目录》的应使用《中国药典》中的名称或化学名称或植物拉丁学名,不得使用商品名或俗名,但复配原料除外;④着色剂应提供《化妆品卫生规范》上载明的着色剂索引号(简称CI号),无CI号的除外;⑤《化妆品卫生规范》对限用物质原料有规格要求的,还应提交由原料生产商出具的该原料的质量规格证明;⑥凡宣称为孕妇、哺乳期妇女、儿童或婴儿使用的产品,应当提供基于安全性考虑的配方设计原则(含配方整体分析报告)、原料的选择原则和要求、生产工艺、质量控制等内容的资料。(二)产品质量安全控制要求应包含下列内容:①颜色、气味、性状等感官指标;②微生物指标(不需检测的除外)、卫生化学指标;③宣称含α-羟基酸或虽不宣称含α-羟基酸,但其总量≥3%(w/w)的产品应当有pH值指标(油包水(油状产品)、粉状、粉饼类、蜡基类除外)及其检测方法。(三)产品中可能存在安全性风险物质的有关安全性评估资料应按照《化妆品中可能存在的安全性风险物质风险评估指南》进行提供。(四)申请资料按上述顺序装订,且各部分有明显的标志,并标明各项资料名称或该项资料所在目录中的序号,整套资料用打孔夹装订成册。共提交2套文字版资料(企业留存一套),每套文字版资料(除检验报告、公证文书、官方证明文件及第三方证明文件原件外)要逐页加盖企业公章和骑缝章;(五)使用A4规格纸张打印(中文不得小于宋体小4号字,英文不得小于12号字,行间距不小于25磅)左边距不小于3cm,页脚居中标示页码;(六)申请资料中提交的复印件必须与原件一致,并且申请人须在复印件上注明“与原件一致”字样和复印日期,并加盖企业公章,现场核查时验证原件;(七)申报资料所附图片、图纸必须清晰易辨。图纸需标明面积及尺寸。
在中国,化妆品的分类分为非特殊用途化妆品(2007年之前称为普通化妆品)和特殊用途化妆品。特殊用途化妆品是指能改变人体局部状态,去除影响人体美的因素的化妆品,包括生发、染发、烫发、脱毛、美乳、健美、除臭、祛斑和防晒化妆品。国产非特殊用途化妆品是指除以上九种情况以外的化妆品。自2014年6月30日起,国产非特殊用途化妆品生产企业应当在产品上市前,按照《国产非特殊用途 化妆品备案要求》,对产品信息进行网上备案。国产非特殊用途化妆品备案的相关企业包括:生产企业(自主生产)和所有实际生产企业(境内委托生产、境外委托境内生产)。非特备案的产品信息经省级食品药品监管部门确认后在食品药品监管总局政务网站统一公布,供公众查询,省级食品药品监管部门不再发放国产非特殊用途化妆品备案凭证。SGS作为国家食品药品监督管理局指定的国产非特殊用途化妆品备案检验机构,承担国产非特殊用途化妆品备案检验中的微生物、卫生化学检测。SGS可为您提供以下服务:1. 微生物检验项目微生物全套:菌落总数、霉菌和酵母菌总数、粪大肠菌群、金黄色葡萄球菌、铜绿假单胞菌2. 卫生化学检验项目评估的卫生化学指标主要包括:重金属(铅、砷、汞)、甲醇、α—羟基酸、抗生素、甲硝唑和PH3. 风险物质评估SGS专家可参照《关于印发化妆品中可能存在的安全性风险物质风险评估指南的通知》(国食药监许 339号)要求进行风险评估。如果风险评估结果能够充分确认产品安全性的,可免于产品相关毒理学测试。
第一次发贴,跟大家分享一下最近广东FDA落实的一些政策,都是一些基础信息/知识。据《关于调整化妆品注册备案管理有关事宜的通告》,自2014年6月30日起,国产非特殊用途化妆品生产企业应当在上市前,按照《国产非特殊用途化妆品备案要求》对产品信息进行网上备案。热点解读:1.所有非特化妆品应按照《通告》履行备案手续2.产品上市前备案手续而非上市后3.提交备案资料后即可上市销售4.产品备案信息在总局网站统一公开那么,究竟需要准备哪些资料呢?根据《国产非特殊用途化妆品备案要求》,生产企业应当在产品上市销售前整理归档以下资料:1.产品配方(不包括含量,限用物质除外)2.产品销售包装(含产品标签、产品说明书)3.产品生产工艺简述4.产品技术要求5.产品检验报告6.委托生产协议复印件(委托生产的产品)另外,将美白化妆品纳入特殊化妆品实施管理。
广东省食药局目标计划:2014年12月31日前,在售化妆品备案覆盖率达100%!附件是非特备案培训资料!有什么关于备案检验的不懂可以咨询我!谢谢!有需要咨询非特备案检测的,请联系15920123833 郑工,qq2517374905 !
据《关于调整非特殊化妆品注册备案管理有关事宜的通告》,自2014年6月30日起,国产非特殊用途化妆品生产企业应当在产品投放市场后2个月内,按照《国产非特殊用途化妆品备案要求》对产品信息进行备案。申请国产非特殊用途化妆品备案的,可自行选择经各省级食品药品监督管理部门指定的检验机构进行备案检验,备案检验的检验项目根据《化妆品行政许可检验规范》(国食药监许82号)中非特殊用途化妆品的检验项目进行确定。热点解读:1.所有非特化妆品应按照《通告》履行备案手续2.产品上市前备案手续而非上市后3.提交备案资料后即可上市销售4.产品备案信息在总局网站统一公开那么,究竟需要准备哪些资料呢?根据《国产非特殊用途化妆品备案要求》,生产企业应当在产品上市销售前整理归档以下资料:1.产品配方(不包括含量,限用物质除外)2.产品销售包装(含产品标签、产品说明书)3.产品生产工艺简述4.产品技术要求5.产品检验报告6.委托生产协议复印件(委托生产的产品)另外,将美白化妆品纳入特殊化妆品实施管理。《摘自本论坛》根据广东省食品药品监督管理局《关于增加指定国产非特殊用途化妆品备案检验机构的公告》(粤食药监妆〔2014〕58号),我中心(广东省微生物分析检测中心)通过了该局组织专家对提交申报资料的审核及现场评审,被指定为国产非特殊用途化妆品备案检验机构,自2014年6月30日开始,可承担国产非特殊用途化妆品的微生物和卫生化学备案检验工作。化妆品卫生指标检测(八项检测):砷铅汞菌落总数霉菌和酵母菌总数粪大肠菌群金黄色葡萄球菌绿脓杆菌的检测或者八项+1(甲醇含量)检测联系人:王先生 15002003939 020-87137565 QQ 2481010083
在ICH分别于2002年2月及2003年2月颁布的《新原料药的杂质研究指导原则》(简称Q3A(R))与《新制剂的杂质研究指导原则》(简称Q3B(R))中,为便于控制各类杂质的限度,将药品中的有机杂质细分为特定杂质(Specified Impurities)和非特定杂质(Unspecified Impurities)。特定杂质是指在质量标准中分别规定了明确的限度,并单独进行控制的杂质。特定杂质包括结构已知的杂质和结构未知的杂质。对于结构未知的杂质,为便于在标准中进行指认,一般采用代号(如未知杂质A等)或合适的定性分析指标(如相对保留时间为0.8的杂质)加以区分。 非特定杂质是指在质量标准中未单独列出,而仅采用一个通用的限度进行控制的一系列杂质,其在药品中出现的种类与几率并不固定。由于非特定杂质的不确定性,因此,在药品的临床前与临床研究中,很难对这些杂质的安全性进行评价。为将这些杂质可能带来的安全性隐患降至最小,在ICH的以上杂质指导原则中,对其限度做了明确的规定。《新原料药的杂质研究指导原则》中要求:在原料药质量标准中任一单个非特定杂质的限度不得过鉴定限度(见表1)。 表1:原料药的杂质限度
[font=&][size=16px][color=#333333]点击链接查看更多:[url]https://www.woyaoce.cn/service/info-8429.html[/url][/color][/size][/font] 化妆品纳入《食品药品安全监管信息公开管理办法》的管理范畴,化妆品违法违规等监管力度将进一步加大,这将对各大化妆品生产企业的产品质量水平以及质量管理水平提出更高要求。[font=&][size=16px][color=#333333]检测内容[/color][/size][/font][font=&][color=#333333][/color][/font] 汇标检测属国家市场监督管理总局指定的化妆品注册和备案检验机构,承担化妆品注册和备案检验工作。可为化妆品质量监测、化妆品生产流程管理、化妆品品质控制提供一站式的技术服务。《化妆品安全技术规范》2015年版 常规9项非特殊用途化妆品备案检测项目中的常规9项包含:细菌总数(菌落总数)--《化妆品安全技术规范》2015年版 第五章微生物检验方法 2菌落总数检验方法霉菌和酵母菌总数--《化妆品安全技术规范》2015年版 第五章微生物检验方法 6霉菌和酵母菌检验方法耐热大肠菌群--《化妆品安全技术规范》2015年版 第五章微生物检验方法 3耐热大肠菌群检验方法金黄色葡萄球菌--《化妆品安全技术规范》2015年版 第五章微生物检验方法 5金黄色葡萄球菌检验方法铜绿假单胞菌--《化妆品安全技术规范》2015年版 第五章微生物检验方法 4铜绿假单胞菌检验方法汞--《化妆品安全技术规范》2015年版 第四章理化检验方法 第一法 氢化物原子荧光光度法铅--《化妆品安全技术规范》2015年版 第四章理化检验方法 第二法 火焰[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法砷--《化妆品安全技术规范》2015年版 第四章理化检验方法 第一法 氢化物原子荧光光度法镉--《化妆品安全技术规范》2015年版 第四章理化检验方法 火焰[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度法[font=&][size=16px][color=#333333]检测标准[/color][/size][/font][font=&][color=#333333][/color][/font][table][tr][td]产品名称[/td][td]检测项目[/td][td]检测标准[/td][/tr][tr][td]化妆品[/td][td]41项激素[/td][td]GB/T 24800.2-2009 化妆品中四十一种糖皮质激素的测定 [url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]/串联质谱法[/td][/tr][/table][font=&][size=16px][color=#333333]我们的优势[/color][/size][/font][font=&][color=#333333][/color][/font] 广州汇标检测技术中心成立于2004年,是一家专业从事食品、环保、医药、农业投入品、农产品、化妆品、烟草及包装材料等领域的权威第三方检测机构。获得实验室认可(CNAS)、资质认定计量认证(CMA)、农产品质量安全检测机构考核合格证书(CATL)、特殊食品验证评价技术机构等资质。 现拥有专业技术保障团队600余人,实验室面积10000余平方米,通过认可、认证资质参数24000余项,大型精密仪器共1600多台/套,设备原值11000万元,为检测服务公平性、科学性、严谨性提供强大保障。
国产非特化妆品备案课件郑工,15920123833,qq2517374905
标准品:水质氨氮浓度:0.778mg/L安瓿瓶包装20mL问:在证书上面其中有一段为 - 本环境标准品应按以下程序稀释后方可使用:临用前小心打开安瓿瓶,用10mL干燥洁净移液管从安瓿瓶中准确量取10mL浓样至250mL容量瓶中,用纯水稀释定容至刻度,混匀后立即使用。请问其意思是稀释定容250mL才是证书上写的0.778mg/L浓度吗?
国产非特殊化妆品备案检测基本流程1. 委托企业需提交的资料和样品1.1 检验申请(表见附件,手签名/加盖公章,最好都有)1.2产品配方(签名/加盖公章,最好都有)1.3中文使用说明书(签名/加盖公章,最好都有) 1.4样品(必须提供数量足够留样及复测)2. 填写检验申请表注意事项2.1. 样品中文名称商标名+通用名+属性名2.2. 规格(必须填咨询)2.2.1. 如同一盒包装内含有10片25ml的面膜,填写为“25ml/片×10片/盒”;2.2.2. 如果是组合包装,不需混合后使用的,分开填写,分别检测,分别填写两张申请表;2.2.3. 如果是组合包装,需混合后使用的,写在一起例如:同一盒包装内装了1瓶**油(15ml)和1瓶***精油(5ml) ,填写为“(**油:15ml/瓶+**精油:5ml/瓶)/盒”;2.3. 送检数量2.3.1. 单位应与规格一致2.3.2. 如果同时还委托检测安全性风险物质,应将这一部分检测样品数量扣除。2.3.3. 要看样品的包装,考虑后期的取样难度和实际能够取出的样品,确定送检数量2.4. 性状 颜色+物态 2.5 生产批号或生产日期、限期使用日期或保质期以如下格式标注:生产批号对应限期使用日期 或 生产日期对应保质期2.6. 保存条件与使用说明书一致2.7. 检验要求 2.7.1. 写详细,例如:铅、砷、汞,菌落总数、粪大肠菌群等2.7.2. 申请企业根据国产非特殊用途化妆品备案检验受理参照表确定相应的检验项目,但我方需要审核,并对遗漏的项目进行提醒,若客户不接受我方提醒加测遗漏的项目,企业需在申请表备注,并且前面加盖公章。3. 产品配方3.1产品配方信息应当符合以下要求:3.1.1全部原料应当详细列明标准中文名称、原料序号、限用物质含量、使用目的等内容。3.1.2复配原料应当以复配形式填报,应当标明各组分的标准中文名称。香精不须列明具体香料组分的种类和含量。3.1.3着色剂应当提供《化妆品卫生规范》载明的着色剂索引号(简称CI号),无CI号的除外。3.1.4来源于石油、煤焦油的碳氢化合物(单一组分的除外)的原料,应当标明化学文摘索引号(简称CAS号) 。3.1.5套装产品内有两个以上(含两个)独立包装,每个产品分别报备。3.1.6不可拆分的组合包装,以一个产品名称报备的,分别报送产品配方。3.1.7两个或两个以上配合使用的产品,按一个产品报备,分别报送产品配方。4. 样品提供4.1. 企业应当一
给化妆品非特备案的实验室需要具备什么资质条件?除了化妆品非特备案检测项目通过CNAS 认可和取得CMA 资质认定外,还需要些什么条件?
食药监保化函57号各省、自治区、直辖市食品药品监督管理局(药品监督管理局),有关单位: 为进一步规范和简化进口非特殊用途化妆品备案管理工作,取消现行进口非特殊用途化妆品审核备案制,加强国产非特殊用途化妆品监管,我司起草了《关于非特殊用途化妆品分类管理的意见》(征求意见稿)及相关配套文件。现公开征求意见,请于2012年3月20日前将修改意见反馈我司。 联 系 人:林庆斌 联系电话:010-88330884 传 真:010-88373268 电子邮件:linqb@sfda.gov.cn 附件: 1. 关于非特殊用途化妆品分类管理的意见(征求意见稿) 2. 关于非特殊用途化妆品分类管理的说明 3. 关于实施非特殊用途化妆品分类管理的通知(征求意见稿) 4. 特殊用途化妆品(II类)行政许可申报资料要求(征求意见稿) 5. 特殊用途化妆品(II类)技术审评要点(征求意见稿) 6. 关于非特殊用途化妆品分类管理的意见及相关文件的起草说明 7. 反馈意见表 国家食品药品监督管理局保健食品化妆品监管司 二〇一二年二月十七日
化妆品非特备案指什么?经常有人听到非特备案,有的搞不懂是什么意思。需要检测哪些项目?
急求:2-萘基氨基甲酸甲脂,S-甲基杀螟硫磷标准品,第一次分析使用,不知道那里可以买到,那位朋友有的话可以联系我:13434173089 吴生wuaguangjun801@163.com
关于非特殊用途化妆品分类管理的意见(征求意见稿)食药监保化函263号 为进一步加强非特殊用途化妆品监管,根据《化妆品卫生监督条例》,基于安全风险管理的原则,在确保产品质量安全的前提下,对现行非特殊用途化妆品实施分类管理。 一、分类原则 (一)依法依规,确保安全。根据产品安全风险程度,修订《化妆品卫生监督条例实施细则》(以下称《实施细则》)有关现行特殊用途化妆品类别含义,将目前公认安全风险程度较高的产品类别,纳入特殊用途化妆品管理。 (二)科学分类,提高效率。考虑产品中有关功效成分的使用情况,以产品具有或宣称的特殊使用功效为分类主要依据,实行严格监管。同时加强对特殊使用部位、特殊原料、特殊适用人群等类别产品的监管,科学合理地实施非特殊用途化妆品分类管理,提高监管工作效率。 (三)合理定位,分步实施。对纳入特殊用途化妆品管理的产品类别,实行特殊用途化妆品行政许可管理。对安全风险程度尚需进一步明确的产品类别,加强安全风险监测与评估,并维持现行进口化妆品管理模式,加强国产非特殊用途化妆品备案管理,强化事后监督,保障产品质量安全。 二、主要内容 (一)调整有关特殊用途化妆品类别含义。 按照部门规章修订程序,拟将《实施细则》第五十六条第八款祛斑化妆品类别含义调整如下: 祛斑化妆品是指用于减轻皮肤表面色素沉着,有利于皮肤美白增白,祛痘或抑制粉刺的化妆品。 (二)对纳入特殊用途化妆品实行审批制。 根据修订后的《实施细则》有关规定,对目前公认安全风险程度较高的具有或宣称美白或增白(仅具有物理遮盖作用的除外)、祛痘或抑制粉等作用的产品,纳入祛斑化妆品管理,实行特殊用途化妆品行政许可管理。 (三)对部分产品类别加强安全风险监测。 对安全风险程度尚需进一步明确的产品类别,连续两年有针对性地开展安全风险监测工作,并进行安全风险评估,根据风险评估结果确定是否需要纳入特殊用途化妆品管理。此类产品主要有: 1.具有或宣称控制头部皮肤油脂分泌作用的发用类产品; 2.具有或宣称去头屑作用的发用类产品; 3.具有或宣称抗皱作用的产品; 4.具有或宣称减轻或减缓眼袋等作用的产品; 5.具有或宣称抑汗、止汗等作用,以消除或减轻人体不良气味的产品(用来掩盖体味的芳香类产品除外); 6.具有或宣称减轻黑眼圈等作用的产品; 7.具有或宣称剥脱皮肤角质等作用的产品; 8.具有或宣称皮肤晒黑或晒成其他颜色作用的产品; 9.用于口唇(不含色素的产品除外)或眼部的产品(眉笔类产品除外)。 (四)对适用于特殊人群产品实行严格监管。 对儿童(含婴幼儿)产品,发布《儿童(含婴幼儿)化妆品申报与审评指南》(以下称《指南》),进一步规范进口儿童产品的申报与审评工作。国产儿童产品应按照《指南》要求提交备案材料,并加强事后监督。 为确保有关特殊人群消费者使用安全,化妆品不得宣称专为孕妇、哺乳期妇女等特殊人群使用。 《关于非特殊用途化妆品分类管理的意见》起草说明 现行特殊用途化妆品、非特殊用途化妆品的分类管理模式是《化妆品卫生监督条例》(以下称《条例》)提出的。由于《条例》颁布实施已有20余年,有些规定已不能满足当前化妆品监管工作的实际需要。为进一步加强非特殊用途化妆品监管,国家食品药品监督管理局保健食品化妆品监管司(以下称保化司)在认真调研、反复论证、广泛征求意见的基础上,基于安全风险管理的原则,在确保产品质量安全的前提下,组织起草了《关于非特殊用途化妆品分类管理的意见》(以下称《意见》)。现将有关起草情况说明如下: 一、起草的必要性 (一)是对公认安全风险程度较高产品实行严格监管迫切需要。 1991年颁布实施的《化妆品卫生监督条例实施细则》(以下称《实施细则》)第五十六条规定了九类特殊用途化妆品含义。随着我国化妆品行业的发展,产品类别日新月异,原九类特殊用途化妆品含义范围已不适应当前化妆品监管工作实际需要。近来,媒体报道民间组织披露美白、祛痘等化妆品存在安全隐患,引起社会广泛关注。经保化司广泛征求意见,目前公认美白、祛痘等类别产品存在较高的安全风险,需要实行严格监管。因此,《意见》提出,拟按照部门规章修订法定程序,对《实施细则》中祛斑化妆品类别含义进行调整,将相关产品纳入特殊用途化妆品管理。 (二)是对安全风险程度尚未明确产品加强监管的需要。 鉴于具有或宣称去屑、抗皱、抑汗等类别产品,以及用于口、眼等特殊使用部位的产品,其安全风险程序尚需进一步明确,应当有针对性地加强监管,开展安全风险监测和风险评估工作,根据风险监测和评估结果,确定是否应该纳入特殊用途化妆品管理。同时,对使用基因、纳米技术等特殊原料或植物精油产品,需要加强原料监管,新原料必须获得批准后方可用于化妆品生产。对适用于特殊人群的产品,儿童(含婴幼儿)产品,应进一步规范行政许可和备案管理工作,并加强上市后监督,确保产品使用安全。为保护有关特殊人群身体健康,化妆品不得宣称专为孕妇、哺乳期妇女使用。 (三)是实现科学监管保障产品质量安全的有效举措。 随着行业发展,目前市售非特殊用途化妆品的形态、种类以及具有或宣称的作用均呈现多元化的特点,其可能存在的风险程度也不可一概而论,为实现科学监管,确保产品质量安全,对非特殊用途化妆品进行合理分类已势在必行。因此按照“整体推进,分步实施”的工作思路,对目前公认安全风险程度高的产品类别纳入特殊用途化妆品管理,对安全风险尚需进一步明确的产品,以及特殊原料、特殊人群产品实行有针对性地严格监管。对非特殊用途化妆品进行分类管理,有利于突出重点,有针对性地对安全风险程度较高的化妆品开展技术审评,确保产品质量安全,进一步完善化妆品安全风险控制体系。 二、主要内容 按照“依法依规,确保安全;科学分类,提高效率;合理定位,分步实施”的原则,根据产品安全风险程度,拟对非特殊用途化妆品实行分类管理。 (一)对目前公认安全风险程度较高的产品,纳入特殊用途化妆品管理。按照部门规章修订程序,拟通过调整《实施细则》第五十六条第八款祛斑化妆品类别含义,对目前公认安全风险程度较高的具有或宣称美白或增白(仅具有物理遮盖作用的除外)、祛痘或抑制粉等作用的产品,纳入祛斑化妆品管理,实行特殊用途化妆品行政许可管理。 (二)对安全风险程度尚需进一步明确的产品,加强安全风险监测与风险评估。对安全风险程度尚需进一步明确的产品类别,如具有或宣称控油、去头屑、抗皱、减轻或减缓眼袋、抑汗止汗、减轻黑眼圈、剥脱皮肤角质、皮肤晒黑或晒成其他颜色作用的产品,以及用于口唇或眼部的产品等,拟连续两年有针对性地开展安全风险监测工作,并进行安全风险评估,根据风险评估结果确定是否需要纳入特殊用途化妆品管理。 (三)对适用于特殊人群产品实行严格监管。以《儿童(含婴幼儿)化妆品申报与审评指南》的出台为契机,进一步规范进口儿童产品的申报与审评工作,国产儿童产品应按照《指南》要求提交备案材料,并加强事后监督。同时,拟进一步明确化妆品不得宣称专为孕妇、哺乳期妇女等特殊人群使用。 三、起草与征求意见过程 为进一步规范非特殊用途化妆品备案管理工作,提高化妆品行政许可工作效率,保化司一直高度重视非特殊用途化妆品分类管理工作。自2009年以来,分别委托北京市药品监督局、国家局保健食品审评中心等单位,开展了化妆品分类管理相关研究工作。各相关研究单位深入化妆品生产企业、许可检验机构,通过实地调研、调查问卷、召开座谈会等多种形式,广泛调研,反复研究,取得了一定的成果。 2011年9月,保化司在相关单位研究成果的基础上,形成了《非特殊用途化妆品分类管理的意见》及相关配套文件,并开展了相关征求意见工作。9~12月,保化司先后7次组织召开了相关专家、部分企业代表参加的非特殊用途化妆品分类管理专题座谈会,主要对非特殊用途化妆品分类原则、特殊用途化妆品含义调整及现行非特殊用途化妆品管理模式调整等进行了研讨,认为应该将产品安全风险程度作为调整非特殊用途化妆品管理模式的首要考虑因素。因此,除了具有或宣称相应特殊功效作用的相关产品外,对特殊使用人群、特殊使用部位和采用特殊原料的产品,均提出按照特殊用途化妆品管理。同时,部分专家提出,实行告知备案管理模式的非特殊用途化妆品应加强事后监督措施。2012年1月,保化司司务会专题研究了非特殊用途化妆品分类管理工作,形成征求意见稿。2012年2月~3月,通过国家食品药品监督管理局官方网站向社会公开征求意见。 公开征求意见取得各界广泛关注,有关化妆品行业协会、化妆品生产企业提出了意见。多数反馈意见认为对具有或宣称控油、去头屑、抗皱、减轻或减缓眼袋、抑汗止汗、减轻黑眼圈、剥脱皮肤角质、皮肤晒黑或晒成其他颜色作用的产品,以及用于口唇或眼部的产品,其安全风险程度尚需进一步明确。2012年3月底,保化司委托有关机构举办了首届中国化妆品法规国际研讨会,对非特殊用途化妆品分类管理从技术层面与中外化妆品技术专家进行沟通交流。通过研讨、交流和各有关方面反映,具有美白或增白(仅具有物理遮盖作用的除外)、祛痘或抑制粉等作用的2类产品,目前公认其安全风险程度较高,应纳入祛斑化妆品管理;具有或宣称控油、去头屑、抗皱、减轻或减缓眼袋、抑汗止汗、减轻黑眼圈、剥脱皮肤角质、皮肤晒黑或晒成其他颜色作用的产品,以及用于口唇或眼部的产品,其安全风险程度尚需进一步明确。 2
3-硫酸甘氨鹅脱氧胆酸 标准品,有可以联系我renzhichu525@163.com.
第二章 备案检验机构指定[b]第十条[/b] 申请指定的检验机构(以下称申请机构)应当具备以下基本条件:(一)具有独立法人资格;(二)卫生安全性检验机构应当按照国家有关认证认可的规定,取得资质认定;人体安全性检验机构应当取得化妆品皮肤病诊断机构资质;(三)卫生安全性检验机构具备独立承担本指南中规定的卫生化学检验必备项目,或卫生化学和毒理学检验必备项目的能力;人体安全性检验机构具备独立承担本指南中规定的人体安全性检验必备项目能力;(四)具备与其检验工作相适应的、有效运行的质量管理体系,并保持其公正性、独立性。[color=#ff0000]在这里没有明确规定化妆品非特备案一定要是第三方实验室吧?[/color][color=#ff0000][color=#333333]在广东省 药品管理监督局中有查到,“[/color]国产非特殊用途化妆品备案检验机构名单[color=#333333]”中有企业在备案检测范围中显示“[/color]可出具本企业产品的微生物和卫生化学(限定于汞、砷、铅、甲醇、a-羟基酸、去屑剂、抗生素、甲硝唑)备案检验报告。[color=#333333]”那意思是不是说本企业通过了CNAS中的非特检测项目后就可以给本企业的化妆品备案提供检测报告了呢?还是需要再做些什么工作吗?同时对本企业的检测机构要求会是什么?第一方实验室?第三方实验室?[/color][/color][color=#ff0000][color=#333333]欢迎大家留言讨论?[/color][/color]
[size=14px]国家药监局化妆品监督管理司在2019年12月发布了一则通知,其中:自2020年1月1日起至6月30日,在上海、重庆、浙江、陕西以及广东省深圳、汕头、中山、江门市,开展国产非特殊用途化妆品量化分级管理第一阶段试点工作[/size][sup][1][/sup][size=14px]。[/size][size=14px]预计7月份全国大范围实施。[/size][b][size=14px]化妆品企业准备好了吗?[/size][/b][size=14px]还有不了解的?[/size][size=14px]小C下面给你们详细讲解。[/size][align=center][size=14px][img]http://www.cttlab.com/examjob/php/upload/20200701/15935641593429.png[/img][/size][/align][align=center][b][size=16px] 什么是量化分级管理 [/size][/b][/align][size=14px]根据非特殊用途化妆品企业的[/size][size=14px]产品备案、备案后检查、产品上市后监管[/size][size=14px]等有关情况,对非特殊用途化妆品企业进行量化评分和分级并采取相应的监管措施。[/size][sup][size=14px][1][/size][/sup][align=center][size=16px][b][b][size=16px] [/size][/b]量化分级评分标准 [b][size=16px] [/size][/b][/b][/size][/align][b][size=14px]原始分数:75分[/size][/b][size=14px]A级[/size][size=14px]评分≥85分[/size][size=14px]B级[/size][size=14px]65分≤评分≤85分[/size][size=14px]C级[/size][size=14px]50分[/size][size=14px]D级[/size][size=14px]评分≤50分[/size][size=14px]▬ [/size][b][size=14px]C、D级企业[/size][/b][size=14px]备案凭证采取不同颜色进行标识,并标注“[b]重点监管对象”[/b]字样。[/size][size=14px][b]所有产品都需要做毒理学试验。[/b][/size][b][size=14px]D级企业[/size][/b][size=14px]采用[color=#ff0000]红色标识[/color]并标注重点监管对象,备案帐号将冻结,[b]无法申请新品备案[/b]。[/size][align=center][b][size=16px] 动态评分结果和等级状态 [/size][/b][/align][size=14px]试点区域内的化妆品企业可以通过国产非特殊用途化妆品网上备案系统平台,获知本企业的动态评分结果和等级状态。[/size][align=center][size=14px][img]http://www.cttlab.com/examjob/php/upload/20200701/15935642927107.png[/img][/size][/align][align=center][b][size=16px] 化妆品企业应对措施 [/size][/b][/align][b][size=14px]1、[/size][size=14px]谨慎选择合作企业[/size][/b][size=14px]品牌商根据量化分级评分规则被减分时,生产企业也会一同被减分。[/size][b][size=14px]2、[/size][size=14px]A级企业更应谨慎[/size][/b][size=14px]化妆品企业被[/size][size=14px]评为[b]A级的[/b][/size][size=14px],已完成备案的产品在备案后资料技术审核环节被抽查的,加分制度按照原来加分原则,[/size][b][size=14px]扣分比例在原来规则基础上扩大至原有的5倍[/size][size=14px]。[/size][size=14px]3、[/size][size=14px]D级企业要引起高度重视[/size][/b][size=14px]当企业评级为D级时,该企业备案账号将冻结。待其企业法定代表人或相关负责人通过省级管理部门组织的业务能力测试后,重新参与动态量化分级等级评定,初始基础分以60分计。这是唯一一次脱离D级的机会,也是唯一一次挽救市场份额的机会。[/size][b][size=14px]4、[/size][size=14px]选择专业的第三方备案[/size][/b][size=14px]当量化分级评分全面实施推广后,化妆品企业合规正确的产品备案对企业发展起着极为重要的因素。不同备案主体专业度优劣分析如图:[/size][align=center][size=14px][img]http://www.cttlab.com/examjob/php/upload/20200701/15935645206129.png[/img][/size][/align][b][size=14px][color=#ff0000]选择专业的第三方备案[/color][/size][/b][size=14px],对国家及地方法规和备案要求了解更精通,从而减少并避免备案审核不通过情况;如出现宣传卖点与法规要求冲突时,可以提供优秀的解决方案。[/size][size=12px][color=#333333]资料来源:[/color][/size][size=12px][1]国家药监局化妆品监督管理司关于在部分地区开展国产非特殊用途化妆品备案量化分级管理试点第一阶段有关工作的通知[/size]
各位老师:想对[font=&]DSC 214 polyma仪器进行校正,耐驰所提供标准品是不是可以重复使用;大家校正都是六个点都做吗?具体升温程序是不是按耐驰所提供的方法呢?[/font]
测柱效标准品,尿嘧啶、萘、芴等样品的浓度是多少?用什么溶解
菜鸟又开始提问啦判断是否为塑化剂会有些不确定,SIM 特征离子的比例都合适但是有些非特特征离子的丰度很大,不知道是否该判?SIM 特征离子和标准图谱都能对上,但是非特征离子丰度大了很多?这种是不是塑化剂呢?全扫描的时候是判断一个物质是按丰度比进行的?这两种不同方法,判断的时候方法也不同?
文/吴海云 华测检测([color=#191919]食农及健康产品事业部)[/color][color=#191919][/color][align=left][b]1.背景[/b][/align][align=left]2017年3月,首次进口非特化妆品管理由审批改备案工作在上海浦东新区率先试点施行。今年3月,在上海浦东新区试点基础上,国务院决定在天津、辽宁、浙江、福建、河南、湖北、广东、重庆、四川和陕西的10个自贸区,推广复制浦东新区经验,扩大首次进口非特化妆品备案试点工作。2018年11月,国家药品监督管理局发布了一则关于在全国范围实施进口非特殊用途化妆品备案管理有关事宜的公告(2018年第88号),该公告指出在2018年11月10日起,首次进口非特殊用途化妆品由现行审批管理和自贸试验区试点实施备案管理,调整为全国统一备案管理,国家药品监督管理部门不再受理进口非特殊用途化妆品行政许可申请。本文将从法规文件,流程与要求,新备案模式与传统注册比较等几个方面进行解析。[/align][align=left][b]2.“备案制”全面推开内容详解[/b][/align][align=left][b]2.1与进口非特化妆品备案相关的法规文件汇总[/b][/align][align=left]* 关于在全国范围实施进口非特殊用途化妆品备案管理有关事宜的公告(2018年第88号);[/align][align=left]* 关于在更大范围试点实施进口非特殊用途化妆品备案管理有关事宜的公告2018年第31号;[/align][align=left][color=#191919]* [/color]关于明确浦东新区试点实施进口非特殊用途化妆品备案检验报告要求等有关事宜的通知〔2017〕72号;[/align][align=left][color=#191919]* [/color]关于在上海市浦东新区开展进口非特殊用途化妆品备案管理试点工作有关事项的公告(2017年第7号);[/align][align=left][color=#191919]* [/color]上海市浦东新区进口非特殊用途化妆品备案管理工作程序(暂行)2017年第10号;[/align][align=left][color=#191919]* [/color]关于印发化妆品行政许可检验管理办法的通知82号;[/align][align=left][color=#191919]* [/color]关于印发化妆品中可能存在的安全性风险物质风险评估指南的通知国食药监许339号;[/align][align=left][color=#191919]* [/color]关于印发化妆品行政许可申报受理规定的通知国食药监许856号;[/align][align=left][color=#191919]* [/color]关于印发化妆品产品技术要求规范的通知国食药监许454号[/align][align=left]2018年第88号指出申请进口非特殊用途化妆品备案的进口化妆品生产企业,应当参照原食品药品监管总局发布的《关于发布上海市浦东新区进口非特殊用途化妆品备案管理工作程序(暂行)的公告》(2017年 第10号)相关要求,进行境内责任人授权、备案系统用户名称注册、产品备案信息报送、备案信息凭证打印等相关工作。[/align][align=left]关于进口非特殊用途化妆品检验报告、境内化妆品企业委托境外企业生产等有关事宜,参照原食品药品监管总局办公厅《关于明确浦东新区试点实施进口非特殊用途化妆品备案检验报告要求等有关事宜的通知》(食药监办药化管〔2017〕72号)执行。[/align][align=left][b]2.2进口非特化妆品备案流程与要求[/b][/align][align=left]在以前,进口非特化妆品审批事权归国家食药监总局,企业每进口一种新化妆品,都要到北京提交材料,并等待专家审评。由审批改为备案管理后,审批时限由以往3个月左右缩减为5个工作日。这意味着,首次非特进口备案试点以来,国外产品在国内的上市时间平均提前了两个半月。那弱化了事前审批流程,服务企业,便利消费者,但是否意味着对产品质量的要求有所降低?答案是否定的,甚至要求更高了,接下来就具体看看备案流程与要求。[/align][align=left]2.2.1进口非特化妆品备案流程[/align][align=left]第一步(形式审查):[/align][align=left][img=,690,279]https://ng1.17img.cn/bbsfiles/images/2019/07/201907011556140017_6074_3051334_3.jpg!w690x279.jpg[/img][/align][align=left] 第二部(技术审评):[/align][align=left][img=,690,312]https://ng1.17img.cn/bbsfiles/images/2019/07/201907011556236121_4915_3051334_3.jpg!w690x312.jpg[/img][/align][align=left] 2.2.2进口非特化妆品备案申请资料(见表1)[/align][align=left]表1[/align][table=662][tr][td] [align=left]序号[/align] [/td][td] [align=left]提交材料名称[/align] [/td][td] [align=left]要求[/align] [/td][/tr][tr][td] [align=left][color=windowtext]1[/color][/align] [/td][td] [align=left][color=windowtext]进口非特殊用途化妆品备案申请表[/color][/align] [/td][td] [align=left][color=windowtext]申请表在线填报后打印纸质申请表,并按要求签名、盖章。内容应完整、清楚,不得涂改[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]2[/color][/align] [/td][td] [align=left][color=windowtext]产品中文名称命名依据[/color][/align] [/td][td] [align=left][color=windowtext]产品中文名称应当符合《化妆品命名规定》、《化妆品命名指南》的要求。[/color][/align] [align=left][color=windowtext]1[/color][color=windowtext])命名依据中应提供申报产品的商标名、通用名(含使用目的或使用部位)、属性名具体含义的解释。约定俗成的、习惯使用的化妆品名称可省略通用名、属性名。[/color][/align] [align=left][color=windowtext]2[/color][color=windowtext])产品中文名称中若有表明产品物理性状或外观形态以及含颜色、色号、气味、适用发质、肤质或特定人群等内容的,应加以解释。[/color][/align] [align=left][color=windowtext]3[/color][color=windowtext])产品中文名称中若使用具体原料名称或表明原料类别词汇的,应加以解释。[/color][/align] [align=left][color=windowtext]4[/color][color=windowtext])产品中文名称中的修饰、形容词或必须使用外文字母、符号等的,应加以解释。[/color][/align] [align=left][color=windowtext]5[/color][color=windowtext])需标注产品中文名称的汉语拼音名。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]3[/color][/align] [/td][td] [align=left][color=windowtext]产品配方[/color][/align] [/td][td] [align=left][color=windowtext]产品配方要求参照《关于印发化妆品行政许可申报受理规定的通知》(国食药监许〔2009〕856号)附件《化妆品行政许可申报资料要求》第十四条、第二十六条执行。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]4[/color][/align] [/td][td] [align=left][color=windowtext]产品质量安全控制要求[/color][/align] [/td][td] [align=left][color=windowtext]应包括在原产国执行的产品质量安全控制要求(外文版及中文译文)及产品符合《化妆品安全技术规范》(2015年版)要求的承诺。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]5[/color][/align] [/td][td] [align=left][color=windowtext]产品包装图片[/color][/align] [/td][td] [align=left][color=windowtext]产品原包装(含产品标签、产品说明书)图片;拟专为中国市场设计包装的,需同时提交产品设计包装(含产品标签、产品说明书)。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]6[/color][/align] [/td][td] [align=left][color=windowtext]产品生产工艺简述[/color][/align] [/td][td] [align=left][color=windowtext]提供的生产工艺简述应包括工艺流程简图,工艺简述应能简明扼要地反映产品的实际生产过程,包括操作步骤、各步骤中涉及的原料等。产品配方中所有原料应在生产工艺中列出,原料名称应与产品配方一致。工艺简述应与工艺简图相符。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]7[/color][/align] [/td][td] [align=left][color=windowtext]产品技术要求[/color][/align] [/td][td] [align=left][color=windowtext]参照《关于印发化妆品产品技术要求规范的通知》(国食药监许〔2010〕454号)要求编制。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]8[/color][/align] [/td][td] [align=left][color=windowtext]化妆品行政许可检验机构出具的检验报告及相关资料[/color][/align] [/td][td] [align=left][color=windowtext]1[/color][color=windowtext])产品检验要求参照《关于印发化妆品行政许可检验管理办法的通知》(国食药监许〔2010〕82号)执行。[/color][/align] [align=left][color=windowtext]2[/color][color=windowtext])检验报告要求参照《关于印发化妆品行政许可申报受理规定的通知》(国食药监许〔2009〕856号)附件《化妆品行政许可申报资料要求》第十八条执行。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]9[/color][/align] [/td][td] [align=left][color=windowtext]产品中可能存在安全性风险物质的有关安全性评估资料[/color][/align] [/td][td] [align=left][color=windowtext]参照《化妆品中可能存在的安全性风险物质风险评估指南》(国食药监许〔2010〕339号)执行。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]10[/color][/align] [/td][td] [align=left][color=windowtext]化妆品适用原料及原料来源符合疯牛病疫区高风险物质禁限用要求的承诺书[/color][/align] [/td][td] [align=left][color=windowtext]参照《卫生部卫生监督中心关于要求对进口化妆品提交承诺书的公告》执行。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]11[/color][/align] [/td][td] [align=left][color=windowtext]产品在生产国(地区)或原产国(地区)生产和销售的证明文件[/color][/align] [/td][td] [align=left][color=windowtext]生产和销售证明文件要求参照《关于印发化妆品行政许可申报受理规定的通知》(国食药监许〔2009〕856号)附件《化妆品行政许可申报资料要求》第二十一条、第二十四条执行。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]12[/color][/align] [/td][td] [align=left][color=windowtext]境外生产企业生产质量管理的相关证明材料[/color][/align] [/td][td] [align=left][color=windowtext]相关证明材料包括质量管理体系或良好生产规范的证明文件或符合生产企业所在国(地区)法规要求的化妆品生产资质的证明文件。证明文件应由认证机构或第三方出具或认可。无法提交原件的,可提交复印件,复印件应由中国公证机关公证或由我国使(领)馆确认;所载明的生产企业名称和地址应与所申报的内容完全一致。[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]13[/color][/align] [/td][td] [align=left][color=windowtext]有助于备案的其他资料[/color][/align] [/td][td] [align=left][color=windowtext]参照《化妆品行政许可申报受理规定》(国食药监许〔2009〕856号,可能有助于备案的其他资料。[/color][/align] [/td][/tr][/table][align=left] [/align][align=left]由以上可以看出,“备案制”与许可申报所需要的资料是一样的,只是在监管模式有了改变,药品监管部门在产品备案后组织对备案资料的监督检查,必要时进行现场检查。发现备案资料不符合要求,但不影响产品安全性判断的,应当要求境内责任人于30日内补充提交相关资料;发现依据现有资料无法判断产品安全性的,应当告知境内责任人补充提交相关资料,并在确认备案资料符合要求前暂停进口及销售该产品;发现存在违法情形或产品质量安全问题的,监管部门将依法予以查处,并对相关产品进行责令下架、召回处理。[/align][align=left][b]2.3新备案模式与传统注册比较(见表2)[/b][/align][align=left]表2[/align][table=546][tr][td] [align=left][color=windowtext]项目[/color][/align] [/td][td] [align=left][color=windowtext]新备案模式[/color][/align] [/td][td] [align=left][color=windowtext]传统注册[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]审核制度[/color][/align] [/td][td] [align=left][color=windowtext]备案制[/color][/align] [/td][td] [align=left][color=windowtext]行政许可申报[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]接收窗口[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][td] [align=left][color=windowtext]境内责任人注册在11个自贸区所在省的,由当地药监局接收,其他仍报国家局[/color][/align] [/td][td] [align=left][color=windowtext]国家药监局[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]授权申请[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][td] [align=left][color=windowtext]国外申请人授权在华公司作为境内责任人[/color][/align] [/td][td] [align=left][color=windowtext]国外申请人授权在华公司作为在华申报责任单位[/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]在华公司责任[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][td] [align=left][color=windowtext]负责产品进口和经营,并承担产品质量安全责任[/color][/align] [/td][td] [align=left][color=windowtext]仅负责产品行政许可[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]批准或备案凭证编号格式[/color][/align] [/td][td] [align=left][color=windowtext]国妆网备进字(境内责任人所在省份简称)+四位年份数字+六位顺序编号[/color][/align] [/td][td] [align=left][color=windowtext]国妆备进字J+四位年份数字+四位编号[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]批准或备案凭证 有效期[/color][/align] [/td][td] [align=left][color=windowtext]未知[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][td] [align=left][color=windowtext]4[/color][color=windowtext]年[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][/tr][tr][td] [align=left][color=windowtext]许可或者备案凭证 生成流程及形式[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][td] [align=left][color=windowtext]形式审查通过后备案系统自动生成电子版备案信息凭证供企业自行下载打印[/color][/align] [/td][td] [align=left][color=windowtext]技术审查通过后发放行政许可批件证书[/color][/align] [align=left][color=windowtext] [/color][/align] [/td][/tr][/table][align=left]由上表看出,新备案模式与传统注册最大的差异体现在备案流程或许可及境内责任人的要求。新备案模式最大优势体现在企业通过资料形式审查后就可以获得备案号进行进口销售。国家局行政许可要求在通过所有形式和技术审查后才能获得许可号进行进口销售。两者相比,前者更利于企业将产品快速投放市场。但在资料要求上,两者几乎保持一致。可见,境内责任人的出现,实际上是为了境外化妆品生产企业和我国监管部门,以及消费者之间,架起一座桥梁,更切实督促企业落实主体责任和社会责任。另外,根据现行规定,无论是进口非特化妆品还是国产非特化妆品,均未设置备案有效期。但是,未设置备案有效期并不意味着一次备案,终生有效。”据悉,国家药监局正起草《非特殊用途化妆品备案管理办法》,将会对已备案产品提出年报制度要求,企业定期通过网上备案平台填报产品的生产进口、上市销售、不良反应监测等情况。未履行报告义务的产品备案信息将会被清理,避免网上备案平台出现“僵尸产品”堆积现象。[/align][align=left] [/align][align=left][b]3.总结[/b][/align][align=left]将首次进口非特化妆品调整为全国统一备案管理,改事前“点头”为事后“摇头”,首次进口非特化妆品备案管理时代。试点期间,全国范围内已经有近3000种首次进口非特化妆品完成备案。其中,上海浦东自贸区试点时间较长,试点一年多来,完成备案进口产品已达2500余个。广东、四川、浙江等省也已有进口产品完成备案。最近,上海市,浙江省,广东省等各个地方药监局相续出台进口化妆品非特备案办事指南,企业可以根据指南进行备案工作。此次88号文件,官方名义是“贯彻国务院落实简政放权和证照分离的改革的要求”,实际意义是“适应化妆品行业发展需要”将进口品和国产品带到了同一起跑线。[/align]
点击链接查看更多:[url]https://www.woyaoce.cn/service/info-1885.html[/url]国产非特殊用途化妆品应在产品投放市场后2个月内,由生产企业向所在行政区域内的省级食品药品监督管理部门申请备案,并按照有关要求提交备案资料,履行备案手续。备案资料里应含有经省级食品药品监督管理部门指定的检验机构出具的检验报告及相关资料,我中心是省级食品药品监督管理部门公布指定的备案检验机构。[color=#0000ff][url=http://www.fenxi.com.cn/client/downloading/downloading_list.jsp?rowId=616310][u][color=#000080]国产非特殊用途化妆品备案检验指南及相关表格下载[/color][/u][/url][/color][b][font=宋体][color=red]国产非特殊用途化妆品检测[/color][/font][/b][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]一般产品检测项目[/font][/b][font=宋体]微生物[/font]5[font=宋体]项(菌落总数,霉菌和酵母菌,粪大肠菌群,铜绿假单胞菌,金黄色葡萄球菌)、重金属[/font]3[font=宋体]项(砷,汞,铅)[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]祛痘除螨类产品检测项目[/font][/b][font=宋体]微生物[/font]5[font=宋体]项,重金属[/font]3[font=宋体]项,甲硝唑及抗生素(盐酸美满霉素、土霉素、四环素、金霉素、盐酸多西环素、氯霉素)[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]去屑类产品检测项目[/font][/b][font=宋体]微生物[/font]5[font=宋体]项,重金属[/font]3[font=宋体]项,去屑剂[/font]4[font=宋体]项(水杨酸、酮康唑、氯咪巴唑、吡罗克酮乙醇胺盐)[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]其他检测项目[/font][/b][font=宋体]甲醇,[/font]pH[font=宋体]值,防晒剂,α[/font]-[font=宋体]羟基酸[/font]5[font=宋体]项(酒石酸、乙醇酸、苹果酸、乳酸、柠檬酸)等[/font][b][font=宋体][color=red]化妆品中有害成分检测[/color][/font][/b][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]美白产品[/font][/b][font=宋体]:对苯二酚、铅、汞、砷、防腐剂等[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]祛痘[/font][font=宋体]祛斑类产品:[/font][/b]41[font=宋体]种糖皮质激素:地塞米松、氢化可的松、泼尼松、倍他米松、曲安萘德、以及肾上腺素等;性激素:雌三醇、己烯雌酚、雌二醇、睾丸酮、甲基睾丸酮、黄体酮、雌酮等;铅、汞、砷、镉、防腐剂等。[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]防腐剂:[/font][/b][font=宋体]甲基氯异噻唑啉酮、甲基异噻唑啉酮、苯甲醇、苯氧乙醇、苯甲酸,对羟基苯甲酸酯类、氯苯甘醚、三氯生、三氯卡班等[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]防晒剂:[/font][/b][font=宋体]二苯酮、对氨基苯甲酸、甲氧基肉桂酸乙基己酯、水杨酸乙基己酯、[/font]4-[font=宋体]甲基苄亚基樟脑、[/font]PABA[font=宋体]乙基己酯、丁基甲氧基二苯酰基甲烷、奥克立林、胡莫柳酯、乙基己基三嗪酮、亚甲基双[/font]-[font=宋体]苯并三唑基、四甲基丁基酚、双[/font]-[font=宋体]乙基己氧苯酚、甲氧苯基三嗪等[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]染发产品:[/font][/b][font=宋体]对苯二胺、氨基苯酚、间苯二酚、苯二胺、氢醌、[/font]p-[font=宋体]甲氨基苯酚、甲苯、[/font]2,5-[font=宋体]二胺、苯酚、铅、汞、砷等[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]口红:[/font][/b][font=宋体]苏丹红、铅、[/font]4-[font=宋体]羟基苯甲酸酯类、各种禁限用着色剂[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]指甲油:[/font][/b][font=宋体]邻苯二甲酸酯类、挥发性有机溶剂(如甲醛、甲苯、丙酮、[/font][url=http://baike.baidu.com/view/444633.htm][size=14px][font=宋体][color=windowtext]醋酸乙酯[/color][/font][/size][/url][font=宋体]等)、苏丹红[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]洗护产品:[/font][/b][font=宋体]二?烷、丙烯酰胺、[/font]N-[font=宋体]亚硝基二乙醇胺等亚硝胺类[/font][font=Wingdings]l[font=&] [/font][/font][b][font=宋体]香水类产品:[/font][/b][font=宋体]甲醇及[/font]24[font=宋体]种过敏源物质([/font]d-[font=宋体]苎烯、芳樟醇、苄醇(苯甲醇)、香茅醇、香叶醇、柠檬醛、羟基香茅醛、[/font]2-[font=宋体]辛炔酸甲酯(庚炔碳酸甲酯)、肉桂醛、茴香醇、肉桂醇、丁香酚、[/font]α-[font=宋体]异甲基紫罗兰酮、异丁香酚、丁苯基甲基丙醛(铃兰醛)、香豆素、戊基肉桂醛、金合欢醇、羟基异己基[/font]-3-[font=宋体]环己烯甲醛([/font]HMPCC[font=宋体],新铃兰醛)、[/font][font=宋体]戊基肉桂醇、己基肉桂醛、苯甲酸苄酯、水杨酸苄酯、肉桂酸苄酯)[/font][b][font=宋体][color=red]原料检测及质量标准制订[/color][/font][/b][font=宋体]中广测按照国内外标准对化妆品及日化产品原料进行检测,并研究原料检测新方法和标准,向社会提供技术服务,[/font][font=宋体]同时可为企业建立检测方法及质量标准。[/font][font=宋体]中广测[/font][font=宋体]设有专门队伍从事标准化研究工作,在日化产品、化妆品的检测方法研究方面取得多项成果,建立了日化原料[/font]AEO[font=宋体]和[/font]AES[font=宋体]等的[/font]EO[font=宋体]分布及碳链分布、二?烷、邻苯二甲酸酯、[/font]24[font=宋体]种过敏源物质等检测新方法,可为日化企业提供的原料质量把关提供技术服务。[/font][b][font=宋体][color=red]日化产品配方剖析[/color][/font][/b][align=left][font=宋体]通过综合的分离和分析手段对复杂的未知化学品的成分进行定性和定量分析。中广测提供化妆品产品配方剖析,涉及洗发、护发用品、护肤用品、美容用品、口腔卫生制品,如?哩、面膜、膏霜、护发、护肤、粉底液等产品。[/font][/align] 中广测设有专门的医药化工实验室,主要从事日化产品、化妆品、药品的检测技术研究和服务工作。该室拥有一支高水平的专业人才队伍,技术人员33人,其中研究员3人、高级工程师4人,具有博士学位3人、硕士8人。 中广测依据卫生部《化妆品卫生规范》、国家食品药品监督管理总局发布的一系列“化妆品中禁限用物质检测方法”、欧盟“化妆品指令”(76/768/EEC)等国内外法规,开展化妆品及日化产品中常规指标及1000多种禁用和限用物质的检测服务。[color=#ff0000]仪器设备[/color][url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]/三重四极杆串联质谱联用仪[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱[/color][/url]/三重四极杆串联质谱联用仪[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]/质谱联用仪高效[url=https://insevent.instrument.com.cn/t/5p][color=#3333ff]液相色谱仪[/color][/url][url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱仪[/color][/url]凝胶渗透色谱仪[url=https://insevent.instrument.com.cn/t/3p][color=#3333ff]离子色谱仪[/color][/url]核磁共振波谱仪(500MHz、300MHz)[url=https://insevent.instrument.com.cn/t/Mp][color=#3333ff]气相色谱[/color][/url]/红外光谱联用仪红外显微镜[url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]电感耦合等离子体质谱仪[/color][/url]([url=https://insevent.instrument.com.cn/t/yp][color=#3333ff]ICP-MS[/color][/url])电感耦合等离子发射光谱仪(ICP-OES)[url=https://insevent.instrument.com.cn/t/Wp][color=#3333ff]原子吸收[/color][/url]分光光度计(火焰、石墨炉)紫外可见分光光度计荧光分光光度计卡氏水分仪微生物检测仪器和设备
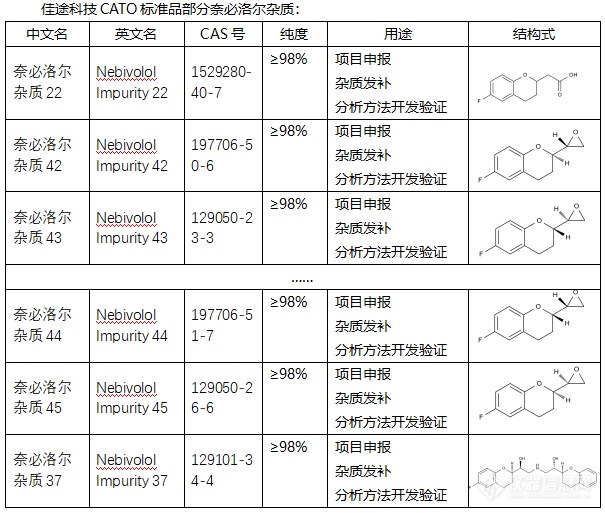
[font=宋体]◇[/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]杂质[/font][font=宋体][font=宋体] 奈必洛尔杂质是指在奈必洛尔([/font][font=Calibri]Nebivolol[/font][font=宋体])的生产或保存过程中产生的非目标化合物。奈必洛尔杂质有多种,包括但不限于以下几种:奈比洛尔杂质([/font][font=Calibri]L-[/font][font=宋体]奈必洛尔),英文名称为[/font][font=Calibri](-)-Nebivolol[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]118457-16-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]9[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]920275-23-6[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]C[/font][font=宋体](非对映体混合物),英文名为[/font][font=Calibri]Nebivolol Impurity C (Mixture of Diastereomers)[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=Calibri]B[/font][font=宋体],英文名为[/font][font=Calibri]Nebivolol impurity B[/font][font=宋体],[/font][font=Calibri]CAS[/font][font=宋体]号为[/font][font=Calibri]119365-25-2[/font][/font][font=宋体];[/font][font=宋体][font=宋体]去氟奈必洛尔,英文名为[/font][font=Calibri]Desfluoro Nebivolol[/font][/font][font=宋体];[/font][font=宋体][font=宋体]奈必洛尔杂质[/font][font=宋体]Ⅰ和奈必洛尔杂质Ⅱ等。[/font][/font][font=宋体][font=Calibri] CATO[/font][font=宋体]标准品提供的[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套的杂质[/font][font=宋体],[/font][font=宋体]这些杂质对于药物的纯度和稳定性研究至关重要,也是药物研发过程中不可或缺的一部分[/font][font=宋体]。[/font][img=,605,513]https://ng1.17img.cn/bbsfiles/images/2024/02/202402182153192686_9605_6381607_3.png!w605x513.jpg[/img][font=宋体][color=#05073b][back=#fdfdfe] 广州[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]佳途科技[/back][/color][/font][font=宋体][color=#05073b][back=#fdfdfe]股份有限公司[/back][/color][/font][font='Segoe UI'][color=#05073b][back=#fdfdfe]深知药物研发与质量控制的重要性[/back][/color][/font][font=宋体][font=宋体],[/font][font=Calibri]CATO[/font][font=宋体]标准品厂家,提供[/font][/font][b][font=宋体]奈必洛尔[/font][/b][font=宋体]全套[/font][font=宋体]的[/font][font=宋体]杂质,为客户提供更加精准、可靠的分析标准品,助力药物研发事业的快速发展[/font][font=宋体],[/font][font=宋体]以满足客户在药物研发和质量控制方面的需求。[/font]
http://www.greenherbs.com.cn/bbs/dispbbs.asp?boardid=2&Id=7661700512 色氨酸杂质A Tryptophan Related Compound A 对照品/标准品1700501 L- 色氨酸 L-Tryptophan 对照品/标准品1700002 结晶胰蛋白酶 Trypsin Crystallized 对照品/标准品1699005 托吡卡胺 Tropicamide 对照品/标准品1698002 氨丁三醇 Tromethamine 对照品/标准品1697000 醋竹桃霉素 Troleandomycin 对照品/标准品1696958 三乙醇胺 Trolamine 对照品/标准品1696200 三水杨酸 Trisalicylic Acid 对照品/标准品1696109 盐酸曲普利啶 Z- 异构体 Triprolidine Hydrochloride Z-Isomer 对照品/标准品1696007 盐酸曲普利啶 Triprolidine Hydrochloride 对照品/标准品1695004 盐酸曲吡那敏 Tripelennamine Hydrochloride 对照品/标准品1693009 三甲沙林 Trioxsalen 对照品/标准品1692710 三甲丙咪嗪杂质A Trimipramine Related Compound A 对照品/标准品1692709 三甲丙咪嗪马来酸盐 Trimipramine Maleate 对照品/标准品1692527 甲氧苄啶杂质B Trimethoprim Related Compound B 对照品/标准品1692516 甲氧苄啶杂质A Trimethoprim Related Compound A 对照品/标准品1692505 甲氧苄啶 Trimethoprim 对照品/标准品1692006 盐酸曲美苄胺 Trimethobenzamide Hydrochloride 对照品/标准品1690000 三甲双酮 Trimethadione 对照品/标准品1689001 酒石酸阿利马嗪 Trimeprazine Tartrate 对照品/标准品1687006 盐酸苯海索 Trihexyphenidyl Hydrochloride 对照品/标准品1686310 曲氟尿苷杂质A Trifluridine Related Compound A 对照品/标准品1686309 曲氟尿苷 Trifluridine 对照品/标准品1686003 盐酸三氟丙嗪 Triflupromazine Hydrochloride 对照品/标准品1685500 2--chlorobenzophenone 对照品/标准品1685000 盐酸三氟拉嗪 Trifluoperazine Hydrochloride 对照品/标准品1683606 枸橼酸三乙酯 Triethyl Citrate 对照品/标准品1683504 盐酸曲恩汀 Trientine Hydrochloride 对照品/标准品1683005 曲地氯铵 Tridihexethyl Chloride 对照品/标准品1682217 三氯生杂质混合物A Triclosan Related Compounds Mixture A 对照品/标准品1682206 三氯生 Triclosan 对照品/标准品1681000 三氯噻嗪 Trichlormethiazide 对照品/标准品1680801 美曲膦酯 Trichlorfon 对照品/标准品1680685 三丁基氧化磷 Tributyl Phosphine Oxide 对照品/标准品1680608 枸橼酸三丁酯 Tributyl Citrate 对照品/标准品1680506 三唑仑CIV Triazolam CIV 对照品/标准品1680030 氨苯蝶啶杂质C Triamterene Related Compound C 对照品/标准品1680029 氨苯蝶啶杂质B Triamterene Related Compound B 对照品/标准品1680018 氨苯蝶啶杂质A Triamterene Related Compound A 对照品/标准品1680007 氨苯蝶啶 Triamterene 对照品/标准品1679008 己曲安奈德 Triamcinolone Hexacetonide 对照品/标准品1678005 醋酸曲安西龙 Triamcinolone Diacetate 对照品/标准品1677002 曲安奈德 Triamcinolone Acetonide 对照品/标准品1676000 曲安西龙 Triamcinolone 对照品/标准品1675007 三醋汀 Triacetin 对照品/标准品1674004 维 A 酸 Tretinoin 对照品/标准品1673839 醋酸群勃龙系统适用性实验用混合物 CIII Trenbolone Acetate System Suitability Mixture CIII 对照品/标准品1673828 醋酸群勃龙 CIII Trenbolone Acetate CIII 对照品/标准品1673806 群勃龙CIII Trenbolone CIII 对照品/标准品1673715 海藻糖 Trehalose 对照品/标准品1673500 盐酸曲唑酮 Trazodone Hydrochloride 对照品/标准品1673012 曲沃前列素杂质A Travoprost Related Compound A 对照品/标准品1673001 曲沃前列素 Travoprost 对照品/标准品1672916 苯环丙胺杂质A Tranylcypromine Related Compound A 对照品/标准品1672905 硫酸苯环丙胺 Tranylcypromine Sulfate 对照品/标准品1672803 反铂 Transplatin 对照品/标准品1672756 氨甲环酸杂质C Tranexamic Acid Related Compound C 对照品/标准品1672745 氨甲环酸 Tranexamic Acid 对照品/标准品1672712 群多普利杂质D Trandolapril Related Compound D 对照品/标准品1672701 群多普利杂质C Trandolapril Related Compound C 对照品/标准品1672687 群多普利 Trandolapril 对照品/标准品1672621 曲马多杂质B Tramadol Related Compound B 对照品/标准品1672610 曲马多杂质A Tramadol Related Compound A 对照品/标准品1672600 盐酸曲马多 Tramadol Hydrochloride 对照品/标准品1672337 托拉塞米杂质C Torsemide Related Compound C 对照品/标准品1672326 托拉塞米杂质B Torsemide Related Compound B 对照品/标准品1672315 托拉塞米杂质A Torsemide Related Compound A 对照品/标准品1672304 托拉塞米 Torsemide 对照品/标准品1672210 托吡酯杂质A Topiramate Related Compound A 对照品/标准品1672206 托吡酯;托佩马特 Topiramate 对照品/标准品1672100 含番茄红素的番茄提取物 Tomato Extract Containing Lycopene 对照品/标准品1672020 对甲苯磺酰胺 p-Toluenesulfonamide 对照品/标准品1672010 邻甲苯磺酰胺 o-Toluenesulfonamide 对照品/标准品1671006 托萘酯 Tolnaftate 对照品/标准品1670502 托美丁钠 Tolmetin Sodium 对照品/标准品1670229 托卡朋杂质 B Tolcapone Related Compound B 对照品/标准品1670218 托卡朋杂质 A Tolcapone Related Compound A 对照品/标准品1670207 托卡朋 Tolcapone 对照品/标准品1670003 甲苯磺丁脲 Tolbutamide 对照品/标准品1669004 盐酸妥拉唑林 Tolazoline Hydrochloride 对照品/标准品1668001 妥拉磺脲 Tolazamide 对照品/标准品1667938 替扎尼定杂质C Tizanidine Related Compound C 对照品/标准品1667924 替扎尼定杂质B Tizanidine Related Compound B 对照品/标准品1667916 替扎尼定杂质A Tizanidine
环保部的标准样品,氨一直买不到标准样品,只能买到氨氮,有一次考核专家说氨氮和氨可以换算,用分子量换算?问题1:换算的理论依据是什么?2:如果作氨的话,使用氨标液测定后换算,还是使用氨氮标液测定后换算?3:如果氨氮的标准值不在曲线范围内,标样能不能浓缩,比如按要求应该10到250容量瓶稀释为0.102+-0.013,现在我10到25,结果大10倍,到标样值为多少?
自三聚氰胺事件之后,中国牛奶消费信心至今未愈。日前中国奶协有关人士在福州建议,对巴氏杀菌鲜牛奶(下称“巴氏鲜奶”,相对于超高温灭菌的“常温奶”)生产企业,国家应给予政策及经济扶持,逐渐恢复巴氏鲜奶主导市场的地位。在此次“南方巴氏鲜奶发展论坛”期间,素有中国乳业“大炮”之称的广州市奶业协会理事长王丁棉对《第一财经(微博)日报》表示,中国乳业行业标准被个别大企业绑架,是全球最差标准,政府应倡导巴氏鲜奶。但昨日,内蒙古奶协秘书长那达木德则认为,中国奶业现状取决于国情,同时披露现行标准门槛低系因农业部顾及散户奶农利益。建议选择“巴氏鲜奶”会上,没有任何添加剂的巴氏鲜奶,被中国奶业协会大力提倡。“为什么要提倡巴氏鲜奶?因为它最完美、最丰富。”农业部原副部长、中国奶业协会名誉会长刘成果指出,巴氏鲜奶没有任何添加剂,原汁原味,低温处理保持活性,营养破坏少,利于增强免疫力。“从未来消费趋势看,绝对是巴氏鲜奶,市场会越来越大。”中国奶协乳品工业委员会副主任曾寿瀛指出,我国以往称之为消毒牛奶的巴氏鲜奶,在世界众多国家市场占有率高达约95%,而在我国近六七年,尤其在三聚氰胺事件发生前两年左右,巴氏鲜奶的销售形势却面临挑战。主因有三,即有关大型乳企的强力宣传、大型乳企产品调香、调稠和销售产品方面的恶性竞争。他建议,在当今重拳打击食品掺假和胡乱使用添加剂的同时,国家应对巴氏鲜奶生产企业给予政策及经济扶持,逐渐恢复巴氏鲜奶主导市场的地位。他建议国家有关部委对以下问题采取相关措施,调整及安排解决。一是完善乳品安全监管体制,尽快解决“九龙治水”即“铁路警察各管一段”的状态,原料奶的监管由技监部门统一监管;二是部委应切实执行“60公里范围内不得重复建厂(乳品厂)及没有自办奶牛场提供奶源的不得建厂”的禁令,调查国内两大乳企在江苏境内投资超亿元建立乳品厂的重复设厂之举;三是乳品电视广告应先由国家监管部门如技监部门先审批后播放,尽快结束有钱就能打广告的乱象;四是有限期地取消手工挤奶,引导散养奶牛户走合作社道路;五是建议主管部委树典型并以点带面,推进巴氏鲜奶的普及推广。细菌数允许200万个/毫升全球最差牛奶标准目前执行的中国乳业行业标准,不仅被与会代表批为增大乳品安全风险,甚至被斥为世界奶业之耻。在我国乳业行业标准中,原奶细菌数允许最大值为200万个/毫升。“这是全球最差的牛奶标准,是世界乳业之耻!”王丁棉炮轰该标准,并称它是遭到大企业利益挟持的结果。“标准是行政部门领导说了算,不是专家说了算。”曾4次参与国家乳业标准制订的西部乳业发展协作会执行副会长魏荣禄感慨,专家们通过的标准送审稿,远严于最后颁布实施的标准内容,现行标准中原奶细菌数最大值为200个/毫升,由于存在有害菌,显然不安全。魏荣禄还指出,现行标准只限于产品标准,未来必须制订专业术语标准和生产工艺标准,以杜绝类似“纯牛奶”却含添加剂的怪象。内蒙古奶协:国情决定现状那达木德认为,“奶业发展由消费水平、冷链储存、交通状况等综合情况决定,巴氏鲜奶在中国发展了七八年,仍在30%的占比内徘徊,而常温奶仍占70%,这符合国情。”昨日,那达木德接受本报记者专访时表示。“巴氏鲜奶是一个发展方向,在国际上占比约达80%,但发展中国家则应客观分析。”那达木德认为巴氏鲜奶与常温奶应分占中国市场。他说,巴氏鲜奶保质期一般为7天,而常温奶可长期保持,受消费水平和冷链系统输送半径的限制,一线城市如北京、上海、广州、深圳这些城市适宜发展巴氏鲜奶,而二线城市及广泛的其他区域比较适合继续搞常温奶。至于内蒙古,那达木德说,由于奶企是做全国市场,地域广,搞巴氏鲜奶“不符合国情”。谈及行标菌落数偏高问题,那达木德指出,标准问题很复杂。他说,农业部制定标准时顾及我国超70%奶农都是散户,生产水平很低,如果把标准定高,散户牛奶都不合格;如果倒掉则害苦奶农。蔡永康则指出,突破乳品安全的瓶颈是养殖模式问题,实现集约化、规模化和标准化是中国乳业发展的必由之路,但企业不能盲目崇拜规模,更应遵循行业发展规律,崇尚资源与市场平衡协调发展,真正实现乳品安全和质量保障。(第一财经日报 邵芳卿)
化验室新加一项氨氮的实验,说买氨氮标准物质来配储备溶液,这个该如何稀释啊?样品编号是130636,标准值是500ml/l,请各位专家指点一下!

乳胶枕标准中氨纶织物不考核顶破强力,我们最近遇到一个样品含0.7%的氨纶,也算氨纶织物吧?[img=,246,92]https://ng1.17img.cn/bbsfiles/images/2019/03/201903251146281717_7304_2154459_3.png!w246x92.jpg[/img]
我是刚从事环境检测的,想请教一下做氨标准曲线时氨含量为0时的吸光度大概在多少?为10时吸光度为多少? 谢谢啦